Abstrak — Logam-logam oksida transisi merupakan sumber penting penggunaan aplikasi berbasis material semikonduktor.
Salah satu yang sedang menjadi diskusi dan objek penelitian saat ini adalah material semikonduktor TiO2 dengan doping Cr (Kromium). Pada penelitian ini akan dibahas tentang sintesa semikonduktor TiO2 tanpa doping dan TiO2:CrO3 (5-15 at.%CrO3) dengan menggunakan metode sol gel dan dikalsinasi dengan variasi temperatur 600 dan 700°C. Hasil sintesis menunjukkan ukuran kristal yang dihasilkan berkisar 45.92- 92.66 nm. Pengaruh temperatur kalsinasi dan penambahan komposisi dopan mulai 10 at.%Cr menimbulkan terjadinya pemisahan sebagian atom Cr dari susunan kristal TiO2 hingga terbentuknya Cr2O3. Hasil SEM menunjukkan pemecahan aglomerasi yang terjadi pada TiO2 hingga berbentuk bulat yang homogen. Ukuran partikel yang dihasilkan berkisar 106.28- 173.85nm. Luas permukaan aktif TiO2 dengan doping menunjukkan nilai yang lebih konsisten dibandingkan TiO2 tanpa doping pada temperatur kalsinasi yang berbeda. Temperatur kalsinasi juga melepas kandungan O2 yang menyebabkan terbentuknya fasa Cr2O3 yang teridentifikasi dari hasil TGA pada temperatur di atas 400ºC. Penambahan doping CrO3 ke dalam TiO2 menimbulkan terjadinya cacat yakni terjadinya substitusi atom Cr ke dalam susunan kristal TiO2.
Kata Kunci — dopant, kalsinasi, semikonduktor, sol-gel, TiO2
I. PENDAHULUAN
ewasa ini material semikonduktor telah menjadi solusi alternatif sebagai sebuah terobosan di bidang elektronika.
Banyak perusahaan dengan latar belakang di bidang elektronika mengembangkan berbagai macam produk dengan memanfaatkan fungsi dari material semikonduktor. Selain perusahaan di bidang tersebut, material semikonduktor juga telah menjadi perbincangan hangat di kalangan akademika bahkan banyak peneliti yang mulai menginovasi dan merekayasa material semikonduktor sehingga memiliki daya guna lebih dari penemuan-penemuan sebelumnya. Sebut saja material semikonduktor seperti SnO
2, ZnO, dan Ga
2O
3yang telah lebih dulu dikembangkan dan menjadi cikal bakal inovasi material semikonduktor.
Resistivitas dari material semikonduktor ini sangat tinggi yakni dalam rentang 10
-2-10
9Ωcm [1] sehingga arus yang dihasilkan sangat kecil. Penambahan doping dinilai dapat memperbaiki sifat dielektrik material semikonduktor. Sebagai contoh nilai resistivitas yang begitu besar dapat diminimalisir dengan adanya penambahan doping dengan harapan untuk menaikkan konduktivitas material semikonduktor [2]. Efek
lainnya dari adanya penambahan materi lain (doping) ke dalam material semikonduktor akan menyebabkan cacat (defect) baik berupa substitusi, vakansi maupun interstisi.
Salah satu yang sedang menjadi diskusi dan objek penelitian saat ini adalah material semikonduktor TiO
2dengan doping Cr (Kromium) dengan menggunakan berbagai macam metode sintesis. Pengaruh penambahan doping terhadap karakteristik TiO
2hingga terbentuknya cacat masih menjadi bahan yang terus didiskusikan karena ada banyak hal yang dapat diinovasi pada material semikonduktor TiO
2. Sejauh ini telah ada beberapa metode yang digunakan untuk mensintesis material semikonduktor TiO
2seperti Flame Spray Synthesis (FSS) yang mana metode ini digunakan untuk menghasilkan serbuk kristal dengan tahapan proses lebih singkat karena menggunakan temperatur pembakaran yang tinggi [3]. Selain itu beberapa penelitian menggunakan sintesa dengan metode sol gel [4]
dengan media larutan sebagai media sintesisnya dan temperatur kamar selama sintesis.
Salah satu karakteristik penting semikonduktor adalah memiliki celah energi yang relatif kecil yaitu berkisar antara 0,2-2,5 eV. Energi celah pita yang kecil ini memungkinkan suatu elektron memasuki level energi yang lebih tinggi.
Perpindahan elektron ini dapat terjadi karena pengaruh temperatur dan penyinaran. Celah energi memisahkan pita valensi dengan pita konduksi. Elektron pada pita valensi dapat loncat menuju pita konduksi dengan cara menyerap sejumlah energi yang melebihi celah energi. Celah energi yang memisahkan kedua pita tersebut yaitu pita terlarang atau disebut juga sebagai bandgap (E
g
) [5,6].
Nanopartikel TiO
2merupakan material semikonduktor yang mempunyai ukuran partikel antara 10 sampai 50 nanometer.
TiO
2mempunyai kemampuan untuk menyerap dye lebih banyak karena di dalamnya terdapat rongga dan ukurannya dalam nano, maka disebut nanoporous. TiO
2memiliki tiga struktur polimorfi yaitu rutile, anatase dan brookit. Hanya
rutile dan anatase yang cukup stabil keberadaannya.Perbedaan fasa juga mempengaruhi karakteristik TiO
2dalam aktivitas katalis [7]. Anatase diketahui sebagai kristal titania yang lebih fotoaktif daripada rutil [8]. Hal ini disebabkan harga Eg TiO
2jenis anatase yang lebih tinggi yaitu sebesar 3,2 eV sedangkan rutil sebesar 3,1 eV. Harga Eg yang lebih tinggi akan menghasilkan luas permukaan aktif yang lebih besar sehingga menghasilkan fotoaktivitas yang lebih efektif [9].
Asam nitrat, baik yang encer maupun yang pekat, membuat kromium menjadi pasif, begitu pula asam sulfat pekat dingin.
PENGARUH VARIASI KOMPOSISI DOPING CrO 3 DAN TEMPERATUR KALSINASI TERHADAP KARAKTERISASI TiO 2 HASIL PROSES SOL GEL
Sardi Septian Nugroho dan Hariyati Purwaningsih, S.Si., M.Si
Jurusan Teknik Material dan Metalurgi, Fakultas Teknologi Industri, Institut Teknologi Sepuluh Nopember (ITS) Jl. Arief Rahman Hakim, Surabaya 60111 Indonesia
e-mail: [email protected]
D
Dalam kromat atau dikromat, anion kromium adalah heksavalen dengan keadaan oksidasi +6. Ion-ion ini diturunkan dari kromium trioksida (CrO
3) [10] . Dalam penelitian sebelumnya [3] kromium (Cr) telah digunakan dopan untuk meningkatkan nilai konduktivitas material semikonduktor.
Ukuran ion dari Cr
3+dan Ti
4+sangat berdekatan yakni masing- masing 0.69 Å dan 0.68 Å. Hal ini memungkinkan ion Cr dapat masuk ke dalam kisi ion Ti sebagai dopan yang mensubstitusi. Kromium dalam bentuk oksida yang sering digunakan adalah kromium (VI) oksida CrO
3, kromium (III) oksida Cr
2O
3dan kromium dioksida hidrat CrO
2.nH
2O.
Beberapa peneliti mengasumsikan bahwa Cr (VI) bisa digunakan sebagai material doping pengganti Cr (III) [11].
Proses sol-gel adalah suatu proses pembentukan bahan anorganik pada temperatur rendah yang melibatkan dua reaksi penting yaitu hidrolisis dari logam alkoksida kemudian dilanjutkan dengan kondensasi. Sol merupakan suatu sistem yang memungkinkan bahan kimia padat tersuspensi stabil di dalam larutan, sedangkan gel ialah cairan yang terjebak dalam jaringan partikel padat. Pembentukan sol menjadi gel bertujuan untuk menyempurnakan pembentukan kisi-kisi kristal pada proses kalsinasi [12, 13, 14].
Tujuan dari penelitian ini sendiri yaitu menganalisa pengaruh variasi konsentrasi doping Cr dan temperatur kalsinasi terhadap struktur dan fasa kristal, morfologi, serta luas permukaan aktif pada sintesa material TiO
2serta menganalisa mekanisme defect/cacat yang terjadi ketika Cr mendoping TiO
2.
II. METODE PENELITIAN
Sintesa Titanium Dioksida (TiO
2) dimulai dengan melarutkan serbuk titanium (IV) dioksida dengan variasi komposisi doping sebesar 0, 5, 10, 15 at.% CrO
3. Kemudian masing-masing campuran tersebut dilarutkan ke dalam 6.25 ml HNO
3dan 100 ml H
2O. Kemudian larutan didiamkan selama 24 jam, setelah itu distirring menggunakan magnetic stirrer dan diletakkan di atas hot plate stirrer dengan temperatur sebesar 120ºC dengan rate sebesar 600 rpm selama 2 jam hingga terbentuk gel.
Drying dilakukan pada temperatur sebesar 100ºC di atas hot
plate stirrer selama satu jam dengan tujuan untukmengeringkan gel supaya pelarut yang terkandung di dalam gel menguap. Setelah itu dilakukan proses pembuatan pelet menggunakan metode kompaksi menggunakan alat press.
Proses pembentukan adalah berupa bahan serbuk dimasukkan kedalam cetakan (dice) kemudian dilakukan kompaksi (compaction). Setelah dilakukan kompaksi serbuk membentuk
green body yang sesuai dengan bentuk cetakan yangdiinginkan. Alat press yang digunakan disetting dengan tekanan maksimal 200 bar hingga terbentuk pelet. Kemudian dilakukan proses kalsinasi dengan variasi temperatur sebesar 600 dan 700ºC.
Setelah itu dilakukan pengujian dan karakterisasi untuk mendapatkan data-data karakteristik TiO
2setelah disintesis dengan adanya variabel temperatur dan komposisi doping.
Pengujian yang dilakukan yaitu XRD, SEM, TGA dan BET.
Untuk memperoleh nilai ukuran kristal dibutuhkan persamaan : ………..(1)
……….(2) III. HASIL DAN DISKUSI
III.1 Identifikasi Fasa dan Struktur Kristal
Gambar 1. Pola difraksi XRD TiO
2dengan doping (a) 0, (b) 5, (c) 10, (d) 15 at.% CrO
3setelah proses drying Hasil karakterisasi XRD setelah proses drying menunjukkan pola difraksi TiO
2dengan fasa anatase untuk semua komposisi (Gambar 1) Berdasarkan referensi pada ICDD pattern no. 03- 65-5714 untuk semua komposisi, struktur kristal fasa anatase (101) yang terbentuk adalah tetragonal. Pada pola difraksi ini, tidak ditemukan senyawa selain TiO
2baik berupa Kromium (Cr) maupun Ti yang berikatan dengan pelarut yang digunakan dalam proses sol gel dalam bentuk Ti(NO
3)
4. Hal ini mengindikasikan bahwa baik dopant maupun pelarut yang digunakan saat sol-gel tidak mengubah struktur kristalin TiO
2dan tidak teridentifikasinya dopant diprediksi bahwa doping telah terjadi dengan kemungkinan adanya substitusi pada struktur kristal TiO
2.
Defect/cacat yang memungkinkan terjadi adalah sebagai
berikut :
Gambar 2. Cacat substitusi yang dapat terjadi pada atom Cr yang menggantikan posisi Ti
Pada Gambar 2, menunjukkan terjadi substitusi Cr dalam
susunan kristal TiO
2menggantikan posisi Ti. Hal ini
dimungkinkan karena ukuran atom Cr dan Ti masing-masing
berdekatan yakni 0.69Å dan 0.68Å.
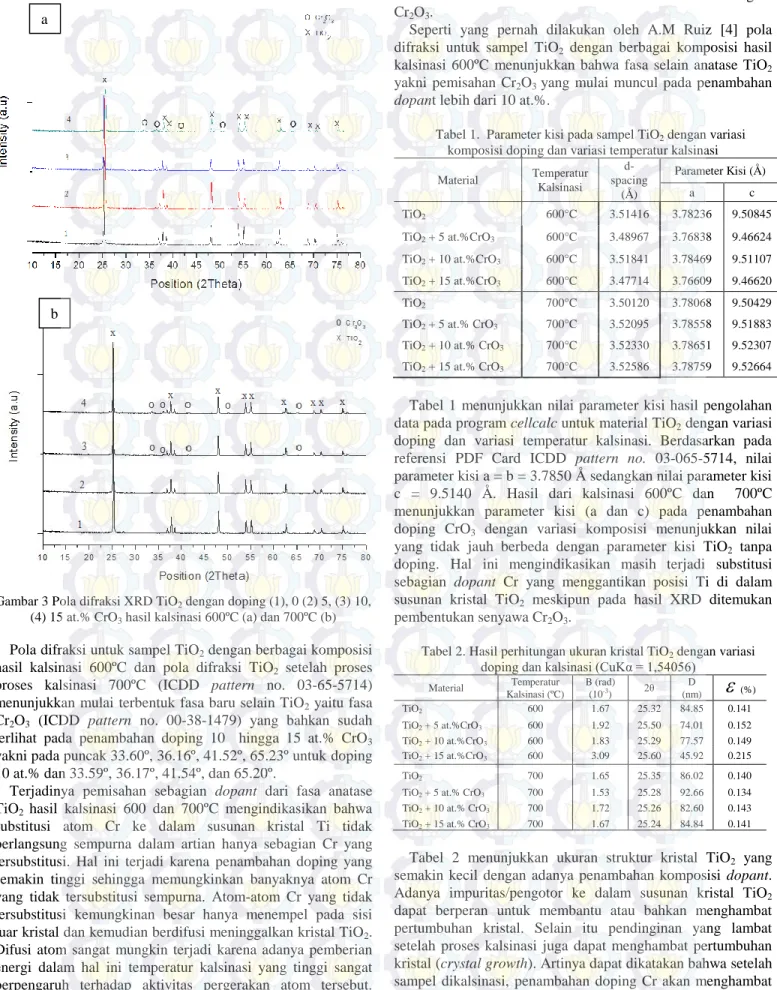
Gambar 3 Pola difraksi XRD TiO2 dengan doping (1), 0 (2) 5, (3) 10, (4) 15 at.% CrO3 hasil kalsinasi 600ºC (a) dan 700ºC (b)
Pola difraksi untuk sampel TiO
2dengan berbagai komposisi hasil kalsinasi 600ºC dan pola difraksi TiO
2setelah proses proses kalsinasi 700ºC (ICDD pattern no. 03-65-5714) menunjukkan mulai terbentuk fasa baru selain TiO
2yaitu fasa Cr
2O
3(ICDD pattern no. 00-38-1479) yang bahkan sudah terlihat pada penambahan doping 10 hingga 15 at.% CrO
3yakni pada puncak 33.60º, 36.16º, 41.52º, 65.23º untuk doping 10 at.% dan 33.59º, 36.17º, 41.54º, dan 65.20º.
Terjadinya pemisahan sebagian dopant dari fasa anatase TiO
2hasil kalsinasi 600 dan 700ºC mengindikasikan bahwa substitusi atom Cr ke dalam susunan kristal Ti tidak berlangsung sempurna dalam artian hanya sebagian Cr yang tersubstitusi. Hal ini terjadi karena penambahan doping yang semakin tinggi sehingga memungkinkan banyaknya atom Cr yang tidak tersubstitusi sempurna. Atom-atom Cr yang tidak tersubstitusi kemungkinan besar hanya menempel pada sisi luar kristal dan kemudian berdifusi meninggalkan kristal TiO
2. Difusi atom sangat mungkin terjadi karena adanya pemberian energi dalam hal ini temperatur kalsinasi yang tinggi sangat berpengaruh terhadap aktivitas pergerakan atom tersebut.
Sebagian atom Cr yang terdifusi dari susunan kristal TiO
2tersebut kemudian teroksidasi membentuk oksida logam Cr
2O
3.
Seperti yang pernah dilakukan oleh A.M Ruiz [4] pola difraksi untuk sampel TiO
2dengan berbagai komposisi hasil kalsinasi 600ºC menunjukkan bahwa fasa selain anatase TiO
2yakni pemisahan Cr
2O
3yang mulai muncul pada penambahan
dopant lebih dari 10 at.%.Tabel 1. Parameter kisi pada sampel TiO2 dengan variasi komposisi doping dan variasi temperatur kalsinasi Material Temperatur
Kalsinasi d- spacing
(Å)
Parameter Kisi (Å)
a c
TiO2 600°C 3.51416 3.78236 9.50845
TiO2 + 5 at.%CrO3 600°C 3.48967 3.76838 9.46624 TiO2 + 10 at.%CrO3 600°C 3.51841 3.78469 9.51107 TiO2 + 15 at.%CrO3 600°C 3.47714 3.76609 9.46620
TiO2 700°C 3.50120 3.78068 9.50429
TiO2 + 5 at.% CrO3 700°C 3.52095 3.78558 9.51883 TiO2 + 10 at.% CrO3 700°C 3.52330 3.78651 9.52307 TiO2 + 15 at.% CrO3 700°C 3.52586 3.78759 9.52664
Tabel 1 menunjukkan nilai parameter kisi hasil pengolahan data pada program cellcalc untuk material TiO
2dengan variasi doping dan variasi temperatur kalsinasi. Berdasarkan pada referensi PDF Card ICDD pattern no. 03-065-5714, nilai parameter kisi a = b = 3.7850 Å sedangkan nilai parameter kisi c = 9.5140 Å. Hasil dari kalsinasi 600ºC dan 700ºC menunjukkan parameter kisi (a dan c) pada penambahan doping CrO
3dengan variasi komposisi menunjukkan nilai yang tidak jauh berbeda dengan parameter kisi TiO
2tanpa doping. Hal ini mengindikasikan masih terjadi substitusi sebagian dopant Cr yang menggantikan posisi Ti di dalam susunan kristal TiO
2meskipun pada hasil XRD ditemukan pembentukan senyawa Cr
2O
3.
Tabel 2. Hasil perhitungan ukuran kristal TiO2 dengan variasi doping dan kalsinasi (CuKα = 1,54056)
Material Temperatur Kalsinasi (ºC)
B (rad)
(10-3) 2θ D
(nm)
(%)TiO2 600 1.67 25.32 84.85 0.141
TiO2 + 5 at.%CrO3 600 1.92 25.50 74.01 0.152 TiO2 + 10 at.%CrO3 600 1.83 25.29 77.57 0.149 TiO2 + 15 at.%CrO3 600 3.09 25.60 45.92 0.215
TiO2 700 1.65 25.35 86.02 0.140
TiO2 + 5 at.% CrO3 700 1.53 25.28 92.66 0.134 TiO2 + 10 at.% CrO3 700 1.72 25.26 82.60 0.143 TiO2 + 15 at.% CrO3 700 1.67 25.24 84.84 0.141
Tabel 2 menunjukkan ukuran struktur kristal TiO
2yang semakin kecil dengan adanya penambahan komposisi dopant.
Adanya impuritas/pengotor ke dalam susunan kristal TiO
2dapat berperan untuk membantu atau bahkan menghambat pertumbuhan kristal. Selain itu pendinginan yang lambat setelah proses kalsinasi juga dapat menghambat pertumbuhan kristal (crystal growth). Artinya dapat dikatakan bahwa setelah sampel dikalsinasi, penambahan doping Cr akan menghambat pertumbuhan kristal. Sama seperti penelitian yang dilakukan a
b
oleh B. Lyson [3], dengan proses Flame Spray Synthesis nya mengatakan bahwa penambahan komposisi Cr menunjukkan semakin kecil ukuran kristal TiO
2yang terbentuk.
III.2 Identifikasi Morfologi Partikel
Gambar 4 Foto hasil karakterisasi SEM serbuk TiO2 doping (a) 0, (b) 5 at.% CrO3 hasil setelah drying dengan perbesaran 2.000x
Gambar 5 Foto SEM TiO2 doping (a), 10 dan (b) 15 at% CrO3 hasil kalsinasi 600ºC, (c) 10 dan (d) 15 at.% CrO3 hasil kalsinasi 700ºC
hasil perbesaran 50.000x
Hasil karakterisasi SEM setelah kalsinasi dengan variasi temperatur menunjukkan bentuk yang lebih seragam dan cenderung berbentuk bulat (spherical). Ukuran partikel rata- rata sudah menunjukkan material mendekati ukuran nanomaterial, dibandingkan hasil setelah drying yang masih berupa aglomerasi dengan skala yang cukup besar meskipun juga masih tampak sedikit aglomerasi pada TiO
2hasil kalsinasi. Hal ini menunjukkan untuk memecah dan mengurangi aglomerasi hingga menghasilkan ukuran partikel yang mendekati ukuran nanomaterial pada TiO
2dibutuhkan temperatur sintesa yang tinggi. Ukuran rata-rata partikel yang dihasilkan setelah kalsinasi berkisar 106.28-173.85. Hasil kalsinasi 700ºC (Gambar 5c dan 5d) memperlihatkan adanya aglomerasi yang lebih besar dibandingkan hasil kalsinasi 600ºC (Gambar 5a dan 5b). Sehingga tampak ukuran rata-rata partikel yang dihasilkan pada kalsinasi 700ºC lebih besar dibandingkan hasil kalsinasi 600ºC. Hal ini dikarenakan sifat kimia TiO
2yang higroskopik sehingga mudah untuk menyerap
air pada lingkungannya dan masih adanya kandungan air selepas drying menyebabkan TiO
2mudah untuk aglomerasi.
III.3 Identifikasi Luas Permukaan Aktif
Tabel 3. Hasil pengujian BETMaterial
BET Surface Area (m2/g) Diameter Pori (nm)
Kalsinasi 600ºC
Kalsinasi 700 ºC
Kalsinasi 600 ºC
Kalsinasi 700 ºC
TiO2 6.767 69.17 133.177 52.272
TiO2 + 5 at.%CrO3 12.338 12.338 3.386 3.386
TiO2 + 10 at.%CrO3 7.921 7.921 12.301 12.301
TiO2 + 15 at.%CrO3 8.685 8.685 3.4 12.278
Hasil pengujian BET menunjukkan Specific Surface Area (SSA) dalam rentang 6.767-69.17 m
2/g. Luas permukaan aktif pada sampel TiO
2dengan doping hasil kalsinasi dengan temperatur yang berbeda menunjukkan nilai yang lebih konsisten dalam menyerap gas ke dalam pori partikel dibandingkan nilai luas permukaan pada sampel TiO
2tanpa doping. Nilai luas permukaan yang besar pada TiO
2tanpa doping hasil kalsinasi 700ºC bisa jadi dikarenakan aglomerasi yang sangat kecil yang mana akan membentuk ukuran rata-rata partikel yang kecil sehingga memberikan luas permukaan aktif yang besar.
Diameter pori material menggambarkan ukuran molekul yang dapat diserap hingga ke dalam partikel suatu material.
Hasil pengujian BET menunjukkan diameter pori material TiO
2untuk semua komposisi. sampel berada pada rentang 3,386-133,177 nm. Ukuran diameter pori TiO
2tanpa doping setelah kalsinasi 600ºC dan 700ºC termasuk jenis macropores karena memiliki ukuran pori > 50 nm, sedangkan komposisi lainnya termasuk jenis micropores karena memiliki ukuran pori < 50 nm.
III.4 Identifikasi Pengaruh Termal
Sampel yang digunakan pada pengujian ini haruslah berbentuk serbuk. Kecepatan pemanasan pada pengujian ini sebesar 10ºC/min dan dipanaskan hingga temperatur 600ºC.
Gambar 6. Kurva TGA pada TiO
2tanpa doping hasil drying Pada gambar 6 menunjukkan berat sampel TiO
2tanpa doping mulai berkurang pada temperatur 25ºC hingga temperatur 600ºC. Mula-mula pada temperatur kamar hingga 60ºC terjadi pengurangan berat sebesar 0.82%. Kemungkinan fenomena yang terjadi sekitar temperatur tersebut adalah penguapan H
2O yang masih tertinggal secara fisik di permukaan sampel setelah drying. Kemudian pada temperatur
a b
a b
c d
60ºC hingga temperatur 200ºC berat terus berkurang sebesar 3.17%. Pada range temperatur tersebut, sampel terus melepaskan residu air fisik dan oksidasi komponen organik hasil sol-gel. Setelah temperatur 200ºC hingga temperatur 230ºC, material mengalami dekomposisi berat yang sangat banyak yakni sebesar 3.54%. Pada temperatur tersebut dapat diprediksi fenomena yang terjadi adalah proses kalsinasi berlangsung dengan menghilangkan unsur-unsur volatil yang terkandung di dalam senyawa TiO
2. Setelah itu pada temperatur 230ºC hingga temperatur 600ºC sampel menunjukkan kestabilan dengan adanya perubahan temperatur.
Gambar 7. Grafik TGA pada TiO
2dengan doping 15 at.%CrO
3hasil drying
Pada gambar 7 menunjukkan kurva hasil pengujian TGA pada TiO
2dengan doping 15 at.%CrO
3hasil proses drying.
Kurva TGA mulai menunjukkan penurunan berat pada temperatur kamar hingga temperatur 600ºC. Mula-mula pada temperatur kamar hingga 60ºC terjadi pengurangan berat sebesar 1.64%. Fenomena yang terjadi berupa penguapan air yang berikatan secara fisik dengan sampel pasca proses sol-gel dan drying. Kemudian pada temperatur 60ºC hingga temperatur 330ºC berat sampel terus berkurang sebesar 3.83%
dengan prediksi berat yang hilang adalah air kristal dan komponen organik hasil drying setelah sol-gel. Setelah itu pada temperatur 330ºC mulai terlihat awal terjadinya proses kalsinasi hingga pada temperatur 412ºC terjadi penurunan berat sampel sebesar 0.92%. Sampel terus berkurang pada temperatur 412ºC hingga temperatur 600ºC, berat sampel yang berkurang sebesar 1.69% atau sekitar 0.3737 gr, berat sampel yang hilang ini dimungkinkan terjadi dekomposisi material doping CrO
3dengan melepaskan gas O
2hingga munculnya Cr
2O
3dengan reaksi sebagai berikut:
2CrO
3Cr
2O
3+ 3/2O
2………...(3) Besarnya berat (gr) untuk 1 mol O
2menurut perhitungan dengan persamaan mol diperoleh sebesar 0.4224. Hasil perhitungan berdasarkan persamaan mol dengan hasil pengurangan berat dari grafik TGA hampir berdekatan, sehingga kemungkinan besar berat sisa yang hilang mulai temperatur sekitar 412ºC hingga temperatur 600ºC adalah berat O
2yang terdesorbsi. Hal ini semakin memperkuat pola difraksi untuk sampel TiO
2dengan doping 15 at.%CrO
3setelah dikalsinasi 600ºC dan 700ºC yang menunjukkan munculnya pemisahan Cr
2O
3. Sama seperti halnya penelitian yang dilakukan oleh B. Lyson [3], menyebutkan bahwa material TiO
2tanpa doping hingga doping Cr sebesar 0.5 at.%
mengalami pengurangan berat hingga temperatur 400ºC, setelah itu material tidak mengalami perubahan berat lagi.
Sedangkan material TiO
2dengan doping di atas 0.5 at.%
mengalami pengurangan berat hingga di atas temperatur 400ºC dengan prediksi berat yang terdekomposisi adalah berat oksigen yang dilepas dari senyawa dopant CrO
3.
a
b
Gambar 8 Kurva TGA dan DTA pada TiO
2tanpa doping hasil setelah kalsinasi (a) 600ºC dan (b) 700ºC Pada gambar 8, kurva TGA dan DTA menunjukkan perubahan berat (%) sampel TiO
2tanpa doping hasil kalsinasi 600ºC dan 700ºC terhadap perubahan temperatur.
Pengujian ini dilakukan untuk mengetahui respon material TiO
2hasil kalsinasi terhadap lingkungan dengan perlakuan termal yang diberikan. Kurva hasil pengujian TGA kemudian dianalisis dengan melakukan 1
st derrivativeuntuk memperoleh kurva DTA yang lebih menjelaskan peristiwa apa saja yang terjadi sehingga dapat dianalisis tiap perubahan temperaturnya. Gambar 8a menunjukkan kurva DTA TiO
2hasil kalsinasi 600ºC stabil pada temperatur kamar hingga temperatur 210ºC. Kemudian terjadi perubahan berat pada temperatur 210ºC hingga temperatur 480ºC sebesar 1.15%. Asumsi yang terjadi adalah dekomposisi material tersebut. Selanjutnya pada temperatur di atas 500ºC material pada kondisi stabil dalam merespon lingkungannya. Adanya pengurangan berat pada temperatur 210 hingga 480ºC menunjukkan bahwa material tersebut mengalami ketidkstabilan apabila beroperasi pada temperatur di atas 210ºC.
Berbeda dengan kurva DTA TiO
2hasil kalsinasi
700ºC (Gambar 8b), material mengalami perubahan berat
pada temperatur kamar hingga temperatur 150ºC. Pada
temperatur tersebut fenomena yang terjadi adalah penguapan
air yang berikatan secara fisik dengan sampel. Hal ini
dikarenakan sifat material TiO
2yang higroskopi mampu
menyerap uap air pada lingkungannya. Setelah temperatur
150ºC hingga temperatur 600ºC sampel cenderung stabil
dalam menanggapi lingkungannya. Bahkan kurva TGA
menunjukkan adanya penambahan berat yang
mengindikasikan adanya gas yang teradsorpsi ke permukaan
sampel. Dari kedua kurva tersebut menunjukkan bahwa material TiO
2hasil kalsinasi 600ºC menunjukkan kestabilan yang lebih baik dari TiO
2hasil kalsinasi 700ºC dalam merespon lingkungan dengan temperatur rendah.
a
b
Gambar 9. Kurva TGA dan DTA pada TiO
2dengan doping 15 at.%CrO
3hasil setelah kalsinasi (a) 600ºC dan (b) 700ºC Gambar 9 menunjukkan kurva TGA dan DTA pada TiO
2dengan doping 15 at.%CrO
3hasil setelah kalsinasi 600ºC dan 700ºC. Kedua kurva DTA tersebut menunjukkan hasil yang identik yakni menunjukkan pengurangan berat mulai temperatur kamar hingga temperatur 160ºC pada sampel hasil kalsinasi 600ºC dan pengurangan berat hingga temperatur 190ºC pada sampel hasil kalsinasi 700ºC. Setelah itu kedua sampel tersebut menunjukkan kestabilan hingga temperatur 600ºC. Pada gambar 9b kurva TGA menunjukkan adanya penambahan berat yang mengindikasikan adanya adsorpsi gas dari lingkungan.
IV. KESIMPULAN
Material TiO
2dengan variasi pendopingan CrO
3dan variasi temperatur kalsinasi telah disintesis menggunakan metode sol-gel. Hasil karakterisasi dan beberapa pengujian dapat disimpulkan sebagai berikut :
1. Variasi temperatur kalsinasi dan variasi penambahan at.%
doping CrO
3memberikan pengaruh terhadap:
a. Ukuran kristal yang dihasilkan setelah dikalsinasi semakin kecil dengan penambahan komposisi dopant.
b. Adanya temperatur kalsinasi dan penambahan komposisi dopant mulai 10 at.%Cr juga menimbulkan terjadinya pemisahan sebagian atom Cr dari susunan kristal TiO
2hingga terbentuknya Cr
2O
3.
c. Temperatur kalsinasi juga dapat memecah dan mengurangi aglomerasi yang terjadi pada TiO
2. d. Luas permukaan aktif TiO
2dengan doping
menunjukkan nilai yang lebih konsisten dibandingkan
TiO
2tanpa doping pada temperatur kalsinasi yang berbeda.
e. Temperatur kalsinasi mendekomposisi CrO
3hingga melepaskan O
2yang menyebabkan terbentuknya Cr
2O
3. 2. Penambahan doping CrO
3ke dalam TiO
2menimbulkan
terjadinya defect yakni terjadinya substitusi atom Cr ke dalam susunan kristal TiO
2.
UCAPAN TERIMA KASIH
“Penulis S.S.N mengucapkan terima kasih kepada Direktorat Pendidikan Tinggi, Kementrian Pendidikan dan Kebudayaan Republik Indonesia yang telah memberikan dukungan finansial melalui Hibah Penelitian tahun 2012-2014”
kepada penulis, dosen pembimbing Hariyati Purwaningsih S.Si., M.Si. Penulis juga mengucapkan terima kasih kepada keluarga dan seluruh elemen Jurusan Teknik Material dan Metalurgi ITS yang selalu memberikan motivasi hingga terselesaikannya jurnal ini.
DAFTAR PUSTAKA
[1] Kittel, C. 1976. Introduction to Solid State Physics. USA : John wiley &
Sons
[2] Zakrzewska, K., Radecka, M., Rekas M, 1997. Effect of Nb, Cr, Sn additions on gas sensing properties of TiO2 thin films, Thin Solid Films 310 (1997) 161–166
[3] Sypiena, B., L., Czapla, A., Lubecka, M., Gwizdz, P., Schneider, K., Zakrzewska, K., Michalow, K., Graule, T., Reszka, A., Rekas, M., Lacz, A., Radecka, M.. 2012. Nanopowders of chromium doped TiO2 for gas sensors, Sens. and Actuators B 175 : 163– 172
[4] Ruiz, A.M., Sakai, G., Cornet, A., Shimanoe, K., Morante, J.R., Yamazoe, N. 2003. Cr-doped TiO2 gas sensor for exhaust NO2 monitoring, Sens. Actuators B Chem. 93 : 509–518
[5] Goetzberger, Adolf et.al. 1998. Crystalline Silicon Solar Cells.
Chichester: John Wiley & Sons Ltd.
[6] Rio, R., Iida, M. 1999. Fisika dan Teknologi Semikonduktor. Jakarta : Pradnya Paramita
[7] Devi, G. S., Hyodo, T., Shimizu, Y., Egashira, M. 2002. Synthesis of mesoporous TiO2-based powders and their gas-sensing properties, Sens. Actuators B : Chem. 87 : 122–129
[8] Hanaor, Dorian, A., H., Sorrell, Charles, C. 2011. "Review of the anatase to rutile phase transformation". Journal of Materials Science 46 (4): 855–874
[9] Qin, D,. Chang, W., Zhou, J., Chen, Y. 1994. An investigation of the preparation of TiO2-based catalysts using methods of thermal analysis, Thermochim. Acta 236 : 205–216J.
[10] Svehla, G. 1979. Vogel : Buku Teks Analisis Anorganik Kualitatif Makro dan Semimikro Ed. 5. Diterjemahkan oleh Setiono, L., Hadyana, A., Pudjaatmaka. Jakarta : Kalman Media Pustaka
[11] Lopez, R., Gomez, R., Ruiz, S., O. 2011. Photophysical and photocatalytic properties of TiO2–Cr sol–gel prepared semiconductors, Catal. Today 166 : 159–165
[12] Mackenzie J., D. 1982. J.Non-Cryst.Solids, 48 : 1-10
[13] Sun, Zhengfei. 2005. Novel Sol-Gel Nanoporous Materials, Nanocomposites and Their Applications in Bioscience. Thesis.
Drexel:Drexel University : 27-59.
[14] Widodo, S. 2010. “Teknologi Sol Gel pada Pembuatan Nano Kristalin Metal Oksida untuk Aplikasi Sensor Gas”. ISSN : 1411- 4216