Nostoc commune Vaucher ex Bornet & Flahault
SEBAGAI FIKOREMEDIATOR LOGAM BERAT KADMIUM (Cd (II))
TESIS
Disusun Untuk Memenuhi Sebagian Persyaratan Mencapai Derajat Magister Program Studi Ilmu Lingkungan
Oleh
Rachmawati Prihantina Fauzi NIM A131208007
PROGRAM PASCASARJANA UNIVERSITAS SEBELAS MARET
ii
Nostoc commune Vaucher ex Bornet & Flahault
SEBAGAI FIKOREMEDIATOR LOGAM BERAT KADMIUM (Cd (II))
TESIS
Rachmawati Prihantina Fauzi NIM A131208007
Komisi
Pembimbing
Nama Tanda Tangan Tanggal
Pembimbing I Dr. M. Masykuri, M.Si.
NIP 19681124 199403 1 001 ………. ………
pembimbing II Dr. Sunarto, M.S.
NIP 19540605 199103 1 002 ………. ………
Telah dinyatakan memenuhi syarat pada tanggal...2014
Ketua Program Studi Ilmu Lingkungan
Program Pascasarjana UNS
Dr. Prabang Setyono, M.Si.
NIP 19720524 199903 1 002
iii
Nostoc commune Vaucher ex Bornet & Flahault
SEBAGAI FIKOREMEDIATOR LOGAM BERAT KADMIUM (Cd (II))
TESIS
Rachmawati Prihantina Fauzi NIM A131208007
Telah dipertahankan di depan penguji dan dinyatakan telah memenuhi syarat
pada tanggal... 2014
Tim Penguji :
Jabatan Nama Tanda Tangan Tanggal
Ketua Dr. Prabang Setyono, M.Si.
iv
PERNYATAAN ORISINALITAS DAN PUBLIKASI ISI TESIS
Yang bertanda tangan di bawah ini :
Nama : Rachmawati Prihantina Fauzi
NIM : A131208007
Program Studi : Ilmu Lingkungan
Menyatakan dengan sesungguhnya bahwa tesis yang berjudul “Nostoc commune
Vaucher ex Bornet & Flahault Sebagai Fikoremediator Logam Berat Kadmium (Cd (II))” adalah benar-benar karya saya sendiri dan belum pernah diajukan untuk memperoleh gelar kesarjanaan di suatu perguruan tinggi. Sepanjang pengetahuan
saya, tidak terdapat suatu karya atau pendapat yang pernah ditulis atau diterbitkan
oleh orang lain, kecuali secara tertulis diacu dalam naskah ini dan disebutkan
dalam pustaka.
Apabila dikemudian hari terbukti pernyataan saya tidak benar, maka saya bersedia
menerima sanksi akademik, berupa pencabutan gelar yang saya peroleh dari tesis
ini.
Surakarta, Agustus 2014
Rachmawati Prihantina Fauzi
v
MOTTO
“Boleh jadi kamu membenci sesuatu, padahal ia
amat baik bagimu dan boleh jadi pula kamu
menyukai sesuatu, padahal ia amat buruk
bagimu. Allah mengatahui, sedang kamu tidak
mengetahui”
-Qs: AL-Baqarah:216-
“Never regret anything that has happened in our
life. It can‟t be changed, undone or forgotten. So
take it as a lesson learned and move o
n”
-Motto pribadi-
“Qodarullahi wama sya‟a fa‟al, Alhamdulillah
„ala kulli hal”
-Doa & Dzikir Rasullullah-
“Ada malaikat yang ditugaskan untuk
mengamini apa yang kita katakan, maka
katakan kata-kata yang baik, indah, optimis,
dan jadikan itu sebagai ke
biasaan”
-Dr. Salman Al-Audah-
vi
HALAMAN PERSEMBAHAN
Karya ilmiah ini penulis persembahkan untuk:
Kedua orang tua yang kuhormati (Hasan Fauzi, MBA.Ak., Ph.D. dan Dra.
Isnawati) atas seluruh cinta, pengorbanan, nasehat, dukungan dan doa
yang tak pernah putus.
Adik-adik yang kusayangi (dr. Cholifatur Ravita Fauzi dan Khoirul Nasrullah Fauzi) atas kasih sayang, pengertian dan dukungannya serta
bantuannya selama penelitian di Laboratorium.
Sahabat-sahabatku (Lila imami, S.Si., Indriana Saraswati, S.Si., dan Farida Nur Fuadiyah, S.Si.) atas persahabatan, nasehat, dukungan dan
kesediaannya berbagi dalam suka maupun duka.
Teman-temanku tersayang (Dhina Selvia, S.Si. dan Siti Rachmawati, M.Si.) atas kebersamaan, pesaudaraan dan bantuan yang senantiasa
diberikan.
Teman-teman seperjuangan di Program Studi Ilmu Lingkungan
Pascasarjana UNS angkatan 2012 (Pak Sammy, Mbak Novi, Bu Yuni, Mas
Danang, Pak SBY, Mas Hendro, Pak Firman, Pak Alex, Mommy Lerato
dan Akmal) atas kebersamaan, nasehat dan persaudaraannya selama 2
tahun ini.
vii
KATA PENGANTAR
Puji syukur penulis panjatkan kepada Allah SWT yang merupakan Tuhan
semesta alam atas segala limpahan rahmat dan hidayah-Nya sehingga penulis
dapat menyelesaikan penyusunan naskah tesis yang berjudul “Nostoc commune Vaucher ex Bornet & Flahault Sebagai Fikoremediator Logam Berat
Kadmium (Cd (II))”. Naskah Tesis ini disusun untuk memenuhi sebagian
persyaratan guna mencapai derajat Magister pada Program Studi Ilmu
Lingkungan di Universitas Sebelas Maret, Surakarta.
Penulis menyadari bahwa dalam pelaksanaan penelitian hingga
penyusunan naskah ini tidak terlepas dari bimbingan, bantuan dan dukungan dari
berbagai pihak. Oleh karena itu, pada kesempatan ini penulis ingin mengucapkan
terimakasih kepada:
1. Prof. Dr. Ravik Karsidi, M.S., selaku Rektor Universitas Sebelas Maret
Surakarta.
2. Prof. Dr. Ir. Ahmad Yunus, M.S., selaku Direktur Program Pascasarjana
Universitas Sebelas Maret Surakarta.
3. Dr. Prabang Setyono, M.Si. selaku Ketua Program Studi Ilmu Lingkungan,
Program Pascasarjana Universitas Sebelas Maret Surakarta sekaligus dosen
penguji atas kesediaanya dalam memberikan arahan dan masukan selama
penyusunan naskah sehingga naskah tesis ini dapat terwujud.
4. Dr. Wiryanto, M.Si. selaku dosen penguji atas kesediaanya dalam
memberikan arahan dan masukan selama penyusunan naskah sehingga
naskah tesis ini dapat terwujud.
5. Dr. M. Masykuri, M.Si. selaku dosen pembimbing I tesis ini atas kesabaran,
bantuan, bimbingan dan arahan selama penyusunan proposal, penelitian
hingga naskah tesis ini dapat terwujud.
6. Dr. Sunarto, M.S. selaku Sekretaris Program Studi Ilmu Lingkungan
viii
dengan penuh kesabaran selama penyusunan proposal, penelitian hingga
naskah tesis ini dapat terwujud.
7. Prof. Dr. MTh. Sri Budiastuti, M.Si. atas motivasi yang terus diberikan dari
penyusunan proposal hingga penulisan naskah Tesis.
8. Kepada seluruh dosen dan staf Program Studi Ilmu Lingkungan Pascasarjana
Universitas Sebelas Maret, Surakarta.
9. Keluarga tercinta, terutama mamah dan papah, atas cinta, pengorbanan, doa,
nasehat dan dukungannya yang tak pernah putus sehingga penulis mampu
menyelesaikan penulisan naskah ini sesuai waktu yang diinginkan.
10.Seluruh staf laboratorium kimia dan biologi, laboratorium pusat MIPA UNS
atas kerjasama dan bantuannya selama penelitian berlangsung.
11.Semua pihak lain yang telah membantu, yang tidak dapat penulis sebutkan
satu persatu.
Akhir kata, penulis menyadari bahwa naskah ini masih jauh dari sempurna.
Oleh karena itu penulis mengharapkan saran dan kritik yang membangun. Semoga
naskah tesis ini dapat bermanfaat dan menambah khasanah pengetahuan bagi kita
semua.
Surakarta, Agustus 2014
Penulis
Rachmawati Prihantina Fauzi
NIM A131208007
ix
DAFTAR ISI
HALAMAN JUDUL ... i
HALAMAN PENGESAHAN PEMBIMBING TESIS ... ii
HALAMAN PENGESAHAN PENGUJI TESIS ... iii
PERNYATAAN ORISINALITAS DAN PUBLIKASI ISI TESIS ... iv
MOTTO ... v
BAB II. TINJAUAN PUSTAKA ... 7
A. Kajian Teori ... 7
1. Fikoremediasi ... 7
x
b. Fikoremediasi oleh Nostoc commune Vaucher ex Bornet & Flahault .. 18
1) Mekanisme Adsorbsi ... 18
2) Mekanisme Fikoremediasi ... 19
3) Kapasitas dan Efisiensi Fikoremediasi ... 21
4) Isoterm Adsorbsi ... 22
2. Logam Berat Kadmium (Cd) ... 24
a. Bahaya Logam Berat Kadmium (Cd) ... 25
b. Metode Pengukuran Kadmium (Cd) dengan Atomic Adsorption Spectrometer-Flame (FAAS) ... 26
3. Asas Lingkungan ... 29
B. Kerangka Berpikir ... 31
C. Hipotesis ... 33
BAB III. METODE PENELITIAN... 34
A. Lokasi dan Waktu Penelitian ... 34
B. Alat ... 34
C. Bahan ... 35
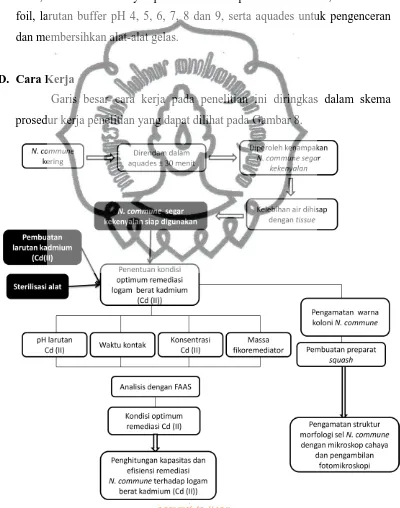
D. Cara Kerja ... 35
E. Analisis Data ... 39
BAB IV. HASIL PENELITIAN DAN PEMBAHASAN ... 41
A. Pengaruh pH Larutan Terhadap Remediasi Logam Berat Kadmium (Cd (II)) oleh Nostoc Commune ... 41
B. Pengaruh Lama Waktu Kontak Larutan Terhadap Remediasi Logam Berat Kadmium (Cd (II)) oleh Nostoc commune ... 44
C. Pengaruh Konsentrasi Ion Kadmium Terhadap Remediasi Logam Berat Kadmium (Cd (II)) oleh Nostoc commune ... 48
D. Pengaruh Massa Fikoremediator Terhadap Remediasi Logam Berat Kadmium (Cd (II)) oleh Nostoc commune ... 52
E. Efisiensi Remediasi dan Kapasitas Remediasi Nostoc commune Terhadap Logam Berat Kadmium (Cd (II)) Pada Kondisi Optimum ... 55
F. Penentuan Isoterm Adsorbsi ... 57
xi
BAB V. KESIMPULAN DAN SARAN ... 87
A. Kesimpulan ... 87
B. Saran ... 88
DAFTAR PUSTAKA ... 89
LAMPIRAN ... 96
xii
DAFTAR TABEL
Tabel Halaman
1. Variabel Pengamatan Koloni dan Struktur Morfologi Sel N.
commune... 40 2. Efisiensi Remediasi dan Kapasitas Remediasi Logam Berat
Kadmium (Cd (II)) Pada Variasi pH Larutan 4 – 9 ………….. 42
3. Efisiensi Remediasi dan Kapasitas Remediasi Logam Berat
Kadmium (Cd (II)) Pada Variasi Waktu Kontak 5 – 60
Menit... 46
4. Efisiensi Remediasi dan Kapasitas Remediasi Logam Berat
Kadmium (Cd (II)) Pada Variasi Konsentrasi Larutan
Kadmium 100 – 600 mg/L... 50 5. Efisiensi Remediasi dan Kapasitas Remediasi Logam Berat
Kadmium (Cd (II)) Pada Variasi Massa Fikoremediator 0,1 –
0,6 gram... 54
6. Nilai Efisiensi dan Kapasitas Remediasi N. commune Terhadap
Logam Berat Kadmium ( Cd (II))... 55
7. Variabel Pengamatan Koloni dan Struktur Morfologi Sel N.
commune Pada Berbagai Variasi pH... 66 8. Variabel Pengamatan Koloni dan Struktur Morfologi Sel N.
commune Pada Berbagai Variasi Waktu Kontak... 71 9. Variabel Pengamatan Koloni dan Struktur Morfologi Sel N.
commune Pada Berbagai Variasi Konsentrasi... 77 10.Penggolongan Tingkat Kerusakan Trikoma N. commune... 79 11.Variabel Pengamatan Koloni dan Morfologi Sel N. commune
Pada Berbagai Variasi Massa ... 85
12.Data Pengukuran Kadmium Pada Perubahan Berbagai Variasi
pH Terhadap Penyerapan Logam Berat Kadmium (Cd (II))
xiii
13.Data Pengukuran Kadmium Pada Perubahan Berbagai Variasi
Waktu Kontak Terhadap Penyerapan Logam Berat Kadmium
(Cd (II)) oleh N. commune... 97
14.Data Pengukuran Kadmium Pada Perubahan Berbagai Variasi
Konsentrasi Terhadap Penyerapan Logam Berat Kadmium (Cd
(II)) oleh N. commune... 98 15.Data Pengukuran Kadmium Pada Perubahan Berbagai Massa
Fikoremediator Terhadap Penyerapan Logam Berat Kadmium
(Cd (II)) oleh N. commune... 99 16.Data Perhitungan Isoterm Langmuir Untuk Adsorbsi Logam
Berat Kadmium (Cd (II)) oleh N. commune... 100 17.Data Perhitungan Isoterm Freundlich Untuk Adsorbsi Logam
Berat Kadmium (Cd (II)) oleh N. commune... 100
xiv
DAFTAR GAMBAR
Gambar Halaman
1. Koloni Nostoc commune (Jamur Selo) di Hutan Wanagama,
Gunung Kidul (Fauzi, 2011)... 8
2. Morfologi Sel Nostoc commune (Wahyudewi, 2009)... 11
3. Koloni Nostoc commune Pada Kondisi Segar dan Kering (Fauzi, 2011)... 12
4. Kurva Pertumbuhan N. commune Pada Batch Kultur (Fogg & Thake,1987; Zoechrova, 2011)... 14
5. Skema Komponen Alat Atomic Adsorption Spectrometer-Flame (FAAS)... 28
6. Empat Belas Asas Lingkungan (Sastrawijaya, 2000)... 30
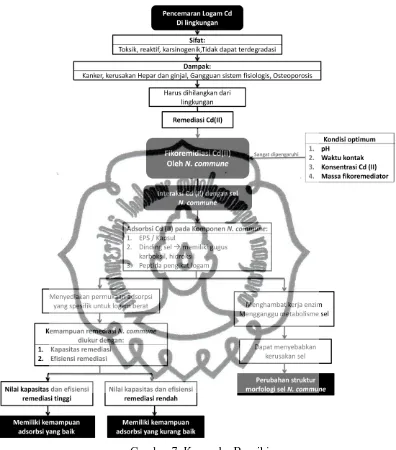
7. Kerangka Berpikir... 33
8. Skema Alur Kerja Penelitian... 35
9. Efisiensi Remediasi Cd (II) oleh N. commune Sebagai Fungsi dari Perubahan pH Larutan (Volume 20 mL, Konsentrasi 100 mg/L, Massa N. commune 0,2 gram)... 41
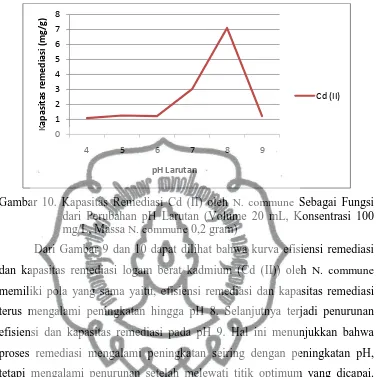
10. Kapasitas Remediasi Cd (II) oleh N. commune Sebagai Fungsi dari Perubahan pH Larutan (Volume 20 mL, Konsentrasi 100 mg/L, Massa N. commune 0,2 gram)... 42
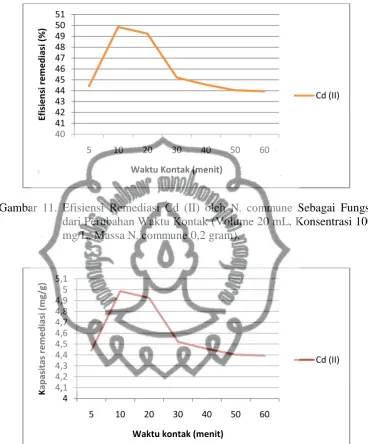
11. Efisiensi Remediasi Cd (II) oleh N. commune Sebagai Fungsi dari Perubahan Waktu Kontak (Volume 20 mL, Konsentrasi 100 mg/L, Massa N. commune 0,2 gram)... 45
12. Kapasitas Remediasi Cd (II) oleh N. commune Sebagai Fungsi dari Perubahan Waktu Kontak (Volume 20 mL, Konsentrasi 100 mg/L, Massa N. commune 0,2 gram)... 45 13.Efisiensi Remediasi Cd (II) oleh N. commune Sebagai Fungsi
dari Perubahan Konsentrasi Larutan (Volume 20 mL, Massa N.
xv
14.Kapasitas Remediasi Cd (II) oleh N. commune Sebagai Fungsi
dari Perubahan Konsentrasi Larutan (Volume 20 mL, Massa N.
commune 0,2 gram)... 49 15.Efisiensi Remediasi Cd (II) oleh N. commune Sebagai Fungsi
dari Perubahan Massa Fikoremediator (Volume 20 mL,
Konsentrasi Ion Kadmium 100 mg/L)... 53
16.Kapasitas remediasi Cd (II) oleh N. commune Sebagai Fungsi dari Perubahan Massa Fikoremediator (Volume 20 mL,
Konsentrasi Ion Kadmium 100 mg/L)... 53
17.Isoterm Langmuir Adsorbsi Logam Berat Kadmium (Cd (II))
oleh N. commune... 58 18.Isoterm Freundlich Adsorbsi Logam Berat Kadmium (Cd (II))
oleh N. commune... 58 19.Struktur Morfologi Sel N. commune Pada Perlakuan Berbagai
Variasi pH Larutan Ion Kadmium (Cd (II)) Pada Konsentrasi
100 mg/L. Perbesaran 400X... 63
20.Perubahan Warna Koloni N. commune Pada Perlakuan
Berbagai Variasi pH Larutan Ion Kadmium (Cd (II)) Pada
Konsentrasi 100 mg/L... 64
21.Struktur Morfologi Sel N. commune Pada Perlakuan Berbagai Variasi Waktu Kontak Pada Larutan Kadmium Konsentrasi 100
mg/L dan pH 8. Perbesaran 400x... 68
22.Perubahan Warna Koloni N. commune Pada Perlakuan
Berbagai Variasi Waktu Kontak dengan Larutan Kadmium
Pada Konsentrasi 100 mg/L dan pH 8... 69
23.Struktur Morfologi Sel N. commune Pada Perlakuan Berbagai Variasi Konsentrasi Larutan Kadmium dengan pH 8 dan Lama
Kontak 10 menit. Perbesaran 400x... 73
24.Perubahan Warna Koloni N. commune Pada Perlakuan
Berbagai Variasi Konsentrasi Larutan Kadmium dengan pH 8
xvi
25.Struktur Morfologi Sel N. commune Pada Perlakuan Berbagai Variasi Massa Fikoremediator dalam Larutan Kadmium dengan
pH 8 dan Lama Kontak 10 menit. Perbesaran 400x... 82
26.Perubahan Warna Koloni N. commune Pada Perlakuan
Berbagai Massa Fikoremediator dalam Larutan Kadmium
dengan pH 8 dan Lama Kontak 10 menit... 83
xvii
DAFTAR LAMPIRAN
Lampiran. Halaman
1. Data Pengukuran Kadmium... 96
2. Alat, Bahan Dan Hasil Penelitian... 101
3. Lampiran Peraturan Pemerintah Nomor 82 Tahun 2001
Tentang Pengelolan Kualitas Air Dan Pengendalian
Pencemaran
Air... 106
xviii
Rachmawati Prihantina Fauzi. NIM A.131208007. 2014. Nostoc commune
Vaucher ex Bornet & Flahault Sebagai Fikoremediator Logam Berat Kadmium (Cd (II)), TESIS, Pembimbing I: Dr. M. Masykuri, M.Si., II: Dr.
Sunarto, M.S., Program Studi Ilmu Lingkungan, Program Pascasarjana, Universitas Sebelas Maret Surakarta.
ABSTRAK
Nostoc commune Vaucher ex Bornet & Flahault diketahui mengandung berbagai gugus anion seperti amino, karboksil, hidroksi dan karbonil serta EPS (Ektraseluller Polymer Substance) yang menyediakan permukaan absorbsi spesifik untuk ion logam berat sehingga spesies ini dapat dimanfaatkan sebagai biomaterial penyerap bahan pencemar, khususnya logam berat. Penggunaan algae untuk menghilangkan bahan pencemar dari lingkungan disebut fikoremediasi. Fikoremediasi adalah salah satu upaya untuk mengatasi pencemaran Cd (II) di lingkungan. Kadmium merupakan salah satu logam berat non esensial yang bersifat toksik. Keberadaaanya yang berlebihan di dalam lingkungan akan membahayakan organisme disekitarnya, oleh karena itu keberadaannya di lingkungan harus di minimalkan atau dihilangkan. Penelitian ini bertujuan untuk
mengetahui kemampuan N. commune dalam meremediasi Cd (II) dan mempelajari
gambaran morfologi N. commune setelah terpapar kadmium.
Penelitian dilakukan dalam skala laboratorium menggunakan metode
batch. Penentuan kondisi optimum meliputi pH, waktu kontak, konsentrasi logam berat dan massa fikoremediator. Analisis Cd (II) diukur dengan menggunakan Spektrofotometri Serapan Atom Nyala (SSA Nyala). Setelah proses remediasi selesai, dilakukan pengamatan terhadap morfologi sel N. commune dengan membuat preparat squash.
Hasil menunjukkan bahwa kondisi optimal remediasi Cd (II) oleh N. commune diperoleh pada konsentrasi kadmium 100 mg/L pada pH 8 dengan waktu kontak 10 menit dan massa fikoremediator 0,6 gram. Analisis SSA menunjukan efisiensi remediasi tertinggi sebesar 98,92% dengan kapasitas remediasi sebesar 3,927 mg/g. N. commune mengalami kerusakan pada struktur sel setelah terpapar Cd (II) pada konsentrasi 200 mg/L – 600 mg/L.
Kata kunci: N. commune Vaucher ex Bornet & Flahault, fikoremediasi, logam berat, kadmium
xix
Rachmawati Prihantina Fauzi. NIM. A131208007. 2014. Ficoremediation of
Cadmium (Cd (II)) by Nostoc commune Vaucher ex Bornet & Flahault.
THESIS. Supervisor I: Dr. M. Masykuri, M.Si., II: Dr. Sunarto, M.S., Program Study of Environmental Science. Postgraduate Program of Sebelas Maret University, Surakarta.
ABSTRACT
Nostoc commune Vaucher ex Bornet & Flahault containing various anionic groups such as amino, carboxyl, hydroxyl and carbonyl and EPS (Ektraseluller Polymer Substance) that provides surface absorption. Therefore this species can be used as biomaterials absorbing pollutants, especially heavy metals. The usage of algae to remove pollutants from the environment is called phycoremediation. Phycoremediation is one of effort to eliminate the pollution of Cd (II) in the environment. Cadmium which is a non-essential heavy metal is toxic. Its presence excessively in the environment will harm the organism, therefore its should minimize or eliminated. This study aimed to determine the ability of N. commune
in remediation of cadmium (Cd (II)) and studied the morphological description of
N. commune after exposure to cadmium.
The study was conducted in a laboratory scale using the batch method. Determination of optimum conditions include pH, contact time, the concentration of heavy metals and mass ficoremediator. Cadmium was measured using Atomic Absorption Spectrophotometry-Flame (FAAS). After the remediation process is complete, then made morphologically observation of N. commune by making squash preparations.
The results showed that the optimal conditions remediation of kadmium (Cd (II)) by N. commune obtained on cadmium concentration of 100 mg /L at pH 8 with a contact time of 10 minutes and 0,6 gram mass of ficoremediator. AAS analysis showed the highest remediation efficiency as much as 98.92% with the remediation capacity of 3.927 mg/g. Cell structure of N. commune was damage after exposure to cadmium (Cd (II)) at a concentration of 200 mg/L -600 mg/L.
Keywords: N. commune Vaucher ex Bornet & Flahault, ficoremediation, heavy metals, cadmium
1
BAB I. PENDAHULUAN
A. Latar Belakang
Nostoc commune Vaucher ex Bornet & Flahault yang selanjutnya disebut N. commune diketahui memiliki banyak manfaat, baik bagi manusia maupun bagi lingkungan. Oleh karena kandungan proteinnya yang tinggi (20 – 60% per gram berat kering) dan kandungan asam amino esensial yang cukup lengkap (mensintesis 8 asam amino esensial, yaitu: metionin, valin, fenilalanin, histidin, isoleusin, leusin, arginin, dan lisin), N. commune telah lama dikenal dan dimanfaatkan oleh beberapa negara seperti China, Jepang,
Filipina, Amerika dan Indonesia sebagai bahan makanan kaya protein
(Trainor, 1978; Lee, 1989; Van Reine & Trono, 2001). N. commune dapat dimanfaatkan untuk menurunkan kadar kolesterol dalam darah (Mujib, 2012).
Hal ini dikarenakan adanya kandungan serat dan fitosterol pada N. commune
yang dapat menurunkan kelarutan kolesterol dan menghambat readsorbsi
asam empedu (Rasmussen et al., 2009). Penghambatan readsorbsi akan berakibat pada peningkatan sintesis asam empedu untuk memenuhi
kebutuhan tubuh. Asam empedu disintesis dari kolesterol, oleh karena itu
peningkatan sintesis asam empedu akan mengakibatkan penurunan kolesterol
dalam darah.
Bagi lingkungan, N. commune memiliki peran dalam perbaikan
kesuburan tanah, khususnya sebagai penyedia nitrogen dalam tanah. Peran N. commune sebagai penyedia nitrogen dalam tanah disebabkan karena kemampuannya dalam memfiksasi nitrogen bebas di alam dan mengubahnya
menjadi senyawa amonia, yang kemudian dilepaskan ke tanah sekelilingnya
untuk kemudian dapat digunakan oleh organisme lain sebagai sumber
nitrogen. N. commune juga dapat dimanfaatkan sebagai biomaterial penyerap bahan-bahan pencemar, khususnya logam berat, sebab spesies ini
mengandung berbagai gugus anion seperti amino, karboksil, hidroksil dan
berat (Morsy et al., 2011). Berdasarkan penelitian Volesky (2004) dalam Apriliani (2010) diketahui bahwa biomaterial yang mengandung gugus fungsi
amino, karboksil, sulfihidril, sulfat dan polisakarida memiliki kemampuan
adsorbsi yang baik (Apriliani, 2010). Oleh karena itu, perlu dilakukan
penelitian lebih lanjut mengenai potensi N. commune sebagai algae penyerap logam berat atau yang bisa disebut sebagai fikoremediator.
N. commune merupakan anggota dari Divisi Cyanophyta (algae biru), yang juga dikenal sebagai anggota dari Cyanobacteria (bakteri
hijau-biru). Penggolongan N. commune ke dalam Cyanobacteria dikarenakan anggota dari divisi Cyanophyta ini memiliki hubungan kekerabatan yang
lebih dekat dengan bakteri dibanding dengan algae eukariotik (Lee, 1989).
Anggota dari Divisi Cyanophyta ini banyak ditemukan tersebar luas di alam,
salah satu diantaranya adalah N. commune. Spesies ini memiliki cakupan distribusi yang sangat luas yaitu dari daerah tropis hingga ke kutub (Whitton
& Potts, 2000). Di Indonesia, N. commune dapat ditemukan di daerah Hutan Wanagama, Gunung Kidul. Di tempat tersebut, spesies ini banyak ditemukan
hidup secara berkoloni membentuk struktur makroskopis menyerupai Jamur Kuping yang menempel pada tanah atau bebatuan. Oleh masyarkat sekitar, koloni makroskopis N. commune disebut dengan sebutan Jamur Selo. Nama lokal tersebut diberikan karena strukturnya yang menyerupai Jamur Kuping
dan banyak ditemukan menempel di bebatuan (dalam bahasa Jawa, Selo
berarti batu), namun demikian penyebutan ini dirasa kurang tepat sebab
koloni ini tampak berwarna hijau-kebiruan yang menandakan adanya klorofil
sebagai pigmen fotosintesis yang tidak dimiliki oleh anggota Fungi
(Wahyudewi, 2009).
Pencemaran logam berat di lingkungan telah menjadi isu global,
dikarenakan perkembangan industri yang sangat pesat. Limbah buangan
industri, baik limbah cair, limbah padat maupun limbah gas memberikan
kontribusi dalam pelepasan logam berat di lingkungan. Salah satu logam berat
yang merupakan sumber polusi dan perlu dihilangkan adalah logam kadmium
keberadaanya tidak dibutuhkan sama sekali dalam tubuh dan cenderung
bersifat toksik. Kadmium memiliki sifat lentur, tahan tekanan, dan tahan
panas sehingga banyak dimanfaatkan untuk bahan campuran logam lain, dan
bahan campuran pembuatan keramik, enamel dan plastik. Logam ini juga
seringkali dimanfaatkan untuk melapisi plat besi dan baja karena kadmium
memiliki sifat tahan terhadap korosi (Lu, 2006). Selain itu, kadmium juga
dimanfaatkan untuk pembuatan pigmen cat dengan membentuk beberapa
garamnya seperti kadmium oksida yang dikenal sebagai kadmium merah dan
dalam pembuatan batu baterai, terutama baterai Ni-Cd (Sarjono, 2009).
Sumber pencemaran kadmium dapat berasal dari limbah industri baterai,
limbah industri plastik, limbah industri cat, limbah pabrik minyak, limbah
penyepuhan logam dan sedikit berasal dari pupuk fosfor. Limbah cair pada
industri-industri tersebut berkontribusi pada pelepasan logam kadmium ke
dalam lingkungan perairan. Keberadaan logam kadmium yang bersifat toksik
di lingkungan tentunya akan berdampak negatif pada makhluk hidup di
sekitarnya. Menurut Peraturan Pemerintah Nomer 82 tahun 2001 tentang
Pengelolaan Kualitas Air dan Pengendalian Pencemaran Air diketahui bahwa
baku mutu kadmium yang boleh dialirkan ke air permukaan adalah sebesar
0,01 mg/L. Oleh karena itu, kandungan logam berat khususnya kadmium
dalam limbah yang melebihi ambang batas seharusnya diminimalkan atau
bahkan dihilangkan terlebih dahulu sebelum dibuang ke lingkungan.
Keberadaan logam kadmium dalam lingkungan secara berlebihan
akan menimbulkan dampak yang luas baik secara langsung maupun tidak
langsung, sebab logam ini mudah diadsorbsi dan terakumulasi oleh tubuh
organisme. Menurut Food and Agriculture Organization (FAO) & World Health Organization (WHO) kadar kadmium yang dapat ditoleransi oleh manusia adalah sebesar 7 µ/kg berat badan (Sarjono, 2009). Keracunan logam
berat kadmium dapat menyebabkan kanker, kerusakan sebagian sistem saraf
yang menyebabkan kelumpuhan, serta menyebabkan kerusakan pada organ
vital manusia yaitu hepar dan ren.
Upaya untuk mengatasi pencemaran logam berat di lingkungan telah
banyak dilakukan, salah satunya adalah dengan fikoremediasi. Fikoremediasi
merupakan salah satu aplikasi bioremidiasi. Bioremediasi adalah upaya
membersihkan lingkungan dari bahan pencemar dengan mengunakan
agen-agen biologis. Pada fikoremediasi, agen-agen biologis yang digunakan adalah
algae, baik mikroalgae maupun makroalgae. Pemanfaatan algae sebagai
fikoremediator untuk menyerap bahan-bahan pencemar, khususnya logam
berat telah banyak diteliti. Beberapa diantaranya yaitu penggunaan Nostoc muscorum sebagai fikoremediator logam-logam berat Chromium (Cr), Timbal (Pb), Nikel (Ni) dan Perak (Ag) (Rai et al., 1990), penggunaan
Spirogyra sp. sebagai fikoremediator logam selenium (Se) (Mane et al., 2011) dan Penggunaan Anabaena variabilis, Aulosira sp., Nostoc muscorum,
Oscillatoria sp. dan Westiellopsis sp. sebagai fikoremediator logam kromiun (Cr) dn nikel (Ni) (Prameswari et al., 2009). Pemanfaatan algae sebagai fikoremediator memiliki beberapa kelebihan yaitu bahan bakunya mudah
diperoleh karena banyak terdapat di alam, mudah dibudidayakan, dan
memiliki biaya operasional rendah. Menurut Arifin (2003), suatu
fikoremediator dapat dikatakan murah apabila bahannya mudah didapat dan
memerlukan sedikit proses sehingga memiliki biaya operasional yang murah.
Dengan demikian metode fikoremediasi dapat digunakan sebagai salah satu
metode remediasi yang murah dan ramah lingkungan.
Pemanfaatan Nosctoc commune Vaucher ex Bornet & Flahault sebagai fikoremediator logam Timbal (Pb) telah dilaporkan oleh Zoechrova (2011).
Spesies ini memiliki potensi dalam mengadsorbsi logam timbal pada
konsentrasi 700 ppm tanpa menghambat pertumbuhannya. Sementara itu,
penelitian mengenai pemanfaatan N. commune sebagai fikoremediator logam kadmium (Cd) telah dilakukan sebelumnya dan dilaporkan bahwa biomassa
morfologi selnya setelah terpapar kadmium. Oleh karena itu perlu dilakukan
penelitian mengenai potensi N. commune sebagai fikoremediator logam berat kadmium (Cd) secara lebih lanjut. Dalam penelitian ini akan dipelajari
potensi N. commune dalam meremediasi logam berat, khususnya terhadap logam berat kadmium (Cd (II)).
B. Rumusan Masalah
Dari latar belakang di atas maka dapat dirumuskan permasalahan
sebagai berikut:
1. Berapakah nilai pH, waktu kontak, konsentrasi logam kadmium dan
massa fikoremediator optimum dalam meremediasi logam berat
kadmium (Cd (II))?
2. Berapakah efisiensi remediasi dan kapasitas remediasi N. commune
dalam meremediasi logam berat kadmium (Cd (II))?
3. Bagaimanakah struktur morfologi sel N. commune setelah terpapar logam berat kadmium (Cd (II)) sebagai fungsi dari perubahan derajat keasaman
(pH), waktu kontak, konsentrasi logam kadmium dan massa
fikoremediator?
C. Tujuan Penelitian
Berdasarkan rumusan masalah di atas, maka penelitian ini bertujuan
untuk:
1. Mengetahui nilai pH, waktu kontak, konsentrasi logam kadmium dan
massa fikoremediator optimum dalam meremediasi logam berat
kadmium (Cd (II)).
2. Mengetahui efisiensi remediasi dan kapasitas remediasi N. commune
dalam meremediasi logam berat kadmium (Cd (II)).
3. Mengetahui struktur morfologi sel N. commune setelah terpapar logam berat kadmium (Cd (II)) sebagai fungsi dari perubahan derajat keasaman
(pH), waktu kontak, konsentrasi logam kadmium dan massa
D. Manfaat Penelitian
Adapun manfaat yang ingin dicapai dalam penelitian ini adalah
sebagai berikut:
1. Manfaat Teoritis
a. Hasil penelitian ini diharapkan dapat menambah khasanah keilmuan di
bidang biologi lingkungan, khususnya dalam aplikasi penggunaan
agen biologis sebagai upaya pembersihan lingkungan dari pencemaran
logam berat.
b. Hasil penelitian ini diharapkan akan diperoleh informasi mengenai
kemampuan fikoremediasi N. commune terhadap logam berat
kadmium (Cd (II)) dengan melihat kondisi optimum, efisiensi,
remediasi, kapasitas remediasi sebagai fungsi dari variasi waktu
kontak, pH, konsentrasi logam berat kadmium dan massa
fikoremediator serta efeknya terhadap struktur morfologi sel N. Commune, dengan demikian akan diperoleh tambahan informasi
mengenai kemampuan N. Commune sebagai fikoremediator logam
bera tkadmium (Cd (II)) yang selanjutnya dapat digunakan sebagai
dasar penelitian lebih lanjut mengenai aplikasi N. commune.
2. Manfaat Praktis
a. Hasil penelitian ini diharapkan dapat dijadikan referensi untuk
pemanfaatan N. commune sebagai fikoremediator logam berat
kadmium (Cd (II)) untuk diterapkan pada limbah cair industri-industri
yang mengandung logam berat kadmium (Cd (II)) seperti industri
penyepuhan logam, industri batu baterai, industri plastik dan industri
cat sebelum di buang ke lingkungan.
b. Hasil penelitian ini diharapkan dapat memberikan tambahan informasi
kepada masyarakat dalam memilih dan memilah N. commune yang akan digunakan sebagai bahan makanan.
7
BAB II. TINJAUAN PUSTAKA
A. Kajian Teori 1. Fikoremediasi
Fikoremediasi merupakan salah satu aplikasi bioremediasi dalam
membersihkan bahan pencemar dari lingkungan dengan menggunakan agen
biologis berupa algae. Lebih lanjut oleh Priadie (2012) bioremediasi
didefinisikan sebagai upaya pembersihan lingkungan dari bahan pencemar
dengan memanfaatkan proses biologis dan agen-agen biologis. Agen biologis
yang dapat digunakan untuk meremediasi yaitu mikroorganisme, fungi,
tumbuhan dan algae. Penggunaan fungi dalam remediasi lingkungan disebut dengan “Mikoremediasi” (berasal dari kata, Mykes = fungi dan remediasi = proses perbaikan lingkungan). Penggunaan tumbuhan untuk meremediasi lingkungan tercemar disebut dengan “Fitoremediasi” (berasal dari kata,
phyton= tumbuhan dan remediasi = proses perbaikan lingkungan), sedangkan penggunaan algae dalam meremediasi lingkungan disebut dengan “Fikoremediasi” (berasal dari kata phycos = algae dan remediasi = proses perbaikan lingkungan). Mikoremediasi, Fitoremediasi dan Fikoremediasi
merupakan aplikasi dari bioremediasi. Oleh karena itu, fikoremediasi dapat
didefnisikan sebagai salah satu aplikasi bioremediasi yang menggunakan
agen biologis yang berupa algae, baik itu mikroalgae maupun makroalgae
untuk membersihkan bahan-bahan pencemar dari lingkungan
Penelitian yang memanfaatkan algae sebagai fikoremediator telah
banyak dilakukan sebelumnya. Beberapa algae yang dapat digunakan sebagai
fikoremediator logam-logam berat yaitu Nostoc muscorum yang berpotensi sebagai adsorben logam-logam berat Kromium (Cr), Timbal (Pb), Nikel (Ni)
dan Perak (Ag) (Rai et al.,1990); Spirulina (Arthrospira) platensis berpotensi
dalam mengakumulasi timbal tanpa menghambat pertumbuhannya
(Zoechrova, 2011); dan Anabaena variabilis, Aulosira sp., Nostoc muscorum,
and Ni (II) dalam kondisi segar dibandingkan dalam kondisi “dorman”
(kering) (Prameswari et al., 2009). Selain algae yang telah disebutkan di atas, salah satu algae yang dapat dimanfaatkan sebagai fikoremediator logam berat
yaitu Nostoc commune Vaucher ex Bornet & Flahault.
a. Nostoc commune Vaucher ex Bornet & Flahault Sebagai Fikoremediator
1) Klasifikasi Nostoc commune
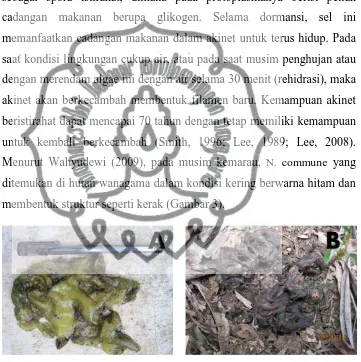
Jamur Selo adalah sebutan untuk koloni N. commune yang ditemukan di wilayah Hutan Wanagama, Gunung kidul. Spesies ini dapat
ditemukan hampir di seluruh wilayah Hutan Wanagama di Gunung
Kidul. Penyebutan Jamur Selo diberikan oleh masyarakat di sekitar
Hutan Wanagama karena melihat kenampakannya seperti Jamur Kuping
yang menempel di permukaan tanah dan bebatuan (dalam bahasa Jawa,
Selo berarti batu). Namun demikan, penyebutan ini sebenarnya dirasa kurang tepat sebab Jamur Selo (koloni N. commune) tampak bewarna hijau-kebiruan yang menandakan adanya klorofil sebagai pigmen
fotosintesis yang tidak dimiliki oleh anggota Fungi (Wahyudewi, 2009).
Gambaran koloni yang ditemukan di Hutan Wanagama, Gunung Kidul N.
commune disajikan pada Gambar 1.
Gambar 1. Koloni Nostoc commune (Jamur Selo) di Hutan Wanagama, Gunung Kidul (Fauzi, 2011)
Keterangan:
Berdasarkan identifikasi serta karakterisasi sel dan koloni yang
dilakukan oleh Wahyudewi (2009) diketahui bahwa algae hijau-biru
penyusun struktur Jamur Selo adalah spesies Nostoc commune Vaucher ex Bornet & Flahault. Berikut ini adalah klasifikasinya menurut Van
Spesies : Nostoc commune Vaucher ex Bornet & Flahault
N. commune merupakan spesies yang masih diperdebatkan klasifikasinya karena spesies ini juga dimasukkan kedalam Kingdom
Bacteria. Algae hijau-biru (Cyanophyta) lebih dikenal dengan sebutan
bakteri hijau-biru (Cyanobacteria), hal ini dikarenakan algae ini memiliki
hubungan yang lebih dekat dengan bakteri prokariotik dibandingkan
dengan algae eukaryotik (Lee, 1989). Berikut adalah klasifikasinya
menurut Guiry (2010):
Spesies : Nostoc commune Vaucher ex Bornet & Flahault Pengklasifikasian N. commune ke dalam Cyanobacteria mengacu pada organisasi sel algae yang bersifat prokaryotik serta hubungan
kekerabatan yang dekat dengan Eubacteria, sedangkan pengklasifikasian
algae yang dapat melakukan fotosintesis karena memiliki struktur
tilakoid yang menyerupai kloroplas pada sel tumbuhan (Hock et al.,
1995; Campbell et al., 2002). Menurut Lee (2008) anggota
Cyanobacteria memiliki beberapa karakteristik, yaitu: 1) sebagian besar
memiliki pigmen fotosintesis berupa klorofil a dan fikobiliprotein, 2)
memiliki produk simpanan dalam betuk glikogen, 3) memiliki dinding
sel yang menyerupai dinding sel bakteri gram negatif dan 4) memiliki
kapsul atau EPS (Extracellular Polymere Substance) berupa selebung lendir (mucilage) dan sedikit selulosa.
2) Nostoc commune
Nostoc merupakan spesies kosmopolitan yang dapat ditemukan pada habitat terestrial maupun akuatik; sebagai fitoplankton maupun
secara berkoloni; ditemukan menempel secara berkoloni di tanah yang
tidak tertutup oleh kanopi bersama dengan rumput-rumput yang lebat dan
lumut; maupun ditemukan berasosiasi dengan fungi sebagai komponen
fikobion dari lichen (Smith, 1966; Lee, 1989; Meeks, 1998, Dembitsky & Rezanka, 2005). N. commune dapat tumbuh optimal pada lingkungan dengan suhu 25 °C dan pH 6 – 7 (Whitton & Potts, 2000). Pada derajat
keasaman (pH) asam (pH kurang dari 4) spesies ini tidak mampu hidup
(Wahyudewi, 2009).
Menurut Trainor (1978), Casteholz & Waterbury (1989) dan Lee
(2008), N. commune merupakan algae filamentous dengan karakteristik filamen tidak bercabang yang merupakan ciri dari anggota Ordo
memiliki ukuran yang lebih besar dibandingkan dengan sel
vegetatif. Pada pengamatan dengan mikroskop cahaya, heterokis
tampak lebih jernih dibanding sel vegetatif (Gambar 2).
3. Akinet merupakan sel yang berperan sebagai spora istirahat pada
kondisi yang tidak menguntungkan dan akan berkecambah
membentuk filamen baru apabila kondisi lingkungan telah sesuai.
Secara umum, akinet juga memiliki ukuran yang lebih besar
dibanding dengan sel vegetatif. Pada pengamatan dengan
mikroskop cahaya akinet tampak jauh lebih gelap dibanding
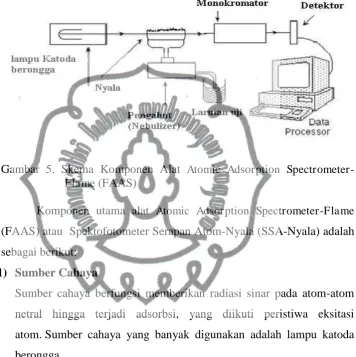
dengan sel vegetatif. Morfologi sel N. commune disajikan pada Gambar 2.
Gambar 2. Morfologi sel Nostoc commune (Wahyudewi, 2009)
Keterangan:
A. Kenampakan di bawah mikroskop cahaya perbesaran 1000X B. Kenampakan di bawah mikroskop cahaya perbesaran 400X ak = akinet; ht = heterokis; v = sel vegetatif
Struktur makroskopis Jamur Selo terbentuk karena adanya
selubung lendir (mucilage) berupa gelatin yang menyatukan filamen-filamen N. commune (Dodds et al., 1995; Wahyudewi, 2010). Selain berfungsi membentuk struktur makroskopis, selubung lendir tersebut
juga berfungsi melindungi sel dari kekeringan (Smith, 1966; Whitton &
Potts, 2000). Spesies ini melakukan reproduksi dengan pembelahan biner
yang dapat terjadi dengan cara perkecambahan akinet dan pembentukan
hormogonia (Trainor, 1978; Lee, 1989).
selama bertahun-tahun. Organisme seperti ini seringkali disebut sebagai
anhydrobiotics, yaitu organisme yang dapat bertahan untuk waktu yang lama pada kondisi kehilangan sebagian besar air di cairan intraselulernya
(Lee, 2008). Pada kondisi kekeringan, N. commune ini akan mengalami “dormansi”. Spesies ini mampu bertahan hidup karena adanya akinet sebagai spora istirahat, dimana pada protoplasmanya berisi penuh
cadangan makanan berupa glikogen. Selama dormansi, sel ini
memanfaatkan cadangan makanan dalam akinet untuk terus hidup. Pada
saat kondisi lingkungan cukup air, atau pada saat musim penghujan atau
dengan merendam algae ini dengan air selama 30 menit (rehidrasi), maka
akinet akan berkecambah membentuk filamen baru. Kemampuan akinet
beristirahat dapat mencapai 70 tahun dengan tetap memiliki kemampuan
untuk kembali berkecambah (Smith, 1996; Lee, 1989; Lee, 2008).
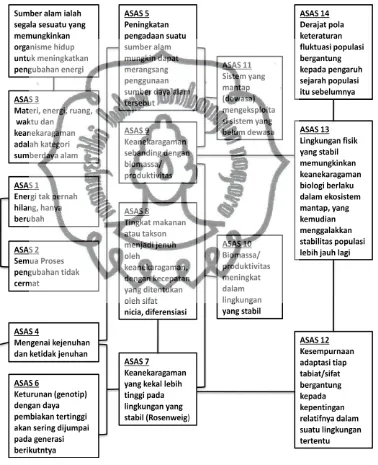
Menurut Wahyudewi (2009), pada musim kemarau, N. commune yang ditemukan di hutan wanagama dalam kondisi kering berwarna hitam dan
membentuk struktur seperti kerak (Gambar 3).
Gambar 3. Koloni Nostoc commune pada Kondisi Segar dan Kering (Fauzi, 2011)
Keterangan:
A. Kondisi segar yang ditemukan pada musim hujan B. Kondisi kering yang ditemukan pada Musim Kemarau
3) Manfaat Nostoc commune
N. commune telah lama dikenal dan dimanfaatkan sebagai bahan makanan oleh manusia. Sejak 1500 tahun lalu N. commune telah dimanfaatkan oleh masyarakat China sebagai bahan penyedap masakan
untuk makanan di kalangan kerajaan (Lee, 1898). Di Filipina dan Jepang
spesies ini dijadikan campuran mie dan salad. Di Amerika Serikat N. commune dijadikan bahan makanan dalam bentuk bola berwarna gelap yang disebut Nostoc ball (Trainor, 1978). Di Indonesia, oleh masyarakat
Gunung Kidul N. commune banyak dimanfaatkan sebagai bahan
makanan (Wahyudewi, 2009). Pemanfaatan N. commune sebagai bahan makanan kaya protein dikarenakan spesies ini memiliki kandungan
protein tinggi dan asam amino essensial yang penting bagi tubuh (Van
Reined & Trono, 2001). Pernyataan tersebut didukung oleh penelitian
Susilowati (2010) yang menyatakan bahwa N. commune mengandung 20,00 – 68,78% protein per gram berat keringnya. Spesies ini juga
mensintesis delapan asam amino essensial yang meliput: metionin, valin, fenilalanin, histidin, isoleusin, leusin, arginin dan lisin sehingga dapat dikatakan bahwa protein pada N. commune memilliki kualitas yang baik karena dapat menyediakan asam amino esensial yang dibutuhkan
manusia.
4) Pertumbuhan Nostoc commune dalam Batch Kultur
Kultur yang umum digunakan untuk percobaan dengan algae
adalah batch culture atau kultur sekali unduh. Hal ini dikarenakan sistem operasi batch culture tergolong sederhana dan cukup mudah dilakukan.
Batch culture merupakan kultur pada medium yang mengandung nutrien yang dibutuhkan dalam jumlah tertentu, tanpa ada pengurangan dan
penambahan dari luar. Pada kultur ini inokulan berupa sebagian kecil
populasi algae yang ditempatkan pada wadah kultur berisi medium
dengan jumlah tertentu dan diinkubasikan pada kondisi lingkungan yang
algae membutuhkan kondisi lingkungan yang cocok untuk dapat tumbuh
(Fogg & Thake, 1987; Lee et al., 2013). Oleh karena itu medium yang digunakan komposisinya disesuaikan dengan kebutuhan algae yang
dikulturkan (Fauzi, 2010). Pada metode batch seringkali terdapat endapan nutrien atau inokulan didasar wadah kultur jika dibiarkan dalam
waktu yang lama, oleh karena itu pengadukan atau mixing sangatlah penting. Pengadukan diperlukan untuk menjamin pertukaran nutrien dan
oksigen secara merata pada medium (Lee et al., 2013).
Batch culture memiliki persyaratan sterilasi yang rendah, yaitu tidak perlu dilakukan sterilisasi secara lengkap dengan membunuh semua
kontaminan yang ada. Metode yang digunakan adalah kultur unialgal, yaitu kultur satu jenis algae namun tidak bebas dari jamur dan bakteri.
Hal ini dikarenakan algae membutuhkan bantuan jamur dan bakteri untuk
dapat tumbuh optimal (Bouterfaz, 2002).
Gambar 4. Kurva Pertumbuhan N. commune Pada Batch Kultur (Fogg & Thake,1987; Zoechrova, 2011)
Keterangan:
1. Fase lag; 2. Fase eksponensial; 3. Fase stasioner; 4. Fase kematian
Dinamika populasi N. commune pada batch kultur dapat
digambarkan dengan kurva sigmoid (Gambar 4). Secara umum dinamika
populasi algae pada batch kultur dapat digambarkan melalui empat fase yaitu (Fogg & Thake, 1987):
1. Fase Lag
Berdasarkan penelitian Zoechrova (2011), N. commune mengalami fase lag pada hari pertama setelah inokulasi. Fase lag pada N. commune berlangsung selama beberapa jam setelah inokulasi dilakukan. Pada fase ini, algae mengalami perubahan lingkungan
(lingkungan kultur) yang berbeda dengan lingkungan sebelumnya.
Selama fase lag ini, algae menyesuaikan diri terhadap kondisi
lingkungan yang baru sehingga laju pertumbuhan menjadi rendah.
Organisme sering tidak mudah beradaptasi dengan lingkungan baru.
Sel menjadi sensitif terhadap suhu atau perubahan lingkungan
lainnya (Fogg & Thake, 1987). Pada saat fase lag, organisme tidak
mengalami penambahan jumlah yang signifikan, karena pada fase ini
terjadi stres fisiologis yang disebabkan terjadinya perbedaan
lingkungan tempat hidup. Lamanya fase ini tergantung dari jenis
algae dan jenis mediumnya. Hal in berkaitan dengan adaptasi algae
terhadap medium yang digunakan (Black, 2008).
2. Fase Eksponensial
Setelah algae beradaptasi terhadap kondisi medium yang diberikan,
sel masuk ke fase pertumbuhan. Dalam sebuah kultur, dimana ada
persediaan nutrien dan cahaya, maka biomassa algae akan bertambah
per waktu secara proposional. Pada fase ini jumlah nutrien masih
cukup banyak, oleh karena itu pertumbuhan terjadi secara
eksponensial yang ditandai dengan jumlah massa sel meningkat
seiring terhadap waktu dan sel-sel membelah pada laju yang konstan.
Keadaan ini sangat penting dalam menentukan keadaan kultur (Fogg
& Thake, 1987; Black, 2008; Zoechrova, 2011). Berdasarkan
penelitian Zoechrova (2011), N. commune mulai mengalami fase eksponensial pada hari pertama setelah inokulasi. Fase eskponensial
berlangsung selama 5 hari hingga hari ke-5.
3. Fase Stasioner
Pada fase ini suplai cahaya untuk sel algae menjadi terbatas yang
dikarenakan kepadatan kultur. Pada fase ini pembelahan sel mulai
berkurang. Jumlah sel baru sama dengan jumlah sel yang mati
sehingga pertumbuhan sel akan berlangsung secara konstan. Kurva
pertumbuhan menunjukkan mendekati nilai limit, yaitu fase stasioner
(Fogg & Thake, 1987; Black, 2008). Berdasarkan penelitian
Zoechrova (2011), tidak ditemukan adanya stasioner pada kurva
pertumbuhan N. commune. Hal ini dikarenakan, kemungkinan fase ini hanya terjadi selama beberapa jam pada hari 5 menuju hari
ke-6, sedangkan pengamatan yang dilakukan oleh Zoechrova adalah per
24 jam.
4. Fase Kematian
Fase ini merupakan berakhirnya fase stasioner, yaitu fase dimana
pertumbuhan terhambat dan populasi sel berkurang. Terjadinya fase
ini disebabkan oleh umur kultur yang sudah tua, suplai cahaya dan
nutrien yang terbatas sehingga tidak mendukung terjadinya
pembelahan sel. Pada fase ini laju kematian menjadi tinggi, jumlah
sel akan berkurang secara logaritmik yang diindikasikan dengan
garis lurus atau garis miring yang menurun dan populasi algae
menjadi rusak secara sempurna (Fogg & Thake, 1987; Black, 2008).
Berdasarkan penelitian Zoechrova (2011), N. commune mulai mengalami fase kematian pada hari ke 6. Fase kematian N. commune
terus berlangsung hingga hari ke-9.
Pertumbuhan algae dalam laboratorium sangat dipengaruhi oleh
beberapa faktor lingkungan, yaitu:
a. Suhu
Secara umum, algae dapat tumbuh pada kisaran suhu 16 – 17ºC.
Namun demikian, sebagian besar kultur algae diletakkan pada
algae dapat tumbuh optimal dalam ruangan dengan temperatur yang
konstan atau dengan variasi temperatur yang rendah (Trainor, 1978).
Menurut Whitton & Potts (2000), N. commune dapat tumbuh dengan optimal pada suhu 25ºC.
b. Cahaya
Cahaya memiliki peran penting bagi pertumbuhan algae, sebab
cahaya merupakan sumber energi bagi proses fotosintesis. Secara
umum algae mampu tumbuh pada kisaran cahaya dengan intensitas
1.000 – 10.000 Lux. Namun demikian algae dapat tumbuh optimal
dengan intensitas cahaya 2.500 – 5.000 Lux. Cahaya buatan yang
biasa digunakan di laboratorium ialah cahaya fluorescent dari lampu
pijar. Lampu ini akan menyediakan cahaya dengan kekuatan 4000 -
6000 Lux (Zoechrova, 2011).
c. Derajat Keasaaman (pH)
Setiap mikroorganisme memiliki pH optimum untuk dapat tumbuh
dengan optimal. Sebagian besar algae hanya dapat tumbuh optimal
pada kondisi lingkungan yang netral, yaitu dg pH berkisar antara 6 –
7 dan tidak dapat hidup pada pH yang lebih rendah, bahkan hanya 1
unit dari pH optimumnya. N. commune dapat tumbuh optimal pada kisaran pH 6 – 7 dan tidak dapat tumbuh pada kondisi pH Asam (di
bawah pH 4) (Whitton & Potts, 2000; Black, 2008).
d. Nutrisi
Pertumbuhan suatu organisme sangat dipengaruhi oleh nutrisi. Oleh
karena itu kultur algae harus diperkaya dengan nutrien untuk
melengkapi kekurangan nutrisi dalam medium kultur (Black, 2008;
Zoechrova, 2011).
e. Mixing
Mixing diperlukan untuk mencegah sedimentasi sel algae, menjamin pemerataan cahaya, pemerataan nutrien, dan meningkatkan
pertukaran gas antara medium kultur dan udara (Zoechrova, 2011;
Ariono, 1996).
b. Fikoremediasi oleh Nostoc commune Vaucher ex Bornet & Flahault 1) Mekanisme Adsorbsi
Adsorbsi merupakan suatu proses penyerapan zat tertentu oleh
suatu padatan yang terjadi pada permukaan zat padat karena adanya gaya
tarik atom atau molekul pada permukaan zat padat tersebut (Atkins,
1999). Ikatan yang bertanggung jawab dalam adsorbsi adalah gaya tarik
Van Der Waals, pembentukan ikatan nitrogen, pertukaran ion dan pembentukan ikatan kovalen (Apriliani 2010). Adsorbsi dapat terjadi
pada antarfasa, padat-cair, padat-gas atau gas-cair. Molekul yang terikat
pada bagian permukaan di sebut adsorbat, sedangkan permukaan yang
menyerap molekul-molekul adsorbat disebut adsorben.
Menurut Apriliani (2010) berdasarkan besarnya interaksi antara
adsorben dan adsorbat, adsorbsi dibedakan menjadi 2 macam, yaitu
adsorbsi fisika dan kimia.
a) Adsorbsi Fisika
Dalam adsorbsi fisika, molekul-molekul teradsorbsi pada permukaan
adsorben dengan ikatan yang lemah. Adsorbsi ini terjadi karena
adanya gaya tarik menarik yang lemah antara adsorbat dengan
permukaan adsorben, gaya ini disebut gaya Van Der Waals. Akibatnya adsorbat dapat bergerak dari satu bagian permukaan ke
bagian permukan lain dari adsorben. Adsorbsi ini berlangsung secara
cepat, dapat membentuk banyak lapisan dan bersifat balik
(reversible). Oleh karena itu molekul-molekul yang teradsorbsi mudah dilepaskan kembali.
b) Adsorbsi Kimia
Pada adsorbsi kimia, molekul-molekul yang teradsorbsi pada
permukaan adsorben bereaksi secara kimia, karena adanya reaksi
ikatan kovalen dengan ion sehingga terjadi pemutusan dan
pembentukan ikatan. Adsorbsi ini bersifat tidak balik (irreversible)
dan hanya membetuk lapisan tunggal.
Proses adsorbsi melalui pertukaran ion dan komplekasi hanya
berlangsung pada lapisan permukaan sel yang mempunyai situs-situs
yang bermuatan berlawanan dengan muatan ion logam sehingga
interaksinya merupakan reaksi pasif dan relatif cepat. Molekul adsorbat
secara kimiawi dianggap mempunyai situs aktif yang mampu berinteraksi
dengan logam permukan sel seperti fosfat, karboksil, amina dan amida.
Proses adsorbsi melalui pertukaran ion ini dipengaruhi oleh banyaknya
proton dalam larutan yang berkompetisi dengan ion logam pada
permukaan adsorben. Pada pH rendah kemelimpahan proton melimpah,
sehinga peluang terjadinya pengikatan logam relatif kecil (Apriliani,
2010).
2) Mekanisme Fikoremediasi
Fikoremediasi adalah upaya pembersihan lingkungan dari
bahan-bahan pencemar dengan menggunakan agen biologi berupa algae, baik
mikroalgae maupun makroalgae sebagai adsorben. Algae yang berperan
sebagai adsorben dapat disebut sebagai fikoremediator. Menurut
Apriliani (2010), pembersihan bahan pencemar dari lingkungan oleh
fikoremediator dapat terjadi melalui 2 cara, yaitu pengikatan aktif dan
pengikatan pasif. Pengikatan aktif melibatkan reaksi metabolisme yang
hanya terjadi pada fikoremediator dalam keadaan hidup (algae segar),
sedangkan pengikatan pasif tidak melibatkan reaksi metabolisme yang
terjadi pada penggunaan fikoremediator yang telah mati (algae kering).
Metode ini dilakukan dengan menggunakan cara batch atau statis, sebab kultur yang paling umum yang digunakan untuk percobaan dengan
algae adalah batch culture atau kultur statis. Metode ini tergolong mudah dan sederhana sehingga tidak membutuhkan biaya operasional yang
tinggi. Penggunaan algae sebagai agen biologis yang mudah diperoleh
serta metode batch sesuai dengan konsep fikoremediasi sebagai salah satu upaya penghilangan logam berat yang murah dan ramah lingkungan.
Proses fikoremediasi ini dilakukan dengan memasukan algae kedalam
suatu wadah berisi larutan dengan komponen logam berat yang
diinginkan, kemudian diaduk dalam waktu tertentu, dan dipisahkan
dengan cara penyaringan (Apriliani, 2010).
Mekanisme interaksi antara ion logam dan algae sangatlah
kompleks, namun pemahaman mengenai proses ini belum banyak
diketahui. Dinding sel algae mengandung berbagai gugus kation dan
anion termasuk gugus hidroksil, sulfihidril, karboksil dan amino.
Komponen dinding sel tersebut dan EPS (Extracellular Polymere Substance) menyediakan permukaan adsorpsi yang spesifik untuk ion logam yang ada dalam suatu larutan. Mekanisme ini melibatkan berbagai
interaksi seperti adsorpsi fisik, kimiawi, ion-exchange,dan complexation
(Wong & Tam, 1998; Crawford & Crawford, 1996).
Secara umum, proses pengambilan ion logam pada mikroalgae
melewati dua tahap yaitu rapid stage dan slow stage.
1) Rapid stage
Pada rapid stage, ion logam diadsorbsi secara langsung oleh permukaan sel dan EPS (Extracellular Polymere Substance) melalu mekanisme passive uptake atau biosorbsi yang terjadi secara cepat. Proses ini bersifat bolak baik dan cepat serta dapat terjadi pada sel
mati dan sel hidup dari suatu biomassa. Pada proses ini, ion logam
berat mengikat dinding sel dengan dua cara yang berbeda, yaitu:
a. Pertukaran ion monovalen dan divalen seperti Na, Mg, dan Ca
pada dinding sel yang digantikan oleh ion-ion logam berat
b. Formasi kompleks antara ion-ion logam berat dengan gugus
fungsional seperti karbonil, karboksil, amino, sulfihidril,
phospat, hidroksil dan fosfatyang berada pada dinding sel.
Pada tahap ini ion logam menjadi terakumulasi pada permukaan sel
2) Slow stage
Slow stage merupakan tahap selanjutnya yang membutuhkan waktu yang lebih lama. Pada tahap ini, ion logam yang terakumulasi di
permukaan sel ditranspor melalui membran sel menuju sitoplasma
dengan mekanisme active uptake. Active uptake dapat terjadi pada berbagai sel hidup. Mekanisme ini secara simultan terjadi dalam
proses konsumsi ion logam untuk pertumbuhan mikroorganisme
(Onrizal, 2005). Sebagai contoh yaitu logam kadmium (Cd)
Staphylococcus aureus yang ikut masuk kedalam sitoplasma bersamaan dengan transport aktif logam Mg. Pada tahap ini ion logam
menjadi terakumulasi di sitoplasma sebagai granula intraseluler.
Bioakumulasi intraselular terjadi karena adanya makromolekul berupa
peptida pengikat logam (metal-binding peptida) seperti
metallothioneins (MTs) dan fitokhelatin. Peptida pengikat logam merupakan peptida yang memiliki banyak mengandung asam amino
sistein dan memiliki berat molekul rendah. Akumulasi ion logam berat
terjadi karena adanya sisi pengikat ion logam dengan afinitas yang
tinggi (high affinity binding sites), yaitu Thiol (Sulfihidril, -SH). (Prasetyawati, 2009; Chen & Pan, 2005)
Proses biosorpsi logam berat oleh algae dipengaruhi oleh
beberapa faktor lingkungan seperti: pH media, konsentrasi logam berat,
waktu kontak antara algae dengan logam, sifat ion logam yang
digunakan, kehadiran ion logam lain, dan sistem biologis organisme yang
digunakan serta lingkungan tempat berlangsungnya proses tersebut
(Pinaz & Bonilla, 1991; Zoechrova, 2011).
3) Kapasitas dan Efisiensi Fikoremediasi
Kemampuan remediasi merupakan sebuah parameter yang
menunjukkan kerja sistem adsorbsi suatu adsorben dalam menyerap
adsorbat. Kemampuan remediasi suatu adsorben dapat diketahui dengan
remediasi. Menurut Apriliani (2010), fikoremediator yang baik adalah
adsorben yang memiliki kapasitas adsorbsi dan presentase penyerapan
tertinggi.
Presentase adsorbsi (Efisiensi adsorbsi) dapat dihitung dengan
menggunakan rumus:
�
=
�1−�2�1
× 100%
...(1) Sedangkan kapasitas adsorbsi dapat dihitung dengan menggunakanrumus:
�
=
�1−�2×
�
...(2)Keterangan:
Q = Kapasitas adsorbsi per bobot molekul (mg/g)
C1 = Konsentrasi awal larutan (mg/L)
C2 = Konsentrasi akhir larutan (mg/L)
m = Massa fikoremediator (g)
V = Volume larutan (L)
E = Efisiensi adsorbsi (%)
4) Isoterm Adsorbsi
Isoterm adsorbsi merupakan fungsi konsentrasi zat terlarut yang
terserap pada padatan terhadap konsentrasi larutan. Persamaan yang
digunakan untuk menjelaskan data percobaan isoterm dikaji oleh
Freundlich, Langmuir, serta Brauner, Emmet dan Teller (BET). Tipe
isoterm adsorbsi untuk mempelajari mekanisme adsorbsi pada fase
cair-padat pada umumnya menganut tipe isoterm Langmuir dan Freundlich
(Atkins, 1999).
Isoterm adsorbsi Langmuir merupakan proses adsorbsi yang
berlangsung secara kimisorpsi satu lapisan. Kimisorpsi adalah adsorbsi
yang terjadi melalui ikatan kimia yang sangat kuat antara sisi aktif
permukaan dengan sisi aktif molekul adsorbat dan dipengaruhi oleh
densitas elektron. Adsorbsi terjadi karena ikatan kimia biasanya bersifat
spesifik, sehingga permukaan adsorben mampu mengikat adsorbat
dengan satu lapisan (Apriliani, 2010).
Menurut Atkins (1999), isoterm Langmuir dapat diperoleh dari
persamaan:
C = konsentrasi adsorbat dalam larutan (mg/L)
Model isoterm Langmuir mendefinisikan bahwa kapasitas maksimum
terjadi akibat adanya lapisan tunggal (monolayer) adsorbat di
permukaan adsorben, dengan asumsi bahwa semua memiliki energi
yang sama dan adsorbsi bersifat dapat balik (irreversible) (Atkins, 1999; Handayani & Sulistiyono, 2009).
Isoterm Freundlich menggambarkan antara sejumlah komponen
yang teradsorbsi per unit adsorben dan konsentrasi komponen tersebut
pada kesetimbangan. Isoterm Freundlich dapat diperoleh dari
persamaan:
log
�= log
�
+
1log
�
...(4)dimana:
x/m = berat zat yang diadsorbsi (mg/g)
C = konsentrasi adsorbat dalam larutan (mg/L)
k, n = tetapan
Isoterm Freundlich menganggap bahwa semua sisi permukaan adsorben
akan terjadi adsorbsi pada kondisi yang diberikan. Isoterm ini
berdasarkan asumsi bahwa adsorben memiliki permukaan heterogen
dan tiap molekul mempunyai potensi adsorbsi yang berbeda-beda
(Apriliani, 2010; Handayani & Sulistiyono, 2009).
2. Logam Berat Kadmium (Cd)
Logam berat adalah semua jenis logam yang mempunyai berat jenis ≥
5g/cm3. Istilah logam berat secara khas mencirikan suatu unsur yang
merupakan konduktor yang baik, mudah ditempa, bersifat toksik dalam
biologi dan mempunyai nomor atom 22-92 dan terletak pada periode III dan
IV dalam sistem periodik unsur (Apriliani, 2010; Cotton &Wilkinson, 1986).
Kadmium (Cd) adalah logam berwarna putih keperakan, mengkilap
dan lunak dengan massa atom 112,41 g/mol dengan titik cair 594,26ºC dan
titik didih 1040ºC. Di dalam persenyawaan yang dibentuknya pada umumnya
memiliki bilangan valensi 2+ (Sunardi, 2006). Logam ini adalah salah satu
logam yang dikelompokkan dalam jenis logam berat non-esensial. Secara
alami kadmium dapat ditemukan pada lapisan kerak bumi dalam jumlah yang relatif sedikit (0,15 – 0,20 g/g) (WEAST, 1981). Logam kadmium ditemukan di alam dalam mineral Greennockite (CdS) dan pada mineral spalerite (ZnS) (Bijih seng). Greennockite (CdS) ini jarang ditemukan di alam, sehingga sebagian besar logam kadmium diperoleh dari produk samping peleburan
bijih seng. Biasanya pada konsentrat bijih seng dapat diperoleh 0,2 – 0,4%
logam kadmium (Darmono, 1999). Kandungan kadmium di alam dapat
meningkat karena proses alamiah, seperti letusan gunung berapi dan
kebakaran hutan, maupun karena aktivitas manusia seperti penggunaan bahan
bakar fosil, pertambangan, aktivitas industri, dan penggunaan pupuk
anorganik (Agency for Toxic Substance and Disease Registry selanjutnya disebut ATSDR, 1999).
Sifat kadmium yang lentur, tahan tekanan dan mempunyai titik lebur
yang rendah menyebabkan unsur ini seringkali dimanfaatkan sebagai bahan
campuran logam lain seperti nikel, perak, tembaga dan besi. Selain itu, karena
sifatnya yang tahan panas, logam ini baik untuk campuran pembuatan
bahan-bahan keramik, enamel dan plastik. Logam ini juga seringkali dimanfaatkan
untuk melapisi plat besi dan baja karena logam ini tahan terhadap korosi (Lu,
2006). Selain itu, logam ini juga dimanfaatkan untuk aplikasi sepuhan listrik
pigmen cat dengan membentuk beberapa garamnya seperti kadmium oksida
yang dikenal sebagai kadmium merah dan dalam pembuatan batu baterai,
terutama baterai Ni-Cd (Sarjono, 2009).
a. Bahaya Logam Berat Kadmium (Cd)
Kadmium merupakan salah satu jenis logam yang berbahaya
karena unsur ini memiliki efek toksisitas yang tinggi, bahkan pada
konsentrasi yang rendah. Hal ini dikarenakan logam ini mudah diadsorbsi
dan terakumulasi pada organisme hidup (manusia, hewan dan tumbuhan).
Dalam tubuh organisme, kadmium (Cd (II)) akan mengalami proses
biotransformasi dan bioakumulasi. Jika kadmium teradsorpsi ke dalam
tubuh, logam ini akan membentuk kompleks dengan protein sehingga
mudah diangkut dan terakumulasi ke hepar dan ren bahkan sejumlah kecil dapat sampai ke pankreas, usus, dan tulang. (Szymczyk &
Zalewski, 2003).
Kadmium dalam tubuh dapat terakumulasi dalam hati dan ginjal,
dimana logam berat kadmium (Cd (II)) terikat dengan gugus sufhidril
(-SH) pada protein-non enzim dengan berat molekul rendah, thionein, yang
membentuk gugus protein logam yang disebut metalothionein, serta
terikat dengan gugus karboksil sisteinil, histidil, hidroksil, dan fosfatil
dari protein purin. Kemungkinan besar pengaruh toksisitas disebabkan
oleh interaksi antara logam berat kadmium (Cd (II)) dan protein tersebut,
sehingga menimbulkan hambatan terhadap aktivitas kerja enzim dalam
tubuh (Darmono, 1995).
Keracunan kadmium bersifat akut dan kronis. Keracunan akut
muncul setelah 4 – 10 jam sejak penderita terpapar oleh logam berat
kadmium (Cd (II)). Paparan kadmium secara akut dapat menyebabkan
kehilangan nafsu makan, daya tahan tubuh melemah, kerusakan hepar, kerusakan ginjal, sakit kepala, kedinginan hingga menggigil, nyeri otot,
menimbulkan penyakit paru-paru akut, diare, dan bahkan bisa
kronis dapat merusak sistem fisiologis tubuh, antara lain: sistem
pernafasan, sistem respirasi, sistem sirkulasi, sistem reproduksi, sistem
saraf, bahkan dapat menyebabkan kerusakan jantung dan kerapuhan
tulang (Widowati dkk., 2008).
Bagi manusia, kadmium merupakan zat karsinogenik yang dapat
menyebabkan kanker paru-paru, prostat, hepar, pankreas dan ren. Sifat karsinogenik kadmium menyebabkan logam berat tersebut diurutkan
sebagai peringkat pertama agen mutagenik bagi organisme hidup.
Toksisitas kadmium di sebebabkan karena unsur ini tidak diketahui
memiliki fungsi biologis di dalam sel tetapi memiliki sifat reaktif yang
sangat tinggi dan dapat menginaktivasi berbagai macam aktivitas enzim
yang diperlukan oleh sel (Rumahlatu dkk., 2012).
b. Metode Pengukuran Kadmium (Cd) dengan Atomic Adsorption Spectrometer-Flame (FAAS)
Untuk pemeriksaan logam kadmium secara kuantitatif dilakukan
dengan metode Atomic Adsorption Spectrometer (AAS) atau
Spektrofotometri Serapan Atom (SSA). AAS merupakan metode yang
memanfaatkan fenomena penyerapan energi sinar oleh atom netral dalam
bentuk gas sebagai dasar pengukuran. Metode ini sangat tepat digunakan
untuk analisis zat pada konsentrasi rendah (Apriliani, 2010).
Dalam analisis AAS, sampel yang akan dianalisis harus diuraikan
menjadi atom-atom netral yang masih dalam keadaan dasar. ada berbagai
alat yang dapat digunakan untuk mengubah suatu sampel menjadi atom
bebasnya, yaitu:
1) Nyala (Flame)
Nyala digunakan untuk mengubah sampel yang berupa padatan atau
cairan menjadi bentuk uap atomnya dan juga berfungsi untuk
atomisasi. Pada cara ini, nyala berfungsi untuk mengeksitasikan atom
dari tingkat dasar ke tingkat yang lebih tinggi. Suhu yang dapat
bara suhunya 1800ºC; gas alam-udara suhunya 1700ºC; asitelin-udara
suhunya 2200ºC; dan asitelin-dinitrogen oksida suhunya 3000ºC.
Pemilihan macam bahan bakar dan gas pengoksidasinya serta
komposisis perbandinganya sangat mempengaruhi suhu nyala. Untuk
logam kadmium (Cd (II)) sumber nyala yang digunakan adalah
campuran asitelin sebagai bahan pembakar dan udara sebagai
pengoksidasi (Sudjadi, 2012).
2) Tanpa nyala (Flameless)
Pada metode ini pengatoman dilakukan dalam tungku dari grafit yang
dikembangkan oleh Masmann. Tungku grafit ini selanjutnya
dipanaskan dengan sistem elektris dengan cara melewatkan arus listrik
pada grafit. Akibat pemanasan ini, maka zat yang akan dianalisis
berubah menjadi atom-atom netral.
Menurut Apriliani (2010), metode AAS berprinsip pada adsorbsi
cahaya oleh atom. Atom-atom tersebut akan menyerap cahaya pada
panjang gelombang tertentu, tergantung pada sifat unsurnya. Kadmium
menyerap cahaya pada panjang gelombang 228,28 nm (Stoeppler, 1992).
AAS adalah cara analisis yang didasarkan pada proses penyerapan energi
radiasi gelombang elektromagnetik oleh populasi atom yang berbeda
pada tingkat energi yang lebih tinggi. Jika pada sejumlah populasi atom
yang berada pada tingkat energi dasar (E0) diberikan seberkas radiasi
gelombang elektromagnetik dengan tingkat energi tertentu (sesuai
dengan besarnya energi untuk menaikkan tingkat energi atom dari
E0→E1) maka sebagian energi radiasi akan diserap oleh atom dan tingkat
energi atom akan naik dari E0→E1. Energi radiasi yang tidak terserap
akan keluar dari populasi atom dan intensitasnya akan berkurang sesuai
dengan jumah atom yang mengalami perpindahan tingkat energi
(Apriliani, 2010). Analisa ini didasarkan pada hukum Lambert-Beer,
yaitu apabila cahaya dengan panjang gelombang tertentu dilewatkan pada