STUDI PENGGUNAAN TANIN TERMODIFIKASI SEBAGAI SENYAWA PEMBAWA (CARRIER) PADA EKSTRAKSI ION LOGAM Zn(II)
DENGAN METODE MEMBRAN CAIR RUAH (BULK LIQUID MEMBRANE)
SKRIPSI Diajukan kepada
Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Negeri Yogyakarta
Untuk Memenuhi Sebagian Persyaratan Guna Memperoleh Gelar Sarjana Sains Kimia
Oleh: Dedi Setiyawan NIM: 09307144042
PROGRAM STUDI KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS NEGERI YOGYAKARTA
MOTTO
“Allah akan mening
gikan orang-orang yang beriman diantaramu
dan orang-orang yang diberi ilmu pengetahuan beberapa derajat,
d
an Allah Maha Mengetahui apa yang kamu kerjakan”
(QS. Al-Mujadilah: 11)
“Bagian terbaik dari hidup seseorang adalah
perbuatan-perbuatan baiknya dan kasihnya yang tidak diketahui orang
lain.”
(Wiliam Wordsworth)
“Dengan harapan dan keyakinan tersebut mari jadikan
hari esok lebih baik dan lebih terang”
(One Ok rock: Be The Light)
“Jika aku hanya mengikuti jejak sampai a
khir. Aku hanya
menelusuri jejak yang bukan hidupku. Kita tidak akan pernah
semuda kita sekarang”
(One Ok Rock: Decision
“Warisan, cita-cita, takdir waktu dan impian manusia
merupakan hal yang tidak bisa dihentikan, selama manusia masih
terus mencari makna kebebasan, mereka tidak akan pernah
berhenti”
(One Piece: Gol D Roger)
“life is short, and it is up to you to make it sweet.”
PERSEMBAHAN
Sujud syukur kepada Sang Khalik Pemilik Jagad Raya ini, Allah SWT
yang selalu melindungi dan mendengarkan keluh kesah
di setiap doaku. Begitu banyak kenikmatan yang telah diberikan-Nya
hingga karya ini terselesaikan
Ucapan Terima Kasih Untuk :
1. Untuk Bapak dan Ibu, yang telah memberiku dukungan dalam segala hal
baik moril, materi, nasehat serta semangat yang tidak pernah berhenti.
2. Untuk adikku tercinta, semoga kau menjadi lebih baik dari kakakmu,
semoga kau mempunyai pendidikan lebih tinggi dan menjadi anak sholeh.
3. Untuk adek safitri, terima kasih supportnya selama aku menyusun Tugas
Akhir Semester sehingga bisa menyelesaikan dengan baik.
4. Untuk anak-anak Kimia Swadana 09 terima kasih kalian sudah menjadi
teman terbaikku selama kuliah, dan aku berharap setelah lulus kita masih
berteman baik seperti dulu meskipun jarak memisahkan kebersamaan kita,
sukses buat kita semua. Ganbatte.
5. Temen-temen KKN Bendungan Lor, Kulon Progo dan warga Bendungan
Lor. Aku pasti merindukan hari-hari bersama kalian
6. Warung Spesial Sambal yang memberi kesempatan bekerja. Personil SS
Babarsari Barat dan Trio KECEWA SS Babarsari Barat, terima kasih telah
menerima aku sebagai keluarga kalian. Temen-temen FUTSAL Spesial
PERNYATAAN
Yang bertanda tangan dibawah ini saya:
Nama : Dedi Setiyawan
NIM : 09307144042
Program Studi : Kimia
Fakultas : FMIPA-UNY
Judul Penelitian : Studi Penggunaan Tanin Termodifikasi sebagai Senyawa
Pembawa (Carrier) pada Ekstraksi Ion Logam Zn (II)
dengan Metode Membran Cair Ruah (Bulk Liquid
Membrane).
Menyatakan bahwa Penelitian ini adalah hasil pekerjaan saya sendiri dan
sepanjang pengetahuan saya tidak berisi materi atau data yang telah
dipublikasikan atau ditulis orang lain atau telah dipergunakan dan diterima
sebagai persyaratan penyelesaian studi pada universitas lain atau institut lain,
kecuali pada bagian-bagian tertentu yang telah dinyatakan dalam teks.
Apabila pernyataan ini tidak benar, sepenuhnya menjadi tanggung jawab saya.
Yogyakarta, 20 Desember 2016
Yang menyatakan
KATA PENGANTAR
Puji syukur atas kehadirat Tuhan yang senantiasa mencurahkan kasih dan
anugerah-Nya, sehingga penulis dapat menyelesaikan penyusunan skripsi yang
berjudul “Studi Penggunaan Tanin Termodifikasi sebagai Senyawa Pembawa
(Carrier) pada Ekstraksi Ion logam Zn (III) dengan Metode Membran Cair Ruah
(Bulk Liquid Membrane)”. Skripsi ini disusun sebagai salah satu syarat untuk
memperoleh gelar sarjana Sains Kimia.
Penulis menyadari bahwa dalam menyelesaikan penyusunan skripsi ini
tidak pernah lepas dari bimbingan, arahan, bantuan dan motivasi dari berbagai
pihak. Oleh karenanya, melalui kesempatan ini penulis ingin mengucapkan terima
kasih kepada:
1. Bapak Dr. Hartono selaku Dekan FMIPA Universitas Negeri Yogyakarta.
2. Bapak Jaslin Ikhsan, M.App.Sc., Ph.D selaku Ketua Jurusan Pendidikan Kimia
dan Ketua Prodi Kimia Jurusan Pendidikan Kimia FMIPA Universitas Negeri
Yogyakarta
3. Ibu C. Budimarwanti selaku Penasehat Akademik, yang telah memberikan
nasehat dan bimbingan kepada penulis.
4. Bapak Drs. I Made Sukarna M.Si selaku Pembimbing Utama, yang telah
memberikan bimbingan, serta arahan, hingga selesainya skripsi ini.
5. Ibu Susila Kristianingrum, M.Si; Ibu Regina Tutik Padmaningrum, M.Si dan
Bapak Erfan Priyambodo, M.Si selaku dosen penguji.
6. Seluruh dosen dan staf pengajar FMIPA Universitas Negeri Yogyakarta yang
7. Seluruh laboran dan karyawan Laboratorium Kimia FMIPA Universitas Negeri
Yogyakarta atas bantuan dan kerjasamanya selama penyusunan skripsi.
8. Semua pihak yang tidak bisa disebutkan satu persatu, yang telah memberikan
bantuan hingga terselesaikannya skripsi ini
Penulis menyadari bahwa dalam skripsi ini masih banyak kekurangan dan
jauh dari kesempurnaan, namun demikian penulis berharap semoga apa yang
penulis peroleh selama penyusunan skripsi ini mempunyai arti dan dapat
memberikan manfaat bagi perkembangan ilmu kimia. Untuk itu penulis
mengharapkan adanya kritik dan saran yang bersifat membangun demi
kesempurnaan skripsi ini.
Yogyakarta, 28 Desember 2016
DAFTAR ISI
HALAMAN JUDUL... i
HALAMAN PERSETUJUAN... ii
HAAMANA PENGESAHAN ... iii
HALAMAN MOTTO... iv
HALAMAN PERSEMBAHAN... v
HALAMAN PERNYATAAN... vi
KATA PENGANTAR ... vii
DAFTA ISI... ix
DAFTAR TABEL... ... xi
DAFTAR GAMBAR... xii
DAFTAR TABEL... ... xiii
ABSTRAK... xiv
ABSTRACT... xv
BAB I. PNDAHULUAN A. Latar Belakang Masalah... 1
B. Identifikasi Masalah... 5
C. Pembatasan Masalah... 6
D. Perumusan Masalah... 6
E. Tujuan Penelitian... 7
F. Manfaat Penelitian... 7
BAB II. TINJAUAN PUSTAKA A. Deskripsi Teori... 8
2. Metode Membran Cair... 12
3. Metode Membran Cair Ruah... 17
4. Logam Berat... 19
5. Seng(II) ... 20
6. Tanin... 22
7. Spektrofotometri Inframerah... 23
8. Atomic Absorption Spectroscopy (AAS)... 25
B. Penelitian Yang Relevan... 29
C. Kerangka Berfikir... 31
BAB III METODE PENELITIAN A. Subyek dan Obyek Peneltian... 32
B. Vaiabel Penelitian... 32
C. Alat dan Bahan Penelitian... 32
D. Prosedur Penelitian... 33
E. Analsis Data Penelitian... 39
BAB IV. HASIL DAN PEMBAHASAN A. Hasil Penelitian... 43
B. Pembahasan... 50
BAB V. KESIMPULAN DAN SARAN A. Kesimpulan ... 58
B. Saran... 58
DAFTAR PUSTAKA... 59
DAFTAR TABEL
Tabel 1. Klarifikasi Beberapa Asam Basa berdasarkan HSBA... 17
Tabel 2. Korelasi Daerah Serapan Inframerah... 24
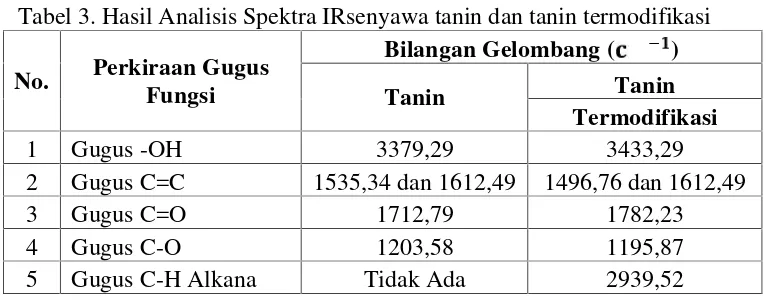
Tabel 3. Hasil Analisis Spektra IR Senyawa Tanin dan Tanin
Termodifikasi... 44
Tabel 4. Data Absorbansi Larutan Standar Zn(II) pada Pengaruh Waktu
Ekstraksi terhadap Transpor Ion Logam Zn(II) ... 45
Tabel 5. Data Pengaruh Waktu terhadap Ttanspor Ion Logam Zn(II) ... 46
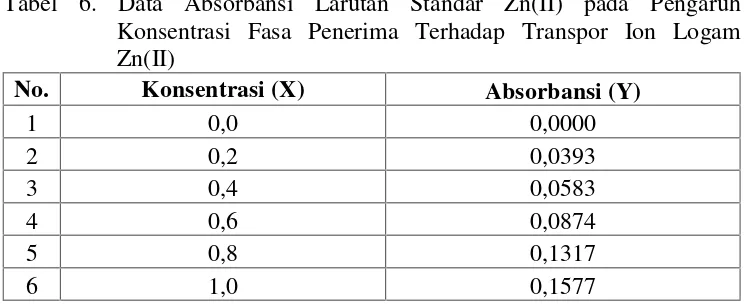
Tabel 6. Data Absorbansi Larutan Standar Zn(II) pada Pengaruh
Konsentrasi Fasa Penerima terhadap Transpor Ion Logam Zn(II)... 47
Tabel 7. Data Pengaruh Konsentrasi Fasa Penerima terhadap Tanspor Ion
Logam Zn(II)... 49
Tabel 8. Perhitungan Garis Regresi Kurva Kalibrasi Pengaruh Waktu
Ekstraksi terhadap Transpor Ion Logam Zn(II) ... 68
Tabel 9. Perhitungan Garis Regresi Kurva Kalibrasi Pengaruh Waktu
Ekstraksi terhadap Transpor Ion Logam Zn(II) ... 71
Tabel 10. Data Pengaruh Waktu terhadap konsentrasi Ion Logam Zn(II)
dalam Fasa Penerima... 74
Tabel 11. Data Akhir Pengaruh Waktu terhadap Konsentrasi Ion Logam
Zn(II) dalam Fasa Penerima dan hasil Ion Logam yang
tertranspor... 77
Tabel 12. Data Pengaruh Konsentrasi Fasa Penerima terhadap
Konsentrasi Ion Logam Zn(II) dalam Fasa Penerima... 78
Tabel 13. Data Akhir Pengaruh Konsentrasi Fasa Penerima terhadap
Konsentrasi Ion Logam Zn(II) dalam Fasa Penerima dan Ion
Logam Zn(II) yang Tertranspor... 82
Tabel 14. Nilai-nilai r Product Moment pada Taraf Signifikansi 5% dan 1%.... 83
DAFTAR GAMBAR
Gambar 1. Mekanisme pemisahan ion logam... 15
Gambar 2. Model reaktor transpor melalui teknik membran cair ruah... 18
Gambar 3. Struktur tanin terhidrolisis... 22
Gambar 4. Skema umum komponen pada Alat AAS... 25
Gambar 5. Kurva kalibrasi larutan standar... 28
Gambar 6. Sistem ekstraksi dengan metode membran cair ruah... 38
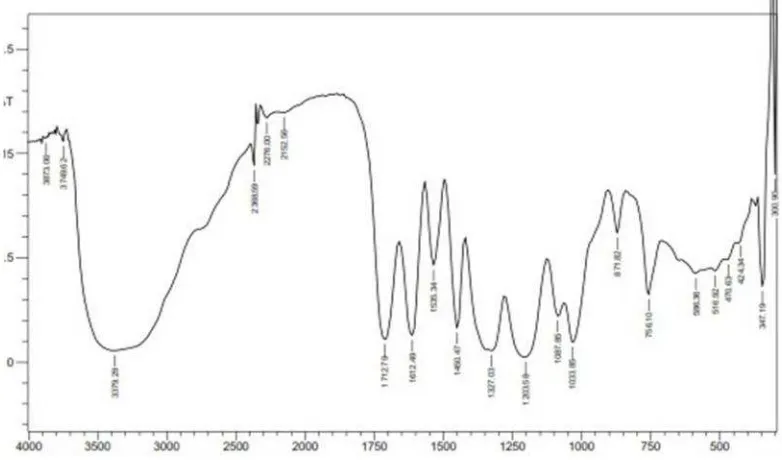
Gambar 7. Spektra IR senyawa tanin... 43
Gambar 8. Spektra IR senyawa tanin termodifikasi... 44
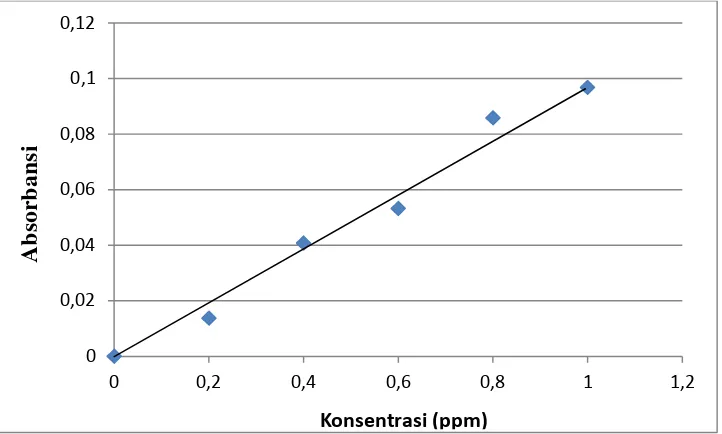
Gambar 9. Kurva kalibrasi larutan standar seng(II) untuk penentuan pengaruh waktu ekstraksi terhadap transpor ion logam seng(II)... 45
Gambar 10. Kurva hubungan antara waktu ekstraksi dengan transpor ion logam seng(II)... 47
Gambar 11. Kurva kalibrasi larutan standar seng(II) untuk penentuan pengaruh konsentrasi terhadap transpor ion logam seng(II) ... 48
Gambar 12. Kurva hubungan antara konsentrasi fasa penerima terhadap transpor ion logam seng(II)... 49
Gambar 13. Reaksi asetilasi tanin... 53
DAFTAR LAMPIRAN
Lampiran 1. Skema prosedur kerja... 64
Lampiran 2. Uji linearitas kurva kalibrasi pengaruh waktu ekstraksi terhadap transpor ion logam Zn(II)... 68
Lampiran 3. Uji linearitas kurva kalibrasi pengaruh konsentrasi ekstraksi terhadap transpor ion logam Zn(II ... 71
Lampiran 4. Perhitungan persentase transpor pada pengaruh wakru ekstraksi terhadap transpor ion logam Zn(II)... 74
Lampiran 5. Perhitungan persentase transpor pada pengaruh konsentrasi ekstraksi terhadap transpor ion logam Zn(II)... 78
Lampiran 6. Daftar Nilai Nilai r (koefisien Korelasi)... 82
Lampiran 7. Daftar Nilai F regresi... 83
Lampiran 8. Gambar Alat Penelitian... 84
STUDI PENGGUNAAN TANIN TERMODIFIKASI SEBAGAI SENYAWA PEMBAWA (CARRIER) PADA EKSTRAKSI ION LOGAM Zn(II)
DENGAN METODE MEMBRAN CAIR RUAH (BULK LIQUID MEMBRANE)
Oleh: Dedi setiyawan
09307144042
Pembimbing Utama : Drs. I Made Sukarna, M.Si
ABSTRAK
Penelitian ini bertujuan untuk mengetahui apakah senyawa tanin termodifikasi dapat digunakan sebagai senyawa pembawa dalam ekstraksi ion logam Zn(II) dengan metode membran cair ruah, dengan cara menentukan waktu ekstraksi terbaik dalam ekstraksi ion logam Zn(II), mengetahui konsentrasi optimum fasa penerima dalam ekstraksi ion logam Zn(II) serta mengetahui persentase transpor ion logam Zn(II) ke fasa penerima.
Subjek penelitian ini adalah penggunaan senyawa tanin termodifikasi untuk ekstraksi ion logam Zn(II) dengan metode membran cair ruah, sedangkan objek penelitiannya adalah persentase transpor ion logam Zn(II). Pada penelitian ini dilakukan modifikasi senyawa tanin dengan reaksi asetilasi dan hasilnya dikarakterisasi dengan Spektrofotometri Infrared. Selanjutnya senyawa tanin yang dimodifikasi digunakan untuk membuat membran dengan cara menambahkan 0,5 gram senyawa tanin termodifikasi ke dalam 50 mL etil asetat. Membran ini kemudian digunakan untuk ekstraksi dengan variasi waktu ekstraksi 2, 4 dan 6 jam. Sedangkan fasa umpan yang digunakan yaitu 50 mL larutan Zn(II) 100 ppm dan fasa penerima berupa H2SO4 divariasikan
konsentrasinya yaitu 0,1; 0,5 dan 1 M. Kandungan ion Zn(II) dalam kedua fase selanjutnya diukur dengan Spektrofotometer Serapan Atom.
Hasil spektra IR menunjukkan perbedaan yaitu adanya serapan dari gugus C-H alkana dari senyawa tanin hasil modifikasi pada 2939,52 cm-1, sedangkan pada spektra senyawa tanin tidak terdapat serapan oleh gugus C-H alkana. Disimpulkan bahwa senyawa tanin termodifikasi dapat digunakan sebagai senyawa pembawa dalam ekstraksi ion logam Zn(II). Selain itu, waktu ekstraksi terbaik yaitu selama 6 jam dengan persentase transpor ion logam Zn(II) sebesar 16,3074 %. Sedangkan konsentrasi optimum fasa penerima yaitu pada konsentrasi H2SO4 0,1 M dengan persentase transpor ion logam
Zn(II) sebesar 16,3074 %.
A STUDY OF USING MODIFIED TANNIN AS CARRIER IN THE EXTRACTION OF Zn(II) METAL IONS
BY BULK LIQUID MEMBRANE METHOD
By: Dedi Setiyawan
09307144042
Supervisor : Drs. I Made Sukarna, M.Si
ABSTRACT
This study aims to determine whether the modified tannin compounds can be used as a carrier in the extraction of Zn(II) metal ions by Bulk Liquid Membrane method, by determining the best extraction time of Zn(II), determine the optimum concentration of receiver phase in the extraction of Zn(II) and to know the transport percentage of metal ion Zn(II) to the receiver phase.
The subject of this study is the use of modified tannin compounds to extraction of Zn(II) metal ions by bulk liquid membrane method, while the study object is the transport percentage of Zn(II) metal ion. In this research, tannin was modified by acetylation reaction and characterized by Infrared Spectrophotometry. Furthermore modified tannin is used to make membranes by adding 0,5 grams tanin modified of the compound into 50 mL ethyl acetate. This membrane then used to extract with the variation of extraction time is 2, 4 and 6 hours. While source phase used is 50 mL solution of Zn(II) 100 ppm and a receiver phase is H2SO4 concentration was varied at 0,1; 0,5 and 1 M. Ion
content of Zn(II) in the two subsequent phases were measured by Atomic Absorption Spectrophotometer.
IR spectra of tannin before and after modification there are differences in the presence of C-H alkane absorption of tannin modified at 2939.52 cm-1, while the spectra of tannin there is no absorption by C-H alkane. So, from these data it can be concluded that the modified tannin compounds can be used as a carrier in the extraction of metal ions Zn(II). The results showed that the best extraction time is 6 hours with the percentage of metal ion transport 16,3074 %. While the optimum concentration of the receiver phase at aconcentration of 1 M H2SO4 with the percentage of metal ion transport 16,3074 %.
BAB I PENDAHULUAN
A. Latar Belakang Masalah
Pertumbuhan kebutuhan manusia harus diatasi dengan berkembangnya
teknologi dalam bidang industri. Hal ini sejalan dengan semakin bertambah
manusia, kebutuhan manusia akan meningkat. Indutri merupakan produsen
bagi segala kebutuhan manusia, selain itu industri merangkap sebagai
produsen limbah. Keberadaan limbah terutama limbah cair dalam jumlah
yang besar menjadi masalah yang semakin serius dampaknya bagi
lingkungan sekitar.
Pencemaran limbah yang terjadi di kawasan industri dapat meluas
seiring dengan berjalannya waktu, meluasnya pencemaran ini dibawa oleh
air, udara dan tanah. Pemukiman penduduk yang berada di kawasan industri
mengalami dampak yang paling besar terhadap kesehatan. Keberadaan
limbah dalam jumlah yang besar tidak bisa dibiarkan begitu saja karena
nanti akan menimbulkan masalah kesehatan yang besar. Limbah yang
menimbulkan masalah besar adalah yang mengandung logam-logam berat.
Logam-logam berat seperti kromium (Cr), tembaga (Cu), kadmium (Cd),
seng (Zn), raksa (Hg), besi (Fe), timbal (Pb), nikel (Ni) dan timah (Sn)
memiliki potensi toksik ( Surna T.Djajadiningrat 1996: 106).
Logam seng(II) merupakan logam mikro yang terakumulasi dalam
tubuh menyebabkan toksik dan beracun. Sudah banyak pembuktian bahwa
akumulasi logam seng(II) hasil dari industri tekstil dalam jaringan manusia
3). Seng (II) termasuk kedalam trace mineral, artinya dibutuhkan oleh tubuh
relatif sedikit. Keracunan seng (II) dalam jumlah besar akan menyebabkan
mual, muntah-muntah, diare dan gangguan pada perut. Sebanyak satu persen
seng (II) dalam ransum hewan dapat menekan pertumbuhan, gangguan pada
alat reproduksi dan anemia.
Proses pemisahan merupakan proses penting dalam industri dan
semakin berkembang dengan permasalahan di industri serta makin
banyaknya pilihan teknologi yang bisa digunakan. Pemisahan unsur logam
berat dalam limbah bertujuan mengurangi resiko limbah buangan agar tidak
membahayakan manusia dan lingkungan. Pemisahan unsur-unsur yang
terkandung dalam suatu limbah dapat dilakukan dengan berbagai cara,
diantaranya dengan pengendapan, penguapan, elektroanalisis, dan ekstraksi
pelarut. Metode pemisahan yang paling baik dan populer adalah ekstraksi
pelarut, karena dapat dilakukan baik dalam tingkat makro maupun mikro
(Khopkar,1990: 290-305).
Penggunaan ekstraksi pelarut sebagai unit operasi dalam
hidrometalurgi. Sekarang digunakan secara luas untuk logam-logam dari
berbagai macam bahan mentah termasuk bijih tingkat rendah, bahan sisa
dan limbah (Rydberg, 1992: 393-412).
Teknik pemisahan ion logam berat dengan membran cair merupakan
salah satu pengembangan metode ekstraksi pelarut yang dapat digunakan
untuk recovery ion logam berat dari air limbah, eksplorasi logam berharga
dari bahan tambang serta untuk kepentingan analisis. Keuntungan metode
sistem tinggi, penggunaan pelarut, pemisahan ion yang dapat dilakukan
secarakontinoudalam satu unit operasi, pengoperasian sederhana dan biaya
pengoperasian yang murah (Misra and Gill, 1996:361-368).
Membran cair telah dikembangkan dan dipelajari untuk pemisahan
logam toksik dan logam bernilai. Teknik didasarkan pada proses distribusi
cair-cair, yang dilakukan dengan menggunakan agen pengekstrak seperti
senyawa pembawa dalam transpor berfasilitas. Membran cair telah
dimanfaatkan untuk pemisahan fenol dari limbah cair hasil buangan industri.
Membran cair juga digunakan untuk proses pemisahan logam (Kopunecdan
Benetiz, 1991:269-280; Nakamura, 1992:863-873; Monh,1992:219-231).
Membran cair ruah (BLM,BulkLiquidMembrane) merupakan metode
yang sering digunakan dalam teknik membran cair yang menggunakan
cairan sebagai membran sehingga dibutuhkan senyawa membran yang lebih
banyak. Metode ini cukup baik untuk mempelajari mekanisme transport dan
pengaruh dari struktur carrier dalam efisiensi dan selektivitasnya. (Misra
and Gill, 1996:361-368).
Keberhasilan ekstraksi pelarut dan teknik pemisahan menggunakan
membran cair ditentukan oleh kestabilan kompleks antara ion logam dengan
senyawa pembawa (carrier). Kestabilan kompleks tersebut ditentukan oleh
beberapafaktor, diantaranya jenis atom donor (gugus aktif) senyawa
pembawa yang sesuai dengan konfigurasi elektron logam. Efisiensi dan
selektivitas dari transport pada berbagai teknik ekstraksi sangat ditentukan
Selain faktor gugus aktif yang mempengaruhi efektifitas dan
selektifitas ekstraksi logam, faktor lainnya adalah ukuran cincin (ring size)
untuk makro siklik atau panjang dan cabang gugus hidrofobik (Walkowiak,
1996: 181-193; Fortunato,2004: 197-209 ). Sumbercarrier dapat diperoleh
dari bahan alam yang melimpah sebagai contoh eugenol yang diekstrak dari
minyak cengkeh.
Teknik membran cair fasa ruah dengan menggunakan zat pembawa
merupakan terobosan baru dalam teknik pemisahan. Teknik ini
mengkombinasikan ekstraksi pelarut dan proses stripping dalam suatu
perpaduan yang sangat menarik dalam perlakuan pada larutan yang
konsentrasi logamnya rendah. Keselektifan dan keefektifan teknik ini dapat
diperoleh dengan menambahkan zat aditif yang cocok sebagai mediator dan
pengaturan kondisi operasi yang tepat saat pemakaian transpor sehingga
tidak terjadi reaksi balik.
Tanin merupakan salah satu senyawa metabolit sekunder yang
terdapat pada tanaman dan disintesis oleh tanaman. Tanin dapat membentuk
senyawa kompleks dengan makromolekul lainnya. Tanin terbagi menjadi
dua kelompok yaitu tanin yang terhidrolisis dan tanin terkondensasi. Tanin
yang mudah terhidrolisis merupakan polimer gallic dan ellagic acid yang
berikatan ester dengan sebuah molekul gula, sedangkan tanin terkondensasi
merupakan polmer senyawa flavonoid dengan ikatan karbon-karbon
Waghorn dan McNabb, 2003: 383-392). Tanin juga dapat membentuk
khelat dengan logam secara stabil, sehingga dari sifat ini tanin digunakan
Tanin yang bersumber dari tanaman mempunyai sifat polar yang larut
dalam air. Sedangkan fasa umpan dan fasa penerima dalam proses ekstraksi
merupakan fasa air sehingga tanin akan larut dalam kedua fasa dan tidak
dapat digunakan sebagai senyawa pembawa (carrier). Oleh karena itu,
dilakukan modifikasi dengan reaksi asetilasi untuk mengganti gugus –OH
dengan gugus asetil sehingga didapatkan tanin termodifikasi yang sifat
kepolarannya lebih kecil.
Berdasarkan hal ini, maka dilakukan penelitian yang bertujuan
mengetahui kapasitas tanin sebagai senyawa pembawa (carrier) untuk
ekstraksi ion logam Zn(II) dengan metode membran cair ruah (Bulk Liquid
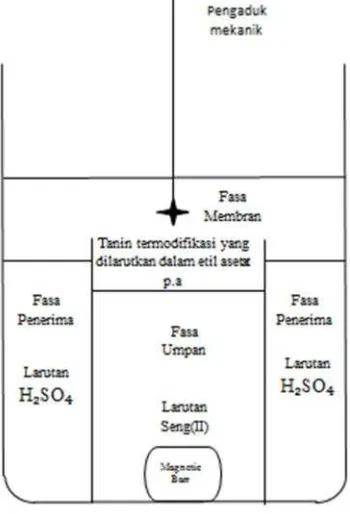
Membrane). Dimana larutan Zn(II) sebagai fasa umpan, tanin termodifikasi
yang dilarutkan dalam etil asetat p.a sebagai fasa membran dan larutan
H SO sebagai fasa penerima. Adapun faktor-faktor yang mempengaruhi
hasil pemisahan dengan metode membran cair ruah antara lain waktu
pengadukan, konsentrasi fasa penerima dan kecepatan pengadukan.
B. Identifikasi Masalah
Berdasarkan pada latar belakang, maka kita dapat mengidentifikasi
beberapa masalah yang terkandung, yaitu :
1. Metode yang digunakan pada ekstraksi ion logam Zn(II).
2. Senyawa pembawa (carrier) yang digunakan pada ekstraksi logam
Zn(II).
3. Kecepatan pengadukan pada ekstraksi ion logam Zn(II).
5. Variasi konsentrasi fasa penerimapada ekstraksi ion logam Zn(II).
C. Pembatasan Masalah
Untuk mempersempit ruang lingkup penelitian ini, maka akan
dilakukan pembatasan masalah sebagai berikut:
1. Metode yang digunakan pada ekstraksi ion logam Zn(II) adalah metode
Membran Cair Ruah (Bulk Liquid Membrane).
2. Senyawa pembawa (carrier) yang digunakan pada ekstraksi ion logam
Zn(II) adalah tanin termodifikasi.
3. Kecepatan pengadukan pada ekstraksi logam Zn(II) adalah kecepatan
pengadukan pada mechanic stirrer 130 rpm dan pada magnetic stirrer
yaitu 500 rpm.
4. Variasi waktu pengadukan pada ekstraksi ion logam Zn(II) adalah 2 jam,
4 jam dan 6 jam.
5. Variasi konsentrasi fasa penerima yaitu 0,1 M ; 0,5 M dan 1 M.
D. Perumusan Masalah
Berdasarkan latar belakang masalah dapat diidentifikasi beberapa
masalah sebagai berikut:
1. Apakah senyawa tanin termodifikasi dapat digunakan sebagai senyawa
pembawa (carrier) dalam ekstraksi ion logam Zn(II) dengan metode
Membran Cair Ruah?
3. Berapa konsentrasi optimum fasa penerima pada ekstraksi ion logam
Zn(II)?
4. Berapa besar persen efisiensi transpor ion logam Zn(II) ke fasa
penerima?
E. Tujuan Penelitian
Penelitian ini bertujuan untuk:
1. Mengetahui apakah senyawa tanin termodifikasi bisa digunakan sebagai
senyawa pembawa (carrier) dalam ekstraksi logam Zn(II) dengan metode
Membran Cair Ruah (Bulk Liquid Membrane).
2. Mengetahui waktu ekstraksi optimum dalam ekatraksi logam Zn(II).
3. Mengetahui konsentrasi optimum fasa penerima ekstraksi logam Zn(II).
4. Mengetahui efisiensi transpor ion logam Zn(II) ke fasa penerima.
F. Manfaat Penelitian
Dengan penelitian ini diharapkan mempunyai manfaat antara lain:
1. Menambah ketrampilan peneliti dalam menerapkan metode-metode
analisis teori secara langsung.
2. Menambah khasanah ilmu pengetahuan khususnya dalam hal analisis
seng (II) dan metode emulsi membran cair
3. Menambah nilai kegunaan senyawa tanin.
4. Memperoleh senyawa organik yang mempunyai kegunaan sebagai
BAB II KAJIAN TEORI A. Deskripsi Teori
1. Ekstraksi
Ekstraksi adalah metode pemisahan yang berdasarkan pada proses
distribusi zat terlarut (solut) dalam dalam dua pelarut yang saling
bercampur. Ekstrasi merupakan proses pemisahan, penarikan atau
pengeluaran suatu komponen cairan atau komponen dari campurannya.
Biasanya menggunakan pelarut sesuai dengan komponen yang diinginkan
Proses ekstraksi memanfaatkan pembagian suatu zat terlarut antara dua
pelarut yang tidak saling tercampur untuk mengambil zat terlarut tersebut
dari satu pelarut ke pelarut lain. Metode ekstraksi memegang peranan yang
penting baik dilaboratorium maupun dunia industri. Di laboratorium,
ekstraksi sering kali dilakukan untuk menghilangkan atau memisahkan zat
terlarut dalam larutan dengan pelarut air yang diekstraksi dengan pelarut lain
seperti eter, kloroform, karbondisulfida atau benzene (Sudjadi, 1986:
167-177).
Apabila suatu solut terdistribusi diantara dua pelarut yang tidak saling
bercampur, maka ada hubungan tertentu antara konsentrasi solut didalam
dua fase pada kesetimbangan. Hubungan ini dikemukan oleh Nerst, yang
menyatakan bahwa suatu solut akan terdistribusi antara dua pelarut yang
tidak bercampur, sedemikian rupa hingga perbandingan konsentrasi dalam
suatu kesetimbangan pada suhu dan tekanan tertentu adalah tetap.
Berdasarkan metode dalam ekstraksi, ekstraksi dibagi menjadi tiga,
a. Ekstraksibatch
Ekstraksi batch merupakan metode yang paling sederhana bila
dibandingkan metode yang lain karena hanya menggunakan corong pisah
dalam ekstraksi. Metode ini digunakan bila perbandingan distribusi solut
antara pelarut organik dan air cukup besar sehingga dapat memberi hasil
optimal.
b. Ekstraksikontinou
Ekstraksi ini digunakan bila perbandingan distribusi antara kedua pelarut
relatif kecil, sehingga dapat digunakan alat soxlet untuk melakukan
ekstraksi.
c. Ektraksicounter current
Ekstraksi counter curent digunakan bila perbandingan distribusi solut
antara dua pelarut hampir sama, sehingga dapat digunakan alat Craig
untuk melakukan ekstraksi (Karger et al, 1979; Skoog et al, 1996).
Berdasarkan prosesnya ekstraksi dibagi menjadi 3, yaitu :
a Ekstraksisolvasi
Ekstraksi solvasi adalah ekstraksi yang prosesnya melalui pembentukan
kompleks asosiasi ion dimana molekul-molekul pelarut terlibat dalam
pembentukan kompleks tersebut sehingga ion logam dapat
terdistribusikan ke fase organik. Contohnya ekstraksi Fe menggunakan
eter (Pudjaatmaka, A.H. dan Setiono. 1994: 229)
b Ekstraksi kelat
Ekstraksi kelat adalah ekstraksi yang prosesnya melalui pembentukan
dengan ligan kelat. Ligan kelat adalah senyawa yang memiliki dua atau
lebih gugus pendonor pasangan elektron. Psangan elektron ini akan
menempati koordinasi logam membentuk senyawa lingkar atau cincin
(Ueno et al, 1992: 313-321, 507-509). Pada pembentukan kelat, ligan
kelat menetralkan muatan dari ion logam sehingga terbentuk senyawa
kelat netral yang dapat diekstrak ke fase organik. Contoh adalah ekstraksi
Cu menggunakan ligan oksin.
c Ekstraksi pasangan ion
Ekstraksi pasangan ion adalah ekstraksi karena ion logam bersosiasi
dengan ion-ion yang bermuatan berlawanan sehingga menghasilkan suatu
spesies tak bermuatan yang dapat diekstrak ke fase organik. Contohnya
adalah ekstraksi Fe menggunakan phenantrolin dan anion klorida
(Pudjaatmaka. A.H. dan Setiono, L., 1994: 235)
Berdasarkan energi/suhu yang digunakan ekstraksi dibagi menjadi 2,
yaitu :
a. Ekstraksi cara dingin
Ekstraksi dengan cara dingin artinya tidak ada proses pemanasan selama
proses ektraksi berlangsung yang bertujuan untuk menghindari
kerusakan senyawa yang dianalisis karena pemanasan. Jenis ekstraksi
dingin yaitu :
1) Maserasi
Istilah meceration berasal dari bahasa latin macerare yang artinya
merendam. Maserasi adalah ekstraksi dengan prinsip pencapaian
suhu kamar. Bila dibantu pengadukan secara konstan disebut maserasi
kinetik. Remaserasi adalah penambahan pelarut kedalam simplisia yang
diekstraksi, maserat (hasil maserasi) pertama disaring, sisa simplisia
diekstraksi dengan menambahkan pelarut baru dengan cara yang sama.
Kekurangan metode ini, buruh waktu yang lama dan memerlukan pelarut
dalam jumlah yang banyak
2) Perkolasi
Istilah perkolasi berasal dari bahasa latin, per yang artinya memulai dan
colare yang artinya merembes. Perkolasi adalah ekstraksi menggunakan
pelarut yang selalu baru sehingga semua pelarut tertarik dengan
sempurna (exhaustive extraction), umumnya dilakukan pada suhu kamar.
Tahapan perkolasi penetesan pelarut serta penampungan perkolatnya
hingga didapat volume 1 sampai 5 kali jumlah bahan.
b. Ekstraksi cara panas
Ekstraksi dengan cara panas melibatkan panas dalam prosesnya. Dengan
adanya panas secara otomatis akan mempercepat proses pencarian
dibandingkan dengan cara dingin.
1) Refluks
Refluks merupakan ekstraksi pelarut pada temperatur didihnya selama
waktu tertentu dan jumlah pelarut terbatas yang relatif konstan dengan
adanya pendingin balik dilakukan sebanyak tiga kali setiap 3-4 jam.
2) Digesti
Digesti adaalah maserasi kinetik pada teperatur lebih tinggi dari
3) Destilasi uap
Pencarian minyak menguap dengan cara simplisia dan air ditempatkan
dalam labu berbeda. Air dipanaskan dan akan menguap, uap air akan
masuk ke dalam labu sampel sambil mengekstraksi minyak menguap
yang terdapat dalam simplisia, uap air dan minyak menguap yang telah
terekstraksi menuju kondensor dan akan terkondensasi, lalu akan
melewati pipa pendingin, campuran air dan minyak yang menguap masuk
kedalam corong pisah dan akan memisah antara air dan minyak atsiri.
4) Infusa
Ekstraksi pelarut air pada temperatur penangas air 90 °C–98 °C.
5) SoxhletasiatauContinous Extraction
Soxhletasiadalah suatu meode pemisahan suatu komponen yang terdapat
dalam sampel padat dengan cara penyaringan berulang-ulang dengan
pelarut yang sama. Sehingga semua komponen yang diinginkan dalam
sampel terisolasi sempurna. Soxhletasi merupakan penyarian simplisia
secara berkesinambungan, cairan penyari dipanaskan sehingga menguap,
uap cairan penyari terkondensasi menjadi molekul-molekul air oleh
pendingin balik dan turun menyari simplisia dalam klonsong dan
selanjutnya masuk kembali kedalam labu alas bulat setelah melewati pipa
sifon .http://ilmu-kefarmasian.blogspot.co.id/2013/02/ekstraksi.html
2. Metode Membran Cair
Ekstraksi secara umum merupakan cara yang paling sederhana dan
mudah untuk memisahkan suatu komponen dari larutannya, akan tetapi
sehingga untuk mengatasi hal tersebut dilakukan beberapa modifikasi dari
metode-metode ekstraksi yang ada. Salah satu metode yang telah
dimodifikasi adalah metode transpor melalui membran cair
Metode transpor melalui membran cair dilakukan menggunakan gelas
kimia dari tiga fase, yaitu fase sumber yang berisi ion logam, fase membran
yang berisi ligan dan fasa penerima yang berisi asam kuat (Hiratani et al,
1990:319-320; Gaikwad, 2003:327-334). Membran sebagai komponen
paling penting berisi ligan dimana ligan tersebut mempunyai struktur yang
memungkinkan terjadinya kompleks (Lamb et al, 1980: 6820-6824).
Membran cair adalah fase cair yang memisahkan dua fase cair lainnya yang
tidak bercampur, dimana ligan pembawa dalam membran cair akan
memfasilitasi transport kation dari fase air(fase sumber) ke fase air lainnya
(fase penerima) melalui membran cair (Lamb etal, 1980: 6820-6824).
Walkowiak (1996: 181-193), Hiratani (1996:167-180), dan Misra
(1996: 361-368) dalam penelitian melaporkan keunggulan teknik membran
cair dibandingkan ekstraksi pelarut tradisional untuk pemisahan ion dalam
hal efisiensi penggunaan larutan organik dan agen pengompleks ion logam.
Efisiensi dengan teknik membran cair emulsi yang didapat mencapai
99 %. Walkowiak (1996:181-193) melaporkan pemisahan selektif kation
logam transisi dengan berbagai pembawa senyawa organofosfos dengan
teknik membran cair emulsi multi tahap dengan berbagai pengaturan pH.
Hayashita memisahkan logam–logam berat dengan mengomplekskan logam
berat sebagai kompleks klorida dengan teknik membran cair emulsi.
masih perlunya upaya pemecahan emulsi yang merepotkan unuk
mendapatkan logam yang diinginkan, berbeda dengan membran cair
berpendukung dimana logam murni didapatkan tanpa perlu pemisahan lagi
Beberapa keunggulan membran cair dibandingkan metode ekstraksi
yang sebelumnya (Aminuddin dan Buchori, 1997: 9-13)
a. Bebas dispersi.
b. Dapat digunakan untuk kondisi ekstraksi pada perbandingan volume fasa
umpan terhadap fasa penerima tinggi, sehingga mampu memberikan
faktor konsentrasi (pemekatan) yang tinggi.
c. Hanya sedikit sekali jumlah pengekstrak (senyawa pembawa), yang
dibutuhkan tidak lebih dari 1% dari jumlah pengekstrak yang digunakan
dalam ekstraksi pelarut biasa.
d. Tidak ada pemisahan lebih lanjut, karena fasa air dan fasa minyak sudah
terpisah dengan sendirinya (satu tahap).
e. Jumlah fasa organik yang terbawa oleh hasil ekstraksi dapat diabaikan.
f. Peralatan yang digunakan cukup sederhana dan mudah dioperasikan.
Logam akan membentuk kompleks dengan ligan pembawa dalam fasa
membran. Kompleks yang terbentuk akan terdisosiasi di antar muka fase
membran-fase penerima dan logam akan terlepas kembali ke fase penerima
(Lamb et al, 1980:6820-6824).
Mekanisme transport ion logam yang terjadi sebagai berikut:
a. Ligan dan ion logam saling berada di antarmuka fase sumber-fase
membran, kemudian ligan melepaskan proton untuk membentuk
b. Didalam fase membran, kompleks ligan-logam berdifusi melalui
membran cair organik menuju ke antarmuka fase membran-fase
penerima.
c. Kompleks ligan-logam yang berada di antarmuka fase membran-fase
penerima menangkap proton dari fase penerima menjadi ligan bebas dan
ion logam ke fasa penerima berasosiasi dengan anion fase di penerima.
d. Ligan bebas terdifusi ke antar mua fase sumber-fase membran untuk
memulai transpor lagi (Abbaspour and Tavakol, 1999: 1005-1008).
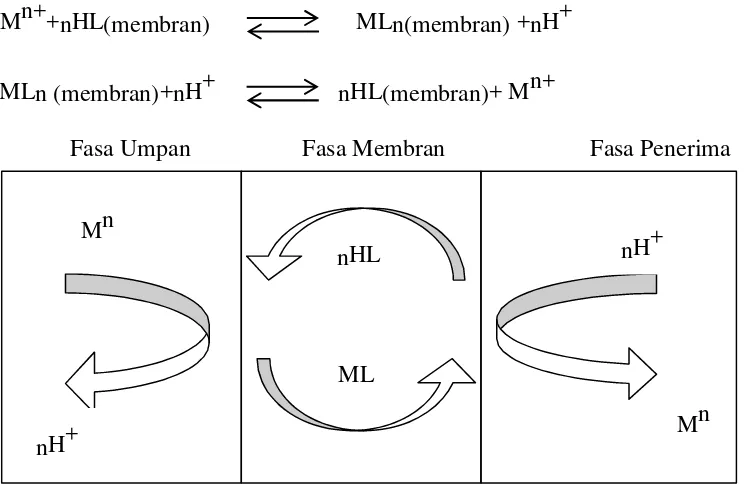
Mekanisme tersebut dapat ditunjukkan melalui Gambar 1.
Mn++nHL(membran) MLn(membran) +nH+
MLn (membran)+nH+ nHL(membran)+ Mn+
Fasa Umpan Fasa Membran Fasa Penerima
Gambar 1. Mekanisme pemisahan ion logam
Dengan penggunaan senyawa pembawa yang tepat, maka ion logam
atau molekul suatu senyawa dapat diekstrak. Mekanisme pemisahan
menggunakan membran cair didasarkan pada transpor ion logam melalui
fasa membran yang didalamnya terkandung senyawa pembawa dan dapat
terpisah dikarenakan adanya muatan H+dari fasa penerima. Dan ion logam
yang terikat pada senyawa pembawa akan tertranspor masuk ke dalam fasa
penerima. Sedangkan kestabilan kompleks itu sendiri ditentukan oleh
beberapa faktor, antara lain jenis atom donor (gugus aktif) senyawa
pembawa yang sesuai dengan konfigurasi elektron logam.
Senyawa logam akan membentuk kopleks dengan ion logam melalui
ikatan kimia antara gugus aktif dengan ion logam. Senyawa pembawa ini
akan membentuk kompleks dengan ion logam melalui ikatan kimia antara
gugus aktif dengan ion logam, pembentukan ini didasarkan pada teori
HSAB (pengelompokan asam basa berdasarkan kekerasan dan kelunakan).
Asam basa lunak (soft acids bases) adalah asam basa yang elektron-elektron
valensinya muadah terpolarisasi atau terlepaskan, sedangkan asam basa
keras (hard acids bases) adalah asam basa yang tidak mempunyai elektron
valensi atau elektron valensinya sukar terpolarisasi. Berdasarkan prinsip
HSBA (Hard and Soft Acid Base), asam keras cenderung lebih suka untuk
berkoordinasi dengan basa keras dan demikian juga halnya dengan asam
lunak cenderung lebih suka berkoordinasi dengan basa lunak. Asam keras
dan basa keras cenderung mempunyai atom kecil, oksidasi tinggi, kepolaran
rendah dan keelektronegatifan tinggi. Sedangkan asam lunak dan basa lunak
cenderung mempunyai atom besar, tingkat oksidasi rendah dan
keelektronegatifan rendah. Interaksi antara asam keras dan basa kera disebut
interaksi ionik, sedangkan interaksi antara asam lemah dan basa lemah lebih
bersifat kovalen (Bowser, JR. 1993:322-325).
Kelas Asam Basa
(seperti logam alkali, alkali tanah, dan Cr3+) lebih kuat kompleksnya dengan
basa keras (seperti RO-), ion asam logam lunak (seperti Cd2+) akan
membentuk kompleks yang lebih kuat dengan basa lunak (seperti yang
berasal dari 2-tiopentanol), dan ion-ion asam logamborderline(seperti Zn2+)
dengan basaborderline(Cahyono, 2007: 39-43)
3. Metode Membran cair fasa ruah
Membran cair ruah adalah salah satu sistem paling sederhana untuk
melakukan proses ekstraksi dengan metode membran cair. Dalam
prakteknya menggunakan gelas tipe-U yang berisi fasa umpan dan fasa
penerima yang dipisahkan oleh cairan membran. Ruah dalam hal ini berarti
membran cair fasa ruah dapat digunakan sebagai salah satu alternatif media
transpor dalam penarikan dan pemisahan ion logam. Transpor selektif
ion-ion logam melalui membran cair diaplikasikan untuk mengatasi masalah
pencemaran yang disebabkan oleh logam-logam berat. Membran cair
bersifat semipermiabel dapat berupa pelarut organik atau anorganik yang
berperan sebagai lintas transpor komponen kimia atau ion logam yang akan
dipisahkan (Molina et. al., 1997. Hlm 10323-10331).
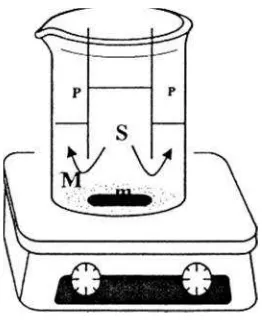
Gambar 2. Model reaktor Transpor melalui teknik membran cair Ruah
Dimana: S = fasa sumber, fasa air yang berisi ion logam
M = fasa membran, pelarut dengan zat pembawa
P = fasa penerima, fasa air larutan penerima
M = batang pengaduk
Mekanisme transpor ion logam melaui membran cair fasa ruah terjadi
pada antar muka fasa sumber-fasa membran terjadi interaksi ion logam
dengan senyawa. Dengan adanya pengadukan akan mempercepat trampor
ion logam dari fasa membran-fasa penerima, dengan kondisi fasa penerima
yang bersifat asam mengakibatkan terjadinya pelepasan ion logam ke fasa
Dalam transpor membran cair ruah, peristiwa transpor dapat terjadi
melalui membran dari fasa sumber ke fasa penerima yang terjadi secara
difusi kompleks logam target di dalam membran ruah yang dibatasi
antarmuka dua fasa larutan/membran. Dalam hal membran cair ruah,
senyawa pembawa diasumsikan dapat berpindah secara bebas dalam
membran. Pada umumnya selektivitas yang baik untuk ion utama dapat
dicapai dengan senyawa pembawa makromolekul, meskipun kadang dapat
berubah secara signifikan tergantung pada struktur kimianya (La Harimu et.
al., 2010: Hlm 69-74).
4. Logam berat
Logam berat adalah bahan-bahan alami yang berasal dan termasuk
bahan penyusun lapisan tanah bumi. Logam berat tidak dapat diurai atau
dimusnahkan. Logam berat dapat masuk ke dalam tubuh mahluk hidup
melalui makanan, air minum, dan udara. Logam berat berbahaya karena
cenderung terakumulasi di dalam tubuh mahluk hidup. Laju akumulasi
logam-logam berat ini di dalam tubuh pada banyak kasus lebih cepat dari
kemampuan tubuh untuk membuangnya. Akibatnya keberadaannya di dalam
tubuh semakin tinggi, dan dari waktu ke waktu memberikan dampak yang
makin merusak.
Berdasarkan sifat kimia dan fisikanya, maka tingkat atau daya racun
logam berat terhadap hewan air dapat diurutkan (dari tinggi ke rendah)
sebagai berikut merkuri (Hg), kadmium (Cd), seng (Zn), timah hitam (Pb),
krom (Cr), nikel (Ni), dan kobalt (Co) (Sutamihardja dkk, 1982). Menurut
rendah terhadap manusia yang mengkomsumsi ikan adalah sebagai berikut
> > > > > > >
Beberapa dari logam berat dapat beracun bagi tubuh mahkluk hidup
dan beberapa yang lain bersifat karsinogen (penyebab cancer) atau beracun/
berefek negatif pada organ-organ tertentu, seperti pada sistem saraf pusat
(Hg, Pb, As), organ ginjal atau liver (Hg, Pb, Cd, Cu), serta kulit, tulang,
atau gigi (Ni, Cd, Cu, Zn), pada takaran jumlah yang sedikit, sebenarnya
berguna bagi mahluk hidup (Co, Cu, Zn, Ni) (Srikandi Fardiaz, 1992: 48).
5. Seng (II)
Seng adalah logam yang putih kebiruan, mudah ditempatmelebur
pada 410oC dan mendidih pada 906oC. Seng dapat larut dalam HCl, H SO
encer untuk membebaskan gas H . Logam seng dengan larutan HNO
encer dapar larut tapi tidak menghasilkan gas. Logam seng dalam H SO
pekat akan menghasilkan gasSO (Abdul Karim Zulkarnain, 1991: 58).
Logamnya yang murni, melarut lambat sekali dalam asam dan dalam alkali.
Adanya zat-zat pencemar atau kontak dengan platinum atau tembaga yang
dihasilkan oleh penambahan beberapa tetes larutan garam dari logam-logam
ini mempercepat reaksi (Svehla, 1990). Limbah industri yang menghasilkan
seng antara lain, industri pelapisan besi dan baja, industri kayu, industri
kulit, industri cat dan industri kosmetik (Heryando Palar, 1994: 97). Seng
dalam bentuk sulfida digunakan untuk industri tabung televisi dan lampu
pendar. Seng dalam bentuk klorida digunakan untuk pengawetan kayu
(http://id.wikipedia.org./wiki/Seng). Sumber utama Seng adalah sphalerit (ZnS)
dibentuk dengan pembakaran logamnya di udara atau dengan pirolisis
karbonat atau nitratnya. Komplek seng juga sangat penting secara biologis.
Senyawaan seng khususnya ZnCO dan ZnO digunakan dalam salep obat
(Cotton dan Wilkinson, 1989: 397-402). Sebagian besar garam Seng larut
dalam air dan larutan ini mengandung ion kompleks tak berwarna heksakuo
seng(II) [Zn(H O) ] . Padatan garam umumnya terhidrat, misalnya
heksahidrat untuk Seng (II) nitrat, heptahidrat untuk seng (II) sulfat dan ini
mirip dengan magnesium(II) dan kobalt(II). Struktur Seng(II) sulfat
heptahidrat yaitu [Zn(H O) ] .H O (Kristian H. Sugiarto. 2003:
158).
Seng digunakan terutama sebagai pelapis besi untuk mencegah
terjadinya korosi. Pelapisan logam dengan logam pelapis seng memiliki
beberapa keuntungan yaitu murah, cukup tersedia di alam dan relatif tahan
lama (Aan Komariyah, 2008: 33). Pelapisan demikian ini dikenal sebagai
proses galvanisasi yang berdasarkan pada sifat elektrokimia proses yang
bersangkutan. Keuntungan pelapisan ini yaitu meskipun lapisan seng telah
terkoyak hingga besi tampak kelihatan dari luar, logam seng akan
teroksidasi lebih dulu. Hal ini terjadi karena nilai potensial reduksi Seng
lebih negatif daripada besi.
6. Tanin
Tanin merupakan salah satu senyawa polifenol dengan berat molekul
memiliki sifat yang khas baik fisik maupun kimianya, struktur tanin dengan
formula empiris C76H52O46 (http://encyclopedia.com/article/12626.html).
Tanin biasanya dalam tumbuhan berfungsi sebagai sistem pertahanan dari
predator, contohnya pada buah yang belum matang, buah akan terasa asam
dan sepat, hal ini sama dengan sifat tanin yang asam dan sepat. Selain itu
tanin juga dapat mengendapkan protein, alkaloid, dan glatin. Tanin juga
dapat membentuk kelat dengan logam secara stabil, sehingga dari sifat ini
tanin digunakan untuk mengekstraksi logam.
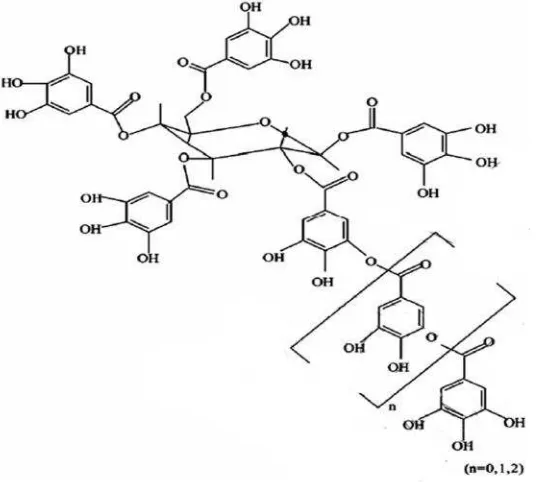
Struktu Tanin terhidrolisis dapat dilhat pada gambar 3.
Gambar 3. Struktur tanin terhidrolisis
Tanin diklasifikasikan menjadi dua jenis yaitu tanin terhidrolisis dan
tanin terkondensasi. Masing-masing jenis memiliki struktur dan sifat yang
berbeda. Untuk tanin yang tehidrolisis memiliki ikatan glikosida yang dapat
terhidrolisis lebih mudah untuk dimurnikan daripada jenis terkondensasi
(Bate-Smith and Swain, 1962, Hal 764).
Tanin memiliki peranan biologis yang kompleks. hal ini dikarenakan
sifat tanin yang sangat kompleks mulai dari pengkelat logam. Dari sifat
sebagai pengkelat logam ini maka tanin dapat digunakan sebagai fase
pembawa dalam penelitian ini (Baeza at al. 1986: 21-31).
7. Spektrofotometri Inframerah
Spektrofotometri IR adalah suatu metode analisis mengenai interaksi
energi cahaya dan materi, dimana energi yang dipancarkan berasal dari
radiasi infra merah dengan panjang gelombang yang lebih pendek dari
radiasi gelombang mikro. Spektrofotometri IR digunakan untuk
mempelajari berbagai jenis sampel, baik identifikasi senyawa organik
maupun anorganik.
Radiasi IR terletak pada daerah panjang gelombang (): 0,78 –1000
μ m atau bilangan gelombang ( ): 12800 – 10 cm-1. Radiasi IR dibedakan
menjadi: IR dekat (Near IR): 0.78-2,5 µm, : 12800-4000 cm-1, IR
pertengahan (middle IR): 2,5-50 µm, : 4000-200 cm-1dan IR jauh (far
IR): 50-1000 µm, : 200-10 cm-1. Sedangkan untuk analisis instrumen
radiasi IR memiliki: 2,5-15µm, : 4000-670 cm-1(Khopkar, 2007: 231).
Syarat suatu gugus fungsi dalam suatu senyawa dapat terukur pada
spektra IR adalah adanya perbedaan momen dipol pada gugus tersebut.
Vibrasi ikatan akan menimbulkan fluktuasi momen dipol yang
menghasilkan gelombang listrik. Untuk pengukuran menggunakan IR
bilangan gelombang ini disebut daerah IR sedang, dan merupakan daerah
optimum untuk penyerapan IR bagi ikatan-ikatan dalam senyawa organik
(Harjono, 1992: 1)
Tabel 2. Korelasi daerah serapan Inframerah
( μ m ) ( ) Ikatan yang menyebabkan Absorpsi
Regang C = O ( asam, aldehida,keton, amida,
ester, anhilida
Regang C = C ( alifatik dan aromatic ) C = N
Lentur C–H
Lentur C = C–H , Ar–H ( luar bidang).
Sumber: www.le.ac.uk/chemistry
Spektrofotometer IR dapat menganalisis letak dan ukuran relatif
absorpsi atau puncak pada daerah IR, dengan memperhatikan ada tidaknya
gugus fungsional yang pokok yaitu C=O, O-H, N-H, C-O, C=C, CC,
CN, dan NO2. Banyaknya gugus yang identik dalam sebuah molekul
mengubah kuat relatif pita absorpsinya dalam suatu spektrum. Pita absorpsi
C-H ( = ± 3000 cm-1) tidak perlu dianalisis secara mendalam karena
hampir semua senyawa memiliki absorbsi ini. Selain itu, hal-hal kecil di
sekeliling gugus fungsional yang didapatkan juga tidak perlu dihiraukan
absorpsi-IR atau spektrum-absorpsi-IR yang sama (fingerprint spectrum) (Day dan Under
wood, 2002: 387).
8. Atomic Absorption Spectroscopy (AAS)
Atomic Absorption Spectroscopy (AAS) atau Spektroskopi serapan
atom adalah suatu teknik atau metode analisis kimia yang pengukurannya
berdasarkan penyerapan cahaya dengan panjang gelombang tertentu oleh
atom logam dalam keadaan bebas (Skoog et. Al., 2000). Prinsip dasar
Spektroskopi serapan atom adalah interaksi antara radiasi elektromagnetik
dengan sampel. Spektroskopi serapan atom merupakan metode yang sangat
tepat untuk analisis zat pada konsentrasi rendah (Khopkar, 1990, Hal
290-305).
Pada alat AAS terdapat dua bagian utama yaitu suatu sel atom yang
menghasilkan atom-atom gas bebas dalam keadaaan dasarnya dan suatu
sistem optik untuk pengukuran sinyal. Suatu skema umum dari alat AAS
adalah sebagai berikut:
Gambar4. Skema Umum Komponen pada Alat AAS
Cara kerja Spektroskopi Serapan Atom ini adalah berdasarkan atas
diubah menjadi atom bebas. Atom tersebut mengapsorbsi radiasi dari
sumber cahaya yang dipancarkan dari lampu katoda berongga (Hollow
Cathode Lamp) yang mengandung unsur yang akan ditentukan. Banyaknya
penyerapan radiasi kemudian diukur pada panjang gelombang tertentu
menurut jenis logamnya (Darmono,1995, Hal 157).
Metode Atomic Absorption Spectroscopy (AAS) berprinsip pada
absorbsi cahaya oleh atom. Atom-atom menyerap cahaya tersebut pada
panjang gelombang tertentu, tergantung pada sifat unsurnya. Metode
serapan atom tergantung pada perbandingan dan tidak bergantung pada
temperatur. Setiap alat Atomic Absorption Spectroscopy (AAS) terdiri dari
tiga komponen yaitu unit atomisasi, sumber radiasi dan sistem pengukur
fotometerik. TeknikAtomic Absorption Spectroscopy (AAS) menjadi teknik
yang paling banyak digunakan dalam analisis. Hal ini disebabkan karena
sebelum pengukuran tidak selalu memerlukan pemisahan unsur yang
ditentukan karena kemungkinan penentuan satu unsur dengan kehadiran
unsur lain dapat dilakukan, asalkan katoda berongga yang diperlukan
tersedia. Atomic Absorption Spectroscopy (AAS) dapat digunakan untuk
analisis logam sebanyak 61 logam.
Apabila cahaya dengan panjang gelombang tertentu dilewatkan pada
suatu sel yang mengandung atom-atom bebas yang bersangkutan maka
sebagian cahaya tersebut akan diserap dan intensitas penyerapan akan
berbanding lurus dengan banyaknya atom bebas logam yang berada dalam
1. Hukum Lambert : Bila suatu sumber sinar monokromatik melewati
medium transparan, maka intensitas sinar yang diteruskan berkurang
dengan bertambahnya ketebalan medium yang mengabsorpsi.
2. Hukum Beer : Intensitas sinar yang diteruskan berkurang secara
eksponensial dengan bertambahnya konsentrasi spesi yang menyerap
sinar tersebut.
Dari kedua hukum tersebut diperoleh suatu persamaan:
It = Io.e-(εbc), atau A= -Log It/Io = εbc
Keterangan : Io = intensitas sumber sinar
It = intensitas sinar diteruskan
Ε = absortivitas Molar (L/mol.cm)
b = panjang medium (cm)
c = konsentrasi atom-atom yang menyerap sinar
(mol/L)
A = absorbansi
Dari persamaan di atas, dapat disimpulkan bahwa absorbansi cahaya
berbanding lurus dengan konsentrasi atom (Day & Underwood, 1989.
421-428).
Kurva kalibrasi dibuat dengan cara mengamati absorbansi
masing-masing konsentrasi larutan standar. Kurva kalibrasi yang diperoleh tidak
selalu linier. Hal ini disebabkan oleh penyimpangan dalam analisis, karena
atom yang dihasilkan dalam nyala tidak sebanding dengan jumlah atom
yang sesungguhnya. Oleh karena itu hukum Lambert-Beer mengalami
regresi linear (Sudjana, 1992:312). Kurva kalibrasi yang diperoleh, tidak
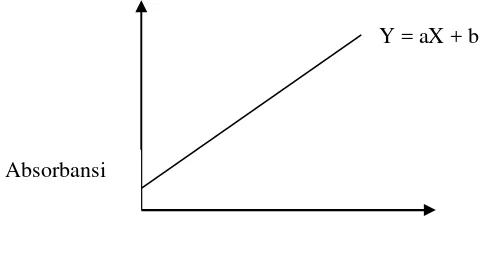
melalui titik (0,0) sebagaimana ditunjuk Gambar 5.
Gambar 5. Kurva Kalibrasi Larutan Standar
Sesuai gambar 5 dapat diambil hubungan antara absorbansi dengan
konsentrasi larutan standar dan diperoleh suatu persamaan yaitu :
Y = aX + b
Keterangan : Y = Absorbansi a = Slope
X = Konsentrasi b = intersep
Penentuan kadar sampel dapat dilakukan dengan memplotkan data
absorbansi terhadap konsentrasi atau dengan cara mensubstitusikan
absorbansi ke dalam persamaan garis lurus.
Penggunaan metode spektroskopi serapan atom dapat digunakan untuk
kepentingan analisis, baik analisis kualitatif dan analisis kuantitatif.
a. Analisis kualitatif
Analisis kualitatif digunakan untuk menentukan ada atau tidaknya suatu
unsur dalam suatu senyawa. Analisis kualitatif dengan metode ini dapat
ditunjukkan apabila sampel yang telah diubah menjadi gas ditembakkan
suatu sinar yang berasal dari hollow cathode lamp dan terdeteksi
Konsentrasi Larutan Standar
Y = aX + b
tersebut mengandung unsur yang dimaksud. Sebagai contoh, dalam
analisis logam Seng dalam sampel limbah penyamakan kulit dengan
metode Spektroskopi Serapan Atom, sampel tersebut memberikan
serapan, sehingga dapat diambil kesimpulan bahwa sampel limbah
penyamakan kulit mengandung logam Seng(II).
b. Analisis kuantitatif
Sedangkan untuk analisis kuantitatif digunakan untuk menentukan
seberapa banyak suatu unsur terkandung dalam senyawa. Untuk analisis
Kuantitatif menggunakan metode kurva kalibrasi. Analisis kuantitatif
pada dasarnya juga menggunakan serapan sebagai indikatornya, tetapi
serapan yang terjadi diukur menggunakan detektor yang selanjutnya
dihitung menggunakan persamaan regresi linear untuk menentukan
kadarnya. Dengan cara memplotkan data absorbansi terhadap konsentrasi
atau dengan cara mensubstitusikan absorbansi ke dalam persamaan garis
lurus.
B. Penelitian Yang Relevan
Penelitian mengenai penggunaan senyawa tanin sebagai senyawa
pembawa (carrier) pada ekstraksi logam Zn(II) didasarkan pada penelitian
sebelumnya. Pada penelitian yang dilakukan oleh M. Djunaidi et.al. (2007
hal 1) telah berhasil diekstrak logam Zn(II) dari larutan fasa umpan.
Penelitian ini menggunakan senyawa polieugenol sebagai senyawa
pembawa dan menghasilkan efisiensi transport yang cukup besar. Senyawa
ekstraksi ion logam Zn(II) merupakan senyawa turunan eugenol yang
dipolimerkan. Senyawa polieugenol memiliki gugus aktif –OH yang dapat
dipertukarkan dengan ion logam, sehingga dapat digunakan sebagai fasa
membran dalam teknik ekstraksi dengan metode membran cair.
Penelitian Olly, Zaharasmi dan Eka (2005: 23-34), hasil penelitian
dapat disimpulkan bahwa transpor ion logam Zn (II) dengan memakai
ditizon sebagai zat pembawa dapat dilakukan melalui teknik membran cair
fasa ruah. Kondisi optimum dari metoda transpor Zn(II) 3,06 x 10-4M antar
fasa adalah pH fasa sumber 8,5, konsentrasi ditizon dalam fasa membran
1,75 x 10-5M, konsentrasi Na2EDTA dalam fasa penerima 0,06 M pada pH
6 dan lama pengadukan 3 jam. Pada kondisi ini didapatkan persentase
transpor ion logam Zn (II) ke fasa penerima 93% dan persentase Zn(II) sisa
di fasa sumber tidak terdeteksi.
Penelitian Arvana Aditya (2013: 35-48), hasil penelitian dapat
disimpulkan bahwa transpor ion logam Cr(III) dengan memakai tanin
termodifikasi sebagai zat pembawa dapat dilakukan melalui teknik
membran cair ruah. Waktu pengadukan terbaik adalah 6 jam dengan
persentase transpor ion logam Cr(III) sebesar 1,408%. Sedangkan konsentrsi
optimum fasa penerima H2SO4 sebesar 0,5 M dengan persentase transpor
ion logam Cr(III) 2,608%.
Penelitian Ramon (2013: 38-53) hasil penelitian dapat disimpulkan
bahwa transpor ion logam Cu(II) dengan memakai tanin termodifikasi
sebagai zat pembawa dapat dilakukan melalui teknik membran cair ruah.
logam Cu(II) sebesar 11,468%. Sedangkan konsentrsi optimum fasa
penerima H2SO4sebesar 1 M dengan persentase transpor ion logam Cr(III)
49,288%.
C. Kerangka Berfikir
Tanin merupakan senyawa fenolik dengan berat molekul cukup tinggi
yang mengandung hidroksil dan kelompok lain seperti karboksil untuk
membentuk komplek yang efektif dengan protein dan makro molekul yang
lain dibawah kondisi lingkungan tertentu, dapat dikatakan tanin merupakan
bentuk komplek dari protein, pati, selulosa dan mineral (Artati, 2007:
33-38). Dengan gugus aktif yang dimilikinya, maka senyawa tanin diduga dapat
digunakan sebagai senyawa pembawa yang dapat mengikat ion logam
Zn(II).
Sintesis senyawa pembawa dalam ekstraksi sudah banyak dilakukan,
tetapi penggunaansenyawa tanin sebagai senyawa belum dilakukan
penelitian. Senyawa tanin modifikasi gugus aktifnya dengan reaksi asetilasi.
Metode yang digunakan dalam penelitian ini adalah metode membran cair
ruah (Bulk Liquid Membrane).
BAB III
A. Subjek dan Objek Penelitian
1. Subjek Penelitian
Subjek penelitian adalah penggunanan senyawa tannin termodifikasi
untuk ekstraksi ion logam Zn(II) dengan metode membran cair ruah.
2. Objek Penelitian
Objek penelitian adalah persentase transport ion logam Zn(II).
B. Variabel Penelitian
1. Variabel bebas pada peneilitian adalah variasi waktu pengadukan dan
variasi konsentrasi fasa penerima (H SO ).
2. Variabel kendali pada penelitian adalah kecepatan pengadukan pada
mechanic stirrer yaitu 130 rpm dan pada magnetic stirreryaitu 500
rpm dan waktu pendiaman yaitu 5 menit.
3. Variabel terikat pada penelitian ini adalah persentase transport ion
logam Zn(II).
C. Alat dan Bahan Penelitian
1. Alat-alat yang digunakan dalam penelitian adalah:
a) Spektrofotometer Serapan Atom merk Hitachi Zeeman-8000
b) Spektrofotometer Infrared merk Shimadzu FTIR Prestige 21
c) Magnetic Stirrer
d) Mechanic Stirrermerk Eyela Z-1100
e) Neraca Analitik AND HF-3000
g) Gelas ukur
h) Gelas arloji
i) Pipet tetes
2. Bahan-bahan yang digunakan dalam penelitian adalah:
a) Tanin
b) Kristal Zn(NO ).4H O p.a
c) Etil Asetat p.a
d) Aquades
e) H SO 98% p.a
f) Piridin p.a
g) HNO 1M
h) Asetat Anhidrat p.a
i) Kertas Saring
D. Prosedur Penelitian
1. Pembuatan Larutan H SO 1 M sebanyak 1000 mL
Sebanyak 54,35 mL larutan H SO 98% pekat diambil dan dimasukan
ke dalam gelas kimia yang telah berisi akuades melalui dinding gelas
kemudian dituangkan ke dalam labu ukur 1000 mL. Kemudian
diencerkan dengan akuades sedikit demi sedikit sampai volume
tanda batas.
Perhitungan :
Persentase HSO = 98% =
Mol HSO = = = 1 mol
Konsentrasi HSO = = , = 18,4 M
V . M = V . M
V . 18,4 M = 1000 mL . 1 M
V = 54,35 mL
2. Pembuatan Larutan H SO 0,1 M dan 0,5 M sebanyak 100 mL
Sebanyak 10 mL dan 50 mL larutan HSO 1M diambil dan
dimasukkan ke dalam labu ukur 100 mL kemudian diencerkan
dengan akuades sampai tanda batas. Volume larutan HSO yang
diambil berdasarkan perhitungan dengan rumus : V . M = V . M
3. Pembuatan Larutan Induk Zn (II) 1000 ppm sebanyak 500 mL
Pembuatan larutan induk Seng(II) 1000 ppm. Larutan Seng dibuat
dengan melarutkan 1,999 gram Zn(NO ) .4H O lalu dimasukkan ke
dalam gelas kimia dan kemudian ditambahkan 1 mL HNO 1 M gelas
kimia. Larutan kemudian dipindahkan ke dalam labu takar 500 mL
kemudian ditambahkan akuades sampai tandai volume 500 mL.
Massa Zn(NO ) .4H O = ( ) . x 0,5
Massa Zn(NO ) .4H O = ,
, x 0,5
Massa Zn(NO ) .4H O =1,999 gram
Jadi untuk 500 mL larutan membutuhkan 1,999 gram kristal
4. Pembuatan Larutan Umpan Zn (II) 100 ppm sebanyak 500 mL
Sebanyak 50 mL larutan induk Zn(NO ) .4H O 1000 ppm diambil dan
dituangkan ke dalam labu ukur 500 mL. Kemudian diencerkan dengan
akuades sampai tanda volume tepat tanda batas. Volume larutan induk
Zn(NO ) .4H O diambil berdasarkan perhitungan dengan rumus :
V . M = V . M
5. Modifikasi Tanin dengan Reaksi Asetilasi
a. Menimbang sebanyak 2 gram tanin.
b. Mengambil 5 mL piridin dengan gelas ukur 10mL.
c. Mengambil 5 mL asetat anhidrat dengan gelas ukur 10mL.
d. Memasukkan tanin kedalam gelas kimia kemudian menambahkan
campuran 5 mL piridin dan 5 mL asetat anhidrat.
e. Mengaduk hingga serbuk tanin larut sempurna.
f. Menuangkan larutan tersebut kedalam 100 mL akuades.
g. Padatan tanin termodifikasi akan terbentuk dan saring dengan kertas
saring.
h. Mencuci padatan tanin termodifikasi dengan asam asetat 0,1 M untuk
menghilangkan piridin.
i. Mencuci padatan tanin termodifikasi dengan akuades.
j. Mengeringkan tanin termodifikasi pada suhu 50°C selama 1 malam
k. Tanin termodifikasi selanjutnya dikarakterisasi dengan
Spektrofotometer Infra Red untuk mengetahui gugus-gugus aktifnya.
Sebanyak 0,5 gram serbuk tanin yang telah termodifikasi dimasukkan
dalam gelas kimia. Kemudian ditambahkan 50 mL etil asetat p.a dan
diaduk sampai serbuk tanin termodifiksai larut sempurna.
7. Ekstraksi Logam Zn(II) dengan metode membrane cair fasa ruah (Bulk Liquid Membrane)
a. Pengaruh waktu ekstraksi terhadap transpor ion logam Zn(II)
1) Memasukkan beker gelas 50 mL ke dalam beker gelas 250 mL terlihat
pada gambar 6.
2) Menuangkan sebanyak 50 mL fasa umpan ke dalam tabung beker
gelas 50 mL.
3) Menuangkan sebanyak 100 ml fasa penerima (H SO ) 0,1 M pada
beker gelas 250 mL.
4) Menuangkan 50 mL fasa membran di atas permukaan kedua fasa.
5) Mengaduk dengan mechanic Stirrer pada kecepatan 130 rpm dan
magnetis Stirrerpada kecepatan 500 rpm selama 2 jam.
6) Mengambil fasa umpan dan fasa penerima kemudian memasukkan ke
dalam botol penyimpan, tutup dengan alumunium foil dan dianalisis
menggunakan AAS.
7) Mengulangi prosedur 1 sampai 5 dengan waktu pengadukan selama 4
jam.
8) Mengambil fasa umpan dan fasa penerima kemudian memasukkan ke
dalam botol penyimpan, tutup dengan alumunium foil dan dianalisis
9) Mengulangi prosedur 1 sampai 5 dengan waktu pengadukan selama 6
jam.
b. Pengaruh konsentrasi fasa penerima terhadap transpor ion logam Zn(II)
1) Memasukkan beker gelas 50 mL ke dalam beker gelas 250 mL terlihat
pada gambar 6.
2) Menuangkan sebanyak 50 mL fasa umpan ke dalam beker gelas 50
mL.
3) Menuangkan sebanyak 100 ml fasa penerima (H SO ) 0,1 M ke dalam
beker gelas 250 mL.
4) Menuangkan 50 mL fasa membran di atas permukaan kedua fasa.
5) Mengaduk dengan mechanic Stirrer pada kecepatan 130 rpm dan
magnetis Stirrer pada kecepatan 500 rpm selama waktu terbaik (6
jam).
6) Mengambil fasa umpan dan fasa penerima kemudian memasukkan ke
dalam botol penyimpan, tutup dengan alumunium foil dan dianalisis
menggunakan AAS.
7) Mengulangi prosedur 1 sampai 5 dengan menggunakan waktu
optimum yang telah didapatkan pada prosedur sebelumnya dan
konsentrasi fasa penerima digunakan 0,1 M.
8) Mengambil fasa umpan dan fasa penerima kemudian memasukkan ke
dalam botol penyimpan, tutup dengan alumunium foil dan dianalisis
9) Mengulangi prosedur 1 sampai 5 dengan menggunakan waktu terbaik
yang telah didapatkan pada prosedur sebelumnya dan konsentrasi fasa
penerima digunakan 0,5 M dan 1 M.
10) Mengambil fasa umpan dan fasa penerima kemudian memasukkan ke
dalam botol penyimpan, tutup dengan alumunium foil dan dianalisis
menggunakan AAS.
11) Dari prosedur diatas didapatkan konsentrasi optimum fasa penerima
pada ektraksi logam Zn(II) dengan metode membran cair fasa ruah.
Gambar 6. Sistem Ekstraksi dengan Metode Membran Cair Ruah
8. Pembuatan Kurva Kalibrasi Larutan standar
a. Diambil 0,0; 0,1; 0,2; 0,3; 0,4 dan 0,5 mL larutan seng(II) 100 ppm.
Dimasukkan dalam labu ukur 50 mL lalu diencerkan dengan akuades
sampai tanda batas sehingga konsentrasi standar adalah 0,0; 0,2; 0,4;
b. Diukur absorbansi dari larutan standar pada panjang gelombang 217
nm.
c. Dibuat kurva larutan standar absorbansi (A) vs konsentrasi (C)
berdasarkan data yang diperoleh.
E. ANALISIS DATA PENELITIAN 1. Analisis kualitatif
Analisis kadar seng(II) dilakukan dengan cara mengukur serapan larutan
standar pada alat Spektrofotometer Serapan Atom sesuai kondisi
pengukuran yang telah ditentukan perlakuan yang sama juga dilakukan
untuk menganalisis larutan sampel. Data analisis kualitatif yang diperoleh
dari AAS meliputi data absorbansi larutan standar dan absorbansi larutan
sampel.
2. Analisis kuantitatif
a. Penentuan Persamaan Garis Regresi Linier
Persamaan regresi linier dirumuskan sebagai Y = aX + b
Dengan,
a = ( )( )
( ) ...(1)
b = ( ) ( )( )
( ) ...(2)
Keterangan :
Y : Absorbansi
X : Konsentrasi
n : jumlah larutan
b. Penentuan Signifikansi Korelasi Konsentrasi (X) dan Absorbansi (Y)
Untuk menentukan korelasi antara konsentrasi dan absorbansi larutan
standard digunakan teknik korelasi momen tangkar (korelasi product
moment)dengan rumus sebagai berikut:
=
( ) ( )...(3)
Dengan,
= -( )( ) ...(4)
²= ²-( )²...(5)
²= ²-( )²...(6)
Kemudian untuk menguji signifikansi harga , harga tersebut
dikonsultasikan dengan r table pada taraf signifikansi 5%. Apabila harga
hasil perhitungan lebih besar dari r table, maka ada korelasi yang
bermakna antara konsentrasi (X) dengan absorbansi (Y) (Sutrisno Hadi,
2005: 5)
c. Uji Lineritas Persamaan Regresi
Tujuan dari uji linearitas persamaan garis untuk mengetahui ada
tidaknya hubungan yang bermakna antara konsentrasi (X) dengan
absorbansi (Y). Penentuan Linearitas garis regresi dari kurva larutan
standar kromium diuji dengan menghitung harga F menggunakan rumus
sebagai berikut: