20 III. METODOLOGI PENELITIAN
3.1 Tempat dan Waktu Penelitian
Penelitian ini dilaksanakan pada bulan Februari 2021 sampai Juli 2021 di Laboratorium Teknologi Pangan Universitas Muhammadiyah Malang.
3.2 Alat dan Bahan
Alat-alat yang digunakan dalam proses pembuatan edible coating adalah cabinet dryer, oven, magnetic stirrer, loyang plastik, plat kaca, ayakan 80 mesh, timbangan analitik, baskom, batang pengaduk, spatula, sendok makan, cup plastik, plastik wrap , gelas ukur, beaker glass, hot plate, termometer, penjepit, dan blender. Alat-alat yang digunakan untuk analisis edible coating adalah pipet tetes, pipet ukur, gelas ukur, beaker glass, texture analyzer, mortal-martil, pisau, tabung reaksi, erlenmeyer, oven, cawan porselen, pipet filler, rak tabung reaksi, kertas saring, plastik wrap,color reader, hot plate, micrometer scrup, Spektrofotometri, desikator, dan rotary evaporator.
Bahan-bahan yang digunakan pada proses pembuatan edible film dan edible coating adalah pati ubi jalar ungu varietas antin 3 yang diperoleh dari Balai Penelitian Tanaman Aneka Kacang dan Umbi, jahe merah yang digunakan berasal dari UPT. Materia Medika, buah nanas madu yang diperoleh dari pasar lokal, gliserol, dan aquades. Bahan-bahan yang digunakan dalam analisa adalah Etanol 96% food grade, dan DPPH.
3.3 Metode Penelitian
Penelitian ini menggunakan metode Rancangan Acak Kelompok (RAK) faktorial yang terdiri dari dua faktor dengan tiga kali ulangan. Kedua faktor merupakan konsentrasi penggunaan bahan penyusun edible coating. Faktor pertama yaitu perbedaan konsentrasi penggunaan pati ubi jalar ungu dan faktor kedua yaitu perbedaan konsentrasi penggunaan ekstrak jahe merah. Setiap faktor mempunyai 3 level sebagai berikut.
Faktor I Konsentrasi Penggunaan Pati Ubi Ungu (P) (b/v) P1: Konsentrasi Pati Ubi Jalar Ungu 3%
P2: Konsentrasi Pati Ubi Jalar Ungu 4% P3: Konsentrasi Pati Ubi Jahe Ungu 5%
21 Faktor II Konsentrasi Ekstrak Jahe Merah (J) (v/v)
J1: Konsentrasi Ekstrak Jahe Merah 0% J2: Konsentrasi Ekstrak Jahe Merah 1,5% J3: Konsentrasi Ekstrak Jahe Merah 3%
Kombinasi dari kedua faktor dengan tiga level menghasilkan 9 kelompok perlakuan sebagai berikut.
Tabel 4. Hasil kombinasi perlakuan
J1 J2 J3
P1 P1J1 P1J2 P1J3
P2 P2J1 P2J2 P2J3
P3 P3J1 P3J2 P3J3
Keterangan Kombinasi Perlakuan:
P1J1: Pati Ubi Ungu 3% + Ekstrak Jahe Merah 0% P1J2: Pati Ubi Ungu 3% + Ekstrak Jahe Merah 1,5% P1J3: Pati Ubi Ungu 3% + Ekstrak Jahe Merah 3% P2J1: Pati Ubi Ungu 4% + Ekstrak Jahe Merah 0% P2J2: Pati Ubi Ungu 4% + Ekstrak Jahe Merah 1,5% P2J3: Pati Ubi Ungu 4% + Ekstrak Jahe Merah 3% P3J1: Pati Ubi Ungu 5% + Ekstrak Jahe Merah 0% P3J2: Pati Ubi Ungu 5% + Ekstrak Jahe Merah 1,5% P3J3: Pati Ubi Ungu 5% + Ekstrak Jahe Merah 3%
Data yang didapatkan akan dianalisa menggunakan Analysis of Variant (ANOVA) dan dilanjutkan uji banding Duncant’s Multiple Range Test (DMRT) dengan taraf nyata 5% (α=0,05) untuk mendapatkan kesimpulan mengenai pengaruh perlakuan.
3.4 Pelaksanaan Penelitian
Pelaksanaan penelitian ini terdiri dari 3 tahap yang meliputi pembuatan pati ubi jalar ungu dan ekstrak jahe merah, pembuatan edible film yang dilanjutkan dengan analisa fisikokimia, dan pelapisan edible coating pada buah Nanas. Kemudian dilakukan analisa pada buah nanas meliputi susut bobot, kadar air, dan intensitas warna dan tekstur.
3.4.1 Proses Pembuatan Pati Ubi Jalar Ungu (Irhami, 2019)
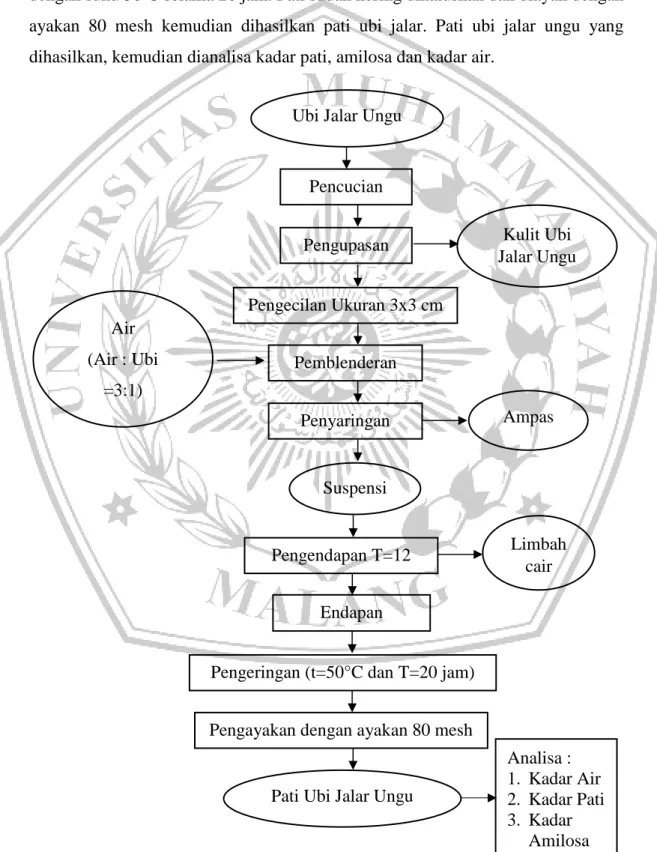
Proses pembuatan pati ubi jalar ungu bersumber pada metode yang telah dilakukan oleh Latifah (2009). Ubi jalar ungu sudah didapatkan dilakukan penyortiran kemudian pencucian ubi jalar ungu hingga bersih dan pengupasan ubi
22 jalar ungu dengan pisau. Setelah itu, ubi jalar ungu dilakukan proses pemotongan sesuai ukuran yaitu 3x3 cm dan dihancurkan dengan blender dengan akumulasi air menggunakan rasio 1:3 sampai menjadi bubur dan disaring dengan kain saring. Suspensi ubi jalar ungu yang dihasilkan, diendapkan selama 12 jam pada suhu ruang. Endapan pati yang sudah terbentuk dikeringkan pada pengering cabinet dengan suhu 50ºC selama 20 jam. Pati sudah kering dihaluskan dan diayak dengan ayakan 80 mesh kemudian dihasilkan pati ubi jalar. Pati ubi jalar ungu yang dihasilkan, kemudian dianalisa kadar pati, amilosa dan kadar air.
Gambar 4. Diagram Alir Pembuatan Pati Ubi Jalar Ungu (Irhami, 2019) Ubi Jalar Ungu
Pencucian Pengupasan Pengecilan Ukuran 3x3 cm Pemblenderan Pengendapan T=12 jam
Pengeringan (t=50°C dan T=20 jam)
Pengayakan dengan ayakan 80 mesh
Pati Ubi Jalar Ungu Air (Air : Ubi =3:1) Penyaringan Kulit Ubi Jalar Ungu Analisa : 1. Kadar Air 2. Kadar Pati 3. Kadar Amilosa Limbah cair Ampas Endapan Suspensi
23 3.4.2 Proses Pembuatan Ekstrak Jahe Merah (Kusuma, 2015 Modifikasi)
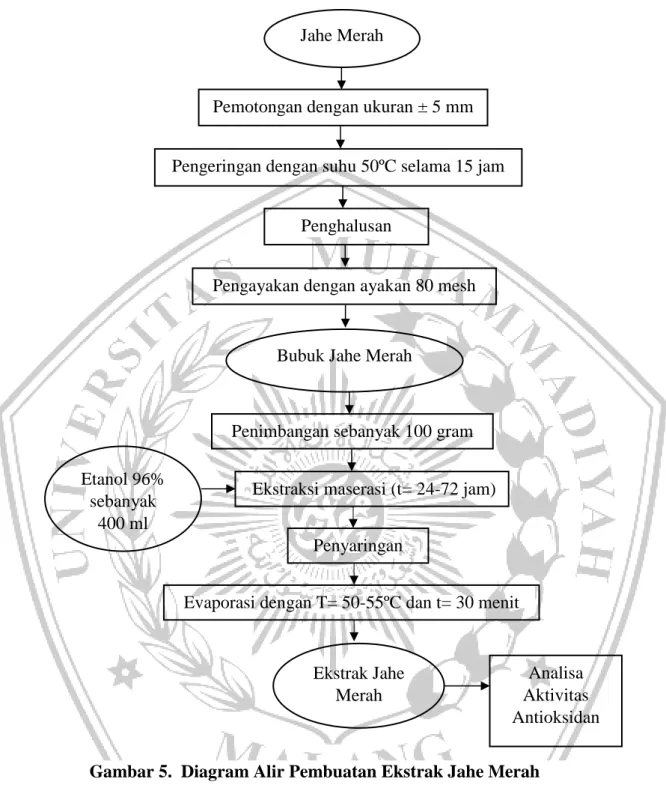
Ekstrak jahe merah dibuat dengan metode ekstraksi maserasi dilakukan pada suhu kamar. Langkah pertama dalam ekstraksi jahe merah adalah 1 kg jahe dicuci dengan air mengalir. Kemudian dipotong-potong sekitar ukuran ± 5 mm, dikeringkan dalam cabinet dryer pada suhu 50 °C selama 15 jam, dihaluskan dengan blender dan diayak dengan ukuran 80 mesh. Serbuk jahe merah yang diperoleh ditimbang hingga 100 gram, kemudian ditambahkan 400 ml etanol 96% ke dalam labu Erlenmeyer, kemudian diaduk selama 5 menit dan dilakukan proses ekstraksi selama 24-72 jam dengan sesekali diaduk rata kembali. Endapan disaring menggunakan kertas Whatman nomer 42 menggunakan serangkaian pompa vakum. Ekstrak yang diperoleh diuapkan pada suhu sekitar 50-55°C selama 30 menit pada rotary evaporator untuk mendapatkan ekstrak pekat. Ekstrak jahe merah yang dihasilkan dianalisis aktivitas antioksidannya menggunakan metode DPPH. Ekstrak jahe merah yang dihasilkan disimpan dalam lemari es sehingga dapat digunakan kembali. (Kusuma, 2015 modifikasi).
24 Jahe Merah
Pemotongan dengan ukuran ± 5 mm
Pengeringan dengan suhu 50ºC selama 15 jam
Ekstrak Jahe Merah Penghalusan
Pengayakan dengan ayakan 80 mesh
Penimbangan sebanyak 100 gram
Ekstraksi maserasi (t= 24-72 jam)
Penyaringan Etanol 96%
sebanyak 400 ml
Bubuk Jahe Merah
Analisa Aktivitas Antioksidan Evaporasi dengan T= 50-55ºC dan t= 30 menit
Gambar 5. Diagram Alir Pembuatan Ekstrak Jahe Merah (Kusuma, 2015 Modifikasi)
Gambar 5. Diagram Alir Pembuatan Ekstrak Jahe Merah (Kusuma, 2015 Modifikasi)
25 3.4.3 Proses Pembuatan Edible Film (Basuki, 2014 Modifikasi)
Proses pembuatan edible film yaitu pati ubi jalar ungu ditimbang dengan berat sebanyak 3%, 5% dan 5% (b/vtotal). Pati ubi jalar ungu dan gliserol 20% (v/bpati) disuspensikan dengan 100 ml akuades, dipanaskan hingga suhu 80 °C dengan kompor listrik atau hotplate dan ditahan selama 5 menit. Suspensi yang dibuat dengan pemanasan didinginkan hingga 37 ° C. Ditambahkan ekstrak jahe merah pada konsentrasi 0% 1,5 dan 3% (v/v). Menggunakan pengaduk, campur suspensi dengan ekstrak jahe merah sampai diperoleh konsistensi yang seragam, lalu tuangkan ke dalam loyang. Larutan edible film dikeringkan pada suhu ± 50°C selama 24 jam, kemudian didinginkan pada suhu kamar selama kurang lebih 15 menit agar edible film mudah dikeluarkan dari cetakan. Edible film siap untuk dianalisis.
Pati ubi jalar ungu (3%,4% dan 5%), gliserol 20% dan aquades 100 ml Pemanasan (T= 80oC) Pendinginan hingga T= 37oC Ekstrak jahe merah (0%,1,5% dan 3%) Penuangan ke cetakan Pengeringan (T= 50oC , t= 24 jam) Edible Film Analisa: 1. Ketebalan 2. Elongasi 3. Kuat Tarik 4. Laju transmisi uap air 5. Aktivitas antioksidan Gambar 6. Diagram Alir Pembuatan edible film (Basuki,2014 Modifikasi)
26 3.4.4 Proses Pembuatan Edible Coating (Basuki, 2014 modifikasi)
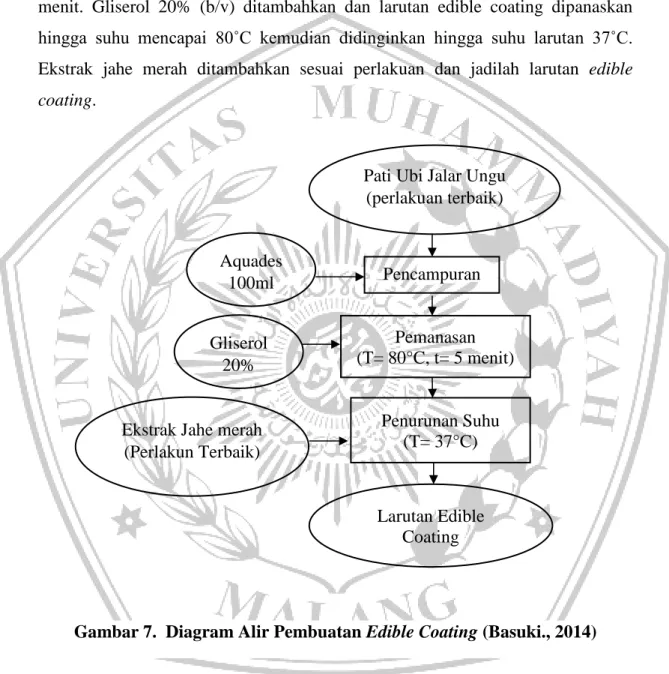
Larutan edible coating dibuat dari pati ubi jalar dengan penambahan ekstrak jahe merah. Pembuatan larutan edible mengacu pada metode Basuki., (2014) yang dimodifikasi. Pati ubi jalar dilarutkan dalam aquades dengan 100 ml, dipanaskan diatas hot plate. Larutan edible coating diaduk hingga campuran merata selama 2 menit. Gliserol 20% (b/v) ditambahkan dan larutan edible coating dipanaskan hingga suhu mencapai 80˚C kemudian didinginkan hingga suhu larutan 37˚C. Ekstrak jahe merah ditambahkan sesuai perlakuan dan jadilah larutan edible coating.
Gambar 7. Diagram Alir Pembuatan Edible Coating (Basuki., 2014) Pati Ubi Jalar Ungu
(perlakuan terbaik) Pencampuran Pemanasan (T= 80°C, t= 5 menit) Penurunan Suhu (T= 37°C) Larutan Edible Coating Aquades 100ml Gliserol 20%
Ekstrak Jahe merah (Perlakun Terbaik)
27 3.4.5 Proses Pelapisan Pada Buah Nanas (Sera, 2018)
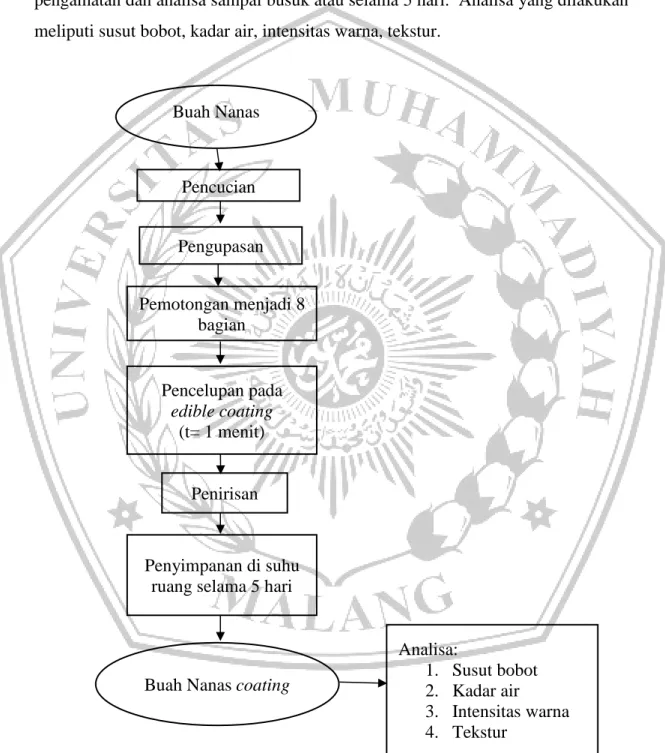
Proses pengaplikasan edible coating dengan cara memasukkan buah nanas yang sudah dipotong potong ke dalam larutan coating selama 30 detik dan dibiarkan hingga larutan edible coating pada buah nanas potong mengering. Buah nanas lalu disimpan dalam wadah berperforasi pada suhu ruang. Kemudian dilakukan pengamatan dan analisa sampai busuk atau selama 5 hari. Analisa yang dilakukan meliputi susut bobot, kadar air, intensitas warna, tekstur.
Buah Nanas
Pencelupan pada edible coating
(t= 1 menit)
Penirisan
Buah Nanas coating Penyimpanan di suhu
ruang selama 5 hari
Analisa: 1. Susut bobot 2. Kadar air 3. Intensitas warna 4. Tekstur Pencucian Pengupasan Pemotongan menjadi 8 bagian
Gambar 8. Diagram Alir Aplikasi Edibe Coating Buah Nanas (Sera,2018) Gambar 8. Diagram Alir Proses Pelapisan Pada Buah Nanas (Sera, 2018)
28 3.5 Parameter Penelitian
3.5.1 Analisa Kadar Pati Metode Hidrolisis Asam (AOAC, 2005) a. Sampel ditimbang sebesar 2-5 gram.
b. 50 ml aquades ditambahkan ke sampel dan diaduk selama 1 jam. c. Suspensi disaring menggunakan kertas saring dan dicuci memakai
aquades sampai batas tera atau sebanyak 250 ml.
d. Residu dipindahkan dari kertas saring ke dalam labu erlenmeyer , dicuci dengan 200 ml aquades dan ditambahkan 20 ml HCl 25%.
e. Labu erlenmeyer dimasukan ke pendingin balik kemudian dipanaskan sekitar 2,5 jam.
f. Didinginkan dan dinetralkan dengan NaOH 45% kemudian diencerkan hingga mempunyai volume 500 ml, kemudian disaring.
g. 1 ml filtrat akhir diambil dan dimasukkan ke dalam tabung reaksi kemudian ditambahkan 1 ml pereaksi arsenomolibdat.
h. Sampel dipanaskan pada suhu 100°C sekitar 20 menit.
i. Sampel didinginkan pada suhu kamar dan ditambahkan 1 ml pereaksi nelson dan divorteks.
j. Sampel diencerkan dengan 7 ml aquades dan divorteks.
k. Absorbansi diukur pada panjang gelombang 540 nm menggunakan spektrofotometer
l. Kadar pati dihitung menggunakan rumus: Berat pati= berat x 0,9 3.5.2 Analisa Kadar Amilosa (AOAC, 2005)
a. Pati sebanyak 100 mg ditempatkan ke dalam labu ukur 100 ml, lalu etanol 95% dan 9 ml NaOH 1N ditambahkan.
b. Larutan dipanaskan pada suhu sekitar 80-100°C selama ±10 menit hingga terjadi proses gelatinisasi.
c. Larutan didinginkan lalu diencerkan aquades hingga batas tera dengan labu takar 100 ml
d. Larutan diambil sebanyak 1 ml dan 0,1 ml iod 0,2%, 0,2 asam asetat 1N, dan 3 ml aquades ditambahkan
29 f. Absorbansi diukur pada panjang gelombang 620 nm.
3.5.3 Analisa Ketebalan Edible Film (ASTM D882-12, 2012)
1. Sampel diukur menggunakan micrometer scrup dengan ketelitian 0,01 mm
2. Pengukuran dilakukan dengan cara mengambil lima titik yang berbeda 3. Data yang diperoleh dihitung menghitung rata rata lima titik sebagai
ketebalan edible film.
3.5.4 Analisa Persen Pemanjangan Edible Film (ASTM D882-12, 2012) 1. Edible film dipotong dengan ukuran sekitar 20 mm x 50 mm
2. Persen pemanjangan edible film dianalisa menggunakan Universal Testing Machine
3. Persen pemanjangan adalah kemampuan fleksibilitas edible film yang dihasilkan. Persen pemanjangan dihitung dengan rumus sebagai berikut :
Elongasi (%) = 𝑑 𝑎𝑓𝑡𝑒𝑟−𝑑 𝑏𝑒𝑓𝑜𝑟𝑒 (𝑚𝑚)𝑑 𝑏𝑒𝑓𝑜𝑟𝑒 𝑥 100
Keterangan : d adalah antara penjepit pemegang sampel sebelum atau setelah sample ditarik hingga putus
3.5.5 Analisa Kuat Tarik Edible Film (ASTM D882-12, 2012) 1. Edible Film dipotong pada ukuran sekitar 20 mm x 50 mm
2. Kuat Tarik edible film dianalisa memakai Universal Testing Machine 3. Sampel akan dianalisa dengan memberikan beban dan gaya tarik lalu
nilai kuat tarik dihitung dengan rumus sebagai berikut :
Kuat Tarik = 𝑙𝑢𝑎𝑠 𝑝𝑒𝑛𝑎𝑚𝑝𝑎𝑛𝑔 𝑚𝑒𝑙𝑖𝑛𝑡𝑎𝑛𝑔 (𝐴)𝑡𝑒𝑔𝑎𝑛𝑔𝑎𝑛 𝑚𝑎𝑘𝑠𝑖𝑚𝑢𝑚 ( 𝐹𝑚𝑎𝑥) Keterangan :
F = Gaya Tekan (N)
A = Luas Permukaan (cm2)
3.5.6 Analisa Laju Transmisi Uap Air Edible Film (ASTM D882-12, 2012) 1. Cawan kurs yang mempunyai ukuran 30 mL atau luas penampang diisi
30 2. Bagian ujung cawan kurs ditutup dengan edible film dan ditali dengan
karet
3. Berat cawan kurs dan edible film ditimbang sebagai berat awal
4. Cawan kurs tersebut dimasukkan kedalam toples plastik yang berisi 100 mL larutan NaCl 40% (RH = 75%) pada suhu ruang dan toples ditutup dengan rapat
5. Cawan kurs ditimbang setiap hari dengan kurun waktu selama 6 hari 6. Berat cawan dari data yang dihasilkan dibuat persamaan regresi linear,
sehingga didapatkan slope kenaikan berat cawan (g/hari) dibagi dengan luas permukaan film yang diuji (m2)
7. Laju transmisi uap air dihitung memakai rumus :
Transmisi uap air = 𝑤 𝑡𝑥𝐴 Keterangaan :
w = Perubahan berat film setelah 1 minngu t = 1 minggu
A = Luas permukaan (cm2).
3.5.7 Analisa Aktivitas Antioksidan ( Hidayah,2013 )
Prinsip dari uji antioksidan metode DPPH (2,2- Diphenyl-1- Picrylhydrazyl) adalah dengan cara menghilangkan warna dan mengukur aktivitas antioksidan yang dekat dengan radikal DPPH langsung, yang ditunjukan dari pengukuran absorbansi meggunakan panjang gelombang 517 nm memakai spektrofotometer. Langkah langkah untuk analisa aktivitas antioksidan dengan metode DPPH sebagai berikut:
A. Pembuatan Larutan DPPH 0,25 mM
1. kebutuhan serbuk DPPH dihitung dengan rumus: Konsentrasi = 𝑚𝑟 𝑥 𝑉𝑜𝑙𝑢𝑚𝑒 (𝐿)𝑀𝑎𝑠𝑠𝑎 (𝑚𝑔)
2. Serbuk DPPH dilarutkan dengan methanol 70% pada labu ukur 50 mL hingga batas tera, dan dihomogenkannya.
3. Larutan DPPH disimpan pada kondisi gelap dan terutup rapat pada kondisi dingin, serta sesegera mungkin untuk digunakan.
B. Ekstraksi Bahan Aktif
31 2. Sampel ditimbang sebanyak 1 gram ke dalam tube centrifuge.
3. Larutan methanol 70% ditambahkan sebanyak 9 mL. 4. Sentrifugasi dengan kecepatan 4000 rpm selama 10 menit. 5. Supernatant dipisahkan untuk uji aktivitas antioksidan. C. Analisis Aktivitas Antioksidan
1. supernatant diambil sebanyak 1 mL kedalam tabung reaksi. 2. Ditambahkan 2 mL larutan DPPH 0,25 mM dan dihomogenkan
3. mulut tabung ditutup dengan plastic wrap, dan badan tabung dengan alumunium foil.
4. sampel disimpan pada kondisi gelap selama 30 menit.
5. Absorbansi dibaca dengan spektrofotometer UV Vis pada λ = 517 nm. 6. % inhibisi dihitung dengan rumus:
% inhibisi = 𝐴 𝑏𝑙𝑎𝑛𝑘𝑜−𝐴 𝑠𝑎𝑚𝑝𝑒𝑙 𝐴 𝑏𝑙𝑎𝑛𝑘𝑜 𝑥 100% 3.5.8 Analisa Susut Bobot (Winarsih, 2018)
1. Sampel buah yang telah dicoating pada hari yang telah ditentukan selama penyimpanan ditimbangan menggunakan timbangan analitik.
2. Berat sampel pada Hari ke-0 ditentukan sebagai berat awal.Susut bobot merupakan selisih dari berat pada sebelum perlakuan dan setelah perlakuan hari ke-n.
3. Susut bobot dihitung dengan rumus sebagai berikut Susut Bobot (%) = 𝑊𝑜−𝑊𝑡𝑊𝑜 × 100 Keterangan:
Wo = berat sampel awal (g) Wt = berat sampel akhir (g) 3.5.9 Warna (Maulida,2014)
Pengamatan intensitas warna dilakukan dengan menggunakan alat color reader. Adapun prosedurnya sebagai berikut.
1. Sampel diletakkan ke dalam wadah transparan (plastik bening). 2. Alat dihidupkan dengan menekan tombol on/off.
3. Posisi diatur hingga sensor bersentuhan dengan sampel yang hendak diukur tingkat warnanya.
32 4. Tombol target ditekan, yang akan diikuti suara beep, pertanda
pembacaan selesai dilakukan.
5. Angka L, a, dan b yang tertera pada layar monitor color reader dicatat. 6. Tombol reset ditekan untuk pengukuran sampel berikutnya.
7. Jika telah selesai alat dimatikan dengan menekan on/off.
3.5.10 Analisa Kadar Air (AOAC, 2005)
1. Sampel buah nanas dihaluskan dengan mortal martil
2. Cawan porselen kosong dikeringkan di oven selama 24 jam dan didinginkan di desikator selama 30 menit, kemudian cawan porselen kosong ditimbang.
3. Sampel buah nanas dimasukkan ke dalam cawan porselen dan ditimbang sebanyak 2 gram.
4. Cawan porselen dimasukkan ke dalam oven selama ±4 jam.
5. Cawan porselen dikeluarkan dari oven dan di dinginkan di dalam desikator selama ±15 menit.
6. Berat akhir ditimbang dan kadar air dihitung dengan rumus:
Kadar Air (%) = 𝑏𝑒𝑟𝑎𝑡 𝑠𝑒𝑡𝑒𝑙𝑎ℎ 𝑑𝑖𝑜𝑣𝑒𝑛−𝑏𝑒𝑟𝑎𝑡 𝑐𝑎𝑤𝑎𝑛
𝑏𝑒𝑟𝑎𝑡 𝑠𝑎𝑚𝑝𝑒𝑙
× 100
3.5.11 Tekstur (Winarsih.,2018)
Tekstur buah nanas yang sudah dicoating diukur memakai alat texture analyze EZ Test EZ-SX. Alat penusuk (jarum) memerlukan gaya tertentu berdasarkan tingkat kekerasan dari buah yang akan dimasukan ke dalam buah, proses pengukuran tekstur dianalisa menggunakan kecepatan 2 mm/s.