UPAYA MEMPERTAHANKAN KEEFEKTIFAN
CENDAWAN ENTOMOPATOGEN UNTUK
MENGENDALIKAN HAMA TANAMAN PANGAN
Yusmani Prayogo
Balai Penelitian Tanaman Kacang-kacangan dan Umbi-umbian, Jalan Raya Kendalpayak, Kotak Pos 66 Malang 65101
ABSTRAK
Cendawan entomopatogen merupakan salah satu jenis bioinsektisida yang dapat digunakan untuk mengendalikan hama tanaman. Beberapa jenis cendawan entomopatogen yang sudah diketahui efektif mengendalikan hama penting tanaman adalah Beauveria bassiana, Metarhizium anisopliae, Nomuraea rileyi, Paecilomyces fumosoroseus,
Aspergillus parasiticus, dan Verticillium lecanii. Namun pemanfaatan berbagai jenis cendawan tersebut sering
menghadapi kendala, antara lain kurangnya pengetahuan petani tentang jenis hama serta manfaat dan upaya mempertahankan viabilitas dan keefektifan cendawan dalam pengendalian hama, termasukcara perbanyakan, penyiapan dan aplikasinya. Pada tanaman pangan, keefektifan cendawan biasanya rendah karena tanaman pangan bersifat semusim. Upaya untuk meningkatkan keefektifan cendawan dapat dilakukan dengan: 1) melakukan identifikasi jenis hama utama yang akan dikendalikan, 2) mengaplikasikan cendawan entomopatogen pada sore hari dengan konsentrasi konidia minimal 107/ml, 3) mengulang aplikasi sebanyak tiga kali, dan 4) menambahkan
bahan perekat dan bahan pembawa pada suspensi konidia sebelum diaplikasikan pada hama sasaran.
Kata kunci: Cendawan entomopatogen, pengendalian hama, tanaman pangan,
ABSTRACT
Efforts in maintaining the effectiveness of entomopathogenic fungi to control insect pests on food crops
Entomopathogenic fungi are one of the most common bioinsecticides that can be used to control insect pests on crops. Species of fungi known to be effective as biopesticide are Beauveria bassiana, Metarhizium anisopliae,
Nomuraea rileyi, Paecilomyces fumosoroseus, Aspergillus parasiticus, and Verticillium lecanii. However, there
are several constraints in using entomopathogenic fungi as biopesticide, namely low experience of farmers in identifying main pest in the field and also effort to sustain viability and effectiveness of entomopathogenic fungi as a control agent, including mass production and application methods. In food crops, effectiveness of the entomopathogenic fungi is commonly low. Increasing the effectiveness of entomopathogenic fungi can be conducted by: 1) identifying the targeted pest in the field before application, 2) applying the entomopathogenic fungi in the afternoon at least 107/ml, 3) applying the bioinsecticide three times, and 4) adding sticker and carrier or mild
surfactant to the conidia suspension before it is applied to control the insect pests.
Keywords: Entomopathogenic fungi, pest control, food crops
B
ioinsektisida adalah mikroorganisme
yang dapat digunakan sebagai agen
pengendalian serangga hama.
Peman-faatan bioinsektisida sebagai agen hayati
pada pengendalian hama merupakan salah
satu komponen pengendalian hama
terpadu (PHT). Terdapat enam kelompok
mikroorganisme yang dapat dimanfaatkan
sebagai bioinsektisida, yaitu cendawan,
bakteri, virus, nematoda, protozoa, dan
ricketsia (Santoso 1993; Tanada dan
Kaya 1993). Empat kelompok pertama
merupakan jenis yang sering digunakan
dan mempunyai prospek yang baik untuk
dikembangkan (Kaaya et al. 1996;
Reithinger et al. 1997; Sosa-Gomez dan
Moscardi 1997; Kim et al. 2001; Prayogo
et al. 2004).
Di Indonesia, pemanfaatan agen
hayati khususnya cendawan
entomo-patogen untuk pengendalian hama mulai
berkembang pesat sejak abad ke-19
khususnya untuk mengendalikan hama
pada tanaman perkebunan (Sudarmadji
dan Gunawan 1994; Junianto 2000). Pada
tanaman pangan, pemanfaatan cendawan
entomopatogen untuk pengendalian hama
masih menemui berbagai kendala, antara
lain kondisi lingkungan mikro yang kurang
kondusif bagi perkembangbiakan
mikro-organisme tersebut (Steinkraus dan
Slaymaker 1994; Glare et al. 1995; Lacey
dan Goettel 1995; Oduor et al. 1996). Hal
ini karena tanaman pangan bersifat
semusim, sehingga apabila tanaman
tersebut dipanen kemudian diganti
dengan jenis tanaman lain maka inokulum
cendawan sebagai sumber infeksi awal di
lapangan sulit untuk bertahan hidup dan
berkembang (Hajek et al. 1990; Farques et
al. 1997; Thomas dan Jenkins 1997). Hal
ini berbeda dengan tanaman perkebunan.
Biasanya tanaman yang dibudidayakan
hanya satu jenis dan bersifat tahunan,
sehingga cendawan entomopatogen yang
diaplikasikan mudah menyesuaikan diri
dan berkembang sesuai dengan kondisi
lingkungan setempat.
Kendala lainnya adalah jika tanaman
yang dibudidayakan beragam bahkan
berganti hampir setiap musim maka jenis
hama yang menyerang juga
berbeda-beda. Jenis hama yang menyerang
tanaman akan menentukan keefektifan
cendawan entomopatogen karena setiap
jenis cendawan entomopatogen
mem-punyai inang yang spesifik, walaupun ada
pula yang mempunyai kisaran inang
cukup luas (Santoso 1993; Suryawan dan
Carner 1993; Prayogo et al. 2002a;
Prayogo 2004). Jenis inang setiap jenis
cendawan entomopatogen biasanya
be-lum dipahami oleh petani.
Keefektifan cendawan
entomo-patogen di lapangan juga ditentukan oleh
stadia inang pada saat cendawan
diapli-kasikan. Biasanya populasi hama di
lapangan sering tumpang tindih, terutama
hama dari ordo Lepidoptera dan
Hemip-tera. Perubahan stadia instar (nimfa)
serangga akan mempengaruhi perilaku
serangga tersebut yang akhirnya akan
menentukan keefektifan cendawan.
Keefektifan cendawan
entomopato-gen juga ditentukan oleh kondisi
ling-kungan, seperti curah hujan dan sinar
matahari khususnya sinar ultra violet
yang dapat merusak konidia cendawan
(Tanada dan Kaya 1993; Wahyunendo
2002; Prayogo 2004; Suharsono dan
Prayogo 2005). Konidia merupakan salah
satu organ infektif (propagule) cendawan
yang menyebabkan infeksi pada
inte-gumen serangga yang diakhiri dengan
kematian. Oleh karena itu, konidia
cen-dawan tersebut perlu dilindungi waktu
diaplikasikan, baik dengan bahan perekat
maupun bahan pembawa sehingga
peng-aruh buruk tersebut dapat dieliminir.
Tulisan ini menyajikan berbagai faktor
yang mempengaruhi keefektifan
cen-dawan entomopatogen dan upaya untuk
meningkatkan keefektifannya dalam
pengendalian hama, terutama pada
tanaman pangan.
JENIS HAMA SASARAN
Salah satu kelemahan petani dalam
pe-ngendalian hama adalah kurangnya
pema-haman tentang jenis hama yang akan
dikendalikan sehingga akan menentukan
keberhasilan usaha pengendalian. Dalam
konsep PHT, identifikasi jenis hama
merupakan salah satu tindakan pertama
yang harus dilakukan petani sebelum
mengambil keputusan tindakan
pengen-dalian (Rauf 1996). Melalui identifikasi
akan diketahui jenis hama sasaran, perilaku
hama, tindakan pengendalian yang
di-perlukan, dan kapan tindakan
pengenda-lian perlu dilakukan.
Dengan mengetahui hama yang
me-nyerang tanaman, secara tidak langsung
dapat diketahui pula jenis cendawan
ento-mopatogen yang sesuai untuk tindakan
pengendalian, karena setiap jenis
cen-dawan entomopatogen mempunyai inang
yang spesifik. Cendawan Metarhizium
anisopliae, misalnya, diketahui dapat
menginfeksi beberapa jenis serangga dari
ordo Coleoptera, Lepidoptera, Homoptera,
Hemiptera, dan Isoptera. (Lee dan Hou
1989; Romero et al. 1997; Luz et al. 1998;
Kanga et al. 2003; Strack 2003). Namun
M. anisopliae paling efektif bila
digu-nakan untuk mengendalikan hama dari
ordo Isoptera (Strack 2003). Hal ini karena
adanya hubungan perilaku antara
serang-ga inang denserang-gan keefektifan cendawan
entomopatogen. Fenomena tersebut
ditunjukkan oleh hasil uji infeksi ulang.
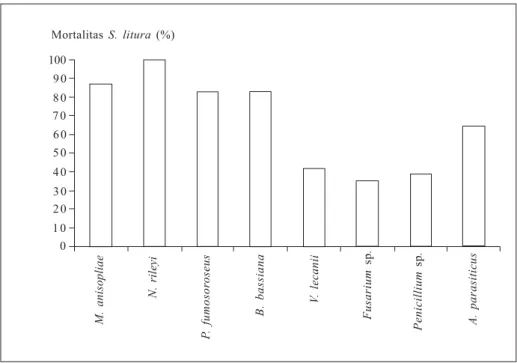
Dari beberapa jenis cendawan
entomo-patogen yang diperoleh dari ulat grayak
Spodoptera litura dan Helicoverpa
armigera, cendawan Nomuraea rileyi
paling efektif mengendalikan S. litura
dengan mortalitas mencapai 100%
(Pra-yogo et al. 2002a; Gambar 1). Cendawan
tersebut dilaporkan merupakan salah satu
agen hayati yang potensial untuk
mengen-dalikan hama dari ordo Lepidoptera,
walau-pun juga mampu menginfeksi serangga
dari ordo lain (Ignofo 1981; Suryawan dan
Carner 1993).
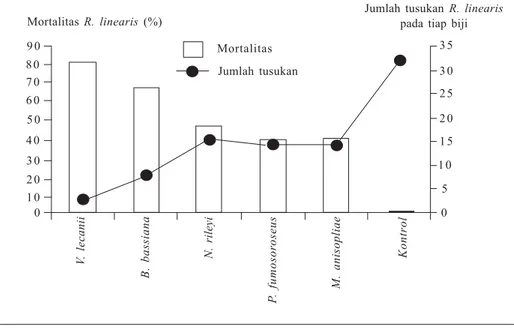
Fakta lain menunjukkan bahwa
cendawan Verticillium lecanii yang
diisolasi dari walang sangit (Leptocoriza
acuta) efektif terhadap hama pengisap
polong kedelai Riptortus linearis
(Pra-yogo 2004) dengan menyebabkan
morta-litas yang cukup tinggi dan biji yang rusak
relatif rendah (Gambar 2). Cendawan V.
lecanii juga dapat mengkolonisasi telur
R. linearis sehingga banyak telur yang
tidak menetas (Gambar 3) (Prayogo 2004;
Prayogo et al. 2004).
Cendawan B. bassiana juga mampu
menginfeksi beberapa jenis serangga
hama, terutama dari ordo Lepidoptera,
Hemiptera, Homoptera, dan Coleoptera
(Varela dan Morales 1996; Hardaningsih
dan Prayogo 2001; Prayogo et al. 2002b).
Namun, cendawan tersebut lebih efektif
mengendalikan hama dari ordo Coleoptera
(Varela dan Morales 1996).
0 1 0 2 0 3 0 4 0 5 0 6 0 7 0 8 0 9 0 100 M. anisopliae N. rileyi P. fumosor oseus B. bassiana V. lecanii Fusarium sp . Penicillium sp . A. parasiticus Mortalitas S. litura (%)
Gambar 1.
Mortalitas ulat grayak (Spodoptera litura) akibat aplikasi beberapa
jenis cendawan entomopatogen (Prayogo et al. 2002a).
WAKTU APLIKASI
Keefektifan cendawan entomopatogen
dipengaruhi oleh waktu aplikasi. Setelah
diaplikasikan, cendawan entomopatogen
memerlukan kelembapan yang tinggi untuk
tumbuh dan berkembang (Lacey dan
Goettel 1995; Mazet et al. 1996).
Kelem-bapan udara yang tinggi diperlukan
selama proses pembentukan tabung
kecambah (germ tube), sebelum terjadi
penetrasi ke integumen serangga
(Stein-kraus dan Slaymaker 1994; Arthurs dan
Thomas 2001). Kelembapan di atas 90%
selama 6−12 jam setelah inokulasi
dibu-tuhkan cendawan untuk melakukan
pene-trasi ke dalam tubuh serangga (Hoddle
1999; Altre dan Vandenberg 2001a; Cloyd
2003).
Waktu aplikasi perlu diperhatikan
karena cendawan entomopatogen sangat
rentan terhadap sinar matahari khususnya
sinar ultra violet (Altre dan Vandenberg
2001b; Cloyd 2003). Bila terkena sinar
matahari dalam waktu 4 jam, cendawan V.
lecanii akan kehilangan viabilitas sebesar
16% (Suharsono dan Prayogo 2005), dan
bila terkena sinar matahari 8 jam, viabilitas
berkurang hingga di atas 50%. Oleh
karena itu, bila cendawan diaplikasikan
pada musim kemarau perlu dihindarkan dari
sinar matahari langsung dan sebaiknya
aplikasi dilakukan pada saat kelembapan
udara tinggi (sore hari). Keberhasilan
aplikasi cendawan entomopatogen pada
musim hujan belum pernah dilaporkan.
Aplikasi V. lecanii pada sore hari
(setelah pukul 16.00) mampu
menyebab-kan kematian hama pengisap polong
kedelai R. linearis hingga 80%. Makin
tinggi mortalitas serangga, jumlah biji yang
rusak pun makin menurun (Prayogo dan
Tengkano 2004b). Penurunan kerusakan
biji tampak pada jumlah tusukan stilet R.
linearis yang hanya 3 tusukan tiap biji
bila cendawan entomopatogen
diapli-kasikan pada sore hari, dan meningkat
menjadi 4,70−6,30 tusukan tiap biji bila
aplikasi dilakukan pada pagi hingga siang
hari (Gambar 4).
KONSENTRASI APLIKASI
Keberhasilan pengendalian hama dengan
cendawan entomopatogen juga
diten-tukan oleh konsentrasi cendawan yang
diaplikasikan (Hall 1980), yaitu kerapatan
konidia dalam setiap mililiter air. Jumlah
konidia berkaitan dengan banyaknya
biakan cendawan yang dibutuhkan setiap
hektar. Kerapatan konidia yang
dibutuh-kan untuk mengendalidibutuh-kan hama
bergan-tung pada jenis dan populasi hama yang
akan dikendalikan (Tohidin et al. 1993;
Wikardi 1993).
Pada tanaman pangan, kerapatan
konidia yang dibutuhkan lebih tinggi
dibandingkan dengan pada tanaman
perkebunan. Untuk mengendalikan hama
wereng coklat, dibutuhkan kerapatan
konidia cendawan M. anisopliae 10
15/ml
(Baehaki dan Noviyanti 1993; Tabel 1).
Sementara itu untuk mengendalikan hama
ulat daun kelapa sawit (Darna catenata)
hanya dibutuhkan kerapatan konidia B.
0 1 0 2 0 3 0 4 0 5 0 6 0 7 0 8 0 9 0 0 5 1 0 1 5 2 0 2 5 3 0 3 5 V. lecanii B. bassiana N. rileyi P. fumosor oseus M. anisopliae Kontrol Mortalitas R. linearis (%) Mortalitas Jumlah tusukanJumlah tusukan R. linearis pada tiap biji
Gambar 2.
Mortalitas Riptortus linearis dan jumlah tusukan pada biji kedelai
pada aplikasi beberapa jenis cendawan entomopatogen (Prayogo
2004).
Gambar 3.
Telur Riptortus linearis yang terkolonisasi cendawan entomopatogen V.
lecanii (kiri) dan kelompok telur R. linearis yang tidak menetas akibat
terinfeksi V. lecanii (kanan) (Prayogo 2004).
Gambar 4.
Jumlah tusukan R. linearis
pada biji kedelai
ber-dasarkan waktu
apli-kasi cendawan V. lecanii
(Prayogo dan Tengkano
2004b).
123 123 123 123 123 123 123 123 123 12345 12345 12345 12345 12345 12345 12345 12345 12345 12345 12345 12345 12345 12345 0 1 2 3 4 5 6 7 07.00 10.00 13.00 16.00 Jumlah tusukan tiap bijibassiana 39,90 x 10
6/ml untuk mencapai
mortalitas 100% (Daud et al. 1993). Hal ini
karena tanaman pangan bersifat semusim,
sehingga sekali aplikasi cendawan harus
mampu menginfeksi dan mengkolonisasi
serangga hama sasaran. Oleh karena itu,
kerapatan konidia yang dibutuhkan lebih
tinggi.
Konsentrasi cendawan
entomopato-gen harus ditentukan secara tepat untuk
mendapatkan hasil pengendalian yang
optimal. Kerapatan konidia M. anisopliae
yang tepat
untuk mengendalikan ulat
grayak (S. litura)
adalah 10
7/ml (Prayogo
dan Tengkano 2004a) (Tabel 2).
Untuk
mengendalikan hama walang sangit (L.
acuta) pada tanaman padi dibutuhkan
kerapatan konidia cendawan B. bassiana
10
7/ml (Tohidin et al. 1993). Kerapatan
konidia B. bassiana 10
7/ml juga efektif
untuk mengendalikan hama penggerek
buah kopi (Hypothenemus hampei), yang
setara dengan biakan cendawan 1 kg/ha
(Haryanta et al. 1993). Untuk tanaman
pangan, dosis yang diperlukan dua kali
lebih banyak, yaitu 2 kg/ha untuk
mem-peroleh hasil yang optimal.
FREKUENSI APLIKASI
Keefektifan cendawan entomopatogen
dalam pengendalian hama juga
ditentu-kan oleh frekuensi aplikasi. Hal ini karena
konidia yang diaplikasikan pada tahap
awal (yang belum mampu menginfeksi
hama sasaran) perlu digantikan oleh
konidia yang diaplikasikan pada tahap
selanjutnya. Frekuensi aplikasi
dipenga-ruhi oleh kondisi cuaca, seperti curah
Tabel 1. Mortalitas imago wereng
coklat pada beberapa
ke-rapatan konidia
Metar-hizium anisopliae.
Kerapatan konidia Mortalitas wereng
co-M. anisopliae klat pada n MSA (%)
1 2 3
0 9,30 13,30 13,30
105 15,30 27,30 27,30
1010 36,70 54,70 55,30
1015 39,30 61,70 63
MSA = minggu setelah aplikasi. Sumber: Baehaki dan Noviyanti (1993).
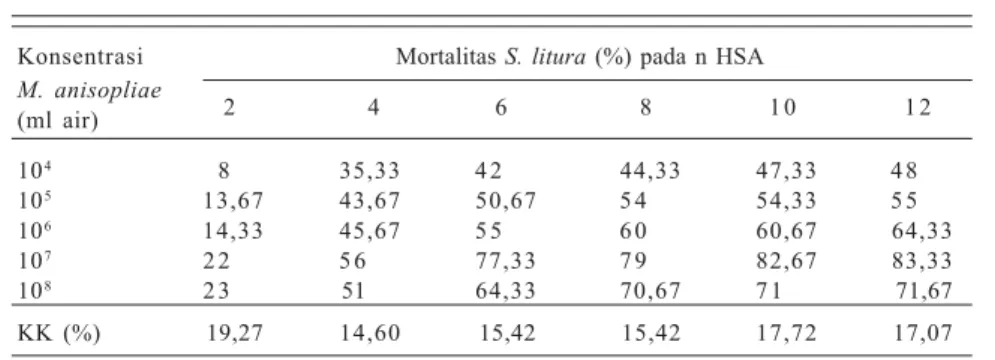
Tabel 2. Kematian larva Spodoptera litura instar 2 pada aplikasi beberapa
konsentrasi konidia M. anisopliae.
Konsentrasi Mortalitas S. litura (%) pada n HSA
M. anisopliae 2 4 6 8 1 0 1 2 (ml air) 104 8 35,33 4 2 44,33 47,33 4 8 105 13,67 43,67 50,67 5 4 54,33 5 5 106 14,33 45,67 5 5 6 0 60,67 64,33 107 2 2 5 6 77,33 7 9 82,67 83,33 108 2 3 51 64,33 70,67 7 1 71,67 KK (%) 19,27 14,60 15,42 15,42 17,72 17,07 HSA = hari setelah aplikasi.
Sumber: Prayogo dan Tengkano (2004a).
1234 1234 1234 1234 1234 1234 1234 1234 1234 1234 1234 1234 1234 1234 1234 1234 1234 1234 1234 1234 1234 1234 1234 1234 1234 1234 1234 1234 1234 1234 1234 1234 1234 1234 1234 1234 1234 1234 1234 1234 1234 1234 1234 0 1 0 2 0 3 0 4 0 5 0 6 0 7 0 8 0 9 0 100
1x aplikasi 2x aplikasi 3x aplikasi Mortalitas S. litura (%) 123 123 123 3 HSA 8 HSA 12 HSA
Gambar 5.
Mortalitas Spodoptera litura pada berbagai waktu dan frekuensi aplikasi
cendawan M. anisopliae (Prayogo dan Tengkano 2004a).
hujan, angin, dan sinar matahari. Aplikasi
juga perlu memperhatikan stadia serangga
hama di lapangan yang saling tumpang
tindih (tidak seragam). Perubahan stadia
instar (nimfa) akan mengakibatkan
peru-bahan perilaku serangga yang akhirnya
berpengaruh pada frekuensi aplikasi.
F
rekuensi aplikasi
perlu diketahui
dengan tepat agar populasi hama di bawah
nilai ambang kendali. Aplikasi M.
ani-sopliae tiga kali berturut-turut selama 3
hari lebih efektif mengendalikan S. litura
hingga menyebabkan kematian 86%,
dibandingkan dengan aplikasi satu kali
yang hanya menimbulkan kematian 40%
(Gambar 5; Prayogo dan Tengkano 2004a).
Bahkan untuk mengendalikan ulat jengkal
(E. bhurmitra) pada tanaman teh
diper-lukan aplikasi cendawan B. bassiana atau
P. fumosoroseus hingga empat kali
(Widayat dan Rayati 1993a; 1993b). Di
daerah dengan curah hujan tinggi
di-anjurkan melakukan aplikasi berulang
kali untuk menghindari kegagalan konidia
dalam menginfeksi serangga (Hoddle
1999; Cloyd 2003).
PENAMBAHAN PEREKAT
Keberhasilan konidia cendawan
entomo-patogen menempel pada integumen
serangga akan menentukan proses infeksi
lebih lanjut yaitu proliferasi dalam organ
yang diakhiri dengan kematian serangga.
Proses infeksi dapat mengalami kegagalan
baik karena faktor internal (viabilitas
cendawan entomopatogen) maupun
faktor eksternal seperti perubahan stadia
instar (nimfa) dan lingkungan (angin, sinar
matahari, dan hujan).
Salah satu upaya untuk menjamin
keberhasilan proses inokulasi adalah
dengan menggunakan bahan perekat
untuk meningkatkan daya rekat konidia
pada integumen serangga (Devi dan
Prasad 1988; Widayat dan Rayati 1993b;
Leland 2001a; 2001b). Dengan cara
demikian, konidia langsung dapat
me-nempel pada integumen serangga serta
melakukan infeksi lebih lanjut.
Penambahan bahan perekat alkil
gliserol ftalat 1 ml/l ke dalam suspensi V.
lecanii sebelum aplikasi mampu
mening-katkan keefektifan cendawan
entomo-patogen hingga 20% dibanding kontrol
(Prayogo dan Tengkano 2004b).
Keefek-tifan cendawan terlihat dari menurunnya
biji yang rusak akibat tusukan stilet hama
pengisap polong R. linearis hingga 43%
(Prayogo dan Tengkano 2004b). Bahan
perekat lainnya, yaitu alkilaril poliglikol
eter juga mampu menekan kerusakan biji
kedelai, dan keefektifan V. lecanii lebih
tinggi dibandingkan dengan penambahan
alkil gliserol ftalat (Gambar 6).
Penambahan perekat ke dalam
sus-pensi cendawan entomopatogen
dianjur-kan dilakudianjur-kan sebelum aplikasi, terutama
untuk mengendalikan hama yang
meng-alami pergantian kulit beberapa kali. Bila
cendawan diaplikasikan saat serangga
berganti kulit maka konidia cendawan
yang diaplikasikan tidak mampu
meng-infeksi integumen serangga karena ikut
terlepas sewaktu serangga mengalami
ganti kulit (Widayat dan Rayati 1993a;
Prayogo dan Tengkano 2002b).
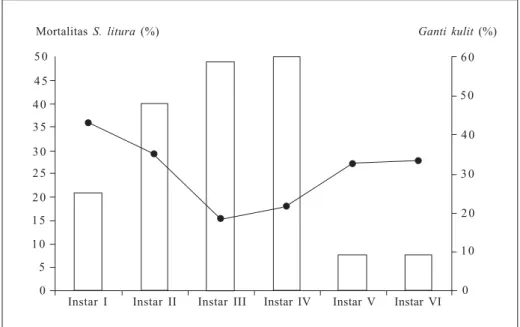
Ulat grayak selama stadia larva
akan mengalami ganti kulit enam kali.
Pergantian kulit yang paling tinggi terjadi
pada larva instar III dan IV yang hampir
mencapai 50% (Gambar 7). Hasil aplikasi
cendawan M. anisopliae pada stadia
instar tersebut menyebabkan mortalitas
lebih rendah yaitu kurang dari 20%
dibandingkan pada instar lainnya.
Sebaliknya instar I, II, V, dan VI mengalami
ganti kulit lebih rendah sehingga aplikasi
cendawan lebih efektif (Prayogo dan
Tengkano 2002b). Hal ini karena selain
ditentukan oleh pergantian kulit, perilaku
serangga juga mempengaruhi keefektifan
cendawan entomopatogen (Widayat dan
Rayati 1993b).
PENAMBAHAN BAHAN
PEMBAWA
Tidak semua konidia cendawan
entomo-patogen yang diaplikasikan berhasil
mencapai sasaran karena mobilitas
se-rangga yang tinggi terutama hama dari
ordo Homoptera dan Hemiptera, cara
aplikasi yang tidak benar, serta adanya
proses ganti kulit pada serangga. Salah
satu upaya untuk mengatasi masalah
tersebut adalah dengan menambahkan
bahan pembawa (carrier) sebagai
ma-kanan cadangan (starter) bagi konidia
sebelum berhasil menginfeksi serangga.
Dengan demikian, konidia yang gagal
menginfeksi serangga masih dapat
bertahan dengan makanan cadangan.
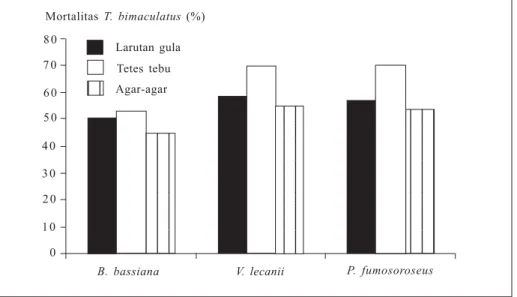
Penambahan bahan pembawa berupa
tetes tebu sebanyak 10 ml/1.000 ml air pada
suspensi konidia cendawan B. bassiana,
V. lecanii, dan P. fumosoroseus mampu
meningkatkan mortalitas hama tungau
merah pada ubi kayu (Gambar 8).
Ke-efektifan cendawan terlihat dari
pening-katan mortalitas tungau merah hingga
mencapai 17%. Bahan pembawa tetes tebu
lebih efektif dibandingkan dengan larutan
gula dan agar-agar, baik pada B. bassiana,
V. lecanii maupun P. fumosoroseus
(Prayogo dan Indiati 2004). Hal ini diduga
karena tetes tebu masih banyak
mengan-dung berbagai unsur nutrisi, terutama gula
dan protein yang sangat diperlukan
cendawan untuk pertumbuhan dan
pembentukan spora (Prayogo dan
Teng-kano 2002a; Mello-Pererira dan daEira
2003; Yuliatin 2004). Sebelum menemukan
hama inang, cendawan entomopatogen
memerlukan lingkungan yang sesuai
seperti tersedianya nutrisi yang cukup
agar viabilitas konidia tetap tinggi dan
konidia tidak mengalami kekeringan
(desiccation) bahkan kematian sebelum
proses infeksi. Viabilitas yang tinggi
123 123 123 123 123 123 123 123 0 1 2 3 4 5 6 7 Alkil gliserol ftalat Alkilaril poliglikol eter Kontrol
Jumlah tusukan R. linearis pada tiap biji
Jenis bahan perekat
Gambar 6.
Kerusakan biji kedelai
pada aplikasi V. lecanii
de-ngan berbagai bahan
perekat (Prayogo dan
Tengkano 2004b).
0 5 1 0 1 5 2 0 2 5 3 0 3 5 4 0 4 5 5 0 Mortalitas S. litura (%) 0 1 0 2 0 3 0 4 0 5 0 6 0Instar I Instar II Instar III Instar IV Instar V Instar VI
Ganti kulit (%)
Gambar 7.
Hubungan antara instar Spodoptera litura dengan mortalitas dan ganti
kulit (Prayogo dan Tengkano 2002b).
DAFTAR PUSTAKA
Altre, J.A. and J.D. Vandenberg. 2001a. Pene-tration of cuticle and proliferation in himolymph by Paecilomyces fumosoroseus isolates that differ in virulence against lepidopteran larvae. J. Invertebr. Pathol. (78): 78−85.
Altre, J.A. and J.D. Vandenberg. 2001b. Factors influencing the infectivity of isolates of
Paecilomyces fumosoroseus against
dia-mondback moth Plutella xylostella. J. Invertebr. Pathol. (78): 31−36.
Arthurs, S. and M.B. Thomas. 2001. Effects of temperature and relative humidity on speculation of Metarhizium anisopliae var.
acridum in mycosed cadavers of Schis-tocerca gregaria. J. Invertebr. Pathol. (78):
59−65.
Baehaki, S.E. dan Noviyanti. 1993. Pengaruh umur biakan Metarhizium anisopliae strain lokal Sukamandi terhadap perkembangan wereng coklat. hlm. 113−124. Dalam E. Martono, E. Mahrub, N.S. Putra, dan Y. Trisetyawati (Ed.). Prosiding Simposium Patologi Serangga I. Yogyakarta, 12−13 Oktober 1993. Universitas Gadjah Mada, Yogyakarta. 1234 1234 1234 1234 1234 1234 1234 1234 1234 1234 1234 1234 1234 1234 1234 1234 1234 1234 1234 1234 1234 1234 1234 1234 1234 1234 123 123 123 123 123 123 123 123 123 123 123 123 123 123 0 1 0 2 0 3 0 4 0 5 0 6 0 7 0 8 0
B. bassiana V. lecanii P. fumosoroseus
Mortalitas T. bimaculatus (%) 12 12 Larutan gula Tetes tebu Agar-agar
Gambar 8.
Mortalitas hama tungau merah akibat aplikasi cendawan
entomo-patogen dengan berbagai bahan pembawa (Prayogo dan Indiati 2004).
sangat menentukan keefektifan cendawan
entomopatogen (James dan Jaronski 2000;
James 2001; Prayogo dan Tengkano
2002a; Suharsono dan Prayogo 2005).
KESIMPULAN
Keefektifan cendawan entomopatogen
untuk pengendalian hama tanaman
pangan dapat ditingkatkan melalui
berbagai upaya, antara lain: 1)
mengeta-hui jenis hama yang akan dikendalikan, 2)
melakukan aplikasi pada sore hari dengan
dosis aplikasi 1−2 kg biakan cendawan tiap
hektar dengan kerapatan konidia minimal
10
7/ml, 3) melakukan aplikasi tiga kali
berturut-turut selama 3 hari, dan 4)
menambahkan perekat alkil gliserol ftalat
dan bahan pembawa berupa tetes tebu
pada suspensi konidia sebelum
diapli-kasikan pada hama sasaran.
UCAPAN TERIMA KASIH
Penulis mengucapkan terima kasih
kepada Ketua Kelompok Peneliti Proteksi
Tanaman Balai Penelitian Tanaman
Kacang-kacangan dan Umbi-umbian
(Balitkabi), Dr. Ir. Suharsono, MS., Kepala
Balitkabi Prof. (Riset) Dr. Subandi, Ketua
PEKI Prof. (Riset) Dr. Titis Adisarwanto,
dan Prof. (Riset) Dr. Nasir Saleh atas saran
dan koreksi terhadap naskah ini.
Cloyd, R. 2003. The entomopathogen
Verti-cillium lecanii. Midwest Biological Control
News. University of Illions. http://www. extension.umn.Edu/distribution/horticulture/ DG7373.html [22 April 2005].
Daud, I.D., A. Papulung, dan Mery. 1993. Efektivitas lima konsentrasi suspensi spora
Beauveria bassiana Vuill. terhadap
mor-talitas tiga instar larva Darna catenata Snellen (Lepidoptera: Limacodidae). hlm. 125−134. Dalam E. Martono, E. Mahrub, N.S. Putra, dan Y. Trisetyawati (Ed.). Prosiding Simposium Patologi Serangga I. Yogyakarta, 12−13 Oktober 1993. Univer-sitas Gadjah Mada, Yogyakarta.
Devi, P.S.V. and Y.G. Prasad. 1988. Com-patibility of soil and atifeedants of plant origin with the entomopathogenic fungus
Nomuraea rileyi. J. Invertebr. Pathol. (68):
91−93.
Farques, J., A. Ouedraogo, M.S. Goettel, and C.J. Lomer. 1997. Effect of temperature, humidi-ty, and inoculation method on susceptibility of Schistocera gregaria to Metarhizium
flavoviridae. Biocontrol Sci. Technol. (7):
345−356.
Glare, T.R., R.J. Townsend, and S.D. Young. 1995. Temperature limitations on field effectiveness of Metarhizium anisopliae against Costelytra zealandica (White) (Coleoptera:Scarabidae) in Canterbury. The New Zealand Plat Protection Society Incor-porated. http://www.hornet.co.nz/publica-tions/nzpps/proceeding/94/94 266.htm [20 December 2003].
Hajek, A.E., R.I. Carruthers, and R.S. Soper. 1990. Temperature and moisture relations of sporulation and germination by
phaga maimaiga (Zygomycetes:
Entomo-phthoraceae), a fungal pathogen of
Lyman-tria dispar (Lepidoptera: Lymantriidae).
Environ. Entomol. (19): 85−90.
Hall, R.A. 1980. Control of aphids by the fungus,
Verticillium lecanii: Effect of spore
con-centration. Entomol. Experiment. App. (27): 1−5.
Hardaningsih, S. dan Y. Prayogo. 2001. Iden-tifikasi dan patogenisitas jamur entomopa-togen untuk mengendalikan hama pengisap polong (Riptortus linearis) dan hama boleng (Cylas formicarius). hlm. 145−150. Dalam B. Praswanto, H. Semangun, N. Widijawati,
D. Rahardjo, A. Prasetyaningsih, dan C. Amarantini (Ed.). Prosiding Lokakarya Nasional Strategi Pengelolaan Sumber Daya Alam Hayati dalam Era Otonomi Daerah. Yogyakarta, 8−9 Juni 2001. Universitas Kristen Duta Wacana, Yogyakarta. Haryanta, D., A. Susilo, dan H. Prasetyono.
1993. Pengaruh dosis dan waktu aplikasi cendawan Beauveria bassiana terhadap efektivitas pengendalian bubuk buah kopi (Hypothenemus hampei). hlm. 249−254.
Dalam E. Martono, E. Mahrub, N.S. Putra,
dan Y. Trisetyawati (Ed.). Prosiding Sim-posium Patologi Serangga I. Yogyakarta, 12−
13 Oktober 1993. Universitas Gadjah Mada, Yogyakarta.
Hoddle, M.S. 1999. The biology and manage-ment of silverleaf whitefly Bemisia
argenti-folii Bellows and Perring (Homoptera:
Aleyrodidae) on greenhouse grown ornamen-t a l s . h ornamen-t ornamen-t p : / / w w w. b i o c o n ornamen-t r o l . u c r. e d u / bemisia.html# verticillium [5 April 2005]. Ignofo, C.M. 1981. The fungus Nomuraea rileyi
as a microbial insecticide. In Microbial Con-trol of Pests and Diseases 1970−1980. Aca-demic Press, London. p. 513−538. James, R.R. and S. Jaronski. 2000. Effect of low
viability on infectivity of Beauveria
bassi-ana conidia toward the silverleaf whitefly.
J. Invertebr. Pathol. (76): 227−228. James, R.R. 2001. Effect of exogeneous nutrients
on conidial germination and virulence against the silverlef whitefly for two hyphomycetes. J. Invertebr. Pathol. (77): 99−107. Junianto, Y.D. 2000. Penggunaan Beauveria
bassiana untuk pengendalian hama tanaman
kopi dan kakao. Workshop Nasional Pengen-dalian Hayati OPT Tanaman Perkebunan, Cipayung, 15−17 Februari 2000. Balai Penelitian Kopi dan Kakao, Jember. 15 hlm. Kanga, L.B.B., W.A. Jones, and R.R. James. 2003. Field trials using fungal pathogen,
Metarhi-zium anisopliae (Deuteromycetes:
Hypho-mycetes) to control the ectoparasitic mite
Varroa destructor (Acari: Varroidae) in honey
bee Aphis mellifera (Hymenoptera: Api-didae) colonies. J. Environ. Entomol. (96): 1.091−1.099. http://www.bioone.org/bioone/ r e q u e s t = g e t - a b s t r a c t & i s s n =00220493&volume=0964issue=048& page=1.091.htm [20 December 2003]. Kaaya, G.P., E.N. Mwangi, and E.A. Ouna. 1996.
Prospects for biological control of livestock ticks Rhipicephalus appendiculatus and
Amblyomma variegatum using the
entomo-genous fungi Beauveria bassiana and
Metarhizium anisopliae. J. Invertebr. Pathol.
(67): 15−20.
Kim, J.J., M.H. Lee, C.S. Yoon, H.S. Kim, and J.K. You. 2001. Control of cotton aphid and greenhouse whitefly with a fungal patho-gen. Food & Fertilizer Technology Center, An international information center for farmers in the Asia Pacific Region. http:// www.agnet.org/library/article/eb502.htm [27 March 2004].
Lacey, L.A. and M.S. Goettel. 1995. Current developments in microbial control of insect pests and prospects for the early 21st
cen-tury. Entomophaga (40): 3−27.
Leland, J.E. 2001a. Enviromental-stress tolerant formulations of Metarhizium anisopliae var.
Acridum for control of African Desert
Lo-cust (Schistocerca gregaria). Dissertation. Faculty of Virginia Polytechnic. http:// s c h o l a r. l i b . v t . e d u / t h e s e s / a v a i l a b l e / etd_12052001_115455/unrestrictited/ JlelandDisertation. PDF [21 July 2005]. Leland, J.E. 2001b. Coating Metarhizium
anisopliae var Acridum with water soluble
lignins for enhanced UVB-protection and effects on virulence to Schistocerca
Americana (Drary). Virginia: Department
of Entomology. http://essa.confex.com/esa/ 2001/echprogram/paper3552.htm [21 July 2005].
Lee, P.C. and R. Hou. 1989. Pathogenesis of
Metarhizium anisopliae var. anisopliae in
the smaller brown planthopper, laodelphax striatellus. Chinese J. Entomol. (9): 13−19. http://www.entsoc.org.tw/english/journal/ 9vol/nol/2.htm. [20 December 2003]. Luz, C., M.S. Tigano, I.G. Silva, C.M.T. Cordeiro,
and S.M. Aljanabi. 1998. Selection of
Beauveria bassiana and Metarhizium anisopliae isolates to control Triatoma infestans. Memorias do instituto Oswaldo
Cruz (93): 839−846 [serial online] http:// memorias.ioc.fiocruz.br/936/3556.html. [20 December 2003].
Mazet, I., J.C. Pendland, and D.G. Boucias. 1996. Dependence of Verticillium lecanii (Fungi:Hypomycetes) on high humidity for infection and sporulation using Myzus
persicae (Homoptera:Aphididae) as host.
Environ. Entomol. (15): 380−382. Mello-Pererira, S.R. and A.F. daEira. 2003.
Methodology for production of Metarhizium
anisopliae (Metsch.) Sorokin in submerged
cultivation: biomass sporulation, sugar concentration effect and inoculation cost. http://www.ufsm.br/ccr/revista/resumes/ rv293/eng/rvi293_1001.html [20 April 2005].
Oduor, G.I., G.J. de-Morales, L.P.S. vander Geest, and J.S. Yaninek. 1996. Production and germination of primary conidia of Neozygites
floridana (Zygomycetes: Entomophthorales)
under constant temperatures, humidities, and photoperiods. J. Invertebr. Pathol. (68): 213−222.
Prayogo, Y. dan W. Tengkano. 2002a. Pengaruh media tumbuh terhadap daya berkecambah, sporulasi, dan virulensi Metarhizium
ani-sopliae (Metchnikoff) Sorokin isolat
Ken-dalpayak pada larva Spodoptera litura. Jurnal Ilmiah Sainteks IX(4): 233−241. Prayogo, Y. dan W. Tengkano. 2002b. Pengaruh
umur larva Spodoptera litura terhadap efektivitas Metarhizium anisopliae isolat Kendalpayak. Majalah Ilmiah Biologi Biosfera 3(19): 70−76.
Prayogo, Y., W. Tengkano, dan Suharsono. 2002a. Jamur entomopatogen pada
Spodop-tera litura dan Helicoverpa armigera.
Seminar Hasil Penelitian Tanaman Kacang-kacangan dan Umbi-umbian. Malang, 25−
26 Juni 2002. Balai Penelitian Tanaman Kacang-kacangan dan Umbi-umbian, Ma-lang. 15 hlm.
Prayogo, Y., W. Tengkano, dan Suharsono. 2002b. Efektivitas jamur Beauveria bassiana isolat Probolinggo untuk mengendalikan hama pengisap polong kacang-kacangan. Seminar Nasional Perkembangan Terkini Pengendalian Hayati di Bidang Pertanian dan Kesehatan. Institut Pertanian Bogor, 5 September 2002. 12 hlm.
Prayogo, Y. dan W. Tengkano. 2004a. Pengaruh konsentrasi dan frekuensi aplikasi
Metar-hizium anisopliae isolat kendalpayak
ter-hadap tingkat kematian Spodoptera litura. Jurnal Ilmiah Sainteks XI(3): 233−243. Universitas Semarang.
Prayogo, Y. dan W. Tengkano. 2004b. Pening-katan keefektifan dan waktu aplikasi yang tepat cendawan Verticillium lecanii untuk mengendalikan hama pengisap polong kedelai Riptortus linearis (Hemiptera: Alydidae). Laporan Tahunan Hasil Penelitian Tahun 2004. Balai Penelitian Tanaman Kacang-kacangan dan Umbi-umbian, Ma-lang.
Prayogo, Y. 2004. Keefektifan lima jenis cendawan entomopatogen terhadap hama pengisap polong kedelai Riptortus linearis (L.) (Hemiptera: Alydidae) dan dampaknya terhadap predator Oxyopes javanus Thorell (Araneida: Oxyopidae). Tesis. Departemen Hama Penyakit Tanaman, Sekolah Pasca-sarjana, Institut Pertanian Bogor. 51 hlm. Prayogo, Y dan S.W. Indiati. 2004. Pengaruh
bahan perekat dan bahan pembawa pada tiga jenis cendawan entomopatogen untuk mengendalikan hama tungau merah pada ubi kayu. Laporan Tahunan Hasil Penelitian Tahun 2004. (belum diterbitkan)
Prayogo, Y., T. Santoso, dan Widodo. 2004. Ke-efektifan lima jenis cendawan entomopa-togen terhadap telur hama pengisap polong kedelai (Riptortus linearis) (Hemiptera: Alydidae). Seminar Nasional Hasil Penelitian Tanaman Kacang-Kacangan dan Umbi-Umbian. 11 hlm (belum terbit).
Rauf, A. 1996. Analisis ekosistem dalam pengen-dalian hama terpadu. Pelatihan Peramalan Hama dan Penyakit Tanaman Padi dan Palawija Tingkat Nasional, Jatisari, 2−9 Januari 1996. Departemen Hama dan Penyakit Tumbuhan Institut Pertanian Bogor.
Reithinger, R., C.R. Davies, H. Cadena, and B. Alexander. 1997. Evaluation of the fungus
Beauveria bassiana as a potential biological
control agent against phlebotomine sand flies in Colombian coffee plantations. J. Invertebr. Pathol. (70): 131−135.
Romero, M., M. Estrada, R.F. Castaneda, and M. Lujan. 1997. Morphological and patho-genical characterization of Metarhizium
anisopliae (Metsch.) Sorokin. Cane Sugar
15(1): 17−25. http://memorias.ioc.fiocruz. br/936/3556.html. [20 December 2003]. Santoso, T. 1993. Dasar-dasar patologi serangga.
Dalam E. Martono, E. Mahrub, N.S. Putra,
dan Y. Trisetyawati (Ed.). Simposium Pato-logi Serangga I. Yogyakarta, 12−13 Oktober 1993. Universitas Gadjah Mada, Yogyakarta. hlm. 1−15.
Sosa-Gomez, D.R. and F. Moscardi. 1997. Laboratory and field studies on the infection of stink bugs Nezara viridula, Piezodorus
guildini, and Euschistus heros (Hemiptera:
Pentatomidae) with Metarhizium anisopliae and Beauveria bassiana in Brazil. J. Inver-tebr. Pathol. (71): 115−120.
Sudarmadji, D. dan S. Gunawan. 1994. Pato-genisitas fungi entomopatogen Beauveria
bassiana terhadap Helopeltis antoni. Balai
Penelitian Kopi dan Kakao, Jember. Menara Perkebunan 62(1): 11 hlm.
Suharsono dan Y. Prayogo. 2005. Pengaruh lama pemaparan pada sinar matahari terhadap viabilitas jamur entomopatogen Verticillium
lecanii. Jurnal Habitat XVI(2): 122−131. Steinkraus, D.C. and P.H. Slaymaker. 1994.
Effect of temperature and humidity on formation, germination, and infectivity of conidia of Neozygites fresenii (Zygomycetes: Neozygitaceae) from Aphis gossypii (Ho-moptera: Aphididae). J. Invertebr. Pathol. (64): 130−137.
Strack, B.H. 2003. Biological control of termites by the fungal entomopathogen Metarhizium
anisopliae. http://www.utoronto.ca/forest/
termite/metani_1.htm [20 December 2003] Suryawan, I.B.G. dan G.R. Carner. 1993. Cendawan patogen dari serangga hama pada tanaman palawija dan sayuran. hlm. 288−
295. Dalam E. Martono, E. Mahrub, N.S. Putra, dan Y. Trisetyawati (Ed.). Prosiding Simposium Patologi Serangga I. Yogyakarta, 12−13 Oktober 1993. Universitas Gadjah Mada, Yogyakarta.
Tanada, Y. and H.K. Kaya. 1993. Insect Pathol-ogy. Academic Press, Inc., California. Thomas, M.B. and N.E. Jenkins. 1997. Effect
of temperature on growth of Metarhizium
flavoviridae and virulence to the variegated
grasshopper Zonocerus variegates. Mycol. Res. (101): 1.469−1.474.
Tohidin, A.T. Lisrianto, dan B.P. Machdar. 1993. Daya bunuh jamur entomopatogen Beauveria
bassiana (Balsamo) Vuillemin (Moniliales:
Moniliacea) terhadap Leptocoriza acuta Thunberg (Hemiptera: Alydidae) di rumah kaca. hlm. 135−143. Dalam E. Martono, E. Mahrub, N.S. Putra, dan Y. Trisetyawati (Ed.). Prosiding Simposium Patologi Se-rangga I. Yogyakarta, 12−13 Oktober 1993. Universitas Gadjah Mada, Yogyakarta. Varela, A. and E. Morales. 1996. Characterization
of some Beauveria bassiana isolates and their virulence toward the coffee berry borer
Hypothenemus hampei. J. Invertebr. Pathol.
(67): 147−152.
Wahyunendo, Y.D. 2002. Sporulasi cendawan entomopatogen Beauveria bassiana (Bals.)
Vuill. pada berbagai media alami dan viabilitasnya di bawah pengaruh suhu dan sinar matahari [Skripsi]. Bogor. Institut Pertanian Bogor. Jurusan Hama dan Penyakit Tumbuhan.
Widayat, W. dan D.J. Rayati. 1993a. Hasil Penelitian Jamur Entomopatogen Lokal dan Prospek Penggunaannya sebagai Insektisida Hayati. hlm. 61−74 Dalam E. Martono, E. Mahrub, N.S. Putra, dan Y. Trisetyawati (Ed.). Simposium Patologi Serangga I. Yogyakarta, 12−13 Oktober 1993. Univer-sitas Gadjah Mada, Yogyakarta.
Widayat, W. dan D.J. Rayati. 1993b. Pengaruh frekuensi penyemprotan jamur entomo-patogenik terhadap ulat jengkal (Ectropis
bhurmitra) di perkebunan teh. hlm. 91−103.
Dalam E. Martono, E. Mahrub, N.S. Putra,
dan Y. Trisetyawati (Ed.). Prosiding Sim-posium Patologi Serangga I. Yogyakarta, 12−
13 Oktober 1993. Universitas Gadjah Mada, Yogyakarta.
Wikardi, E.A. 1993. Teknik perbanyakan
Beauveria bassiana dan aplikasinya di
lapang. hlm. 205−214. Dalam E. Martono, E. Mahrub, N.S. Putra, dan Y. Trisetyawati (Ed.). Prosiding Simposium Patologi Se-rangga I. Yogyakarta, 12−13 Oktober 1993. Universitas Gadjah Mada, Yogyakarta. Yuliatin, E. 2004. Pengaruh berbagai jenis
media alami terhadap pertumbuhan dan perkembangan cendawan entomopatogen
Verticillium lecanii. Laporan Praktek Kerja
Lapangan. Universitas Negeri Malang. 25 hlm.