BAB 2
TINJAUAN PUSTAKA
2.1 Definisi
Sindrom nefrotik, suatu manifestasi penyakit glomerular, ditandai dengan
proteinuria berat (ekskresi protein ≥ 40 mg/m2LPB/jam, atau rasio
albumin/kreatinin pada urin sewaktu > 2 mg/mg, atau dipstick ≥ 2+), hipoalbuminemia, edema, dan dapat disertai hiperlipidemia (Pais, Avner, 2011, Nanjundaswamy, Phadke, 2002).
Terdapat beberapa definisi/batasan yang dipakai pada sindrom nefrotik, antara lain (Noer, 2011, Bagga, Mantan, 2005, Nanjundaswamy, Phadke, 2002):
1. Remisi : Proteinuria negatif atau trace (proteinuria < 4 mg/m2 LPB/jam) selama 3 hari berturut-turut dalam 1 minggu.
2. Relaps : Proteinuria ≥ 2+ (proteinuria ≥ 40 mg/m2LPB/jam) 3 hari berturut-turut dalam 1 minggu, dimana sebelumnya pernah mengalami remisi.
3. Relaps jarang : Relaps terjadi kurang dari 2 kali dalam 6 bulan pertama setelah respons awal atau kurang dari 4 kali per tahun pengamatan. 4. Relaps sering : Relaps terjadi ≥ 2 kali dalam 6 bulan pertama setelah
respon awal, atau ≥ 4 kali dalam periode 1 tahun.
5. Sensitif steroid : Remisi tercapai dalam 4 minggu atau kurang setelah pengobatan steroid dosis penuh (full dose).
6. Dependen steroid : Relaps terjadi pada saat dosis steroid diturunkan, atau dalam waktu 14 hari setelah pengobatan steroid dihentikan, dan hal ini terjadi 2 kali berturut-turut.
7. Resisten steroid : tidak terjadi remisi setelah 4 minggu pengobatan steroid dosis penuh (full dose).
2.2 Etiologi
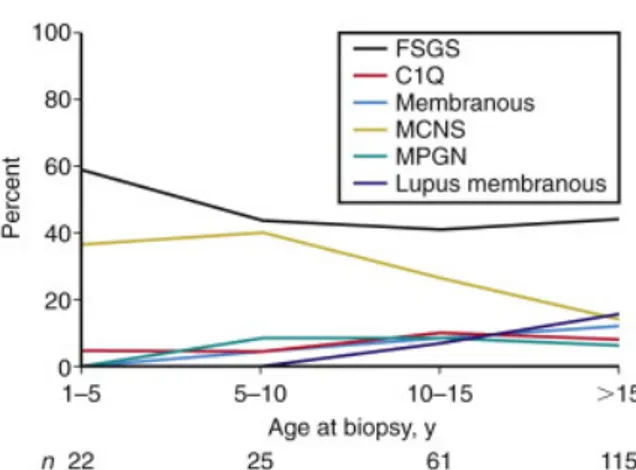
Kebanyakan anak dengan sindrom nefrotik memiliki bentuk sindrom nefrotik primer atau idiopatik (Tabel 2.1). Lesi glomerulus yang berhubungan dengan sindrom nefrotik idiopatik termasuk penyakit kelainan minimal (yang paling umum), glomerulosklerosis fokal segmental, glomerulonefritis membranoproliferatif, nefropati membranosa dan proliferasi mesangial difus. Etiologi-etiologi ini memiliki distribusi usia yang berbeda (Gambar 2.1) (Pais, Avner, 2011).
Sindrom nefrotik juga mungkin sekunder terhadap penyakit sistemik seperti lupus eritematosus sistemik, purpura Henoch-Schönlein, keganasan (limfoma dan leukemia), dan infeksi (hepatitis, HIV, dan malaria) (Tabel 2.1) (Pais, Avner, 2011).
Sindrom nefrotik juga bisa disebabkan oleh kelainan genetik. Sindrom nefrotik kongenital (hadir sejak lahir hingga usia 3 bulan) telah dikaitkan dengan kelainan pada gen nephrin (NPHS1), fosfolipase C epsilon 1 gen (PLCE1), dan gen supresor tumor Wilms.Selain itu, sindrom genetik lainnya telah dikaitkan dengan sindrom nefrotik, seperti sindrom Nail-patella, sindrom Pierson, Schimke immuno-osseus displasia, dan lain-lain (Lane, 2013).
Tabel 2.1 – Penyebab Sindrom Nefrotik Pada Anak
KELAINAN GENETIK
Sindrom Nefrotik (Tipikal) :
Sindrom nefrotik congenital tipe Finnish (Kehilangan nephrin)
Glomerulosklerosis fokal segmental (mutasi pada podocin, α-actinin 4, TRPC6)
Sklerosis mesangial difus (mutasi pada rantai laminin β2)
Sindrom Denys-Drash (mutasi pada factor transkripsi WT1)
Proteinuria Dengan atau Tanpa Sindrom Nefrotik :
Sindrom Nail-patella (mutasi pada factor transkripsi LMX1B)
Sindrom Alport (mutasi pada gen biosintesis kolagen)
Sindrom Multisistem Dengan atau Tanpa Sindrom Nefrotik :
Sindrom Galloway-Mowat
Penyakit Charcot-Marie-Tooth
Sindrom Jeune
Sindrom Cockayne
Sindrom Laurence-Moon-Biedl-Bardet
Gangguan Metabolik Dengan atau Tanpa Sindrom Nefrotik :
Sindrom Alagille
Defisiensi α1 Antitrypsin
Penyakit Fabry
Acidemia glutarat
Penyakit penyimpanan glikogen
Sindrom Hurler
Gangguan Lipoprotein
Sitopati mitokondria
Penyakit sel sabit (Sickle cell disease)
SINDROM NEFROTIK IDIOPATIK
Penyakit kelainan minimal
Glomerulosklerosis fokal segmental
Nefropati membranosa PENYEBAB SEKUNDER Infeksi : Hepatitis B, C HIV-1 Malaria Sifilis Toksoplasmosis Obat-obatan : Penicillamine Emas
Obat anti-inflamasi nonsteroidal
Pamidronate
Interferon
Mercury
Heroin
Lithium
Gangguan Imun atau Alergi :
Penyakit Castleman
Penyakit Kimura
Sengatan lebah
Alergi makanan
Terkait Dengan Penyakit Malignan :
Limfoma
Leukemia
Hiperfiltrasi Glomerulus :
Oligomeganephronia
Obesitas morbid
Gambar 2.1 - Hasil biopsi ginjal dari 223 anak-anak dengan proteinuria dirujuk untuk biopsi ginjal diagnostik (Glomerular Disease Collaborative Network, J. Charles Jennette, MD, Hyunsook Chin, MS, and D.S. Gipson, 2007). n, jumlah pasien, C1Q, nefropati, FSGS, glomerulosklerosis fokal segmental, MCNS, sindrom nefrotik kelainan minimal; MPGN, glomerulonefritis membranoproliferative.
2.3 Patofisiologi
Kelainan yang mendasari sindrom nefrotik adalah peningkatan permeabilitas dari dinding kapiler glomerulus, yang meyebabkan proteinuria masif dan hipoalbuminemia. Pada biopsi, penipisan ekstensif proses kaki podocyte (ciri khas sindrom nefrotik idiopatik) menunjukkan
peran penting untuk podocyte. Sindrom nefrotik idiopatik adalah
berhubungan dengan gangguan yang kompleks dalam sistem
kekebalan/imun tubuh, terutama imunitas diperantarai sel T (T cell–
mediated immunity). Pada glomerulosklerosis fokal segmental, suatu faktor plasma, yang mungkin dihasilkan oleh subset limfosit aktif, mungkin bertanggung jawab untuk peningkatan permeabilitas dinding kapiler. Atau, mutasi pada protein podocyte (podocin, α-actinin 4) dan MYH9 (gen podocyte) dapat berhubungan dengan glomerulosklerosis fokal segmental. Sindrom nefrotik resisten steroid (steroid-resistant nephrotic syndrome) dapat dikaitkan dengan mutasi pada NPHS2 (podocin) dan gen WT1, serta komponen lain dari proses filtrasi glomerulus, seperti pori celah (slit pore), dan termasuk nephrin, NEPH1, dan protein yang terkait dengan CD-2 (Pais, Avner, 2011).
Untuk mekanisme pembentukan edema pada sindrom nefrotik, hilangnya protein urin masif menyebabkan hipoalbuminemia, yang menyebabkan penurunan tekanan onkotik plasma dan transudasi cairan dari kompartemen intravaskular ke ruang interstisial. Penurunan volume intravaskular menurunkan tekanan perfusi ginjal, yang mengaktifkan sistem renin-angiotensin-aldosteron, yang merangsang reabsorpsi natrium di tubular. Penurunan volume intravaskular juga merangsang pelepasan hormon antidiuretik, yang meningkatkan reabsorpsi air dalam collecting duct (Pais, Avner, 2011).
Teori ini tidak berlaku untuk semua pasien dengan sindrom nefrotik karena beberapa pasien sebenarnya ada peningkatan volume intravaskular dengan kadar renin dan aldosteron plasma berkurang. Oleh karena itu, faktor-faktor lain, termasuk aviditas ginjal primer (primary renal avidity) untuk natrium dan air, mungkin terlibat dalam pembentukan edema pada beberapa pasien dengan sindrom nefrotik (Pais, Avner, 2011).
Dalam keadaan nefrotik, tingkat lipid dalam darah/serum (kolesterol, trigliserida) yang meningkat adalah disebabkan dua alasan. Hipoalbuminemia merangsang sintesis protein hepatik umum, termasuk sintesis lipoprotein. Ini juga mengapa sejumlah faktor koagulasi meningkat, lalu meningkatkan risiko trombosis. Selain itu, katabolisme lipid berkurang akibat dari pengurangan kadar lipoprotein lipase plasma yang berkaitan dengan peningkatan kehilangan enzim ini ini melalui urin (Pais, Avner, 2011).
Pasien dengan sindrom nefrotik berada ada peningkatan risiko infeksi (sepsis, peritonitis, pielonefritis), terutama dengan organisme berkapsul seperti Streptococcus pneumoniae dan Haemophilus influenza. Beberapa alasan untuk hal ini termasuk hilangnya faktor komplemen C3b, opsonins seperti properdin faktor B, dan imunoglobulin dalam urin. Faktor
risiko tambahan adalah penggunaan obat imunosupresif untuk mengobati sindrom nefrotik (Pais, Avner, 2011).
Sindrom nefrotik adalah keadaan hiperkoagulasi yang disebabkan beberapa faktor yaitu stasis vaskular, peningkatan produksi hepatik fibrinogen dan faktor pembekuan lainnya, penurunan kadar faktor antikoagulan serum, peningkatan produksi trombosit plasma (sebagai reaktan fase akut), dan peningkatan agregasi platelet. Koagulopati dimanifestasi dengan kejadian tromboemboli (Pais, Avner, 2011).
2.4 Sindrom Nefrotik Idiopatik/Primer
Sekitar 90% anak dengan sindrom nefrotik merupakan sindrom nefrotik idiopatik/primer. Sindrom nefrotik idiopatik berhubungan dengan penyakit glomerulus primer tanpa bukt i adanya penyebab penyakit sistemik tertentu. Sindrom nefrotik idiopatik mempunyai beberapa tipe secara
histologis: penyakit kelainan minimal, proliferasi mesangial,
glomerulosklerosis fokal segmental, nefropati membranosa, dan glomerulonefritis membranoproliferatif (Pais, Avner, 2011).
2.4.1 Manifestasi Klinis
Sindrom nefrotik idiopatik lebih sering terjadi pada anak laki-laki daripada anak perempuan (2: 1) dan paling sering muncul antara usia 2 dan 6 tahun (lihat Gambar 2.1). Sindrom nefrotik kelainan minimal (SNKM) terjadi pada 85% hingga 90% pasien dibawah usia 6 tahun. Sebaliknya, hanya 20% hingga 30% dari remaja yang tampil untuk pertama kalinya dengan sindrom nefrotik memiliki SNKM. Penyebab yang lebih umum dari sindrom nefrotik idiopatik pada kelompok usia yang lebih tua adalah glomerulosklerosis fokal segmental (GSFS). Insidensi GSFS dapat meningkat, mungkin lebih umum pada pasien Afrika-Amerika, Hispanik, dan Asia (Pais, Avner, 2011, Nanjundaswamy, Phadke, 2002).
Anak-anak biasanya tampil dengan edema ringan, yang awalnya terdapat di sekitar mata dan di ekstremitas bawah. Sindrom nefrotik awalnya dapat disalah diagnosis sebagai gangguan alergi karena adanya pembengkakan periorbital yang menurun sepanjang hari. Dengan waktu, edema menjadi generalisasi, dengan adanya perkembangan asites, efusi pleura, dan edema genital. Anoreksia, iritabilitas, nyeri abdomen, dan diare adalah gejala umum. Fitur penting dari sindrom nefrotik idiopatik kelainan minimal adalah ketiadaan hipertensi dan gross hematuria (sebelumnya disebut fitur nephritik) (Pais, Avner, 2011, Nanjundaswamy, Phadke, 2002).
Diagnosis differensial anak yang ditandai dengan edema mencakup enteropati kehilangan protein, gagal hati, gagal jantung, glomerulonefritis akut atau kronis, dan malnutrisi protein. Diagnosis selain SNKM harus dipertimbangkan pada anak dibawah usia 1 tahun, riwayat keluarga positif sindrom nefrotik, adanya temuan ekstrarenal (misalnya, artritis, ruam, anemia), hipertensi atau edema paru, insufisiensi ginjal akut atau kronis, dan gross hematuria (Pais, Avner, 2011).
2.4.2 Pemeriksaan Penunjang
Langkah pertama dalam mengevaluasi anak dengan edema adalah untuk menetapkan apakah adanya sindrom nefrotik, karena hipoalbuminemia dapat terjadi tanpa adanya proteinuria (seperti pada enteropati kehilangan protein), dan edema dapat terjadi tanpa adanya hipoalbuminemia (misalnya, pada angioedema, kebocoran kapiler, insufisiensi vena, gagal jantung kongestif) (Lane, 2013).
Dalam rangka menetapkan adanya sindrom nefrotik, tes laboratorium harus mengkonfirmasi (1) proteinuria nefrotik, (2) hipoalbuminemia, dan (3) hiperlipidemia (Lane, 2013, Nanjundaswamy, Phadke, 2002). Oleh karena itu, pengujian laboratorium awal harus mencakup sebagai berikut:
1. Protein urin - Dengan ekskresi protein ≥ 40 mg/m2LPB/jam atau > 50 mg/kgBB/24 jam, atau rasio albumin/kreatinin pada urin sewaktu > 2 mg/mg, atau dipstick≥ 2+
2. Albumin serum - Kurang dari 2,5 g/dL
3. Panel lipid - Peningkatan kolesterol total, kolesterol low-density lipoprotein (LDL), peningkatan trigliserida dengan hipoalbuminemia berat, kolesterol high-density lipoprotein (HDL) (normal atau rendah)
Setelah menentukan adanya sindrom nefrotik, tugas selanjutnya adalah untuk menentukan apakah sindrom nefrotik primer (idiopatik) atau sekunder terhadap gangguan sistemik dan, jika sindrom nefrotik idiopatik (SNI) telah ditentukan, apakah ada tanda-tanda penyakit ginjal kronis , insufisiensi ginjal, atau tanda-tanda yang dapat mengecualikan
kemungkinan sindrom nefrotik kelainan minimal (SNKM) (Lane, 2013,
Nanjundaswamy, Phadke, 2002). Oleh karena itu, di samping tes di atas, berikut ini harus dimasukkan dalam hasil pemeriksaan:
1. Jumlah sel darah lengkap (Complete Blood Count (CBC)) –
Peningkatan hemoglobin dan hematokrit, jumlah trombosit meningkat 2. Panel metabolik - Elektrolit serum rendah, BUN dan kreatinin tinggi,
kalsium rendah, fosfor, dan kadar kalsium terionisasi normal
3. Pengujian untuk HIV, hepatitis B dan C - Pertimbangkan pemeriksaan enzim hati, seperti alanin aminotransferase (ALT) dan aspartat aminotransferase (AST), ketika skrining untuk penyakit hati.
4. Studi komplemen (C3, C4) – Kadar rendah
5. Antibodi antinuklear (ANA), antibodi anti–double-stranded DNA
(pada pasien yang dipilih)
Pada pasien dengan SNI dapat terjadi kehilangan protein yang mengikat vitamin D, yang dapat mengakibatkan tingkat vitamin D rendah, dan globulin yang mengikat tiroid, yang dapat mengakibatkan kadar hormon tiroid yang rendah. Pertimbangan harus diberikan, terutama pada
anak yang sering kambuh atau sindrom nefrotik resisten steroid, untuk melakukan pengujian untuk 25-OH-vitamin D, 1,25-di (OH)-vitamin D, T4 bebas, dan thyroid-stimulating hormone (TSH) (Lane, 2013).
Tes dan prosedur lain pada pasien tertentu mungkin termasuk yang berikut:
1. Studi genetik - Mutasi NPHS1, NPHS2, WT1, dan LAMB2
2. Ultrasonografi ginjal - Ginjal biasanya membesar karena edema
jaringan
3. Radiografi dada - Radiografi dada diindikasi pada anak dengan
gangguan pernapasan. Efusi pleura adalah umum, namun edema paru jarang terjadi
4. Uji Mantoux - Harus dilakukan sebelum pengobatan steroid untuk
menyingkirkan infeksi TB.
5. Biopsi ginjal - Biopsi ginjal juga harus dilakukan apabila hasil anamnesis, pemeriksaan fisik, atau laboratorium menunjukkan sindrom nefrotik sekunder atau sindrom nefrotik primer selain SNKM
Umur memainkan peran penting dalam evaluasi diagnostik sindrom nefrotik. Anak-anak yang mengalami sindrom nefrotik dibawah usia 1 tahun harus dievaluasi untuk sindrom nefrotik kongenital (Lane, 2013). Selain tes di atas, bayi harus dilakukan tes berikut:
1. Infeksi kongenital (sifilis, rubella, toksoplasmosis, sitomegalovirus, HIV)
2. Biopsi ginjal
3. Tes genetik untuk mutasi NPHS1, NPHS2, WT1, dan LAMB2
sebagaimana dibimbing berdasarkan temuan biopsi dan presentasi klinis
Kadang-kadang, pasien dengan sindrom nefrotik juga
menunjukkan atau membentuk tanda-tanda klinis dari abdomen akut, yang sering karena peritonitis. Diagnosis biasanya dapat dibuat secara klinis dan
dikonfirmasi dengan pemeriksaan bakteriologis dari aspirasi cairan peritoneal. Organisme yang paling sering dijumpai pada peritonitis adalah Streptococcus pneumoniae, namun bakteri enterik usus juga dapat menyebabkan peritonitis. Penatalaksanaan adalah secara medis daripada bedah (Lane, 2013).
2.4.3 Histopatologi
Klasifikasi kelainan histopatologis glomerulus pada sindrom nefrotik yang digunakan sesuai dengan rekomendasi Komisi Internasional (1982). Kelainan glomerulus ini sebagian besar ditegakkan dengan pemeriksaan mikroskop cahaya, ditambah dengan pemeriksaan mikroskop electron dan imunofluoresensi. Pada Tabel 2.2, dipakai istilah/terminologi yang sesuai
dengan laporan International Study of Kidney Disease in Children
(ISKDC) (1970) dan Habib dan Kleinknecth (1971) (Wirya, 2002, Bagga, Mantan, 2005, Mubarak, Kazi, 2013).
Tabel 2.2 – Klasifikasi Kelainan Glomerulus Pada Sindrom Nefrotik Primer
Kelainan minimal (KM) Glomerulosklerosis (GS)
Glomerulosklerosis fokal segmental (GSFS) Glomerulosklerosis fokal global (GSFG)
Glomerulonefritis proliferatif mesangial difus (GNPMD) Glomerulonefritis proliferatif mesangial difus eksudatif Glomerulonefritis kresentik (GNK)
Glomerulonefritis membranoproliferatif (GNMP) GNMP tipe I dengan deposit subendotelial GNMP tipe II dengan deposit intramembran
GNMP tipe III dengan deposit transmembran/subepitelial Glomerulopati membranosa (GM)
2.4.4 Diagnosa Differensial
Diagnosa differensial dari sindrom nefrotik adalah (Leung, Wong, 2010): 1. Glomerulonefritis poststreptococcal
2. Sindrom Alport
3. Henoch-Schönlein purpura
4. Systemic lupus erythematosus (SLE) 5. Diabetes mellitus
6. Sindrom nefrotik congenital
7. Sindrom nefrotik kelainan minimal (SNKM)
8. Glomeruloskleresis fokal segmental (GSFS)
9. Glomerulonefritis proliferatif mesangial difus (GNPMD) 10. Glomerulonefritis membranoproliferatif (GNMP)
11. Glomerulopati membranosa (GM) 12. Keganasan (malignancy)
13. Acute tubular necrosis
14. Acute tubulointerstitial nephritis 15. Polycystic kidney disease
16. Proximal renal tubular acidosis 17. Pyelonephritis
18. Toksin
2.4.5 Penatalaksanaan
Pada sindrom nefrotik pertama kali, sebaiknya dirawat di rumah sakit dengan tujuan untuk mempercepat pemeriksaan dan evaluasi pengaturan diet, penanggulangan edema, memulai pengobatan steroid, dan edukasi orang tua. Sebelum pengobatan steroid dimulai, dilakukan pemeriksaan uji Mantoux. Bila hasilnya positif diberikan profilaksis isoniazid (INH) bersama steroid, dan bila ditemukan tuberkulosis diberikan obat anti tuberkulosis (OAT). Perawatan pada sindrom nefrotik relaps hanya dilakukan bila disertai edema anasarka yang berat atau disertai komplikasi
muntah, infeksi berat, gagal ginjal, atau syok. Tirah baring tidak perlu dipaksakan dan aktivitas disesuaikan dengan kemampuan pasien. Bila edema tidak berat anak boleh sekolah (Noer, 2011, Nanjundaswamy, Phadke, 2002)
2.4.5.1 Dietetik
• Diberikan diet protein normal sesuai dengan RDA (recommended
daily allowances) yaitu 1,5-2 g/kgBB/hari dengan kalori yang adekuat.
• Lemak dapat diberikan dengan jumlah yang tidak melebihi 30%
jumlah total kalori keseluruhan, lebih dianjurkan memberikan karbohidrat kompleks daripada gula sederhana.
• Restriksi garam dan cairan tidak diperlukan pada sebagian besar
kasus sindrom nefrotik sensitif steroid.
• Diet rendah garam (1-2 g/hari atau 2 mmol/kg/hari) plus
menghindari makanan ringan yang asin, dianjurkan selama anak mengalami edema atau hipertensi (Noer, 2011, Gipson, et al., 2009, Nanjundaswamy, Phadke, 2002).
2.4.5.2 Edema/Sembab
• Sebagian pasien dengan sembab ringan tidak memerlukan diuretik.
• Pasien dengan sembab nyata tanpa deplesi volume intravaskular
diberikan furosemid 1-3 mg/kgBB/hari 2 kali sehari. Bila tidak ada respons, dosis dinaikkan sampai 4-6 mg/kgBB/hari bersama dengan spironolakton (antagonis aldosteron) 2-3 mg/kg/hari, sebagai potassium-sparing agent (diuretik hemat kalium). Bila dengan terapi tersebut masih gagal, dapat ditambahkan thiazide (hidroklorotiazid). Kadang-kadang perlu diberikan furosemid bolus intravena atau infus.
• Intake air tidak perlu direstriksi, kecuali pada pasien dengan sembab hebat. Pada keadaan tersebut, intake cairan dibatasi sesuai dengan insensible loss plus jumlah urin sehari sebelumnya.
• Terapi diuretik kadang-kadang tidak efektif bahkan dapat
membahayakan pasien yang mengalami hipoalbuminemia (albumin serum < 1,5 g/dL) plus deplesi volume intravascular. Pemberian infuse albumin 20% (kadang-kadang diperlukan beberapa kali infus) dengan furosemid dapat memacu diuresis dan mengurangi sembab.
• Bila pemberian diuretik tidak berhasil mengurangi edema (edema
refrakter), biasanya disebabkan oleh hipovolemia atau hipoalbuminemia berat (kadar albumin ≤ 1 g/dL), dapat diberikan infus albumin 20 hingga 25% dengan dosis 1 g/kgBB selama 4 jam untuk menarik cairan dari jaringan interstitial, dan diakhiri dengan pemberian furosemid intarvena 1-2 mg/kgBB.
• Bila pasien tidak mampu dari segi biaya, dapat diberikan plasma
sebanyak 20 ml/kgBB/hari secara pelan-pelan 10 tetes/menit untuk mencegah terjadinya komplikasi dekompensasi jantung.
• Bila diperlukan, albumin atau plasma dapat diberikan selang sehari untuk memberikan kesempatan pergeseran cairan dan mencegah overload cairan (Noer, 2011, Nanjundaswamy, Phadke, 2002).
2.4.5.3 Pengobatan Inisial Sindrom Nefrotik
• Prednison dosis penuh (full dose) 2 mg/kg/hari atau 60
mg/m2LPB/hari (maksimal 80 mg/hari) dibagi 3 dosis diberikan
setiap hari selama 4 minggu, dilanjutkan dengan prednisone dosis
40 mg/m2LPB/hari (2/3 dosis penuh), dapat diberikan secara
intermitent (3 hari berturut-turut dalam 1 minggu) atau alternating (selang sahari), 1 kali sehari setelah makan pagi, selama 4 minggu.
• Bila remisi terjadi dalam 4 minggu pertama, maka prednisone intermittent/alternating dosis 40 mg/m2LPB/hari diberikan selama 4 minggu.
• Bila remisi tidak terjadi pada 4 minggu pertama, maka pasien
tersebut didiagnosis sebagai sindrom nefrotik resisten steroid (Noer, 2011, Nanjundaswamy, Phadke, 2002).
2.4.5.4 Pengobatan Sindrom Nefrotik Relaps
• Prednison dosis penuh setiap hari (dosis tunggal atau terbagi)
sampai remisi (maksimal 4 minggu) kemudian dilanjutkan dengan prednison intermittent/alternating (dosis tunggal pada pagi hari) dosis 40 mg/m2LPB/hari selama 4 minggu.
• Bila sampai pengobatan dosis penuh selama 4 minggu tidak juga
terjadi remisi, maka pasien didiagnosis sebagai sindrom nefrotik resisten steroid dan harus diberikan terapi imunosupresif lain (Noer, 2011, Nanjundaswamy, Phadke, 2002).
2.4.5.5 Pengobatan Sindrom Nefrotik Relaps Sering atau Dependen Steroid
• Prednison dosis penuh setiap hari sampai remisi (maksimal 4
minggu) kemudian dilanjutkan dengan prednison intermittent/alternating dosis 40 mg/m2LPB/hari diturunkan perlahan/bertahap 0,2 mg/kgBB sampai dosis terkecil yang tidak
menimbulkan relaps yaitu antara 0,1-0,5 mg/kgBB alternating.
Dosis ini disebut dosis threshold dan dapat diteruskan selama 6 hingga 12 bulan, kemudian dicoba dihentikan.
• Bila terjadi relaps pada dosis prednison rumatan > 0,5 mg/kgBB alternating, tetapi < 1,0 mg/kgBB alternating tanpa efek samping yang berat, dapat dicoba dikombinasikan dengan levamisol dosis 2,5 mg/kgBB dosis tunggal selang sahari, selama 4 hingga 12 bulan, atau langsung diberikan siklofosfamid (CPA). Diberikan
CPA dengan dosis 2-3 mg/kgBB/hari, dosis tunggal selama 8 hingga 12 minggu (Madani, et al., 2010).
• Pada sindrom nefrotik yang tidak responsif dengan pengobatan
steroid atau sitostatik (siklofosfamid (CPA)) dianjurkan pemberian siklosporin (suatu inhibitor calcineurin) dengan dosis 5-6 mg/kgBB/hari (Noer, 2011, Nanjundaswamy, Phadke, 2002).
2.4.5.6 Pengobatan Sindrom Nefrotik Resisten Steroid
• Sebelum pengobatan dimulai, pada pasien sindrom nefrotik resisten steroid sebaiknya dilakukan biopsi ginjal untuk melihat gambaran patologi anatomi ginjal, karena gambaran patologi anatomi tersebut mempengaruhi prognosis (Noer, 2011, Gipson, et al., 2009).
• Sitostatik oral : siklofosfamid (CPA) 2-3 mg/kgBB/hari dosis
tunggal selama 3-6 bulan.
• Prednison dosis 40 mg/m2LPB/hari alternating selama pemberian siklofosfamid oral. Kemudian prednison ditapering-off dengan dosis 1 mg/kgBB/hari selama 1 bulan, dilanjutkan dengan 0,5 mg/kgBB/hari selama 1 bulan (lama tapering off 2 bulan).
• Atau, siklofosfamid puls dengan dosis 500-750 mg/m2LPB
diberikan melalui infus satu kali sebulan selama 6 bulan, dapat dilanjutkan tergantung keadaan pasien.
• Prednison alternating dosis 40 mg/m2LPB/hari selama pemberian siklofosfamid puls (6 bulan). Kemudian prednison ditapering-off dengan dosis 1 mg/kgBB/hari selama 1 bulan, dilanjutkan dengan
0,5 mg/kgBB/hari selama 1 bulan (lama tapering off 2 bulan)
2.4.5.7 Pemberian Non Imunosupresif untuk Mengurangi Proteinuria
• Pada pasien sindrom nefrotik yang telah resisten terhadap obat
kortikosteroid, sitostatik, dan siklosporin (atau tidak mampu membeli obat ini), dapat diberikan diuretik (bila ada edema)
dikombinasikan dengan inhibitor ACE (angiotensin converting
enzyme) untuk mengurangi proteinuria.
• Jenis obat ini yang biasa dipakai adalah kaptopril 0,3 mg/kgBB, 3 kali sehari, atau enalapril 0,5 mg/kgBB/hari dibagi 2 dosis.
• Tujuan pemberian inhibitor ACE juga untuk menghambat
terjadinya gagal ginjal terminal (renoprotektif), dapat dikombinasikan dengan golongan anti reseptor bloker (ARB) misalnya losaktan 0,75 mg/kgBB dosis tunggal (Noer, 2011, Nanjundaswamy, Phadke, 2002).
2.4.6 Komplikasi
Infeksi merupakan komplikasi utama dari sindrom nefrotik. Anak-anak yang kambuh telah terjadi peningkatan kerentanan terhadap infeksi bakteri karena kehilangan imunoglobulin dan faktor B properdin dari urin, cacat imunitas cell-mediated, terapi imunosupresif, malnutrisi, dan edema atau ascites bertindak sebagai medium kultur potensial. Peritonitis bakterial spontan adalah infeksi umum, namun sepsis, pneumonia, selulitis, dan
infeksi saluran kemih juga dapat dilihat. Meskipun Streptococcus
pneumonia adalah organisme yang paling umum yang menyebabkan peritonitis, bakteri gram negatif seperti Escherichia coli juga dapat ditemui. Keluarga pasien harus diberi konseling untuk mencari bantuan medis jika anak tampak sakit, mengalami demam, atau mengeluh sakit abdomen terus-menerus. Apabila terjadi kecurigaan yang tinggi untuk bacterial peritonitis, evaluasi cepat (termasuk kultur darah dan cairan peritoneal), dan inisiasi awal terapi antibiotik sangat penting (Al Salloum, et al., 2012, Pais, Avner, 2011, Bagga, Mantan, 2005).
Anak-anak dengan sindrom nefrotik harus menerima vaksin pneumokokus serotype-23 (selain vaksin pneumokokus konjugat 7-valent), diberikan sesuai dengan jadwal imunisasi rutin, idealnya diberikan ketika anak berada dalam fase remisi dan terapi selang sehari. Vaksin virus hidup tidak boleh diberikan kepada anak-anak yang menerima steroid dosis tinggi harian atau selang sehari (≥ 2 mg/kg/ hari prednison atau yang setara, atau ≥20 mg/hari jika anak memiliki berat >10kg). Vaksin dapat diberikan setelah terapi kortikosteroid telah dihentikan selama sekurangnya 1 bulan. Anak dengan nefrotik nonimmune yang kambuh, jika terkena varicella, harus menerima immunoglobulin varicella-zoster (1 dosis ≤ 96 jam setelah eksposur yang signifikan). Vaksin influenza harus diberikan secara tahunan (Al Salloum, et al., 2012, Pais, Avner, 2011,
Bagga, Mantan, 2005).
Anak-anak dengan sindrom nefrotik juga mengalami peningkatan risiko kejadian tromboemboli. Insidensi komplikasi ini pada anak-anak adalah 2% hingga 5%, yang merupakan risiko yang jauh lebih rendah dibandingkan orang dewasa dengan sindrom nefrotik. Trombosis baik arteri dan vena dapat dilihat, termasuk trombosis vena ginjal, emboli paru, trombosis sinus sagital, dan trombosis kateter arteri dan vena. Risiko trombosis terkait dengan peningkatan faktor prothrombotik (fibrinogen, trombositosis, hemokonsentrasi, imobilisasi relatif) dan penurunan faktor fibrinolitik (kehilangan antitrombin III, protein C dan S urin). Antikoagulan profilaksis tidak dianjurkan pada anak-anak kecuali sebelumnya pernah ada riwayat tromboemboli. Untuk meminimalkan risiko komplikasi tromboemboli, penggunaan agresif obat diuretik dan
penggunaan kateter indwelling harus dihindari jika mungkin.
Hiperlipidemia, terutama pada pasien dengan sindrom nefrotik yang rumit, dapat menjadi faktor risiko penyakit jantung; infark miokard merupakan komplikasi yang jarang pada anak-anak. Telah dikemukakan bahwa obat
harus digunakan untuk mengobati hiperlipidemia yang terlihat pada sindrom nefrotik persisten, namun data terkontrol mengenai risiko atau manfaatnya tidak tersedia (Al Salloum, et al., 2012, Pais, Avner, 2011).
2.4.7 Prognosis
Meskipun tidak ada cara yang terbukti untuk memprediksi perjalanan penyakit anak secara individu, anak-anak yang member respon dengan cepat terhadap steroid dan mereka yang tidak kambuh semula selama 6 bulan pertama setelah diagnosis cenderung jarang kambuh sindrom nefrotiknya. Untuk meminimalkan efek psikologis dari kondisi dan terapinya, anak-anak dengan sindrom nefrotik idiopatik tidak boleh dianggap sakit kronis dan boleh berpartisipasi dalam semua kegiatan anak sesuai dengan usia dan mempertahankan diet yang tak terbatas ketika dalam fase remisi (Pais, Avner, 2011, Al Salloum, et al., 2012).
Anak-anak dengan sindrom nefrotik resisten steroid, paling sering disebabkan oleh GSFS, umumnya memiliki prognosis yang jauh lebih buruk. Anak-anak dapat terjadi insufisiensi ginjal progresif, akhirnya mengarah ke stadium akhir penyakit ginjal yang memerlukan dialisis atau transplantasi ginjal. Sindrom nefrotik berulang/rekuren terjadi pada 30% hingga 50% dari penerima transplantasi dengan GSFS (Pais, Avner, 2011, Al Salloum, et al., 2012).
2.5 Sindrom Nefrotik Sekunder
Sindrom nefrotik dapat terjadi sebagai karakteristik sekunder dari penyakit glomerulus. Nefropati membranosa, glomerulonefritis membranoproliferatif, glomerulonefritis pascainfektsi, nefritis lupus, dan nefritis Henoch-Schönlein purpura semua dapat memiliki komponen nefrotik (lihat Tabel 2.1). Sindrom nefrotik sekunder harus dicurigai pada pasien diatas usia 8 tahun dan mereka dengan hipertensi, hematuria,
disfungsi ginjal, gejala ekstrarenal (ruam, arthralgia, demam), atau penurunan tingkat komplemen serum (Pais, Avner, 2011).
Di daerah tertentu di dunia, malaria dan schistosomiasis adalah penyebab utama dari sindrom nefrotik. Agen infeksi lainnya yang terkait dengan sindrom nefrotik termasuk virus hepatitis B, virus hepatitis C, filaria, kusta, dan HIV (Pais, Avner, 2011).
Sindrom nefrotik telah dikaitkan dengan malignansi, khususnya pada populasi orang dewasa. Pada pasien dengan tumor padat, seperti karsinoma pada paru-paru dan saluran pencernaan, patologi ginjal sering menyerupai glomerulopati membranosa. Kompleks imun terdiri dari antigen tumor dan antibodi spesifik tumor mungkin memediasi keterlibatan ginjal. Pada pasien dengan limfoma, terutama limfoma Hodgkin, patologi ginjal paling sering menyerupai sindrom nefrotik kelainan minimal (SNKM). Mekanismenya adalah bahwa limfoma menghasilkan limfokin yang meningkatkan permeabilitas dinding kapiler glomerulus. Sindrom nefrotik dapat terjadi sebelum atau setelah keganasan terdeteksi, setelah regresi tumor, dan kembali jika tumor berulang (Pais, Avner, 2011).
Sindrom nefrotik juga dapat terjadi selama terapi dengan berbagai obat-obatan dan bahan kimia. Gambaran histologis dapat menyerupai
glomerulopati membranosa (penisilamin, kaptopril, anti-inflamasi
nonsteroid, senyawa merkuri), SNKM (probenesid, ethosuximide, methimazole, lithium), atau glomerulonefritis proliferatif (procainamide, chlorpropamide, phenytoin, trimethadione, paramethadione) (Pais, Avner, 2011).
2.6 Sindrom Nefrotik Kongenital
Sindrom nefrotik memiliki prognosis yang buruk apabila terjadi dalam 1 tahun kehidupan, bila dibandingkan dengan sindrom nefrotik yang terjadi
pada masa kanak-kanak. Sindrom nefrotik kongenital didefinisikan sebagai sindrom nefrotik yang hadir pada saat lahir atau dalam 3 bulan kehidupan. Sindrom nefrotik kongenital dapat diklasifikasikan sebagai primer atau sebagai sekunder untuk beberapa etiologi seperti infeksi di rahim (sitomegalovirus, toksoplasmosis, sifilis, hepatitis B dan C, HIV), lupus eritematosus sistemik infantil, atau paparan merkuri (Pais, Avner, 2011).
Sindrom nefrotik kongenital primer adalah disebabkan berbagai sindrom yang diwariskan sebagai gangguan resesif autosomal. Sejumlah kelainan struktural dan fungsional dari barrier filtrasi glomerulus menyebabkan sindrom nefrotik kongenital yang telah dijelaskan. Barrier filtrasi glomerulus, baik ukuran dan muatan selektif, terdiri dari 3 lapisan: endotelium fenestrated, membran basal glomerulus, dan podocyte foot processes. Podosit saling berhubungan dengan menjembatani struktur, celah diafragma, yang bertindak sebagai filter ukuran, sedangkan membran basal glomerulus membatasi molekul berdasarkan muatan ion mereka (Pais, Avner, 2011).
Dalam studi kohort di Eropa menunjukkan anak-anak dengan sindrom nefrotik kongenital, 85% menunjukkan penyakit, menyebabkan mutasi di 4 gen (NPHS1, NPHS2, WT1, dan LAMB2), 3 yang pertama yang mengkode komponen penghalang filtrasi glomerulus. Sindrom nefrotik kongenital tipe Finnish disebabkan oleh mutasi pada gen NPHS1 atau NPHS2, yang mengkode nephrin dan podocin, komponen-komponen penting dari celah diafragma. Bayi yang terkena paling sering terlihat saat lahir dengan edema akibat proteinuria masif, dan mereka biasanya dilahirkan dengan plasenta membesar (> 25% dari berat bayi). Hipoalbuminemia berat, hiperlipidemia, dan hypogammaglobulinemia adalah hasil dari hilangnya penyaringan selektivitas pada penghalang filtrasi glomerulus. Diagnosis prenatal dapat dilakukan dengan adanya
Sindrom Denys-Drash disebabkan oleh mutasi pada gen WT1, yang menghasilkan fungsi podosit abnormal. Pasien datang dengan onset awal sindrom nefrotik, insufisiensi ginjal progresif, ambigu genitalia, dan tumor Wilms (Pais, Avner, 2011).
Mutasi pada gen LAMB2, terlihat pada sindrom Pierson,
menyebabkan kelainan β2 laminin, komponen penting dari glomerulus dan membran basal okular. Selain sindrom nefrotik kongenital, bayi yang
terkena menunjukkan bilateral microcoria (penyempitan tetap pupil)
(Pais, Avner, 2011).
Tanpa memperhatikan dari etiologi sindrom nefrotik kongenital, diagnosis dibuat secara klinis pada bayi baru lahir atau bayi yang menunjukkan edema generalisasi berat, pertumbuhan dan gizi yang buruk dengan hipoalbuminemia, peningkatan kerentanan terhadap infeksi, hipotiroidisme (karena kehilangan globulin pengikat tiroksin urin), dan meningkatkan risiko trombotik. Kebanyakan bayi memiliki insufisiensi ginjal progresif (Pais, Avner, 2011).
Sindrom nefrotik kongenital sekunder dapat diterapi dengan pengobatan penyebab yang mendasari, seperti sifilis. Pengelolaan sindrom nefrotik kongenital primer meliputi perawatan suportif intensif dengan albumin intravena dan diuretik, pemberian rutin intravena globulin-gamma, dan dukungan nutrisi yang agresif (sering parenteral), angiotensin-converting enzyme inhibitor, angiotensin II receptor inhibitor, dan penghambat sintesis prostaglandin atau bahkan nefrektomi unilateral. Jika manajemen konservatif gagal, dan pasien menderita anasarka persisten atau infeksi berat berulang, nefrektomi bilateral dilakukan dan dialisis kronis dimulai. Transplantasi ginjal adalah pengobatan definitif sindrom nefrotik kongenital, meskipun kekambuhan dari sindrom nefrotik telah dilaporkan terjadi setelah transplantasi (Pais, Avner, 2011).