14 BAB II
DESKRIPSI PROSES
2. 1. Spesifikasi Bahan Baku dan Produk 2. 1. 1. Spesifikasi Bahan Baku
1. Sodium Hidroksida (NaOH)
a. Bentuk : Padat
b. Warna : Putih
c. Densitas (20°C) : 1,5605 g/ml d. Titik Leleh (1 atm) : 26,7°C
e. Titik Didih : 107,8°C
f. Kemurnian : 98%
g. Impuritas (Na 2 CO 3 ) : 2%
h. Kelarutan dalam air (20°C) : 111 g/100 ml
(PT Asahimas Chemical) 2. Silika (SiO 2 )
a. Bentuk : Padat
b. Warna : Abu-abu kehitaman
c. Kemurnian : 95,3 %
d. Ukuran : 4 – 6 mesh
e. Kelarutan dalam air (20°C) : 0,079 g/100 ml f. Impuritas : - Al 2 O 3 : 2,68%
- Fe 2 O 3 : 0,14%
- H 2 O : 0,48%
(PT Petrochem Sinergy Indonesia) 2. 1. 2. Spesifikasi Produk
1. Sodium Silikat (Na 2 O(SiO 2 ) x )
a. Bentuk : Padat
b. Warna : Putih
c. Ratio Na 2 O:SiO 2 : 1:2 – 1:2,5
d. Ukuran : >95 mesh
e. Kemurnian : 99%
f. Kelarutan dalam air (20 0 C) : 0,012 g/100 ml
g. Impuritas : Al 2 O 3 maksimal 0,25 % Fe 2 O 3 maksimal 0,15 %
(Coogee Chemicals) 2. Air (H 2 O)
a. Bentuk : Cair
b. Warna : Bening
c. Titik Didih : 100°C
d. Titik Beku : 0°C
e. Densitas : 0,998 g/cm 3 (25°C)
2. 2. Konsep Proses 2.2.1. Dasar Reaksi
Metode untuk memproduksi sodium silikat adalah dengan mencampur sodium hidroksida dan pasir silika. Reaksi yang terjadi bersifat endotermis yaitu pada saat reaksi berlangsung akan membutuhkan panas. Suhu reaksi berkisar antara 200°C – 250°C. Secara sederhana reaksi yang terjadi dapat dituliskan sebagai berikut:
2NaOH + 2,5SiO 2 + H 2 O Na 2 O(SiO 2 ) 2,5 + 2H 2 O
Kondisi operasi dalam proses pembuatan sodium silikat mempunyai tekanan operasi 23 bar dan temperatur 220 ° C di dalam reaktor. Dengan konversi 75%.
Pada suhu tersebut kondisi reaktan adalah fase cair maka digunakan reaktor jenis fixed bed singletube. Pada reaksi ini digunakan bahan baku NaOH yang banyak terdapat dipasaran berupa NaOH dengan kadar 98% yaitu NaOH yang diproduksi dari pabrik-pabrik yang ada di Indonesia. Pada reaksi ini digunakan bahan baku NaOH yang didapat dari PT Asahimas Chemical dengan kadar 98%.
2.2.2. Tinjauan Kinetika
Berdasarkan percobaan Mgaidi et, al. (2004) data konstanta kecepatan
reaksi dapat diketahui dengan perhitungan berikut :
y = 0,1626ln(x) + 0,3479 R² = 0,8524
0 0,2 0,4 0,6 0,8 1 1,2
0 10 20 30 40 50 60 70
1 -(1 -α )
1/3Waktu reaksi (menit)
1-(1-α)
1/3vs waktu
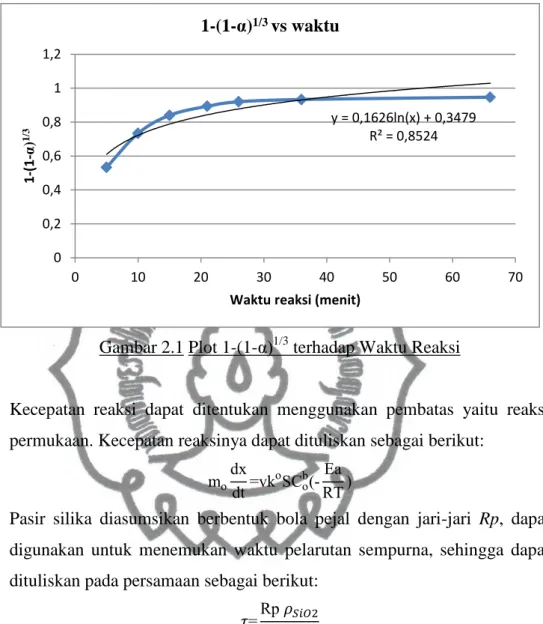
Gambar 2.1 Plot 1-(1-α) 1/3 terhadap Waktu Reaksi
Kecepatan reaksi dapat ditentukan menggunakan pembatas yaitu reaksi permukaan. Kecepatan reaksinya dapat dituliskan sebagai berikut:
- )
Pasir silika diasumsikan berbentuk bola pejal dengan jari-jari Rp, dapat digunakan untuk menemukan waktu pelarutan sempurna, sehingga dapat dituliskan pada persamaan sebagai berikut:
Sehingga waktu yang diperlukan untuk mencapai konversi yang diinginkan melalui shringking core model dapat dirumuskan sebagai berikut:
Dari data percobaan yang dilakukan Mgaidi et al (2004), data kinetika
diperoleh dengan plot persamaan kinetika 1-(1-α) 1/3 terhadap waktu seperti
yang ditampilkan pada Gambar 2.1. Setelah dilakukan plot 1-(1-α) 1/3
terhadap waktu diperoleh persamaan y=0,1626ln(x)+0,3749. Sesuai
dengan persamaan kinetika yang diperoleh dari percobaan yang dilakukan
Mgaidi et, al. (2004), fungsi kecepatan reaksi dapat dituliskan dengan 1-
(1-α) 1/3 = k.t. Slope yang diperoleh dari persamaan y=0,1626ln(x)+0,3749 merupakan nilai k sebagai konstanta kecepatan reaksi. Dengan demikian nilai k=0,1626/menit.
Persamaan kecepatan reaksi:
2NaOH (l) + 2SiO 2(s) Na 2 Si 2 O 5(l) + H 2 O SO + PS SS
-r = k.C SO .C PS
-r = 0,1626.C SO .C PS
2. 2. 3. Mekanisme Reaksi
Berikut tahapan reaksi non-katalitik padat-cair
1. Difusi NaOH melalui lapisan film permukaan padatan
2. Difusi NaOH melalui ash film ke permukaan inti yang tidak bereaksi 3. Reaksi kimia dengan padatan pada permukaan
4. Difusi produk melalui ash film kembali ke permukaan luar padatan 5. Difusi produk melalui lapisan film gas kembali ke dalam tubuh utama
cairan
Menurut Mgaidi et, al. (2004) reaksi sintesis natrium silikat dapat digambarkan dengan metode shrinking core model dengan reaksi dikendalikan oleh difusi pada lapisan abu. Waktu konversi dapat ditunjukkan dengan persamaan:
Dengan:
: konversi yang diinginkan (0,75) B : parameter fungsi D e (B=2,62) 2. 2. 4. Tinjauan Termodinamika
Ditinjau dari segi termodinamika dengan harga-h rg ΔH f untuk
masing-masing komponen pada suhu 25°C (298,15 K) dapat dilihat pada
Tabel 2.1.
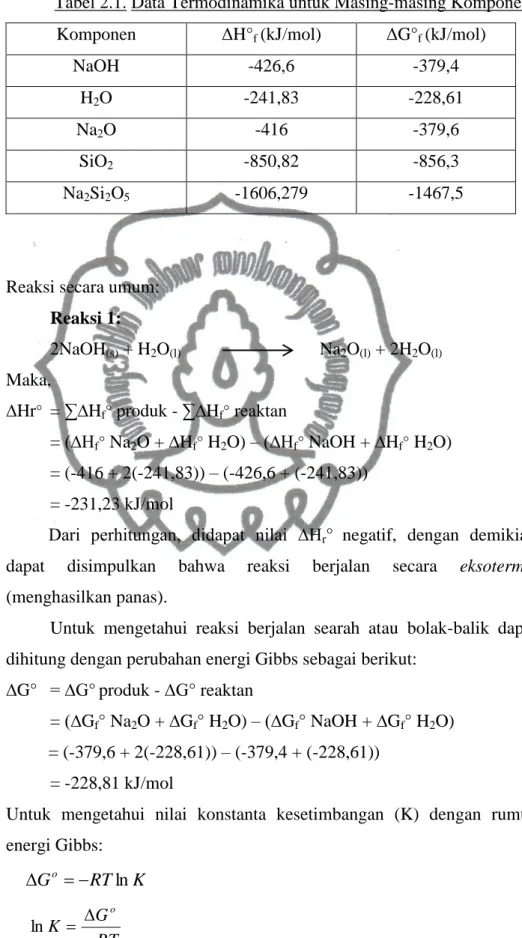
Tabel 2.1. Data Termodinamika untuk Masing-masing Komponen Komponen ΔH° f (kJ/mol) ΔG° f (kJ/mol)
NaOH -426,6 -379,4
H 2 O -241,83 -228,61
Na 2 O -416 -379,6
SiO 2 -850,82 -856,3
Na 2 Si 2 O 5 -1606,279 -1467,5
Reaksi secara umum:
Reaksi 1:
2NaOH (s) + H 2 O (l) Na 2 O (l) + 2H 2 O (l) Maka,
∆Hr ° = ∑∆H f ° produk - ∑∆H f ° reaktan
= ∆H f ° Na 2 O + ∆H f ° H 2 O) – ∆H f ° NaOH + ∆H f ° H 2 O)
= (-416 + 2(-241,83)) – (-426,6 + (-241,83))
= -231,23 kJ/mol
D ri erhi ung n, i nil i ∆H r ° negatif, dengan demikian dapat disimpulkan bahwa reaksi berjalan secara eksotermis (menghasilkan panas).
Untuk mengetahui reaksi berjalan searah atau bolak-balik dapat dihitung dengan perubahan energi Gibbs sebagai berikut:
∆G° ∆G° produk - ∆G° reaktan
= ∆G f ° Na 2 O + ∆G f ° H 2 O) – ∆G f ° NaOH + ∆G f ° H 2 O)
= (-379,6 + 2(-228,61)) – (-379,4 + (-228,61)) = -228,81 kJ/mol
Untuk mengetahui nilai konstanta kesetimbangan (K) dengan rumus energi Gibbs:
K RT G
o ln
RT
K G
o
ln
=
ln K = 92,3
K = 1,2246x10 40
Untuk mencari K 2 (K pada temperatur reaksi) digunakan Smith Van Ness Equation (15.17)
(
) (
)
Pada suhu 220°C (493,15 K) besarnya konstanta kesetimbangan dapat dihitung sebagai berikut:
(
) (
)
( ) (
)
Karena harga konstanta kesetimbangan sangat besar yaitu maka reaksi berlangsung searah (irreversible).
Reaksi 2:
Na 2 O (l) + 2SiO 2(s) Na 2 Si 2 O 5(l)
Maka, ∆Hr 0 = ∑∆H f 0
produk - ∑∆H f 0
reaktan = ∆H f 0
Na 2 Si 2 O 5 ) – ∆H f 0
Na 2 O + ∆H f 0
SiO 2 ) = (-1606,279) – ((-416) + 2(-850,82))
= 511,36 kJ/mol
D ri erhi ung n, i nil i ∆H r 0
positif, dengan demikian dapat disimpulkan bahwa reaksi berjalan secara endotermis (membutuhkan panas).
Untuk mengetahui reaksi berjalan searah atau bolak-balik dapat dihitung dengan perubahan energi Gibbs sebagai berikut:
∆G° ∆G° produk - ∆G° reaktan
= ∆G f ° Na 2 Si 2 O 5 ) – ∆G f ° Na 2 O + ∆G f ° SiO 2 )
= (-1467,5) – ((-379,6) + 2(-856,3))
= 624,7 kJ/mol
Untuk mengetahui nilai konstanta kesetimbangan (K) dengan rumus energi Gibbs:
K RT G
o ln
RT
K G
o