TOKSIKOLOGI FORENSIK Alphonse Poklis
PENDAHULUAN
Toksikologi mempelajari mengenai racun, lebih spesifik lagi bersangkutan dengan sifat kimia dan fisika dari suatu bahan beracun dan efek fisiologisnya pada makhluk hidup, analisis kualitatif dan kuantitatif pada bahan biologis dan
nonbiologis, dan prosedur untuk mengobati keracunan. Racun adalah suatu substansi yang bila digunakan pada jumlah yang cukup dapat menyebabkan kesakitan atau kematian. Proses menelan air dalam jumlah besar dalam waktu yang lama, disebut polidipsia psikogenik, dapat terjadi dalam bentuk skizofrenia, menyebabkan ketidakseimbangan elektrolit yang fatal. Sebaliknya, tertelannya arsenik, sianida, dan racun lainnya dalam hitungan menit tidak menyebabkan toksisitas yang nyata. Paracelsus, seorang dokter pada abad ke-16 mengamati, “Semua zat adalah racun; tidak ada satu pun yang bukan racun. Dosis yang tepat membedakan racun dari obat.”
toksikologi forensik kemudian menafsirkan hasil untuk efek fisiologis dan / atau perilaku dari meracuni orang yang menjadi sampelnya. Hasil analisis jaringan otopsi dapat mengungkapkan bahwa orang tersebut meninggal karena keracunan. Pada pasien hidup, ditemukannya suatu zat dalam darah atau sampel urin dapat menjelaskan koma, kejang, atau perilaku aneh.
Penyelidikan lengkap adalah tanggung jawab penting untuk menetapkan penyebab kematian berdasar pemeriksa medis, koroner, atau ahli patologi, tetapi keberhasilan atau kegagalan dalam kedatangan pada kesimpulan yang benar sering tergantung pada upaya gabungan ahli patologi dan ahli toksikologi forensik. Keracunan sebagai penyebab kematian dibuktikan dengan analisis toksikologi yang menunjukkan adanya racun dalam jaringan atau cairan tubuh korban. Sebagian besar obat dan racun tidak dapat diamati langsung dalam jaringan tubuh, hanya dapat ditunjukkan oleh metode isolasi kimiawi dan identifikasi. Jika tidak dilakukan analisis toksikologi, suatu kematian dapat dianggap sebagai keracunan tanpa bukti yang pasti, atau kematian karena keracunan dapat secara salah dikaitkan dengan penyebab lainnya.
Pada kasus kematian bukan akibat keracunan, ahli toksikologi forensik dapat memberikan bukti tentang lingkungan terjadinya kematian. Perilaku mengemudi yang aneh pada korban kecelakaan lalulintas dapat diakibatkan adanya alkohol dalam darah atau jaringan. Obat-obatan psikoaktif, yang
memengaruhi perilaku, sering terkait dengan kematian mendadak atau kekerasan. Deteksi dari alkohol, narkotika, halusinogen, atau obat-obatan lain dapat
irasional dari orang yang meninggal pada saat insiden terjadi. Sebaliknya, hasil toksikologi negatif menggugurkan penggunaan narkoba. Temuan negatif juga penting pada pasien yang seharusnya rutin minum obat untuk mengendalikan kondisi patologis. Dalam kasus epilepsi, konsetrasi obat rendah atau negatif dapat menunjukkan orang yang meninggal tidak minum obatnya sehingga mengalami kejang yang fatal.
SEJARAH TOKSIKOLOGI FORENSIK
Hingga abad ke-19, dokter, pengacara, dan aparat penegak hukum memiliki gagasan yang salah tentang tanda dan gejala keracunan. Dahulu, dipercaya bahwa jika tubuh berwarna hitam, biru, atau "berbau busuk" maka disebabkan karena racun. Pemahaman lain addalah bahwa jantung orang yang diracuni tidak bisa dihancurkan oleh api, atau bahwa tubuh seseorang yang meninggal karena keracunan arsenik tidak akan membusuk. Pada awal abad ke-18, seorang dokter Belanda, Hermann Boerhoave, berteori bahwa berbagai racun dalam kondisi panas, dalam bentuk uap menghasilkan bau yang khas, sehingga melakukan pengujian zat yang dicurigai beracun dengan menempatkan zat tersebut di atas bara panas dan menguji baunya. Meskipun Boerhave tidak berhasil menerapkan metodenya, dia adalah yang pertama kali menyarankan metode kimia untuk membuktikan keberadaan racun.
merkuri). Selama masa Renaisans Prancis dan Italia, pembunuhan politik dengan racun dibangkitkan oleh Paus Alexander VI dan Cesare Borgia.
Penggunaan arsenik putih (arsenik trioksida) untuk pembunuhan digunakan luas di kalangan masyarakat umum dan disebut dengan "bubuk warisan". Popularitas tersebut adalah tonggak pertama isolasi kimia dan identifikasi racun dalam jaringan tubuh dan cairan yang berpusat pada arsenik. Pada 1775, Karl Wilhelm Scheele, ahli kimia Swedia terkenal, menemukan bahwa arsenik putih diubah menjadi asam arsenous oleh air klorin. Penambahan seng logam dapat mengurangi perubahan asam arsenous menjadi gas arsin beracun. Jika dipanaskan, gas yang terbentuk dapat menyimpan logam arsenik pada permukaan bejana dingin. Pada tahun 1821, Sevillas mengguakan dekomposisi arsin untuk mendeteksi arsenik yang terdapat pada isi perut dan urin dalam kasus-kasus keracunan. Pada tahun 1836, James M. Marsh, seorang ahli kimia di Royal British Arsenal di Woolwich, menggunakan gas arsin untuk mengembangkan metode pertama untuk menentukan racun yang diserap dalam jaringan dan cairan, tubuh seperti hati, ginjal, dan darah.
Tahun 1800 merupakan tahun perkembangan toksikologi forensik sebagai suatu disiplin ilmiah. Pada tahun 1814, Mathieiv J. B. Orfila (1787–1853), “bapak toksikologi”, menerbitkan Traité des Poisons - pendekatan sistemik pertama dalam penelitian sifat kimia dan fisiologis racun. Orfila berperan sebagai seorang saksi ahli dalam banyak percobaan pembunuhan terkenal, dan khususnya
merangsang minat populer dan ilmiah dalam sains. Sebagai Dekan Medis Fakultas di Universitas Paris, Orfila melatih banyak siswa di bidang forensic toksikologi.
Isolasi racun alkaloid pertama yang berhasil dilakukan pada tahun 1850 oleh Jean Servials Stas, seorang ahli kimia Belgia, menggunakan larutan asam asetat dietil alkohol untuk mengekstrak nikotin dari jaringan tubuh Gustave yang dibunuh Fougnie. Dimodifikasi oleh kimiawan Jerman, Friedrich Otto, Stas-Otto metode cepat diterapkan untuk isolasi berbagai racun alkaloid, termasuk kolkisin, konin, morfin, narkotin, dan strychnin; metode ini masih digunakan sampai sekarang.
Pada pertengahan kedua abad ke-19, para ahli toksikologi Eropa terkemuka dalam pengembangan dan penerapan ilmu forensik. Prosedur dikembangkan untuk mengisolasi dan mendeteksi alkaloid, logam berat, dan racun yang mudah menguap.
Di Amerika, Rudolph A. Witthaus, Profesor Kimia di Cornell Universitas Medical School, membuat banyak kontribusi untuk toksikologi dan melakukan analisis untuk New York City di beberapa kasus keracunan terkenal: pembunuhan Helen Potts oleh Carlyle Harris dan Annie Sutherland oleh Dr. Robert W.
Buchanan, keduanya menggunakan morfin. Pada tahun 1911, Tracy C. Becker dan Profesor Witthaus menyunting empat jilid karya tentang yurisprudensi medis, Kedokteran Forensik dan Toksikologi, buku teks forensik standar pertama yang diterbitkan di AS. Pada tahun 1918, Kota New York mendirikan sistem
Kontribusi Dr. Gettler pada sains terbesar adalah pelatihan dan pengarahannya pada pemimpin masa depan dalam toksikologi forensik.
Pada tahun 1949, Akademi Ilmu Forensik Amerika didirikan untuk
mendukung dan melanjutkan praktik semua tahap pengobatan hukum di AS. Para anggota bagian toksikologi mewakili sebagian besar forensik toksikologis yang bekerja di kantor koroner atau pemeriksa kesehatan. Beberapa yang lain
organisasi ilmu forensik internasional, nasional, dan lokal, seperti Society of Forensic Toxicologists dan California Association of Toxicologists, menawarkan forum untuk pertukaran data ilmiah yang berkaitan dengan analitis teknik dan laporan kasus yang melibatkan racun dan obat baru yang masih jarang digunakan. Asosiasi Internasional Ahli Toksikologi Forensik, didirikan di 1963, dengan lebih dari 750 anggota di 45 negara, memungkinkan kerjasama di seluruh dunia dalam menyelesaikan masalah teknis yang dihadapi ahli toksikologi.
Pada tahun 1975, Dewan Toksikologi Forensik Amerika memeriksa dan mengesahkan ahli toksikologi forensik. Salah satu tujuan yang dinyatakan adalah “untuk menyiapkan sistem peradilan, dan publik lainnya, sistem praktis dan adil untuk mengidentifikasi orang-orang yang mengaku spesialis dalam toksikologi forensik yang memiliki kualifikasi dan kompetensi yang diperlukan.” Secara umum, mereka yang disertifikasi harus memiliki gelar Doctor of Philosophy atau gelar Doktor dalam bidang ilmu sains, memiliki minimal 3 tahun penuh
KEMATIAN YANG DISELIDIKI OLEH AHLI TOKSIKOLOGI KERACUNAN YANG TIDAK DISENGAJA
Kecelakaan keracunan palimng banyakn terjadi di rumah. Anak-anak, karena rasa ingin tahu dan sifat petualang mereka, dapat memperoleh akses dan menelan obat, deterjen, pestisida, dan pembersih rumah tangga. Kesadaran akan penyimpanan bahan kimia rumah tangga yang aman, ketersediaan pusat-pusat informasi pengendalian racun, dan prosedur-prosedur ruang gawat darurat yang lebih baik untuk mengobati keracunan anak semuanya telah berkontribusi baik, ditandai dengan penurunan kematian. Keracunan tiddak disengaja pada orang dewasa biasanya karena salah pelabelan obat, penyimpanan zat beracun dalam wadah selain yang asli.
Keracunan yang tidak disengaja dapat terjadi di industri karena
kecerobohan atau kecelakaan yang mengekspos pekerja ke zat beracun. Sementara potensi keracunan yang tidak disengaja dalam industri adalah besar, standar dan peraturan keselamatan dan ketersediaan layanan medis darurat hari ini mencegah industri dari menjadi sumber dari banyak intoksikasi yang fatal.
KEMATIAN KARENA PENYALAHGUNAAN OBAT
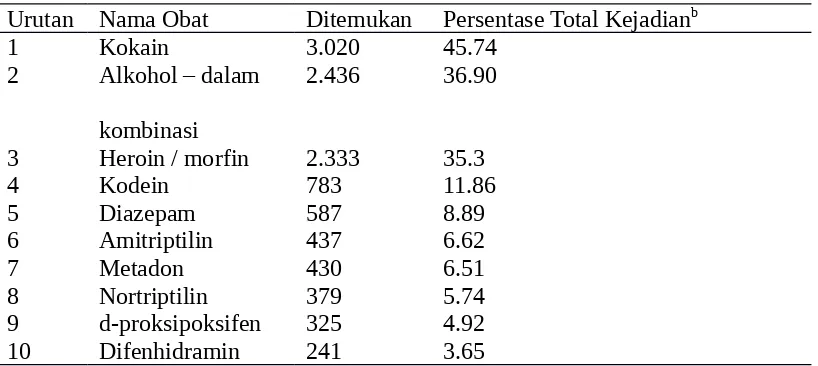
amfetamin; atau penggunaan bahan kimia dengan cara yang bertentangan dengan fungsi obat - seperti menghirup pelarut dan produk aerosol. Sejak perkembangan "budaya narkoba" pada pertengahan 1960-an, kematian disebabkan penggunaan obat terlarang adalah keracunan fatal yang paling umum yang diinvestigasi oleh ahli racun, khususnya di daerah perkotaan besar. Tabel 8.1 menyajikan obat-obatan yang paling sering ditemui dalam investigasi kematian; perhatikan tingginya insiden kokain, alkohol, dan heroin / morfin.
Dalam arti yang lebih luas, penyalahgunaan narkoba juga termasuk penggunaan yang berlebihan zat yang legal secara hukum, seperti alkohol dan obat resep. Penyalahgunaan alkohol adalah masalah narkoba terbesar di AS. Alkohol memainkan peran penting dalam kematian dengan kekerasan. Dari 40.000 kematian kecelakaan mobil yang terjadi setiap tahun di AS, 50%
Tabel 8.1
Obat yang Paling Sering Ditemukan pada Pemeriksaan Kesehatan, 1991a
Urutan Nama Obat Ditemukan Persentase Total Kejadianb
1 Kokain 3.020 45.74
2 Alkohol – dalam kombinasi
2.436 36.90
3 Heroin / morfin 2.333 35.3
4 Kodein 783 11.86
a Drug Abuse Warning Network, data dari 27 area maju berdasar Institusi nasional
penyalahgunaan obat
b Persentase dari total kejadian dapat mencapai 100%, karena satu kasus dapat
melibatkan lebih dari satu jenis obat
BUNUH DIRI DENGAN RACUN
Bunuh diri dengan racun adalah kasus yang umum terjadi, kasus bunuh diri berhasil pada pria sebanyak dua kali dibanding pada wanita. Namun
yang menderita depresi dan gangguan emosional lainnya biasanya memiliki persediaan obat yang banyak, bunuh diri melibatkan beberapa konsumsi obat; biasanya tiga hingga tujuh obat yang berbeda dicerna pada satu waktu. Dengan menganalisa lambung dan isi usus, darah, urin, dan organ utama tubuh, ahli toksikologi dapat menentukan jumlah minimum racun yang tertelan. Dalam kasus bunuh diri, hasil analisis tersebut menunjukkan kuantitas dosis besar; sehingga membuktikan bahwa orang yang meninggal sengaja mengambil dosis tersebut.
KERACUNAN YANG MEMBUNUH
Keracunan yang tidak sengaja dan bunuh diri dengan racun sangat umum terjadi, membunuh dengan racun jarang terjadi. Menentukan bahwa seseorang meninggal sebagai akibat racun yang bersifat membunuh menjadi investigasi yang paling sulit untuk petugas penegak hukum dan ahli medis. Bukti umum keracunan diperoleh dari pengetahuan tentang gejala yang ditampilkan oleh orang yang meninggal sebelum kematian, pemeriksaan postmortem tubuh oleh ahli patologi, isolasi dan identifikasi racun oleh ahli toksikologi. Untuk menuntut tersangka, petugas penegak hukum harus menetapkan bahwa pelaku memiliki akses ke pasokan racun, mengetahui efek racun yang mematikan, dan bahwa tersangka punya kesempatan memberikan racun pada orang yang meninggal.
sering terjadi di dalam rumah, jarang ada gejala keracunan yang tidak terduga diakibatkan oleh penyakit tertentu seperti muntah, diare, kolaps dengan cepat, dan lemahnya nadi, semua gejala keracunan arsenik, mungkin juga disebabkan oleh ulkus lambung pecah atau peradangan pankreas atau usus buntu. Demikian juga, strychnine dan tetanus menyebabkan kejang. Pupil yang mengecil dan narkosis mungkin berasal dari obat narkotika atau lesi pada otak. Namun, terdapat keadaan yang membuat diagnosis keracunan cukup pasti. Onset dan perkembangan gejala kematian cepat segera setelah makan atau minum menunjukkan keracunan akut, keracunan makanan dari bakteri memiliki onset gejala yang tertunda.
Ahli patologi dapat mengenali efek racun tertentu pada otopsi. Asam kuat dan alkali dapat menyebabkan luka bakar yang luas di sekitar mulut atau
permukaan tubuh, dengan kerusakan berat pada jaringan internal. Racun metalik dapat menyebabkan kerusakan intensif pada saluran pencernaan, hati, dan ginjal. Fosfor, hidrokarbon terklorinasi, dan jamur beracun menyebabkan degenerasi lemak pada hati. Namun, sebagian besar racun tidak menghasilkan perubahan yang dapat diamati dalam jaringan tubuh; karenanya, dalam banyak contoh keracunan, nilai pemeriksaan ahli patologi tubuh adalah menetapkan bahwa kematian bukan karena penyebab alami atau cedera traumatis dan bahwa tidak ada bukti penyebab kematian kecuali dari kemungkinan keracunan. Di kebanyakan kasus, analisis toksikologi menghasilkan bukti pembunuhan dengan racun.
INVESTIGASI TOKSIKOLOGI DARI KEMATIAN AKIBAT RACUN
1. Memperoleh riwayat kasus dan spesimen yang sesuai 2. Analisis toksikologi
3. Interpretasi hasil analisis
RIWAYAT KASUS DAN SPESIMEN
Terdapat ribuan senyawa yang mematikan jika dicerna, disuntikkan, atau dihisap. Ahli toksikologi hanya terbatas jumlah bahan yang digunakan untuk melakukan analisisnya; oleh karena itu, sangat penting bahwa sebelum memulai analisis, diberikan sebanyak mungkin informasi mengenai fakta pendukung kasus seperti usia, jenis kelamin, berat badan, riwayat medis, dan pekerjaan orang yang meninggal, serta setiap perawatan yang diberikan sebelum kematian, temuan otopsi kotor, obat yang tersedia untuk orang yang meninggal, dan interval waktu antara onset gejala dan kematian. Pada tahun tertentu, laboratorium toksikologi akan melakukan analisis pada jaringan untuk racun sebagai obat resep (analgesik, antidepresan, hipnotik, penenang), obat yang disalahgunakan (halusinogen, narkotika, stimulan), produk komersial (antibeku, produk aerosol, insektisida, rodentisida, gosok senyawa, pembunuh gulma), dan gas (karbon monoksida, sianida). Identitas yang mungkin menjadi racun sebelum analisis akan sangat membantu.
seluruh tubuh, dan ahli toksikologi awalnya menganalisis organ-organ yang diperkirakan memiliki konsentrasi obat tertinggi, Gambar 8.1. Sejumlah besar setiap spesimen diperlukan untuk analisis toksikologi menyeluruh karena prosedur mengekstrak dan mengidentifikasi satu senyawa atau kelas senyawa mungkin tidak efektif dalam mengekstraksi atau mengidentifikasi.
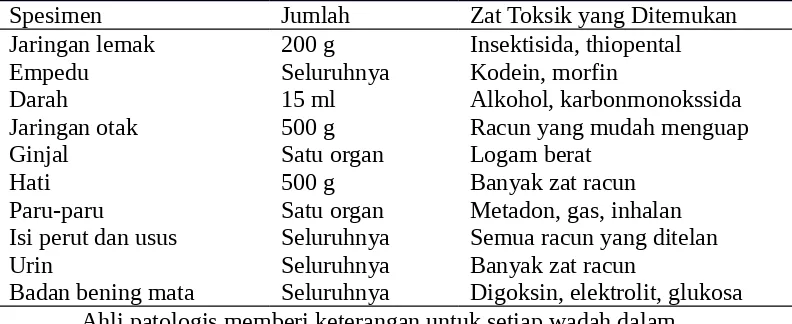
Tabel 8.2 Barang Bukti yang Terkumpul pada Otopsi untuk Analisis Toksikologi
Spesimen Jumlah Zat Toksik yang Ditemukan
Jaringan lemak 200 g Insektisida, thiopental
Empedu Seluruhnya Kodein, morfin
Darah 15 ml Alkohol, karbonmonokssida
Jaringan otak 500 g Racun yang mudah menguap
Ginjal Satu organ Logam berat
Hati 500 g Banyak zat racun
Paru-paru Satu organ Metadon, gas, inhalan
Isi perut dan usus Seluruhnya Semua racun yang ditelan
Urin Seluruhnya Banyak zat racun
Badan bening mata Seluruhnya Digoksin, elektrolit, glukosa Ahli patologis memberi keterangan untuk setiap wadah dalam pengambilan sampel, yaitu tanggal dan waktu otopsi, nama orang yang
meninggal, identitas sampel, dan tanda tangan ahli patologi. Ahli toksikologi, saat menerima spesimen, memberi ahli patologi tanda terima tertulis dan menyimpan spesimen di kulkas terkunci sampai analisis. Prosedur ini memadai untuk
ANALISIS TOKSIKOLOGI
Sebelum memulai analisis, seorang ahli toksikologi harus
mempertimbangkan : jumlah specimen yang tersedia, sifat racun yang akan dicari, dan kemungkinan biotransformasi dari racun. Oleh karena jumlah spesimen terbatas, maka harus mengikuti prosedur analisis yang disesuaikan dengan jumlah sampel. Gambar 8.2 menguraikan skema untuk isolasi pada senyawa yang tidak diketahui. Dalam kasus yang melibatkan pemberian racun oral, isi gastrointestinal dianalisis pertama kali, karena sejumlah besar residu racun yang tidak terserap mungkin ditemukan. Urin dapat dianalisis selanjutnya karena ginjal adalah organ utama ekskresi untuk sebagian besar racun sehingga konsentrasi racun yang tinggi sering ada dalam urin. Selanjutnya penyerapan dari saluran cerna, obat-obatan atau racun pertama kali dibawa ke hati sebelumnya memasuki sirkulasi sistemik umum; Oleh karena itu, analisis pertama dari suatu organ internal dilakukan pada hati. Jika racun tertentu dicurigai atau diketahui terlibat dalam kematian, ahli toksikologi memilih untuk menganalisis terlebih dahulu jaringan dan cairan di mana racun terkonsentrasi paling banyak.
bahwa obat atau racun telah diberikan sebelumnya. Bukti heroin atau kokain penggunaan ditunjukkan dengan adanya metabolitnya masing-masing, morfin dan benzoylekgonin.
Ahli toksikologi harus menyadari perubahan kimia normal yang terjadi selama dekomposisi tubuh. Otopsi atau analisis toksikologi harus dimulai segera setelah kematian karena proses dekomposisi dapat menghancurkan racun yang ada pada awalnya atau dapat menghasilkan zat atau senyawa dengan sifat kimia atau fisik yang mirip dengan racun. Sebagai contoh, selama dekomposisi, fenilalanin, asam amino yang biasanya ada dalam tubuh, diubah menjadi phenylethylamine, yang memiliki sifat kimia dan fisik yang sangat mirip untuk amfetamin.
Kandungan etil alkohol dan sianida darah mungkin menurun atau meningkat tergantung pada tingkat pembusukan dan mikroba aktivitas. Namun, banyak racun, seperti arsenik, barbiturat, merkuri, dan strychnine, mungkin masih bisa dideteksi bertahun-tahun setelah kematian.
Dalam penyelidikan keracunan, pertama-tama diperlukan ahli toksikologi untuk mengisolasi dan mengidentifikasi racun. Oleh karena itu, toksikologi forensik sesuai dengan metode yang digunakan sebaiknya mengisolasi zat dari jaringan tubuh atau cairan.
Kelompok I: Gas
Kelompok II: Steam Volatile Poisons
Senyawa dalam kelompok ini diisolasi oleh distilasi uap. Contoh (darah, urin, atau homogenat jaringan) dibuat asam dengan asam klorida atau basa dengan magnesium oksida padat. Racun yang dapat disuling dari media asam termasuk karbon tetraklorida, kloroform, sianida, etanol, metanol, fenol, nitrobenzen, dan kuning fosfor. Racun yang bisa disuling dari media basa termasuk amfetamin, anilin, meperidin, metadon, dan nikotin.
Kelompok III: Racun Metalik
Logam diisolasi dari jaringan dengan menghancurkan semua bahan organik. Jaringan dapat dihancurkan oleh panas yang berlebihan (kering) atau direbus dengan asam pekat atau oksidator kuat (ashing basah). Berbagai metode dapat digunakan untuk mengidentifikasi racun logam tertentu yang tersisa di dalam abu jenazah.
Kelompok IV: Racun Organik yang Tidak Mudah Menguap
Senyawa dalam kelompok ini biasanya hadir dalam jaringan hanya dalam hitungan menit. Beberapa obat (misalnya, barbiturat) dapat langsung diekstrak dari jaringan oleh pelarut organik. Namun, banyak senyawa terpisah dari sebagian besar matriks jaringan menjadi filtrat bebas protein di jaringan. Filtrat ini
kondisi keasaman. Menggunakan teknik tersebut, obat-obatan diisolasi menjadi lima kelompok :
1. Asam kuat (misalnya, chlorothiazide, salisilat) 2. Asam lemah (misalnya, acetaminophen, barbiturat) 3. Netral (mis., Meprobamate, methaprylon)
4. Basa (mis., Kodein, phenothiazines, quinine, strychnine) 5. Amfoterik (mis., Hidromorfon, morfin)
Kelompok V: Racun jenis lain
Kelompok ini mencakup semua racun yang tidak diklasifikasikan dalam empat kelompok sebelumnya. Zat yang termasuk dalam kelompok ini adalah anion anorganik (Bromin), ion organik yang larut dalam air (kurare, fluoroasetat, parkuat), dan senyawa organik yang tidak larut dalam air atau alkohol.
Membutuhkan teknik khusus untuk mengisolasi dan mengidentifikasi senyawa-senyawa ini dari sampel biologis.
Uji Warna
Tes warna adalah prosedur kimia di mana zat yang diuji menyebabkan perubahan dalam reagen, sehingga menghasilkan perubahan warna yang bisa diamati. Tes warna dapat digunakan untuk menentukan kehadiran senyawa spesifik atau komponen utama zat tersebut. Prosedur cepat dan mudah dilakukan. Utilitas warna terbesar tes dalam toksikologi adalah pemeriksaan urin, karena dapat dianalisis secara langsung tanpa prosedur ekstraksi. Sebuah contoh uji warna adalah “Tes Trinder” untuk mendeteksi salisilat di dalam darah atau urin. Reagen dari besi nitrat dan merkuri klorida dicampur dengan 1 ml darah atau urin; jika ada salisilat, terjadi perubahan warna menjadi ungu. Tes Trinder positif diamati untuk asam salisilat (metabolit aspirin), salisilamida, dan metil salisilat sehingga harus dikonfirmasi dengan uji lainnya. Positif palsu, yaitu terjadi perubahan warna tanpa adanya senyawa salisilat, dapat ditemukan pada urin pasien diabetes yang mengekskresi asam asetoasetat dan pada konsumen dosis tinggi fenotiazin.
Tes Mikrodifusi
reagen atau pelarut di mana zat volatil tertentu akan mudah larut. Setelah sampel dan absorben ditambahkan ke sel yang tepat, piringan disegel dengan bahan penyegel dan pelat penutup. Jika dipanaskan, racun yang mudah menguap akan berdifusi dari sampel ke atmosfer dan terperangkap oleh larutan penyerap berupa reagen warna. Saat racun terlepas dari sampel, dapat diamati
pembentukan/perubahan warna dalam absorben. Zat yang dapat dideteksi antara lain acetaldehyde, karbon monoksida, sianida, etanol, fluorida, hidrokarbon terhalogenasi, dan metanol.
Kromatografi
Kromatografi adalah teknik pemisahan. Komponen campuran sampel didistribusikan antara dua fase, fase tetap dan fase gerak yang akan merembes melalui matriks atau di atas permukaan fase tetap. Komponen tersebut
senyawa diketahui. Ada banyak jenis analisis kromatografi namun, hanya tiga yang paling sering diterapkan oleh ahli toksikologi, yaitu kromatografi lapis tipis (TLC), kromatografi cair gas (GLC), dan kromatografi cair kinerja tinggi (HPLC) Kromatografi Lapis Tipis
Pada jenis ini, fase tetap adalah "lapisan tipis" dari penyerap, biasanya silika gel, yang tersebar seperti plat kaca. Ekstrak sampel terkonsentrasi dan standar obat diterapkan sebagai serangkaian bintik di sepanjang bagian bawah plat dan dibiarkan kering, kemudian ditempatkan dalam tangki tertutup, di mana lapisan penyerap menyebabkan kontak dengan "pelarut pengembang" (fase gerak) di bawah tempat yang diterapkan. Pelarut bergerak ke atas plat melalui kapiler, melarutkan dan memisahkan komponen dari ekstrak. Ketika pelarut telah mencapai bagian atas plat atau naik ke jarak yang telah ditentukan sebelumnya, pelat dihapus dari tangki dan pelarut menguap dari plat. Setiap zat dari obat akan terpisah selama migrasi, menghasilkan serangkaian bintik atau pita sempit yang membentang dari bawah ke atas atau pada pelarut. Migrasi senyawa diekspresikan oleh faktor retensi (Rf) yang didefinisikan sebagai rasio jarak yang dipindahkan oleh senyawa ke jarak fase gerak naik plat dari titik penerapan senyawa.
Kehadiran obat divisualisasikan dengan menyemprot atau mencelupkan ke plat berbagai reagen yang menghasilkan warna reaksi dengan komponen tertentu. Beberapa obat akan bereaksi dengan reagen tetapi tidak dengan yang lain.
primer seperti amfetamin atau efedrin. Selanjutnya, ia dapat mengaplikasikan etanol dalam sulfur asam, yang menghasilkan serangkaian warna merah muda, oranye, biru, atau hijau yang cerah bintik-bintik dengan obat penenang fenotiazin dan metabolitnya. Plat mungkin kemudian disemprot dengan iodoplatinat, yang bereaksi dengan semua basa nitrogen.
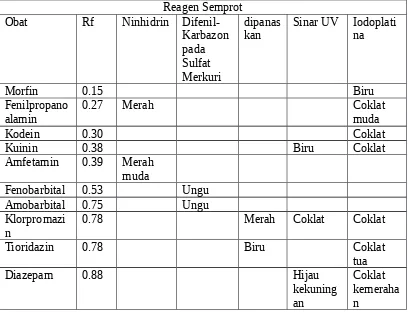
Ada banyak reagen semprot TLC, tetapi ahli toksikologi harus dipandu oleh sifat kimia dari senyawa yang ingin dikenali. Setelah identifikasi tentatif dari senyawa didapatkan, selanjutnya dikonfirmasi oleh tes kimia lain. Tabel 8.3 menyajikan Rfs dan reaksi dengan reagen visualisasi beberapa obat yang biasanya dicari dalam skrining toksikologi.
Tabel 8.3 Data Kromatografi Lapis Tipis untuk Beberapa Obat yang Sering Dicari Reagen Semprot
alamin 0.27 Merah Coklat muda
Kodein 0.30 Coklat
n 0.78 Merah Coklat Coklat
Tioridazin 0.78 Biru Coklat
Amitriprilin 0.98 Biru Coklat muda
Kromatografi Gas Cair
Pada jenis ini, fase gerak adalah pembawa gas inert (misalnya, helium, nitrogen) yang mengalir melalui kolom yang dikemas dengan packed column atau lebih dari satu fase tetap melapisi dinding kolom kapiler. Terdapat banyak jenis bahan cair yang tersedia, variasi fase tetap tergantung pada sifat senyawa atau kelompok senyawa yang ingin diidentifikasi. Sampel yang diekstraksi akan diuapkan dan dibawa melalui kolom oleh gas ke detektor, yang menghasilkan sinyal elektronik yang diperkuat dan ditampilkan pada perekam. Migrasi senyawa melalui kolom biasanya diekspresikan oleh waktu retensi (Rt), yaitu waktu antara injeksi sampel dan deteksi senyawa. Waktu retensi memberikan identifikasi tentatif dari senyawa, dan kekuatan sinyal elektronik ke perekam dapat digunakan untuk menentukan jumlah senyawa yang ada dalam sampel. Ekstrak spesimen pada kondisi yang sama seperti referensi dan menghasilkan waktu puncak pada saat yang sama dapat menjadi referensi obat dalam spesimen. Ketinggian puncak dan area di bawah puncak secara langsung berkaitan dengan konsentrasi obat yang ada. Kromatografi gas sangat cocok untuk analisis zat yang mudah menguap seperti alkohol.
Kromatografi Cair Kinerja Tinggi
jenis bahan stasioner tersedia, dan ahli toksikologi dapat menggunakan hampir semua pelarut atau banyak air campuran sebagai fase cair. Oleh karena itu, prosedur khusus dapat dikembangkan untuk memisahkan senyawa yang tidak mudah diatasi dengan metode kromatografi lainnya. Metode ini sangat cocok untuk senyawa yang mudah terbakar panas, yang dapat terdekomposisi ketika diuapkan untuk pemisahan GLC. Seperti pada GLC, obat dapat diidentifikasi dari Rt, dan respon detektor sesuai dengan konsentrasi obat yang ada dalam sampel.
Spektroskopi
Spektroskopi menyangkut penyerapan atau produksi energi radiasi. Menyerap radiasi adalah karakteristik semua molekul; Namun, panjang
dengan memilih panjang gelombang penyerapan maksimum, konsentrasi suatu senyawa yang ada dalam sampel dapat ditentukan.
Spektrofotometer digunakan untuk mengukur penyerapan energi radiasi terdiri dari sumber radiasi, sel sampel yang dilalui radiasi melewati, dan detektor untuk mengukur penyerapan radiasi. Instrumen komersial yang digunakan untuk mengukur penyerapan bentuk-bentuk cahaya ini bervariasi dari kolorimeter sederhana, digunakan untuk mengukur penyerapan dalam rentang yang terlihat, untuk spektrofotometer yang sangat canggih menggunakan cahaya monokromatik dan elektronik sensitif untuk mendeteksi, memperkuat, dan merekam tingkat radiasi rendah.
Penyerapan sinar ultraviolet (UV) dapat menghasilkan transisi elektronik dalam molekul organik, menyebabkan perpindahan elektron dari energi rendah ke orbit berenergi tinggi. Panjang gelombang sebenarnya dari penyerapan maksimum tergantung kelompok kimia yang ada dalam molekul, pelarut di mana senyawa terlarut, pH, dan suhu larutan. Larutan berair dan alkohol adalah pelarut yang paling umum digunakan oleh ahli toksikologi. Plotting atau grafik elektronik absorbansi senyawa dibandingkan dengan panjang gelombang (210-350 nm) menghasilkan penyerapan ultraviolet spektrum. Kebanyakan obat untuk
di 263, 257, dan 252 nm. Keterbatasan ini dapat diatasi dengan memisahkan senyawa dengan HPLC dan kemudian merekam spektrum UV sebagai obat yang terisolasi. Konsentrasi obat ditentukan dengan membandingkan besar daya serap pada panjang gelombang maksimal dengan serangkaian konsentrasi standar obat murni yang dianalisis di bawah kondisi eksperimen yang sama.
Spektrometri massa
Dalam spektrometri massa, sampel ditembak dengan berkas elektron yang menghasilkan molekul bermuatan atau menghancurkan sampel menjadi fragmen ionik dari sampel asli, partikel bermuatan dipisahkan dan dideteksi menurut massa atomnya. "Spektrum massa" adalah tampilan dari fragmen massa-ke-muatan yang berbeda yang dihasilkan dan kelimpahan relatif. Pola fragmentasi dari molekul kompleks menghasilkan spektrum karakteristik yang sangat spesifik. Identifikasi triazolam didasarkan pada ion molekuler pada 343, pola fragmentasi mass-to-charge (m / e) karakteristik, dan kelimpahan relatif masing-masing ion. Misalnya: 313 m / e, kelimpahan 100; 238 m / e, kelimpahan 87; 75 m / e, kelimpahan 60; 342m / e, kelimpahan 50; dan seterusnya. Umumnya, tujuh kecocokan sampel yang tidak diketahui dibandingkan dengan standar referensi cukup untuk identifikasi. Meskipun prinsipnya ssederhana, instrumentasi yang digunakan untuk menghasilkan spektra massa sangat kompleks.
menampilkan spektrum massa yang dihasilkan dan secara otomatis mencari spektrum yang tersimpan dari senyawa yang diketahui untuk mengidentifikasi sampel yang tidak diketahui.
Immunoassay
Merupakan teknik yang membutuhkan antibodi yang berikatan erat dengan obat yang spesifik. Terdapat tiga sistem yang tersedia secara komersial dan
digunakan dalam toksikologi forensik: enzyme multiplied immunoassay technique (EMIT), fluorescent polarization immunoassay (FPIA), dan radioimmunoassay (RIA). Sebuah immunoassay terdiri dari campuran antibodi spesifik obat dan antibodi disiapkan. "Label" mungkin atom radioaktif (RIA), atau senyawa fluorescent yang melekat secara kimiawi (FPIA), atau enzim (EMIT). Ketika sampel mengandung obat ditambahkan ke campuran, bersaing dengan "label obat" untuk mengikat antibodi. Kehadiran obat yang dicari ditunjukkan oleh perubahan radioaktivitas (RIA), fluorescence polarization (FPIA), atau reaksi enzim (EMIT). Teknik-teknik ini dapat digunakan untuk analisis kualitatif dan kuantitatif, cepat dan mudah diterapkan, sampel dapat dianalisis secara langsung tanpa ekstraksi sebelumnya. Teknik immunoassay sangat berguna dalam skrining racun dalam spesimen biologi seperti urin. Teknik ini sangat spesifik untuk obat atau kelas obat tertentu, karena obat adalah satu-satunya antigen yang akan bereaksi atau
Interpretasi Hasil
Setelah analisis spesimen selesai, dilakukan interpretasi hasil mengenai efek fisiologis dari zat racun pada jenazah pada konsentrasi yang ditemukan. Pertanyaan khusus tentang jalur masuk, konsentrasi racun cukup atau tidak untuk menyebabkan kematian atau melibatkan tindakan orang yang meninggal untuk berkontribusi sampai kematiannya, harus dapat dijawab. Masalah yang paling sulit adalah untuk menilai makna fisiologis hasil analisis.
Dalam menentukan jalur masuk, dievaluasi hasil analisis berbagai spesimen. Sebagai aturan umum, konsentrasi racun tertinggi akan ditemukan di jalur masuk. Adanya sejumlah besar obat dalam saluran cerna dan hati
menunjukkan konsumsi oral, konsentrasi yang tinggi di paru-paru menunjukkan inhalasi, dan konsentrasi racun yang tinggi di jaringan di sekitar tempat suntikan menunjukkan suntikan intramuskular. Injeksi intravena mengantarkan obat langsung ke sirkulasi sistemik, melewati efek konsentrasi awal di hati.
Adanya bahan beracun di saluran pencernaan tidak membuktikan agen tersebut adalah penyebab kematian. Harus ditunjukkan telah terjadi penyerapan racun, dibawa ke sirkulasi umum menuju organ yang akan memberikan efek yang fatal. Kecuali bahan kimia korosif kuat dengan efek merusak langsung jaringan, sehingga menyebabkan perdarahan dan syok. Contohnya adalah hidroklorik terkonsentrasi dan sulfur asam, alkali, dan fenol.
dengan berbagai faktor yang mempengaruhi tingkat ekskresi senyawa spesifik dan volume urin.
Efek fisiologis sebagian besar obat dan racun berkorelasi dengan konsentrasi dalam darah dan menetapkan bahwa penyerapan telah terjadi. Oleh karena itu, konsentrasi darah seringkali merupakan indikator toksisitas terbaik; akibatnya, darah adalah spesimen yang paling berharga bagi ahli toksikologi.
konsentrasi racun yang efeknya dapat menyebabkan kematian didapatkan pada kasus-kasus yang terdokumentasi dan diselidiki dengan baik.
Pada kasus tertentu, ahli toksikologi dapat membedakan keracunan akut atau kronis. Sebagai contoh, rambut adalah spesimen pilihan untuk diagnosis paparan arsenik kronis. Arsenik yang beredar di darah disimpan di folikel rambut, di mana ia terperangkap oleh keratin dan mengangkat folikel di rambut yang sedang tumbuh. Sel-sel germinal dari rambut dalam ekuilibrium yang relatif dekat dengan arsenik yang beredar, konsentrasi arsenik dalam darah naik atau turun, demikian juga jumlah arsenik yang disimpan di rambut yang sedang tumbuh. Rambut tumbuh sekitar 0,4 hingga 0,5 mm / hari atau sekitar setengah inci (12,5 mm) per bulan. Oleh karena itu, analisis segmen 1,0 cm atau kurang menunjukkan pemaparan bulanan. Kandungan arsenik normal dari rambut bervariasi dengan faktor gizi, lingkungan, dan fisiologis; Namun, batas atas maksimum pada orang yang tidak terkena arsenik adalah sekitar 5 ppm. Setelah seseorang tidak terpapar arsenik, nilai pada rambut kembali normal dalam beberapa minggu.
Faktor-faktor yang dapat mempengaruhi respon seseorang terhadap suatu konsentrassi racun yang diberikan meliputi usia, jenis kelamin (status normal), berat badan, kematangan, dan status gizi, genetik, dan imunologi. Penyakit atau kondisi patologi organ tertentu dan aktivitas sistem saraf pusat (depresi, stres, dll.) harus dipertimbangkan. Faktor tambahan yang sering mempersulit interpretasi adalah fenomena farmakologis dari "toleransi". Toleransi adalah keadaan
pengembangan toleransi, adaptasi sel adalah yang paling bermasalah bagi ahli toksikologi. Adaptasi sel adalah bentuk toleransi yang semakin meningkat pada darah atau jaringan obat diperlukan konsentrasi lebih tinggi untuk memperoleh respon farmakologis obat terseebut. Sebagai contoh, pecandu narkoba dapat secara teratur mengambil dosis metadon yang bagi mereka tidak menghasilkan depresi sistem saraf pusat, sementara dosis yang sama dapat menyebabkan kematian pada seseorang yang tidak secara teratur menerima opiat.
Faktor-faktor yang mempengaruhi konsentrasi darah atau jaringan berhubungan dengan sifat senyawa dan susunan biologis individu. Komposisi kimia dan karakteristik fisik suatu bahan sering mempengaruhi toksisitasnya. Sebagai contoh, garam hidroklorida atau oksida dari logam tertentu jauh lebih banyak larut dalam saluran pencernaan dan lebih cepat diserap daripada garam sulfida. Secara umum, semakin cepat penyerapan suatu agen, semakin tinggi konsentrasi darah. Sediaan farmasi dapat diformulasikan dalam sedemikian rupa sehingga, dapat diatur setelah ditelan, obat diserap dengan cepat atau lambat. Faktor biologis yang terutama mempengaruhi konsentrasi darah adalah pengikatannya dengan protein jaringan dan laju biotransformasi dari racun. Tingkat biotransformasi suatu zat secara genetik terkontrol dan sering mengikuti variasi individu yang signifikan. Jika beberapa individu diberi dosis obat yang sama per berat badan, konsentrasi darah masing-masing dapat sangat bervariasi karena perbedaan tingkat biotransformasi obat tersebut.
morfin, melalui empedu dan feses. Meskipun bukan merupakan rute utama ekskresi, sebagian besar racun disekresi tubuh melalui: air susu, keringat, dan air mata. Rute utama ekskresi sebagian besar racun melalui urin. Tingkat eliminasi racun melalui urin sangat mempengaruhi jumlahnya dalam darah atau jaringan. Ekskresi urin tergantung pada volume dan keasaman urin. Secara teoritis, dapat dihasilkan perubahan sepuluh kali lipat eliminasi asam lemah atau basa dengan mengubah keasaman satu pH urin.
Setelah meninjau riwayat kasus, dengan mempertimbangkan faktor toksisitas, distribusi, dan biotransformasi dan membandingkan hasil analitik dengan kasus serupa yang pernah dilaporkan dalam literatur profesional atau kasus serupa dari pengalamannya sendiri, ahli toksikologi dapat memberikan interpretasi terhadap suatu kasus.
Ahli Toksikologi sebagai Saksi Ahli
Toksikologi forensik sering dipanggil untuk memberi kesaksian di
pengadilan terkait dengan atau temuan analitisnya dan interpretasinya. Meskipun hanya beberapa yang memiliki gelar medis, diizinkan untuk memberikan
pernyataan di pengadilan tentang efek obat atau racun pada tubuh manusia. Ahli toksikologi harus terlebih dahulu menetapkan bahwa telah disusun rantai
prosedur, dan batasan semua uji yang dilakukan. Interpretasinya harus sesuai ilmu pegetahuan dan pengalaman sendiri pada kasus serupa. Meskipun terdapat
ketidakcocokan dengan ahli di lapangan, semua kesimpulan harus berdasar ilmiah atau pengetahuan medis. Seperti semua saksi ahli, ahli toksikologi forensik harus menyajikan semua kesaksian dengan kejujuran dan integritas. Tidak ada yang mengetahui semua hal tentang bidang medis atau ilmiah tertentu. Kesaksian yang sukses di pengadilan dapat menegakkan keadilan; paling buruk, mungkin