Potensi Fitoremediasi Dan
Constructed Wetland
Pada Pengolahan
Limbah Cair Industri Kulit Samak
Febriani Purba
Departemen Teknologi Industri Pertanian, Institut Pertanian Bogor
PENDAHULUAN
Latar belakang
Industri kulit samak merupakan salah satu industri yang tidak ramah lingkungan. Hal ini karena banyaknya jumlah limbah padat dan cair yang dihasilkan. Dalam setiap pengolahan 1 ton kulit mentah menjadi kulit samak dibutuhkan sekitar 50-150 liter air dan sekitar 300 kg bahan kimia. Bahan kimia yang biasa digunakan pada proses produksi adalah kromium, sulfat, sodium sulfat, kapur, ammonium sulfat, sodium klorida, asam sulfat, formaldehid, pigment, pewarna, dan bahan antijamur Bahan-bahan kimia ini membuat intensitas racun yang dihasilkan per unit output tinggi (Khan 2001). Di Indonesia kromium merupakan bahan penyamak yang banyak digunkan karena harganya yang murah, proses penyamakan yang cepat, serta menghasilkan kulit samak yang stabil.
Membuang langsung limbah cair penyamakan kulit tanpa melalui pengolahan terlebih dahulu dapat menyebabkan masalah lingkungan serius karena kandungan COD, BOD, kromium dan pewarna yang tinggi (Song et al. 2000). Limbah cair industri kulit samak mengandung sekitar 500-1000 ppm kromium (Aravindhan et al. 2004). Kromium dapat meracuni hewan dan tanaman (Chidambaran et al. 2009).
Biaya pengolahan limbah cair industry kulit samak tergolong mahal sehingga banyak negara berkembang yang menggunakan pengolahan primer dan/atau sekunder berupa proses biologis dan pysico-kimia seperti, pertukaran ion resin (ion exchange), reverse osmosis, sistem elektrolisis, precipitation, koagulasi dan adsorpsi (Kacaoba et al. 2002, Hafez
et al. 2002). Sistem pengelolaan ini biasanya mahal dan menghasilkan polutan sekunder serta tidak efektif secara ekonomi bagi industry skala kecil dan menegah padahal menurut data Asosiasi Pengusaha Kulit Samak Indonesia sebanyak 75% industri kulit samak di Indonesia merupakan industry skala kecil dan menegah. Oleh sebab itu dibutuhkan teknik pengelolaan limbah cair yang lebih sederhana dan murah.
Pengolahan limbah cair dengan
constructed wetland merupakan teknik yang banyak dilakukan karena efisisien, murah dan powerful (Lu et al. 2016). Sistem constructed wetland (CW) telah banyak digunakan untuk mengolah berbagai bentuk limbah cair, seperti limbah industri, limbah rumah tangga pedesaan, limbah rumah tangga perkotaan dan nonpoint-source pollutant
Tujuan
Paper ini bertujuan untuk mengulas potensi pengolahan limbah cair industry penyamakan kulit dengan teknik fitoremediasi dan constructed wetland.
PEMBAHASAN
Karakteristik Limbah Cair Industri Kulit Samak
Limbah cair industry penyamakan kulit pada umumnya berwarna keruh dan berbau tidak sedap, karena umumnya mengandung sisa-sisa daging serta darah, bubur kapur, bulu halus, protein terlarut, sisa garam, asam, sisa cat dan zat samak krom (Yazid et al. 2007). Kromium (Cr) merupakan logam dengan nilai oksidasi mulai 2+ sampai 6+ Cr, namun biasanya ada sebagai kromium trivalen Cr (III) dan kromium heksavalen Cr (VI) (Cheung et al.
2007). Kromium dalam bentuk Cr(VI) memiliki tingkat toksisitas yang paling tinggi sekitar 10 sampai 100 kali dari Cr(III) (Chauhan et al. 2015). The United States Environmental Protection Agency telah menggolongkan Cr6 + sebagai salah satu
dari 17 bahan kimia beracun bagi manusia. Hal ini dianggap sebagai salah satu dari 20 kontaminan yang perlu ditangani sebelum di buang ke lingkungan. Karakteristik limbah cair industry penyamakan kulit dari beberapa hasil penelitian oleh peneliti terdahulu disajikan pada Gambar 1.
Tabel 1 Kandungan zat kimia limbah cair Parameter Singgih
et al.
Tanaman merupakan paru-paru alam yang memilikim kemampuan untuk membersihkan udara melalui mekanisme fotosintesis dan meminimumkan jumlah logam beracun dari tanah dengan bantuan mikroorganisme melalui mekanisme asimlilasi dan proses biotransformasi. Vaskular tanaman menyerap racun dari udara melalui daun atau dari tanah dan air melalui akar. Berbagai spesies tanaman diketahui dan telah diuji memiliki kemampuan untuk menyerap dan mengakumulasi beragam jenis logam beracun, senyawa fenolik, pewarna azo, berbagai kontaminan organik dan anorganik lainya. Spesies tanaman ini dapat bertindak sebagai excluders, akumulator dan hiper-akumulator.
Excluders menumpuk polutan dari substrat ke dalam akar dan membatasi perpindahanya ke bagian lain, misalnya tunas.
Akumulator menumpuk dan mengubah polutan menjadi bentuk inert dalam jaringan aerial, sedangkan
hyperaccumlators mampu
Tabel 2 Karakteristik fitoremediasi Keuntungan Kekurangan Sistem
input nutrisi sedikit,
Cost effective Bioavailabilitas polutan terbatas Strategi yang
berkelanjutan dan ramah lingkungan
Risiko kontaminasi pada rantai makanan
Sumber: Khandare et al. 92011a,b); Telke
et al. (2011;) Ali et al. (2013)
Fitoremediasi merupakan proses yang murah, efisien, dan ramah lingkungan. Teknik ini memanfaatkan secara efisien penggunaan tanaman, enzim yang terkait dan mikroba yang ikut berperan untuk isolasi, trasnportasi, penyerapan, detoksifikasi dan penghilangan mineral beracun melalui proses biologis, fisiologi, dan kimia yang kompleks (Sureshvarr et al. 2010; Khandare et al. 2011a,b; Etim 2012; Ali et al. 2013). Tanaman ini selanjutnya dapat dipanen dan diproses atau dibuang secara aman. Cara ini cocok dilakukan untuk menghilangkan kontaminan pada level rendah sampai sedang (Ghosh dan Singh 2005). Berdasarkan proses detoksifikasi, jenis bahan pencemar, medium, dan kadar polutan, fitoremediasi dapat diklasifikasikan menjadi
phytoextraction, phytofiltration, phytostabilization, rhizodegradation dan
phytovolatilization (Tabel 3) (Raskin dan Ensley 2000; Sureshvarr et al. 2010; Ali et al. 2013). Efektivitas fitoremediasi dan mekanisme penyerapan polutan (baik
organik maupun anorganik) sangat dipengaruhi oleh spesies tanaman dan karakteristiknya, interaksi pada zona akar, sifat medium, sifat kimia kontaminan, bioavailabilitas kontaminan, efek penambahan chelating agents, kondisi lingkungan, dll (Cunningham and Ow 1996; Tangahu et al. 2011).
Constructed Wetland
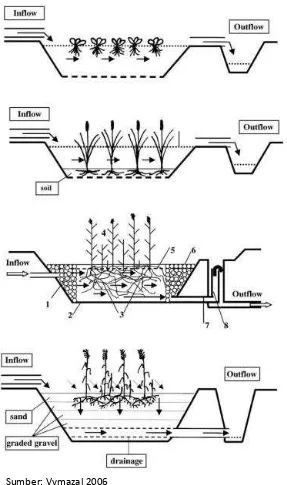
Constructed wetlands (CW) merupakan sistem yang dirancang dan dibangun untuk memanfaatkan proses alami yang melibatkan vegetasi di rawa, tanah, dan kumpulan mikroba yang saling terkait untuk mengolah air limbah. CW dirancang untuk dapat mengambil keuntungan yang maksimum dari proses yang terjadi di rawa alami namun dalam lingkungan yang lebih terkontrol. CW diklasifikasikan berdasarkan karakteristik tanaman air yang paling mendominasi, atau
macrophyte dan bentuk alur aliran air (Gambar 1 dan Gambar 2).
Sumber: Vymazal (2001
Gambar 1 Klasifikasi constructed wetland
untuk pengolahan limbah cair
Mekanisme penghilangan logam
terdapat di permukaan atau di dalam akar untuk waktu yang lama. Hidrologi kemungkin menjadi faktor penentu utama pada proses pembentukan dan pemeliharaan jenis CW tertentu. Kejenuhan yang terjadi secara permanen atau periodik akan menghasilkan kondisi anaerob di tanah sehingga berakibat pada terjadinya proses biogeo-chemical. Proses ini menyebabkan perkembangan karakteristik tanah pada wetland, yang akan mendukung adaptasi tanaman dominan di tanah jenuh (Mitsch and Gosselink 1993; ITRC 2003). Kompartemen hidrologi juga mengandung polyligands yang heterogen yaitu fulvat, humat dan tannic acids, logam oxyhydroxides amorf, tanah liat, bakteri di permukaan, dan exocopolymers
terkait, partikel tersuspensi dan makro-molekul mis polisakarida, protein dll (Matagi et al. 1998).
Proses penghilangan logam di dalam CW terjadi melalui mekanisme yang sangat kompleks. Proses ini dipengaruhi oleh komposisi substrat, pH sedimen, karakteristik air limbah yang mengalir, dan jenis tanaman. Selanjutnya berbagai proses penghilangan logam di CW dapat terjadi melalui tiga mekanisme berikut: Fisik, Kimia dan Proses Biologi.
Penghilangan logam melalui proses fisik
Penghilangan melalui proses fisik dapat terjadi akibat settling dan sedimentasi. Sedimentasi telah lama dikenal sebagai prinsip dasar dalam penghilangan logam berat dari air limbah di CW. Hal ini bukan merupakan reaksi fisik yang berlangsung secara sederhana. Proses kimia lainnya seperti presipitasi dan co-presipitasi harus terjadi terlebih dahulu. Sedimentasi terjadi setelah proses fisik lain mengakibatkan terbentuknya agregat logam berat sehingga menjadi partikel yang cukup besar sehingga dapat tenggelam (Walker dan Hurl 2002). Proses pembentukan sedimen pada CW ditingkatkan dengan peningkatkan pH air
limbah, konsentrasi bahan terlarut, keuatan ion dan konsentrasi alga yang besar (Matagi et al. 1998). Dengan cara ini logam berat dipisahkan dari air limbah dan terperangkap di dalam sedimen CW, sehingga dapat melindungi ekosistem perairan di atasnya.
Penghilangan logam melalui proses kimia
Penghilangan melalui proses kimia dapat terjadi melalui mekanisme sorpsi, adsorpsi, oksidasi dan hidrolisis logam, presipitasi dan co-presipitasi, metal carbonates, dan metal sulfit. Sorpsi merupakan transfer ion dari air ke tanah, misal dari fase cairan ke fase padat. Sorpsi sebenarnya menggambarkan sekelompok proses, yang meliputi adsorpsi dan reaksi presipitasi (Sheoran dan Sheoran 2006).
Di dalam sedimen logam berat ter-adsorpsi pada partikel tanah akibat adanya pertukaran kation atau
chemisorption. Pertukaran kation melibatkan pelekatan secara fisik kation (ion bermuatan positif) pada permukaan tanah liat dan bahan organik akibat tarik-menarik elektrostatik. Apabila logam berat telah diserap ke humic atau koloid tanah liat, logam berat akan tetap dalam bentuk atom logam, tidak seperti polutan organik, yang pada akhirnya akan terurai. karakteristik dapat berubah seiring dengan waktu sebagai akibat perubahan kondisi sedimen (Batty et al. 2002; Wiebner et al. 2005). Lebih dari 50% logam berat dapat dengan mudah diadsorbsi ke dalam bentuk partikulat di dalam CW sehingga dapat dihilangkan dari air dengan sedimentasi. Besi, aluminium dan mangan dapat membentuk senyawa tidak larut air melalui hidrolisis dan / atau oksidasi yang terjadi di CW, sehingga menyebabkan pembentukan berbagai oksida, oxyhydroxides dan hidroksida (Batty et al. 2002; Woulds dan Ngwenya 2004).
sedimen CW. Pembentukan endapan logam berat tidak larut air adalah salah satu dari banyak faktor yang membatasi bioavailabilitas logam berat ke berbagai ekosistem perairan. Presipitasi tergantung pada kelarutan logam yang terlibat Ksp, pH dari CW dan konsentrasi ion logam dan anion yang relevan. Ketika konsentrasi kation dan anion melebihi Ksp, maka presipitasi terjadi. Co-presipitasi juga merupakan fenomena adsorptive dalam sedimen CW. Logam berat mengalami co-presipitasi dengan mineral sekunder di CW. Tembaga, nikel, seng, mangan dll mengalami co-presipitasi dengan oksida Fe dan kobalt, besi, nikel dan seng mengalami co-presipitasi dengan oksida mangan (Stumm dan Morgan 1981; Noller et al, 1994). CW dengan substrat yang sesuai dapat memepercepat pertumbuhan bakteri pengurai sulfat dalam kondisi anaerobic. Dalam air limbah dengan kadar sulfat tinggi bakteri ini akan menghasilkan hidrogen sulfida. Sebagian besar logam berat bereaksi dengan hidrogen sulfida dan menyebabkan pembentukan sulfida logam yang sangat tidak larut (Stumm dan Morgan 1981).
Penghilangan logam melalui proses biologis
Proses penghilangan logam dengan proses biologis terjadi akibat proses fitoremediasi oleh tumbuhan. Sharpe dan Denny (1976) serta Welsh dan Denny (1979) melaporkan bahwa sebagian besar penyerapan logam oleh jaringan tanaman terjadi melalui mekanisme penyerapan anionik di dinding sel dan logam tidak dapat memasuk ke dalam tanaman secara langsung. Dalam biota, konversi biologis terjadi melalui asimilasi dan metabolisme mikroorganisme yang hidup di dan di sekitar macrophyte serta penyerapan dan metabolism tanaman. Dalam kondisi air yang toxic secara permanen, dekomposisi bahan organik terjadi lewat pengurangan dan akumulasi bahan organik pada permukaan sedimen. Sehingga
permukaan sedimen bertanggung jawab untuk menangkap logam berat dari influen (Matagi et al. 1998; Walker and Hurl 2002; Manios et al. 2003).
Mikroorganisme juga dapat mennghilangkan dan menyimpan sejumlah logam berat melalui proses metabolism. Reduksi logam ke dalam bentuk imobil oleh aktivitas mikroba di CW telah dilaporkan oleh Sobolewski (1999); Logam seperti kromium dan uranium menjadi imobil ketika direduksi melalui proses biologis yang dikatalisis oleh mikroorganisme (Fude et al. 1994). Schiffer (1989), Sinicrope et al. (1992), Nelson et al. (2002) dan Adriano (2001) melaporkan bahwa kromium dapat dihilangkan melalui aktivitas bakteri, dengan tingkat penghilangan kromium dari 40% sampai 84%.
Mekanisme Penghilangan Nitrogen
Nitrogen memiliki siklus biogeokimia yang kompleks dengan beberapa transformasi biotik/abiotik yang melibatkan tujuh valensi (+5 sampai -3) (Vymazal 2005). Di dalam limbah cair industri kulit samak nitrogen berada dalam bentuk ammonium (NH4+) dan
ammonia (NH3). Transformasi nitrogen
Model Matematika untuk Prediksi Penghilangan Nitrogen
Model matematika dapat digunakan untuk memprediski jumlah nitrogen yang dapat diuraikan selama jangka waktu tertentu pada suatu jenis konstruksik wetland. Pemodelan ini sangat membantu engineer dalam merancang konstruksi wetland yang tepat. Model matematika untuk satu constructed wetland berbeda dengan model matematika untuk jenis constructed wetland lainnya. Karakteristik limbah cair, suhu, keadaan lingkungan, jenis tanaman, jenis batuan yang digunakan, laju alir limbah cair, merupakan hal-hal yang dapat mempengaruhi model matematika suatu constructed wetland.
Mayo dan Bigambo (2015) mengusulkan model matematika yang menngambarkan mekanisme perubahan nitrogen di dalam horizontal subsurface constructed wetland dengan karakteristik limbah domestik. Model matematika ini memperhitungkan aktivitas biomassa yang terlarut dalam air limbah dan agregat biofilm yang terbentuk serta akar tanaman dengan variable berupa konsentrasi bahan organic, amoniak, dan nitrat-nitrogen serta tanaman dan agregat. Adapun proses transformasi nitrogen utama yang dipertimbangkan adalah mineralisasi, nitrifikasi, denitrifikasi, penyerapan tanaman, pembusukan tanaman dan sedimentasi. Fungsi lain yang dianggap mempengaruhi model adalah adalah suhu, pH dan oksigen terlarut. Gambar 3 adalah salah satu persamaan matematika yang digunakan untuk memodelkan proses nitrifikasi oleh bakteri dan nitrifikasi biofilm. Model ini pertama kali dikembangkan oleh Polprasert dan Agarwalla (1994) disebut dengan model Monod.
Sumber: Mayo dan Bigambo (2015) Gambar 2 Persamaan untuk model Monod
dengan ln adalah laju pertumbuhan maksimum Nitrosomonas (d-1), Yn adalah
koefisien yield untuk bakteri Nitrosomonas dalam mg VSS/mg N, KN adalah konstanta ammonia Nitrosomonas
half saturation (g/m3), KNO adalah konstanta oksigen Nitrosomonas half saturation (g/m3), CT adalah temperature
yang merupakan faktor dependen, CpH adalah faktor penghambat pertumbuhan Nitrosomonas untuk pH, rb1 aadalah
konstanta laju reaksi biofilm untuk agregat (d-1), rb
2 adalah konstanta laju
reaksi biofilm untuk tanaman (d-1).
Potensi Aplikasi untuk Pengolahan Limbah Cair Industri Kulit Samak
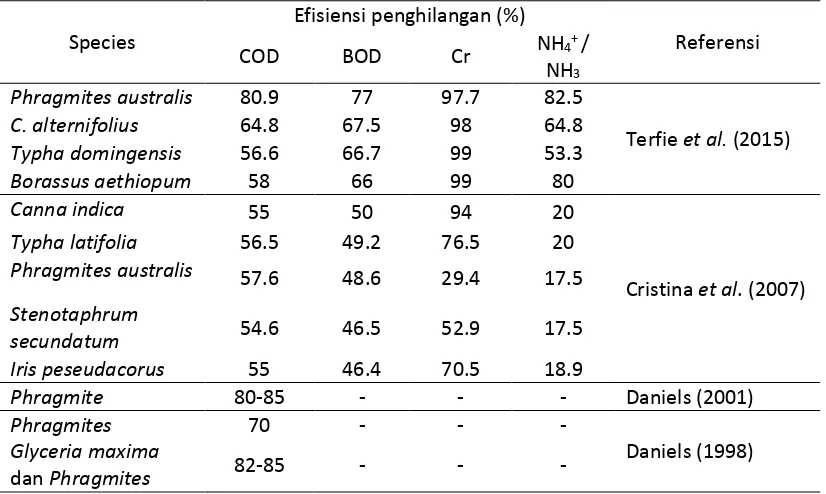
Penelitian tentang pengolahan limbah cair industry penyamakan kulit dengan memanfatkan teknik fitoremediasi di dalam constructed wetland belum banyak dilakukukan. Beberapa peneliti melakukan penelitian pemilihan jenis tanaman untuk fitoremediasi di CW (Tabel 5 dan Gambar 4). Dari data pada Tabel 5 diketahui bahwa spesies tanaman Typha domingensis dan Borassus aethiopium
memiliki efisiensi penghilangan krom yang paling tinggi yakni mencapai 99%, spesies
Phragmites (reeds) memiliki efisiensi penghilangan COD paling tinggi mencapai 85%, dan spesies Phragmites australis
horizontal sub-surface flow diketahui merupakan jenis CW terbaik untuk pengolahan limbah cair industry kulit samak. Jenis ini mampu mentolerir fluktuasi input, termasuk jika terjadi kelebihan input. Kemampuan ini sangat penting karena pada umumnya kapasitas produksi industry kulit samak skala kecil dan menegah khususnya di Indonesia berfluktuasi sepanjang tahun.
KESIMPULAN
Hasil studi literature menunjukkan bahwa penerapan sistem CW untuk pengolahan limbah industry penyamakan kulit merupakan pendekatan yang menjanjikan untuk tahapan pengolahan sekunder.
DAFTAR PUSTAKA
Ali H, Khan E, Sajad MA. 2013.
Phytoremediation of heavy metals:
concepts and applications.
Chemosphere 91, 869–881.
Aravindhan R, Madhan B, Rao J R, Nair U,
Ramasami T. 2004. Bioaccumulation of
chromium from tannery wastewater:
An approach for chrome recovery.
Environmental science and
Technology. American chemical society
38, 1: 300-306.
Batty LC, Baker AJ, Wheeler BD. 2002.
Aluminium and Phosphate Uptake by
Phragmites australis: the Role of Fe,
Mn and al Root Plaques. Annals of
Botany 89, 443–449.
Chauhan S, Das M, Nigam H, Pandey P,
Swati P, Tiwari A, Yadav M. 2015.
Implementation of phytoremediation
to remediate heavy metals from
tannery waste: A review. Advanced in
Applied Science research 6(3):
119-128.
Cheung K, Gu JD. 2007. International
Biodeterioration & Biodegradation,
59(1): 8-15.
Chidambaram A, Sundaramoorthy P,
Murugan A, Ganesh K S. 2009.
Chromium induced cytotoxicity in black
gram. J. Environ Health. Sci. Eng., 6: 17–
22.
Cristina SC, Calheiros, Rangel AOSS, Castro
PML. 2007. Constructed wetland
systems vegetated with different
plants applied to the treatment of
tannery wastewater. Water research
41: 1790-1798.
Cunningham SD, Ow DW. 1996. Promises
and prospect of phytoremediation.
Plant Physiol. 110, 715–719.
Daniel, R. 1998. You’re now entering the
root zone-investigation: the potential
of reed beds for treating waste waters
from leather manufacture. World
Leather 11 (7): 48–50
Daniels R. 200. Enter the root-zone: green
technology for the leather
manufacturer, part 1. World Leather 14
(4), 63–67.
Etim EE. 2012. Phytoremediation and its
mechanisms: a review. Int. J. Environ.
Galanopoulos, Christos, Sazakli, Eleni,
Leotsinidis, Michalis, Lyberatos,
Gerasimos. 2013. A pilot-scale study
for modeling a free water surface
constructed wetlands wastewater
treatment system. J. Environ. Chem.
Eng. 1, 642e651.
Ghosh M, Singh S. 2005. Asian J Energy
Environ, 6(4): 18.
Hefez AL, El-Manharawy MS, khedr MA.
2002. RO Membrane Removal of
Unreacted Chromium from Spent
tanning Effluent: A Pilot-Scale Study,
Part 2.
ITRC. 2003. Technical and regulatory
guidance document for constructed
treatment wetlands. The Interstate
Technology and Regulatory Council
Wetlands Team. 128 pp.
Kacaoba S, Akcin G. 2002. Removal and
Recovery of Chromium and Chromium
Speciation with MINTEQA2. Talanta 57:
23-30.
Khan AG. 2001. Relationships between
Chromium Biomanification Ratio,
Accumulation Factor, and Mycorrhizae
in Plants Growing on tannery
effluent-Polluted Soil. Environ. Int. 26: 417-423.
Khandare RV, Kabra AN, Kurade MB,
Govindwar SP. 2011a.
Phytoremediation potential of
Portulaca grandiflora Hook.
(Moss-Rose) in degrading a sulfonated diazo
reactive dye Navy Blue HE2R (Reactive
Blue 172). Bioresour. Technol. 102,
6774– 6777.
Khandare RV, Kabra AN, Kurade MB,
Govindwar SP. 2011b. The role of Aster
amellus Linn in the degradation of a
sulfonated azo dye Ramazol Red: a
phytoremediation strategy.
Chemosphere 82, 1147–1154.
Lu S, Wang J, Pei L. 2016. Study on the
effects of irrigation with reclaimed
water on the content and distribution
of heavy metals in soil. Int. J. Environ.
Res. Public Health 13, 298.
Lone ML et al..2009. Journal of Zhejiang
University Science B, 9(3): 210-220.
Malik N, Biswas AK. 2012. Role of higher
plants in remediation of metal
contaminated soils. Sci. Rev. Chem.
Commun. 2, 141–146.
Matamoros, Víctor, Salvado, Victoria.
2012. Evaluation of the seasonal
performance of a water reclamation
pond-constructed wetland system for
removing emerging contaminants.
Matagi SV, Swai D, Mugabe R. 1998. A
review of heavy metal removal
mechanisms in wetlands. African
Journal for Tropical Hydrobiology and
Fisheries 8, 23–35.
Mayo AW, Bigambo T. 2015. Nitrogen
transformation in horizontal
Model Development. Journal of Physics
and Chemistry of the Earth 30:
658-667.
Memon AR, Aktoprakligil D, Ozdemir A,
Vertii A. 2001. Heavy metal
accumulation and detoxification
mechanisms in plants. Turk. J. Bot. 25,
111–121.
Memon AR, Schroder P. 2009.
Implication of metal accumulation
mechanisms to phytoremediation.
Environ. Sci. Pollut. Res. 16: 162–175.
Mitsch WJ, Gosselink JG. 1993. Wetlands.
Van Nostrand Reinhold, New York, 722
pp.
Noller BN, Woods PH, Ross BJ. 1994. Case
studies of wetland filtration of mine
waste water in constructed and
naturally occurring systems in northern
Australia. Water Science and
Technology 29: 257–266.
Raskin RD, Salt DE. 1997.
Phytoremediation of metals: using
plants to remove pollutants from the
environment. Curr. Opin. Biotechnol. 8
(2), 2–6.
Raskin I., Ensley BD. 2000. Recent
developments for in situ treatment of
metal contaminated soils. In:
Phytoremediation of Toxic Metals:
Using Plants to Clean Up the
Environment. John Wiley and Sons Inc.,
New York.
Sheoran V, Sheoran A, Poonia P. 2011.
Role of hyperaccumulators in
phytoextraction of metals from
contaminated mining sites: a review.
Crit. Rev. Environ. Sci. Technol. 41,
168–214.
Shao, Ling, Wu, Zi, Zeng L, Chen ZM, Zhou
Y, Chen GC. 2013. Embodied energy
assessment for ecological wastewater
treatment by a constructed wetland.
Ecol. Model. 252, 63e71.
Sheoran AS, Sheoran V. 2005. Heavy
metal removal mechanism of acid mine
drainage in wetlands: A critical review.
Minerals Engineering Journal, 19:
105-116.
Song Z, Williams CJ, Edyvean RGJ. 2000.
Sedimentation of tannery wastewater.
Water Res. 34 (7), 2171–2176.
Sinha RK, Herat S, Tandon PK. 2007.
Phytoremediation: role of plants in
contaminated site management. In:
Singh SN, Tripathi RD. (Eds.),
Environmental Bioremediation
Technologies. Springer-Verlag, Berlin
Heidelberg, pp. 315–330.
Sureshvarr K, Bharathiraja B, Jayakumar
M, Jayamuthunagai J, Balaji L. 2010.
Removal of azo-dye compounds from
paper industries wastes using
phytoremediation methodology. Int.
Stumm W, Morgan J. 1981. Aquatic
Chemistry, second ed. John Wiley &
Sons, New York, 780 pp.
Tangahu BV, Abdullah SRS, Basri H, Idris
M, Anuar N, Mukhlisin M. 2011. A
review on heavymetals (As, Pb and Hg)
uptake by plants through
phytoremediation. Int. J. Chem. Eng.
201: 1–31.
Terife TA, Sfaw SL. 2015. Evaluation of
selected wetland plants for removal of
chromium from tannery wastewater in
constructed wetlands, Ethiophia.
African Journal of Environmental
Science and Technology. 9(5): 420-427
Vymazal J. 2001. Types of constructed
wetlands for wastewater treatment:
their potential for nutrient removal. In:
Vymazal J, editor. Transformations of
nutrients in natural and constructed
wetlands. Leiden, The Netherlands:
Backhuys Publishers, p. 1-93.
Vymazal J. Constructed wetlands for
wastewater treatment in Europe. In:
Dunne EJ, Reddy R, Carton OT, editors.
Nutrient management in agricultural
watersheds: a wetland solution.
Wageningen, The Netherlands:
Wageningen Academic Publishers;
2005a. p. 230–44.
Walker DJ, Hurl S. 2002. The reduction of
heavy metals in a storm water wetland.
Ecological Engineering 18 (4), 407–414.
Wiebner A, Kappelmeyer U, Kuschk P,
Kastner M. 2005. Influence of the redox
condition dynamics on the removal
efficiency of a laboratory-scale
constructed wetland. Water Research
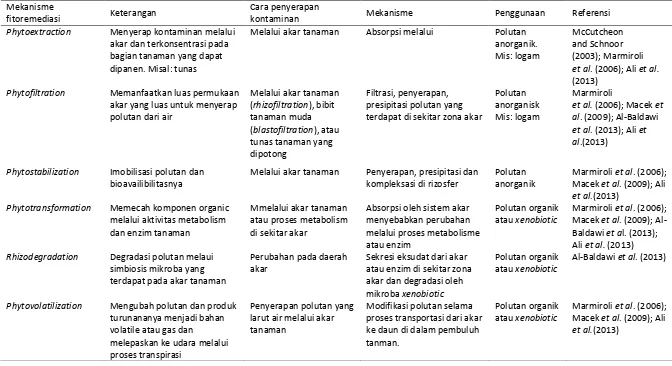
Tabel 3 Ringkasan berbagai proses dan mekanisme fitoremediasi Mekanisme
fitoremediasi Keterangan
Cara penyerapan
kontaminan Mekanisme Penggunaan Referensi
Phytoextraction Menyerap kontaminan melalui akar dan terkonsentrasi pada bagian tanaman yang dapat dipanen. Misal: tunas
Melalui akar tanaman Absorpsi melalui Polutan anorganik.
Phytofiltration Memanfaatkan luas permukaan akar yang luas untuk menyerap polutan dari air
Melalui akar tanaman (rhizofiltration), bibit tanaman muda (blastofiltration), atau tunas tanaman yang dipotong
Filtrasi, penyerapan, presipitasi polutan yang terdapat di sekitar zona akar
Polutan anorganisk Mis: logam
Marmiroli
et al. (2006); Macek et al. (2009); Al-Baldawi
et al. (2013); Ali et al.(2013)
Phytostabilization Imobilisasi polutan dan bioavailibilitasnya
Melalui akar tanaman Penyerapan, presipitasi dan kompleksasi di rizosfer
Polutan anorganik
Marmiroli et al. (2006); Macek et al. (2009); Ali
et al.(2013)
Phytotransformation Memecah komponen organic melalui aktivitas metabolism dan enzim tanaman
Mmelalui akar tanaman atau proses metabolism di sekitar akar
Absorpsi oleh sistem akar menyebabkan perubahan melalui proses metabolisme atau enzim
Rhizodegradation Degradasi polutan melaui simbiosis mikroba yang terdapat pada akar tanaman
Perubahan pada daerah akar
Sekresi eksudat dari akar atau enzim di sekitar zona akar dan degradasi oleh mikroba xenobiotic
Polutan organik atau xenobiotic
Al-Baldawi et al. (2013)
Phytovolatilization Mengubah polutan dan produk turunananya menjadi bahan volatile atau gas dan
melepaskan ke udara melalui proses transpirasi
Penyerapan polutan yang larut air melalui akar tanaman
Sumber: Vymazal 2006
Tabel 4 Transformasi nitrogen di dalam constructed wetland
Proses Transformasi
Volatilisasi Ammonia-N (aq) ammonia-N (g) Amonifikasi Organic-N ammonia-N
Nitrifikasi Ammonia-N nitrit-N nitrat-N Nitrat-amonifikasi Nitrat-N ammonia-N
Denitrifikasi Nitrit-N nitrit-N N(g), N2O
Fiksasi N2 N2(g) ammonia-N (organic-N) Plant/microbial uptake (asimilasi) Ammonia-, nitrit-, nitrat-N organic-N
Ammonia adsorption Organic nitrogen burial ANAMMOX (anaerobic ammonia oxidaton)
Ammonia-N N2(g)
Sumber: Vymazal (2005)
Tabel 5 Jenis tanaman potensial untuk fitoremediasi limbah cair industri kulit samak
Species
Efisiensi penghilangan (%)
Referensi
COD BOD Cr NH4
+ /
NH3 Phragmites australis 80.9 77 97.7 82.5
Terfie et al. (2015)
C. alternifolius 64.8 67.5 98 64.8
Typha domingensis 56.6 66.7 99 53.3
Borassus aethiopum 58 66 99 80
Canna indica 55 50 94 20
Cristina et al. (2007)
Typha latifolia 56.5 49.2 76.5 20
Phragmites australis 57.6 48.6 29.4 17.5 Stenotaphrum
secundatum 54.6 46.5 52.9 17.5
Iris peseudacorus 55 46.4 70.5 18.9
Phragmite 80-85 - - - Daniels (2001)
Phragmites 70 - - -
Daniels (1998)
Glyceria maxima
dan Phragmites 82-85 - - -
Typha domingensis Canna indica
Iris peseudacorus Glyceria maxima
Stenotaphrum secundatum