PENGEMBANGAN DAN VALIDASI METODE
PENGUJIAN KADAR SIANIDA DALAM LIMBAH
CAIR SECARA SPEKTROSKOPI UV-Vis
RA ERIKA JULISTIANA
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
BOGOR
2009
ABSTRAK
RA ERIKA JULISTIANA. Pengembangan dan Validasi Metode Pengujian Kadar Sianida dalam
Limbah Cair secara Spektroskopi UV-Vis. Dibimbing oleh HENDRA ADIJUWANA dan
AGUSTINA MALINDA.
Pengujian kadar sianida dalam limbah cair merupakan suatu hal yang harus dip enuhi karena senyawaan sianida seringkali digunakan untuk tujuan industri dan keberadaan sianida sangat membahayakan makhluk hidup. Metode pengujian sianida dalam limbah cair menggunakan pereaksi Ninhidrin diperkirakan menghasilkan data yang terpercaya. Dalam hal ini, metode tersebut harus memenuhi syarat penerimaan parameter validasi, yaitu linearitas, batas kelinearan, ketelitian, ketepatan, limit deteksi (LD), limit kuantitasi (LK), selektivitas, dan ketangguhan metode.
Validasi metode pengujian sianida dengan pereaksi ninhidrin mempunyai linearitas yang baik dengan koefisien korelasi sebesar 0. 9968 pada konsentrasi 34.60-76.90 ppb, batas kelinearan dihasilkan bahwa pada konsentrasi sianida 50 ppb masih menunjukkan linearitas yang baik, %RSD yang diperoleh pada penentuan ketelitian sebesar 4.58%, persen perolehan kembali (PK) pada penentuan ketepatan masing-masing pada konsentrasi 34.60, 49.40, dan 76.90 ppb adalah 89.83%, 88.81%, dan 88.33%, LD dan LK diperoleh berturut-turut 0.0967 ppb dan 0.3222 ppb, selektivitas yang diperoleh adalah 0.26%, serta dari ketangguhan metode diperoleh bahwa konsentrasi, waktu, dan matriks berpengaruh dalam pengukuran. Menurut kriteria yang ditetapkan dalam Association
of Official Analytical Chemist, hasil uji parameter-param eter validasi di atas menunjukkan bahwa
metode pengujian kadar sianida secara spektroskopi UV-Vis dapat dikatakan memadai untuk menghasilkan data analisis yang absah.
ABSTRACT
RA ERIKA JULISTIANA. Development and Validation of Cyanide Level Determination in
Liquid Waste Using UV-Vis Spectroscopy. Supervised by HENDRA ADIJUWANA and
AGUSTINA MALINDA.
Determination of cyanide in liquid waste needs to be done because cyanide compounds were oftenly used for industrial purposes and environment ally hazardous. Cyanide determination method in liquid waste by using ninhydrin reagent was expected to produce more reliable data. In this case, the method should fulfill the requirements of validation parameters, such as linearity, limit of linearity, precision, accuration, limit of detection (LOD), limit of quantitation (LOQ), selectivity, and robustness.
Validation of cyanide determination method by using ninhydrin reagent produced good linearity data with coefficient correlation 0.9968 at contentration about 34.60-76.90 ppb, limit of linearity resulted that at contentration 50 ppb, data still show ed good linearity, %RSD on precission test was 4.58%, recovery for accuration test for each 34.60, 49.40, and 76.90 ppb were 89.83%, 88. 81%, and 88.33%, LOD and LOQ were 0.0967 ppb and 0.3222 ppb, selectivity of method was 0.26%, also robbustness of method showed that concentration, time and matrix effect on determination. According to the criteria of Association of Official Analytical Chemist, the result of validation parameters test fro m the determination using UV-Vis spectroscopy showed satisfactory result s.
PENGEMBANGAN DAN VALIDASI METODE
PENGUJIAN KADAR SIANIDA DALAM LIMBAH
CAIR SECARA SPEKTROSKOPI UV-Vis
RA ERIKA JULISTIANA
Skripsi
sebagai salah satu syarat memperoleh gelar Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
BOGOR
2009
RIWAYAT HIDUP
Penulis dilahirkan di Lahat pada tanggal 20 Juli 1985 dari ay ah Adji Supriajasa dan ibu Mutiah Muchtar. Penulis merupakan putri tunggal.
Tahun 2003 penulis lulus dari SMU Negeri 7 Jakarta dan pada tahun yang sama lulus seleksi masuk IPB melalui jalur Undangan Seleksi Masuk IPB. Penulis memilih Program Studi Kimia, Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam.
Selama mengikuti perkuliahan, penulis pernah menjadi asisten praktikum Kimia Dasar pada tahun ajaran 2007/2008, Kimia Anorganik pada tahun 2007/2008 untuk Program Studi D3 Analisis Kimia. Penulis juga pernah mengikuti Praktik Kerja Lapangan di Laboratorium Kimia Air, Balai Besar Industri Agro, Bogor selama bulan Juni sampai Agustus 2007.
PRAKATA
Segala puji syukur kepada Allah SWT selalu penulis ucapkan atas rahmat, hidayah, dan ridho-Nya sehingga karya ilmiah ini berhasil diselesaikan. Karya ilmiah yang berjudul Pengembangan dan Validasi Metode Pengujian Kadar Sianida dalam Limbah Cair secara Spektroskopi UV- Vis disusun berdasarkan penelitian yang dilaksanakan mulai bulan Mei sampai dengan Oktober 2008 di Laboratorium Kimia Air, Balai Besar Industri Agro.
Selama melaksanakan kegiatan penelitian dan menyusun karya ilmiah, penulis banyak mendapatkan bimbingan dan bantuan dari berbagai pihak. Oleh karena itu penulis mengucapkan terima kasih kepada Bapak Ir. Hendra Adijuwana, MST dan Ibu Agustina Malinda, S.Si atas saran, bimbingan, dan arahan yang telah diberikan kepada penulis dalam pelaksanaan penelitian dan penulisan skripsi. Penulis juga mengucapkan terima kasih yang terdalam kepada Bapak Chaerul Anwar atas bimbingan, arahan, dan sarannya. Terima kasih tidak lupa diucapkan kepada Kepala Departemen Kimia IPB, Kepala Balai Besar Industri Agro dan staf pegawai Balai Besar Industri Agro yang telah membantu penulis. Ucapan terima kasih penulis yang tak terhingga kepada Mama yang selalu memberikan semangat, mendukung, dan mendoakan penulis .
Semoga karya ilmiah ini bermanfaat dalam bidang ilmu pengetahuan.
Bogor, Desember 2008
DAFTAR ISI
Halaman
DAFTAR TABEL ... vii
DAFTAR GAMBAR ... vii
DAFTAR LAMPIRAN ... vii
PENDAHULUAN ... 1 TINJAUAN PUSTAKA Sianida ... 1 Ninhidrin ... 2 Spektrofotometri... 2 Validasi Metode ... 3
Parameter-P arameter Validasi ... 3
BAHAN DAN METODE Alat dan Bahan ... 4
Metode Percobaan ... 4
HASIL DAN PEMBAHASAN Pengukuran Panjang Gelombang ... 5
Validasi Metode Pengujian Sianida ... 6
SIMPULAN DAN SARAN Simpulan ... 10
Saran ... 10
DAFTAR TABEL
Halaman
1 Perolehan batas kelinearan ... 7
2 Hasil uji ketepatan ... 8
3 Hasil uji F pada ketangguhan metode ... 9
4 Hasil uji t pada ketangguhan metode ... 9
DAFTAR GAMBAR
Halaman
1 Reaksi asam amino dengan ninhidrin . ... 22. Spektrum absorpsi sianida dengan ninhidrin ... 6
3. Reaksi sianida dengan ninhidrin . ... 6
4. Kurva standar hubungan antara konsentrasi sianida dan absorbans ... 7
5. Hubungan antara konsentrasi sianida dalam kisaran 0-60 ppb dan absorbans ... 7
6. Hubungan antara konsentrasi sianida dalam kisaran 0-55 ppb dan absorbans... 7
7. Hubungan antara konsentrasi sianida dalam kisaran 0-50 ppb dan absorbans ... 8
DAFTAR LAMPIRAN
Halaman
1 Baga n alir percobaan ... 132 Perhitungan linearitas metode pengujian sianida dengan pereaksi ninhidrin... 14
3 Penentuan batas kelinearan metode pengujian sianida dengan pereaksi ninhidrin ... 15
4 Penentuan ketelitian metode pengujian sianida dengan p ereaksi ninhidrin ... 16
5 Penentuan ketepatan metode pengujian sianida dengan pereaksi ninhidrin ... 17
7 LD dan LK metode pengujian sianida dengan pereaksi ninhidrin ... 19
8 Penentuan selektivitas metode pengujian sianida dengan pereaksi ninhidri n ... 20
PENDAHULUAN
Pembuangan limbah berbahaya menjadi persoalan besar, bila air yang dikonsumsi oleh manusia, hewan, dan organisme tercemar limbah yang mengandung senyawa berbahaya. Kondisi ini dapat menimbulkan gangguan, kerusakan, dan bahaya bagi semua makhluk hidup. Salah satu pencemar yang sangat berbahaya adalah sianida. Sianida berdampak negatif terhadap makhluk hidup, yakni mengganggu fungsi hati, pernap asan, dan menyebabkan kerusakan tulang (Moore 1991). Oleh karena itu, perlu dilakukan analisis kimia oleh suatu badan atau lembaga tertentu untuk menentukan susunan bahan, baik secara kualitatif maupun kuantitatif.
Metode spektrofotometri untuk penentuan sianida jauh lebih baik dibandingkan metode lain, seperti titrimetri, polarografi, fluorometri, dan kromatografi. Metode penentuan sianida umumnya menggunakan spektrofotometri dengan metode piridin-benzidin (Aldridge), metode piridin-pirazolon (Epstein), metode piridin-asam barbiturat (Asmus dan Garschagen), dan metode piridin-p-fenilendiamina (Bark dan Higson). Namun metode-metode tersebut memiliki banyak kekurangan, seperti sifat karsinogenik dari benzidin, tidak stabilnya pereaksi piridin-pirazolon, pembentukan warna yang lamban pada metode piridin-p-fenilendiamina, dan cepat pudarnya warna pada metode piridin -asam barbiturat.
Saat ini, dikembangkan metode penentuan sianida menggunakan ninhidrin sebagai pereaksi dalam suasana basa (Nagaraja et al. 2002). Metode ini melakukan langkah yang mudah dan akurat untuk penentuan sianida menggunakan ninhidrin sebagai reagen yang tunggal dan murah. Metode ini sensitif, umumnya bebas dari gangguan yang berasal dari spesi pengganggu, dan tidak membutuhkan pemanasan atau ekstraksi. (Nagaraja et al 2002).
Metode penelitian yang dilakukan ini merupakan metode yang dikembangkan dari Nagaraja et al (2002) dengan melakukan beberapa modifikasi. Dasar dari metode ini adalah reaksi antara sianida dan ninhidrin dalam suasana basa. Penetapan sianida menggunakan spektrofotometer cahaya tampak double beam. Metode spektrofotometri
UV/Vis sebagai metode analisis yang sederhana dan relatif murah dan sering digunakan untuk analisis kualitatif dan kuantitatif berbagai jenis senyawa berdasarkan interaksi antara radiasi elektromagnetik dengan materi. Hasil analisis yang akurat dan teliti akan diperoleh apabila metode yang digunakan telah divalidasi.
Validasi merupakan suatu tindakan penilaian terhadap parameter tertentu berdasarkan percobaan laboratorium untuk membuktikan bahwa parameter tersebut memenuhi persyaratan untuk penggunaannya (Harmita 2004). Menurut Levin (2002), validasi dibagi menjadi empat kelas, yaitu kelas A, B, C, dan D. Kelas A digunakan untuk identifikasi suatu senyawa. Kelas B digunakan untuk mendeteksi dan menentukan adanya pengotor. Kelas C dapat menentukan senyawa secara kuantitatif dan kelas D untuk mencari ciri suatu senyawa. Validasi pada penelitian ini tergolong ke dalam kelas C. Validasi metode bermanfaat untuk mengevaluasi unjuk kerja suatu metode analisis, menjamin prosedur analisis yang akurat, menekan sekecil-kecilnya risiko penyimpangan yang timbul, dan menjamin kedapatulangan yang tepat. Suatu metode analisis dikatakan absah jika telah memenuhi syarat penerimaan parameter validasi. Parameter yang dimaksud meliputi linearitas, batas kelinearan, ketelitian, ketepatan, limit deteksi, limit kuantitasi, selektivitas, dan ketangguhan metode.
Penelitian ini bertujuan melakukan pengembangan dan validasi metode pengujian kadar sianida dalam limbah cair secara
spekt roskopi UV-Vis. Penelitian ini
dilaksanakan di Laboratorium Kimia Air, Balai Besar Industri Agro, dan berlangsung dari bulan Mei sampai Oktober 2008.
TINJAUAN PUSTAKA
SianidaIon renik (trace) adalah ion yang terdapat di perairan dalam jumlah yang sangat sedikit, biasanya dinyatakan dalam satuan nanogram/liter (Haslam 1995). Salah satu ion renik yang berada di perairan adalah sianida (CN-). Sianida merupakan kelompok senyawa anorganik dan organik dengan siano (CN)
sebagai struktur utama. Biasanya, senyawa ini dihasilkan dalam pemrosesan logam. Sianida tersebar luas di perairan dan berada dalam bentuk ion sianida (CN-), hidrogen sianida (HCN), dan metalosianida.
Keberadaan sianida sangat dipengaruhi oleh pH, suhu, oksigen terlarut, salinitas, dan keberadaan ion lain. Sianida mengalami disosiasi seperti yang ditunjukkan dalam persamaan reaksi:
KCN + H2O ? HCN + KOH CN-+H+
Sianida dalam bentuk ion mudah terserap oleh bahan-bahan yang tersuspensi maupun oleh sedimen dasar. Sianida bersifat sangat reaktif. Sianida bebas menunjukkan adanya kadar HCN dan CN-. Pada pH yang lebih kecil dari 8, sianida berada dalam bentuk HCN yang dianggap lebih toksik bagi organisme akuatik daripada CN-.
Sianida yang terdapat di perairan terutama berasal dari limbah industri, misalnya industri pelapisan logam, pertambangan emas, pertambangan perak, industri pupuk, dan industri besi baja. Kadar sianida yang digunakan dalam pertambangan emas dan perak dapat mencapai 250 mg/liter (US-EPA 1988 dalam Moore 1991). Sianida bersifat mudah mengurai dan mudah berikatan dengan ion logam, misalnya tembaga dan besi.
Sianida dapat menghambat pertukaran oksigen pada makhluk hidup. Sianida juga bersifat toksik bagi ikan; kadar sianida 0.2 mg/liter sudah mengakibatkan toksisitas akut bagi ikan. Kadar sianida perairan yang dianjurkan adalah sekitar 0.005 mg/liter (Moore 1991). Menurut WHO, kadar maksimum sianida yang diperkenankan pada air minum adalah 0.1 mg/liter (Moore 1991).
Ninhidrin
Ninhidrin pertama kali ditemukan pada tahun 1910 dan telah ditetapkan sebagai pereaksi yan penting dalam bidang kimia, biokimia, dan ilmu forensik. Ninhidrin digunakan untuk mendeteksi keberadaan asam amino selama lebih dari 50 tahun. Ninhidrin dikenal sebagai triketohidridena, atau 2,2-dihidroksi-1,3-indanedion.
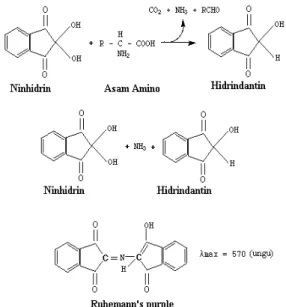
Reaksi ninhidrin digunakan sebagai dasar untuk penentuan kuantitas asam amino. Gugus amina dapat bereaksi dengan pereaksi ninhidrin membentuk amonia, karbon dioksida
dan aldehida. Warna biru menunjukkan secara khas gugus amino.
Ninhidrin banyak pula digunakan untuk mengawasi deproteksi pada sintesis peptida lewat Uji Kaiser. Ketika rantai peptida terdeproteksi, ninhidrin memberikan warna biru pada hasil. Sebaliknya, bila rantai peptida selanjutnya kembali berpasangan, maka hasil uji menghasilkan warna kuning.
Selain itu, larutan yang diduga mengandung ion amonium, juga dapat diuji menggunakan senyawa ninhidrin dengan meneteskannya pada medium padat seperti silika gel. Perlakuan dengan ninhidrin ini akan menghasilkan warna ungu bila larutan tersebut mengandung ion amonium. Ninhidrin banyak pula digunakan dalam kromatografi lapis tipis untuk menguji adanya amina, karbamat, dan juga amida.
Gambar 1 Reaksi asam amino dengan ninhidrin (Girindra 1986)
Spektrofotometri
Spektrofotometri adalah metode analisis yang didasarkan pada interaksi antara radiasi elektromagnetik dengan materi. foton dari spektrum elektromagnetik daerah ultraviolet dan sinar tampak mempunyai energi yang cukup untuk mempromosikan elektron dari keadaan dasar dalam senyawa organik ke keadaan tereksitasinya. Perbedaan energi di antara dua keadaan ini terkuantisasi sehingga
hanya foton-foton dengan energi tertentu yang akan diabsorbsi (Brown et al. 1988).
Penyerapan sinar tampak dan ultraviolet oleh suatu molekul akan menghasilkan transisi di antara tingkat energi elektronik molekul tersebut. Transisi tersebut pada umumnya antara orbital ikatan atau orbital pasangan bebas serta orbital bukan ikatan atau orbital anti ikatan (Sudjadi 1983). Penyerapan radiasi dapat dihubungkan dengan kandungan analit dalam contoh. Pada spektrofotometri, nilai
absorbans yang diperoleh dari analat
dipengaruhi oleh pH larutan, suhu, konsentrasi, pelarut, serta matriks dari analat. Gabungan dua hukum empiris telah merumuskan tentang intensitas serapan, yaitu hukum Lambert-Beer. Prinsip dari hukum Lambert -Beer menjelaskan bahwa seberkas sinar dilewatkan pada suatu larutan dengan panjang gelombang tertentu sehingga sinar tersebut sebagian diteruskan dan sebagian lagi dilewatkan oleh larutan. Hukum Lambert menyatakan bahwa fraksi penyerapan sinar tidak tergantung dari intensitas sumber cahaya. Hukum Beer menyatakan bahwa penyerapan sebanding dengan molekul yang menyerap. Hukum Lambert -Beer menjelaskan hubungan antara absorbans, t ebal cuplikan dan konsentrasi analat.
Pada penentuan analat secara kuantitatif, spektrofotometri melibatkan pengukuran absorbans untuk pembuatan kurva kalibrasi hubungan antara konsentrasi standar dan nilai absorbansnya. Kurva ini lebih dikenal dengan kurva standar. Persamaan yang diperoleh dari kurva standar digunakan untuk menghitung konsentrasi analat yang terukur dari sampel. Persamaan tersebut dirumuskan sebagai y = a+bx dengan y sebagai nilai absorbans dan x sebagai konsentrasi standar yang diukur. Spektrofotometer adalah suatu instrumen untuk mengukur transmitans atau absorbans suatu sampel sebagai fungsi panjang gelombang. Pengukuran terhadap sederetan sampel pada suatu panjang gelombang tunggal dapat pula dilakukan. Instrumen semacam itu dapat dikelompokkan secara manual dan merekam atau sebagai berkas tunggal dan berkas rangkap. Pengelompokkan cara lain didasarkan pada daerah spectral, yaitu spektrofotometer inframerah, ultraviolet, dan sebagainya (Day & Underwood 2002).
Validasi Metode
Validasi adalah sebuah evaluasi mengenai ketepatan dan ketelitian yang dicapai dari suatu prosedur analisis yang layak digunakan untuk menyelesaikan suatu masalah. Bahkan, validasi menjamin bahwa penulisan prosedur/alur prosedur yang sama mendapatkan hasil yang dapat dibandingkan. Perbandingan analisis ini dapat digunakan untuk mengevaluasi ketelitian dan ketepatan prosedur tersebut (Harvey 2000). Tujuan dari validasi metode adalah menilai kemampuan sekaligus keterbatasan dari metode untuk hasil yang dapat dipercaya dan sesuai dengan yang dikehendaki dalam penerapan metode tersebut. Hal tersebut menyebabkan validasi metode menjadi keharusan sebelum suatu metode dipakai secara rutin dan juga untuk metode yang baru dikembangkan. Validasi metode berguna untuk penyimpangan yang dapat dihindari dari suatu metode pada kondisi normal, memperkirakan tingkat kepercayaan suatu metode, dan mengevaluasi unjuk kerja suatu metode analisis pada lingkup parameter tertentu. Parameter validasi metode analisis, yaitu spesifisitas, sensitivitas, ketelitian, ketepatan, linearitas, kisaran (range), limit deteksi, limit kuantitasi, ketidakpastian, batas kelinearan, kepastian, dan ketangguhan metode.
Linearitas suatu prosedur analisis merupakan kemampuan suatu metode analisis untuk memperoleh hasil pengujian yang sesuai dengan konsentrasi analat dalam contoh pada kisaran konsentrasi tertentu (ICH 1995). Linearitas suatu metode analisis adalah ukuran yang menunjukkan tingkat kesesuaian atau korelasi antara kadar analat dengan respon detektor. Linearitas diukur dengan menghitung koefisien korelasi (r) yang didapat dari kurva hubungan antara kadar analat dengan respon detektor (Depkes 2001). Respon detektor yang digunakan adalah luas puncak. Koefisien korelasi (r) menunjukkan kemampuan suatu metode untuk menghasilkan angka analisis yang proporsional terhadap konsentrasi analat dalam contoh pada interval konsentrasi tertentu. Koefisien korelasi didapat dengan menghitung regresi dari persamaan linearnya, sedangkan perpotongan dengan sumbu y menyatakan ukuran biasnya. Interval linearitas adalah selang antara konsentrasi tertinggi dan terendah dari analat yang dapat ditetapkan menggunakan suatu metode dengan tingkat
ketelitian, kecermatan, dan koefisien korelasi yang telah dilakukan. Nilai r yang dihasilkan dapat dikatakan baik jika lebih besar dari 0.9950 (AOAC 2002).
Batas kelinearan adalah konsentrasi analat terbesar yang dapat dikuantisasi dengan baik oleh suatu metode dan secara statistik masih memberikan hubungan yang linear terhadap respon analitiknya. Pada beberapa acuan yang berkaitan dengan makanan atau obat-obatan syarat berketerimaan limit linearitas adalah konsentrasi yang masih memberikan koefisien korelasi = 0.9950 (AOAC 2002).
Ketelitian adalah ukuran yang menunjukkan derajat kesesuaian antara hasil uji individual, diukur melalui penyebaran hasil individual dari rerata prosedur yang dilakukan secara berulang pada contoh-contoh yang diambil dari campuran yang homogen (Harmita 2004). Analisis kimia dikatakan mempunyai ketelitian tinggi jika selisih antarhasil pengukuran tersebut kecil. ICH membagi ketelitian menjadi dua, yaitu ketertiruan (reproducibility) dan keterulangan (repeatibility). Ketertiruan adalah ketelitian yang dihitung dari hasil penetapan ulangan dengan menggunakan metode yang sama, namun dilakukan oleh operator, peralatan, laboratorium, dan waktu yang berbeda. Keterulangan adalah ketelitian yang diperoleh dari hasil pengulangan dengan menggunakan metode, operator, peralatan, laboratorium, dan waktu yang sama. Ketelitian diukur dengan menghitung Relative Standard Deviation
(RSD). Syarat penerimaan %RSD sesuai standar AOAC (2002) adalah sebagai berikut: (1) sangat teliti: %RSD <1, (2) teliti: %RSD 1 -2, (3) sedang: %RSD 2-5, dan (4) tidak teliti: %RSD >5.
Ketepatan suatu prosedur analisis merupakan kedekatan hasil yang diterima (baik sebagai nilai teoritis maupun dengan nilai rujukan yang diterima) dengan nilai yang diperoleh dari hasil pengukuran (ICH 1995). Analisis kimia dapat dikatakan tepat bila nilai yang diperoleh dari hasil pengukuran dekat dengan nilai absolut. Ketepatan diukur dengan menghitung perolehan kembali (PK) menggunakan metode penambahan standar. Persen PK adalah angka yang menunjukkan besarnya penambahan standar yang mampu diidentifikasi kembali dengan suatu metode. Nilai PK bergantung pada matriks sampel, prosedur proses sampel, dan konsentrasi
analat. Batas penerimaan PK adalah 80-110% (AOAC 2002).
Limit deteksi (LD) merupakan jumlah atau konsentrasi terkecil dari analat dalam contoh yang dapat dideteksi namun tidak perlu diukur sesuai dengan nilai sebenarnya (ICH 1995). Pendekatan yang dapat dilakukan untuk menentukan limit deteksi memanfaatkan rerata kemiringan kurva kalibrasi. Limit kuantitasi (LK) adalah jumlah analat terkecil dalam contoh yang dapat ditentukan secara kuantitatif pada kondisi percobaan yang tetap. LK merupakan parameter pengujian kuantitatif untuk konsentrasi analat yang rendah dalam matriks yang kompleks dan digunakan untuk menentukan pengotor atau degradasi produk (ICH 1995). Limit deteksi dan limit kuantitasi dihitung dari simpangan baku dan rerata kemiringan kurva larutan standar pada kurva standar (ICH 1996).
Selektivitas atau spesifisitas suatu metode adalah kemampuannya yang hanya mengukur zat tertentu saja secara cermat dan seksama dengan adanya komponen lain yang mungkin ada dalam matriks sampel. Selektivitas seringkali dapat dinyatakan sebagai derajat penyimpangan (degree of bias) metode yang dilakukan terhadap sampel yang mengandung bahan yang ditambahkan berupa cemaran, hasil urai, senyawa sejenis, senyawa asing lainnya, dan dibandingkan terhadap hasil analisis sampel yang tidak mengandung bahan lain yang ditambahkan. Metode dikatakan mempunyai selektivitas yang baik jika respon analitik yang didapat dari blanko matriks = 2% dari respon analitik konsentrasi uji.
Ketangguhan metode atau robustness adalah kemampuan prosedur untuk memberikan hasil uji dengan tingkat ketepatan dan ketelitian yang dapat diterima dibawah kondisi yang bervariasi. Ketegaran memberikan indikasi keandalan prosedur analisis itu selama aplikasi normal. Variasi tersebut dapat berupa suhu, kelembaban ruangan atau inkubator, pH pereaksi, dan sebagainya.
BAHAN DAN METODE
Bahan dan AlatBahan-bahan yang digunakan antara lain larutan natrium karbonat 10%, larutan
ninhidrin 2%, larutan NaOH 2.5 M, larutan baku sianida, limbah cair, dan akuades. Alat-alat yang digunakan antara lain perangkat spektrofotometer U V-Vis Perkin Elmer Lambda 25, neraca analitik, gelas arloji, gelas piala 150 ml, batang pengaduk, pipet volumetrik, pipet tetes, buret, labu takar 50 ml, dan labu semprot.
Metode
Penetapan Blanko dan Kurva Standar Kurva standar dengan konsentrasi 5, 10, 15, 20, 25 ppb dari larutan stok sianida 1000 ppb ke dalam labu takar 50 ml, kemudian ditambahkan empat ml larutan ninhidrin 2% dan empat ml larutan natrium karbonat 10% dan ditambahkan air hingga 25 ml, lalu dihomogenkan dan didiamkan sekitar 30 menit untuk memberikan kompleks warna merah, lalu diencerkan dengan NaOH 2.5 M sampai tanda tera, larutan stabil selama 30 menit. Untuk penetapan blanko, ke dalam labu takar 50 ml dipipet, empat ml larutan ninhidrin 2% dan empat ml larutan natrium karbonat 10% kemudian ditambahkan air hingga 25 ml lalu dihomogenkan dan didiamkan sekitar 30 menit untuk memberikan kompleks warna merah, lalu diencerkan dengan NaOH 2.5 M sampai tanda tera. Larutan-larutan tersebut dibaca absorbansnya dengan spektrofotometer pada panjang gelombang 606 nm.
Linearitas
Preparat deret kalibrasi dibuat menggunakan blanko matriks yang ke dalamnya ditambahkan secara kuantitatif analat standar yang diketahui konsentrasinya secara pasti. Konsentrasi preparat yang dibuat meliputi lima konsentrasi yang melingkupi konsentrasi uji contoh 34.60, 40.00, 49.40, 60.00, dan 76.90. Analisis dilakukan pada masing-masing preparat menggunakan metode yang akan divalidasi dengan jumlah pengulangan sebanyak tujuh kali ulangan. Korelasi antara respon analitik rerata yang didapat dengan konsentrasi teoritis analat dalam preparat dapat dihitung.
Batas Kelinearan
Dibuat preparat deret kalibrasi menggunakan blanko matriks yang ke dalamnya ditambahkan secara kuantitatif analat standar yang diketahui konsentrasinya secara pasti. Konsentrasi preparat yang dibuat meliputi 12 konsentrasi, yaitu: 5, 10, 15, 20, 25, 30, 35, 40, 45, 50, 55, dan 60 ppb. Analisis dilakukan pada masing-masing preparat menggunakan metode yang akan divalidasi dengan jumlah pengulangan sebanyak enam kali pembacaan. Korelasi antara respon analitik rerata yang didapat dengan konsentrasi teoritis analat dalam preparat yang masih menunjukkan kelinearan dapat dihitung. Ketelitian
Uji ketelitian dengan keterulangan (repeatability), analisis dilakukan pada konsentrasi 49.40 ppb konsentrasi uji dengan metode yang akan divalidasi. Analisis dilakukan sebanyak tujuh kali ulangan oleh analisis yang sama pada waktu yang berdekatan, menggunakan peralatan dan pereaksi yang sama. Berdasarkan hasil analisis berulang tersebut dihitung %RSD (% Relative
Standar Deviation) dengan persamaan:
SD =
(
)
1 n x x 1 2 i − ∑ − = n i % RSD = x 10000 x SD dengan SD = standar deviasix
= kadar analat rerata KetepatanDibuat blanko matriks contoh berdasarkan perolehan kembali. Analisis dilakukan pada tiga konsentrasi yang ditambahkan analat kedalamnya sebesar 34.60, 49.40, dan 76.90 ppb. Kemudian analisis dilakukan berulang terhadap contoh tersebut sebanyak tujuh kali ulangan untuk tiap konsentrasi menggunakan metode yang akan divalidasi. Hasil diukur dan dibandingkan terhadap konsentrasi analat teoritis. Metode dikatakan akurat jika didapatkan persen perolehan kembali sesuai syarat keberterimaan. PK (%) = x 10000 c b a− dengan
yang terukur b = konsentrasi sampel
c = konsentrasi standar teoritis yang ditambahkan
Limit Deteksi dan Limit Kuantitasi
Analisis dilakukan menggunakan blanko matriks sebanyak sepuluh kali ulangan. Contoh yang digunakan adalah limbah cair, kemudian dianalisis menggunakan metode yang akan divalidasi. Penentuan limit deteksi (LD) dan limit kuantitasi (LK) dapat dilakukan dengan menghitung kadar yang didapat dari respons blanko matriks tersebut dari deret standar. Kemudian dihitung rerata dan standar deviasi dari kadar-kadar tersebut.
LD = S SD 3 LK = S SD 10 dengan
SD = standar deviasi respon blanko matriks S = rerata kemiringan kurva standar Selektivitas
Analisis dilakukan terhadap blanko matriks dan konsentrasi uji pada 49.40 ppb menggunakan metode yang akan divalidasi, masing-masing dilakukan sebanyak tujuh kali ulangan. Metode dikatakan memiliki selektivitas yang baik jika respon analitik yang didapat dari blanko matriks = 2% dari respon analitik konsentrasi uji 49.40 ppb.
Ketangguhan Metode (robustness)
Analisis dilakukan dengan membandingkan konsentrasi uji pada 49.40 ppb dengan larutan standar dengan variasi waktu kestabilan. Kedua larutan tersebut masing-masing dianalisis dengan metode yang akan divalidasi dan diukur dengan selang waktu 15 menit selama 1 jam. Kemudian dilakukan uji beda nyata terhadap data pengukuran awal.
Analisis statistik
Uji perbandingan dalam evaluasi akurasi suatu metode menjadi alternatif yang dapat dilakukan jika terdapat metode analisis lain yang telah diakui dan tersedia data validasinya. Nilai kepercayaan yang digunakan adalah 95% (a = 0.05) dan 99% (a = 0.01). Untuk membandingkan tingkat persisi
kedua metode lakukan uji F dua arah terhadap SD (standar deviasi) masing-masing kumpulan data; Ho: SD1 = SD2; H1: SD1 ? SD2.
Kesimpulan ditarik sesuai dengan hipotesis berdasarkan nilai F hitung. Jika nilai Fhitung <
Ftabel maka hipotesis nol (H0) diterima, tetapi
jika nilai Fhitung > Ftabel maka H0
ditolak/hipotesis satu (H1) diterima. Untuk
membandingkan tingkat akurasi kedua metode lakukan uji t-student dua arah terhadap rata-rata masing-masing kesimpulan data; Ho:
x
1=2
x
; H1:x
1?x
2. Kesimpulan ditarik sesuaidengan hipotesis berdasarkan nilai t hitung. Jika nilai thitung < ttabel maka hipotesis nol (H0)
diterima, tetapi jika nilai thitung > ttabel maka H0
ditolak/hipotesis satu (H1) diterima. Begitu
juga untuk uji ketangguhan metode, kedua variasi tersebut dibandingkan berdasarkan perhitungan secara statistik, yaitu uji-F dan uji-tstudent. Fhitung = 2 2 2 1 SD SD Sgabungan = 2) n (n 1)SD (n 1)SD (n 2 1 2 2 2 2 1 1 − + − + − thitung = 2 1 gabungan 2 1 n 1 n 1 S x x + × − db = n1 + n2 – 2 dengan
Keterangan : SD = Standar deviasi n = jumlah data
x
= konsentrasi rerataPEMBAHASAN
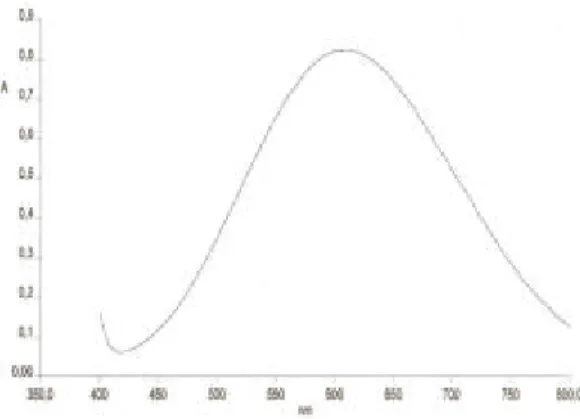
Pengukuran Panjang Gelombang Berdasarkan penelitian ini, spektrum absorbsi pada konsentrasi sianida 15 ppb diperoleh pada panjang gelombang (? maks) 606 nm. Serapan pada 606 nm untuk larutan sianida dengan konsentrasi 15 ppb sebesar 0.8209. Spektrum absorbsi sianida dengan ninhidrin tertera pada Gambar 1Gambar 2 Spektrum absorpsi sianida dengan ninhidrin.
Validasi Metode Pengujian Sianida Metode pengujian kadar sianida dalam limbah cair secara spektroskopi UV-Vis dikembangkan dari metode Nagaraja et al (2002). Pada metode ini, ninhidrin bereaksi dengan sianida dalam keadaan basa dan membentuk hindrindantin yang akan terurai karena keberadaan natrium karbonat. Ketika NaOH ditambahkan akan terbentuk larutan berwarna biru. Reaksi antara sianida dan ninhidrin dapat dilihat pada Gambar 3.
Gambar 3 Reaksi sianida dengan ninhidrin (Nagaraja et al. 2002)
Sebelum metode ini dipakai secara rutin untuk pengujian, metode ini harus divalidasi terlebih dahulu agar hasil pengukuran bersifat sah dan diakui. Suatu metode dikatakan absah jika memenuhi batas penerimaan parameter-parameter validasi yang berlaku. Parameter-parameter validasi yang diuji antara lain, linearitas, batas kelinearan, ketelitian, ketepatan, limit deteksi, limit kuantitasi, selektivitas, dan ketangguhan metode. Nilai
parameter tersebut dibandingkan dengan batas penerimaan parameter validasi yang ditetapkan.
Linearitas ditent ukan dengan membuat lima konsentrasi dari sianida sehingga menggambarkan hubungan antara konsentrasi terhadap absorbansnya. Perolehan penentuan linearitas dari metode pengujian sianida ditampilkan pada Gambar 4. Lima konsentrasi ini melingkupi konsentrasi uji contoh, yaitu 34.60, 40.00, 49.40, 60.00, dan 76.90 ppb dan masing-masing sebanyak tujuh kali ulangan. Metode spektrofotometri untuk pengujian kadar sianida dengan pereaksi ninhidrin memenuhi syarat linearitas yang diterima, yaitu lebih besar dari 0.9950 (AOAC 2002). Meningkatnya konsentrasi sianida akan menghasilkan nilai absorbans yang semakin besar pula. Nilai r yang diperoleh dari metode pengujian sianida adalah 0.9968, sehingga dapat dikatakan bahwa metode tersebut menghasilkan kelinearan yang baik.
Gambar 4 Kurva standar hubungan antara konsentrasi sianida dan absorbans.
Batas kelinearan pada prinsipnya sama dengan linearitas, hanya saja konsentrasi uji yang digunakan diatas konsentrasi uji yang diperkirakan sudah tidak memberikan respon yang linear. Konsentrasi uji contoh yang digunakan dari 0-60 ppb, dengan masing-masing konsentrasi enam kali pembacaan. Penentuan batas kelinearan dari metode pengujian sianida ditampilkan pada Gambar 5, 6 dan 7. Pada konsentrasi sianida 0-60 ppb didapatkan koefisien korelasi sebesar 0.9862. Dari kurva hubungan antara konsentrasi sianida terhadap absorbans dalam kisaran
konsentrasi 0-60 ppb, dapat dilihat
ppb. Pada kurva hubungan antara konsentrasi sianida terhadap absorbans dalam kisaran konsentrasi 0-55 ppb memberikan nilai r yang sudah tidak lagi linear, yaitu 0.9860, sedangkan dari kurva hubungan antara sianida terhadap absorbans dari kisaran konsentrasi sianida 0-50 ppb memberikan hubungan linear terhadap respon analitik, dengan nilai r sebesar 0.9952. Nilai r dari kisaran konsentrasi 0-50 ppb memenuhi syarat linearitas yang diterima, yaitu lebih besar dari 0.9950 (AOAC 2002). Sehingga dalam metode pengujian sianida dengan pereaksi ninhidrin memberikan batas kelinearan pada konsentrasi sianida 0-50 ppb, dan diatas konsentrasi tersebut nilai r sudah menunjukkan ketidaklinearan lagi.
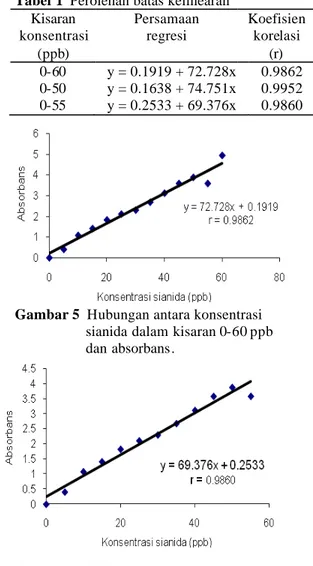
Tabel 1 Perolehan batas kelinearan Kisaran konsentrasi (ppb) Persamaan regresi Koefisien korelasi (r) 0-60 y = 0.1919 + 72.728x 0.9862 0-50 y = 0.1638 + 74.751x 0.9952 0-55 y = 0.2533 + 69.376x 0.9860 Gambar 5 Hubungan antara konsentrasi
sianida dalam kisaran 0-60 ppb dan absorbans.
.
Gambar 6 Hubungan antara konsentrasi sianida dalam kisaran konsentrasi 0-55 ppb dan absorbans.
Gambar 7 Hubungan antara konsentrasi sianida dalam kisaran konsentrasi 0-50 ppb dan absorbans.
Ketelitian metode pengujian sianida dilakukan dengan menggunakan blanko matriks yang ditambahkan sianida kedalamnya pada konsentrasi uji 49.40 ppb kemudian diukur sebanyak tujuh kali pada hari yang sama. Berdasarkan hasil yang diperoleh dari penelitian, metode pengujian mempunyai ketelitian yang sedang. Hal ini ditunjukkan dengan persentase RSD sebesar 4.58% yang masuk ke dalam kriteria yang ditetapkan oleh AOAC (2002) untuk dapat disebut sebagai metode yang menghasilkan ketelitian sedang, dengan batas penerimaan % RSD 2-5. Perolehan dan perhitungan parameter ketelitian disajikan pada Lampiran 4.
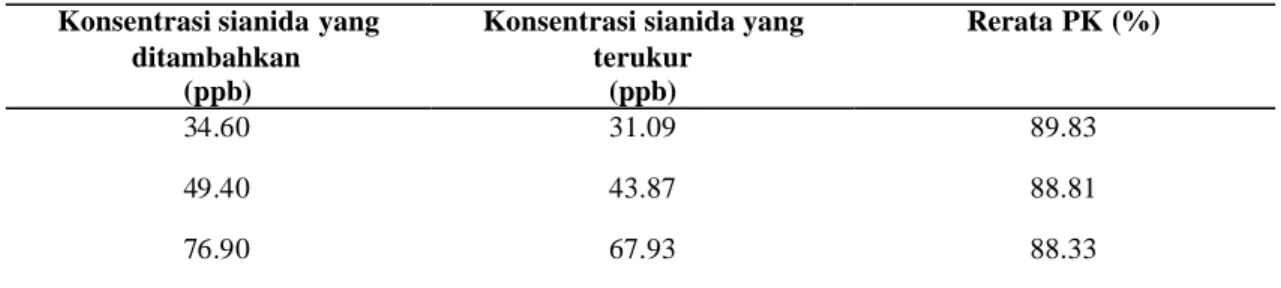
Parameter ketepatan suatu metode dapat dilihat berdasarkan nilai PK standar yang ditambahkan ke dalam contoh dengan menggunakan metode penambahan standar. Analisis dilakukan menggunakan konsentrasi uji 34.60, 49.40, dan 76.90 dengan masing-masing sebanyak tujuh kali ulangan. Batas penerimaan ketepatan suatu metode berdas arkan AOAC (2002), yaitu PK berkisar antara 80 hingga 110%. Nilai PK yang dihasilkan dari metode pengujian sianida masing-masing pada konsentrasi 34.60, 49.40, dan 76.90 ppb adalah 89.83%, 88.81%, dan 88.33%. Perolehan uji ketepatan dari metode pengujian sianida memperlihatkan bahwa kisaran PK memenuhi batas penerimaan AOAC. Berdasarkan dari nilai PK yang dapat pengujian sianida memperlihatkan bahwa kisaran PK memenuhi batas penerimaan AOAC. Berdasarkan dari nilai PK dapat dilihat bahwa konsentrasi sianida yang terukur cenderung kurang dari nilai sebenarnya, hal ini
Tabel 2 Hasil uji ketepatan
dikarenakan sifat dari sianida yang tidak stabil juga mudah menguap dan kemungkinan oleh adanya matriks (selain senyawa target) yang ikut bereaksi dengan ninhidrin sehingga mempengaruhi hasil pengukuran konsentrasi total. Perolehan parameter ketepatan dapat
dilihat pada Tabel 2 sedangkan untuk
perhitungan pada Lampiran 5.
Parameter limit deteksi (LD) sangat diperlukan dalam validasi metode, karena apabila nilai konsentrasi analat berada di bawah limit deteksi suatu metode, maka keberadaan analat dapat tidak terdeteksi atau data konsentrasi yang diperoleh menjadi tidak sesuai dengan kenyataan. Nilai LD dan LK ditentukan berdasarkan simpangan baku dari respon blanko matriks dan rerata kemiringan dari kurva standar. LD pada analisis sianida diperoleh sebesar 0.0967 ppb, sedangkan LK diperoleh sebesar 0.3222 ppb. Hal ini menandakan konsentrasi terendah sianida yang dapat terdeteksi dengan metode ini adalah 0.0967 ppb, sedangkan konsentrasi terendah sianida yang dapat terkuantitasi adalah 0.3222 ppb. Persamaan dari deret standar sianida dapat dilihat pada lampiran. Perolehan dan perhitungan parameter limit deteksi dan limit kuantitasi dapat dilihat pada Lampiran 6. Selektivitas merupakan salah satu parameter validasi yang diuji untuk meyakinkan bahwa respon analitik hanya berasal dari analat. Selektivitas diukur dengan membandingkan respon analitik antara blanko matriks dengan konsentrasi uji 49.40 ppb yang dilakukan berulang sebanyak tujuh kali. Metode memiliki selektivitas yang baik jika respon analitik yang didapat dari blanko matriks = 2% dari respon analitik konsentrasi uji 49.40 ppb. Dari data yang diperoleh didapatkan bahwa selektivitas dihasilkan metode pengujian sianida adalah 0.26%. Hal ini menunjukkan bahwa metode ini memiliki
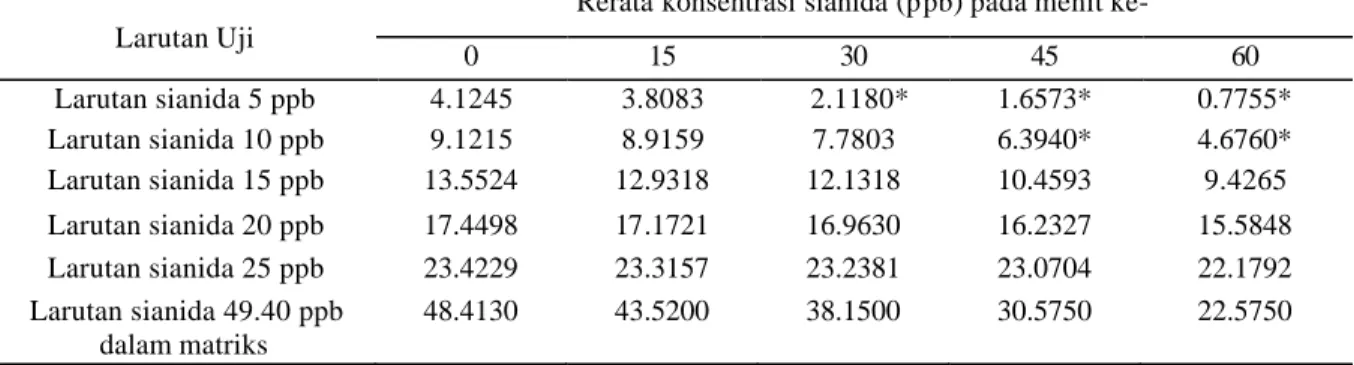
selektivitas yang baik, dan juga matriks tidak memberikan pengaruh yang berarti terhadap analat. Perolehan perhitungan parameter selektivitas disajikan pada Lampiran 7. Ketangguhan metode dalam penelitian ini dilakukan untuk melihat pengaruh waktu kestabilan terhadap larutan standar dan matriks. Pengukuran dilakukan setiap 15 menit sekali selama 1 jam. Pada larutan standar dilakukan sebanyak 6 pembacaan dengan konsentrasi sianida 5-25 ppb, sedangkan pada matriks digunakan level konsentrasi uji 49.40 ppb sebanyak empat kali ulangan. Kemudian dilakukan uji beda nyata, antara nilai pengukuran pertama kali dengan nilai yang telah didiamkan setiap 15 menit. Perolehan ketangguhan metode dapat di lihat pada tabel 3 dan 4. Berdasarkan nilai pengukuran ketangguhan metode, pada larutan standar menunjukkan bahwa semakin tinggi konsentrasi sianida,maka kestabilan larutan akan semakin lama. Pada konsentrasi sianida 5 ppb menunjukkan pada menit ke-15 masih menunjukkan ketelitian yang baik, namun pada menit ke-30 menunjukkan ketelitian dan ketepatan yang berbeda nyata pada selang kepercayaan 95% namun pada peada selang kepercayaan 99% menunjukkan hasil tidak berbeda nyata.
Pada konsentrasi sianida 25 ppb menunjukkan hingga menit ke-45 masih memiliki ketelitian dan ketepatan yang baik. Hal ini disebabkan pengaruh dari sifat sianida yang tidak stabil dan mudah menguap sehingga pada konsentrasi kecil, sianida sudah tidak dapat terbaca. Pada konsentrasi uji 49.40 ppb memberikan hasil yang berbeda dengan larutan standar, pada menit ke-60 larutan masih memberikan ketelitian yang baik, sedangkan pada menit ke-15 menunjukkan hasil ketepatan yang sudah berbeda nyata. Hal ini disebabkan pada konsentrasi uji 49.40 Konsentrasi sianida yang
ditambahkan (ppb)
Konsentrasi sianida yang terukur (ppb) Rerata PK (%) 34.60 31.09 89.83 49.40 43.87 88.81 76.90 67.93 88.33
ppbterdapat matriks (selain sianida) yang ikut bereaksi dengan ninhidrin sehingga mempengaruhi konsentrasi sianida. Peroleh parameter ketangguhan metode dapat dilihat
pada tabel 3 dan tabel 4, sedangkan
perhitungannya disajikan pada Lampiran 8.
Tabel 3 Hasil uji F pada ketangguhan metode Larutan Uji
Rerata konsentrasi sianida (ppb) pada menit ke-
0 15 30 45 60 Larutan sianida 5 ppb 4.1245 3.8083 2.1180* 1.6573* 0.7755* Larutan sianida 10 ppb 9.1215 8.9159 7.7803 6.3940* 4.6760* Larutan sianida 15 ppb 13.5524 12.9318 12.1318 10.4593 9.4265 Larutan sianida 20 ppb 17.4498 17.1721 16.9630 16.2327 15.5848 Larutan sianida 25 ppb 23.4229 23.3157 23.2381 23.0704 22.1792 Larutan sianida 49.40 ppb dalam matriks 48.4130 43.5200 38.1500 30.5750 22.5750
Keterangan: *) Berbeda nyata pada a = 0.05 Tabel 4 Hasil uji t pada ketangguhan metode Larutan Uji
Rerata konsentrasi sianida (ppb) pada menit ke-
0 15 30 45 60 Larutan sianida 5 ppb 4.1245 3.8083** 2.1180** 1.6573** 0.7755** Larutan sianida 10 ppb 9.1215 8.9159** 7.7803** 6.3940** 4.6760** Larutan sianida 15 ppb 13.5524 12.9318 12.1318** 10.4593** 9.4265** Larutan sianida 20 ppb 17.4498 17.1721 16.9630 16.2327** 15.5848** Larutan sianida 25 ppb 23.4229 23.3157 23.2381 23.0704 22.1792** Larutan sianida 49.40 ppb dalam matriks 48.4130 43.5200** 38.1500** 30.5750** 22.5750**
Keterangan: **) Berbeda nyata pada a = 0.01
SIMPULAN DAN SARAN
SimpulanMetode pengujian sianida dengan pereaksi ninhidrin mempunyai linearitas yang baik, yaitu 0.9968. Pada uji batas kelinearan menunjukkan bahwa sampai dengan konsentrasi sianida 50 ppb masih menghasilkan linearitas yang baik, diatas konsentrasi 50 ppb linearitas yang dihasilkan sudah tidak baik. Berdasarkan nilai persentase RSD untuk parameter ketelitian metode pengujian sianida dengan pereaksi ninhidrin mempunyai ketelitian sebesar 4.58%. Nilai Perolehan Kembali berturut-turut untuk konsentrasi 34.60, 49.40, dan 76.90 ppb adalah 89.83%, 88.81%, dan 88.33%. Metode pengujian sianida dengan pereaksi ninhidrin menhasilkan nilai limit deteksi dan limit
kuantitasi berturut-turut adalah 0.0967 ppb dan 0.3222 ppb. Pada uji selektivitas, didapatkan bahwa metode pengujian sianida dengan pereaksi ninhidrin memiliki selektivitas yang baik, yaitu selektivitas = 2%. Pada parameter ketangguhan metode, diperoleh bahwa metode pengujian sianida dengan pereaksi ninhidrin sangat dipengaruhi oleh waktu, konsentrasi analat, dan matriks. Menurut kriteria yang ditetapkan oleh Association of Official Analytical Chemist (AOAC) validasi metode
pengujian kadar sianida secara spektroskopi UV-Vis dapat dikatakan memadai untuk menghasilkan data analisis yang absah.
Saran
Perlu dilakukan uji terhadap parameter ketidakrataan (ruggedness), kepastian,
ketidakpastian dan kalibrasi alat secara berkala pada validasi metode pengujian sianida dengan pereaksi ninhirin dengan spektroskopi UV-Vis. Uji ketertiruan untuk parameter ketelitian juga perlu dilakukan untuk mengetahui pengaruh dari kerja analis, kondisi instrumen, dan waktu analisis yang berbeda dalam laboratorium yang berbeda.
DAFTAR PUSTAKA
Aisjah G. 1986. Biokimia 1. Jakarta: PT Gramedia.
[AOAC] Association of Official Analytical Chemist. 2002. AOAC International
Methods Committee Guidelines for Validation of Qualitative and Quantitative Food Microbiological Official Methods of Analysis. [terhubung
berkala]. J AOAC Int. 85:5.
[APHA] America Public Health Association.
1992. Standard Methods for the
Examination of Water and Wastewater .
18th ed. Washington DC: USA.
[ASEAN] Association of South East Asian Nation. 2000. Operational Manual for
Implementation of GMP. Jakart a:
ASEAN.
[BPOM RI] Badan Pengawas Obat dan Makanan Republik Indonesia. 2004.
Monografi Ekstrak Tumbuhan Obat Indonesia Volume 1. Jakarta: BPOM.
Brown DW, Floyd AJ, Sainsbury M. 1988.
Organic Spectroscopy. New York: John
Wiley & Sons.
Chan CC. 2004. Potency Method Validation. Di dalam: Chan CC, Lee YC, Lam H, Zhang XM, editor. Analytical method
Validation and Instrument Performance Verification. New Jersey: John Wiley &
Sons.
Day RA, Underwood AL. 1981. Analisis Kimia Kuantitatif. Terjemahan dari R Soendoro. Jakarta:Erlangga. Terjemahan dari
Quantitatif Analysis Chemistry.
[Depkes] Departemen Kesehatan, Ditjen POM. 2001. Petunjuk Operasional Penerapan
CPOB. Ed ke-2. Jakarta.
Harmita. 2004. Petunjuk Pelaksanaan Validasi Metode dan Cara Perhitungannya. [terhubung berkala]. Majalah Ilmu Kefarmasian I (3): 117-135.
Harvey D. 2000. Modern Analytical Chemistry. New York: Mc Graw Hill.
Haslam, S.M. 1995. River Pollution and
Ecological Perspective. Chichester: John
Wiley and Sons.
Green JM. 1996. A Practical Guide to Analytical Methode Validation. Anal
Chem 68:305A-309A
.
[ICH] International Conference on Harmonization. 1995. Text on validation
of analytical Procedures. USA.
Levin S. 2002. Quantitatif Work in HPLC . WWW Forumsci [terhubung berkala]. http://www.forumsci.co.il/HPLC. Miller JN, Miller JM. 2000. Statistics and
Chemometrics for Analytical Chemistry.
4th ed. Harlow: Pearson. USA.
Moore, JW. 1991. Inorganic Contaminants of
Surface Water. New York: Springer
Verlag.
Nagaraja P, Kumar MSH, Yathirajan HS, Prakash JS. 2002. Novel Sensitive
pectrophotometric Method for the trace Determination of Cyanide in Industrial Effluent. J. Anal Sci. 18:1027-1030.
Nur, M A & H. Adijuwana. 1989. Teknik
Pemisahan dalam Analisis Biologi.
Bogor: Pusat Antar Universitas Ilmu Hayati IPB.
Rao, CS. 1992. Environmental Pollution Control Engineering. Wiley Eastern, New Delhi.
Skoog DA, Holler FJ, Timothy AN. 1998.
Principle of Instrumental Analysis . Ed
ke-5. Florida: Harcourt Brace Collage.
Sudjadi. 1983. Penentuan Struktur Senyawa
Lampiran 1 Bagan alir p ercobaan
Metode Pengujian Sianida dengan pereaksi Ninhidrin
Pengukuran secara Spektrofotometri UV-Vis
Kurva Standar
Kadar sianida dari sampel
Validasi Metode Pengujian Sianida dengan Spektroskopi UV-Vis
Linearitas Batas Kelinearan Limit Deteksi dan Limit Kuantitasi Ketepatan
Lampiran 2 Perhitungan lineritas metode pengujian sianida dengan pereaksi ninhidrin
Konsentrasi Teoritis Sianida (ppb) Absorbans Rerata 34.60 1.1300 40.00 1.4077 49.40 1.7216 60.00 2.1364 76.90 2.5154 Persamaan regresi: y = 0.0244 + 33.639x r = 0.9968
Lampiran 3 Penentuan batas kelinearan metode pengujian sianida dengan pereaksi ninhidrin
Konsentrasi sianida (ppb) Absorbans rerata
0 0.0028 5 0.4074 10 1.0802 15 1.4097 20 1.8225 25 2.1050 30 2.2973 35 2.6758 40 3.1105 45 3.5750 50 3.8717 55 3.5764 60 4.9242
Persamaan regresi pada konsentrasi sianida 0-60 ppb: y = 0.1919 + 72.728x r = 0.9862 Persamaan regresi pada konsentrasi sianida 0-55 ppb: y = 0.2533 + 69.376x
r = 0.9860 Persamaan regresi pada konsentrasi sianida 0-50 ppb: y = 0.1638 + 74.751x
Lampiran 4 Penentuan ketelitian metode pengujian sianida dengan pereaksi ninhidrin Pengukuran kurva standar
Konsentrasi (ppb) Absorbans 0 0 4.90 0.1466 10.00 0.6145 14.80 1.0631 19.80 1.4010 24.70 1.8354
Kurva standar sianida
Penentuan simpangan baku relatif pada penetapan ketelitian
Ulangan Konsentrasi Sianida (ppb) Absorbans
1 50.20 1.8307 2 49.50 1.8000 3 47.30 1.7161 4 44.30 1.6002 5 48.10 1.7476 6 45.00 1.6287 7 47.60 1.7280 Rerata±Simpangan baku: 4.74x10-2±2.17x10-3 Contoh perhitungan:
Persamaan kurva standar: y = -0.1136 + 77.387x, r = 0.9938 Konsentrasi sianida: 1.8307 = -0.1136 + 77.387x x = 50.20 ppb % RSD = x 10000 X SD = x 100% 2 4.74.10 3 2.17.10 − − = 4.58%
Lampiran 5 Penentuan ketepatan pada metode pengujian sianida dengan pereaksi ninhidrin Pengukuran kurva standar
Konsentrasi (ppb) Absorbans 0 0 4.90 0.1466 10.00 0.6145 14.80 1.0631 19.80 1.4010 24.70 1.8354
Kurva standar sianida Penentuan ketepatan Konsentrasi-ulangan Standar yang ditambahkan (ppb) Konsentrasi sianida terukur (ppb) Absorbans Perolehan Kembali (%) Rerata PK (%) 34.60-1 34.60 31.80 1.1154 91.80 89.83 34.60-2 32.50 1.1421 93.80 34.60-3 31.30 1.0975 90.46 34.60-4 30.70 1.0742 88.72 34.0-5 31.30 1.0985 90.54 34.60-6 28.60 0.9933 82.70 34.60-7 31.40 1.1022 90.81 49.40-1 49.40 47.30 1.7161 95.75 88.81 49.40-2 44.30 1.6002 89.66 49.40-3 41.00 1.4745 83.08 49.40-4 41.60 1.4961 84.21 49.40-5 45.00 1.6287 91.15 49.40-6 47.60 1.7280 96.34 49.40-7 40.30 1.4443 81.50 76.90-1 76.90 68.00 2.5173 88.42 88.33 76.90-2 67.40 2.4963 87.71 76.90-3 70.80 2.6300 92.05 76.90-4 68.50 2.5355 89.03 76.90-5 67.90 2.5134 88.29 76.90-6 66.30 2.4528 86.25 76.90-7 66.60 2.4625 86.58
Lanjutan Lampiran 5 Penentuan ketepatan pada metode pengujian sianida dengan pereaksi ninhidrin Contoh perhitungan:
Persamaan kurva standar: y = -0.1136 + 77.387x, r = 0.9938 Konsentrasi sianida: 1.7161 = -0.1136 + 77.387x x = 47.30 ppb % Perolehan kembali = x 10000 c b a− = x 10000 49.4 0 47.3− = 95.75% Keterangan:
a = konsentrasi sampel + konsentrasi standar yang terukur b = konsentrasi sampel = 0
Lampiran 6 Limit deteksi dan limit kuantitasi metode pengujian sianida dengan pereaksi ninhidrin Pengukuran kurva standar
Konsentrasi (ppb) Absorbans 0 0 50 0.2924 10 0.6705 15 1.1301 20 1.3579 25 1.7698
Kurva standar sianida Data pengukuran blanko matriks
Ulangan Absorbans 1 0.0063 2 0.0069 3 0.0065 4 0.0027 5 0.0034 6 0.0047 7 0.0043 8 0.0097 9 0.0038 10 0.0086
Simpangan baku blanko matriks: 2.30x10-3 LD = S 3SD = 71.458 3 2.30.10 x 3 − = 0.0967 ppb LK = S 10SD = 71.458 3 2.30.10 x 10 − = 0.3222 ppb Keterangan: SD = Standar deviasi blanko matriks
Lampiran 7 Penentuan selektivitas pada metode pengujian sianida dengan pereaksi ninhidrin
Ulangan Absorbans
Blanko matriks Konsentrasi uji 49.40 ppb 1 0.0063 1.7161 2 0.0065 1.6002 3 0.0027 1.7476 4 0.0034 1.7280 5 0.0047 1.6287 6 0.0043 1.8307 7 0.0038 1.8000 Rata-rata 0.0045 1.7216
Contoh perhitungan: selektivitas = x 10000 2 x 1 x = x 10000 1.7216 0.0045 = 0.26%
Lampiran 8 Penentuan ketangguhan metode pada pengujian sianida dengan pereaksi ninhidrin Penentuan ketangguhan metode dalam larutan standar
STD 5 ppb Waktu (menit) Ulangan 0 15 30 45 60 1 4.1233 3.8233 2.1142 1.6521 0.7807 2 4.1325 3.8245 2.1145 1.6544 0.7783 3 4.1453 3.8241 2.1256 1.6632 0.7760 4 4.1566 3.8253 2.1126 1.6549 0.7736 5 4.1332 3.8367 2.1167 1.6528 0.7701 6 4.0562 3.7156 2.1246 1.6665 0.7745 Rerata 4.1245 3.8083 2.1180 1.6573 0.7755 SD 0.0354 0.0457 0.0056 0.0060 0.0037 Fhit 0.6013 39.4645 34.6533 90.9967 Ftabel (a=0.05) 7.1460
Penerimaan F Tidak Berbeda Nyata Berbeda Nyata Berbeda Nyata Berbeda Nyata
Ftabel (a=0.01) 10.967
Penerimaan F
Tidak Berbeda Nyata
Tidak Berbeda
Nyata Tidak Berbeda Nyata
Tidak Berbeda Nyata
S 0.0409 0.0325 0.0058 0.0050
Thit 13.4067 106.8207 168.2619 230.4087
Ttabel (a=0.05) 2.23
Penerimaan T Berbeda Nyata Berbeda Nyata Berbeda Nyata Berbeda Nyata
Ttabel (a=0.01) 3.17 Penerimaan T Berbeda Sangat Nyata Berbeda Sangat Nyata Berbeda Sangat Nyata Berbeda Sangat Nyata STD 10 ppb Waktu (menit) Ulangan 0 15 30 45 60 1 9.1251 8.9135 7.7943 6.3956 4.6704 2 9.1256 8.9112 7.8365 6.3951 4.6701 3 9.1243 8.9157 7.7622 6.3932 4.6716 4 9.1286 8.9210 7.7625 6.3925 4.6705 5 9.1121 8.9217 7.7617 6.3921 4.6711 6 9.1132 8.9125 7.7645 6.3955 4.6700 Rerata 9.1215 8.9159 7.7803 6.3940 4.6706 SD 0.0070 0.0045 0.0303 0.0016 0.0006 Fhit 2.4751 0.0534 19.7437 129.0477 Ftabel (a=0.05) 7.1460
Penerimaan F Tidak Berbeda Nyata Tidak Berbeda Nyata Berbeda Nyata Berbeda Nyata
Ftabel (a=0.01) 10.967
Penerimaan F Tidak Berbeda Nyata Tidak Berbeda Nyata Tidak Berbeda Nyata Tidak Berbeda Nyata
S 0.0059 0.0220 0.0051 0.0032
Thit 60.6695 105.5948 930.6194 1550.6292
Ttabel (a=0.05) 2.23
Penerimaan T Berbeda Nyata Berbeda Nyata Berbeda Nyata Berbeda Nyata
Ttabel (a=0.01) 3.17
STD 15 ppb Waktu (menit) Ulangan 0 15 30 45 60 1 13.5891 12.2771 11.8075 11.0176 10.9968 2 14.0167 13.9458 12.9123 10.8352 9.2144 3 14.0420 13.8003 12.9041 10.8710 9.3239 4 13.2123 12.5691 11.2699 9.3604 8.0457 5 13.0568 12.7217 12.8535 10.8487 10.0329 6 13.3972 12.2765 11.0433 9.8233 8.9453 Rerata 13.5524 12.9318 12.1318 10.4593 9.4265 SD 0.4104 0.7505 0.8671 0.6908 1.0027 Fhit 0.2990 0.2240 0.3529 0.1675 Ftabel (a=0.05) 7.1460
Penerimaan F Tidak Berbeda Nyata Tidak Berbeda Nyata Tidak Berbeda Nyata Tidak Berbeda Nyata
Ftabel (a=0.01) 10.967
Penerimaan F Tidak Berbeda Nyata Tidak Berbeda Nyata Tidak Berbeda Nyata Tidak Berbeda Nyata
S 0.6048 0.6783 0.5682 0.7661
Thit 1.7772 3.6273 9.4290 9.3279
Ttabel (a=0.05) 2.23
Penerimaan T Tidak Berbeda Nyata Berbeda Nyata Berbeda Nyata Berbeda Nyata
Ttabel (a=0.01) 3.17
Penerimaan T Tidak Berbeda Nyata Berbeda Sangat Nyata Berbeda Sangat Nyata Berbeda Sangat Nyata
STD 20 ppb Waktu (menit) Ulangan 0 15 30 45 60 1 18.0251 17.8067 17.5828 16.0129 15.8207 2 17.3415 17.0018 16.8778 16.0270 15.7683 3 17.6289 17.3134 17.1737 16.8324 15.2134 4 17.6723 17.2890 17.0062 16.4247 15.0535 5 17.0046 16.8457 16.5702 16.0561 15.7886 6 17.0264 16.7758 16.5675 16.0432 15.8643 Rerata 17.4498 17.1721 16.9630 16.2327 15.5848 SD 0.4004 0.3818 0.3869 0.3329 0.3238 Fhit 1.0999 1.0714 1.4466 1.5291 Ftabel (a=0.05) 7.1460
Penerimaan F Tidak Berbeda Nyata Tidak Berbeda Nyata Tidak Berbeda Nyata Tidak Berbeda Nyata
Ftabel (a=0.01) 10.967
Penerimaan F
Tidak Berbeda
Nyata Tidak Berbeda Nyata Tidak Berbeda Nyata Tidak Berbeda Nyata
S 0.3912 0.3937 0.3682 0.3642
Thit 1.2295 2.1414 5.7247 8.8706
Ttabel (a=0.05) 2.23 Penerimaan T
Tidak Berbeda
Nyata Tidak Berbeda Nyata Berbeda Nyata Berbeda Nyata
Ttabel (a=0.01) 3.17
Penerimaan T
Tidak Berbeda
Nyata Tidak Berbeda Nyata Berbeda Sangat Nyata
Berbeda Sangat Nyata
STD 25 ppb Waktu (menit) Ulangan 0 15 30 45 60 1 23.6231 23.5522 23.4905 23.3869 22.3345 2 23.3157 23.2021 23.1164 22.4745 21.9971 3 23.6371 23.4564 23.3977 23.2926 21.9399 4 23.5234 23.4783 23.3894 23.2902 21.9257 5 23.2368 23.1045 23.0070 22.9948 22.5567 6 23.2012 23.1007 23.0278 22.9835 22.3214 Rerata 23.4229 23.3157 23.2381 23.0704 22.1792 SD 0.1956 0.2029 0.2119 0.3365 0.2614 Fhit 0.9293 0.8522 0.3379 0.5602 Ftabel (a=0.05) 7.146
Penerimaan F Tidak Berbeda Nyata Tidak Berbeda Nyata Tidak Berbeda Nyata Tidak Berbeda Nyata
Ftabel (a=0.01) 10.967
Penerimaan F Tidak Berbeda Nyata Tidak Berbeda Nyata Tidak Berbeda Nyata Tidak Berbeda Nyata
S 0.1993 0.2039 0.2752 0.2308
Thit 0.9315 1.5692 2.2180 9.3316
Ttabel (a=0.05) 2.23
Penerimaan T Tidak Berbeda Nyata Tidak Berbeda Nyata Tidak Berbeda Nyata Berbeda Nyata
Ttabel (a=0.01) 3.17
Penerimaan T Tidak Berbeda Nyata Tidak Berbeda Nyata Tidak Berbeda Nyata Berbeda Sangat Nyata
Penentuan ketangguhan metode dalam contoh
Waktu (menit) Ulangan 0' 15' 30' 45' 60' 1 47.2000 44.2000 29.0000 20.8000 12.1000 2 49.3000 41.8000 36.4000 29.2000 22.4000 3 48.7000 41.5000 45.6000 38.1000 29.8000 4 48.4000 46.5000 41.6000 34.2000 26.0000 Rerata 48.4000 43.5000 38.1500 30.5750 22.5750 SD 0.8832 2.3367 7.1691 7.4656 7.6089 Fhit 0.1429 0.0152 0.0140 0.0135 Ftabel a=0.05) 7.1460
Penerimaan F Tidak Berbeda Nyata Tidak Berbeda Nyata Tidak Berbeda Nyata Tidak Berbeda Nyata
Ftabel
(a=0.01) 10.967
Penerimaan F Tidak Berbeda Nyata Tidak Berbeda Nyata Tidak Berbeda Nyata Tidak Berbeda Nyata
Thit 4.8048 3.4759 5.8079 8.2582
Ttabel 2.23
Penerimaan T Berbeda Nyata Berbeda Nyata Berbeda Nyata Berbeda Nyata
Ttabel
(a=0.01) 3.17
Contoh perhitungan ketangguhan metode:
Larutan standar 25 ppb menit ke-15 (a = 0.05) Fhitung = 2 2 SD 2 1 SD = 2 (0.2029) 2 (0.1956) = 0.9293 Ftabel = 7.1460 Hipotesis: Ho: SD1 = SD2 H1: SD1 ? SD2
Fhitung < Ftabel = Terima H0 = SD1 = SD2
= Tidak berbeda nyata
Sgabungan = 2) 2 n 1 (n 2 2 1)SD 2 (n 2 1 1)SD 1 (n − + − + − Sgabungan = 2) 6 (6 2 1)(0.2029) (6 2 1)(0.1956) (6 − + − + − Sgabungan = 0.1993 thitung = 2 n 1 1 n 1 gabungan S 2 x 1 x + × − thitung = 6 1 6 1 0.1993 23.3157 23.4229 + × − thitung = 0.9315 ttabel = 2.23 Hipotesis: Ho:
x
1=x
2 H1:x
1?x
2thitubg < ttabel = Terima H0 =