TUGAS KELOMPOK 1
PENETAPAN KADAR ASAM SALISILAT DENGAN SPEKTROFOTOMETRI VISIBLE
Penetapan Kadar Asam Salisilat dalam krim anti jerawat secara Spektrofotometri Vis 1. Pembuatan Larutan Stok
a. Ditimbang 10,0 mg baku pembanding asam salisilat. Dimasukkan dalam labu takar 25,0 ml, larutkan dalam 2,5 ml etanol.
b. Ditambah aquadest sampai tanda.
2. Penetapan Panjang Gelombang Maksimum
a. Masukkan 1,0 ml larutan stok ke dalam labu takar 10 ml, Ditambah 0,5 ml FeCl3 1%
dalam HCl 1%, tambahkan aquadest sampai tanda.
b. Dengan menggunakan blanko, ukur transmitannya dengan panjang gelombang 400 nm sampai 600 nm.
c. Hasil
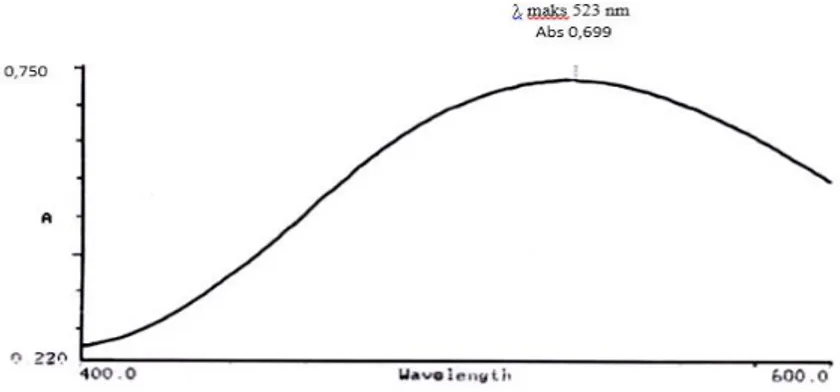
panjang gelombang 523 nm dengan Absorban 0,699
Gambar 1. Kurva Panjang Gelombang Maksimum Asam Salisilat
3. Penentuan operating time
a. Dipipet 1,0 ml larutan stok ke dalam labu takar 10 ml. Ditambah 1,0 ml FeCl3 1%
dalam HCl 1%, tambah aquadest sampai tanda.
b. Pembuatan blanko.
1) Dipipet 1,0 ml etanol dimasukkan dalam labu takar 10 ml, ditambah aquadest sampai tanda (larutan blanko).
2) Dipipet 1,0 ml larutan blanko dimasukkan dalam labu takar 10 ml.
3) Ditambah 0,5 ml FeCl3 1% dalam HCl 1%.
4) Ditambah aquadest sampai tanda.
c. Diukur absorban pada menit 1 sampai 20.
Tabel 1. Data Hasil Operating Time
Menit ke Absorbansi Menit ke Absorbansi
1. 0,690 11. 0,692
2. 0,690 12. 0,690
3. 0,690 13. 0,690
4. 0,691 14. 0,690
5. 0,691 15. 0,691
6. 0,691 16. 0,691
7. 0,690 17. 0,692
8. 0,690 18. 0,693
9. 0,692 19. 0,693
10. 0,692 20. 0,693
4. Pembuatan Kurva Kalibrasi Larutan Asam Salisilat a. Disiapkan 5 buah labu takar 10 ml.
b. Dipipet larutan stok asam salisilat masing-masing 0,5 ml; 1,0 ml; 1,5 ml; 2,0 ml; 2,5 ml; ke dalam labu takar 10 ml sehingga didapatkan larutan seri standar dengan konsentrasi 20 ppm, 40 ppm, 60 ppm, 80 ppm, 100 ppm.
c. Disiapkan blanko.
d. Ke dalam labu takar masing- masing labu takar ditambah 0,5 ml FeCl3 1% dalam HCl 1% kemudian tambah aquadest sampai tanda.
e. Diukur absorban masing-masing dengan menggunakan data panjang gelombang maksimum. Diukur absorban pada panjang gelombang 523 nm.
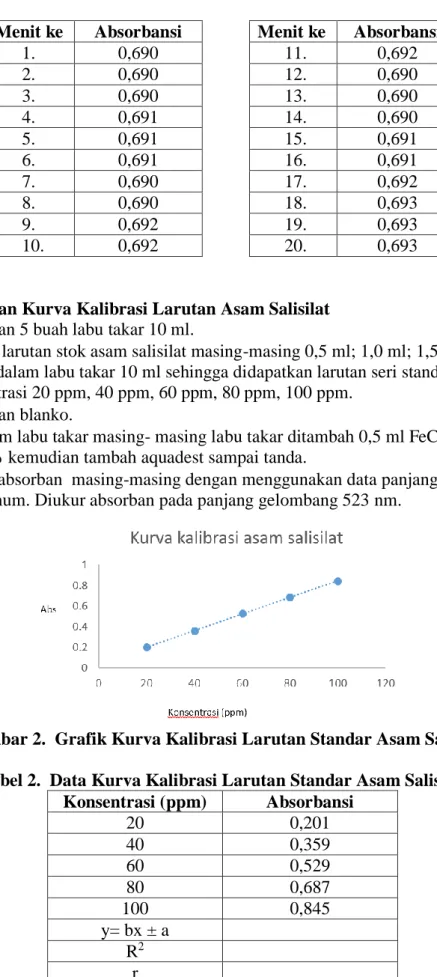
Gambar 2. Grafik Kurva Kalibrasi Larutan Standar Asam Salisilat Tabel 2. Data Kurva Kalibrasi Larutan Standar Asam Salisilat
Konsentrasi (ppm) Absorbansi
20 0,201
40 0,359
60 0,529
80 0,687
100 0,845
y= bx ± a R2
r
5. Penetapan Kadar Sampel
Disiapkan sampel A, B, dan C dalam krim anti jerawat (antiacne) dan setiap sampel dilakukan 3 kali penetapan kadar dengan perlakuan sebagai berikut:
a. Pengukuran absorban sampel
▪ Ditimbang sejumlah cuplikan 1,0 gram sampel asam salisilat dari masing-masing sampel. (3 kali penetapan kadar setiap sampel)
▪ Dimasukkan dalam labu takar 25 ml dilarutkan dengan 5 ml etanol dan ditambah aquadest sampai tanda.
▪ Homogenkan, kemudian disaring dan ditampung filtratnya.
▪ Dipipet 2,0 ml filtrat dimasukkan dalam labu takar 10 ml. Dipipet 0,5 ml FeCl3
1% dalam HCl 1% ditambah aquadest sampai tanda.
b. Diukur absorban sampel pada panjang gelombang 523 nm
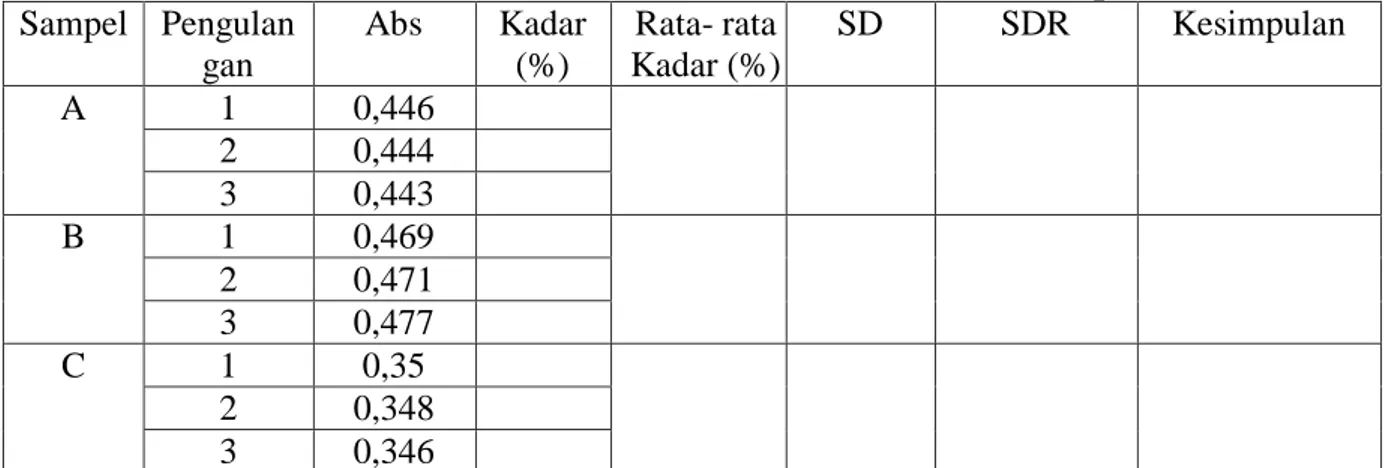
Tabel 3.Data Hasil Konsentrasi Asam Salisilat Pada Sampel Sampel Pengulan
gan
Abs Kadar (%)
Rata- rata Kadar (%)
SD SDR Kesimpulan
A 1 0,446
2 0,444
3 0,443
B 1 0,469
2 0,471
3 0,477
C 1 0,35
2 0,348
3 0,346
Keterangan :
MS = Memenuhi Syarat
Standar : Peraturan Kepala Badan Pengawas Obat dan Makanan RI tahun 2010 yaitu tidak lebih dari 2%.
Sumber:
Niken Feladita, Agustina Retnaningsih, Puji Susanto. Penetapan kadar asam salisilat pada krim wajah anti jerawat yang dijual bebas di daerah kemiling menggunakan metode spektrofotometri uv-vis. Jurnal Analis Farmasi Volume 4, No. 2 Oktober 2019, Hal 101 - 107
TUGAS KELOMPOK 2
PENETAPAN KADAR β-KAROTEN DENGAN SPEKTROFOTOMETRI VISIBLE
Penetapan Kadar β-karoten dalam ekstrak etanol 96% Spirulina maxima secara Spektrofotometri Vis
1. Pembuatan Larutan Stok
a. Ditimbang 10,0 mg baku pembanding β-karoten. Dimasukkan dalam labu takar 10,0 ml, larutkan dalam aseton.
b. Ditambah aseton sampai tanda.
2. Penetapan Panjang Gelombang Maksimum
a. Masukkan 0,2 ml larutan stok ke dalam labu takar 10 ml, ditambah aseton sampai tanda.
b. Dengan menggunakan blanko aseton, ukur absorban dengan panjang gelombang 400 nm sampai 600 nm.
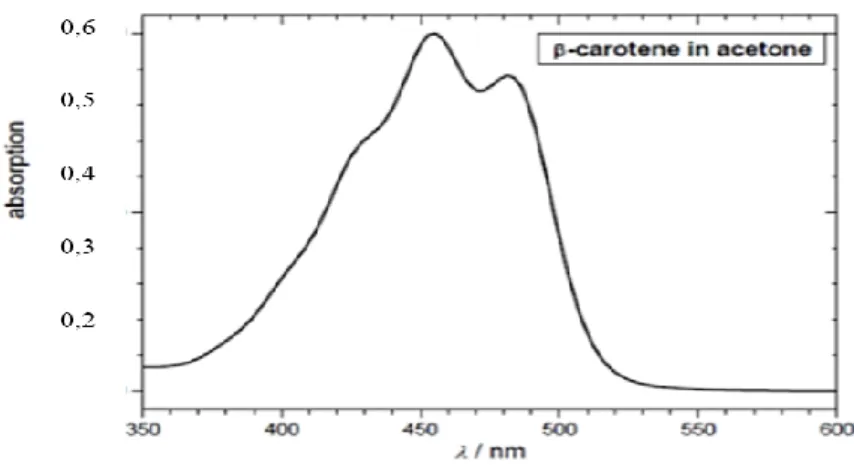
c. Hasil. Panjang gelombang 454 nm dengan Absorban 0,610
Gambar 1. Spektra serapan β-Karoten (Kopczynski et al,2007).
3. Penentuan operating time
a. Masukkan 100 µl larutan stok ke dalam labu takar 5 ml, Ditambah aseton sampai tanda.
Dengan menggunakan blanko aseton.
b. Diukur absorban Panjang gelombang 454nm pada menit 1 sampai 20.
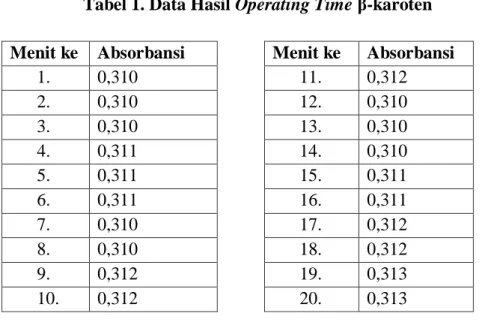
Tabel 1. Data Hasil Operating Time β-karoten
Menit ke Absorbansi Menit ke Absorbansi
1. 0,310 11. 0,312
2. 0,310 12. 0,310
3. 0,310 13. 0,310
4. 0,311 14. 0,310
5. 0,311 15. 0,311
6. 0,311 16. 0,311
7. 0,310 17. 0,312
8. 0,310 18. 0,312
9. 0,312 19. 0,313
10. 0,312 20. 0,313
4. Pembuatan Kurva Kalibrasi Larutan β-karoten a. Disiapkan 6 buah labu takar 5 ml.
b. Dipipet larutan stok β-karoten masing-masing 0,14 ml; 0,16 ml; 0,18 ml; 0,20 ml; 0,22 ml;
dan 0,24 ml; ke dalam labu takar 10 ml sehingga didapatkan larutan seri standar dengan konsentrasi 14 ppm, 16 ppm, 18 ppm, 20 ppm, 22 ppm dan 24 ppm.
c. dilarutkan dengan aseton hingga tanda batas.
d. Diukur absorban pada panjang gelombang 454 nm.
Gambar 2. Grafik Kurva Kalibrasi Larutan Standar β-karoten
Tabel 2. Data Kurva Kalibrasi Larutan Standar β-karoten Konsentrasi (ppm) Absorbansi
14 0,415
16 0,466
18 0,528
20 0,593
22 0,654
24 0,701
y= bx ± a R2
r 5. Penetapan Kadar Sampel
Disiapkan sampel ekstrak Spirulina maxima merek D, E, dan F dan setiap sampel dilakukan 3 kali penetapan kadar dengan perlakuan sebagai berikut:
a. Pengukuran absorban sampel
1) Ditimbang 10,0 mg ekstrak dimasukkan ke dalam labu takar 10 mL dan ditambahkan aseton p.a sampai tanda.
2) Larutan divortek 10 menit kemudan disentrifus 10 menit.
3) Bagian supernatan diambil, disaring dengan kertas saring.
4) Larutan dibaca pada λ maksimal.
5) Penetapan kadar dilakukan replikasi sebanyak 3 kali b. Diukur absorban sampel pada panjang gelombang 454 nm
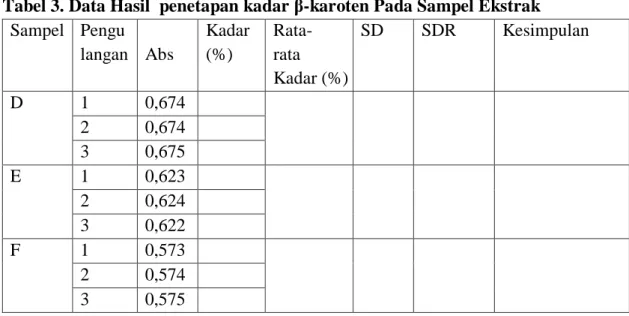
Tabel 3. Data Hasil penetapan kadar β-karoten Pada Sampel Ekstrak Sampel Pengu
langan Abs
Kadar (%)
Rata- rata Kadar (%)
SD SDR Kesimpulan
D 1 0,674
2 0,674
3 0,675
E 1 0,623
2 0,624
3 0,622
F 1 0,573
2 0,574
3 0,575
Sumber
Siti Fatmawati Fatimah, Vani Aisyah, Laela Hayu Nurani, Citra Ariyani Edityaningrum. Validasi metode analisis β-karoten dalam ekstrak etanol 96% spirulina maxima dengan spektrofotometri visibel. Fakultas Farmasi, Universitas Ahmad Dahlan Yogyakarta. Media Farmasi Vol. 15 No.1 Maret 2018 : 1-13
TUGAS KELOMPOK 3
PENETAPAN KADAR SENYAWA Fe2+ /BESI DENGAN SPEKTROFOTOMETRI VISIBLE
Penetapan Kadar besi dalam sediaan tablet multivitamin secara Spektrofotometri Vis
1. Pembuatan Larutan untuk Pereaksi warna Pereaksi yang disiapkan adalah
a. dapar ammonium asetat pH 3,3 b. asama klorida pekat
c. hidroksilamin HCl d. 1,10- fenantrolin
2. Pembuatan Larutan Stok
a. Ditimbang 10,0 mg baku pembanding Fe(NO3)2. Dimasukkan dalam labu takar 10,0 ml, larutkan dalam akuades sampai tanda batas. Larutan Baku Primer
b. Dari larutan diambil 5,0ml encerkan dengan akuades dalam labu 50 ml dengan akuades sampai tanda batas. Larutan Baku Sekunder
3. Penetapan Panjang Gelombang Maksimum
a. Masukkan 1,5 ml larutan baku sekunder ke dalam labu takar 50 ml, Ditambah akuades sampai tanda batas.
b. Larutan diambil 25,0 ml ditambah 1,0 ml HCl Pekat dan 0,5ml Hidroksilamin HCl, kemudian dipanaskan selam 5 menit. Tambahkan 5,0 ml dapar ammonium asetat dan 1,0 ml pereaksi 1,10-fenantrolin hingga terjadi perubahan warna menjadi merah.
c. Dengan menggunakan blanko akuades, ukur absorban dengan panjang gelombang 400 nm sampai 600 nm.
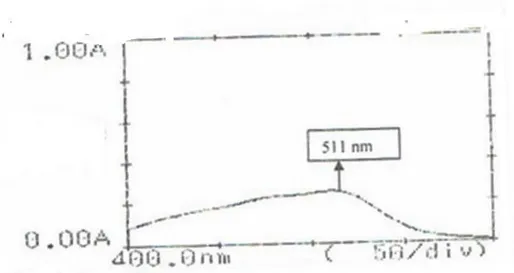
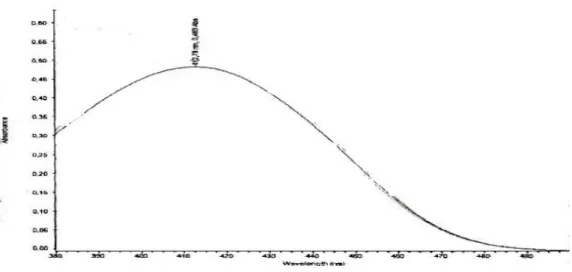
d. Hasil. Panjang gelombang 511 nm dengan Absorban 0,305
Gambar 1. Spektrum Fe (III)
4. Penentuan operating time
a. Masukkan 2,0 ml larutan baku sekunder ke dalam labu takar 50 ml, Ditambah akuades sampai tanda batas.
b. Larutan diambil 25,0 ml ditambah 1,0 ml HCl Pekat dan 0,5 ml Hidroksilamin HCl, kemudian dipanaskan selam 5 menit. Tambahkan 5,0 ml dapar ammonium asetat dan 1,0 ml pereaksi 1,10-fenantrolin hingga terjadi perubahan warna menjadi merah.
c. Diukur absorban pada Panjang gelombang 511,0 nm pada menit 1 sampai 20.
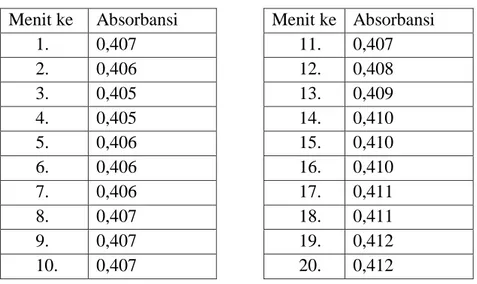
Tabel 1. Data Hasil Operating Time Fe (III)
Menit ke Absorbansi Menit ke Absorbansi
1. 0,407 11. 0,407
2. 0,406 12. 0,408
3. 0,405 13. 0,409
4. 0,405 14. 0,410
5. 0,406 15. 0,410
6. 0,406 16. 0,410
7. 0,406 17. 0,411
8. 0,407 18. 0,411
9. 0,407 19. 0,412
10. 0,407 20. 0,412
5. Pembuatan Kurva Kalibrasi Larutan Fe (III) a. Disiapkan 5 buah labu takar 50 ml.
b. Dipipet dari larutan baku sekunder Fe masing-masing 1,0 ml; 1,75 ml; 2,5 ml; 3.25 ml;
dan 4.0 ml ke dalam labu takar 50 ml. Ditambah akuades sampai tanda batas. Sehingga didapatkan larutan seri standar dengan konsentrasi 2 ppm, 3,5 ppm, 5 ppm, 6,5 ppm dan 8 ppm.
c. Masing-masing Larutan diambil 25,0 ml ditambah 1,0 ml HCl Pekat dan 0,5 ml Hidroksilamin HCl, kemudian dipanaskan selam 5 menit. Tambahkan 5,0 ml dapar ammonium asetat dan 1,0 ml pereaksi 1,10-fenantrolin hingga terjadi perubahan warna menjadi merah.
d. Diukur absorban pada panjang gelombang 511,0 nm.
Gambar 2. Grafik Kurva Kalibrasi Larutan Standar Fe
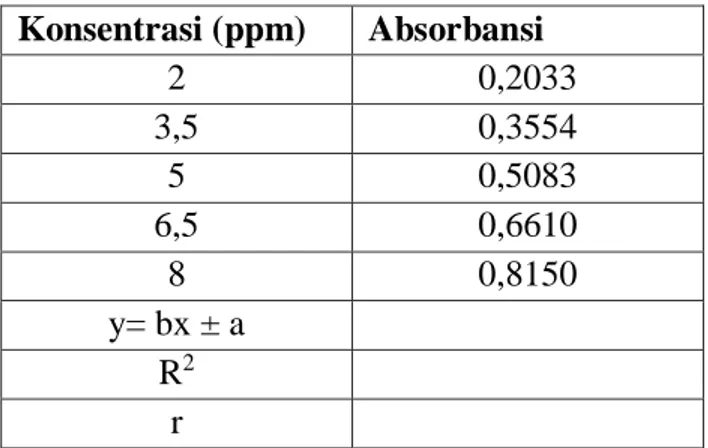
Tabel 2. Data Kurva Kalibrasi Larutan Standar Fe Konsentrasi (ppm) Absorbansi
2 0,2033
3,5 0,3554
5 0,5083
6,5 0,6610
8 0,8150
y= bx ± a R2
r 6. Penetapan Kadar Sampel tablet
Disiapkan sampel 20 tablet multivitamin yang mengandung zat besi merek X, Y, dan Z dan setiap sampel dilakukan 3 kali penetapan kadar dengan perlakuan sebagai berikut:
a. Persiapan sampel
1) Ditimbang 20 tablet (masing-masing merek), dihitung bobot tablet rata-rata dimasukkan ke dalam lumpang, gerus homogen.
2) Kemudian timbang serbuk tablet seksama 500,0mg. sebanyak 3 kali (triplo) 3) Masing-masing penimbangan dimasukkan dalam beaker gelas tambahkan asam
klorida sebanyak 25,0ml, kemudian panaskan Selama 15 menit, dinginkan selama 15 menit setelah itu disaring, masukkan dalam labu ukur 50 ml, cukupkan volume dengan akuades hingga tanda batas.
b. Pengukuran absorban sampel
1) masing-masing Larutan sampel diambil 25,0 ml ditambah 1,0 ml HCl Pekat dan 1 ml Hidroksilamin HCl, kemudian dipanaskan selam a 5 menit. Tambahkan 5,0 ml dapar ammonium asetat dan 1,0 ml pereaksi 1,10 fenantrolin hingga terjadi perubahan warna menjadi merah.
2) Larutan Diukur absorban sampel pada panjang gelombang 511,0 nm. Penetapan kadar dilakukan replikasi sebanyak 3 kali
Tabel 3. Data Hasil penetapan Fe Pada Sampel tablet multivitamin
Sampel Pengul angan
Abs Kadar (%) Rata- rata Kadar (%)
SD SDR Kesimpulan
X 1 0,374
2 0,373 3 0,375
Y 1 0,323
2 0,324 3 0,322
Z 1 0,273
2 0,274 3 0,275 Sumber:
Wiranti Sri Rahayu, dkk. Validasi Penetapan Kadar Besi dalam Sediaan Tablet Multivitamin dengan Metode Spektrofotometer. Fakultas Farmasi Universitas Muhammadiyah Purwokerto.
Pharmacy. Vol 05 No 01 April 2007. ISSN 1693-3591.
TUGAS KELOMPOK 4
PENETAPAN KADAR FORMALIN DENGAN SPEKTROFOTOMETRI VISIBLE
Penetapan Kadar Formalin dalam ikan secara Spektrofotometri Vis 1. Persiapan pembuatan pereaksi Nash
Sebanyak 2,0 mL asetil aseton, 3,0 mL asam asetat dan 150,0 g ammonium asetat dilarutkan dengan akuades dan dicukupkan volumenya hingga 1 L.
2. Persiapan pembuatan Larutan Stok formalin Standar 1000 mg/L
Larutan formalin 37% diambil 0,25 mL diencerkan dengan akuades dalam labu 100
mL, kemudian dilarutkan dengan pengenceran bertingkat untuk mendapatkan konsentrasi yang kita inginan.
3. Penetapan Panjang Gelombang Maksimum
a. Panjang gelombang maksimum pengukuran yang dilakukan pada larutan formalin pada kosentrasi 10 μg/mL yang dilarutkan dengan akuades dan reagen Nash yang memberikan hasil warna kuning menggunakan spektrofotometri UV-Vis pada rentang panjang gelombang 380 – 490 nm.
b. Menurut literatur, formalin memiliki serapan optimum pada panjang gelombang 412 nm.
Hasil panjang gelombang 412,78 nm nm dengan Absorban 0,501
Gambar 1. Kurva Panjang Gelombang Maksimum Formalin
4. Penentuan operating time
a. Salah satu konsentrasi standar formalin yaitu 10 μg/mL dipipet 5,0 mL dimasukkan ke dalam labu ukur 25 mL.
b. Ditambahkan 5 mL akuades dan 5 mL pereaksi Nash, dipanaskan dalam penangas air pada suhu 40 dan 60oC selama 30 menit sambil ditutup. Setelah dingin ditepatkan volumenya menggunakan akuades, dikocok hingga homogen.
c. Diamati serapannya 380 - 490 nm dengan alat spektrofotometer UV-Vis hingga didapat panjang gelombang maksimum untuk setiap suhu.
d. Diukur absorban pada pada panjang gelombang 412,78 nm di menit 1 sampai 20.
Tabel 1. Data Hasil Operating Time
Menit ke Absorbansi Menit ke Absorbansi
1. 0,690 11. 0,692
2. 0,690 12. 0,689
3. 0,690 13. 0,688
4. 0,691 14. 0,687
5. 0,691 15. 0,686
6. 0,691 16. 0,685
7. 0,690 17. 0,684
8. 0,690 18. 0,683
9. 0,692 19. 0,682
10. 0,692 20. 0,681
5. Pembuatan Kurva Kalibrasi Formalin
a. Dibuat Larutan formalin dengan konsentrasi 4, 7, 10, 13, 6μg/mL. Masing-masing larutan standar diambil 5,0 mL dimasukkan dalam labu ukur 25 mL kemudian ditambahkan 5,0 mL akuades dan 5,0 mL pereaksi Nash lalu dipanaskan dalam penangas air pada suhu optimum selama 30 menit sambil ditutup.
b. Setelah dingin tepatkan volumenya menggunakan akuades, dikocok hingga homogen.
Diamati serapannya pada panjang gelombang 412,78 nm dengan alat spektrofotometer UV- Vis.
c. Kemudian dibuat kurva kalibrasi hingga didapat persamaan liner y = a + bx. Lineritas dari kurva kalibrasi dilihat dengan menghitung koefisien korelasi (r) dari persamaan garis regresi linier.
Gambar 2. Grafik Kurva Kalibrasi Larutan Standar Formalin
Tabel 2. Data Kurva Kalibrasi Larutan Standar formalin Konsentrasi (ppm) Absorbansi
4 0,2015
7 0,3505
10 0,5009
13 0,6521
16 0,8101
y= bx ± a R2
r 5. Penetapan Kadar Sampel
a. Sampel ikan jenis K, L, dan M yang sudah dibeli kemudian dicuci dengan aquadest dan dikeringkan.
b. Masing-masing Sampel ikan diambil daging di bagian badan ikan dan ditimbang sebanyak 10,0 g dan ditambah akuades sebanyak 50 mL.
c. Dihaluskan dengan lumpang kemudian disaring dengan kertas saring. Diambil 5,0 mL filtrat dimasukkan ke dalam labu ukur 25 mL. Ditambahkan akuades sebanyak 5,0 mL dan 5,0 mL pereaksi Nash lalu dipanaskan ke dalam penangas air pada suhu optimum selama 30 menit sambil ditutup, setelah dingin dan ditepatkan volumenya menggunakan akuades.
Dikocok hingga homogen.
d. Diukur dengan spektrofotometer UV-Vis dengan panjang gelombang 412,78 nm.
Tabel 3. Data Hasil Konsentrasi Formalin Pada Sampel
Sampel Pengulan gan
Abs Kadar (%)
Rata- rata Kadar (%)
SD SDR Kesimpulan
A 1 0,446
2 0,444
3 0,443
B 1 0,469
2 0,471
3 0,477
C 1 0,35
2 0,348
3 0,346
Keterangan : MS = Memenuhi Syarat
Standar : Peraturan Kepala Badan Pengawas Obat dan Makanan RI tahun 2010 yaitu tidak lebih dari 2%.
Sumber:
Yulizar Yusuf, Zamzibar Zuki, MP dan Ruci Riski Amanda. Pengaruh beberapa perlakuan terhadap pengurangan kadar formalin pada ikan yang ditentukan secara spektrofotometri . Laboratorium Kimia Analitik Terapan Jurusan Kimia FMIPA Universitas Andalas. J. Ris. Kim. Vol. 8, No. 2, Maret 2015