LAPORAN TUGAS KHUSUS PRAKTEK KERJA
LAPORAN TUGAS KHUSUS PRAKTEK KERJA PROFESI
PROFESI
APOTEKER DI SUKU DINAS KESEHATAN KOTA
APOTEKER DI SUKU DINAS KESEHATAN KOTA
ADMINISTRASI JAKARTA UTARA
ADMINISTRASI JAKARTA UTARA
PERIODE 7 JANUARI - 18 JANUARI 2013
PERIODE 7 JANUARI - 18 JANUARI 2013
PERIZINAN USAHA MIKRO OBAT TRADISIONAL (UMOT)
PERIZINAN USAHA MIKRO OBAT TRADISIONAL (UMOT)
FURQON DWI CAHYO, S. Farm.
FURQON DWI CAHYO, S. Farm.
1206313135
1206313135
ANGKATAN LXXVI ANGKATAN LXXVI FAKULTAS FARMASI FAKULTAS FARMASIPROGRAM PROFESI APOTEKER DEPOK PROGRAM PROFESI APOTEKER DEPOK
JUNI 2013 JUNI 2013
HALAMAN
HALAMAN JUDUL JUDUL ... ... ii DAFTAR
DAFTAR ISI ISI ... ... iiii DAFTAR
DAFTAR LAMPIRAN LAMPIRAN ... ... iiiiii BAB 1
BAB 1 PENDAHULUPENDAHULUAN AN ... ... 11 1.1
1.1 Latar Latar Belakang Belakang ... ... 11 1.2
1.2 Tujuan Tujuan ... ... 22 BAB 2
BAB 2 TINJAUAN TINJAUAN KHUSUS KHUSUS ... ... 33 2.1
2.1 Usaha Usaha Mikro Mikro Obat Obat Tradisional Tradisional ... . 33 2.2
2.2 Perizinan Perizinan Usaha Usaha Mikro Mikro Obat Obat Tradisional Tradisional (UMOT) (UMOT) ... ... 33 2.3
2.3 Registrasi Registrasi Produk Produk Obat Obat Tradisional Tradisional ... ... 55 2.4
2.4 Cara Cara Pembuatan Pembuatan Obat Obat Tradisional Tradisional Yang Yang Baik Baik (CPOTB) (CPOTB) ... ... 77 BAB 3
BAB 3 METODOLOGI METODOLOGI ... ... 1313 3.1 Waktu D
3.1 Waktu Dan Tempat an Tempat ... ... 1313 3.2 Cara
3.2 Cara Kerja Kerja ... ... 1313 BAB 4
BAB 4 PEMBAHASANPEMBAHASAN ... 14... 14 4.1
4.1 Pembahasan Pembahasan Umum Umum Umot Umot Dan Dan Perbedaanya Perbedaanya Terhadap Terhadap Usaha ObatUsaha Obat Tradisional Lainnya
Tradisional Lainnya ... ... 1414 4.2
4.2 Penerapan Penerapan Perizinan Perizinan Umot Umot Di Di Suku Suku Dinas Dinas Kesehatan Kesehatan Kota Kota AdministrasiAdministrasi Jakarta
Jakarta Utara Utara ... ... 1616 BAB 5 KESIM
BAB 5 KESIMPULAN DAN SAPULAN DAN SARAN RAN ... . 1919 5.1
5.1 Kesimpulan Kesimpulan ... ... 1919 5.2
5.2 Saran Saran ... ... 1919 DATAR AC
HALAMAN
HALAMAN JUDUL JUDUL ... ... ii DAFTAR
DAFTAR ISI ISI ... ... iiii DAFTAR
DAFTAR LAMPIRAN LAMPIRAN ... ... iiiiii BAB 1
BAB 1 PENDAHULUPENDAHULUAN AN ... ... 11 1.1
1.1 Latar Latar Belakang Belakang ... ... 11 1.2
1.2 Tujuan Tujuan ... ... 22 BAB 2
BAB 2 TINJAUAN TINJAUAN KHUSUS KHUSUS ... ... 33 2.1
2.1 Usaha Usaha Mikro Mikro Obat Obat Tradisional Tradisional ... . 33 2.2
2.2 Perizinan Perizinan Usaha Usaha Mikro Mikro Obat Obat Tradisional Tradisional (UMOT) (UMOT) ... ... 33 2.3
2.3 Registrasi Registrasi Produk Produk Obat Obat Tradisional Tradisional ... ... 55 2.4
2.4 Cara Cara Pembuatan Pembuatan Obat Obat Tradisional Tradisional Yang Yang Baik Baik (CPOTB) (CPOTB) ... ... 77 BAB 3
BAB 3 METODOLOGI METODOLOGI ... ... 1313 3.1 Waktu D
3.1 Waktu Dan Tempat an Tempat ... ... 1313 3.2 Cara
3.2 Cara Kerja Kerja ... ... 1313 BAB 4
BAB 4 PEMBAHASANPEMBAHASAN ... 14... 14 4.1
4.1 Pembahasan Pembahasan Umum Umum Umot Umot Dan Dan Perbedaanya Perbedaanya Terhadap Terhadap Usaha ObatUsaha Obat Tradisional Lainnya
Tradisional Lainnya ... ... 1414 4.2
4.2 Penerapan Penerapan Perizinan Perizinan Umot Umot Di Di Suku Suku Dinas Dinas Kesehatan Kesehatan Kota Kota AdministrasiAdministrasi Jakarta
Jakarta Utara Utara ... ... 1616 BAB 5 KESIM
BAB 5 KESIMPULAN DAN SAPULAN DAN SARAN RAN ... . 1919 5.1
5.1 Kesimpulan Kesimpulan ... ... 1919 5.2
5.2 Saran Saran ... ... 1919 DATAR AC
Halaman Halaman Lampiran
Lampiran 1. 1. Formulir Formulir 18 ...18 ... ... 2222 Lampiran 2. Formulir 19
Lampiran 2. Formulir 19 ... ... 2424 Lampiran
Lampiran 3. 3. Formulir Formulir 20a 20a ... ... 2525 Lampiran
Lampiran 4. 4. Formulir Formulir 20b ...20b ... ... 2727 Lampiran
Lampiran 5. 5. Formulir Formulir 20c 20c ... ... 2828 Lampiran
BAB 1
PENDAHULUAN
1.1 Latar Belakang
Masyarakat Indonesia merupakan masyarakat yang mengonsumsi obat tradisional cukup tinggi, berdasarkan riset kementrian kesehatan, 59,12% dari masyarakat Indonesia dilaporkan mengkonsumsi obat-obatan tradisional (Kementerian Kesehatan RI, 2010). Obat tradisional adalah bahan atau ramuan bahan yang berupa bahan tumbuhan, bahan hewan, bahan mineral, sediaan sarian (galenik), atau campuran
dari bahan tersebut yang secara turun temurun telah digunakan untuk pengobatan, dan
dapat diterapkan sesuai dengan norma yang berlaku di masyarakat
(Kementrian Kesehatan Republik Indonesia, 2012a). Hal tersebut didukung dengan sejarah masyarakat Indonesia yang secara turun temurun menggunakan obat tradisional asli Indonesia yang dikenal dengan nama Jamu.
Tingginya angka konsumsi obat tradisional membuat usaha di bidang ini menjadi potensial untuk berkembang, terutama untuk jumlah produsennya. Oleh karena itu perlu dilakukan pembinaan, pengawasan serta pengendalian terhadap produsen obat tradisional agar melindungi masyarakat dari obat tradisional yang tidak memenuhi syarat mutu, khasiat, dan keamanan. Sebelumnya telah dibuat Peraturan Menteri Kesehatan Nomor 246/Menkes/Per/V/1990 tentang izin usaha industri obat tradisional dan pendaftaran obat tradisional dalam upaya pemerintah untuk pembinaan, pengawasan serta pengendalian terhadap produsen obat tradisional. Seiring berjalannya waktu kini peraturan menteri tersebut sudah tidak sesuai dengan perkembangan ilmu pengetahuan dan teknologi serta kebutuhan hukum, sehingga diterbitkanlah Peraturan Menteri Kesehatan Republik Indonesia Nomor 006 Tahun 2012 tentang industri dan usaha obat tradisional. Peraturan baru tersebut berbeda dengan peraturan sebelumnya sehingga perlu dipelajari lagi secara lebih mendalam.
Terkait dengan Praktek Kerja Profesi Apoteker yang dilakukan di Suku Dinas Kesehatan Kota Administrasi Jakarta Utara maka dilakukan pembuatan tugas khusus yang mengulas lebih jauh mengenai perizinan Usaha Mikro Obat Tradisional (UMOT). Usaha Mikro Obat Tradisional (UMOT) adalah usaha yang hanya membuat sediaan obat tradisional dalam bentuk param, tapel, pilis, cairan obat luar dan rajangan. Usaha tersebut diawasi, dibina dan dikendalikan kegiatannya oleh Dinas Kesehatan Kota/
Kabupaten setempat, sebagai bagian pelaksanaan dari Peraturan Menteri Kesehatan Republik Indonesia Nomor 006 Tahun 2012. Peraturan tersebut merupakan regulasi terbaru mengenai Industri dan Usaha Obat Tradisional, sehingga perlu diketahui lebih mendalam, mengenai tata cara dan persyaratan perizinan UMOT di Suku Dinas Kesehatan Kota khususnya di tempat PKPA dilaksanakan, yaitu Suku Dinas Kesehatan Kota Jakarta Utara.
1.2 Tujuan
Mengetahui dan memahami tata cara dan persyaratan perizinan Industri Obat tradisional berdasarkan PERMENKES No. 006 Tahun 2012 di Suku Dinas Kesehatan Kota, dalam bentuknya yaitu Usaha Mikro Obat Tradisional (UMOT).
BAB 2
TINJAUAN KHUSUS
2.1 Usaha Mikro Obat Tradisional
Usaha Mikro Obat Tradisional (UMOT). UMOT merupakan salah satu usaha obat tradisional yang hanya membuat sediaan obat tradisional dalam bentuk param (obat tradisional dalam bentuk padat, pasta, atau seperti bubur yang
digunakan dengan cara melumurkan di kaki dan tangan atau di bagian tubuh lain), tapel (obat tradisional dalam bentuk padat, pasta, atau seperti bubur yang digunakan dengan cara melumurkannya di seluruh bagian perut), pilis (obat tradisional dalam bentuk padat, pasta, yang digunakan dengan cara mengoleskannya di dahi), cairan obat luar dan rajangan. (Kementerian Kesehatan RI, 2012a dan Firmansyah, 2009). Obat tradisional sendiri didefinisikan sebagai bahan atau ramuan bahan yang berupa bahan tumbuhan, bahan hewan, bahan mineral, sediaan sarian (galenik), atau campuran dari bahan tersebut yang secara turun temurun telah digunakan untuk pengobatan, dan dapat diterapkan sesuai dengan norma yang berlaku di masyarakat (Kementrian Kesehatan Republik Indonesia, 2012a)..
2.2 Perizinan Usaha Mikro Obat Tradisional (UMOT) (Kementerian
Kesehatan RI, 2012a dan Firmansyah, 2009)
Setiap industri dan usaha di bidang obat tradisional wajib memiliki izin dari menteri. Dikecualikan dari ketentuan sebagaimana dimaksud usaha jamu gendong dan usaha jamu racikan. Selain usaha jamu gendong dan racikan wajib memiliki izin. Izin industri dan usaha obat tradisional berlaku seterusnya selama industri dan usaha obat tradisional yang bersangkutan masih berproduksi dan memenuhi ketentuan peraturan perundang-undangan. Menteri kesehatan dalam pemberian izin mendelegasikan kewenangan pemberian izin untuk UMOT kepada
kepala dinas kesehatan kabupaten/Kota. (Kementerian Kesehatan RI, 2012a)
Untuk dapat menyelenggarakan usahanya, adapun persyaratan yang harus dilengkapi oleh UMOT adalah sebagai berikut:
b. Fotokopi akta pendirian badan usaha perorangan yang sah sesuai ketentuan peraturan perundang-undangan;
c. Susunan direksi/dan komisaris/badan pengawas dalam hal permohonan bukan perseorangan;
d. Fotokopi KTP/identitas pemohon dan/atau direksi/pengurus dan
Komisaris/Badan Pengawas;
e. Pernyataan pemohon dan/atau direksi/pengurus dan komisaris/badan pengawas tidak pernah terlibat pelanggaran peraturan perundang-undangan
di bidang farmasi;
f. Fotokopi bukti penguasaan tanah dan bangunan;
g. Surat tanda daftar perusahaan dalam hal permohonan bukan perseorangan; h. Fotokopi surat izin usaha perdagangan dalam hal permohonan bukan
perseorangan;
i. Fotokopi Nomor Pokok Wajib Pajak (NPWP); dan
j. Fotokopi surat keterangan domisili.
Permohonan izin UMOT diajukan oleh pemohon kepada kepala dinas kesehatan kabupaten/kota dengan menggunakan contoh sebagaimana tercantum dalam formulir 18 (Lampiran. 1). Paling lama 7 (tujuh) hari kerja sejak menerima permohonan untuk izin UMOT. Selanjutnya kepala dinas kesehatan kabupaten atau kota setempat menunjuk tim untuk melakukan pemeriksaan kelokasi sesuain dengan permohonan. Paling lama 7 (tujuh) hari kerja setelah menerima penugasan, tim melakukan pemeriksaan terhadap kesiapan administrasi dan teknis, dan menyampaikan hasil pemeriksaan kepada kepala dinas kesehatan kabupaten/kota dengan menggunakan contoh sebagaimana tercantum dalam formulir 19 (Lampiran. 2).
Paling lama 7 (tujuh) hari kerja setelah menerima hasil pemeriksaan, kepala dinas kesehatan kabupaten/kota menyetujui, menunda, atau menolak permohonan izin UMOT dengan tembusan kepada kepala dinas kesehatan provinsi dan kepala balai pengawas obat dan makanan setempat, dengan menggunakan contoh sebagaimana tercantum dalam formulir 20a (Lampiran. 3), formulir 20b (Lampiran. 4) atau formulir 20c (Lampiran. 5). Apabila dalam 30 (tiga puluh) hari kerja setelah surat permohonan diterima oleh Kepala dinas kesehatan kabupaten/kota tidak dilakukan pemeriksaan ataupun verifikasi
sebagaimana yang dimaksud perturam sebelumnya, pemohon dapat membuat surat pernyataan siap berproduksi kepada kepala dinas kesehatan kabupaten/kota dengan menggunakan contoh sebagaimana tercantum dalam formulir 21 (Lampiran 6).
Izin UMOT diberikan kepada pemohon yang telah memenuhi persyaratan. Permohonan izin UMOT dapat ditunda atau ditolak apabila ternyata belum memenuhi persyaratan. Dalam hal penundaan pemberian izin UMOT, maka kepada pemohon diberi kesempatan untuk melengkapi persyaratan yang belum dipenuhi paling lama 6 (enam) bulan sejak diterimanya surat penundaan.
Dalam penyelenggaraan UMOT berkewajiban:
a. Menjamin keamanan, khasiat/manfaat dan mutu produk obat tradisional yang dihasilkan;
b. Melakukan penarikan produk obat tradisional yang tidak memenuhi ketentuan keamanan, khasiat/manfaat dan mutu dari peredaran; dan
c. Memenuhi ketentuan peraturan perundang-undangan lain yang berlaku. Selain itu untuk usaha dan industri obat tradisional dilarang membuat:
a. Segala jenis obat tradisional yang mengandung bahan kimia atau hasil
sintetik yang berkhasiat obat;
b. Obat tradisional dalam bentuk intravaginal, tetes mata, sediaan parenteral, supositoria kecuali untuk wasir; dan/atau
c. Obat tradisional dalam bentuk cairan obat dalam yang mengandung etanol dengan kadar lebih dari 1% (satu persen).
UMOT yang telah mendapat izin, yang melakukan perubahan nama, alamat, atau tenaga teknis kefarmasian penanggung jawab wajib melaporkan secara tertulis kepada kepala dinas kesehatan kabupaten/kota dengan tembusan kepada kepala balai POM setempat. UMOT wajib menyampaikan laporan secara berkala setiap 6 (enam) bulan meliputi jenis dan jumlah bahan baku yang digunakan serta jenis, jumlah, dan nilai hasil produksi. Laporan UMOT disampaikan kepada kepala dinas kesehatan kabupaten/kota dengan tembusan kepada kepala balai POM setempat.
2.3 Registrasi produk obat tradisional (Kementrian Kesehatan
Republik
Obat tradisional yang diedarkan di wilayah Indonesia wajib memiliki izin edar. Izin edar untuk produk obat tradisional diberikan oleh kepala badan pengawas obat dan makanan. Pemberian izin edar dilaksanakan melalui
mekanisme registrasi sesuai dengan tatalaksana yang ditetapkan. Izin edar berlaku 5 (lima) tahun dan dapat diperpanjang selama memenuhi persyaratan. Adapun pengecualian terhadap obat tradisional yang dibuat oleh usaha jamu racikan dan usaha jamu gendong, simplisia dan sediaan galenik untuk keperluan industri dan keperluan layanan pengobatan tradisional, serta obat tradisional yang digunakan untuk penelitian dan sampel untuk registrasi dan pameran dalam jumlah terbatas dan tidak diperjualbelikan, tidak wajib memiliki izin edar.
Adapun kriteria yang harus dipenuhi oleh produk obat tradisional yang dapat memperoleh izin edar, adalah:
a. Menggunakan bahan yang memenuhi persyaratan keamanan dan mutu;
b. Dibuat dengan menerapkan CPOTB;
c. Memenuhi persyaratan Farmakope Herbal Indonesia atau persyaratan lain yang diakui;
d. Berkhasiat yang dibuktikan secara empiris, turun temurun, dan/atau secara ilmiah; dan
e. Penandaan berisi informasi yang objektif, lengkap, dan tidak menyesatkan. Selain persyaratan tersebut di atas, terdapat ketentuan lain mengenai produk obat tradisional, yaitu adanya larangan untuk obat tradisional mengandung: a. Etil alkohol lebih dari 1%, kecuali dalam bentuk sediaan tingtur yang pemakaiannya dengan pengenceran;
b. Bahan kimia obat yang merupakan hasil isolasi atau sintetik berkhasiat obat;
c. Narkotika atau psikotropika; dan/atau
d. Bahan lain yang berdasarkan pertimbangan kesehatan dan/atau
berdasarkan penelitian membahayakan kesehatan.
Obat tradisional juga dilarang dibuat dan/atau diedarkan dalam bentuk sediaan intravaginal, tetes mata, sediaan parenteral dan supositoria, kecuali
digunakan untuk wasir. Registrasi obat tradisional produksi dalam negeri hanya dapat dilakukan oleh IOT, UKOT, atau UMOT yang memiliki izin sesuai ketentuan peraturan perundang-undangan.
2.4 Cara Pembuatan Obat Tradisional yang Baik (CPOTB) (Badan
Pengawas Obat dan Makanan, 2011)
Cara Pembuatan Obat Tradisional yang Baik (CPOTB) meliputi seluruh aspek yang menyangkut pembuatan obat tradisional, yang bertujuan untuk menjamin agar produk yang dihasilkan senantiasa memenuhi persyaratan mutu yang telah ditentukan sesuai dengan tujuan penggunaannya. Mutu produk tergantung dari bahan awal, proses produksi dan pengawasan mutu, bangunan, peralatan dan personalia yang menangani.
Penerapan CPOTB merupakan persyaratan kelayakan dasar untuk menerapkan sistem jaminan mutu yang diakui dunia internasional. Untuk itu sistem mutu hendaklah dibangun, dimantapkan dan diter apkan sehingga kebijakan yang ditetapkan dan tujuan yang diinginkan dapat dicapai. Dengan demikian penerapan CPOTB merupakan nilai tambah bagi produk obat tradisional Indonesia agar dapat bersaing dengan produk sejenis dari negara lain baik di pasar dalam negeri maupun internasional. Mengingat pentingnya penerapan CPOTB maka pemerintah secara terus menerus memfasilitasi industri obat tradisional baik skala besar maupun kecil untuk dapat menerapkan CPOTB melalui
langkah-langkah dan pentahapan yang terprogram.
Dengan adanya perkembangan jenis produk obat bahan alam tidak hanya dalam bentuk obat tradisional (jamu), tetapi juga dalam bentuk obat herbal terstandar dan fitofarmaka, maka pedoman cara pembuatan obat tradisional yang baik ini dapat pula diberlakukan bagi industri yang memproduksi obat herbal terstandar dan fitofarmaka. Berikut merupakan aspek penting yang terdapat dalam CPOTB, antara lain:
a. Manajemen Mutu
Suatu infrastruktur atau sistem mutu yang tepat mencakup struktur organisasi, prosedur, proses dan sumber daya, serta tindakan sistematis yang diperlukan untuk mendapatkan kepastian dengan tingkat kepercayaan yang tinggi, sehingga produk (atau jasa pelayanan) yang dihasilkan akan selalu memenuhi
persyaratan yang telah ditetapkan. Keseluruhan tindakan tersebut disebut pemastian mutu. Semua bagian sistem pemastian mutu hendaklah didukung dengan ketersediaan personil yang kompeten, bangunan dan sarana serta peralatan yang cukup dan memadai. Tambahan tanggung jawab legal hendaklah diberikan kepada kepala manajemen mutu (pemastian mutu).
b. Personalia
Sumber daya manusia sangat penting dalam pembentukan dan penerapan sistem pemastian mutu yang memuaskan dan pembuatan obat tradisional yang benar. Oleh sebab itu industri obat tradisional bertanggung jawab untuk
menyediakan personil yang terkualifikasi dalam jumlah yang memadai untuk melaksanakan semua tugas. Tanggung jawab tiap personil hendaklah dipahami masing-masing dan dicatat. Seluruh personil hendaklah memahami prinsip CPOTB dan memperoleh pelatihan awal dan berkesinambungan, termasuk instruksi mengenai higiene yang berkaitan dengan pekerjaannya.
c. Bangunan, fasilitas, dan peralatan
Bangunan, fasilitas dan peralatan untuk pembuatan obat tradisional hendaklah memiliki desain, konstruksi dan letak yang memadai, serta disesuaikan kondisinya dan dirawat dengan baik untuk memudahkan pelaksanaan operasi yang benar. Tata letak dan desain ruangan harus dibuat sedemikian rupa untuk memperkecil risiko terjadi kekeliruan, pencemaran silang dan kesalahan lain, dan
memudahkan pembersihan, sanitasi dan perawatan yang efektif untuk
menghindarkan pencemaran silang, penumpukan debu atau kotoran, dan dampak lain yang dapat menurunkan mutu obat tradisional tradisional. Karena berpotensi untuk terdegradasi dan terserang hama serta sensitivitasnya terhadap kontaminasi mikroba maka produksi dan terutama penyimpanan bahan yang berasal dari tanaman dan binatang memerlukan perhatian khusus. Bangunan dan fasilitas serta semua peralatan kritis hendaklah dikualifikasi untuk menjamin reprodusibiltas dari bets-ke-bets.
d. Sanitasi dan higiene
Tingkat sanitasi dan higiene yang tinggi hendaklah diterapkan pada setiap aspek pembuatan obat tradisional. Ruang lingkup sanitasi dan higiene meliputi personil, bangunan, peralatan dan perlengkapan, bahan produksi serta wadahnya, dan segala sesuatu yang dapat merupakan sumber pencemaran produk. Sumber
pencemaran potensial hendaklah dihilangkan melalui suatu program sanitasi dan higiene yang menyeluruh dan terpadu. Karena sumbernya, bahan obat tradisional dapat mengandung cemaran mikrobiologis, di samping itu, proses pemanenan atau pengumpulan dan proses produksi obat tradisional sangat mudah tercemar oleh mikroba. Untuk menghindarkan perubahan mutu dan mengurangi kontaminasi, diperlukan penerapan sanitasi dan higiene berstandar tinggi. Bangunan dan fasilitas serta peralatan hendaklah dibersihkan dan, di mana perlu, didisinfeksi menurut prosedur tertulis yang rinci dan tervalidasi.
e. Dokumentasi
Dokumentasi adalah bagian dari sistem informasi manajemen dan dokumentasi yang baik merupakan bagian yang esensial dari pemastian mutu. Dokumentasi yang jelas adalah fundamental untuk memastikan bahwa tiap personil menerima uraian tugas yang relevan secara jelas dan rinci sehingga
memperkecil risiko terjadi salah tafsir dan kekeliruan yang biasanya timbul karena hanya mengandalkan komunikasi lisan. Spesifikasi, dokumen produksi induk/formula pembuatan, prosedur, metode dan instruksi, laporan dan catatan harus bebas dari kekeliruan dan tersedia secara tertulis. Keterbacaan dokumen adalah sangat penting.
f. Produksi
Produksi hendaklah dilaksanakan dengan mengikuti prosedur tervalidasi yang telah ditetapkan; dan memenuhi ketentuan CPOTB yang menjamin senantiasa menghasilkan produk yang memenuhi persyaratan mutu serta memenuhi ketentuan izin pembuatan dan izin edar (registrasi). Untuk bahan mentah baik yang dibudidayakan maupun yang hidup secara liar, dan yang digunakan baik dalam bentuk bahan mentah maupun sudah melalui tehnik pengolahan sederhana (misal perajangan atau penghalusan) tahap kritis pertama dalam proses produksi, dalam hal ini di mana persyaratan teknis ini mulai diterapkan, hendaklah ditentukan dengan jelas. Penjelasan tentang hal tersebut hendaklah dinyatakan dan didokumentasikan.
g. Pengawasan mutu
Pengawasan mutu merupakan bagian yang esensial dari Cara Pembuatan Obat Tadisional yang Baik untuk memberikan kepastian bahwa produk secara konsisten mempunyai mutu yang sesuai dengan tujuan pemakaiannya.
Keterlibatan dan komitmen semua pihak yang berkepentingan pada semua tahap merupakan keharusan untuk mencapai sasaran mutu mulai dari awal pembuatan sampai kepada distribusi produk jadi. Ruang lingkup Pengawasan Mutu mencakup pengambilan sampel, spesifikasi dan pengujian serta organisasi, dokumentasi dan prosedur pelulusan yang memastikan bahwa pengujian yang diperlukan dan relevan dilakukan, dan bahwa bahan-bahan yang tidak diluluskan untuk digunakan, atau produk jadi diluluskan untuk dijual atau didistribusikan, sampai kualitasnya dinilai memenuhi syarat. Pengawasan Mutu tidak terbatas pada kegiatan laboratorium, tapi juga harus terlibat dalam semua keputusan yang terkait dengan mutu produk. Independensi pengawasan mutu dari produksi adalah fundamental sehingga pengawasan mutu dapat melakukan kegiatan dengan benar. h. Pembuatan dan analisis berdasarkan kontrak
Pembuatan dan analisis berdasarkan kontrak harus dibuat secara benar, disetujui dan dikendalikan untuk menghindarkan kesalahpahaman yang dapat menyebabkan produk atau pekerjaan dengan mutu yang tidak memuaskan. Kontrak tertulis antara pemberi kontrak dan penerima kontrak harus dibuat secara jelas menentukan tanggung jawab dan kewajiban masing-masing pihak. Kontrak
harus menyatakan secara jelas prosedur pelulusan tiap bets produk untuk diedarkan yang menjadi tanggung jawab penuh kepala bagian manajemen mutu (pemastian mutu).
i. Cara penyimpanan dan pengiriman obat tradisional yang baik
Penyimpanan dan pengiriman adalah bagian yang penting dalam kegiatan dan manajemen rantai pemasokan produk yang terintegrasi. Dokumen ini menetapkan langkah yang tepat untuk membantu pemenuhan tanggung jawab bagi semua yang terlibat dalam kegiatan pengiriman dan penyimpanan produk. Dokumen ini memberikan pedoman bagi penyimpanan dan pengiriman produk jadi dari pabrik ke distributor. Mutu produk dapat dipengaruhi oleh kekurangan pengendalian yang diperlukan terhadap kegiatan selama proses penyimpanan dan pengiriman.Tujuan persyaratan teknis ini adalah untuk membantu dalam menjamin mutu dan integritas produk selama proses penyimpanan dan pengiriman produk.
j. Penanganan keluhan terhadap produk, penarikan kembali produk dan produk kembalian
Semua keluhan dan informasi lain yang berkaitan dengan kemungkinan terjadi kerusakan obat hendaklah dikaji dengan teliti sesuai dengan prosedur tertulis. Untuk menangani semua kasus yang mendesak, hendaklah disusun suatu sistem, bila perlu mencakup penarikan kembali produk yang diketahui atau diduga cacat dari peredaran secara cepat dan efektif.
k. Inspeksi diri
Tujuan inspeksi diri adalah untuk mengevaluasi apakah semua aspek produksi dan pengawasan mutu industri obat tradisional memenuhi ketentuan
Cara Pembuatan Obat Tradisional yang Baik (CPOTB). Program inspeksi diri hendaklah dirancang untuk mendeteksi kelemahan dalam pelaksanaan CPOTB dan untuk menetapkan tindakan perbaikan yang diperlukan. Inspeksi diri hendaklah dilakukan secara independen dan rinci oleh petugas yang kompeten dari perusahaan. Ada manfaatnya bila juga menggunakan auditor luar yang independen. Inspeksi diri hendaklah dilakukan secara rutin dan, di samping itu, pada situasi khusus, misalnya dalam hal terjadi penarikan kembali produk jadi
atau terjadi penolakan yang berulang. Semua saran untuk tindakan perbaikan supaya dilaksanakan.
Prosedur dan catatan inspeksi diri hendaklah didokumentasikan dan dibuat program tindak lanjut yang efektif. Hal-hal mengenai personalia, bangunan dan fasilitas, peralatan, dokumentasi, produksi, pengawasan mutu, distribusi produk jadi, penanganan keluhan dan penarikan produk jadi serta inspeksi diri hendaklah
diinspeksi secara berkala mengikuti program yang telah disusun sebelumnya untuk memverifikasi pemenuhan terhadap prinsip pemastian mutu. Semua inspeksi diri hendaklah dicatat. Laporan hendaklah mencantumkan semua observasi selama inspeksi dan usul untuk tindakan korektif yang diperlukan. Laporan tindak lanjut hendaklah dicatat juga.
Berdasarkan poin dalam CPOTB, dapat disimpulkan bahwa CPOTB adalah bagian dari pemastian mutu yang memastikan bahwa obat tradisional dibuat dan dikendalikan secara konsisten untuk mencapai standar mutu yang sesuai dengan tujuan penggunaan dan dipersyaratkan dalam izin edar dan
spesifikasi produk. CPOTB mencakup produksi dan pengawasan
a. Semua proses pembuatan obat tradisional dijabarkan dengan jelas, dikaji secara sistematis berdasarkan pengalaman dan terbukti mampu secara konsisten menghasilkan obat tradisional yang memenuhi persyaratan mutu dan spesifikasi yang telah ditetapkan;
b. Tahap proses yang kritis dalam proses pembuatan, pengawasan dan sarana penunjang serta perubahannya yang signifikan divalidasi;
c. Tersedia semua sarana yang diperlukan untuk CPOTB termasuk: 1. Personil yang terkualifikasi dan terlatih;
2. Bangunan dan sarana dengan luas yang memadai; 3. Peralatan dan sarana penunjang yang sesuai; 4. Bahan, wadah dan label yang benar;
5. Prosedur dan instruksi yang disetujui; dan
6. Tempat penyimpanan dan transportasi yang memadai.
d. Prosedur dan instruksi ditulis dalam bentuk instruksi dengan bahasa yang jelas, tidak bermakna ganda, dapat diterapkan secara spesifik pada sarana yang tersedia;
e. Operator memperoleh pelatihan untuk menjalankan prosedur secara benar; f. Pencatatan dilakukan secara manual atau dengan alat pencatat selama
pembuatan yang menunjukkan bahwa semua langkah yang dipersyaratkan dalam prosedur dan instruksi yang ditetapkan benar-benar dilaksanakan dan jumlah serta mutu produk yang dihasilkan sesuai dengan yang diharapkan. Tiap penyimpangan dicatat secara lengkap dan diinvestigasi; g. Catatan pembuatan termasuk distribusi yang memungkinkan penelusuran
riwayat bets secara lengkap, disimpan secara komprehensif dan dalam bentuk yang mudah diakses;
h. Penyimpanan dan distribusi obat tradisional yang dapat memperkecil risiko terhadap mutu obat tradisional;
i. Tersedia sistem penarikan kembali bets obat tradisional mana pun dari peredaran; dan
j. Keluhan terhadap produk yang beredar dikaji, penyebab cacat
mutu diinvestigasi serta dilakukan tindakan perbaikan yang tepat dan pencegahan pengulangan kembali keluhan.
BAB 3 METODOLOGI
3.1 Waktu dan Tempat
Penelusuran literatur dilakukan di Suku Dinas Kesehatan Kota Administrasi Jakarta Utara Seksi Sumber Daya Kesehatan bagian Koordinator Farmasi Makanan dan Minuman dan Seksi Kesehatan Masyarakat pada minggu kedua dan ketiga selama masa PKPA.
3.2 Cara Kerja
Literatur dan data yang didapat baik dari keterangan pihak Suku Dinas Kesehatan maupun melalui penelusuran regulasi terkait UMOT melaui internet, kemudian dikaji dan dipahami mengenai aspek-aspek terkait perizinan, maupun dan penerapannya pada Suku Dinas Kesehatan Kota Administrasi Jakarta Utara dengan tata cara perizinan Usaha Mikro Obat Tradisional (UMOT).
14 Universitas Indonesia BAB 4
PEMBAHASAN
4.1 Pembahasan Umum UMOT dan Perbedaanya terhadap Usaha obat
Tradisional Lainnya
UMOT (Usaha Mikro Obat Tradisional) merupakakan salah satu jenis usaha obat tradisional yang diklasifikasikan berdasarkan PERMENKES RI No. 006 tahun 2012 tentang industri dan usaha obat tradisional. Peraturan tersebut merupakan amandemen dari bentuk usaha jamu racikan yang terdapat pada peraturan sebelumnya, yaitu PERMENKES 246/MenKes/Per/1990 tentang izin usaha industri obat tradisional dan pendaftaran obat tradisional, yang dapat membuat bentuk sediaan param, tapel, pilis, cairan obat luar dan rajangan. Perbedaannya pada peraturan terbaru dinyatakan bahwa UMOT dapat diproduksi secara masal dengan merek dan penandaan, karena untuk sediaan yang diproduksi UMOT harus melalui tahapan registrasi produk.
Pada awalnya klasifikasi industri obat tradisional di Indonesia mengikuti peraturan PERMENKES 246/MenKes/Per/1990 tentang izin usaha industri obat tradisional dan pendaftaran obat tradisional, yang menggolongkan produsen obat tradisional berdasarkan jumlah pemilikan modal dan bentuk sediaan, Industri Kecil Obat Tradisional (IKOT), adalah industri obat tradisional dengan total aset tidak lebih dari Rp. 600.000.000,- (enam ratus juta rupiah), tidak termasuk harga tanah dan bangunan, berbeda dengan Industri Obat Tradisional (IOT), yang merupakan industri yang memproduksi obat tradisional dengan aset di atas Rp. 600.000.000,- (enam ratus juta rupiah), tidak termasuk harga tanah dan bangunan, sedangkan usaha lainnya terdapat antara lain adlah Usaha jamu racikan, yaitu usaha peracikan, pencampuran, dan atau pengelolaan obat tradisional dalam bentuk rajangan, serbuk, cairan, pilis, tapel atau parem dengan skala kecil, dijual di satu tempat tanpa penandaan atau merek dagang. Usaha jamu gendong, adalah usaha peracikan, pencampuran, dan pengedaran obat tradisional dalam bentuk cairan, pilis, tapel, atau parem, tanpa penandaan dan atau merek dagang serta dijajakan untuk langsung digunakan
Klasifikasi industri dan usaha obat tradisional berdasarkan PERMENKES 246/MenKes/Per/1990 secara garis besar dilakukan berdasarkan jumlah kepemilikan modal. Hal tersebut dirasa sudah tidak sesuai dengan perkembangan ilmu pengetahuan dan teknologi serta kebutuhan hukum. Oleh karena itu dikeluarkanlah PERMENKES RI No. 006 tahun 2012 tentang industri dan usaha obat tradisional yang mengklasifikasikan bentuk industri dan usaha obat tradisional berdasarkan bentuk sediaan yang dapat dibuat. Bentuk usaha obat tradisional berdasarkan PERMENKES RI No. 006 tahun 2012 tentang industri dan usaha obat tradisional dikelompokkan menjadi industri obat tradisional yang selanjutnya disebut IOT, adalah industri yang membuat semua bentuk sediaan obat tradisional. Industri ekstrak bahan alam yang selanjutnya disebut IEBA, adalah industri yang khusus membuat sediaan dalam bentuk ekstrak sebagai produk akhir. Usaha kecil obat tradisional yang selanjutnya disebut UKOT, adalah usaha yang membuat semua bentuk sediaan obat tradisional, kecuali bentuk sediaan tablet dan efervesen. Usaha mikro obat tradisional yang selanjutnya disebut UMOT adalah usaha yang hanya membuat sediaan obat tradisional dalam bentuk param, tapel, pilis, cairan obat luar dan rajangan. Usaha jamu racikan adalah usaha yang dilakukan oleh depot jamu atau sejenisnya yang dimiliki perorangan dengan melakukan pencampuran sediaan jadi dan/atau sediaan segar obat tradisional untuk dijajakan langsung kepada konsumen. Usaha jamu adalah usaha yang dilakukan oleh perorangan dengan menggunakan bahan obat tradisional dalam bentuk cairan yang dibuat segar dengan tujuan untuk dijajakan langsung kepada konsumen. (Kementerian Kesehatan RI, 2012). Adapun pendelegasian pemberian kewenangan pemberian izin berdasarkan Peraturan Menteri Kesehatan Republik Indonesia Nomor 006 Tahun 2012 tentang industri dan usaha obat tradisional, yaitu: Industri Obat Tradisional (IOT) dan Industri Ekstrak Bahan Alam kepada Direktur Jenderal Kementrian Kesehatan, Usaha Kecil Obat Tradisional (UKOT) kepada Kepala Dinas Kesehatan Provinsi, dan Usaha Mikro Obat Tradisional kepada Kepala Dinas Kesehatan Kabupaten/Kota. (Kementrian Kesehatan Republik Indonesia, 2012a).
Persyaratan yang diajukan kepada kepala dinas kesehatan Kota/Kabupaten untuk pengajuan perizinan UMOT secara garis besar memiliki kesamaan untuk pengajuan IOT, IEBA, dan UKOT. Perbedaan terdapat pada tujuan pengajuan
surat permohonan, untuk UMOT pengajuan ditujukkan kepada kepala dinas kesehatan kota/kabupaten. Untuk UMOT tidak dipersyaratkan memiliki apoteker sebagai penanggung jawab teknis, serta tidak diwajibkan untuk memiliki fasilitas sesuai CPOTB. Hal tersebut mungkin dikarenakan pertimbangan kemampuan finansial UMOT dalam pemenuhan syarat CPOTB serta pembayaran apoteker sebagai penanggung jawabnya. Namun sebaiknya UMOT tetap memiliki sarana produksi sesuai dengan ketentuan CPOTB, agar dihasilkan sediaan obat tradisional yang terjamin mutu, khasiat serta keamanannya ketika beredar di masyarakat.
Adapun untuk registrasi produk obat tradisional UMOT dilakukan dengan
mengajukan registrasi kepada Kepala Badan Pengawas Obat dan
Makanan. Dalam persyaratan yang ada dalam Peraturan Menteri Kesehatan Nomor 007 Tahun 2012 Registrasi Obat Tradisional, disebutkan salah satu ketentuan obat tradisional yang dapat memperoleh izin edar adalah dibuat dengan menerapkan CPOTB. Terkait dengan ketentuan tersebut, bagi UMOT yang belum memiliki fasilitas produksi sesuai CPOTB dapat melakukan kontrak produksiproduk obat tradisional kepada IOT ataupun UKOT yang telah
mememuhi persyaratan CPOTB. Di mana izin edar yang diberikan dimiliki oleh pemberi kontrak. (Kementerian Kesehatan RI, 2012b)
4.2 Penerapan perizinan UMOT di Suku Dinas Kesehatan Kota Jakarta
utara
Pengaplikasian peraturan tersebut dalam hal perolehan izin sendiri belum dilakukan oleh pihak suku dinas kesehatan kota administrasi Jakarta Utara. Hal tersebut dibuktikan bahwa tercatat dalam tahun 2012, setelah peraturan diundangkan yaitu pada bulan februari 2012 sampai akhir tahun 2012, perizinan di Suku Dinas Kesehatan Jakarta Utara masih menggunakan peraturan lama, dimana perizinan di Suku Dinas Kesehatan dilakukan oleh IKOT, tabel 4.1. Belum adanya dokumen baku prosedur mutu yang berisi tentang persyaratan, tahapan serta
penanggung jawab dalam setiap tahapan perizinannya, diindikasikan sebagai penyebab peraturan PERMENKES RI No. 006 tahun 2012 tentang perizinan UMOT belum dilaksanakan di Suku Dinas Kesehatan kota Jakarta Utara. Dokumen baku prosedur mutu di suku dinas kesehatan kota administrasi Jakarta Utara sendiri dibuat oleh kepala seksi sumber daya kesehatan. Belum adanya dokumen prosedur mutu ini, dikarenakan belum adanya keputusan kepala dinas kesehatan Provinsi DKI Jakarta tentang perizinan UMOT.
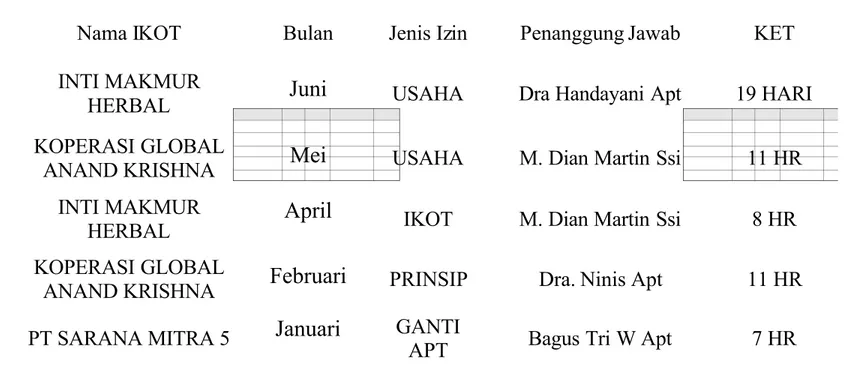
Tabel 4.1 Daftar Perizinan Usaha Obat Tradisional Tahun 2012 di Suku Dinas Kesehatan Kota Jakarta Utara
Nama IKOT Bulan Jenis Izin Penanggung Jawab KET INTI MAKMUR
HERBAL Juni USAHA Dra Handayani Apt 19 HARI KOPERASI GLOBAL
ANAND KRISHNA Mei USAHA M. Dian Martin Ssi 11 HR INTI MAKMUR
HERBAL April IKOT M. Dian Martin Ssi 8 HR KOPERASI GLOBAL
ANAND KRISHNA Februari PRINSIP Dra. Ninis Apt 11 HR PT SARANA MITRA 5 Januari GANTI
APT Bagus Tri W Apt 7 HR
Izin industri dan usaha obat tradisional lama yang telah dikeluarkan berdasarkan Peraturan Menteri Kesehatan Nomor 246/Menkes/Per/V/1990
tentang izin usaha industri obat tradisional dan pendaftaran obat tradisional dinyatakan masih tetap berlaku. Izin industri dan usaha obat tradisional harus diperbaharui sesuai dengan persyaratan dalam PERMENKES RI No. 006 tahun 2012 tentang industri dan usaha obat tradisional paling lama 2 (dua) tahun sejak peraturan menteri ini diundangkan.
Sedangkan untuk izin UMOT yang dterbitkan berdasarkan PERMENKES RI No. 006 tahun 2012 tentang industri dan usaha obat tradisional berlaku seumur hidup selama usaha obat tradisional yang bersangkutan masih berproduksi dan memenuhi ketentuan peraturan perundang-undangan. Untuk pengajuan izin UMOT tersebut, ditujukan kepada kepala dinas kesehatan kota/kabupaten.
Adapun fungsi dinas kesehatan kabupaten/kota terkait pembinaan dalam bentuk pemberian informasi, sosialisasi peraturan, memberikan bimbingan teknis
secara langsung ke lapangan maupun tidak langsung kepada pemilik izin industri kecil obat tradisional maupun yang akan mengajukan perizinan terkait produksi
obat tradisional untuk meningkatkan pemahaman mengenai adanya
BAB 5
KESIMPULAN DAN SARAN
5.1 Kesimpulan
UMOT (Usaha Mikro Obat Tradisional) merupakakan salah satu jenis usaha obat tradisional berdasarkan PERMENKES RI No. 006 tahun 2012 tentang usaha industri obat tradisional dan pendaftaran obat tradisional, yang dapat membuat bentuk sediaan param, tapel, pilis, cairan obat luar dan rajangan. Usaha tersebut berbeda dengan
kelompok usaha lain yang diklasifikasikan pada PERMENKES RI No. 006 tahun 2012, yaitu IOT, IEBA, UKOT dan Usaha jamu racikan dan Usaha Jamu gendongan. Klasifikasi pada peraturan tersebut dibedakan berdasarkan bentuk sediaan yang boleh diproduksi oleh masing-masing Industri ataupun Usaha.
Tata cara perizinan Usaha Mikro Obat Tradisional (UMOT) surat pengajuan izin ditujukan kepada kepala dinas kesehatan kota/kabupaten dengan mencantumkan persyaratan dokumen, seperti yang tercantum dalam PERMENKES RI No. 006 tahun 2012 tentang industri dan usaha obat tradisional. Produk UMOT harus produk tersebut harus dibuat dengan cara yang sesuai dengan CPOTB untuk memiliki izin edar,. Oleh karena itu, untuk UMOT yang masih belum memenuhi syarat CPOTB untuk produksi obat tradisionalnya, dapat melakukan kotrak produksi kepada IOT (Industri Obat Tradisional) dan UKOT (Usaha Kecil Obat Tradisional), dengan pemilik izin edar berupa pemberi kontrak.
Penerapan perizinan UMOT berdasarkan PERMENKES RI No. 006 tahun 2012 di suku dinas kesehatan kota administrasi Jakarta Utara sendiri belum dilaksanakan. Hal tersebut dikarenakan belum adanya dokumen prosedur mutu tentang perizinan UMOT, dikarenakan belum adanya keputusan kepala dinas kesehatan Provinsi DKI Jakarta tentang perizinan UMOT.
5.2 Saran
Perlu adanya tindakan sosialisasi oleh dinas kesehatan kepada pengusaha obat tradisional yang telah memiliki izin atau yang akan mengajukan izin tentang adanya PERMENKES RI No. 006 tahun 2012 tentang industri dan usaha obat tradisional Solsialisasi tersebut dilakukan agar penerapan peraturan tersebut akan berjalan baik.
DAFTAR ACUAN
Badan Pengawas Obat dan Makanan. (2011). Peraturan Kepala Badan Pengawas Obat dan Makanan Republik Indonesia Nomor HK.03.1.23.06.11.5629 Tahun 2011 Tentang Persyaratan Teknis Cara Pembuatan Obat Tradisional yang Baik . Jakarta: Badan Pengawas Obat dan Makanan Republik Indonesia.
Kementrian Kesehatan Republik Indonesia. (1990). Peraturan Menteri Kesehatan Nomor 246 Tahun 1990 tentang Izin Usaha Industri Obat Tradisional dan Pendaftaran Obat Tradisional. Jakarta: Kementrian Kesehatan Republik Indonesia. Kementrian Kesehatan Republik Indonesia. (2012a). Peraturan Menteri Kesehatan
Nomor 006 Tahun 2012 tentang Izin Usaha Industri Obat Tradisional dan Pendaftaran Obat Tradisional. Jakarta: Kementrian Kesehatan RI.
Kementrian Kesehatan Republik Indonesia. (2012b). Peraturan Menteri Kesehatan Nomor 007 Tahun 2012 Registrasi Obat Tradisional. Jakarta: Kementrian
Kesehatan RI.
Firmansyah, Muhamad. (2009). Tata Cara Mengurus Perizinan Usaha Farmasi dan Kesehatan. Jakarta: Visimedia.
Gubernur Provinsi DKI Jakarta. (2009). Peraturan Gubernur Provinsi DKI Jakarta Nomor 150 tahun 2009 tentang Organisasi dan Tata Kerja Dinas Kesehatan.
Jakarta: Pemerintah Provinsi DKI Jakarta.
Kementerian Kesehatan RI. (2010). Riset Kesehatan Dasar (RISKESDAS 2010). Jakarta: Badan Penelitian dan Pengembangan Kesehatan Kementrian Kesehatan RI.
Pemerintah Provinsi DKI Jakarta. (2009). Peraturan Daerah Provinsi DKI Jakarta Nomor 4 Tahun 2009 tentang Sistem Kesehatan Daerah. Jakarta: Pemerintah
Provinsi DKI Jakarta.
Pemerintah Republik Indonesia. (2000). Peraturan Pemerintah Republik Indonesia Nomor 25 Tahun 2000 tentang Kewenangan Pemerintah dan Kewenangan
Propinsi sebagai Otonom. Jakarta: Pemerintah Republik Indonesia.
Pemerintah Republik Indonesia. (1999). Undang-Undang Republik Indonesia Nomor 22 Tahun 1999 tentang Pemerintahan Daerah. Jakarta: Pemerintah Republik Indonesia.
Lampiran 1. Formulir 18 (lanjutan)
h. Nomor pokok wajib pajak : terlampir
i. Surat keterangan domisili : terlampir
Demikianlah permohonankami.
Pemohon,
Lampiran 3. Formulir 20a
KEPUTUSAN
KEPALA DINAS KESEHATAN KABUPATEN/KOTA ... NOMOR ………
TENTANG
IZIN USAHA MIKRO OBAT TRADISIONAL ...
Membaca : Surat permohonan Nomor ... tanggal ……….Perihal Pemohonan Izin Usaha Mikro Obat Tradisional dengan kelengkapan dokumen pertanggal …………
Menimbang : bahwa permohonan …………. tersebut dapat disetujui,
oleh karena itu perlu menerbitkan Izin Usaha Mikro Obat Tradisional.
MEMUTUSKAN:
Menetapkan :
Kesatu : Memberikan Izin Usaha Mikro Obat Tradisional
kepada... Nomor Pokok Wajib Pajak (NPWP) ... dengan ketentuan sebagai berikut :
1. Jenis Usaha ………
2. Bentuk Sediaan yang diproduksi ……… 3. Lokasi Usaha:
a. Alamat Kantor ... b. Alamat Usaha ...
c. Alamat gudang ………
(bila berada di luar lokasi usaha)
4. Harus mematuhi peraturan perundang-undangan yang berlaku;
5. Melaksanakan pelaporan sesuai yang ditetapkan oleh Menteri;
6. Izin Usaha Mikro Obat Tradisional berlaku untuk seterusnya selama Usaha Mikro Obat Tradisional yang bersangkutan masih aktif melakukan kegiatan produksi
dan memenuhi ketentuan peraturan
perundang- undangan.
Kedua : Keputusan ini mulai berlaku sejak tanggal ditetapkan
Ditetapkan di ……… Pada tanggal: ………
Kepala Dinas KesehatanKabupaten/Kota ………,
………..……… NIP ...
Lampiran 3. Formulir 20a (lanjutan)
Tembusan:
1. Direktur Jenderal Bina Kefarmasian dan Alat Kesehatan, Kementerian Kesehatan RI
2. Kepala Badan Pengawas Obat dan Makanan
3. Kepala Balai Besar/Balai Pengawas Obat dan Makanan di ... 4. Kepala Dinas Kesehatan Provinsi ...