BAB II
TINJAUAN PUSTAKA
2.1. Infark Miokardium Non Elevasi Segmen ST
SKA adalah suatu definisi operasional yang menggambarkan spektrum
kondisi terjadinya iskemia dan atau infark miokardium yang disebabkan penurunan
aliran darah koroner yang bersifat tiba-tiba (Amsterdam, 2014)
Berdasarkan pedoman tatalaksana SKA yang dikeluarkan oleh PERKI
tahun 2015 diagnosis SKANEST yang terdiri dari IMANEST dan APTS ditegakkan
jika terdapat keluhan angina pektoris akut tanpa adanya elevasi segmen ST yang
persisten pada dua sadapan yang bersebelahan. Rekaman EKG saat presentasi
dapat berupa depresi segmen ST, inversi gelombang T, gelombang T yang datar,
gelombang T pseudo-normalization, atau bahkan tanpa perubahan. IMANEST dan
APTS dibedakan berdasarkan peningkatan marka jantung. Marka jantung yang
lazim digunakan adalah Troponin I/T atau CK-MB. Bila hasil pemeriksaan
biokimia marka jantung terjadi peningkatan bermakna, maka diagnosis menjadi
IMANEST. Pada APTS marka jantung tidak meningkat secara bermakna. Pada
SKA, nilai ambang untuk peningkatan CK-MB yang abnormal adalah beberapa unit
melebihi nilai normal atas (Irmalita, 2015).
Berdasarkan pedoman tatalaksana SKA oleh PERKI tahun 2015 depresi segmen ST yang diagnostik untuk iskemia adalah sebesar ≥ 0,05 mV di sadapan V1-V3 dan ≥ 0,1 mV di sadapan lainnya. Inversi gelombangT yang simetris ≥ 0,2 mV mempunyai spesifisitas tinggi untuk untuk iskemia akut. Semua perubahan
EKG yang tidak sesuai dengan kriteria EKG diagnostik dikategorikan sebagai
perubahan EKG nondiagnostik (Irmalita, 2015).
Pasien dengan IMANEST memiliki mortalitas yang lebih tinggi
dibandingkan dengan APTS. Pasien dengan APTS memiliki risiko kematian jangka
pendek sebesar 1,5-2,0% sedangkan pasien dengan IMANEST dan IMAEST
2.2. Stratifikasi Risiko Pasien IMANEST
SKANEST memiliki spektrum klinis dan risiko yang amat lebar maka
proses stratifikasi risiko harus dilakukan sesegera mungkin. Stratifikasi risiko awal
memiliki peranan penting dalam menentukan prognosis dan strategi pengobatan
yang akan dilakukan (Hamm, 2011; Akkerhuis, 2001). Stratifikasi risiko adalah
suatu proses berkelanjutan hingga pasien dipulangkan dari rumah sakit dan proses
ini dapat mengubah berbagai strategi pengobatan setiap waktunya. Bahkan setelah
pasien dipulangkan, pasien masih dapat berada dalam risiko tinggi untuk terjadinya
KKvM (Hamm, 2011).
Beberapa cara stratifikasi risiko telah dikembangkan dan divalidasi untuk
SKA. Beberapa stratifikasi risiko yang paling sering digunakan adalah skor TIMI
dan GRACE. Skor TIMI dihasilkan dari penelitian TIMI 11b dan divalidasi pada
beberapa percobaan seperti TACTICS-TIMI 18. Kekurangan dari skor TIMI adalah
ketidakmampuannya untuk mendiskriminasi risiko secara lebih rinci. Skor GRACE
merupakan skor paling mutakhir namun lebih rumit dan membutuhkan penggunaan
aplikasi komputer dalam penghitungannya. Satu skor lagi yang tidak terlalu
terkenal adalah skor PURSUIT (Platelet glycoprotein IIb/IIIa in Unstable angina:
Receptor Suppression Using Integrilin Therapy). Pada suatu penelitian oleh Goncalves dkk yang meneliti penggunaan skor GRACE, TIMI, dan PURSUIT pada
populasi yang sama di suatu pusat kesehatan pada 460 pasien. Hasilnya terlihat
bahwa skor GRACE merupakan yang terbaik dalam menilai risiko kematian atau
infark miokardium dalam 1 tahun (De Araujo Goncalves, 2005). Hal ini sejalan
dengan penelitian Aragam dkk yang melihat bahwa daya diskriminasi skor GRACE
lebih baik dibandingkan TIMI (Aragam, 2009). Perbandingan variabel yang
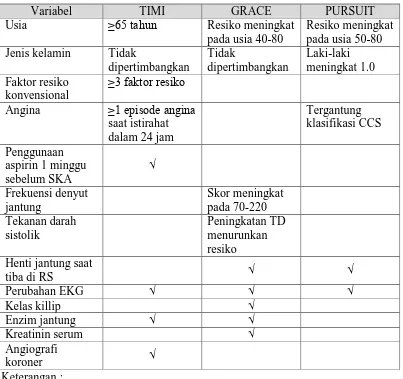
Tabel 2.1. Perbandingan tiga sistem skor pada SKANEST (Chandra, 2012)
Variabel TIMI GRACE PURSUIT
Usia ≥65 tahun Resiko meningkat
pada usia 40-80
Angina ≥1 episode angina
saat istirahat
√: termasuk dalam variabel penilaian
2.2.1. Skor GRACE pada IMANEST
Skor GRACE adalah sistem skor yang direkomendasikan oleh pedoman
tatalaksana oleh ESC yang diaplikasikan pada saat pasien masuk dan pulang.
Klasifikasi GRACE ditujukan untuk memprediksi mortalitas saat perawatan di
rumah sakit dan dalam 6 bulan, 1 tahun, dan 3 tahun setelah keluar dari rumah sakit
(Granger, 2003; Elbarouni, 2009). Skor GRACE dan klasifikasinya dapat dilihat
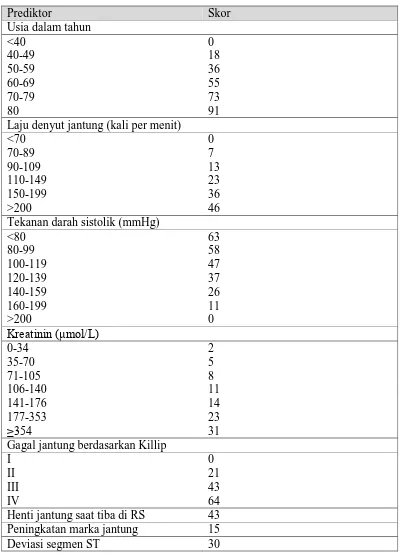
Tabel 2.2. Skor GRACE untuk SKANEST (Granger, 2003)
Laju denyut jantung (kali per menit)
<70 0 Peningkatan marka jantung 15
Tabel 2.3. Stratifikasi risiko berdasarkan skor GRACE (Fox, 2006; Hamm, 2011)
Prediktor Kematian di RS Prediktor Kematian 6 bulan
Skor Risiko Skor Risiko
≤108 <1% ≤88 Rendah (<3%)
109-140 1-3% 89-118 Sedang (3-8%)
>140 >3% >118 Tinggi (>8%)
2.2.2 Penentuan Risiko Pasien IMANEST
Selain stratifikasi risiko yang telah disebutkan di atas, pada pedoman
tatalaksana oleh ESC yang diadopsi oleh PERKI pasien juga dibagi dalam beberapa
kelompok risiko, yaitu risiko sangat tinggi dan risiko tinggi (Hamm, 2011).
Penentuan risiko ini berperan dalam penentuan perlu atau tidaknya dilakukan
strategi invasif seperti terlihat pada tabel 2.4..
Tabel 2.4. Kriteria stratifikasi risiko sangat tinggi dan tinggi untuk strategi invasif
berdasarkan pedoman tatalaksana ESC 2011 (Hamm, 2011)
Kelompok Risiko Kriteria
Risiko Sangat Tinggi Angina refrakter Gagal jantung akut
Aritmia ventrikel mengancam jiwa Keadaan hemodinamik tidak stabil Risiko Tinggi
Primer Kenaikan atau penurunan troponin yang relevan Perubahan gelombang T atau segmen ST yang dinamis (simptomatik maupun tanpa gejala)
Sekunder Diabetes mellitus
Insufisiensi ginjal (eGFR <60 mL/menit/1,73m2) Penurunan fungsi ventrikel kiri (fraksi ejeksi <40%) Paska infark baru
Riwayat IKP dalam 1 bulan Riwayat CABG
Skor GRACE menengah hingga tinggi
2.3. Ekokardiografi Pada Pasien IMANEST
Penggunaan ekokardiografi pada pasien IMA memiliki beberapa peranan,
antara lain:
1. Diagnosis IMA pada pasien dengan nyeri dada dimana hasil EKG tidak
adanya abnormalitas gerakan miokardium secara cepat. Abnormalitas ini
merupakan akibat dari adanya infark miokardium (Cheitlin, 2003).
2. Estimasi besarnya miokardium yang terkena dampak IMA dan melihat
perbedaan luasnya infark setelah terapi reperfusi. Fungsi sistolik global dan
regional ventrikel kiri dapat meningkat terutama setelah terapi reperfusi
(Cheitlin, 2003).
3. Evaluasi pasien dengan ketidakstabilan hemodinamik (Cheitlin, 2003).
4. Deteksi komplikasi. Ekokardiografi juga berguna dalam melihat adanya
komplikasi dari IMA yakni perluasan disfungsi miokardium, abnormalitas
katup, defek septum interventrikular, dan ruptur miokardium (Cheitlin, 2003).
5. Stratifikasi risiko. Indikator prognostik yang paling kuat pada pasien pasca IMA
adalah derajat disfungsi sistolik ventrikel kiri, volume ventrikel kiri, bentuk
ventrikel kiri (sferisitas), adanya abnormalitas gerakan miokardium akibat suatu
PJK, regurgitasi mitral, disfungsi diastolik, dan adanya gagal jantung
(Braunwald, 2012; Bursi, 2006; Cheitlin, 2003; Scirica, 2010; Vartdal, 2007;
Wong, 2004)
Sebagai alat non invasif yang mudah dan dapat dilakukan sewaktu-waktu
maka ekokardiografi menjadi alat yang sangat berguna pada pasien IMA (Cheitlin,
2003).
2.3.1. Pemeriksaan FEVK Pada Pasien IMANEST
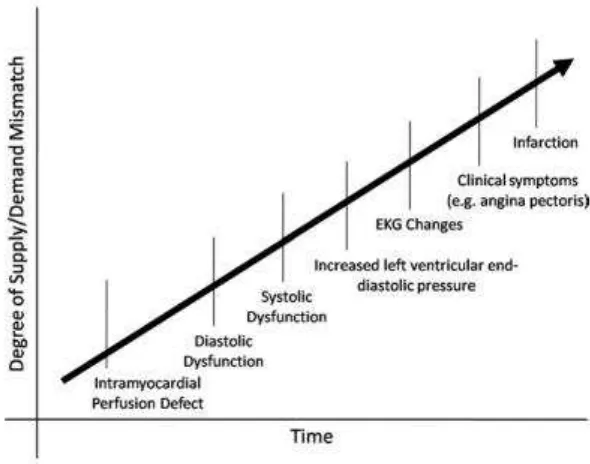
Berdasarkan kaskade iskemia, yang dimunculkan oleh Hauser dkk tahun
1985 terjadi tahapan kejadian klinis yang terjadi sejalan dengan iskemia. Perfusi ke
miokardium ditentukan oleh aliran darah koroner dan konsumsi oksigen oleh
miokardium. Adanya ketidakseimbangan antara suplai dengan kebutuhan ini akan
menyebabkan terjadinya iskemia. Kejadian ini dapat menimbulkan manifestasi
klinis atau tidak. Ekokardiografi dapat menilai terjadinya perubahan patofisiologi
ini mulai dari tahap awal dan lebih sensitif dibandingkan anamnesis, pemeriksaan
Gambar 2.1. Kaskade Iskemia (Herzog E 2009)
Sekali terjadi ketidakseimbangan antara suplai dengan kebutuhan oksigen dan melewati ambang batas maka akan terjadi abnormalitas fungsi miokardium. Karakteristik dari disfungsi akibat iskemia adalah terjadi gangguan secara regional sesuai dengan distribusi aliran koroner. Segmen yang dinilai adalah 17 segmen berdasarkan ketetapan dari American Society of Echocardiography (ASE). Segmen yang paling awal terpengaruh adalah yang paling distal. Seperti contoh pada kasus oklusi total pada pembuluh darah Left Anterior Descending (LAD) maka terjadi abnormalitas mulai dari paling distal yakni di daerah apeks, kemudian diikuti daerah medial dan basal. Pengukuran fungsi sistolik lebih bermakna dibandingkan pengukuran fungsi diastolik dalam diagnosis, pengobatan, dan prognosis pasien dengan SKA (Herzog E 2009).
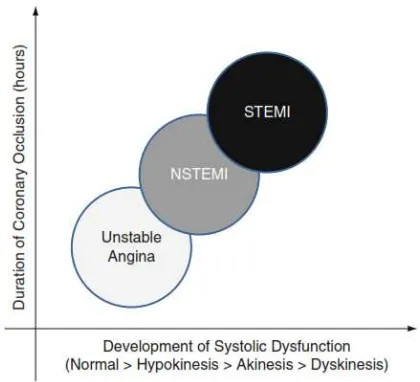
Oklusi dari pembuluh darah koroner epikardium pada saat SKA akan mengakibatkan kehilangan fungsi kontraksi dari segmen miokardium yang disuplai oleh arteri tersebut. Luasnya kerusakan ini bergantung pada keparahan dan lamanya terjadi oklusi. Pada pasien APTS, gerakan dinding biasanya masih normal kecuali
pemeriksaan dilakukan pada saat episode nyeri dada. Pada pasien IMANEST oklusi biasanya terjadi pada cabang pembuluh darah pada pasien dengan distribusi
pada daerah subendokardium. Namun pada pemeriksaan ekokardiografi transtoraks biasa terlihat pada seluruh lapisan dinding jantung. Sedangkan pada IMAEST, oklusi biasa terjadi pada pembuluh darah utama tanpa tersedia pembuluh kolateral sehingga terjadi gangguan kontraktilitas lebih luas (Herzog, 2009).
Herzog (2009) menyatkan perhitungan luasnya kerusakan kontraktilitas dilakukan semikuantitatif dengan menggunakan tiga parameter, yaitu:
1. Keparahan kehilangan kontraktilitas a. Normal : kontraktilitas bagus
b. Hipokinetik : kontraktilitas berkurang parsial c. Akinetik: kontraktilitas tidak ada
d. Diskinesis: gerakan paradoks dari segmen yang terkena pada saat sistol
e. Aneurisma: pergerakan ke arah luar dari segmen yang terkena pada saat sistol dan diastol
2. Jumlah dan lokasi terjadinya disfungsi miokardium 3. Kemungkinan area distribusi koroner yang terlibat
Gambar 2.2. Perkembangan disfungsi miokardium pada SKA (Herzog, 2009).
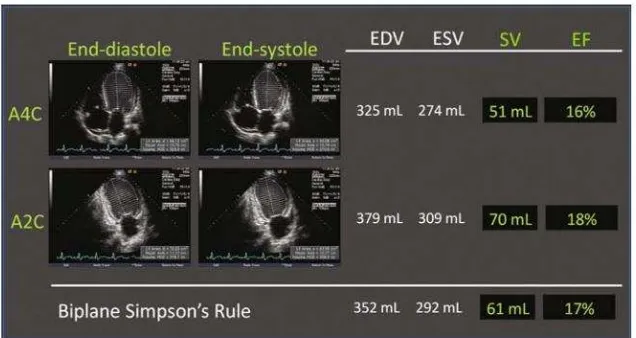
volume sistolik dan diastolik ventrikel kiri dan membaginya dengan rumus pada gambar 2.3.
Gambar 2.3. Metode pengitungan FEVK (Rimington, 2007)
Nilai FEVK yang didapatkan kemudian dapat diklasifikasikan menjadi
beberapa tingkatan seperti terlihat pada tabel 2.5.
Tabel 2.5. Tingkatan fungsi sistolik berdasarkan FEVK (Rimington, 2007)
Normal Menurun ringan Menurun sedang Menurun berat
≥55% 45-54% 30-44% <30%
Penghitungan ini dapat dilakukan dengan metode Teichholtz dengan modalitas M-mode dan metode Simpson dengan menghitung volume. Penghitungan dengan metode Teichholtz ini hanya bisa dilakukan bila tidak terjadi abnormalitas gerakan dinding. Dikarenakan pada IMA terjadi abnormalitas gerakan dinding jantung maka sebaiknya dilakukan penghitungan dengan metode Simpson (Rimington, 2007). Pengukuran ini dapat dilakukan manual dan pada beberapa alat
ekokardiografi dapat dilakukan secara semiotomatis dimana pemeriksa cukup
Gambar 2.4. Penghitungan FEVK menggunakan rumus Simpson secara semiotomatis (Herzog, 2009)
Walaupun penghitungan dengan metode Simpson lebih akurat namun pada penelitian Arora dkk yang melihat perbedaan penghitungan FEVK dengan metode
Teichholtz dengan Simpson pada pemeriksaan Cardiac Magnetic Resonance
Imaging (CMRI), menyimpulkan bahwa tidak ditemukan perbedaan pada rata-rata
FEVK (Arora, 2010).
Pada beberapa keadaan dimana terjadinya regurgitasi aorta dan mitral maka pengukuran dengan metode Simpson juga memiliki kekurangan dimana metode ini menghitung volume sekuncup yang merupakan jumlah dari volume regurgitan ditambah volume sekuncup sebenarnya sehingga memberi hasil yang lebih tinggi dari normal (Herzog, 2009).
Pemeriksaan FEVK dinilai lebih akurat dibandingkan dengan indeks skor
gerakan dinding. Hal ini karena pada pemeriksaan indeks skor gerakan dinding
tidak memperkirakan daerah yang normal dan hiperdinamik pada pasien IMA.
Sebagai contoh pada dua pasien dengan IMA akibat oklusi di LAD. Satu pasien
mengalami hiperkinesis gerakan dinding, satu lagi tidak. Bila dengan penghitungan
indeks skor gerakan dinding maka nilainya akan sama sedangkan bila dengan
FEVK maka pasien dengan hiperkinesis akan memperlihatkan nilai lebih tinggi (Herzog, 2009).
ventrikel kiri menempati rekomendasi kelas I tingkat bukti C dalam diagnosis
(Roffi, 2015).
Berbagai penelitian telah memperlihatkan bahwa FEVK merupakan salah satu prediktor yang paling kuat dalam menilai prognosis pasien dengan penyakit jantung iskemik termasuk SKA (Herzog, 2009; Multicenter Postinfarction Research Group, 1983). Pada pasien IMA, FEVK merupakan prediktor paling kuat
untuk mortalitas dan risiko aritmia mengancam jiwa pada pasien IMA. Setelah kejadian SKA terlewati, maka FEVK tersisa juga menjadi indikator penting dalam penatalaksanaan pasien, yakni dalam penentuan pemakaian alat bantu implantable cardioverter-defibrillator (ICD) (Herzog, 2009; Zorzi, 2015).
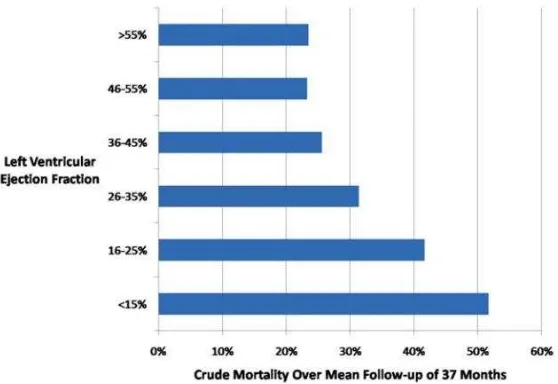
Pada pasien dengan gagal jantung paska IMA, maka terdapat grafik yang
linear antara mortalitas dengan nilai FEVK (Curtis, 2003; Herzog, 2009).
Gambar 2.5. Hubungan FEVK dengan mortalitas pasien gagal jantung paska IMA
(Herzog, 2009)
2.4. Nilai Prognostik FEVK dan Skor GRACE pada Pasien SKA dan IMANEST
Penelitian Bedetti dkk pada 487 pasien SKA tahun 2008 menunjukkan
bahwa echo score merupakan suatu prediktor yang sangat kuat dalam memprediksi
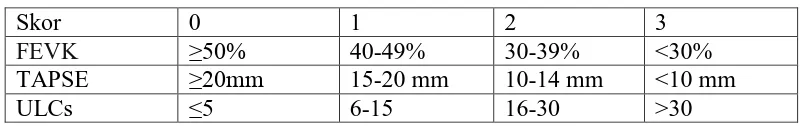
dan tricuspid annular plane systolic excursion (TAPSE). Rentang skornya dari nilai
0 hingga 9. Skornya dapat dilihat pada tabel 2.6 (Bedetti, 2010).
Tabel 2.6 Penilaian Echo Score (Bedetti, 2010)
Skor 0 1 2 3
FEVK ≥50% 40-49% 30-39% <30%
TAPSE ≥20mm 15-20 mm 10-14 mm <10 mm
ULCs ≤5 6-15 16-30 >30
Penilaian echo score ini terbukti akurat dalam memprediksi keluaran klinis
pasien dengan SKA. Pada uji Kaplan-Meier terlihat bahwa nilai echo score terbukti
memberikan nilai prognostik kematian selama dan 6 bulan. Pada uji multivariat,
nilai echo score juga terlihat bermakna bersama skor GRACE, bahkan lebih tinggi
dibandingkan skor GRACE. Lebih khususnya, nilai echo score sangat baik diaplikasikan pada pasien risiko sedang untuk memprediksi lebih lanjut risiko
pasien (Bedetti, 2010).
Penelitian Liu dkk tahun 2011 yang meneliti nilai prediktif penambahan
HbA1C pada skor GRACE pada 549 pasien SKA tanpa diabetes militus (DM) yang
menjalani intervensi koroner perkutan (IKP) memperlihatkan bahwa FEVK dan skor GRACE serta nilai HbA1C bermakna dalam memprediksi KKvM yakni
kematian dan IMA nonfatal. FEVK dan skor GRACE juga terlihat konsisten memberikan nilai prognostik bahkan setelah dilakukan uji univariat dan multivariat
(Liu, 2015).
Penelitian Kobayashi dkk yang meneliti nilai prognostik left ventricular end
diastolik pressure (LVEDP) pada 367 pasien NSTEMI tahun 2013-2014 yang menjalani prosedur angiografi koroner terhadap KKvM (mortalitas dan gagal
jantung akut selama perawatan) memperlihatkan bahwa peningkatan LVEDP >22
mmHg berhubungan dengan risiko KKvM. Nilai FEVK terlihat berhubungan secara signifikan dengan nilai LVEDP. Pasien dengan LVEDP < 22 mmHG
memiliki nilai rerata FEVK sebesar 60% dibandingkan dengan 52% pada pasien dengan LVEDP >22 mmHg (Kobayashi, 2015).
Penelitian Zorzi dkk tahun 2015 yang meneliti faktor-faktor risiko
dari 1325 pasien (69.7% pria, usia rata-rata 70 tahun) angka kejadian aritmia
mengancam jiwa sebesar 1.5% dan kematian sebesar 4.7%. Prediktor independen
kejadian aritmia mengancam jiwa adalah skor GRACE >140 (odds ratio = 6.9 95%
CI 1.5-30.6, nilai p 0.01) dan FEVK < 35% (OR=3.7 95% CI 1.5-9.4, nilai p 0.006).
Kedua parameter ini juga bermakna dalam prediksi kematian dengan OR
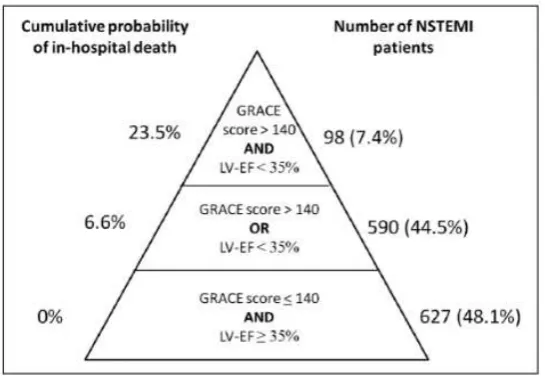
masing-masing sebesar 11.9 dan 3.7. Probabilitas kumulatif pasien dengan skor GRACE
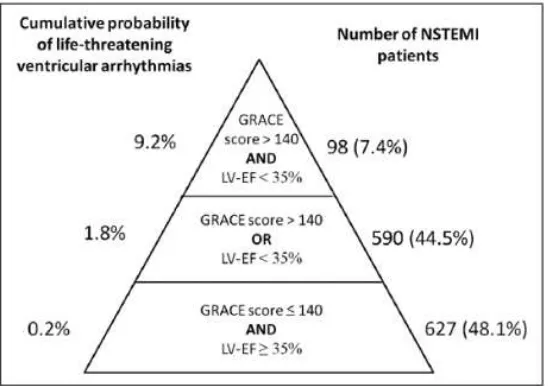
>140 dan FEVK <35% untuk mengalami aritmia mengancam jiwa sebesar 9.2% dan kematian sebesar 23%. Hal ini sangat bermakna dibandingkan pada pasien dengan skor GRACE ≥ 140 namun dengan FEVK ≥35% yang hanya 0.2% risiko aritmia mengancam jiwa dan 0% risiko kematian. Probabilitas kumulatif dapat
dilihat pada beberapa gambar 2.6. dan 2.7. (Zorzi, 2015).
Gambar 2.6. Stratifikasi risiko untuk kejadian aritmia mengancam jiwa selama
Gambar 2.7. Stratifikasi risiko untuk kejadian kematian selama perawatan.
Piramida risiko berdasarkan skor GRACE dan FEVK (Zorzi, 2015)
Penelitian Barthel dkk yang meneliti nilai prognostik laju pernafasan
sebagai prediktor risiko mortalitas jangka panjang (hingga 5 tahun) pada 941 pasien
dengan IMA pada tahun 2005 juga memperlihatkan bahwa FEVK dan skor GRACE
merupakan prediktor independen untuk mortalitas (Barthel, 2013).
Pada uji statistik log-rank di studi Barthel dkk ini memperlihatkan bahwa
pada pasien dengan skor GRACE < 120, berapapun nilai FEVK dan laju respirasi,
tidak akan memperlihatkan pengaruh nilai prognostik yang signifikan. Sebaliknya pada nilai skor GRACE ≥120, kedua nilai baik laju pernafasan maupun nilai FEVK memberikan nilai prognosis yang signifikan seperti terlihat pada gambar 2.8
Gambar 2.8. Nilai kumulatif rata-rata untuk resiko kematian berdasarkan skor
GRACE, frekuensi pernafasan, dan FEVK (Barthel, 2013)
Studi Guler dkk pada 115 pasien SKANEST tahun 2009 yang meneliti nilai
prognostik penambahan nilai lipoprotein(a) [Lp(a)] pada skor GRACE
memperlihatkan bahwa variabel yang signifikan untuk memprediksi KKvM
(kematian dan rehospitalisasi dalam 1 tahun) pada uji univariat adalah kadar
hemoglobin, kraetinin, usia, FEVK, riwayat IMA, dan kelas Killip. Namun kemudian pada uji multivariat yang bermakna hanya riwayat IMA dan kadar Lp(a).
Pada studi ini dilakukan uji penambahan nilai Lp(a) pada skor GRACE dan terlihat
memberikan penambahan nilai prognostik. (Guler, 2013).
Penelitian Abu-Assi dengan jumlah populasi yang cukup besar yakni 5985
pasien dengan SKA tahun 2010 yang bertujuan melihat apakah FEVK kiri memberikan peningkatan nilai prognostik pada skor GRACE memperlihatkan
2.5.Kerangka Teori
2.6. Kerangka Konsep