PENGHILANGAN KESADAHAN AIR YANG MENGANDUNG ION
Ca
2+DENGAN MENGGUNAKAN ZEOLIT ALAM LAMPUNG
SEBAGAI PENUKAR KATION
Atastina S.B,
Praswasti P.D.K. Wulan
, dan Syarifudin
Jurusan Teknik Gas dan Petrokimia
Fakultas Teknik – Universitas Indonesia
Kampus Baru UI, Depok 16424
Abstrak
Pemanfaatan zeolit sebagai media filter sekaligus media adsorbsi merupakan terobosan baru karena sumber daya alam Indonesia memiliki kandungan zeolit yang banyak. Uji adsorbsi ion kalsium pada zeolit menghasilkan kurva terobosan yang mengikuti S-Shape. Dari kurva terobosan tersebut dapat dilihat zeolit mampu mengadsorbsi ion kalsium dari 1200 ppm hingga di bawah 500 ppm. Zeolit dengan unggun 5 cm mampu mengadsorbsi hingga 500 ppm, zeolit dengan unggun 10 cm mampu mengadsorbsi hingga 300 ppm, dan zeolit dengan unggun 15 cm mampu mengadsorbsi hingga 200 ppm. Dari kurva terobosan dapat ditentukan kemampuan adsorbsi zeolit. Zeolit dengan unggun 5 cm mampu mengadsorbsi sebesar 10,83 mg ion Ca/gr zeolit. Untuk zeolit dengan unggun 10 cm mampu mengadsorbsi ion Ca sebesar 6,25 mg ion Ca/gr zeolit dan untuk zeolit dengan unggun 15 cm mampu mengadsorsi sebesar 3,61 mg ion Ca/gr zeolit. Kapasitas adsorbsi tergantung pada jumlah massa zeolit dan temperatur adsorbsi. Zeolit dengan unggun 5cm (300 gr) memiliki kapasitas yang lebih tinggi daripada zeolit dengan unggun 10 cm (600 gr) dan zeolit dengan unggun 15 cm (900gr) walaupun pada awal reaksi unggun zeolit 15 cm mampu mengadsorbsi sampai 200 ppm.
Abstract
The use of zeolite for medium of filtration and adsorption became interesting because of the large amount of zeolite in Indonesia. The adsorption performance of zeolite was indicated by the breakthrough curve for each concentration of ion calcium. It was show that zeolite could adsorb ion calcium concentration from 1200 ppm to 500 ppm. Zeolit with 5 cm bed level could reach 500 ppm maximum of adsorption, meanwhile the 10 cm bed of zeolite could reach 300 ppm dan the 15 cm could reach 200 ppm. As many as 10,83 mg of Ca ion/gr zeolite could be adsorbed by 5 cm bed of zeolite. With 10 cm bed level, zeolite could adsorb 6,25 mg of Ca ion/gr zeolite. With 15 cm bed level, zeolite could adsorb 3,61 mg of Ca ion/gr zeolite.The adsorption capacity of zeolite depended on its mass and the adsorption temperature. 5 cm bed of zeolit with 300 gr mass had higher capacity than the 10 cm (600 gr of mass zeolite) and 15 cm ones (900 gr of mass zeolite), although in the first reaction as many as 200 ppm could be adsorbed by 15 cm bed of zeolite.
PENDAHULUAN
Air merupakan unsur penting dalam kehidupan. Hampir seluruh kehidupan di dunia ini tidak terlepas dari adanya unsur air ini. Sumber utama air yang mendukung kehidupan di bumi ini adalah laut, dan semua air akhirnya akan kembali ke laut yang bertindak sebagai “reservoir” atau penampung. Air dapat mengalami daur hidrologi. Selama menjalani daur itu air selalu menyerap zat-zat yang menyebabkan air itu tidak lagi murni. Oleh karena itu, pada hakekatnya tidak ada air yang betul-betul murni.
Zat-zat yang diserap oleh air alam dapat diklasifikasikan sebagai padatan terlarut, gas terlarut dan padatan tersuspensi. Pada umumnya, jenis zat pengotor yang terkandung dalam air bergantung pada jenis bahan yang berkontak
dengan air itu, sedangkan banyaknya zat pengotor bergantung pada waktu kontaknya. Bahan-bahan mineral yang dapat terkandung dalam air karena kontaknya dengan batu-batuan terutama terdiri dari : kalsium karbonat (CaCO3),
magnesium karbonat (MgCO3), kalsium sulfat
(CaSO4), magnesium sulfat (MgSO4), dan
sebagainya.
Air yang banyak mengandung mineral kalsium dan magnesium dikenal sebagai “air sadah”, atau air yang sukar untuk dipakai mencuci. Senyawa kalsium dan magnesium bereaksi dengan sabun membentuk endapan dan mencegah terjadinya busa dalam air. Oleh karena senyawa-senyawa kalsium dan magnesium relatif sukar larut dalam air, maka senyawa-senyawa itu cenderung untuk memisah dari larutan dalam bentuk endapan atau presipitat yang akhirnya menjadi kerak.
Dengan cara-cara pengolahan yang khusus, persediaan air tawar juga dapat diambil dari air laut atau air payau (brackish water). Perbedaan utama antara air laut dan air tawar adalah kadar garamnya. Air laut mengandung sekitar 35.000 mg mineral per kg air, sedangkan kadar maksimum kalsium dalam air tawar adalah 1000 mg per kg air. Oleh karena itu pengolahan air laut dapat lebih kompleks dan lebih mahal.
Untuk memperoleh air bersih yang layak konsumsi diperlukan suatu cara yang lebih baik. Salah satu metode yang banyak digunakan adalah filtrasi (penyaringan). Metode ini dapat diterapkan di daerah pedesaan yang berada di tepi sungai ataupun sumber air lain.
Media filter yang biasa digunakan adalah pasir, kerikil, ijuk, arang dan zeolit. Di Indonesia zeolit tampaknya belum mendapat perhatian yang memadai sebagai media filtrasi air bersih. Padahal Indonesia secara geografis terletak pada jalur gunung berapi memiliki potensi zeolit yang cukup besar. Akan tetapi tidak semua zeolit dapat digunakan sebagai media filter. Zeolit alam Lampung yang merupakan jenis zeolit klinoptilolit cocok digunakan sebagai media filter. Zeolit alam lampung yang telah dipreparasi dengan perlakuan tertentu dapat menyerap ion Ca2+ penyebab kesadahan dalam air.
PENELITIAN
Prosedur Preparasi Zeolit
Untuk memperoleh zeolit alam Lampung dengan komposisi kimia didominasi oleh kation Na+ dilakukan proses pemanasan, prosedurnya adalah:
1. Serpihan zeolit diayak dengan siever
berukuran kurang lebih 20-30 mesh, untuk memperoleh butiran zeolit berukuran seragam.
2. Timbang zeolit yang telah diayak masing-masing 800 gr
3. Siapkan larutan garam NaCl 3 M sebanyak 1600 ml, sesuai dengan perbandingan solid : liquid (zeolit : larutan garam ) yaitu 1: 2 [gr : ml]
4. Bahan-bahan yang telah disiapkan, dipanaskan pada temperatur yang diusahakan konstan 100oC selama 4 jam, disertai dengan pengadukan.
5. Setelah 4 jam, tuang zeolit yang telah dipanaskan ke corong-corong yang dilapisi
kertas saring. Penyaringan dilakukan secara gravimetric.
6. Kemudian bilas dengan aquades. Pembilasan dilakukan sampai air bilasan yang terakhir menetes dari mulut corong terbukti bebas ion Cl-, menggunakan indikator AgNO3.
7. pengeringan sampel yang telah bebas ion Cl -di furnace pada temperatur 110oC selama 2 jam.
8. Sampel siap digunakan sebagai unggun filtrasi.
Pelaksanaan Penelitian
Kesadahan air dibuat dengan melarutkan CaCl2 sebanyak 120 gram ke dalam
air 100 liter. Dalam air CaCl2 akan terionisasi
menjadi Ca2+ dan Cl-. Ion Ca2+ inilah yang akan dikurangi konsentrasinya dalam air keluaran. Dengan laju alir tetap sebesar 30 lt/jam, ketinggian unggun zeolit 20-30 mesh divariasikan 5 cm, 10 cm, 15 cm. Selama 1 jam air sadah dialirkan dan setiap 10 menit diambil sampelnya untuk dianalisa dengan AAS di Lab. TEL Jurusan TGP UI. Dalam penelitian ini tidak dilakukan regenerasi zeolit.
Pertukaran ion dapat dituliskan sebagai berikut:
NaZ + CaCl2 CaZ + 2 NaCl
NaZ = Natrium -Zeolit CaZ = Calsium -Zeolit
Proses pertukaran ion berlangsung secara kontinyu dengan model aliran upflow (dari atas ke bawah).
HASIL DAN PEMBAHASAN
Kurva terobosan
Bentuk khas hasil adsorbsi dengan menggunakan unggun tetap beraliran kntinyu adalah berupa kurva terobosan. Kurva terobosan adalah kurva yang menunjukkan hubungan antara konsentrasi adsorbat keluaran kolom adsorbsi terhadap waktu adsorbsi. Waktu adsorbsi disini adalah waktu yang diukur pada interval tertentu selama terjadinya kontak antara adorbat dengan zeolit yang berlangsung secara kontinyu. Kurva terobosan adsorbsi ion Ca2+ hasil penelitian dapat dilihat pada gambar 1
Gambar 1. Kurva terobosan ion Ca Dari gambar di atas nampak perbedaan kurva penyerapan ion Ca2+. Proses adsorbsi yang paling baik terjadi pada zeolit dengan unggun 15 cm yang mencapai 200 ppm. Zeolit dengan unggun 10 cm mencapai 300 ppm, sedangkan zeolit dengan unggun 5 cm hanya mencapai 500 ppm. Dari sini terlihat semakin tinggi unggun zeolit makin rendah konsentrasi ion Ca2+. Akan tetapi laju peningkatan ion Ca2+ yang terendah adalah zeolit dengan unggun 10 cm. Seharusnya laju peningkatan yang terendah terjadi pada unggun zeolit 15 cm. Hal ini dapat terjadi disebabkan oleh perubahan laju alir ketika mengoperasikan percobaan pada unggun zeolit 15 cm, dimana laju alir telah berkurang karena jumlah air pada raw water berkurang sehingga tekanan airnya juga berkurang.
Dalam literature tentang adsorbsi (Sundstrom,1979), konsentrasi suatu spesi yang diadsorb dalam effluent selama beberapa waktu pertama menunjukkan kecenderungan konstan. Setelah unggun mulai jenuh barulah konsentrasi spesi tersebut meningkat tajam. Pada kondisi ini kurva yang terjadi berbentuk huruf S. titik dimana konsentrasi dalam effluent mulai meningkat disebut titik tembus (break point) sedangkan kurvanya dinamakan kurva terobosan (breakthrough curve). Dalam percobaan ini terjadi kurva terobosan titik tembusnya.
Dari fenomena yang ada, dalam penelitian ini adsorbsi yang terjadi adalah adsorbsi fisika di mana ion Ca2+ yang telah teradsorb dapat mengikat ion Na+. Dengan demikian terjadi pertukaran ion antara ion Na+ dari zeolit dan ion Ca2+ dari air.
Kapasitas Adsorbsi ion Ca terhadap
waktu adsorbsi
Dari hasil kurva terobosan yang terbentuk pada gambar 1 dibuat suatu grafik yang menyatakan hubungan antara jumlah
adsorbat yang terasorbsi (q) oleh zeolit terhadap waktu adsorbsi.
Grafik hubungan q vs t untuk adsorbsi ion Ca2+ menggunakan zeolit disajikan dalam gambar 2. 0 50 100 150 200 250 300 350 0 10 20 30 40 50 60 waktu (menit) q (mg ion Ca/gr zeolit) unggun zeolit 5 cm unggun 10 cm unggun 15 cm
Gambar 2. Kapasitas adsorbsi ion Ca pada zeolit. Dari gambar 2 terlihat pada kurva semakin lama semakin meningkat. Seharusnya kapasitas adsorbsi pada rentang waktu tertentu awalnya meningkat dan selanjutnya mencapai kesetimbangan (konstan). Hal ini disebabkan pengambilan sampel didasarkan pada waktu selama 60 menit sehingga tidak dapat diketahui sampai seberapa lama kondisi unggun akan jenuh. Akan tetapi dari hasil kurva terobosan dapat dilihat perkiraan kondisi unggun yang mencapai kejenuhan. Perbedaan ini disebabkan pada perhitungan kapasitas adsorbsi menggunakan satuan mg ion Ca/gr zeolit. Berdasarkan hal tersebut maka dimungkinkan untuk unggun 5 cm dengan berat 300 gram memiliki kapasitas terbesar zeolit dengan unggun 15 cm dengan berat 900 gram memiliki kapasitas adsorbsi terkecil.
Hasil perhitungan kapasitas adsorbsi pada ketiga jenis unggun zeolit disajikan dalam tabel berikut.
Tabel 1. Kapasitas adsorbsi ion Ca pada zeolit
zeolit C* (mg/lt) q* (mg ion Ca/gr zeolit) 600 10,83 900 43,33 1200 105,83 unggun 5 cm 1300 193,33 600 6,25 900 22,50 1100 50,83 unggun 10 cm 1200 91,25 500 3,61 800 13,33 1000 30,56 unggun 15 cm 1100 55,28 0 2 0 0 4 0 0 6 0 0 8 0 0 1 0 0 0 1 2 0 0 1 4 0 0 0 2 0 4 0 6 0 w a k t u ( m e n i t ) konsentrasi (ppm) u n g g u n 5 c m u n g g u n 1 0 c m u n g g u n 1 5 c m
Penentuan Konstanta Freundlich dan
Langmuir
Untuk melihat apakah adsorbsi ion ca mengikuti isoterm adsorbsi model Freundlich atau langmuir, maka dapat dibuktikan melalui koefisien determinasi (R2) yang ditunjukkan oleh grafik linierisasi kedua model tersebut. Konstanta Freundlich (Kf dan n) dapat dicari dengan menggunakan persamaan sebagai berikut:
Log q = log Kf + 1/n log C
Dengan menggambarkan grafik linieisasi antara log C vs log q, maka KF dan n
dapat ditentukan. Sedangkan konstanta Langmuir (KA dan qm) dapat dicari dengan
menggunakan persamaan dengan menggambarkan grafik linierisasi antara 1/C vs 1/q maka KA dan qm dapat diketahui.
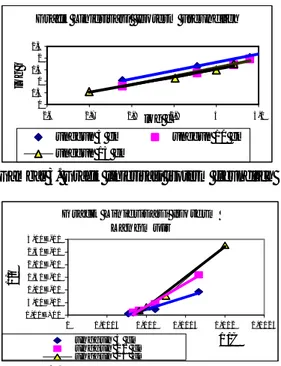
Gambar 3. Grafik linierisasi isoterm freundlich
Gambar 4. Grafik linierisasi isoterm Langmuir Dari gambar 3 dan 4 dapat dilihat bahwa pengujian data-data dengan menggunakan isoterm model Freundlich dan Langmuir menunjukkan grafik linierisasi yang baik untuk adsorbsi yang menggunakan zeolit. Hal ini ditunjukkan oleh nilai determinasi berkisar 0,98 - 0,99 (hampir mendekati 1). Nilai koefisien determinasi (R2) yang hampir sama dari setiap adsorben untuk ketiga jenis unggun menunjukkan bahwa adsorbsi mengikuti kedua model isoterm Freundlich dan Langmuir.
Tabel 2. Harga Konstanta Freundlich dan Langmuir
Tipe isoterm Parameter Unggun Unggun Unggun isoterm 5 cm 10 cm 15 cm Freundlich KF 1.339 2.479 3.417
n 0,287 0,268 0,300 Langmuir KA 7,62E-01 8,07E+00 8,7E-4
qm 134.408 68.027 47.509
KESIMPULAN
1. Zeolit alam Lampung dengan ukuran 20-30 mesh memiliki kemampuan yang besar dalam menyerap ion Ca2+.
2. Zeolit alam Lampung dengan variasi tinggi unggun 5 cm, 10 cm dan 15 cm memiliki kecenderungan yang berbeda-beda. Tinggi unggun 5 cm mampu menurunkan hingga 500 ppm, ketinggian 10 cm mampu menurunkan hingga 300 ppm,sedangkan ketinggian 15 cm mampu menurunkan hingga 200 ppm.
3. Zeolit dengan tinggi unggun 15 cm memiliki kecenderungan yang lebih baik pada awal reaksi dalam mengadsorbsi ion Ca2+ sampai 200 ppm. Hal ini disebabkan semakin tinggi unggun semakin luas zona adsorbsi.
4. Operasi dilaksanakan pada tekanan udara 1 atm dan suhu kamar (25oC). Pada kondisi ini terjadi pertukaran ion antara ion Na+ dari zeolit dengan ion Ca2+ dari air sadah (terbentuk ikatan kimia antara Na+ dan Cl-). 5. Adsorbsi isoterm ion Ca dapat mengikuti
kedua model adsorbsi isoterm baik model Freundlich maupun Langmuir.
Daftar Pustaka
1. Austin, George T.,Shreve’s Chemical
Process Industries, edisi kelima, Mc-Graw
Hill Book Company,1985.
2. Arfandy, Munsir, Teknik Penyediaan Air
Bersih untuk Daerah Pedesaan “Skala Prioritas Pemilihan Sumber Air”, Makalah
dalam Proceeding Kursus Penyediaan Air di Pedesaan, Bandung,1983.
3. Cheremisinoff, Paul N., Handbook of Water
and Wastwater Treatment Technology,
Marcel Decker Inc., New Yorl,1995. 4. Djannah, Pathul, Pengaruh Panas Terhadap
Ketahanan Zeolit Alam dan Pembuatan H-Zeolit dengan Larutan Amonium Asetat dan Grafik Linierisasi Isoterm Freundlich
0 0,5 1 1,5 2 2,5 2,6 2,7 2,8 log c2,9 3 3,1 log q unggun 5 cm unggun 10 cm unggun 15 cm G r a f i k L i n i e r i s a s i I s o t e r m L a n g m u ir 0 , 0 0 E + 0 0 5 , 0 0 E - 0 2 1 , 0 0 E - 0 1 1 , 5 0 E - 0 1 2 , 0 0 E - 0 1 2 , 5 0 E - 0 1 3 , 0 0 E - 0 1 0 0 , 0 0 0 5 0 , 0 0 1 0 , 0 0 1 5 0 , 0 0 2 0 , 0 0 2 5 1/C 1/q u n g g u n 5 c m u n g g u n 1 0 c m u n g g u n 1 5 c m
Amonium Hidroksida, Skripsi TGP
FTUI,1997.
5. Sundstrom, Donald W., et.al.,
Wastwater Treatment, Prentice Hall,
Englewood Clifts,1979.
6. Sutarti, Mursi et.al., Zeolit, Tinjauan
Literatur, Pusat Dokumentasi dan Informasi
LIPI,1994.
7. Yanti, Evi, Pengaruh Ukuran Zeolit dan
Konsentrasi awal Amonia terhadap Adsorbsi Amonia secara Batch oleh Zeolit Alam Lampung, Seminar TGP FTUI,1997
8. Yoediartini, Dessy, Studi Literatur Tentang
Modifikasi dan Karakterisasi Zeolit Alam Lampung untuk Aplikasi Adsorben, Seminar
TGP FTUI,1996.