SKRIPSI – TK141581
PENGARUH PELARUT TERHADAP
PEMBENTUKAN PARTIKEL KURKUMIN DARI
EKSTRAK TEMULAWAK DENGAN METODE
SUPERCRITICAL ANTI-SOLVENT (SAS)
Oleh :Anovia Dyah Riswardani NRP. 2313100037
Ahmad Kharis Nova A. NRP. 2313100061
Dosen Pembimbing
Dr. Siti Machmudah, S.T., M.Eng. NIP. 19730512 199903 2 001
Prof. Dr. Ir. Sugeng Winardi, M.Eng. NIP. 19520916 198003 1 002
DEPARTEMEN TEKNIK KIMIA FAKULTAS TEKNOLOGI INDUSTRI
INSTITUT TEKNOLOGI SEPULUH NOPEMBER SURABAYA
FINAL PROJECT – TK141581
THE EFFECT OF SOLVENT IN THE FORMATION
OF PARTICLE CURCUMIN FROM TEMULAWAK
EXTRACT USING SUPERCRITICAL
ANTI-SOLVENT (SAS) METHOD
By :
Anovia Dyah Riswardani NRP. 2313100037
Ahmad Kharis Nova A. NRP. 2313100061
Advisor
Dr. Siti Machmudah, S.T., M.Eng. NIP. 19730512 199903 2 001
Prof. Dr. Ir. Sugeng Winardi, M.Eng. NIP. 19520916 198003 1 002
DEPARTMENT OF CHEMICAL ENGINEERING FACULTY OF INDUSTRIAL ENGINEERING INSTITUT TEKNOLOGI SEPULUH NOPEMBER SURABAYA
i
PENGARUH PELARUT TERHADAP
PEMBENTUKAN PARTIKEL KURKUMIN
DARI EKSTRAK TEMULAWAK DENGAN
METODE SUPERCRITICAL ANTI-SOLVENT
(SAS)
Nama Mahasiswa : Anovia Dyah Riswardani (2313100037) Ahmad Kharis Nova A. (2313100061) Dosen Pembimbing : Dr. Siti Machmudah, S.T., M.Eng
Prof. Dr. Ir. Sugeng Winardi,M.Eng
ABSTRAK
Penelitian ini bertujuan untuk membentuk mikropartikel kurkumin dari ekstrak temulawak (curcuma xanthorrhiza) dengan menggunakan CO2 superkritis, mempelajari pengaruh pelarut,
suhu, tekanan, dan rasio laju alir CO2 terhadap laju alir larutan pada
pembentukan partikel kurkumin. Kurkumin adalah ekstrak dari akar Curcuma longa L yang tidak larut dalam air. Salah satu cara meningkatkan kelarutan kurkumin dalam air yaitu dengan memperkecil ukuran partikel. Saat ini sedang berkembang teknik mikropartikel yang menggunakan fluida superkritis yaitu SAS (Supercritical Anti-Solvent). Metode ini menggunakan CO2
superkritis sebagai anti-solvent.
Penelitian ini menggunakan rangkaian alat SAS
(supercritical Anti-Solvent) melewati inner tube dari concentric nozzle menggunakan HPLC pump. Pelarut yang digunakan berupa
aseton murni, aseton 95% volume + etanol 5% volume, dan aseton 90% volume + etanol 10% volume. Tekanan operasi yang digunakan 10 MPa dan 12 MPa dengan temperatur operasi 35oC
dan 40oC. Rasio laju alir CO
2 terhadap larutan divariasikan 15:0,25
ml/min dan 15:0,3 ml/min. Partikel yang terbentuk kemudian dianalisa dengan menggunakan SEM (Scanning Electron
Microscopy) untuk mengetahui morfologi partikel, FTIR (Fourier Transform Infrared Spectroscopy) untuk mengetahui gugus fungsi
ii
partikel dan UV-Vis Spectrophotometer untuk mengetahui
dissolution rate, kadar kurkumin dalam partikel yang terbentuk dan
kandungan aseton di dalam partikel yang terbentuk.
Partikel kurkimin menggunakan proses SAS yang terbentuk memiliki ukuran yang lebih kecil dibandingkan dengan kurkumin standar sebesar 7,96 ± 4,23 μm. Morfologi partikel kurkumin standar berbentuk batang dan partikel kurkumin yang melalui proses SAS berbentuk keping tidak beraturan. Diameter partikel yang dihasilkan dengan pelarut aseton murni sebesar 287,27 ± 218,45 nm berukuran lebih besar dibandingkan dengan diameter partikel yang dihasilkan dengan pelarut aseton + 5% etanol sebesar 200,98 ± 98,96 nm dan pelarut aseton + 10% etanol sebesar 261,95 ± 238,6 nm. Diameter partikel saat tekanan 12 MPa sebesar 145,56 ± 62,04 nm mempunyai ukuran lebih kecil dibandingkan saat tekanan 10 MPa sebesar 287,27 ± 218,45 nm. Saat temperatur operasi 35oC menghasilkan partikel dengan ukuran
diameter yang lebih kecil yaitu 287,27 ± 218,45 nm dibandingkan saat suhu operasi 40oC sebesar 506,88 ± 178,06 nm. Laju alir
larutan sebesar 0,25 ml/min menghasilkan ukuran diameter partikel lebih kecil sebesar 287,27 ± 218,45 nm dibandingkan saat laju alir larutan 0.3 ml/min sebesar 370.58 ± 220.13 nm. Partikel kurkumin yang dihasilkan melalui proses SAS memiliki gugus fungsi khas yang dimiliki oleh kurkumin yaitu C=O, C=C, C, C-O dan C-H. Kadar kurkumin tertinggi dihasilkan pada kondisi temperatur 35 oC, tekanan 10 MPa, rasio laju alir CO
2 terhadap laju
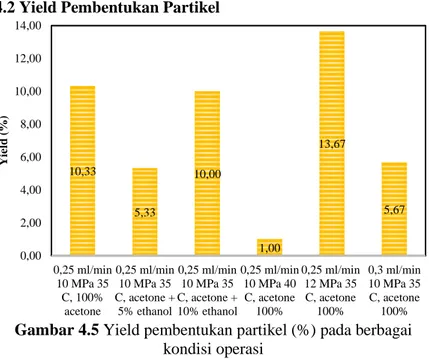
alir larutan ekstrak 15:0,25 ml/min dengan menggunakan aseton murni sebagai pelarut sebesar 3.7%. % yield terbesar dihasilkan pada kondisi operasi tekanan 12 MPa, suhu 35oC, laju alir larutan
ekstrak 0,25 ml/min dengan pelarut aseton murni yaitu sebesar 13,67%. Partikel kurkumin melalui proses SAS sudah tidak mengandung aseton hal ini dapat diketahui melalui uji UV-Vis
Spectrophotometer. Dengan proses SAS, laju disolusi partikel
lebih tinggi daripada yang tidak melalui proses SAS.
iii
THE EFFECT OF SOLVENT IN THE
FORMATION OF PARTICLE CURCUMIN
FROM TEMULAWAK EXTRACT USING
SUPERCRITICAL ANTI-SOLVENT (SAS)
METHOD
Name of Student : Anovia Dyah Riswardani (2313100037)
Ahmad Kharis Nova A. (2313100061)
Advisor : Dr. Siti Machmudah, S.T., M.Eng Prof. Dr. Ir. Sugeng Winardi, M.Eng
ABSTRACT
The aim of this research is to compose curcumin microparticle from temulawak extract (Curcuma xanthorrhiza) using supercritical CO2, to study the effects of solvents,
temperature, pressure, and supercritical CO2 to solution flowrate
ratio on the formation of curcumin particle. Curcumin is an extract from Curcuma longa L root that insoluble in water. One of method to increase solubility of curcumin in water is decrease particle size. Currently, microparticle methods using supercritical fluids is SAS (Supercritical Anti-Solvent). SAS (Supercritical Anti-Solvent) method is being chosen using supercritical CO2 as anti-solvent
because curcumin from temulawak extract slightly soluble in supercritical CO2.
This research uses SAS devices (supercritical Anti-Solvent) through the inner tube of concentric nozzle using HPLC pump. The solvent used is pure acetone, 95% acetone + 5% ethanol (v/v), and acetone 90% acetone + ethanol 10% (v/v). Pressure is being operated in 10 MPa and 12 MPa and in temperature 35oC and
40oC. Supercritical CO
2 to solution flowrate ratio is 15:0.25 ml/min
and 15:0.3 ml/min. The obtain particle will analyze with SEM (Scanning Electron Microscopy) to determine the particle morphology, FTIR (Fourier Transform Infrared Spectroscopy) to determine the functional groups of particles and UV-Vis
iv
Spectrophotometer to determine the dissolution rate, the content of
curcumin in the particle and the content of acetone in the particle. The curcumin particles using the SAS method have a smaller size than the standard curcumin is 7.96 ± 4.23 μm. The morphology of standard curcumin particles is rod-like crystal and curcumin particles through the SAS process is spherical and irregular. The diameter of particles formed by acetone solvent is 287.27 ± 218.45 nm is bigger than the diameter particle formed by aceton + 5% ethanol is 200.98 ± 98.96 nm and the diameter particle formed by aceton + 10% ethanol is 261.95 ± 238.6 nm. The diameter of particles when the pressure is 12 MPa is 145.56 ± 62.04 nm has a smaller size than when the pressure is 10 MPa is 287.27 ± 218.45 nm. The diameter of particles when the temperature of 35oC has smaller diameter size is 287.27 ± 218.45 nm compared to
temperature is 40oC is 506.88 ± 178.06 nm. The diameter of
particles when solution flow rate is 0.25 ml/min has smaller particle diameter sizes is 287.27 ± 218.45 nm compared to the solution flow rate 0.3 ml/min is 370.58 ± 220.13 nm. The curcumin particles produced by the SAS process have typical functional groups possessed by curcumin are C=O, C=C, C-C, C-O and C-H. The highest content of curcumin is at temperature of 35°C, pressure is 10 MPa, the ratio of the solution flow rate is 0.25 mL/min using pure acetone as the solvent is 3.7%. The largest % yield is produced at pressure is 12 MPa, 35°C, the ratio of the solution flow rate is 0.25 ml/min with pure acetone solvent is 13.67%. The curcumin particles formed through the SAS process isn’t contain acetone, where acetone is a carcinogenic organic solvent. The curcumin particles formed through the SAS process have a higher dissolution rate compared to the standard curcumin that isn’t through the SAS process.
v
KATA PENGANTAR
Puji dan syukur penulis haturkan kepada Tuhan Yang Maha Esa karena atas rahmat dan karunia-Nya, sehingga penulis dapat menyelesaikan Skripsi yang berjudul “Pengaruh Pelarut
Terhadap Pembentukan Partikel Kurkumin dari Ekstrak Temulawak dengan Metode Supercritical Anti-Solvent (SAS)”
dengan sebaik-baiknya sebagai salah satu tugas akhir di Teknik Kimia ITS Surabaya.
Skripsi ini merupakan salah satu syarat untuk memperoleh gelar sarjana di Teknik Kimia ITS. Namun demikian penulis berharap skripsi ini tidak hanya sebagai pemenuh kewajiban tetapi lebih dari itu akan bermanfaat khususnya bagi penulis sendiri dan juga bagi pembaca, terlebih pada bidang keteknikkimiaan dan aplikasinya dalam bidang industri.
Penulisan skripsi ini dapat diselesaikan tidak lepas dari dukungan, bimbingan, dan bantuan dari banyak pihak yang sangat berarti bagi penulis. Oleh karena itu, dalam kesempatan ini penulis menyampaikan ucapan terima kasih kepada:
1. Kedua orang tua serta saudara-saudara kami, atas doa, bimbingan, perhatian, serta kasih sayang yang selalu tercurah selama ini.
2. Bapak Prof. Dr. Ir. Sugeng Winardi, M.Eng selaku Dosen Pembimbing dan Kepala Laboratorium Mekanika Fluida dan Pencampuran, atas bimbingan dan motivasi yang telah diberikan.
3. Ibu Dr. Siti Machmudah, S.T., M.Eng. selaku Dosen Pembimbing kami selama mengerjakan skripsi kami di Laboratorium Mekanika Fluida dan Pencampuran, Departemen Teknik Kimia FTI-ITS, atas bimbingan, saran, dan motivasi yang diberikan.
4. Dr. Tantular Nurtono, S.T., M.Eng, Suci Madha Nia, S.T., M.T., dan Siti Zulaikah S.T. M.T Ph.D, selaku dosen penguji. 5. Seluruh dosen Teknik Kimia ITS atas semua ilmu serta
vi
6. Teman-teman kami di Laboratorium Mekanika Fluida dan Pencampuran yang telah berjuang bersama dalam menyelesaikan tugas akhir.
7. Teman-teman angkatan K-53 Teknik Kimia ITS yang selalu memberi semangat dan dukungan.
8. Bang Farid Indra, S.T selaku laboran Laboratorium Mekanika Fluida dan Pencampuran yang selalu membantu kami dalam mempersiapkan alat-alat dan melakukan percobaan.
9. Serta semua pihak lainnya yang tidak bisa disebutkan satu persatu yang telah membantu kami selama penulisan laporan.
Penulis menyadari bahwa skripsi ini masih terdapat kekurangan, oleh karena itu kritik dan saran yang bersifat membangun sangat diharapkan oleh penulis. Akhir kata kami selaku penulis memohon maaf apabila dalam penyusunan skripsi ini terdapat kesalahan. Semoga skripsi ini dapat bermanfaat bagi penulis dan pembaca.
Surabaya, 10 Juli 2017
Penulis
vii
DAFTAR ISI
HALAMAN JUDUL LEMBAR PENGESAHAN ABSTRAK ... i ABSTRACT ... iii KATA PENGANTAR ...vDAFTAR ISI ... vii
DAFTAR GAMBAR ... ix
DAFTAR TABEL ... xiii
BAB I PENDAHULUAN ...1
1.1 Latar Belakang ...1
1.2 Rumusan Masalah ...3
1.3 Tujuan ...3
1.4 Manfaat Penelitian ...3
BAB II TINJAUAN PUSTAKA ...5
2.1 Temulawak ...5
2.2 Kurkumin ...7
2.3 Metode Pemisahan dan Pemurnian Kurkumin ...9
2.4 Formulasi Mikropartikel ...13
2.4.1 Mikropartikel Fluida Superkritis ...14
2.4.1.1 RESS (Rapid Expansion of Supercritical Solution) ...15
2.4.1.2 PGSS (Particles From Gas Saturated Solutions) ...15
2.4.1.3 SAS (Supercritical Anti-Solvent) ...16
2.5 Fluida Superkritis ...16
2.5.1 Solubilitas ...18
2.5.2 Viskositas dan Difusifitas ...18
2.5.3 Densitas ...18
2.6 Karbon Dioksida Superkritis ...19
2.7 Penelitian Terdahulu ...20
BAB III METODOLOGI PENELITIAN ...23
3.1 Alat dan Bahan Penelitian ...23
viii
3.1.2 Alat Penelitian ...24
3.1.2.1 Alat yang digunakan untuk Tahap Ekstraksi ...25
3.1.2.2 Alat yang digunakan untuk Tahap Distilasi ...25
3.1.2.3 Alat yang digunakan untuk Tahap Presipitasi Partikel dengan Supercritical Anti-Solvent (SAS) ...25
3.2 Prosedur Percobaan ...27
3.2.1 Tahap Persiapan Bahan Baku ...27
3.2.2 Tahap Ekstraksi ...27
3.2.3 Tahap Distilasi ...27
3.2.4 Tahap Presipitasi Partikel ...28
3.2.5 Tahap Analisa ...28
3.2.5.1 SEM (Scanning Electron Microscopy) ..28
3.2.5.2 FTIR (Fourier Transform Infrared Spectroscopy) ...29
3.2.5.3 Uv-Vis Spectrophotometer ...29
BAB IV HASIL DAN PEMBAHASAN ...31
4.1 Kadar Kurkumin dalam Partikel ...31
4.2 Yield Pembentukan Partikel ...37
4.3 Kandungan Aceton dalam Partikel Kurkumin ...38
4.4 Dissolution Rate ...39
4.5 Morfologi Partikel ...44
4.6 Gugus Fungsi Partikel Kurkumin ...57
BAB V KESIMPULAN DAN SARAN ...61
5.1 Kesimpulan ...61
5.2 Saran ...61
DAFTAR PUSTAKA...xv
DAFTAR NOTASI ... xxiii
APENDIKS ...xxv BIODATA PENULIS
ix
DAFTAR GAMBAR
Gambar 2.1 Morfologi temulawak (a) tanaman (b) rimpang ..5
Gambar 2.2 Struktur Kurkumin ...9 Gambar 2.3 Viskositas CO2 pada Beberapa Temperatur
dan Tekanan ...20
Gambar 2.4 Difusivitas pada Beberapa Temperatur dan
Tekanan ...20
Gambar 3.1 Rangkaian alat Tahap Ekstraksi...24 Gambar 3.2 Rangkaian alat Tahap Distilasi ...25 Gambar 3.3 Rangkaian alat Supercritical Anti-Solvent
(SAS) ...26
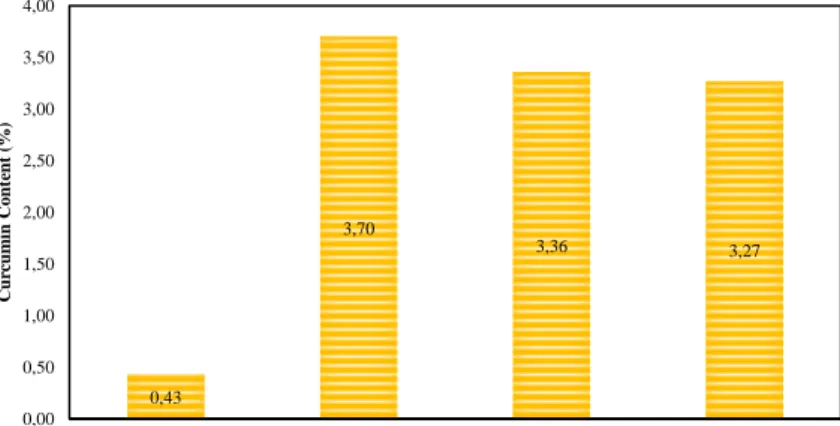
Gambar 4.1 Pengaruh Pelarut Terhadap Pembentukan
Partikel Kurkumin. ...33
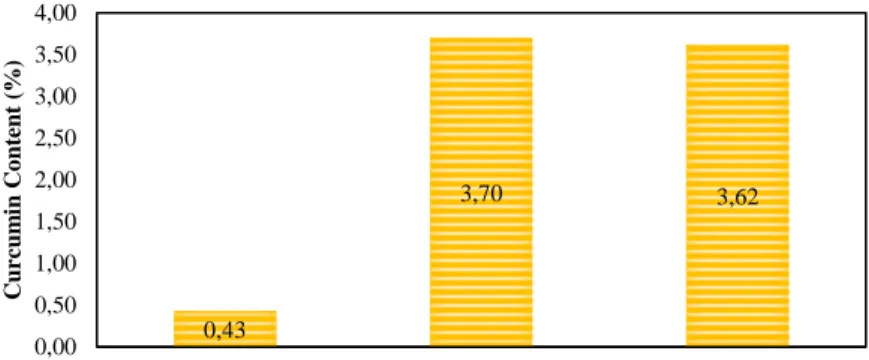
Gambar 4.2 Pengaruh Tekanan Terhadap Pembentukan
Partikel Kurkumin. ...34
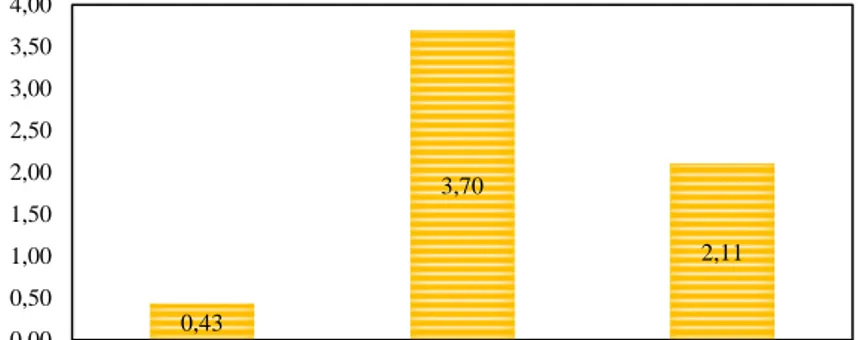
Gambar 4.3 Pengaruh Temperatur Terhadap Pembentukan
Partikel Kurkumin ...35
Gambar 4.4 Pengaruh Laju Alir Larutan Terhadap Kadar
Kurkumin dalam Partikel yang Terbentuk...36
Gambar 4.5 Yield Pembentukan Partikel (%) pada berbagai
kondisi operasi ...37
Gambar 4.6 Chromatogram spektrofotometer pelarut dan
partikel ...39
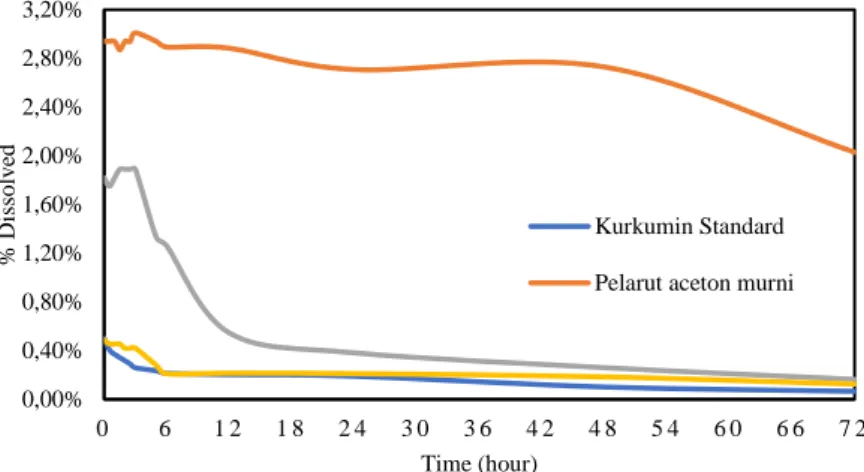
Gambar 4.7 Pengaruh Pelarut terhadap Dissolution Rate
pada Tekanan 10 MPa, Temperatur 35 oC dan
Laju Alir Larutan Ekstrak 0,25 ml/min ...40
Gambar 4.8 Pengaruh Tekanan terhadap Dissolution Rate
pada Temperatur 35 oC, Laju Alir Larutan
Ekstrak 0,25 ml/min dan pelarut aseton murni ..41
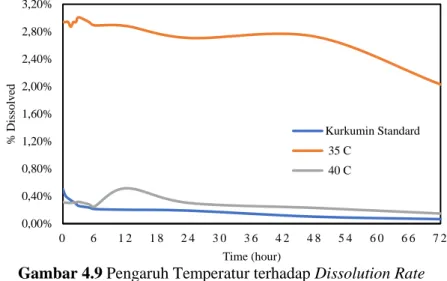
Gambar 4.9 Pengaruh Temperatur terhadap Dissolution Rate
pada Tekanan 10 MPa Laju Alir Larutan Ekstrak 0,25 ml/min dan pelarut aseton murni ...42
x
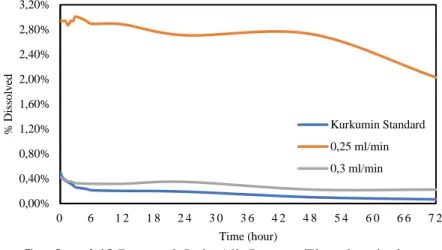
Gambar 4.10 Pengaruh Laju Alir Larutan Ekstrak terhadap
Dissolution Rate pada Tekanan 10 MPa
Temperatur 35 oC dan pelarut aseton murni ...43
Gambar 4.11 Citra SEM partikel standart kurkumin ...44 Gambar 4.12 Diagram distribusi ukuran partikel kurkumin ....44 Gambar 4.13 Citra SEM partikel kurkumin dengan pelarut
aseton murni (b), pelarut aseton 95% +etanol 5% (b), pelarut aseton 90% + etanol 10% (d) kondisi operasi temperatur 35oC, tekanan 10
MPa, laju alir larutan 0.25 ml/min
dibandingkan dengan kurkumin standart (a) ...45
Gambar 4.14 Diagram distribusi ukuran partikel kurkumin
dengan pelarut aseton murni, kondisi operasi temperatur 35oC, tekanan 10 MPa, laju alir
larutan 0.25 ml/mi ...46
Gambar 4.15 Diagram distribusi ukuran partikel kurkumin
dengan pelarut Aseton 95% + etanol 5%, temperatur 35oC, tekanan 10 MPa, laju alir
larutan 0.25 ml/min ...47
Gambar 4.16 Grafik distribusi ukuran partikel kurkumin
dengan pelarut aseton 90% + etanol 10%, temperatur 35oC, tekanan 10 MPa, laju alir
larutan 0.25 ml/min ...48
Gambar 4.17 Diameter partikel kurkumin yang terbentuk
pada temperatur 35oC, tekanan 10 MPa, laju
alir larutan 0.25 ml/min, dengan pelarut aseton murni, aseton 95% + etanol 5%, aseton 90% + etanol 10% ...49
Gambar 4.18 Citra SEM partikel kurkumin dengan pelarut
aseton murni dan kondisi operasi temperatur 35oC, laju alir larutan 0.25 ml/min, tekanan
10 (b) dan 12 MPa (c) dibandingkan dengan kurkumin standart (a) ...50
Gambar 4.19 Diagram distribusi ukuran partikel kurkumin
xi
temperatur 35oC, tekanan 12 MPa, laju alir
larutan 0.25 ml/min ...51
Gambar 4.20 Diameter partikel kurkumin dengan pelarut
aseton murni pada temperatur 35oC, laju alir
larutan 0.25 ml/min, dengan tekanan 10
dan 12 MPa ...52
Gambar 4.21 Citra SEM partikel kurkumin dengan pelarut
aseton murni dan kondisi operasi tekanan 10 MPa, laju alir larutan 0.25 ml/min, temperatur 35 (b) dan 40oC (c) dibandingkan dengan
kurkumin standart ...53
Gambar 4.22 Diagram distribusi ukuran partikel kurkumin
dengan pelarut aseton murni, kondisi operasi temperatur 40oC, tekanan 10 MPa, laju alir
larutan 0.25 ml/min ...54
Gambar 4.23 Diagram diameter partikel kurkumin yang
terbentuk dengan pelarut aseton murni pada tekanan 10 MPa, laju alir larutan 0.25 ml/min, temperatur 35oC dan 40oC dibandingkan
dengan partikel kurkumin standart ...54
Gambar 4.24 Citra SEM partikel kurkumin dengan pelarut
aseton murni dan kondisi operasi temperatur 35oC, tekanan 10 MPa, laju alir larutan
0.3 ml/min ...55
Gambar 4.25 Diagram distribusi ukuran partikel kurkumin
dengan pelarut aseton murni, kondisi operasi temperatur 35oC, tekanan 10 MPa, laju alir
larutan 0.3 ml/min ...56
Gambar 4.26 Diagram diameter partikel kurkumin yang
terbentuk dengan pelarut aseton murni pada temperatur 35oC, tekanan 10 MPa, laju
alir larutan 0,25 dan 0,3 ml/min...57
Gambar 4.27 Pengaruh Solvent terhadap hasil FTIR pada
Tekanan 10 MPa, Temperatur 35oC dan Laju
xii
Gambar 4.28 Pengaruh Tekanan terhadap Hasil FTIR pada
Temperatur 35 oC, Laju Alir Larutan Ekstrak
0,25 ml/min dan pelarut aseton murni ...59
Gambar 4.29 Pengaruh Temperatur terhadap hasil FTIR
pada Tekanan 10 MPa, Laju Alir Larutan
xiii
DAFTAR TABEL
Tabel 2.1 Komposisi Rimpang Temulawak ...7 Tabel 2.2 Properti Fisika dari Gas, Liquid, dan Fluida
Superkritis ...17
Tabel 2.3 Kondisi Kritis dari Beberapa Pelarut ...17 Tabel 4.1 Hasil Analisa Kadar Kurkumin ...32
xiv
1
BAB I
PENDAHULUAN
1.1 Latar Belakang
Indonesia merupakan negara tropis yang memiliki kekayaan alam yang melimpah. Salah satu diantaranya adalah keanekaragaman flora di Indonesia. Hampir segala jenis tumbuhan dapat tumbuh di wilayah negeri ini. Sebagian besar tumbuhan tersebut sudah dimanfaatkan oleh masyarakat dalam bidang kesehatan sebagai obat tradisional. (Triyono, 2013)
Tanaman temulawak (Curcuma xanthorrhiza Roxb), disebut juga sebagai Curcumajavanica (Devaraj dkk., 2010), merupakan tanaman asli Indonesia. Tumbuhan ini dijadikan sebagai biofarmaka andalan komoditas Indonesia, karena termasuk dalam kelompok lima besar tanaman obat yang berpotensial untuk dikembangkan. Temulawak dimanfaatkan sebagai pewarna alami pada pengolahan makanan serta sebagai salah satu bahan untuk pembuatan jamu tradisional. Temulawak dengan kandungan kurkumin yang tinggi juga dikenal sebagai anti-tumor, antioksidan, obat malaria dan juga dapat mencegah tertularnya HIV pada manusia. Dengan mengekstrak kukurmin dari temulawak tentu akan lebih baik dalam penggunaanya. (Ramdja dan Army, 2009)
Kurkumin dari temulawak dapat diambil dengan cara ekstraksi. Kurkumin merupakan hasil ekstrak dari akar Curcuma
longa L yang tidak larut dalam air, dan memiliki sifat sebagai
antioksidan, anti kanker, anti inflamasi, anti bakteri, anti malaria, antimiloid, dan anti parasit. Kurkumin memiliki kelarutan yang sangat kecil dalam air yaitu sekitar 0,0004 mg/L pada pH 7,3. Selain itu, kurkumin memiliki bioavailabilitas sangat rendah sehingga sangat sulit untuk berinteraksi dengan jaringan-jaringan tubuh karena darah mengandung 90% air. (Patra dan Sleem, 2013) Salah satu cara meningkatkan kelarutan kurkumin dalam air yaitu dengan memperkecil ukuran partikel. Metode pembentukan mikropartikel termasuk re-crystallization komponen terlarut dapat dilakukan menggunakan berbagai macam teknik
2
seperti crushing, milling, freeze drying, dan spray-drying. Saat ini, teknik mikropartikel dengan menggunakan fluida superkritis secara luas dipelajari karena teknik ini memerlukan suhu operasi yang tidak terlalu tinggi sehingga cocok untuk komponen yang sensitif terhadap suhu tinggi. Selain itu teknik ini juga menguntungkan dalam rekristalisasi beberapa material padat yang tidak mudah dihancurkan bila menggunakan metode crushing, milling, serta teknik drying lainnya. (Warlinda dan Sumarno, 2009).
Pembentukan mikropartikel menggunakan fluida superkritis yang telah banyak digunakan antara lain adalah SAS (Supercritical Anti-Solvent), RESS (Rapid Expansion Supercritical Solutions), PGSS (Particles from Gas-Saturated Solutions) dan SAA (Supercritical Assisted Atomization). Metode
RESS mempunyai syarat yaitu senyawa organik yang ada harus mempunyai kelarutan yang tinggi pada fluida superkritis. Metode PGSS menggunakan fluida superkritis sebagai solute, dimana fluida superkritis ini harus mempunyai kelarutan yang tinggi pada bahan organik. Kedua metode ini mempunyai kelemahan yang hampir sama yaitu baik fluida superkritis maupun bahan organik harus mempunyai tingkat kelarutan yang tinggi. Pada penelitian ini menggunakan fluida superkritis sebagai anti-solvent. Senyawa organik dilarutkan terlebih dahulu ke dalam pelarut organik kemudian dikontakkan dengan fluida superkritis untuk menghasilkan partikel microsphere. Pelarut organik yang digunakan misalnya berupa etanol dan aceton. Fluida super kritis akan melarutkan solvent, sehingga terjadi pemisahan antara solvent dengan senyawa organik. Kelebihan metode ini adalah fluida superkritis digunakan sebagai anti-solvent, sehingga cocok untuk bahan-bahan organik yang tidak mudah larut pada fluida superkritis (Mira dkk., 2010). Sehingga, dalam penelitian ini, metode yang dipilih adalah metode SAS. Pada penelitian ini CO2
superkritis digunakan sebagai anti-solvent karena kurkumin dari ekstrak temulawak sedikit larut dalam CO2 superkritis.
3
1.2 Rumusan Masalah
Masalah umum yang terjadi diindustri farmasi antara lain banyaknya obat-obatan yang memiliki kelarutan yang relatif rendah dalam air contohnya senyawa kurkumin dari ekstrak temulawak. Beberapa teknologi mikronisasi yang telah diaplikasikan secara luas di dunia farmasi antara lain spray drying dan milling. Teknologi-teknologi seperti ini cukup sederhana secara konsep, tetapi dalam prakteknya memerlukan konsumsi energi yang besar dan pada proses mekanis menghasilkan distribusi ukuran partikel yang luas. Pada penelitian ini memberikan alternatif untuk membentuk mikropartikel kurkumin dari ekstrak temulawak (curcuma xanthorrhiza) dengan menggunakan CO2 superkritis dan untuk mengetahui pengaruh
kondisi operasi seperti jenis pelarut, temperatur, tekanan dan rasio laju alir CO2 terhadap laju alir larutan pada pembentukan partikel
kurkumin.
1.3 Tujuan Penelitian
Tujuan penelitian ini adalah untuk:
1. Membentuk mikropartikel kurkumin dari ekstrak temulawak (curcuma xanthorrhiza) dengan menggunakan CO2 superkritis.
2. Mempelajari pengaruh pelarut, temperatur, tekanan, dan rasio laju alir CO2 terhadap laju alir larutan pada
pembentukan partikel kurkumin.
1.4 Manfaat Penelitian
Manfaat yang diharapkan dari penelitian ini adalah: 1. Mendapatkan mikropartikel kurkumin dari ekstrak
temulawak (curcuma xanthorrhiza) dengan menggunakan CO2 superkritis sehingga mudah terlarut dalam tubuh.
2. Memberikan informasi mengenai faktor-faktor pembentukan mikropartikel kurkumin dari ekstrak temulawak menggunakan CO2 superkritis.
4
5
BAB II
TINJAUAN PUSTAKA
2.1 Temulawak
Temulawak termasuk tanaman tahunan yang tumbuh merumpun hingga mencapai ketinggian 2 – 2,5 meter dengan tiap anakan di setiap rumpunnya memiliki 2-9 helai daun. Daun temulawak memiliki panjang sekitar 50 – 55 cm dan lebar ± 18 cm. Warna bunga umumnya kuning dengan kelopak bunga kuning tua dan pangkal bunganya berwarna ungu. Rimpang temulawak bentuknya bulat seperti telur dengan warna kulit rimpang sewaktu masih muda maupun tua adalah kuning kotor (Nugraha dkk, 2008). Warna daging rimpang adalah kuning dengan cita rasa pahit, berbau tajam dan keharumannya sedang. Morfologi tanaman ditunjukkan oleh Gambar 2.1. Tanaman ini dapat tumbuh dengan baik pada dataran rendah sampai ketinggian 1500 meter di atas permukaan laut dan di daerah dengan berhabitat hutan tropis (Ahmad Said, 2006).
(a) (b)
6
Klasifikasi tumbuhan temulawak ditunjukkan sebagai berikut (Wahyuni dkk, 2004 dan Rezki dkk, 2015):
Divisi : Spermatophyta Sub divisi : Angiospermae Kelas : Monocotyledonae Ordo : Zingiberales Keluarga : Zingiberaceae Genus : Curcuma
Spesies : Curcuma xanthorrhiza ROXB
Temulawak (Curcuma xanthorrhiza) adalah tumbuhan obat yang tergolong dalam suku temu-temuan (Zingiberaceae) dan tersebar di beberapa wilayah Indonesia (Prana, 2008). Data statistik Kementerian Pertanian Indonesia juga menunjukkan bahwa temulawak menyumbangkan hasil 21 juta kg pada produksi Biofarmaka di tahun 2016. Eksistensi temulawak sebagai tumbuhan obat juga dibuktikan dengan adanya 50 resep lebih obat tradisional menggunakan temulawak (Hwang dkk, 2000). Temulawak memiliki banyak khasiat diantaranya adalah memelihara kesehatan, mengobati berbagai macam penyakit antara lain gangguan pada hati, sembelit, diare, disentri, gangguan lambung, wasir, gangguan kulit, serta sebagai sediaan fitoterapi yang kegunaannya dapat dipertanggung jawabkan. Beberapa penelitian melaporkan bahwa temulawak memiliki efek farmakologis antara lain antialergi (Matsuda dkk, 2004), antidemensia (Lim dkk, 2001), antiinflamasi (Banerjee dkk, 2003), dan antikanker (Piantino dkk, 2009; Li dkk, 2013). Aktivitas inflamasi merupakan komponen penting dari pencegahan perkembangan tumor yang ada pada manusia (Riki, 2015). Hal tersebut dikarenakan banyak kanker muncul dari daerah inflamasi, iritasi kronis dan infeksi (Basnet dan Basnet, 2012). WHO (1999) dalam Jayaprakasha dkk (2006) juga menjelaskan bahwa bagian akar (rimpang) temulawak secara empiris berpotensi sebagai antioksidan untuk menangkal adanya radikal bebas penyebab kanker yang sangat berbahaya bagi kesehatan manusia. Komponen bioaktif yang bertanggung jawab sebagai antioksidan dalam
7
rimpang temulawak adalah kurkumin, demetoksikurkumin dan bisdemetoksikurkumin (Cahyono dkk, 2011). Komponen bioaktif lain pada rimpang temulawak ditunjukkan pada Tabel 2.1 di bawah ini.
Tabel 2.1 Komposisi Rimpang Temulawak
Komponen Komposisi (%) Pati 27,62 Lemak 5,38 Minyak Atsiri 10,96 Kurkumin 1,93 Protein 6,44 Serat Kasar 6,89 Sumber: Srijanto dkk, 2004 2.2 Kurkumin
Kurkumin (diferuloylmethane), atau [1,7-bis(4-hydroxy-3-methoxyfenil)-1,6-heptadiene-3,5-dione], adalah senyawa aktif polifenol dengan rumus kimia C21H20O6 dan memiliki dua bentuk
tautomer (keton dan enol) (Zaibunnisa dkk, 2009). Struktur keton lebih dominan dalam bentuk padat sedangkan struktur enol ditemukan dalam bentuk cairan.. Senyawa turunan kurkumin disebut kurkuminoid dengan dua macam yaitu desmetoksikurkumin dan bis-desmetoksikurkumin (Cahyono dkk, 2011). Dalam keadaan in vivo, kurkumin akan berubah menjadi senyawa metabolit berupa dihidrokurkumin atau tetrahidrokurkumin sebelum kemudian dikonversi menjadi senyawa konjugasi monoglusuronida. Kurkumin selain digunakan sebagai antitumor dan antioksidan juga memiliki kegunaan dalam bidang medis (Fujiwara dkk, 2008) yakni:
a.
Melindungi saraf, mengurangi risiko radang otak vasospasma dan mengembalikan homeostasis energi pada sistem otak yang terganggu akibat terluka atau trauma.8
b.
Menghambat dan mengurangi penumpukan plak amiloid-beta pada penderita Alzheimer.c.
Melindungi hati dari hemangioendotelioma, hepatokarsinoma, Hepatitis B.d.
Melindungi pankreas dari akibat rasio sitokina yang berlebihan, bahkan setelah transplantasi, serta menurunkan resistansi terhadap insulin dan leptin. Kurkumin memiliki sifat kimia dan sifat fisik tertentu. Sifat kimia kurkumin terlihat dari perubahan warna yang bergantung pada perubahan pH lingkungan. Kurkumin berubah menjadi kuning atau kuning jingga pada suasana asam dan berubah menjadi merah dalam suasana basa. Keadaaan basa yakni di pH 8,5-10,0 dalam waktu yang relatif lama akan membuat kurkumin mengalami proses disosiasi membentuk asam ferulat dan feruloilmetan yang menghasilkan warna kuning coklat. Kurkumin juga stabil pada cahaya karena adanya gugus metilen aktif (-CH2-)diantara dua gugus keton pada senyawa tersebut. Kurkumin mempunyai aroma yang khas dan tidak bersifat toksik apabila dikonsumsi oleh manusia dalam jumlah normal yakni maksimal 100 mg/hari (Stankovic, 2004). Sifat fisika yang dimiliki kurkumin menurut the merck Index (1976) dalam Wahyuni dkk (2004) adalah berat molekulnya sebesar 368,37 gram/mol, titik leleh sebesar 183oC, tidak larut dalam air, namun larut dalam alkohol
dan asam asetat glasial.
Beberapa penelitian telah dilakukan untuk mengetahui aktivitas antioksidan lebih mendalam pada kurkumin dari temulawak. Pada penelitian Toda dkk (1985) dijelaskan bahwa aktivitas antioksidan komponen kurkuminoid sebagai turunan kurkumin masing-masing 20,9 dan 8 kali lebih tinggi apabila dibandingkan dengan senyawa tokoferol yang diuji dengan oksigen aktif termodifikasi. Tokoferol sebagai pembanding digunakan karena menurut Shahidi (1999) senyawa tersebut dapat disebut juga vitamin E yang merupakan antioksidan yang larut dalam lipid dan penangkap radikal peroksil. Tingginya aktivitas antioksidan kurkumin ini tidak lepas dari struktur senyawa kurkumin.
9
Kurkumin mempunyai gugus penting dalam proses antioksidan tersebut. Struktur kurkumin terdiri dari gugus hidroksi fenolik dan gugus β diketon. Gugus hidroksi fenolik berfungsi sebagai penangkap radikal bebas pada fase pertama mekanisme antioksidatif. Pada struktur senyawa kurkumin terdapat 2 gugus fenolik, sehingga 1 molekul kurkumin dapat menangkal 2 radikal bebas. Gugus β diketon berfungsi sebagai penangkap radikal pada fase berikutnya. Struktur turunan kurkumin dijelaskan lebih lanjut pada Gambar 2.2 (Popuri, 2013 dalam Rezki dkk, 2015).
Gambar 2.2 Struktur Kurkumin
2.3 Metode Pemisahan dan Pemurnian Kurkumin
Di Indonesia, bahan baku kurkuminoid dari rimpang temulawak dimanfaatkan oleh industri obat dalam bentuk ekstrak segar atau dalam bentuk simplisia. Penyimpanan simplisia dalam bentuk kering sangat dibutuhkan masyarakat guna mengatasi kendala over suplay pada saat musim panen. Secara tradisional,
10
bahan ini diproduksi melalui tahapan perajangan dengan pisau atau mesin, diikuti dengan pengeringan di bawah sinar matahari dan pengemasan. Sekelompok kecil masyarakat telah menggunakan oven sebagai alat pengering (Cahyono, 2011). Pengeringan ini dinilai kurang praktis dan dapat menurunkan kandungan kurkumin yang ingin diperoleh. Oleh karena itu, metode ekstraksi menawarkan solusi lebih baik daripada simplisia dan Riki (2015) juga menjelaskan bahwa gabungan beberapa komponen bioaktif dapat memberikan efek sinergis sehingga meningkatkan aktivitas antikanker dan antioksidan dari kurkumnoid.
Definisi umum ekstraksi yaitu proses pemisahan dan isolasi zat dari suatu zat dengan penambahan pelarut tertentu untuk mengeluarkan komponen campuran dari zat padat atau zat cair. Dalam hal ini fraksi padat yang diinginkan bersifat larut dalam pelarut (solvent), sedangkan fraksi padat lainnya tidak dapat larut. Komponen yang dipindahkan dari zat padat ke dalam pelarut disebut “solute” sedangkan padatan yang tidak terlarut dalam pelarut disebut “inert” (Susiana dkk, 2009). Pada umumnya proses ekstraksi dilakukan dengan beberapa metode, diantaranya operasi satu tahap (single stage) dan operasi multi tahap (multi stage). Proses ekstraksi tersebut akan menjadi sempurna jika dilakukan permurnian dan pemisahan solut dari pelarutnya, misalnya dengan cara distilasi/penguapan (Anggoro dkk, 2015).
Berdasarkan teknik yang digunakan, ekstraksi terbagi menjadi 3 yakni metode maserasi, sokletasi, dan perkolasi yang dijelaskan sebagai berikut:
(a) Metode maserasi, yaitu suatu teknik ekstraksi dengan cara perendaman bahan yang sudah halus pada temperatur kamar dengan pelarut yang sesuai supaya zat-zat dapat larut secara sempurna. Proses ini memiliki keuntungan dalam isolasi senyawa bahan alam karena melalui perendaman akan terjadi pemecahan dinding dan membran sel akibat perbedaan tekanan antara di dalam dan di luar sel sehingga metabolit sekunder yang ada dalam sitoplasma akan terlarut dalam pelarut
11
organik dan ekstraksi senyawa akan sempurna karena dapat diatur lama perendaman yang dilakukan. Pemilihan pelarut untuk proses maserasi akan memberikan efektifitas yang tinggi dengan memperhatikan kelarutan senyawa bahan alam dalam pelarut tersebut (Heinrich dkk, 2004).
(b) Metode sokletasi, yaitu teknik ekstraksi dengan menggunakan alat soklet. Pelarut pada labu alas bulat diuapkan dan mengalami kondensasi setelah sampai di kondensor, selanjutnya bersama ekstrak turun kembali ke dalam labu bundar. Proses ini berlangsung secara kontinu dan berulang-ulang. Keuntungan dari metode ini adalah dapat menghemat penggunaan pelarut sebab terjadi sirkulasi pelarut yang selalu membasahi sampel. Metode ini sangat baik untuk senyawa yang tidak terpengaruh oleh panas (Darwis, 2000; Pavia dkk, 1990).
(c) Metode perkolasi yaitu metode ekstraksi dengan bahan yang sudah halus diekstraksi dalam pelarut yang sesuai dengan cara pelarut secara perlahan-lahan dialirkan ke dalam suatu kolom yang berisi sampel sehingga diperlukan pelarut yang lebih banyak. Pelarut yang digunakan tidak mudah menguap dan dapat melarutkan senyawa kimia yang akan diisolasi dengan baik. Alat yang digunakan untuk perkolasi dinamakan perkolator yang terdiri dari bejana dilengkapi kran untuk mengeluarkan pelarut pada bagian bawahnya. Tetapi efektifitas dari proses ini hanya akan lebih besar untuk senyawa organik yang sangat mudah larut dalam pelarut yang digunakan (Pavia dkk, 1990).
Proses ekstraksi dilakukan sampai seluruh senyawa metabolit habis terekstrak, pengamatan sederhana dilihat dari warna pelarut, bila pelarut sudah tidak berwarna biasanya metabolit sudah terekstrak (Hismiaty dkk, 2011 dan Istiqomah, 2013). Pemilihan pelarut organik juga menjadi aspek penting
12
dalam proses ekstraksi. Menurut Jayaprakasha dkk (2005), kurkuminoid dapat diekstraksi menggunakan pelarut yang sesuai dengan polaritas senyawa. Beberapa jenis pelarut organik yang dapat digunakan adalah heksan, aseton, etil asetat, dan metanol. Spiro dkk. (1990) juga menjelaskan bahwa kecepatan ekstraksi [6]-gingerol menggunakan pelarut organik menurun dengan urutan aseton > aseton + air > diklorometan > etanol> isopropanol. Sedangkan penelitian lain, Zahro dkk (2008) dalam Nugraha (2010), menggunakan pelarut etanol 96% dengan perbandingan bahan:pelarut sebesar 1:5 (b/v). Etanol merupakan pelarut yang sesuai untuk melarutkan senyawa organik yang memiliki polaritas medium dan sifat mudah menguap. Indeks polaritas etanol yang sebesar 5,2 lebih kecil dibandingkan air yang sebesar 7,7 sehingga cocok untuk mengekstrak antioksidan alami dalam sari temulawak. Pemisahan kurkumin dari pelarut etanol dapat dilakukan dengan proses distilasi atau penyulingan merupakan proses pemisahan komponen yang berupa cairan atau padatan dari 2 macam campuran atau lebih berdasarkan perbedaan titik didihnya. Campuran distilasi juga harus memiliki perbedaan titik didik yang cukup, sifat penguapan yang relatif tinggi dan tidak membentuk campuran azeotrop. Proses pemisahan secara distillasi terdiri dari tiga langkah dasar yaitu proses penguapan atau penambahan panas dalam larutan yang dipisahkan, proses pembentukan fase seimbang dan proses pemisahan kedua fase seimbang serta terbagi menjadi 3 metode (Gorak dan Sorensen, 2014):
a. Penyulingan dengan air (water distillation)
Pada sistem penyulingan dengan air, bahan yang akan disuling langsung kontak dengan air mendidih. Sistem ini sangat baik digunakan untuk menyuling bahan yang berbentuk tepung dan minyak yang mudah membentuk gumpalan jika terkena panas. Sistem ini bekerja kurang baik apabila digunakan untuk bahan fraksi sabun, bahan yang larut dalam air. Kelemahan lainnya adalah apabila suhu penyulingan bahan tidak diawasi maka bahan tersebut dapat hangus.
13
b. Penyulingan dengan air dan uap (water and steam
distillation)
Pada sistem penyulingan ini, bahan diletakkan di atas piring yang berupa ayakan yang terletak beberapa sentimeter di atas permukaan air dalam ketel penyuling. Keuntungan dengan menggunakan sistem penyulingan ini adalah meratanya uap yang berpenetrasi ke dalam jaringan bahan. Selain itu, hasil rendemen menggunakan distilasi campuran air dan uap ini biasanya lebih baik dari hasil rendemen yang menggunakan distilasi air. c. Penyulingan dengan uap (steam distillation)
Pada sistem ini, air sebagai sumber uap panas terdapat dalam “boiler” yang letaknya terpisah dari ketel penyulingan. Uap yang dihasilkan mempunyai tekanan lebih tinggi dari tekanan udara luar. Penyulingan dengan uap sebaiknya dimulai dengan tekanan uap yang rendah (± 1 atm), kemudian secara perlahan tekanan uap dinaikkan menjadi kurang lebih sebesar 3 atm. Jika permulaan penyulingan dilakukan pada tekanan tinggi, maka komponen kimia dalam bahan akan mengalami
dekomposisi. Kelebihan distilasi uap adalah komponen
senyawa yang dimurnikan tidak dikhawatirkan rusak karena uap dipanaskan sebelum mendekati titik didihnya dan tanpa pemanasan berlebih.
2.4 Formulasi Mikropartikel
Hasil ekstraksi kurkumin memiliki keterbatasan dalam hal aplikasi klinis karena kurkuminoid sulit larut dalam air dan sistem bioavailabilitasnya yang rendah. Penggabungan kurkuminoid dengan makromolekul, formulasi nano, formulasi mikropartikel, siklodekstrin, liposom dan hidrogel telah terbukti meningkatkan kelarutannya dalam air, dengan demikian meningkatkan waktu sirkulasi dan bioavailabilitasnya (Dhule et al. 2012). Salah satu cara yang telah dikembangkan adalah menggabungkan kurkuminoid ke dalam sistem nanopartikel dan mikropartikel
14
dengan controlled particle size (PS) dan particle size distribution
(PSD). Mujib (2011) melakukan penelitian nanoemulsi
kurkuminoid temulawak tersalut lemak padat yang memperoleh nanoemulsi dengan ukuran 199.03 ± 67.62 nm dan efisiensi penjerapan kurkuminoid sebesar 77.65%. Namun, nanoemulsi tidak stabil dalam waktu penyimpanan yang cukup lama (Shah et
al. 2014), sehingga perlu dibuat sediaan dalam metode lain dengan
seperti metode fluida superkritis yang dikembangkan dalam usaha memanfaatkan kekuatan difusivitas solven yang tinggi (Wang dkk, 2000). Mikronisasi dengan berdasar pada pemanfaatan properti gas bertekanan tinggi, seperti fluida superkritis akan menguntungkan dalam rekristalisasi beberapa material padat yang tidak mudah dihancurkan dan tidak tahan temperatur tinggi. Upaya microsphere tersebut telah digunakan dalam berbagai industri makanan, farmasi, catalyst supports, dan adsorbents (Kurniawansyah dan Sumarno, 2008).
Beberapa teknologi mikronisasi yang telah diaplikasikan secara luas di dunia farmasi antara lain spray drying dan milling. Teknologi-teknologi seperti ini cukup sederhana secara konsep, tetapi dalam prakteknya memerlukan konsumsi energi yang besar dan pada proses mekanis menghasilkan distribusi ukuran partikel yang luas (Kurniawansyah, 2008). Akan tetapi, teknologi ini lebih baik jika dibandingkan dengan teknologi konvensional pembuatan komposit obat-polimer yang biasanya dilakukan dengan presipitasi larutan organik menjadi bentuk solid (Pasquali dan Bettini, 2008). Penggunaan larutan organik dan temperatur operasi yang tinggi (dalam proses spray drying) tidak diinginkan karena akan mempengaruhi kinerja obat (Davies dkk., 2008). Kekurangan lain dari proses konvensional meliputi perlunya proses tambahan untuk mengekstraksi sisa solvent (kelebihan solvent organik) yang berbahaya untuk kesehatan dan lingkungan (Tandya dkk., 2007).
2.4.1 Mikropartikel Fluida Superkritis
Berdasarkan fungsinya, perkembangan teknologi fluida superkritis dapat dibedakan menjadi tiga, yaitu sebagai solvent,
15
solute dan antisolvent bagi material padat. Bila fluida superkritis
digunakan sebagai solvent, maka saat larutan disemburkan melalui
nozzle, fluida superkritis akan terpisahkan langsung dengan microsphere yang terbentuk, karena kelarutannya berkurang.
Sedangkan bila sebagai antisolvent, fluida superkritis akan saling melarut dengan solvent menyebabkan penurunan daya larut dan menguap bersama meninggalkan mikropartikel (microsphere) yang terbentuk (Jung dan Perrut, 2001). Beberapa metode teknologi fluida superkritis yang telah dikembangkan antara lain
Rapid Expansion of Supercritical Solutions (RESS), Gas anti Solvent (GAS), Supercritical Anti Solvent process (SAS), Solution Enhanced Dispersion by Supercritical Fluids (SEDS), dan Particle from Gas saturated Solutions (PGSS).
2.4.1.1 RESS (Rapid Expansion of Supercritical Solution)
Teknik RESS (Rapid Expansion of Supercritical Solution) adalah teknik yang pertama kali dikembangkan dengan karbondioksida superkritis sebagai solvent bagi polipropilen, menghasilkan microsphere berukuran 1-5 μm. Pada teknik ini, larutan polimer dijenuhkan dengan fluida superkritis, kemudian larutan polimer diekspansikan (melalui nozzle yang dipanasi) ke dalam vessel bertekanan rendah. Kondisi ini menyebabkan partikel polimer ternukleasi sangat cepat dan membentuk microsphere. Teknik ini mempunyai kelemahan karena kebanyakan polimer mempunyai kelarutan yang kecil ke dalam fluida superkritis. RESS banyak dikembangkan dalam pembuatan microsphere bahan organik (Jung dan Perrut, 2001).
2.4.1.2 PGSS (Particle from Gas saturated Solutions)
Teknik Particles From Gas Saturated Solution/Suspensions (PGSS) adalah teknik yang menggunakan
fluida superkritis sebagai solute. Fluida superkritis yang digunakan harus mempunyai kelarutan yang tinggi dalam suspensi polimer, dimana kelarutannya tergantung dari suhu dan tekanan. Larutan tersebut diekspansikan ke dalam vessel (melalui nozzle) sehingga
16
larutan berubah menjadi supersaturasi, dan microsphere akan terbentuk (Rantakyla, 2004).
2.4.1.3 SAS (Supercritical Anti-Solvent)
Metode fluida superkritis yang banyak dikembangkan saat ini yaitu berdasarkan proses Supercritical Anti Solvent (SAS) menggunakan CO2 superkritis sebagai anti-solvent dan telah
diaplikasikan pada beberapa komponen misalnya bubuk micron bahan-bahan farmasi, polimer dan biopolimer, superkonduktor dan katalis, zat pewarna dan bahan peledak. Proses Supercritical Anti
Solvent (SAS) diaplikasikan pada industri farmasi karena mudah
dalam pemisahan dan recovery solvent dan anti-solvent sehingga menghasilkan produk dengan kemurnian tinggi. Pada polimer, penggunaan CO2 superkritis sebagai anti-solvent dimaksudkan
untuk menurunkan daya larut solven dalam larutan polimer sehingga polimer dapat terkristalkan kembali (Lee dkk., 2008).
Teknik SAS (Supercritical Anti-solvent) adalah teknik yang menggunakan fluida superkritis sebagai anti-solvent. Sampai kini teknik ini berkembang menjadi beberapa teknik, antara lain
Precipitated With a Compressed Fluid Anti-solvent (PCA), Gas Anti-Solvent (GAS), Aerosol Solvent Extraction System (ASES),
dan Solution Enhanced Dispersion by Supercritical Fluids (SEDS). Pada keempat teknik ini, polimer dilarutkan terlebih dahulu ke dalam pelarut organik kemudian dikontakkan dengan fluida superkritis untuk menghasilkan microsphere (Yeo dan Kiran, 2005).
2.5 Fluida Superkritis
Kondisi fluida superkritis terbentuk apabila kondisi fluida berada diatas temperatur dan tekanan kritisnya. Tidak seperti gas, fluida superkritis tidak dapat dikondensasikan menjadi keadaan liquid-gas dengan pengaturan tekanan. Hal ini dapat digunakan untuk mengontrol solubilitas dari pelarut. Fluida superkritis dikarakterisasikan dengan densitas tinggi, viskositas rendah, dan
17
difusivitas menengah antara gas dan cairan. Properti yang tidak biasa ini, justru menjadikan fluida superkritis sebagai pelarut yang ideal dan potensial. Berikut ini merupakan keuntungan dari fluida superkritis:
a. Koefisien difusi tinggi dan viskositas rendah dibandingkan dengan liquid
b. Recovery solvent cepat dengan minimal residu dalam
produk c. Tidak beracun
d. Tidak menghasilkan kebakaran
e. Secara komersial mudah di dapat dalam kemurnian tinggi
f. Kompatibel dengan kondisi lingkungan karena tidak menghasilkan limbah
Tabel 2.2 Properti Fisika dari Gas Liquid, dan Fluida Superkritis Physical State Density (gr/ml) Viscosity (g/cm.s) Diffusivity (cm2/s) Gas 10-3 10-4 10-1 Liquid 1 10-2 10-6 Sumber: Dvoyashkin, 2010
Tabel 2.3 Kondisi Kritis dari Beberapa Pelarut
Compounds Tc (oC) Pc (atm) Density (g/ml)
CO2 31.3 72.9 0.448 Ammonia 132.4 112.5 0.235 Water 374.15 218.3 0.315 Nitrous Oxide 36.5 71.7 0.45 Methane -82.1 45.8 0.2 Ethane 32.28 48.1 0.203 Ethylene 9.21 49.7 0.218 Methanol 240.5 78.9 0.272 Sumber: Dvoyashkin, 2010
18
2.5.1 Solubilitas (Kelarutan)
Solubilitas gas dalam suatu solvent biasanya menurun dengan kenaikan temperatur. Namun pada temperatur tinggi, mendekati temperatur kritis dari solvent solubilitas dari gas umumnya naik sebanding dengan temperatur (Arie, 2014). Umumnya solubilitas dinyatakan dalam satuan fraksi mol atau konstanta Henry. Kelarutan solute dalam solvent dipengaruhi oleh dua hal yaitu jarak antara molekul yang memungkinkan terjadinya interaksi antara molekul tersebut dan gaya intermolekul antara
solvent-solvent, solute-solvent, dan solute-solute. 2.5.2 Viskositas dan Difusifitas
Pada keadaan superkritis, gaya interaksi antarmolekul relatif rendah. Hal ini menyebabkan tingginya mobilitas dari molekul dan menyebabkan viskositas dari superkritis menjadi rendah bila dibandingkan dengan solvent liquid. Pada temperatur dibawah minimum, fluida superkritis berkelakuan seperti liquid yaitu viskositas menurun seiring dengan kenaikan temperatur. Pada temperatur diatas minimum, fluida superkritis berkelakuan seperti gas yaitu viskositas meningkat seiring dengan kenaikan temperatur (Grandison, 1996). Seperti halnya densitas, nilai viskositas dan difusivitas tergantung pada temperatur dan tekanan. Viskositas dan difusivitas dari fluida superkritis mendekati gas selama tekanan dinaikkan. Kenaikan temperatur berpengaruh pada kenaikan viskositas gas, namun pada fluida superkritis hal ini menjadi kebalikan. Difusivitas akan meningkatkan seiring dengan kenaikan temperatur. Rendahnya viskositas dan tingginya difusivitas akan memudahkan pelarut untuk melakukan penetrasi ke bahan yang akan diekstrak (Taylor, 1996).
2.5.3 Densitas
Kemampuan pelarut untuk melarutkan zat terlarut dinyatakan dengan jumlah pelarut per satuan volume. Ini disebabkan karena energi pelarutan ditentukan oleh jumlah
19
interaksi pelarut dengan solute yang terjadi dimana densitas merupakan kunci parameter yang ditentukan oleh pengaruh tekanan dan temperatur pada ekstraktor. Fluida superkritis memiliki densitas yang hampir sebanding dengan cairan. Dengan densitas yang tinggi, maka banyak molekul yang dapat melarutkan solut. Sehingga kemampuan melarutkan menjadi lebih besar (Taylor, 1996).
2.6 Karbondioksida Superkritis
Banyak liquida dikembangkan sebagai pelarut superkritis dengan pemanasan dan menaikkan tekanan. Gas CO2 biasanya
sering digunakan sebagai pelarut untuk proses ekstraksi fluida superkritis. Ini dikarenakan temperatur kritis CO2 yang rendah
sehingga memungkinkan proses eksperimen mendekati temperatur lingkungan (dapat dilihat dari tabel 2.6). Supercritical CO2,
merupakan CO2 pada temperatur dan tekanan di atas titik kritis.
Dimana nilai tekanan kritis CO2 (Pc) adalah 7,38 MPa dan
temperatur kritis (Tc ) adalah 31.1 oC (Kirk-Othmer, 1991).
Kondisi tersebut relatif mudah dicapai karena tidak terlalu banyak energi yang dibutuhkan. Nilai viskositas gas CO2 ditunjukkan oleh Gambar 2.3. Beberapa kelebihan yang dimiliki CO2 antara lain
sebagai berikut (Grandinson, 1996) :
a. Ideal solvent untuk ekstraksi material yang memiliki suhu labil. b. Secara komersial tersedia dengan kemurnian tinggi.
c. Tidak mengandung residu yang berbahaya, tidak berbau, tidak berasa, inert, dan tidak beracun.
d. Pemisahan CO2 dari ekstrak dapat dilakukan dengan mudah dan
sempurna.
e. Temperatur proses yang rendah f. Selektifitas tinggi.
g. Relatif murah, tidak mengubah sifat solute, tidak mudah terbakar, tidak korosif, tidak berwarna, dan tidak berbau.
20
Gambar 2.3 Viskositas CO2 pada Beberapa Temperatur dan
Tekanan
Gambar 2.4 Diffusivitas pada Beberapa Temperatur dan
Tekanan
2.7 Penelitian Terdahulu
Chu dkk (2006), melakukan mikronisasi pada cefpodoxime
21
metilen klorida, aseton dan etil asetat. Penelitian ini dilakukan pada range tekanan 100 - 150 bar dan range suhu 35 - 40 oC dengan
konsentrasi 0.3 – 1% berat. Konsentrasi tinggi menyebabkan partikel yang satu kontak dengan partikel yang lain sehingga terjadi aglomerasi, dan partikel yang dihasilkan merupakan partikel yang berukuran lebih besar. Aglomerasi diminimalisasi dengan menggunakan pelarut etil asetat dan dengan meningkatkan ratio CO2/larutan CPD. Meningkatnya tekanan presipitator
menghasilkan partikel yang makin kecil (Chu dkk., 2006). Machmudah dkk (2013), melakukan mikronisasi
lycopene dan β-cyclodextrin menggunakan proses fluida
superkritis (SEDS). Pencantuman kompleks, dipersiapkan dalam
N,N – dimethylformamide (DMF) dilarutkan dalam pelarut yang
sama kemudian mikronisasi dengan SEDS, menggunakan karbondioksida (CO2) sebagai superkritis anti-solvent. Pengaruh
dari konsentrasi awal lycopene dan β-cyclodextrin, laju alir CO2,
laju alir larutan, tekanan dan suhu yang mana proses dilakukan diuji. Morfologi dari partikel yang dihasilkan diamati menggunakan Scanning Electron Microscopy (SEM) dan Field
Emission – Scanning Electron Microscopy (FE – SEM). Partikel
kecil berbentuk bola didapatkan pada semua kondisi operasi. Pada tekanan tinggi, temperatur tinggi, laju alir CO2 tinggi, dan laju alir
larutan rendah. Ukuran partikel rata-rata yang didapatkan kira-kira 40 nm.
Boonnoun dkk (2013), melakukan miikronisasi
supercritical anti-solvent (SAS) berasal dari marigold lutein
dilarutkan dalam diklorometana dan etanol. Didalam penelitian ini diperoleh hasil dimana ukuran partikel pada laju alir CO2 20
ml/min didapat sebesar 2,05-2,49 µm dan pada laju alir CO2 25
ml/min didapat sebesar 1,58-1,94 µm. Kurniawansyah dkk (2015) melakukan penelitian yaitu “Perumusan kurkumin dapat dihirup : mikronisasi dan bioassay”. Di dalam penelitiannya digunakan metode “Atomized Rapid Injection Solvent Extraction (ARISE)” dimana menghasilkan pertikel berukuran 2µm.
22
23
BAB III
METODOLOGI PENELITIAN
Pada penelitian ini hasil ekstrak temulawak akan diproses menggunakan CO2 superkritis untuk mendapatkan partikel
temulawak dengan ukuran mikrometer pada berbagai kondisi operasi meliputi temperatur, tekanan, laju alir CO2 terhadap laju
alir larutan dan jenis pelarut. CO2 superkritis yang dialirkan secara
kontinyu digunakan sebagai anti-solvent. Temperatur operasi yang digunakan adalah 35oC dan 40oC pada tekanan 10 MPa dan 12
MPa. Rasio laju alir CO2 terhadap larutan divariasikan 15:0,25 ;
15:0,3 ml/min. Solvent untuk pelarutan kurkumin juga divariasikan yaitu aseton murni, aseton 95% volume + etanol 5% volume, dan aseton 90% volume + etanol 10% volume. Partikel yang terbentuk kemudian dianalisa dengan menggunakan SEM (Scanning
Electron Microscopy), FTIR (Fourier Transform Infrared Spectroscopy), kadar kurkumin dalam partikel yang terbentuk,
kandungan aseton dalam partikel yang terbentuk dan Dissolution
rate partikel akan dianalisa menggunakan UV-Vis
Spectrophotometer.
3.1 Alat dan Bahan Penelitian 3.1.1 Bahan Penelitian
1. Temulawak
Didapatkan dari Surabaya 2. Aseton
Diproduksi oleh Merck untuk solvent SAS. 3. Etanol 99,8%
Diproduksi oleh Merck untuk solvent proses ekstraksi, proses cleaning, solvent SAS dan analisa Spektrofotometer
UV-Vis.
4. Karbon dioksida (CO2) liquid dengan kemurnian 99,7%
Dibeli dari PT.Samator. 5. NaOH
24
Larutan NaOH 0,2 M digunakan untuk mengukur
dissolution rate partikel kurkumin.
6. KH2PO4
6,8 gram KH2PO4 digunakan untuk mengukur dissolution
rate partikel kurkumin.
7. Curcumin standar untuk analisa Spektrofotometer UV-Vis. Diproduksi untuk standard analisa kadar kurkumin dan
dissolution rate partikel kurkumin. 3.1.2 Alat Penelitian
3.1.2.1 Alat yang digunakan untuk Tahap Ekstraksi
1. Perangkat Soxhlet 2. Heater
3. Labu leher dua
4. Penutup (karet/plastik)
5. Saluran air pendingin masuk dan keluar
25
3.1.2.2 Alat yang digunakan untuk Tahap Distilasi
1. Perangkat Distilasi 2. Heater
3. Labu distilasi
4. Penutup (karet/plastik)
5. Saluran air pendingin masuk dan keluar
Gambar 3.2 Rangkaian alat Tahap Distilasi
3.1.2.3 Alat yang digunakan untuk Tahap Presipitasi Partikel dengan supercritical anti-solvent (SAS)
1. High Performance Liquid Chromatography (HPLC) Pump ada 2 pompa yang digunakan :
a) Jasco PU-1586, pompa ini digunakan untuk memompa karbon dioksida (CO2) liquid sampai pada tekanan
operasi yang diinginkan. Pompa mempunyai tekanan maksimum 50 MPa. Laju alir maksimal pada pompa adalah 20 mL/min.
b) Shimadzu LC-10AT VP, pompa ini digunakan untuk memompa larutan ekstrak dengan laju alir maksimal 9.999 mL/min dengan tekanan maksimumnya 400 kgf/cm2.
26 2. Oven
Oven digunakan sebagai pemanas untuk menaikkan dan menjaga temperature operasi ekstraksi. Oven ini bisa beroperasi hingga mencapai suhu 200OC.
3. Chiller
Chiller yang digunakan adalah Yamato Neocool Circulator
CF 600. Chiller ini berfungsi sebagai pendingin bagi karbon dioksida (CO2)sebelum masuk pompa. Hal ini dimaksudkan
agar karbon dioksida (CO2) tetap dalam keadaan cair
sebelum masuk ke dalam kolom ekstraksi. 4. Filter
Filter untuk tempat penampung partikel yang terbentuk.
5. Back Pressure Regulator (BPR)
BPR berfungsi sebagai pengatur tekanan proses dimana tekanan maksimumnya 40 MPa. BPR dilengkapi dengan pemanas yang bertujuan agar CO2 yang keluar dari BPR
tidak mengalami freezing (pembekuan) sehingga tidak menyumbat tube produk yang keluar.
6. Gas Flowmeter
Gas Flowmeter berfungsi sebagai pengukur banyaknya
karbon dioksida yang terpakai selama proses berlangsung. Alat pengukur ini beroperasi dalam satuan m3 dan liter,
namun untuk penelitian ini digunakan satuan liter.
27
3.2 Prosedur Percobaan
Percobaan ini dibagi menjadi 5 tahapan yaitu : 1. Tahap Persiapan Bahan Baku
2. Tahap Ekstraksi 3. Tahap Distilasi
4. Tahap Presipitasi Partikel 5. Tahap Analisa
3.2.1 Tahap Persiapan Bahan baku
Temulawak dicuci dengan menggunakan air bersih untuk menghilangkan kotoran. Selanjutnya, temulawak dipotong dan diblender agar ukurannya menjadi lebih kecil. Lalu, temulawak dikeringkan di dalam oven pada suhu 60oC selama 6 jam untuk
menghilangkan air.
3.2.2 Tahap Ekstraksi
Pada tahap ini temulawak yang sudah dikeringkan sebanyak 20 gram dimasukan ke dalam soxhlet untuk dilakukan proses ekstraksi menggunakan pelarut ethanol 99,8% sebanyak 300 ml. Peralatan ekstraksi ini juga dipasangkan dengan air pendingin. Selanjutnya, soxhlet dipanaskan dengan pemanas listrik dan dijaga pada suhu 80oC. Pemanasan dilakukan selama 12 jam.
Rata-rata untuk satu kali cycle terjadi selama 6 menit.
3.2.3 Tahap Distilasi
Pada tahap ini larutan hasil ekstrak temulawak yang sudah terbentuk akan dilakukan pemurnian dengan cara memisahkan ethanol dengan cara distilasi. Larutan hasil ekstrak dimasukkan kedalam labu distilasi untuk kemudian dilakukan pemanasan menggunakan heater. Suhu operasi distilasi dijaga sekitar 74-76oC,
selama 1,5 jam. Kemudian dilanjutkan dengan pengovenan selama 1.5 jam pada temperatur 400C.
28
3.2.4 Tahap Presipitasi Partikel
Tahap pertama penelitian ini adalah memompa karbondioksida (CO2) cair ke dalam rangkaian alat SAS
(supercritical Anti-Solvent) seperti pada gambar III.3 pada kondisi
temperatur, tekanan, dan rasio laju alir CO2 cair terhadap larutan
yang telah ditentukan. Selanjutnya, larutan ekstrak dipompa juga ke dalam rangkaian alat SAS (supercritical Anti-Solvent) melewati
inner tube dari concentric nozzle menggunakan HPLC pump. Hasil
presipitasi ditahan oleh filter di bagian bawah kolom. Setelah proses mikronisasi selesai, aliran kurkumin diberhentikan namun karbondioksisa (CO2) terus dialirkan selama satu jam untuk
memastikan semua solvent hilang dari partikel kurkumin. Hasil partikel kurkumin yang terbentuk selanjutnya akan dianalisa menggunakan SEM, FTIR dan UV-Vis Spectrophotometer. Laju alir CO2 diatur konstan sebesar 15 mL/min sebagai variabel tetap.
Sedangkan untuk variabel bebas yang digunakan dalam penelitian ini dapat dilihat pada Tabel 3.1.
Tabel 3.1 Variabel Bebas Pada Tahap Presipitasi Partikel
No. Variabel Variasi
1. Pelarut
Aseton murni
Aseton 95% + Etanol 5% (v/v) Aseton 90% + Etanol 10% (v/v) 2. Tekanan 10 dan 12 MPa
3. Temperatur 35 dan 40 oC
4. Laju Alir Larutan 0.25 dan 0.30 mL/min
3.2.5 Tahap Analisa
3.2.5.1 SEM (Scanning Electronic Microscopy)
Partikel yang terbentuk pada proses presipitasi dianalisa menggunakan SEM untuk mengetahui morfologi partikel yang terbentuk.
29
3.2.5.2 FTIR (Fourier Transform Infrared Spectroscopy)
Partikel yang terbentuk pada proses presipitasi dianalisa menggunakan FTIR untuk mengetahui gugus fungsi senyawa kurkumin.
3.2.5.3 UV-Vis Spectrophotometer
Partikel yang terbentuk pada proses SAS dianalisa menggunakan spektrofotometer UV-Vis untuk diketahui kadar kurkumin dalam partikel, kandungan aseton dalam partikel dan laju pelarutannya (dissolution rate). Analisa kadar kurkumin dalam partikel ditentukan dengan cara sebagai berikut. Mula-mula menyiapkan etanol 99,8% yang digunakan sebagai pelarut dan kurkumin standar. Melarutkan kurkumin standar ke dalam etanol 99,8% dengan konsentrasi 100, 10, 4, 3, 2, 1, dan 0.1 ppm. Melakukan scanning dengan panjang gelombang 190 nm – 547 nm. Mendapatkan panjang gelombang untuk mengukur absorbansi yaitu 424 nm. Mengukur absorbansi masing-masing konsentrasi larutan selama 1 jam dengan interval 5 menit. Membuat grafik kurkumin standar antara nilai absorbansi dengan konsentrasi. Selanjutnya melarutkan partikel yang terbentuk sebanyak 0,2 mg dalam 10 ml etanol 99,8% lalu disonikasi agar terlarut sempurna selama 10 menit. Kemudiam, mengambil 3 ml untuk dilakukan pengukuran nilai absorbansi pada panjang gelombang 424 nm. Pengukuran dilakukan selama 1 jam dengan interval 5 menit. Untuk uji variabel partikel yang terbentuk lainnya dilakukan dengan cara yang sama.
Analisa kandungan aseton dalam partikel dilakukan dengan cara berikut. Menyiapkan etanol 99,8% sebanyak 3 ml lalu dilakukan scanning dengan panjang gelombang 196 nm -1099 nm dan melakukan scanning untuk campuran etanol dan aseton (5:1). Lalu melarutkan partikel sebanyak 0,1 mg kedalam 3 ml etanol, disonikasi selama 5 menit dan dilakukan scanning dengan panjang gelombang 196 nm - 1099 nm. Membuat grafik hasil scanning untuk etanol 99.8%, etanol + aseton (5:1) dan masing-masing partikel
30
Analisa laju pelarutan ditentukan dengan cara sebagai berikut. Mula-mula menyiapkan campuran 0,2 M NaOH sebanyak 77 mL dengan 6,8 g KH2PO4 dalam 1000 mL aquadest sebagai
dissolution medium. Melarutkan kurkumin standar ke dalam medium dissolution dengan konsentrasi 10, 3, 2, dan 1 ppm.
Mengukur absorbansi masing-masing konsentrasi larutan selama 1 jam dengan interval 5 menit. Membuat grafik kurkumin standar antara nilai absorbansi dengan konsentrasi. Selanjutnya, 0,5 mg partikel kurkumin hasil mikronisasi ditambahkan ke dalam 10 ml
dissolution medium kemudian diaduk dengan kecepatan 80 rpm
pada 37 oC. Selanjutnya mengukur absorbansi dari 3 ml sampel
dengan interval waktu 3 jam pertama, 5 jam berikutnya, 12 jam berikutnya, 24 jam, 48 jam, 72 jam untuk masing-masing interval waktu selama 1 jam pada panjang gelombang 424 nm menggunakan spektrofotometer UV-Vis.
31
BAB IV
HASIL DAN PEMBAHASAN
Dalam penelitian ini, pengaruh pelarut dan kondisi operasi pada pembentukan partikel kurkumin dari ekstrak temulawak dipelajari menggunakan metode Supercritical Anti-Solvent (SAS). Pelarut yang digunakan adalah 100% volume aseton, 95% volume aseton : 5% volume etanol, dan 90% volume aseton : 10% volume etanol. Proses SAS dilakukan pada tekanan 10 MPa dan 12 MPa, temperatur 35oC dan 40oC dengan rasio laju alir CO
2 terhadap laju
alir larutan ekstrak kurkumin 15:0,25 ml/min dan 15:0,30 ml/min. Kurkumin sebagai starting material diperoleh dari temulawak yang diekstrak menggunakan etanol sebagai pelarut pada alat soklet ekstraksi.
Berdasarkan eksperimen yang telah dilakukan, maka didapatkan hasil analisa dari penelitian ini berupa % kadar kurkumin dalam partikel, % yield pembentukan partikel,
dissolution rate partikel yang terbentuk, kandungan aseton dalam
partikel, bentuk morfologi partikel, dan gugus fungsi partikel yang terbentuk.
4.1 Kadar Kurkumin dalam Partikel
Pada penelitian ini, kurkumin yang akan diproses menjadi partikel diperoleh dari hasil soklet ekstraksi rimpang temulawak yang sudah dikeringkan dan diperkecil ukurannya. Untuk mengetahui kadar kurkumin di dalam partikel yang terbentuk, maka dilakukan analisa UV-Vis Spectrophotometer dengan metode yang telah dijelaskan pada Bab III. Berdasarkan hasil analisa menggunakan UV-Vis Spectrophotometer didapatkan bahwa kadar kurkumin di dalam ekstrak sebelum proses SAS sebesar 0,43%, sedangkan kadar kurkumin di dalam partikel hasil proses SAS berkisar antara 1,35-3,7%, seperti terlihat pada Tabel 4.1. Hal ini menunjukan bahwa selain terjadi pembentukan partikel, juga terjadi peningkatan kadar kurkumin di dalam partikel. Peningkatan ini terjadi dikarenakan pelarutan kembali
32
ekstrak yang terbentuk menggunakan aseton dan sedikit etanol, dimana kurkumin mempunyai kelarutan yang tinggi dibandingkan komponen lain seperti minyak atsiri yang terkandung di dalam ekstrak. Selain itu, pada proses SAS, karbondioksida superkritis telah melarutkan sebagian minyak atsiri dalam ekstrak sehingga terpisah dari partikel yang terbentuk (Muffidah, 2015).
Kadar kurkumin tertinggi dihasilkan pada partikel yang diproses pada temperatur 35oC, tekanan 10 MPa, rasio laju alir CO
2
terhadap laju alir larutan ekstrak 15:0,25 ml/min dengan menggunakan aseton murni sebagai pelarut, seperti terlihat pada Tabel 4.1.
Tabel 4.1. Hasil Analisa Kadar Kurkumin
Sampel Kadar
Kurkumin (%)
Ekstrak Sebelum Proses SAS 0,43
Partikel 1 (35oC, 10 MPa, 15:0,25, Aseton
murni) 3,7
Partikel 2 (35oC, 10 MPa, 15:0,25, Aseton + 5
% etanol) 3,36
Partikel 3 (35oC, 10 MPa, 15:0,25, Aseton +
10 % etanol) 3,27
Partikel 4 (40oC, 10 MPa, 15:0,25, Aseton
murni) 1,35
Partikel 5 (35oC, 12 MPa, 15:0,25, Aseton
murni) 3,62
Partikel 6 (35oC, 10 MPa, 15:0,30, Aseton