STUDI KINETIKA REAKSI PADA METANOLISIS MINYAK
JARAK PAGAR
M. Said, Wenny Septiarty, Tri Tutiwi
Jurusan Teknik Kimia Fakultas Teknik Universitas Sriwijaya
Abstrak
Penelitian ini dilakukan untuk melihat pengaruh rasio reaktan, temperatur, dan waktu reaksi terhadap konversi minyak jarak menjadi metil ester dan mengetahui pengaruh temperature reaksi transesterifikasi terhadap konstanta kecepatan reaksi. Metil ester merupakan bahan bakar alternatif yang dihasilkan dari reaksi transesterifikasi minyak jarak dengan methanol. Variabel yang diteliti adalah rasio reaktan (minyak jarak : metanol), yaitu 1 : 2, 1 : 4, dan 1 : 6, temperatur reaksi yaitu 60°C,70°C, dan 80°C, dan waktu reaksi yaitu 10, 20, 30, 40, 50, dan 60 menit. Hasil penelitian menunjukan bahwa konstanta kecepatan reaksi terbaik sebesar 7,4.10-2 menit-1 diperoleh pada rasio reaktan 1 : 6 dan temperatur reaksi 80°C. Sedangkan konstanta kecepatan reaksi terkecil sebesar 3,4.10-2 menit-1 diperoleh pada rasio reaktan 1 : 6 dan temperatur reaksi 60 °C. Energi aktivasi yang didapat pada reaksi ini sebesar 38457,32 J mol-1 menit -1 dengan faktor frekuensi sebesar 38739,69252 menit-1.
Kata kunci : transesterifikasi, minyak jarak, metil ester, energi aktivasi
Abstract
This research has been done to know Effection of Reactant Ratio, Reaction Temperature, and Reaction Time to conversion of jatropha oil to produce Methyl Ester and to know the effection of transeterification reactions temperature toconstant velocity of reactions. Methyl ester is an alternative fuel oil produced from transesterification of jatropha oil and methanol. Variables that were examined are reactant ratios (jatrohpa oil : methanol), that are 1 : 2, 1 : 4, and 1 : 6, reaction temperatures that are 60oC, 70oC, 80oC, and reaction times that are 10, 20, 30, 40, 50, and 60 minutes. The result of research show that the best rate reactions is 7,4.10-2 minutes-1 achieved at ratio of reactant 1 : 6 with reaction temperature is 80oC. While the least rate reactions is 3,4.10-2 achieved at ratio reactant is 1:6 with reaction temperature 60oC. Activation energy that was got from this reactions is 38457,32 J mol-1 menit-1 with frekwention factor is 38739,69252 menit-1.
Key words : transesterification, jatrohpa oil, methyl ester, activation energy.
I. PENDAHULUAN
Kebutuhan BBM mengalami peningkatan sejalan dengan peningkatan kebutuhan masyarakat akan bahan bakar ini untuk kegiatan transportasi, aktivitas industri, PLTD, aktivitas rumah tangga dan sebagainya. Berdasarkan data Automotive Diesel Oil, konsumsi bahan bakar minyak di Indonesia sejak tahun 1995 telah melebihi produksi dalam negeri dan diperkirakan dalam kurun waktu 10 – 15 tahun lagi, cadangan minyak Indonesia akan habis. Perkiraan ini terbukti karena sering terjadi kelangkaan BBM di beberapa daerah di Indonesia.
Kondisi ini memicu kenaikan harga BBM di berbagai negara termasuk Indonesia.
16 Jurnal Teknik Kimia, No. 1, Vol. 17, Januari 2010 fosil. Pemanfaatan minyak jarak pagar sebagai
biodisel memberikan peluang yang besar karena minyak jarak pagar tidak dapat dikonsumsi sebagai minyak makan (non edible oil).
Tanaman jarak pagar menghasilkan biji yang memiliki kandungan minyak sekitar 30 – 50 %. Minyak jarak pagar mengadung 16 – 18 atom karbon per molekul sedangkan minyak bumi sebagai bahan baku minyak diesel mengadung 8 – 10 atom karbon. Kandungan atom karbon yang lebih besar pada minyak jarak pagar mengakibatkan viskositas minyak jarak pagar lebih tinggi (lebih kental) bila dibandingkan dengan viskositas minyak bumi. Minyak jarak pagar memiliki daya pembakaran yang masih rendah untuk dapat digunakan sebagai bahan bakar (biodiesel). Proses transesterifikasi dapat digunakan untuk menurunkan viskositas minyak jarak pagar dan meningkatkan daya pembakarannya sehingga sesuai dengan standar minyak diesel untuk kendaraan bermotor. Proses transesterifikasi minyak jarak dilakukan dengan menggunakan alkohol untuk mengubah trigliserida menjadi metil ester (biodiesel) dan gliserol.
Biodiesel dapat digunakan baik secara murni maupun dicampur dengan minyak diesel pada mesin kendaraan tanpa mengalami modifikasi mesin. Biodiesel bersifat lebih ramah lingkungan dan dapat diperbaharui (renewable) dapat terurai (biodegradable), memiliki sifat pelumasan terhadap piston karena termasuk kelompok minyak tidak mengering, mampu mengeliminasi efek rumah kaca dan kontinuitas ketersediaan bahan baku terjamin. Biodiesel bersifat ramah lingkungan karena menghasilkan emisi gas buang yang jauh lebih baik dibandingkan minyak diesel/solar, yaitu bebas sulfur, bilangan asap rendah dan angka cetana antara 57-62, terbakar sempurna dan tidak beracun.
Hasil penelitian ini diharapkan dapat dimanfaatkan untuk perancangan reaktor pada skala pilot plant dan sebagai pengembangan teknologi transesterifikasi menghasilkan metil ester sebagai bahan bakar alternatif.
II. FUNDAMENTAL 2.1. Biodiesel
Biodiesel adalah nama untuk jenis fatty ester, umumnya merupakan monoalkyl ester yang terbuat dari minyak tumbuh-tumbuhan (minyak nabati). Minyak nabati yang dapat digunakan sebagai bahan baku biodiesel dapat berasal dari kacang kedelai, kelapa, kelapa sawit, padi, jagung,
jarak, papaya dan banyak lagi melalui proses transesterifikasi. (Mardiah, Agus Widodo, Efi Trisningwati, dan Aries Purijatmiko, 2006)
Keuntungan dari biodiesel :
a. Campuran dari 20 % biodisel dengan 80 % petroleum diesel dapat digunakan pada mesin diesel tanpa modifikasi.
b. Industri biodiesel dapat menggunakan lemak atau minyak daur ulang.
c. Biodiesel tidak beracun.
d. Biodiesel memiliki cetane number yang tinggi, yaitu di atas 100 sedangkan cetane number bahan bakar diesel hanya 40.
e. Penggunaan biodiesel dapat memperpanjang umur mesin diesel karena biodisel lebih licin. f. Biodiesel menggantikan bau petroleum
dengan bau yang lebih enak.
2.2. Minyak Jarak Pagar (Crude Jatropha Curcas Oil)
Tanaman jarak pagar merupakan jenis tanaman perdu dengan tinggi 1 – 7 m bercabang tidak teratur. Tanaman ini memiliki batang berkayu, berbentuk silindris dan jika tergores mengeluarkan getah. Daun tanaman jarak pagar lebar dan berbentuk jantung dengan panjang 5 -15 cm. Bunga tanaman ini merupakan bunga majemuk berbentuk malai dan berwarna kuning kehijauan. Buah tanaman jarak berbentuk telur dengan diameter 2 – 4 cm dan memiliki 3 ruang dengan masing-masing ruang terdapat satu biji yang berbentuk bulat lonjong berwarna coklat kehitaman. Biji ini mengandung minyak dengan rendemen 30 – 50 % dan mengandung toksin sehingga tidak dapat dikonsumsi oleh manusia.
Tabel 1. Komponen kimia biji jarak Komponen Jumlah (%)
Minyak Karbohidrat
Serat Abu Protein
55 12 12,5
Tabel 2. Sifat Fisika dan Kimia Minyak Jarak Pagar
Karakteristik Nilai Wujud
Kelarutan dalam alkohol (20oC) kuning dan tidak menjadi keruh meski disimpan dalam waktu yang lama
Jernih (tidak keruh) 145 – 154
230 oC 322
39,9 dyne/cm (sumber Bailey dikutip dari Ketaren, 1986)
2.3. Metanol
Metanol adalah alkohol yang dapat dibuat dari batubara, gas alam, atau kayu Metanol disebut juga metil alkohol merupakan senyawa paling sederhana dari gugus alkohol. Rumus kimianya adalah CH3OH. Metanol berwujud cairan yang tidak berwarna, dan mudah menguap. Metanol merupakan alkohol yang agresif sehingga bisa berakibat fatal bila terminum, dan memerlukan kewaspadaan yang tinggi dalam penanganannya. Jika menghirup uapnya cukup lama atau jika kena mata dapat menyebabkan kebutaan, sedangkan jika tertelan akan mengakibatkan kematian. (Andi Nur Alam Syah, 2006)
Sebagian besar produksi metanol diubah menjadi formaldehid yang pada akhirnya digunakan untuk membuat polimer, juga digunakan sebagai pelarut. Memiliki berat molekul 32,042, titik leleh -98oC dan titik didih 64oC.
Alkohol yang paling umum digunakan untuk transesterifikasi adalah metanol, karena harganya lebih murah dan daya reaksinya lebih tinggi dibandingkan dengan alkohol rantai panjang, sehingga metanol ini mampu memproduksi biodiesel yang lebih stabil.
2.4. Katalis Natrium Hidroksida (NaOH)
Katalis adalah suatu bahan yang digunakan untuk memulai reaksi dengan bahan lain. Katalis dimanfaatkan untuk mempercepat suatu reaksi, terlibat dalam reaksi tetapi tidak ikut terkonsumsi menjadi produk Pemilihan katalis ini sangat bergantung pada jenis asam lemak yang terkandung di dalam minyak tersebut. Jenis asam lemak dalam minyak sangat berpengaruh terhadap karakteristik fisik dan kimia biodiesel, karena asam lemak ini yang akan membentuk ester atau biodiesel itu sendiri (Mardiah, Agus Widodo, Efi Trisningwati, dan Aries Purijatmiko, 2006).
2.5. Transesterifkasi
Transesterifikasi merupakan suatu proses penggantian alkohol dari suatu gugus ester (trigliserida) dengan ester lain atau mengubah asam–asam lemak ke dalam bentuk ester sehingga menghasilkan alkyl ester. Proses tersebut dikenal sebagai proses alkoholisis. Proses alkoholisis ini merupakan reaksi biasanya berjalan lambat namun dapat dipercepat dengan bantuan suatu katalis. Katalis yang biasa dipergunakan adalah katalis asam seperti HCl dan H2SO4, dan katalis basa NaOH dan KOH. (Yuli Setyo Indartono, 2006)
2.6. Bahan bakar
Spesifikasi minyak diesel secara lengkap dapat dilihat pada Tabel berikut ini:
Tabel 3. Spesifikasi Minyak Solar
Sifat Batasan Meto
de Min Mak
s 1. Spesifik grafity
60/60 OF 0.82 0.87
D-4. Alternatively
18 Jurnal Teknik Kimia, No. 1, Vol. 17, Januari 2010 Residue, %wt - 0.1
10. Water Content,
% vol - 0.05 D-95
11. Sediment, %wt - 0.01 D-473 12. Ash Content,
%wt - 0.01
D-482
Neutralization Value 1. Strong Acid
Number, mg KOH/g
- Nil
D-974
2. Total Acid Number, mg
KOH/g - 0.6
D-974
3. Flash Point
P.M.cc, OF 150 - D-93 4. Dist. Rec. At
300 OC, %vol 40 - D-86
III. METODOLOGI PENELITIAN 3.1. Analisa Bahan Baku
Analisa bahan baku dilakukan untuk mengetahui asam lemak bebas, asam lemak total, dan berat jenisnya.
3.2. Perlakuan Dan Rancangan Penelitian 3.2.1. Perlakuan Penelitian
Proses transesterifikasi minyak jarak dilakukan dengan memberikan perlakuan minyak jarak dengan metanol dengan variasi rasio reaktan tertentu dan ditambahkan katalis NaOH sebanyak 1 % dari volume minyak kedalam reaktor berpengaduk. Reaksi yang terjadi dalam reaktor berlangsung secara batch yang dikondisikan pada temperatur dan waktu reaksi tertentu. Konversi reaksi ditentukan pada berbagai variasi temperatur dan waktu reaksi tersebut.
3.2.2. Rancangan Penelitian
Konversi reaksi merupakan fungsi waktu reaksi dan temperatur reaksi. Waktu reaksi divariasikan dari 10 sampai 60 menit dengan interval waktu 10 menit, temperatur reaksi divariasikan dari 60oC sampai 80oC dengan interval 10oC, dan rasio reaktan minyak jarak – metanol pada (1 : 2), (1 : 4), (1 : 6). Jumlah run penelitian adalah 54.
3.3. Prosedur Penelitian
1) Masukkan minyak jarak ke dalam labu leher tiga yang dilengkapi dengan termometer, pemanas, dan kondensor. Kemudian dipanaskan sampai suhu 60ºC.
2) Dicampurkan methanol, dan katalis dengan perbandingan berat dari minyak jarak ratio 1:2 ke dalam beker gelas. Kemudian dipanaskan sampai suhu 40ºC.
3) Campuran katalis dan methanol dimasukkan ke dalam labu leher tiga.
4) Selama 60 menit, sampel diambil sebanyak 10 ml setiap 10 menit pemanasan.
5) Kemudian dimasukan ke dalam botol sampel yang didiamkan selama 24 jam agar terlihat dua lapisan, kemudian dipisahkan dengan pipet tetes.
6) Setelah didapatkan campuran lapisan gliserol (pada lapisan bawah) yang kemudian dianalisa dengan Metode Griffin untuk mengetahui konversi dari minyak jarak pagar.
7) Percobaan yang sama dilakukan kembali untuk suhu 70 oC sampai 80 oC.
8) Kemudian diulang kembali untuk rasio reaktan 1 : 4 dan 1 : 6 pada suhu 70 oC sampai 80 oC.
9) Kemudian lapisan atas yang terbentuk (metil ester) dicuci dengan menggunakan air panas dengan temperatur sekitar 60oC. 10) Air tersebut dicampurkan ke dalam corong
pemisah, sehingga terbentuk dua lapisan. Lapisan bawah yang terbentuk (air) dibuang.
11) Kemudian lakukan pencucian berulang-ulang sampai lapisan bawah yang terbentuk (air) menjadi jernih. Dan didapatkan metil ester yang murni.
12) Terakhir lakukan pemanasan selama 2 jam pada metil ester sampai suhu 100ºC, lakukan sampai tidak ada lagi gelembung. 13) Metil ester yang didapat dianalisa.
3.3.1. Analisa Kadar Gliserol
Gliserol dianalisa dengan cara Asetin (Griffin, 1955). Sampel dibiarkan semalam didalam corong pemisah agar sisa metanol menguap hingga terbentuk dua lapisan, yaitu lapisan gliserol berada di bawah dan metil ester di lapisan atas. Lapisan ester dipisahkan dengan gliserol, kemudian gliserol dianalisa dengan cara sebagai berikut :
1. Ambil 1,5 gr gliserol, masukkan ke dalam erlenmeyer.
2. Lalu ditambahkan 3 gr natrium asetat dan 7,5 ml asam asetat anhidrid.
4. Campuran yang telah didinginkan sampai suhu 60oC, kemudian ditambahkan air 50 ml dengan suhu yang sama 60oC.
5. Campuran yang telah didinginkan dinetralkan dengan larutan NaOH 3 N dengan memakai indikator phenolpthalin kurang lebih 4 tetes sampai terbentuk warna merah muda.
6. Selanjutnya ditambahkan lagi larutan NaOH 1 N sebanyak 10 ml.
7. Kemudian campuran dididihkan kembali selama 15 menit dan selanjutnya didinginkan.
8. Titrasi dengan HCl 1 N sampai warna merah hilang.
Gliserol yang terbentuk dihitung dengan persamaan Griffin :
HCl Wr : Berat campuran minyak – metanol (gr) Ws : Berat sampel yang diambil (gr) Wg : Berat lapisan gliserol (gr)
Wa : Berat lapisan gliserol yang dianalisis (gr) Vb : Volume HCl titrasi blanko (ml)
Vs : Volume HCl titrasi sampel (ml) NHCl : Normalitas HCl (mgek/ml)
Konversi dihitung dengan persamaan berikut :
)
3.3.2. Analisa Metil Ester
Metil ester yang merupakan hasil atas reaksi dipisahkan dari gliserol pada lapisan bawah dengan corong pemisah. Sebelum diuji sifat fisisnya, metil ester ini perlu dimurnikan dengan cara mencucinya dengan Aquades untuk mengikat gliserol yang masih tersisa. Setelah terbentuk dua lapisan, kemudian dipisahkan dengan memakai corong pemisah. Lapisan atas merupakan metil ester dipanaskan pada temperatur kurang lebih 100oC untuk menghilangkan sisa metanol dan air.
Metil ester murni diuji sifat fisinya dengan cara ASTM (American Soceity for Testing Material) di laboratorium Penguji Pertamina UP-III Palembang, kemudian hasil pengujian dibandingkan dengan spesifikasi minyak diesel. Analisa sifat – sifat fisis metil ester yang akan diuji adalah :
- Densitas (ASTM D-1298) - Kinematic viscosity (ASTM D-445) - Flash point (ASTM D-93) - Water content (ASTM D-95) - Colour ASTM (ASTM D-1500)
- Ash Content (ASTM D-482) - Nilai kalor (Kalkulasi)
- Conradson Carbon Residue (ASTM D-189)
- Distillation (ASTM D-86) - Centane Index (ASTM D-976) - Appearance (ASTM D-4176)
IV. HASIL DAN PEMBAHASAN 4.1. Pengaruh Temperatur Terhadap Konversi Reaksi
Hubungan temperatur dengan konversi reaksi ini dapat dilihat dengan memvariasikan temperatur pada rasio reaktan dan waktu reaksi yang konstan. Variasi temperatur pada penelitian ini ada tiga yaitu 60oC, 70oC, 80oC. hubungan temperatur dapat dilihat dengan jelas pada grafik 4.1. Grafik ini menunjukkan hubungan temperatur terhadap konversi reaksi pada rasio reaktan 1 : 2 dalam berbagai waktu reaksi.
20 Jurnal Teknik Kimia, No. 1, Vol. 17, Januari 2010 Tabel 4. Hubungan Temperatur terhadap Konversi
Reaksi pada Rasio Reaktan 1:2 dalam berbagai Variasi Waktu Reaksi
t (waktu), Konversi
menit T = 60oC T = 70oC T = 80oC 10 4,71761 6,14910 4,34657 20 6,88059 8,29129 28,13642 30 9,89581 13,47021 26,15160 40 10,62242 16,42147 17,57922 50 7,64608 13,58537 14,70140 60 6,03849 10,50692 10,60512
Tabel 5. Hubungan Temperatur terhadap Konversi Reaksi pada Rasio Reaktan 1:4 dalam berbagai Variasi Waktu Reaksi
Tabel 6. Hubungan Temperatur terhadap Konversi Reaksi pada Rasio Reaktan 1:6 dalam berbagai Variasi Waktu Reaksi
Kenaikan konversi pada setiap kenaikan temperatur ini terjadi karena kesempatan partikel – partikel untuk saling bertumbukan menjadi lebih besar, karena menurut teori kinetika, kenaikan temperatur akan memberikan input energi kepada partikel sehingga probability terjadinya tumbukan akan semakin besar, sehingga akan meningkatkan konversi reaksi yang dicapai.
4.2. Energi Aktivasi
Nilai k ditentukan dari slope kurva -ln (1 – x) Vs waktu t pada temperatur tertentu. Nilai konstanta kecepatan reaksi (k) pada temperatur 60 - 80 oC untuk rasio reaktan 1 : 6 dapat dilihat pada tabel 4.
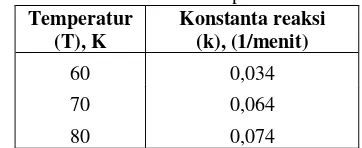
Tabel 7. Nilai Konstanta Kecepatan Reaksi
Temperatur (T), K
Konstanta reaksi (k), (1/menit)
60 0,034
70 0,064
80 0,074
Tabel diatas dapat digunakan untuk menentukan energi aktivasi (E) dan faktor frekuensi (A) dengan menggunakan persamaan Arrhenius, yaitu :
RT
/
E
e
A
k
=
−
RT
E
A
ln
k
ln
=
−
maka, y = ax + b, dengan : y : ln k
a : - (E/R) x : 1/T b : ln A
Tabel 8. Tabulasi Data ln k dan 1/T
T (K) 1/T k ln k
333.15 0.00300 0,034 -3,3814 343.15 0.00291 0,064 -2,7489 353.15 0.00283 0,074 -2,6037
Faktor frekuensi (A) dan –(E/R) diperoleh dati regresi linear data 1/T dan ln K pada tebel diatas. Hasil regresi linear didapatkan faktor frekuensi (A) sebesar 0,056 menit-1 dan –(E/R) sebesar -9,324 x 10-4 K/menit. Energi aktivasi didapatkan dengan mengalikan nilai –(E/R) dengan nilai R = 8,314 J mol-1K-1 sehingga didapat energi aktivasi sebesar 7,752 Jmol-1menit -1
.
4.3. Pengujian Sifat Fisis Metil Ester
Metil ester diuji sifat fisisnya dengan metode ASTM (American Society for Testing Material) di Laboratorium Pertamina UP-III Palembang. Sampel metilester yang dianalisis pada kondisi operasi temperatur 80oC, waktu 30 menit dan ratio reaktan 1:6.
t (waktu), Konversi
menit T = 60oC T = 70oC T = 80oC 10 73,04550 57,58089 51,16985 20 80,12878 76,22693 73,84337 30 86,42400 88,14717 88,80204 40 75,06968 69,88652 67,41450 50 39,60499 45,42248 41,06180 60 25,78250 38,08110 32,18946
t (waktu), Konversi
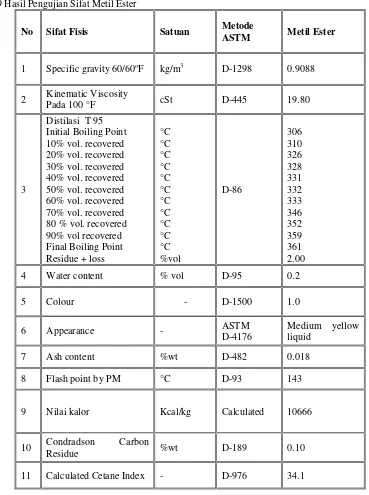
Tabel 9 Hasil Pengujian Sifat Metil Ester
No Sifat Fisis Satuan Metode
ASTM Metil Ester
1 Specific gravity 60/60oF kg/m3 D-1298 0.9088
2 Kinematic Viscosity
Pada 100 °F cSt D-445 19.80
3
Distilasi T 95 Initial Boiling Point 10% vol. recovered 20% vol. recovered 30% vol. recovered 40% vol. recovered 50% vol. recovered 60% vol. recovered 70% vol. recovered 80 % vol. recovered 90% vol recovered Final Boiling Point Residue + loss
°C °C °C °C °C °C °C °C °C °C °C %vol
D-86
306 310 326 328 331 332 333 346 352 359 361 2.00
4 Water content % vol D-95 0.2
5 Colour - D-1500 1.0
6 Appearance - ASTM
D-4176
Medium yellow liquid
7 Ash content %wt D-482 0.018
8 Flash point by PM °C D-93 143
9 Nilai kalor Kcal/kg Calculated 10666
10 Condradson Carbon
Residue %wt D-189 0.10
11 Calculated Cetane Index - D-976 34.1
V. KESIMPULAN DAN SARAN 5.1. Kesimpulan
Dari hasil penelitian dan pembahasan dapat diambil kesimpulan sebagai berikut :
1) Semakin tinggi rasio reaktan (minyak jarak pagar : metanol), maka konversi reaksi yang dihasilkan juga semakin tinggi.
2) Semakin tinggi temperatur reaksi, maka konstanta kecepatan reaksi semakin tinggi.
3) Kondisi operasi yang paling optimal dengan konversi terbesar yaitu 88,80204 % diperoleh
pada rasio reaktan 1 : 6 dengan temperatur reaksi 80oC dan waktu reaksi 30 menit.
22 Jurnal Teknik Kimia, No. 1, Vol. 17, Januari 2010
5.2.Saran
Penelitian lanjutan disarankan menggunakan reaktor pada skala yang lebih besar dengan kondisi optimum dari skala laboratorium.
VI. DAFTAR PUSTAKA
Prihandana, Rama, dkk. 2005. Meraup Untung dari Jarak Pagar. Tangerang: Agromedia Pustaka.
Hambali, Erliza,dkk. 2007. Jarak Pagar Tanaman Penghasil Biodiesel. Jakarta: Penebar Swadaya.
Hambali, Erliza,dkk. 2008. Divesifikasi Produk Olahan Jarak Pagar dan Kaitannya Dengan Corporate Social Responsibility (CSR) Perusahaan Swasta di Indonesia. Bioenergy Alliance.
Tim Pusat Penelitian Surfaktan dan Bioenergi, 2008 dalam www.sbrc-ipb.com
Tim Pusat Penelitian dan Pengembangan Perkebunan. 2007. dalam www.puslibang perkebunan.com
Subair, Muhammad. 2008. dalam www.balitbangda@litbangda-sulsel.go.id Fessenden&Fessenden.1982. Kimia Organik, ed.
Ke-3. Jakarta: Erlangga
Pertamina. 1997. Bahan Bakar Minyak. Direktorat Pembekalan dan Pemasaran Dalam Negeri. Sudarmadji, S., Haryono, Bambang., dan Suhandi.
1997. Prosedur Analisa Untuk Bahan Makanan dan Pertanian, ed. ke-4. Yogyakarta: Liberty
Ismail, Syarifuddin. 2004. Kinetika Kimia. Inderalaya: Universitas Sriwijaya.
Levenspiel, Octave. 1972. Chemical Reaction Engineering, second edition. United State of America.
Prihandana, Rama, dkk. 2005. Menghasilkan Biodiesel Murah Mengatasi Polusi & Kelangkaan BBM. Tangerang: Agromedia Pustaka.
Alamsyah, Andi Nur. 2006. Biodiesel Jarak Pagar. Bogor: PT. Agromedia Pustaka. Mardiah ; Widodo, Agus ; Trisningwati, Efi ;