OPTIMASI METODA KRISTALISASI STEVIOSIDA DARI
Stevia rebaudiana (Bert.)
Yohanes Martono, Yohan, Lusiawati Dewi
Prodi Kimia Fakultas Sains dan Matematika Universitas Kristen Satya Wacana Jl. Diponegoro 52-60 Salatiga
e-mail: [email protected]
ABSTRAK
Seiring dengan perkembangan produksi pangan dunia, pemanis di Indonesia didominasi oleh kehadiran gula sukrosa dan pemanis sintetis, tetapi penggunaannya dalam jangka waktu yang lama memiliki efek negatif bagi kesehatan. Oleh karena itu, masyarakat cenderung mencari alternatif pemanis alami rendah kalori. Salah satu alternatif pemanis alami rendah kalori adalah senyawa steviosida dari Stevia rebaudiana (Bert.) Tujuan dari penelitian ini adalah mendapatkan kristal stevisioda dari Stevia rebaudiana (Bert.) dengan metode kristalisasi, menetapkan kadar steviosida dalam larutan di setiap tahap kristalisasi secara Kromatografi Cair Kinerja Tinggi (KCKT), dan menetapkan kadar tertinggi steviosida dalam kristal secara KCKT. Metoda yang digunakan yaitu preparasi, ekstraksi, deklorofilasi, redefatisasi, klarifikasi, dan kristalisasi. Hasil penelitian ini menunjukkan bahwa, metode kristalisasi yang dikembangkan dapat menghasilkan kristal steviosida. Larutan di setiap tahap kristalisasi mengandung steviosida dengan kadar antara 1.323 – 4.285 µg/ml. Kadar tertinggi steviosida dalam kristal yang diperoleh adalah 20,16% b/b.
Kata kunci: steviosida, kristalisasi, KCKT
1. Pendahuluan
Kebutuhan pemanis semakin meningkat seiring dengan peningkatan produksi pangan dunia. Saat ini, pemenuhan kebutuhan pemanis di masyarakat dipenuhi dengan kehadiran gula sukrosa. Bila dilihat dari sisi kesehatan, gula sukrosa memiliki efek samping seperti obesitas, bahkan dapat memicu timbulnya penyakit diabetes. Dari efek samping tersebut, berbagai macam solusi dihadirkan seperti penggunaan pemanis sintetis yang rendah kalori seperti sakarin dan siklamat. Sebenarnya, pemanis sintetis ini hanya ditujukan untuk penderita diabetes atau konsumen dengan diet rendah kalori. Berdasarkan beberapa penelitian, ternyata pemanis ini bersifat karsinogenik apabila digunakan secara berlebihan dan berkesinambungan dalam jangka waktu yang lama (Mudjajanto, 2005).
Dewasa ini, masyarakat cenderung mencari alternatif pemanis alami pengganti gula sukrosa maupun pemanis sintetis yang tidak hanya aman dikonsumsi tetapi juga rendah kalori. Salah satu alternatif pemanis alami tersebut adalah steviosida dari Stevia rebaudiana (Bert.) dengan tingkat kemanisan 200 hingga 300 kali sukrosa (Philip, 1987). Beberapa penelitian menyebutkan bahwa steviosida mengandung kalori yang rendah sampai dengan nol kalori (Moraes dkk, 2001) sehingga aman bagi penderita diabetes atau konsumen yang sedang melakukan diet. Berdasarkan hasil penelitian, steviosida aman dikonsumsi oleh masyarakat umum karena tidak mempunyai efek teratogenik (Yodyingguard dan Bunyawong, 1991), mutagenik (Suttajit dkk., 1993), atau karsinogenik (Xili dkk., 1992). Oleh sebab itu, penelitian untuk mengekstrak daun stevia menjadi kristal yang mengandung steviosida yang tinggi dan mempunyai visualisasi kristal yang dapat diterima masyarakat akan memiliki potensi ekonomi yang besar.
Salah satu cara untuk mendapatkan kristal dari steviosida adalah dengan metoda ekstraksi. Ekstraksi yang dikembangkan adalah ekstraksi pelarut yang dikombinasi dengan langkah-langkahh yang lain seperti klarifikasi, penyesuaian pH dan kristalisasi (Moraes dkk, 2001; Philips, 1987). Keuntungan dari penggunanan metoda ini adalah mudah digunakan. Tujuan dari penelitian ini adalah: mendapatkan kristal stevisioda dari Stevia rebaudiana (Bert.) dengan metode kristalisasi, menetapkan kadar steviosida dalam larutan di setiap tahap
kristalisasi secara Kromatografi Cair Kinerja Tinggi (KCKT), menetapkan kadar tertinggi steviosida dalam kristal secara KCKT.
2. Bahan dan Metode
BahanSampel yang digunakan adalah daun Stevia rebaudiana (Bert.) yang diperoleh dari Tawangmangu, Kabupaten Karanganyar, Jawa Tengah. Bahan kimia yang digunakan diantaranya adalah aquades, eter, etanol, heksan, kaolin, CaO (Merck), asam sitrat, asetonitril (J.T. Baker 9017-03), metanol (Merck 1.06009.2500), standar steviosida (WAKO Jepang, kemurnian 99,8%).
Alat
Sedangkan alat yang digunakan antara lain almunium, buchner, cabinet drying, cawan petri, kolf (Schott duran, made in German), corong pisah (Schott duran, made in German), erlenmeyer, gelas ukur (Pyrex), grinder (AIRLUX), kertas saring, labu ukur (Pyrex), mortar, neraca analitik (Mettler H80), penangas air (Memmert), pH meter (Hanna Hl9812, made in Romania), plat almunium (3 × 15 cm), power supply (Goldstar), rotary evaporator (Buchi R114), sentrifuge (Swing Type centrifuge Model C-40N Tomy seiko co, ltd), Kromatografi Cair Kinerja Tinggi (KCKT) (Smart Line, Knauer Advanced Scientific Instruments), spektrofotometer (Shimadzu, UVmini 1240), dan sokhlet.
Metode
Preparasi Sampel
Sampel dibersihkan dari tanah, kemudian dikeringkan dengan cabinet drying selama 24 jam dan dihaluskan menggunakan grinder.
Ektraksi Sampel Dengan Metoda Maserasi
100 gram sampel dimaserasi dengan 4 L etanol secara bertingkat (8×500 mL selama 8 jam). Kemudian residu dan filtrat dipisahkan melalui penyaringan.
Deklorofilasi
Filtrat hasil metoda maserasi dan ekstraksi berkelanjutan dipekatkan dengan rotary evaporator hingga volume menjadi setengah dari volume awal. Selanjutnya, hasil dari pemekatan ditambahkan aquades dengan perbandingan 1:1 dan penambahan 1% garam (NaCl) dari total volumenya. Elektrolisis dilakukan selama 2,5 jam dengan menggunakan plat alumunium (ukuran 3×15 cm) sebagai elektrode. Arus dan tegangan digunakan power supply adalah 0,9 A dan 16,9-31,6 V secara berurutan. Filtratnya disaring dan siap untuk perlakuan selanjutnya
Redefatisasi
Larutan hasil deklorofilasi dipisahkan dari pengotornya dengan corong pisah menggunakan pelarut eter. Langkah ini digunakan untuk memisahkan fase air yang mengandung steviosida dan fase organik sebagai pengotornya. Partisi dilakukan secara bertingkat dengan penambahan eter 2×100 mL.
Klarifikasi
Fase air hasil defatisasi diatur pH-nya menggunakan asam sitrat 50% hingga pH 3.
Kristalisasi
Larutan sampel yang telah diklarifikasi diatur kembali pH-nya menjadi pH 10,5 menggunakan larutan CaO 50%. Filtrat hasil penyaringan diatur kembali pH-nya menjadi pH 7 dengan menggunakan asam sitrat 50%. Untuk menghilangkan sisa-sisa lemak, larutan didefatisasi kembali dengan pelarut eter (1×100 mL), kemudian dipartisi dengan pelarut etil asetat secara bertingkat (5×100 mL). Fase organik diambil dan dipekatkan dengan rotary evaporator.
Setelah dipekatkan maka akan terbentuk kristal putih. Untuk memaksimalkan pembentukan kristal, maka larutan disimpan dalam lemari es semalam (0-5 °C).
Analisis Sampel
Analisis Ekstrak Kromatografi Cair Kinerja Tinggi
Identifikasi steviosida dilakukan dengan menggunakan KCKT. Sebagai fase diam KCKT adalah RP C18 dan fase geraknya adalah asetonitril, metanol, dan air dengan flow rate 1,5mL/menit. Elusi fase gerak dilakukan secara isokratik menggunakan (aquades:methanol=70:20):(acetonitril)=76:24, dan volume sampel yang diinjeksikan adalah 20μL. Deteksi pemisahan menggunakan Detektor UV Smart Line Knauer pada panjang gelombang 217nm.
Analisis Spektra Steviosida dari Ektraksi Secara Spektroskopi
Kristal steviosida dilarutkan dalam metanol. Larutan steviosida kemudian dilihat pola serapan cahayanya pada panjang gelombang 200-400 nm.
3. Hasil dan Pembahasan
Optimasi Awal Preparasi dan Ekstraksi Sampel
Ekstraksi steviosida dari Stevia rebaudiana (Bert.) telah melalui beberapa tahap antara lain ekstraksi sampel, defatisasi sampel, dan kristalisasi sampel. Ekstraksi sampel dilakukan dengan menggunakan variasi empat metode yaitu metode defatisasi-berkesinambungan (A), defatisasi-maserasi (B), nondefatisasi-berkesinambungan (C), dan nondefatisasi-maserasi (D). Keempat metode ini menggunakan pelarut etanol. Hasil penelitian Moraes dkk (2001) menunjukkan bahwa penggunaan pelarut etanol memberikan hasil yang lebih jernih bila dibandingkan dengan menggunakan air dan metanol, dan relatif aman bagi konsumsi masyarakat. Dalam penelitian ini tahap penghilangan pengotor juga dilakukan agar tidak menghambat pembentukan kristal. Proses penjernihan larutan steviosida menggunakan kaolin karena kaolin mudah didapatkan, murah, dan sangat cepat dalam mengikat pengotor yang menghambat pembentukan kristal steviosida. Selain pengotor, lemak dalam ekstrak steviosida dapat dihilangkan dengan defatisasi sampel menggunakan pelarut dietil eter secara ekstraksi cair-cair. Hasil yang didapat menunjukkan bahwa komponen-komponen non polar seperti lemak dapat terangkat dan dipisahkan.
Langkah penting lain dalam penelitian ini adalah menghilangkan pengaruh warna hijau pigmen daun dengan cara deklorofilasi menggunakan metode elektrokoagulasi selama 2,5 jam (Jumpatong dkk, 2006). Hal ini dimaksudkan supaya warna hijau dari pigmen nantinya tidak mempengaruhi visualisasi kristal saat pemisahan (Moraes dkk, 2001). Langkah deklorofilasi memiliki efektifitas penyusutan warna lebih dari 85%. Penyusutan intensitas warna diakibatkan dari pemecahan klorofil menjadi turunannya yaitu feofitin yang dikarenakan kehilangan atom Mg. Hasil ini sesuai dengan hasil penelitian Jumpatong dkk (2006) dan Martono dkk (2007) yang menyatakan bahwa deklorofilasi menghilangkan pigmen yang memperbaiki visualisasi kristal.
Setelah deklorofilasi, proses klarifikasi dilakukan dengan mengatur pH-nya menjadi 3 kemudian penambahan kaolin untuk menghilangkan sisa klorofil. Klarifikasi merupakan langkah penting karena akan memberikan kualitas visual produk yang lebih baik (Moraes dkk, 2001).
Pembentukan kristal juga dipengaruhi oleh perubahan pH larutan secara ekstrim (DuBois, 2005). Oleh karena itu, pada penelitian ini, pH larutan steviosida dirubah secara ekstrim dari pH 3 menjadi pH 10,5. Pada penelitian ini, pH larutan disesuaikan ke lingkungan asam dengan menggunakan asam sitrat 50%. Penggunaan asam sitrat ini berfungsi untuk mengikat logam, protein, dan warna sebagai pengotor agar diperoleh kristal yang lebih baik (Kumar dan Sampath, 1986).
Tabel 1. Data Kadar Steviosida %w/w Kristal.
Metoda Kadar Steviosida
Defatisasi – Berkesinambungan (A) 5,42
Defatisasi – Maserasi (B)
Nondefatisasi – Berkesinambungan (C)
10,30 -
Nondefatisasi – Maserasi (D) 9,17
Pada Tabel 1. dapat dilihat data kadar steviosida dalam kristal pada berbagai metode preparasi ekstraksi sampel yang dilakukan. Perbedaan utama antara metode A, B, C, dan D adalah pada proses ekstraksinya. Metode A dan C menggunakan suhu yang lebih tinggi (70oC) dalam waktu yang lama secara berkesinambungan. Penggunaan suhu tinggi dalam waktu yang lama secara berkesinambungan ternyata dapat menyebabkan senyawa steviosida terdegradasi dan atau berubah bentuk (Kroyer, 2010). Hal ini terlihat dari hasil penelitian yaitu pada metode A dan C memiliki kadar steviosida yang lebih rendah dibanding metode B dan D. Salah satu faktor yang harus dipertimbangkan secara aplikatif adalah efisiensi. Walaupun metode B mengandung steviosida lebih tinggi dibanding metode D, tetapi metode D lebih efisien dibanding metode B. Kadar steviosida metode D (9,17%) tidak berbeda jauh dengan metode B (10,30%). Oleh karena itu, metode D menjadi metode yang selanjutnya dioptimalkan untuk proses kristalisasi steviosida.
Analisa Steviosida Setiap Tahap Kristalisasi
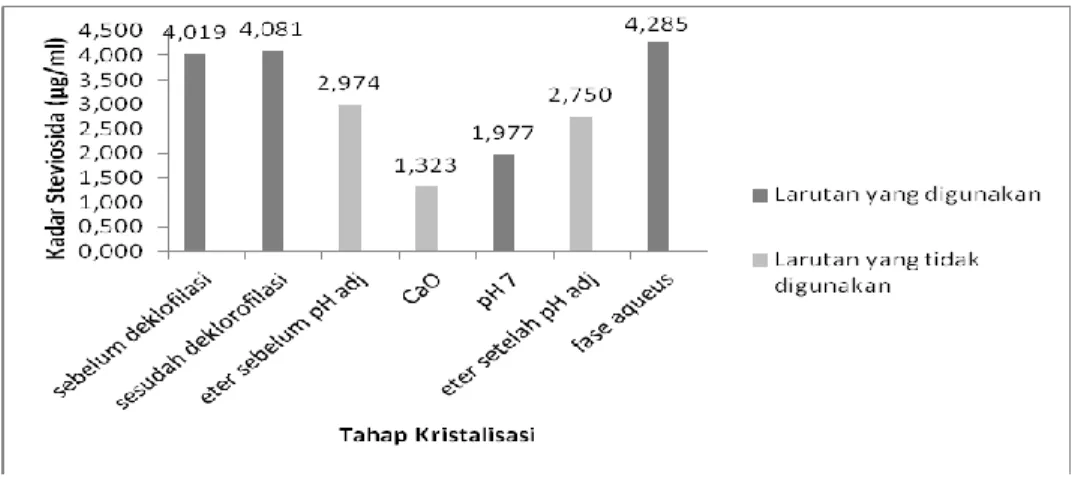
Analisa kuantitatif kadar steviosida secara KCKT juga dilakukan untuk setiap tahap kristalisasi. Pada setiap langkah dianalisa seberapa besar kadar steviosida yang masih terkandung. Data analisanya dapat dilihat pada grafik pola steviosida yang terkandung pada setiap tahap dapat dilihat pada Gambar 1. Gambar kromatogram analisa kadar steviosida dengan KCKT dapat dilihat pada Gambar 2.
Gambar 1. Grafik Analisa KCKT Steviosida Setiap Tahap Kristalisasi.
Pada Gambar 1. kadar steviosida dalam ektrak etanol sebelum deklorofilasi 4,019 µg/ml (gambar kromatrogram dapat dilihat pada Gambar 4 kromatogram [A]) tidak berbeda dengan larutan setelah deklorofilasi 4,081 µg/ml (gambar kromatrogram dapat dilihat pada Gambar 4 kromatogram [B]). Pada penelitian ini, proses deklorofilasi dapat menurunkan warna hijau larutan ekstrak sampai 99.65% (A663) dan 96.68% (A446) dimana panjang gelombang 663 dan
446 sudah mewakili klorofil sebagai pigmen hijau daun. Setelah langkah deklorofilasi larutan disaring dan dipartisi mengunakan eter.
[A]
[A] [B] [C]
[D] [E] [F]
[G]
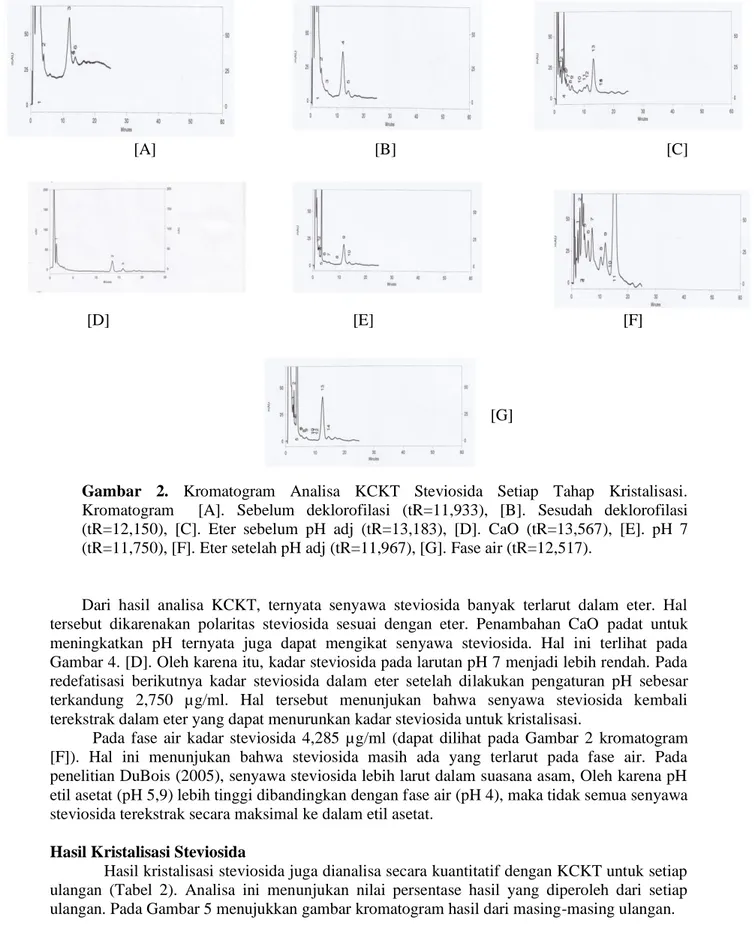
Gambar 2. Kromatogram Analisa KCKT Steviosida Setiap Tahap Kristalisasi. Kromatogram [A]. Sebelum deklorofilasi (tR=11,933), [B]. Sesudah deklorofilasi (tR=12,150), [C]. Eter sebelum pH adj (tR=13,183), [D]. CaO (tR=13,567), [E]. pH 7 (tR=11,750), [F]. Eter setelah pH adj (tR=11,967), [G]. Fase air (tR=12,517).
Dari hasil analisa KCKT, ternyata senyawa steviosida banyak terlarut dalam eter. Hal tersebut dikarenakan polaritas steviosida sesuai dengan eter. Penambahan CaO padat untuk meningkatkan pH ternyata juga dapat mengikat senyawa steviosida. Hal ini terlihat pada Gambar 4. [D]. Oleh karena itu, kadar steviosida pada larutan pH 7 menjadi lebih rendah. Pada redefatisasi berikutnya kadar steviosida dalam eter setelah dilakukan pengaturan pH sebesar terkandung 2,750 µg/ml. Hal tersebut menunjukan bahwa senyawa steviosida kembali terekstrak dalam eter yang dapat menurunkan kadar steviosida untuk kristalisasi.
Pada fase air kadar steviosida 4,285 µg/ml (dapat dilihat pada Gambar 2 kromatogram [F]). Hal ini menunjukan bahwa steviosida masih ada yang terlarut pada fase air. Pada penelitian DuBois (2005), senyawa steviosida lebih larut dalam suasana asam, Oleh karena pH etil asetat (pH 5,9) lebih tinggi dibandingkan dengan fase air (pH 4), maka tidak semua senyawa steviosida terekstrak secara maksimal ke dalam etil asetat.
Hasil Kristalisasi Steviosida
Hasil kristalisasi steviosida juga dianalisa secara kuantitatif dengan KCKT untuk setiap ulangan (Tabel 2). Analisa ini menunjukan nilai persentase hasil yang diperoleh dari setiap ulangan. Pada Gambar 5 menujukkan gambar kromatogram hasil dari masing-masing ulangan.
Tabel 2. Data Kadar Steviosida % (b/b) Kristal Tiap Ulangan. Sampel Kadar Steviosida Keterangan
Maserasi 1 0,83 kristal
Maserasi 2 0,83 karamel
Maserasi 3 20,16 kristal
Maserasi 4 33,79 karamel
Maserasi 5 7,11 kristal
Dengan metode KCKT, kita dapat mengidentifikasi kadar steviosida dalam kristal. Kadar steviosida hasil pengembangan metode maserasi – nondefatisasi dapat dilihat pada Tabel 2, dan kromatogram steviosida hasil pengembangan metode maserasi – nondefatisasi dapat dilihat pada Gambar 3.
Faktor pertama yang menyebabkan belum optimalnya proses kristalisasi steviosida pada penelitian ini adalah kadar steviosida dalam sampel tanaman yang lebih rendah pada musim penghujan, dimana berdasarkan analisa KCKT, kadar steviosida dalam sampel tanaman yang digunakan yaitu sebesar 2,31%. Padahal menurut penelitian Melis (1992), Stevia rebaudiana (Bert.), dapat mengandung steviosida hingga sebesar 3% - 8% dari berat keringnya. Faktor kedua yang menyebabkan belum optimalnya kristal yang terbentuk adalah belum maksimalnya steviosida yang terekstrak ke dalam etil asetat. Hal ini dapat dilihat bahwa masih ada steviosida yang terlarut dalam fase airnya. Faktor ketiga yang menyebabkan kristalisasi belum optimal adalah perubahan pH dari pH 3 menjadi pH 10,5 yang dapat menyebabkan steviosida berubah bentuk (Abou-Arab dkk., 2010). Hal ini disebabkan karena steviosida stabil pada pH maksimal 10 sehingga peningkatan pH larutan ke 10,5 dapat mempengaruhinya.
[C]
[A] [B] [C]
[D] [E]
Gambar 3. Kromatogram Hasil Kristalisasi Steviosida. Kromatogram [A]. Sampel 1 (tR=11,867), [B]. Sampel 2 (tR=12,467), [C]. Sampel 3 (tR=11,950), [D]. Sampel 4 (tR=12,117), [E]. Sampel 5 (tR=11,850).
tR: retention time.
4. Kesimpulan
Dari hasil yang diperoleh dapat disimpulkan bahwa metode kristalisasi yang dikembangkan dapat menghasilkan kristal steviosida. Larutan di setiap tahap kristalisasi mengandung steviosida dengan kadar antara 1.323 – 4.285 µg/ml. Kadar tertinggi steviosida dalam kristal yang diperoleh adalah 20,16% b/b.
5. Daftar Pustaka
Du Bois, G. E. 2005. SteviolmonosideAnalogs.
http://www.freepatentsonline.com/4402990.html
Jumpatong, Kanlaya. 2006. Weerachai Phutdhawong, and Duang Buddhasukh. Dechlorophyllation by Electrocoagulation.
http://www.mdpi.org
Kim KK, Sawa Y, dan Shibata H. 1996. Hydroxylation of ent-kaurenoic acid to steviol in Stevia rebaudiana Bertoni-purification and partial characterization of enzyme. Arch Biochem Biophys; 332(2):223-230
Kumar dan Sampath, 1986. Method For Recovery of Stevioside. United States Patent 4599403
Kroyer Gerhard, 2010, Stevioside and Stevia-sweetener in food: application, stability and interaction with food ingredients. Switzerland 2010
Martono, Yohanes., Hari Kristopo, Lydia Ruth Sihasale. 2007. Recovery Produk Ekstrak Steviosida sebagai Alternatif Pengganti Gula dari Stevia rebaudiana (Bert.). Salatiga, Program Penelitian Dosen Muda (dibiayai oleh dikti).
Moraes, Ĕlida de Paula., Machado, Nádia Regina Camargo Fernandes. 2001.Clarification of Stevia Rebaudiana (Bert.) Bertoni extract by adsorption in modified zeolites.
Maringáv.23, n. 6, p. 1375-1380
Mudjajanto, E.S. 2005. Keamanan Jajanan Tradisional. http://www.kompas.com/kompas-cetak/0502/17/ilpeng/1563189.htm.
Philips, K.C. 1987. Stevia: step in developing a new sweetener. In:T.H.Grenby (Ed.), Development in Sweeteners 3, Elsevier, New York, p.1.
Shibata, H., Sawa, Y., Oka, T., Sonoke, S., Kim, K.K. dan Yoshioka, M. 1995. Steviol and steviol-glycoside. Glucosyltransferase activities in Stevia rebaudiana Bertoni. Purification and partial characterization. Arch. Biochem. Biophys. 321:390-396.
Suttajit, M., Vinitketaumnuem, U., Meevatee, U. dan Buddhasukh, D. 1993Mutagenicity and Human Chromosomal Effect of Stevioside, a Sweetener From Stevia rebaudiana Bertoni. Environmental Health Perspective, 101 (Suppl.3), 53-56
Xili, L., Chengjiany, B.,Eryi X., Reiming, S., Yuenming, W., Haodong, S., dan Zhiyian, H. 1992 Chronic Oral Toxicity and Carcinogenicity Study of Stevioside in Rats. Food and Chemical Toxiology, 30, 957-965.
Yodyinguard, V. dan Bunyawong, S. 1991. Effect of Stevioside on Growth and Reproduction. Human Reproduction,6 158-165.