BAB II
TINJAUAN PUSTAKA
2.1 Human ImmunodeficiencyVirus/Acquired Immunodeficiency Syndrome dan Terapi Anti Retroviral
Acquired Immunodeficiency Syndrome (AIDS) dapat diartikan sebagai kumpulan gejala atau penyakit yang disebabkan menurunnya kekebalan tubuh akibat infeksi dari virus HIV (Human Immunodeficiency Virus). AIDS merupakan tahap akhir dari infeksi HIV. Kasus pertama AIDS dilaporkan pertama kali tahun 1981. Pada tahun 1983 virus penyebab AIDS diidentifikasi oleh Lue Montagnier, diberi nama LAV (Lymphadenopathy virus) sedangkan Robert Gallo menemukan virus penyebab AIDS pada 1984 yang dinamakan HTLV-III, selanjutnya didemontrasikan bahwa virus tersebut merupakan penyebab AIDS. Metode pemeriksaan Enzyme Linked Immunosorbent Assay (ELISA) dikembangkan pada tahun 1985, pemeriksaan ini memberikan apresiasi yang positif terhadap epidemi HIV di Amerika Serikat dan negara lainnya.1,2
Berbagai penelitian tentang HIV terus dilakukan, mulai tahun 1986 dimana HIV-2 berhasil diisolasi dari pasien AIDS di Afrika hingga. Pada tahun 1996-1997 obat HAART digunakan untuk menekan replikasi HIV. 25 tahun setelah HIV diidentifikasi, pada tahun 2008 Luc Montagnier menerima penghargaan nobel atas penelitian yang berhasil mengisolasi HIV dari pasien dengan limfadenopati.19
tersedia pemeriksaan CD4. Dimana stadium lanjut didefinisikan sebagai kadar CD4 < 350 sel/mm3 tanpa memandang stadium klinis.21
2.1.1 Etiologi
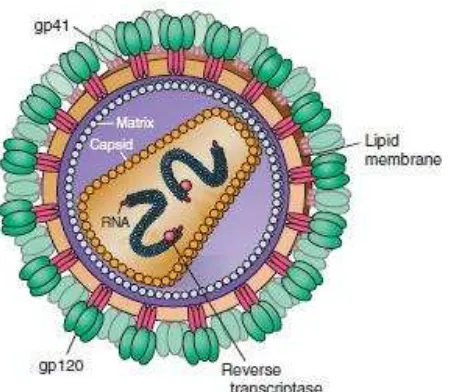
Human Immunodefiency Virus adalah virus sitopatik yang diklasifikasikan dalam famili Retroviridae, subfamili Lentivirinae, genus Lentivirus. Berdasarkan strukturnya (Gambar 1) HIV termasuk famili retrovirus, suatu virus ribonucleic acid (RNA) dengan berat molekul 9.7 kD (kilo Dalton) dan memiliki diameter 120 nm.21,22
Virus ini terdiri dari dua salinan RNA berantai tunggal yang mengkode sembilan gen tertutup (gag, pol, vif, vpr, vpu, env, rev, tat dan nef) dan terdiri dari 2.000 kopi protein virus p24 dikelilingi oleh kapsid. Kapsid dikelilingi oleh selubung virus (envelope). Selubung virus terdiri atas dua lapis membran lipid, dimana masing-masing unit selubung virus terdiri atas dua protein membran non kovalen yaitu glycoprotein 120 (gp120) dan glycoprotein 41 (gp41).1, 22
Gambar 2.1 Struktur HIV-1. Membran luar gp120, komponen transmembran gp41, RNA genom, enzim reverse transkriptase, p18 (17) membran dalam
2.1.2. Status Imunologi
Patogenesis infeksi HIV berhubungan dengan penurunan jumlah limfosit-T yang mengandung reseptor CD4. Agar dapat terjadi infeksi HIV, diperlukan reseptor spesifik pada sel host yaitu molekul CD4. Diantara sel tubuh yang memiliki molekul CD4 paling banyak adalah sel limfosit-T. Status imunologi penderita HIV dapat dinilai dengan mengukur jumlah absolut (per mm3 darah) atau persentase dari sel CD4, dan ini dianggap sebagai pemeriksaan standar untuk menilai dan menentukan derajat imunosupresi yang berhubungan dengan infeksi HIV. Penurunan progresif dari CD4 sel-T berhubungan dengan progresifitas infeksi HIV dan peningkatan resiko infeksi oportunistik serta manifestasi klinis lainnya, termasuk wasting syndrome dan kematian.6, 21
Tabel 2.1 Hubungan kadar CD4 dengan derajat imunosupresi.22
Derajat Imunosupresi Kadar CD4
Imunosupresi tidak signifikan >500 sel/mm3
Imunosupresi ringan 350-499 sel/mm3
Imunosupresi sedang 200-349 sel/mm3
Imunosupresi berat <200 sel/mm3
2.1.3. Siklus Hidup HIV
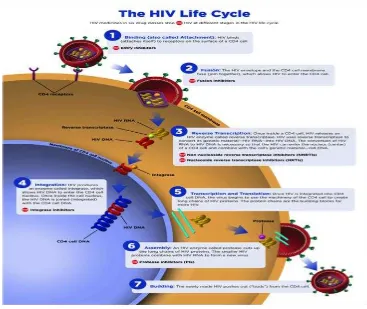
kopi dari genom HIV, juga rantai yang lebih pendek dari RNA yang disebut messenger RNA (mRNA) dimana digunakan sebagai blueprint untuk menghasilkan rantai panjang dari protein HIV. Enzim HIV yang disebut protease memotong rantai panjang protein HIV menjadi protein-protein yang lebih kecil. Ketika protein HIV yang lebih kecil bersatu dengan kopi dari gen RNA HIV maka partikel virus baru terbentuk. Virus yang baru terbentuk dikeluarkan dari sel host. Selama pengeluaran, virus baru mengambil bagian dari lapisan luar amplop sel. Amplop ini yang bertugas untuk melapisi dan mengandung glikoprotein HIV yang penting bagi virus untuk mengikat CD4 dan ko-reseptor. Kopi baru HIV kemudian sudah dapat pindah dan menginfeksi sel lainnya.23
Gambar 2.2. Siklus hidup HIV23
2.1.4. Stadium klinis
penderita saat diagnosis HIV ditegakan dan follow-up penatalaksanaan, serta menjadi pedoman untuk memulai terapi profilaksis kotrimoxazol dan/atau intervensi lainnya yang berhubungan dengan infeksi HIV, termasuk kapan memulai terapi ARV. Stadium klinis berhubungan dengan angka harapan hidup, prognosis dan progresifitas penyakit tanpa terapi ARV.8, 21
Tabel 2.2 Penilaian Stadium klinis infeksi HIV pada dewasa8, 21
Stadium klinis 1 Asimptomatis
Limfadenopati generalisata persisten
Stadium klinis 2
Penurunan berat badan <10%
ISPA berulang, sinusitis, tosilitis, otitis media dan faringitis Herpes zoster
Luka disekitar bibir (keilitis angularis) Ulkus mulut berulang
Ruam kulit yang gatal (seboroik atau prurigo-PPE (Pruritic papular eruption))
Dermatitis seboroik Infeksi jamur kuku
Stadium klinis 3
Penurunan berat badan >10%
Diare, demam yang tidak diketahui penyebabnya, lebih dari 1 bulan Kandidosis oral atau vaginal
Oral hairy leukoplakia
TB Paru dalam 1 tahun terakhir
Infeksi bakterial yang berat (pneumonia, piomiositis, dll) TB limfadenopati
Pneumonia pnemosistis, pnemonia bakterial yang berat berulang Herpes simpleks ulseratif lebih dari satu bulan
Kandidosis esofageal
histoplasmosis ekstra paru, cocidiodomikosis
Limfoma serebral atau B-cell, non-Hodgkin (gangguan fungsi neurologis tanpa sebab lain seringkali membaik dengan terapiARV)
Kanker serviks invasive Leismaniasis atipik meluas
Gejala nefropati atau kardiomiopati terkait HIV
2.1.5. Kriteria Diagnosis
Pemeriksaan laboratorium untuk mengetahui secara pasti apakah seseorang terinfeksi HIV sangat penting, karena pada infeksi HIV gejala klinisnya dapat baru terlihat setelah bertahun-tahun lamanya pada tabel berikut ini.
Tabel.2.3 Gejala dan tanda klinis yang patut diduga infeksi HIV8
Keadaan Umum
Kehilangan berat badan > 10% dari berat badan dasar
Demam (terus menerus atau intermiten, temperatur oral >37,5 oC) yang lebih dari satu bulan
Diare (terus menerus atau intermiten) yang lebih dari satu bulan Limfadenopati meluas
Kulit
PPE dan kulit kering yang luas merupakan dugaan kuat infeksi HIV. Beberapa kelainan seperti kutil genital (genital warts), folikulitis dan psoriasis sering terjadi pada ODHA tapi tidak selalu terkait dengan HIV
Infeksi
Infeksi Jamur Kandidosis oral *
Dermatitis seboroik
Kandidosis vagina kambuhan
Infeksi viral Herpes zoster (berulang atau melibatkan lebih dari satu dermatom)
Herpes genital (kambuhan) Moluskum kontagiosum Kondiloma
Gangguan Pernapasan
Batuk lebih dari satu bulan Sesak napas
TB
Pneumonia kambuhan Sinusitis kronis atau berulang
Gejala neurologis Nyeri kepala yang semakin parah (terus menerus dan tidak jelas
penyebabnya) Kejang demam
Menurunnya fungsi kognitif *Keadaan tersebut merupakan dugaan kuat terhadap infeksi HI
terhadap HIV yaitu Rapid Test digunakan untuk mengetahui dan menentukan antigen HIV-1 atau HIV-2 secara kualitatif. Western Blot merupakan Imunobolting yang digunakan untuk menentukan kadar relative dari suatu campuran berbagai jenis protein atau molekul lain. Tes ELISA digunakan untuk menyaring pasien HIV, biasanya digunakan untuk mendeteksi HIV-1 tipe M,N, dan O serta HIV-2, dimana hasil ELISA yang positif harus dikonfirmasi dengan satu kali tes atau lebih tes menggunakan darah yang sama. Kriteria diagnostik bervariasi pada setiap tes. Hasilnya yaitu positif atau negatif dengan 3 metode berbeda. PCR dan pemeriksaan untuk mendeteksi keberadaan virus HIV yaitu dengan isolasi dan biakan virus, deteksi antigen dan deteksi materi genetik dalam darah pasien.
Prosedur pemeriksaan laboratorium untuk HIV sesuai dengan panduan nasional yang berlaku pada saat ini, selalu didahului dengan konseling pra-tes atau informasi singkat. Setelah dinyatakan terinfeksi HIV maka pasien perlu menjalani serangkaian pemeriksaan yang meliputi penilaian stadium klinis, penilaian imunologis (pemeriksaan jumlah CD4) dan pemeriksaan laboratorium lainnya sebelum memulai terapi.8, 21
2.1.6 Terapi Antiretroviral
Setelah ditemukannya virus HIV berbagai upaya telah dilakukan untuk menghambat ataupun menyembuhkan penyakit ini. Berbagai terapi baru AIDS dapat segera diaplikasikan pada pasien, mengingat sifat penyakit ini yang memiliki morbiditas dan mortalitas tinggi. Ditemukannya obat golongan NRTI yang mampu memperbaiki masa hidup penderita AIDS, namun belum mampu mengeradikasi virus secara total. Dengan diperkenalkannya kombinasi obat golongan protease inhibitor (PI) dengan NRTI yang dikenal sebagai HAART digunakan untuk menekan replikasi HIV, maka saat ini penyakit AIDS tidak lagi sefatal dulu selama pengobatan dilakukan secara teratur dan dalam jangka waktu yang panjang.8
ditujukan terhadap risiko efek samping, terjadinya resistensi terhadap ARV lini pertama, ketersediaan cadangan obat dan tidak tersedianya regimen lini kedua.7
Untuk memulai terapi antiretroviral perlu dilakukan pemeriksaan kadar CD4 (bila tersedia) dan penentuan stadium klinis infeksi HIVnya. Hal tersebut adalah untuk menentukan apakah penderita sudah memenuhi syarat terapi antiretroviral atau belum.8
Peraturan Menteri Kesehatan tahun 2014 merekomendasikan pemberian ARV terhadap :
- Inisiasi ART pada orang terinfeksi HIV stadium 3 dan 4, atau jika jumlah
CD4 ≤γ50 sel/mm3
tanpa memandang stadium klinis.
- Inisiasi ART tanpa melihat stadium klinis WHO dan berapapun CD4:
Koinfeksi TB
Koinfeksi Hepatitis B
Ibu hamil dan menyusui terinfeksi HIV
Orang terinfeksi HIV yang pasangannya HIV negatif (pasangan serodiskordan), untuk mengurangi resiko penularan.
LSL, PS, Waria, atau Penasun.
Populasi umum pada daerah dengan epidemi HIV meluas.
Selama pemberian terapi ARV, perlu dilakukan pemantauan klinis dalam pengawasan dokter minimal sebulan sekali selama 6 bulan pertama, selanjutnya dapat dilakukan minimal 3 bulan sekali atau lebih sering.3
kombinasi dari beberapa obat ARV. Penggunaan tiga atau lebih obat ARV dikenal sebagai terapi HAART. Terdapat lebih dari 20 obat ARV dan tersedia untuk regimen kombinasi. Masing-masing memiliki cara yang berbeda dalam merusak atau menghambat HIV:24,25
2.1.6.1 Reverse Transcriptase Inhibitors
Reverse transcriptase adalah suatu enzim yang dibutuhkan HIV untuk menginfeksi sel inang dan mereproduksi dirinya. Reverse Transcriptase Inhibitor berfungsi untuk memperlambat produksi dari enzim transcriptase dan membuat HIV tidak dapat menginfeksi sel dan menduplikasi sel-selnya. Golongan obat reverse transcriptase ini terdiri dari :
Nucleoside Reverse Transcriptase InhibitorsObat Nucleoside Reverse Transcriptase Inhibitors (NRTIs) juga dikenal sebagai nukleoside analog adalah obat jenis pertama untuk menghambat HIV. Obat golongan ini dikenal sejak tahun 1987.
Non- Nucleoside Reverse Transcriptase Inhibitors
Obat Non-Nucleoside Reverse Transcriptase Inhibitors (NNRTIs) mulai dikenal pada tahun 1997. Obat golongan ini secara umum dikenal sebagai non-nukleosid.
Nukleotide Reverse Transcriptase Inhibitors
Hanya ada satu jenis obat golongan ini yaitu tenovovir. Obat ini bekerja dengan cara mencegah enzim reverse transcriptase, namun dengan cara yang berbeda dengan obat reverse transcriptase lain.
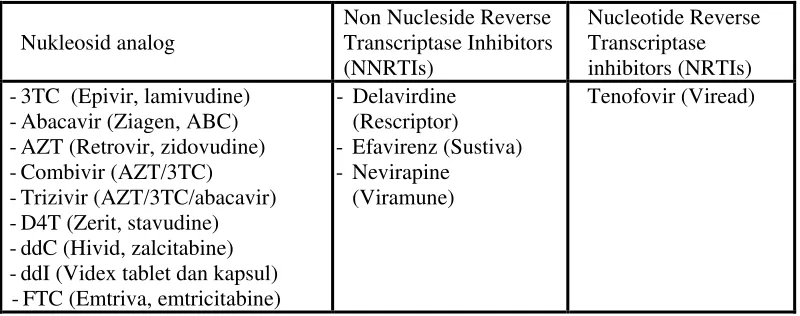
Tabel 2.4. ARV golongan Reverse Transcriptase Inhibitors
Nukleosid analog
-3TC (Epivir, lamivudine)
-Abacavir (Ziagen, ABC)
-ddI (Videx tablet dan kapsul)
2.1.6.2 Protease Inhibitor (PI)
Jenis kedua dari obat ARV adalah Protease Inhibitor (PI), diperkenalkan pertama kali tahun 1995. PI menghambat protease yaitu suatu enzim digestif yang berfungsi untuk memecah protein dan merupakan salah satu dari banyak enzim yang digunakan oleh HIV untuk menduplikasikan dirinya. Enzim protease pada HIV berperan untuk merusak dan memotong rantai protein menjadi potongan-potongan kecil. Potongan ini kemudian digunakan oleh HIV untuk menduplikasi diri dan menginfeksi sel lainnya. PI berperan dalam mencegah sebelum enzim protease dalam HIV merusak dan memotong rantai enzim dan protein. Ini adalah cara protease untuk menghambat proses duplikasi dari virus dan mencegah HIV menginfeksi sel-sel baru.
Tabel 2.5 Obat Protease Inhibitor
Protease Inhibitor (PI)
- Amprenavir (Agenerase)
- Atazanavir (Reyataz)
- Indinavir (Crixivan)
- Lopinavir/ritonavir (Kaletra)
- Nelfinavir (Viracept)
- Ritonavir (Norvir)
- Saquinavir (Fortovase (soft gel) Invirase (hard gel))
- Tipranavir (PNU)
2.1.6.3 FusionInhibitor (FI)
2.1.6.4 Co-reseptor Antagonist
Sebagai tambahan untuk reseptor CD4, HIV juga membutuhkan ko-reseptor untuk memasuki target sel. Pada pertengah tahun 1990 ditemukan dua buah reseptor yaitu reseptor CXCR4 dan reseptor CCR5. Reseptor-reseptor ini, yang diduga lebih dari 200, dinamakan berdasarkan natural chemokines yang biasanya mengikat mereka. Varian HIV menggunakan kedua reseptor ini untuk masuk ke sel target. Varian HIV disebut R5 apabila menggunakan CCR5 sebagai ko-reseptornya, sedangkan virus yang menggunakan CXCR4 disebut virus X4. Virus R5 adalah virus yang didominasi dengan menginfeksi makrofag, sedangkan virus X4 terutama menginfeksi sel-T. Pada kebanyakan pasien, virus R5 ditemukan pada awal-awal stadium infeksi, virus X4 lebih mematikan dan dapat menginfeksi sel dengan spektrum yang lebih luas, muncul pertama kali pada stadium lanjut.
2.1.6.5 Integrase Inhibitors
Integrase inhibitor pertama kali dikenal mulai tahun 2000. Tahun 2005
studi klinis berkembang dengan cepat sehingga akhirnya integrase inhibitor menjadi kelas obat baru yang menjanjikan dalam pengobatan HIV. Tiga enzim utama dalam siklus replikasi HIV-1 yaitu integrase, reverse transkriptase dan protease. Enzim ini mengandung 288 asam amino, terlibat dalam integrasi virus DNA ke host genome, dan penting untuk proliferasi HIV. Integrasi virus DNA memiliki 4 langkah yang semuanya dihambat oleh integrase inhibitor yang berbeda:
Pengikatan integrase inhibitor pada sitoplasma terhadap virus DNA, sehingga membentuk kompleks pre-integrasi yang stabil (langkah ini dapat dicegah dengan pyranodipyridimine sebagai integrase-DNA-binding inhibitor).
Proses γ’: sebuah langkah katalik awal, integrase memotong
Strand transfer. Integrase mengikat host DNA terjadi setelah
kompleks pre-integrasi diubah dan ditransfer ke dalam nukleus sel melalui pori-pori nuklear. Hal ini memediasi ikatan irreversibel ujung hydroxyl dari virus DNA terhadap jembatan phosphodiesterase host DNA (langkah ini dihambat 2 integrase inhibitor yaitu raltegravir dan elvitegravir), yang disebut strand transfer inhibitor (STI).
Gap repair. Kombinasi dari virus DNA dan host DNA yang
merupakan produk menengah dengan gap, yang dapat diperbaiki dengan enzim perbaikan sel host.
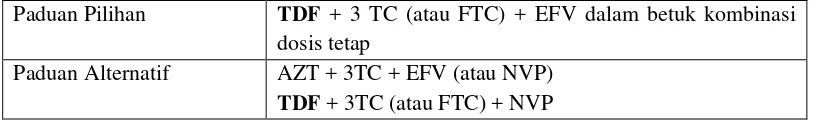
Berdasarkan Pedoman Nasional Tatalaksana HIV 2014 di Indonesia, pemerintah menganjurkan pengobatan antiretroviral lini pertama adalah 2 NRTI + 1 NNRTI, dengan salah satu dari paduan dibawah ini:
Tabel 2.6 Panduan ARV lini pertama.3
Paduan Pilihan TDF + 3 TC (atau FTC) + EFV dalam betuk kombinasi
dosis tetap
Paduan Alternatif AZT + 3TC + EFV (atau NVP)
TDF + 3TC (atau FTC) + NVP
2.2 Mikroalbuminuria
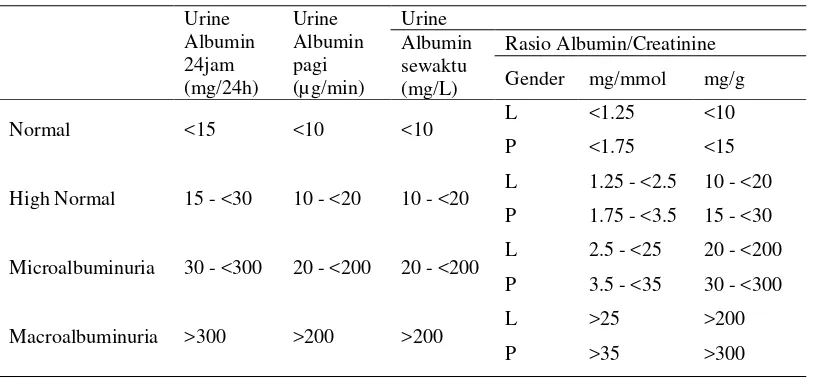
Pada keadaan normal, albumin yang diekskresikan pada urin tidak melebihi 30 mg/hari. Bila kadar albumin pada urin antara 30-300mg/hari atau 30-350 mg/hari disebut mikroalbuminuria. Biasanya sering ditemukan pada pasien diabetes melitus, hipertensi esensial dan beberapa penyakit glomerulonefritis (misalnya glomerulonefritis proliferative mesangial diffuse). Mikroalbuminuria merupakan suatu marker (petanda) untuk proteinuria klinis yang disertai penurunan faal ginjal atau laju filtrasi glomerulus (LFG) dan penyakit kardiovaskular sistemik.9, 26
albuminuria pada awal diagnosis dan pencegahan penyakit ginjal dan kardiovaskular sangat penting ditinjau dari sudut demografi dan epidemiologi pada negara-negara berkembang.17, 27
Albuminuria tidak hanya merupakan pertanda resiko penyakit kardiovaskular dan penyakit ginjal, tetapi juga berguna sebagai target keberhasilan pengobatan. Hipotesis mengapa mikroalbuminuria dihubungkan dengan resiko penyakit kardiovaskuar adalah karena adanya disfungsi endotel yang luas. Tetapi belum jelas apakah mikroalbuminuria secara spesifik berhubungan dengan kegagalan sintesis nitric oxide pada individu-individu dengan atau tanpa diabetes melitus. Beberapa penelitian telah membuktikan adanya peranan kegagalan sintesis nitric oxide pada sel endotel yang berhubungan antara mikroalbuminuria dengan resiko penyakit kardiovaskular.9, 27, 28
Tabel 2.7 Klasifikasi Albuminuria abnormal.29 Urine
Macroalbuminuria >300 >200 >200 L P
>25
>35
>200
>300
2.3 Hubungan Tenofovir dan Mikroalbuminuria 2.3.1 Farmakologi Tenofovir
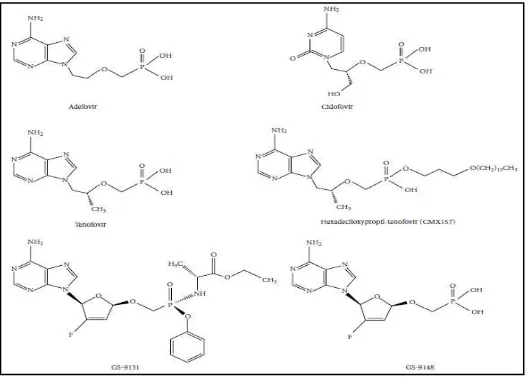
(HPMP) untuk cidofovir, fosfonometoksietil (PME) untuk adefovir dan fofonometoksipropil (PMP) untuk tenofovir. Tenofovir difosfat adalah analog struktural dari deoksiadenosin 5’-trifosfat, yang merupakan substrat yang biasa untuk viral DNA-directed DNA polymerase dan inhibitor lemah dari DNA α dan
polimerase sertamitokondrial DNA -polimerase.9,28
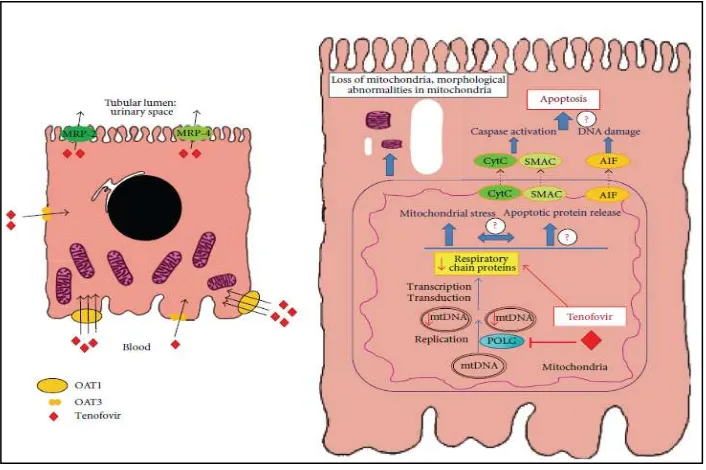
Tenofovir dieliminasi secara utuh didalam urine melalui kombinasi filtrasi glomerular dan sekresi tubulus proksimal. 20-30% obat tersebut secara aktif ditransport ke dalam sel tubulus proksimal oleh transporter anion organic (hOAT1) dalam membran basolateral. Kemudian obat tersebut akan disekresikan ke lumen tubulus oleh transporter membran apikal MRP-4 dan MRP-2. Sejumlah obat-obat dapat berinteraksi dengan transporter ini dan dapat menyebabkan berlebihnya obat yang masuk atau pengurangan outflow obat yang menyebabkan akumulasi intraselular dan meningkatkan toksisitas ginjal.9,30
Gambar 2.3. Struktur kimia dari asiklik nukleotide analogue, adefovir, cidofovir dan tenofovir.9
2.3.2 Patogenesis Nefrotoksisitas akibat Tenofovir
Presentasi klinik nefrotoksisitas tenofovir yang utama adalah disfungsi tubulus proksimal dengan fungsi ginjal yang masih dapat dipertahankan (preserved) dan penurunan fungsi ginjal. Penurunan fungsi ginjal dapat diklasifikasikan sebagai AKI, CKD atau penurunan Glomerular Filtration Rate (GFR) dibandingkan baseline meskipun dalam batas normal. Kasus yang paling banyak dilaporkan dari nefropati yang berhubungan dengan tenofovir adalah sindroma Fanconi parsial atau komplit dengan atau tanpa penurunan GFR. Sindrom Fanconi merupakan tubulopati proksimal menyeluruh, dan bentuk komplitnya berhubungan dengan asidosis tubular renal, glikosuria dengan normoglikemia, aminoasiduria, hipofosfatemia, hipourisemia dan tubular proteinuria. Disfungsi tubular dapat menyebabkan penurunan fungsi ginjal.9,11,31
Proteinuria tubular memperlihatkan peningkatan jumlah protein ukuran kecil pada urine yang secara bebas difiltrasi di tubulus yang kemudian akan direabsorbsi oleh proksimal tubulus. 2-mikroglobulinuria sering ditemukan pada pasien yang diobati dengan tenofovir, meskipun dengan GFR yang normal. Manifestasi lain dari tubulopati proksimal meliputi osteomalasia dan penurunan massa tulang akibat phosphate wasting dan/atau defisiensi kalsitriol, karena kalsitriol diproduksi oleh tubulus proksimal.9,10,13