SENYAWA TERPENOID HASIL ISOLASI DARI DAUN LADA
(Piper nigrum, Linn) DAN UJI BIOAKTIVITASNYA
TERHADAP HAMA Callosobruncus chinensis
Syaiful Bahri dan Rinawati
Jurusan Kimia FMIPA Universitas Lampung
Jl. S. Brojonegoro No.1 Bandar Lampung 35145
E-mail: muzaki@maiser.unila.ac.id
Diterima 8 Juli 2005, perbaikan 25 November 2005, disetujui untuk diterbitkan 2 Desember 2005
ABSTRACT
The isolation of terpenoid from pepper leaves (Piper nigrum, Linn) has successfully been performed. The compound (3 mg) was isolated by the use of 100 % chloroform eluen with the RF of 0.46 as white crystal. The compound shows activity against Callosobruncus chinensis. Based on the infrared and the mass spectrometry spectra, the compound obtained is classified as sesquiterpen containing the main functional groups of –OH and C=C, with the relative molecular mass of 220 m/e. The bioactivity test of this compound against Callosobruncus chinensis on mung bean leaves showed that the compound causing not only to the death of the plant diseases but also reducing the feeding activity with the contact time of 72 hours.
Keywords: pepper leaves, terpenoid, bioactivity, Callosobruncus chinensis
1. PENDAHULUAN
Dewasa ini ketergantungan petani akan penggunaan insektisida sintetik untuk menanggulangi hama cukup tinggi bila dibandingkan dengan insektisida botani. Padahal penggunaan insektisida tersebut umumnya dapat berpengaruh buruk bagi lingkungan dan dapat mengakibatkan hama menjadi resisten terhadap insektisida tersebut, akhir-akhir inipun harga pestisida sintetik relatif mahal dan terkadang sulit untuk memperolehnya. Untuk itu perlu dicari tumbuh-tumbuhan yang memiliki khasiat insektisida khususnya yang mudah diperoleh dan dapat diramu sebagai sediaan insektisida1 untuk pengendalian hama gudang yang efektif dan tidak berpengaruh buruk terhadap manusia dan lingkungannya2.
Lada merupakan salah satu tanaman yang mengandung senyawa terpenoid sekitar1 – 4 %. Penggunaan lada sebagai sumber potensial insektisida botani pernah dilaporkan oleh Arnason (1993) dan Isman (1995)1 sedangkan daun lada dilaporkan pula dapat digunakan sebagai insektisida terhadap ngengat dalam lemari pakaian3. Daya insektisidal yang terdapat dalam buah lada cukup efektif untuk melindungi produk pertanian misalnya digunakan sebagai pencegah daya makan (antifeedant) terhadap hama gudang1. Pengendalian hama gudang (Callosobruncus chinensis) dengan menggunakan daun lada merupakan salah satu contoh penggunaan
insektisida botani yang memiliki sifat mudah terurai (biodegradable)4 di alam sehingga tidak mencemari lingkungan dan relatif aman bagi manusia karena residunya mudah hilang. Insektisida tersebut juga bersifat pukul dan lari, yaitu apabila diaplikasikan akan membunuh hama pada waktu itu setelah hamanya terbunuh maka residunya akan cepat menghilang di alam5.
Hingga saat ini informasi tentang pemanfaatan daun lada sebagai sumber insektisida botani masih sangat terbatas, sehingga perlu diadakan penelitian tentang pemanfaatan daun lada tersebut. Penelitian ini bertujuan mengisolasi dan meng-identifikasi senyawa terpenoid pada daun lada dan menguji sifat bioaktivitas terhadap hama gudang Callosobruncus chinensis pada biji kacang hijau.
2. METODE PENELITIAN
2.1. Persiapan sampel
Sampel daun lada diambil dari Way Kanan. Daun lada yang diperoleh kemudian dibersihkan dari kotoran yang menempel dan kemudian dikeringkan pada suhu kamar. Setelah kering sampel daun lada digiling untuk mendapatkan ukuran yang lebih kecil.
2.2. Proses isolasi dan pemurnian
aseton selama 2 x 24 jam. Hasil perendaman kemudian disaring untuk mendapatkan filtrat. Filtrat tersebut lalu dipekatkan dengan penguap putar vakum hingga diperoleh ekstrak kental. Ekstrak kental tersebut kemudian dipartisi dengan menggunakan pelarut n-heksana : H20 (1 : 1). Fasa n-heksana diambil dan dipekatkan dengan penguap putar vakum. Kemudian dilakukan uji KLT dengan eluen n-heksana dan kloroform, plat KLT tersebut dilihat pada lampu UV kemudian disemprot dengan pereaksi Liebermann-Burchad untuk mengetahui letak senyawa terpenoid. Setelah itu dilakukan uji bioaktif dengan menggunakan hama gudang Callosobruncus chinensis dan bahan uji biji kacang hijau
2.3. Pemisahan dengan Kromatografi Kolom
Ekstrak kental hasil partisi dimasukkan ke dalam kolom dan dielusi dengan pelarut mulai dari n-heksana, kloroform, metanol dan perbandingan dari pelarut-pelarut tersebut. Dari hasil pemisahan fraksi-fraksi tersebut kemudian dilakukan uji KLT dan uji bioaktif untuk mendapatkan fraksi yang aktif dan mengandung senyawa terpenoid. Untuk memurnikan fraksi yang diperoleh dari hasil kromatografi kolom ,
Uji bioaktif dilakukan dengan tujuan mengetahui pengaruh daun lada sebagai insektisida5. Uji bioaktif dilakukan pada semua fraksi hasil setiap tahapan pemurnian. Pengujian bioaktivitas dilakukan dengan metode percobaan makan. Pengamatan mortalitas hama uji dilakukan setiap 6 jam sekali sampai didapatkan fraksi aktif yaitu
2.5. Identifikasi Senyawa Terpenoid
Sampel yang telah diisolasi kemudian
diidentifikasi dengan metode spektroskopi, yaitu spektroskopi UV-Vis, IR dan GC-MS.
3. HASIL DAN PEMBAHASAN
Hasil perendaman daun lada disaring sehingga didapatkan filtrat yang kemudian dipekatkan dengan penguap putar yang bertujuan memekatkan filtrat dengan suhu (30 – 400C dan putaran 60
rpm) rendah menggunakan bantuan vakum sehingga senyawa-senyawa dalam filtrat relatif aman dari kerusakan akibat pemanasan yang berlebihan. Dari hasil pemekatan didapatkan ekstrak kental sebanyak 50 gram. Ekstrak kasar aseton yang diperoleh dipartisi dengan menggunakan n-heksana : air (1 : 1). Partisi ini bertujuan untuk memperkecil pola penyebaran range komponen senyawa hasil maserasi berdasarkan kelarutannya. Setelah didiamkan beberapa saat kemudian akan didapatkan 2 lapisan yang selanjutnya dipisahkan dan dihasilkan fasa n-heksana dan fasa air. Pada kedua fasa tersebut diuji dengan pereaksi Liebermann-Burchard. Pada fasa air tidak terbentuk endapan yang mencirikan terdapatnya senyawa terpenoid, sedangkan pada fasa n-heksana ternyata didapatkan endapan berwarna ungu sehingga fasa inilah yang dilanjutkan ketahap berikutnya.
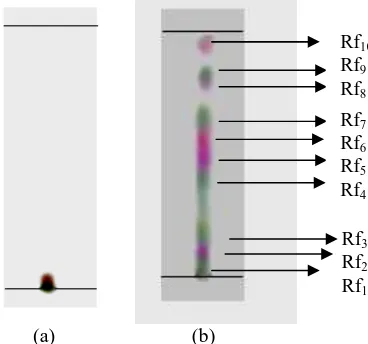
Fasa n-heksana yang didapat kemudian dipekatkan dengan penguap putar vakum sehingga didapatkan crude n-heksana sebanyak 10 gram. Selanjutnya dilakukan uji KLT menggunakan plat KLT dengan SiO2 sebagai fasa diam. Dari hasil KLT fasa n-diberikan pada Gambar 1.
(a) (b)
Gambar 1. Hasil KLT Crude n-heksana Hasil Partisi (a) Eluen n-heksana 100 % (b) Eluen CHCl3 100 %
Hal itu menunjukkan bahwa dalam ekstrak n-heksana terkandung sedikitnya 10 komponen senyawa dan dengan pereaksi Liebermann-Burchard dapat dilihat adanya senyawa terpenoid pada bercak noda dengan Rf2, Rf5, Rf6, Rf8 dan Rf10 ditandai dengan terbentuknya warna ungu, merah jambu dan ungu kemerahan.
3.1. Pemisahan dengan Kromatografi Kolom
Pemisahan komponen senyawa pada crude n-heksana dilakukan menggunakan kromatografi kolom dengan fasa diam silika gel 60 dan fasa gerak menggunakan cara elusi landaian dimulai dengan pelarut n-heksana, kloroform, dan perbandingan dari pelarut tersebut terakhir menggunakan pelarut metanol. Dari hasil penampungan kolom kromatografi didapatkan 5 fraksi yaitu fraksi n-heksana (1), fraksi n-heksana : CHCl3 (2), fraksi CHCl3 (3), fraksi CHCl3 : MeOH (4) dan fraksi MeOH (5). Hasil kromatografi kolom fasa n-heksana diberikan pada Tabel 1.
Hasil fraksi-fraksi tersebut dipekatkan dengan penguap putar vakum, kemudian diambil sejumlah cuplikan dan dilarutkan dengan aseton untuk uji bioaktif terhadap hama Callosobruncus chinensis untuk mengetahui fraksi yang bersifat aktif.
Dari hasil uji bioaktivitas yang disajikan pada Tabel 2. dapat dilihat bahwa fraksi n-heksana : CHCl3 dan fraksi CHCl3 bersifat aktif. Pada fraksi n-heksana : CHCl3 mempunyai sifat aktif terhadap hama uji tetapi tidak mengandung senyawa terpenoid sedangkan fraksi CHCl3 merupakan fraksi yang aktif terhadap hama gudang Callosobruncus chinensis dan mengandung senyawa terpenoid ditandai dengan adanya bercak noda yang berwarna ungu kemerahan. Fraksi CHCl3 memiliki keaktifan terhadap hama Callosobruncus chinensis dengan waktu kontak selama 24 jam untuk dapat mematikan semua hama uji pada lima kali pengulangan.
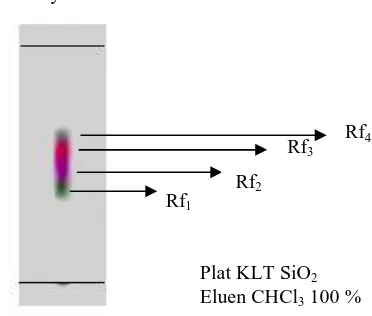
Hasil KLT pada fraksi CHCl3 menunjukkan bahwa dalam fraksi tersebut masih terdapat 4 komponen senyawa dengan harga Rf masing-masing senyawa adalah Rf1 = 0,41, Rf2 = 0,46, Rf3 = 0,5 dan Rf4 = 0,61. Pada Rf = 0,46 dan Rf = 0,5 diidentifikasi sebagai senyawa terpenoid karena berwarna ungu kemerahan dan merah jambu setelah disemprot dengan Liebermann-Burchard, maka komponen
yang berada pada Rf tersebut menjadi target isolasi berikutnya.
Plat KLT SiO2 Eluen CHCl3 100 %
Gambar 2. Hasil KLT Senyawa Fraksi CHC3
Untuk memisahkan senyawa yang menjadi target isolasi dari komponen yang lain dilakukan kembali kromatografi kolom dengan menggunakan silika gel 60 sebagai fasa diam dan fasa gerak n-heksana, kloroform, perbandingan pelarut-pelarut yang digunakan dan MeOH. Hasil rekolom dari fraksi CHCl3 dapat dilihat pada Tabel 3.
Dari hasil rekolom fraksi CHCl3 didapatkan 4 fraksi. Pada fraksi-fraksi tersebut kemudian diuji bioaktivitas dan uji terpenoid. Didapatkan senyawa target berada difraksi 3.3 dengan eluen CHCl3 : MeOH dan setelah diuji bioaktivitas ternyata fraksi tersebut aktif terhadap hama gudang Callosobruncus chinensis, hasil uji bioaktif diberikan pada Tabel 4.
Hasil KLT fraksi 3.3 diberikan pada Gambar 3. Dari gambar tersebut dapat dilihat hasil KLT rekolom fraksi 3.3 bercak noda yang dihasilkan sudah satu spot tetapi masih agak memanjang sehingga perlu dilakukan lagi kromatografi kolom terhadap fraksi tersebut untuk mendapatkan senyawa target yang lebih murni.
Tabel 1. Hasil Kromatografi Kolom Crude n-heksana
Fraksi Eluen Warna Fraksi Hasil Uji
Bioaktif Uji Terpenoid
1. n-heksan Kuning pekat - +
2. n-heksan : CHCl3 Hijau pekat - +
3. CHCl3 100 % Kuning kemerahan + +
4. CHCl3 : MeOH Hijau kehitaman + +
5. MeOH 100% Hitam - -
Keterangan : + = Hasil uji aktif / terdapat terpenoid
- = hasil uji tidak aktif / tidak mengandung terpenoid
Rf2 Rf1
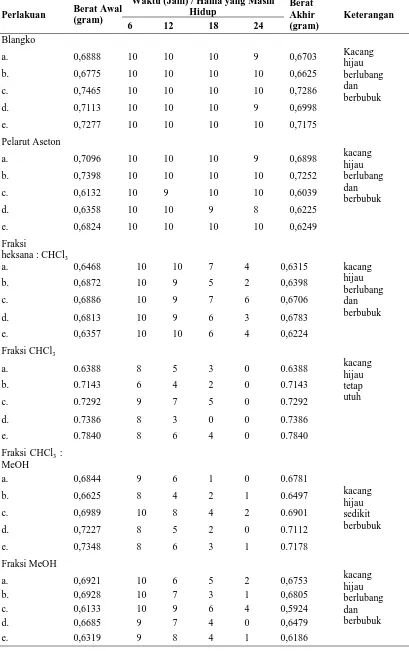
Tabel. 2. Data Hasil Uji Bioaktif Kromatografi Kolom Fase n-heksana
Perlakuan Berat Awal (gram)
Waktu (Jam) / Hama yang Masih Hidup
Berat Akhir (gram)
Keterangan
6 12 18 24
Blangko
Kacang hijau berlubang dan berbubuk
a. 0,6888 10 10 10 9 0,6703
b. 0,6775 10 10 10 10 0,6625
c. 0,7465 10 10 10 10 0,7286
d. 0,7113 10 10 10 9 0,6998
e. 0,7277 10 10 10 10 0,7175
Pelarut Aseton
kacang hijau berlubang dan berbubuk
a. 0,7096 10 10 10 9 0,6898
b. 0,7398 10 10 10 10 0,7252
c. 0,6132 10 9 10 10 0,6039
d. 0,6358 10 10 9 8 0,6225
e. 0,6824 10 10 10 10 0,6249
Fraksi heksana : CHCl3
kacang hijau berlubang dan berbubuk
a. 0,6468 10 10 7 4 0,6315
b. 0,6872 10 9 5 2 0,6398
c. 0,6886 10 9 7 6 0,6706
d. 0,6813 10 9 6 3 0,6783
e. 0,6357 10 10 6 4 0,6224
Fraksi CHCl3
kacang hijau tetap utuh
a. 0.6388 8 5 3 0 0.6388
b. 0.7143 6 4 2 0 0.7143
c. 0.7292 9 7 5 0 0.7292
d. 0.7386 8 3 0 0 0.7386
e. 0.7840 8 6 4 0 0.7840
Fraksi CHCl3 : MeOH
kacang hijau sedikit berbubuk
a. 0,6844 9 6 1 0 0.6781
b. 0,6625 8 4 2 1 0.6497
c. 0,6989 10 8 4 2 0.6901
d. 0,7227 8 5 2 0 0.7112
e. 0,7348 8 6 3 1 0.7178
Fraksi MeOH
kacang hijau berlubang dan berbubuk
a. 0,6921 10 6 5 2 0,6753
b. 0,6928 10 7 3 1 0,6805
c. 0,6133 10 9 6 4 0,5924
d. 0,6685 9 7 4 0 0,6479
Tabel 3. Hasil Rekolom Fraksi Kloroform (CHCl3)
Fraksi Eluen Warna Fraksi Hasil Uji
Bioaktif Uji Terpenoid 3.1 heksana 100 %,
n-heksana : CHCl3
Kuning muda - -
3.2 CHCl3 100 % Kuning - -
3.3 CHCl3 : MeOH Kuning kemerahan ++ +
3.4 MeOH 100 % Kuning + +
Keterangan : ++ = Hama mati semua
+ = Hama masih ada yang hidup - = Hama masih bayak yang hidup
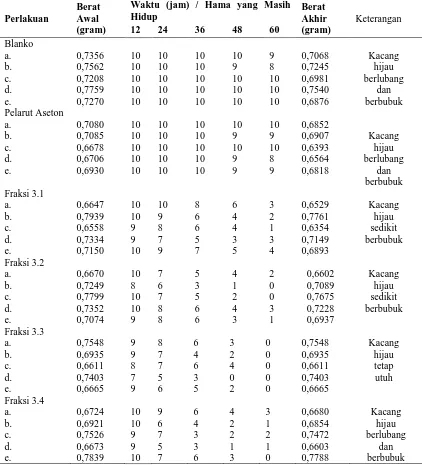
Tabel 4. Data Hasil Uji Bioaktif Fraksi 3 (CHCl3)
Perlakuan
Berat Awal (gram)
Waktu (jam) / Hama yang Masih Hidup
Berat Akhir (gram)
Keterangan
12 24 36 48 60
Blanko
Kacang hijau berlubang
dan berbubuk
a. 0,7356 10 10 10 10 9 0,7068
b. 0,7562 10 10 10 9 8 0,7245
c. 0,7208 10 10 10 10 10 0,6981
d. 0,7759 10 10 10 10 10 0,7540
e. 0,7270 10 10 10 10 10 0,6876
Pelarut Aseton
Kacang hijau berlubang
dan berbubuk
a. 0,7080 10 10 10 10 10 0,6852
b. 0,7085 10 10 10 9 9 0,6907
c. 0,6678 10 10 10 10 10 0,6393
d. 0,6706 10 10 10 9 8 0,6564
e. 0,6930 10 10 10 9 9 0,6818
Fraksi 3.1
Kacang hijau sedikit berbubuk
a. 0,6647 10 10 8 6 3 0,6529
b. 0,7939 10 9 6 4 2 0,7761
c. 0,6558 9 8 6 4 1 0,6354
d. 0,7334 9 7 5 3 3 0,7149
e. 0,7150 10 9 7 5 4 0,6893
Fraksi 3.2
Kacang hijau sedikit berbubuk
a. 0,6670 10 7 5 4 2 0,6602
b. 0,7249 8 6 3 1 0 0,7089
c. 0,7799 10 7 5 2 0 0,7675
d. 0,7352 10 8 6 4 3 0,7228
e. 0,7074 9 8 6 3 1 0,6937
Fraksi 3.3
Kacang hijau tetap utuh
a. 0,7548 9 8 6 3 0 0,7548
b. 0,6935 9 7 4 2 0 0,6935
c. 0,6611 8 7 6 4 0 0,6611
d. 0,7403 7 5 3 0 0 0,7403
e. 0,6665 9 6 5 2 0 0,6665
Fraksi 3.4
a. 0,6724 10 9 6 4 3 0,6680 Kacang
b. 0,6921 10 6 4 2 1 0,6854 hijau
c. 0,7526 9 7 3 2 2 0,7472 berlubang
d. 0,6673 9 5 3 1 1 0,6603 dan
Plat KLT SiO2 Eluen CHCl3 100 %
Gambar 3. Hasil KLT Rekolom Fraksi 3.3
Pada tahap pemurnian ini, hasil tampungan dilakukan setiap 1 ml per botol sampel dengan menggunakan eluen n-heksana : CHCl3, CHCl3, CHCl3 : MeOH dan MeOH. Dari hasil kolom didapatkan hasil penampungan sebanyak 210 botol sampel dan tiap botol diuji KLT dan disemprot dengan pereaksi Liebermann-Burchard. Berdasarkan hasil KLT yang dilihat dari harga Rf bercak noda yang terbentuk didapatkan 6 fraksi. Setelah didiamkam selama beberapa hari pada masing-masing fraksi terbentuk kristal berbentuk jarum. Kristal yang terbentuk tiap fraksi memiliki bentuk yang hampir sama dan memiliki nilai Rf yang memiliki perbedaan sangat tipis. Hasil kristal terbanyak terdapat pada fraksi 3.3.4. Hasil kolom kromatografi pemurnian ini diberikan pada Tabel 5.
Pada masing-masing fraksi yang didapat dari hasil kromatografi kolom fraksi 3.3 kemudian dilakukan uji bioaktivitas terhadap hama gudang Callosobruncus chinensis. Berdasarkan hasil uji bioaktivitas yang diberikan pada Tabel 6. fraksi 3.3.4. bersifat aktif terhadap hama uji, sehingga kristal yang ada pada fraksi ini yang kemudian diidentifikasi dengan alat spektroskopi.
Pemeriksaan dengan KLT memperlihatkan bahwa senyawa target yang diperoleh selalu memberikan bercak tunggal walaupun telah digunakan berbagai
eluen dengan kepolaran yang berbeda-beda, harga Rf 0,17 dengan eluen n-heksana : CHCl3 (1 : 1) (a), Rf 0,46 dengan eluen CHCl3 100 % (b), eluen n-heksana : CHCl3 : MeOH ( 5 : 4 : 1) Rf 0,60 (c) dan Rf 0,9 dengan eluen CHCl3 : MeOH (1 : 1) (d). Kristal yang dihasilkan sebanyak 3 mg berbentuk seperti jarum dan berwarna putih. Hasil plat KLT senyawa target yang dihasilkan dengan beberapa eluen diberikan pada gambar berikut:
(a) (b) (c) (d)
Gambar 4. Hasil KLT Senyawa Hasil Isolasi (Terpenoid)
3.2. Uji Bioaktif
Hasil pengujian uji bioaktivitas Callosobruncus chinensis pada biji kacang hijau menunjukkan bahwa pada ekstrak daun lada mengandung senyawa terpenoid yang dapat menyebabkan kematian pada hama uji dan juga dapat mengurangi aktivitas makan. Hal ini dapat dilihat dari banyaknya hama yang mati dan biji kacang hijau pada fraksi yang aktif masih dalam keadaan utuh. Sedangkan biji kacang hijau pada blangko, pelarut dan fraksi yang lain menjadi berlubang dan berbubuk sehingga menyebabkan penurunan berat kacang hijau. Berkurangnya berat kacang hijau disebabkan karena selama perkembangannya larva Callosobruncus chinensis memakan kotiledon maupun embrio dari kacang hijau. Serangan yang dilakukan oleh hama ini menyebabkan kacang hijau berlubang bahkan sampai hampa (tinggal kulitnya saja) dan bobotnya menjadi ringan9.
Tabel 5. Hasil Kromatografi Rekolom Fraksi 3.3 (Fraksi CHCl3 : MeOH)
Fraksi No. Tabung Eluen Hasil Uji
Bioaktif
Uji Terpenoid
Kristal yang terbentuk
3.3.1 1 – 20 n-hek : CHCl3 - + sedikit
3.3.2 31 – 69 CHCl3 - + sedikit
3.3.3 76 – 84 CHCl3 + + cukup banyak
3.3.4 88 – 151 CHCl3 : MeOH + + banyak
3.3.5 159 – 173 MeOH - + sedikit
Gambar 5. Spektrum IR Senyawa Hasil Isolasi
Gambar 6. Spektrum massa Senyawa Hasil Isolasi
3.3. Identifikasi dengan Spektroskopi Infra Merah
Pemeriksaan spektrum infra merah dari senyawa terpenoid yang diperoleh, memberikan pita-pita serapan pada bilangan gelombang 3317,3 cm -1 (s) merupakan serapan dari uluran – OH. Serapan pada 2931,6 cm -1 (k) yang didukung dengan serapan pada 1458,1 cm -1 (s) merupakan uluran metil, pada bilangan gelombang 2862,2 cm -1 merupakan uluran =C-H dan serapan di daerah sidik jari pada 1373,2 cm -1 menunjukkan uluran - CH2. Pada 1643,2 cm -1 (l) yang didukung oleh serapan di daerah sidik jari pada 887,2 cm -1 (l) merupakan uluran C=C yang terdapat dalam struktur lingkar. Serapan di daerah sidik jari pada 1126,4 cm -1 (s) merupakan serapan dari C-O (Sastrohamidjojo, 1990). Data hasil pengukuran spektroskopi IR diberikan pada Gambar 5.
3.4. Identifikasi dengan Spektroskopi Massa
Dari hasil pengukuran spektroskopi massa didapatkan senyawa dengan berat molekul 220 m/e dengan puncak dasar (100 %) adalah 43. Senyawa dengan berat molekul 220 diduga memiliki rumus molekul C15H24O. Jumlah ekivalen ikatan rangkap
dalam rumus molekul tersebut dapat dihitung berdasarkan rumus DBE dan dihasilkan sebanyak 4 buah ekivalen ikatan rangkap, yaitu 3 buah lingkar (siklik) dan 1 buah ikatan rangkap C=C7. Adanya gugus – OH pada struktur dugaan dibuktikan dengan adanya puncak 202 m/e pada data MS dimana ion molekul melepaskan molekul netral H2O dan didukung dengan adanya serapan pada bilangan gelombang 3317,3 cm-1 pada data IR. Gugus metil dilihat dari munculnya puncak 205 m/e dimana ion radikal metil dilepaskan dari ion molekul dan juga puncak 187 m/e setelah pelepasan H2O dan gugus metil dari ion molekul, dari data IR gugus metil ditunjukkan dengan adanya serapan pada 2931,6 cm-1 dan 1458,1 cm-1. Adanya ikatan rangkap pada siklik ditunjukkan dengan adanya serapan pada 1643,2 cm-1 dan 887,2 cm-1. Ikatan =C-H pada ikatan rangkap ditunjukkan dengan adanya peak pada 2862,2 cm-1. Hasil pengukuran Spektroskopi Massa diberikan pada Gambar 6.
4. KESIMPULAN DAN SARAN
terpenoid dari daun lada (Piper nigrum, Linn) yang bersifat bioaktif terhadap hama Callosobruncus chinensis berupa kristal berwarna putih sebanyak 3 mg dengan harga Rf 0,46 menggunakan eluen CHCl3 100 %. Dari hasil analisis spektroskopi IR dan Spektroskopi Massa diperkirakan senyawa hasil isolasi merupakan senyawa terpenoid jenis seskuirterpenoid dengan gugus-gugus fungsi utama OH dan C=C serta berat molekul relatif 220 m/e.
Adapun saran yang dapat diberikan dari hasil penelitian ini adalah sebagai berikut : agar didapatkan senyawa hasil isolasi yang memiliki kemurnian lebih tinggi dilakukan pengukuran dengan menggunakan HPLC, perlu dilakukan pengukuran lebih lanjut dengan NMR agar dapat menentukan struktur molekul senyawa terpenoid yang didapat dari daun lada (Piper nigrum, Linn) secara pasti. Perlu dilakukan uji bioaktivitas terhadap hama Callosobruncus chinensis dengan menggunakan beberapa taraf konsentrasi sehingga dapat dihitung LC50 (Lethal Concentration).
DAFTAR PUSTAKA
1. Suprapto dan Nurjanah, N. 2001. Daya Insektisida Buah Lada Terhadap Beberapa Hama Gudang. J. Sains Tek.7(3): 141-146.
2. Idris, A.B dan E. Garfius. 1993. Pesticides Affect Immature Stangst of Diadegme Insulare (Hymenoptra: Plutellidea) and it’s
Host, The Diamondbackmoth (Lepidoptera: Plutellidea). J. Econ. Ento. 48 (6): 435-411.
3. Bahri, S. dan Rinawati. 2005. Isolasi Senyawa Alkaloid pada buah lada dengan uji aktifitas terhadap hama beras (Sithopilus oryzae L). J. Ilmiah MIPA. VIII(1): 42-47
4. Arnason, B.J.R., I. M Gagnon, N. Lesage, L.egrave. 2005. Efficacy of Botanical Insecticides from Piper Species (Piperaceae) Extracts For Control of European Chafer (Coleoptera: Scarabaeidae). J. Econ. Ento. 98 (3): 845-855(11)
5. Isman, M. 2002. Pesticide Outlook, J. Royal Soc. Chem. 10.1039/b206507j: 30-37.
6. SAS Institut. 1990. SAS/STAT User’s Guide, Version 6, Fourth Edition, Volume 2. North Carolina. SAS Institut Inc.
7. Hamid, A., Y. Nuryani. 1992. Kumpulan Abstrak Seminar dan Lokakarya Nasional Etnobotani, Bogor. Dalam S. Riyadi, A. Kuncoro, dan A.D.P. Utami. Tumbuhan Beracun. Malang : Balitnas.
8. Rismunandar. 2001. Lada, Budidaya dan Tata Niaganya. Penebar Swadaya. Jakarta. Halaman 6-34.