DARI MINYAK JELANTAH MELALUI
TRANSESTERIFIKASI YANG DIBANTU
GELOMBANG ULTRASONIK
Oleh
Viffit Desiyana
Skripsi
Sebagai salah satu syarat untuk mencapai gelar SARJANA TEKNOLOGI PERTANIAN
Pada
Jurusan Teknik Pertanian
Fakultas Pertanian Universitas Lampung
FAKULTAS PERTANIAN
UNIVERSITAS LAMPUNG
PENGARUH RASIO MOLAR DAN WAKTU REAKSI TERHADAP HASIL DAN MUTU BIODISEL DARI MINYAK JELANTAH MELALUI TRANSESTERIFIKASI YANG DIBANTU GELOMBANG ULTRASONIK
Oleh
Viffit Desiyana
Biodiesel merupakan senyawa alkil ester yang diproduksi melalui proses alkoholisis (transesterifikasi) antara trigliserida dengan metanol atau etanol dengan bantuan katalis basa. Tujuan penelitian yang ini adalah untuk mengetahui pengaruh rasio molar dan waktu reaksi terhadap hasil dan mutu biodisel dari minyak jelantah melalui proses transesterifikasi yang dibantu gelombang
ultrasonik pada frekuensi 42 kHz. Penelitian ini dilakukan menggunakan minyak jelantah yang diperoleh dari pabrik kerupuk di Sukarame, Bandar Lampung. Bahan kimia yang digunakan adalah metanol teknis dan NaOH teknis sebagai katalis.
Penelitian dilakukan dengan dua faktor, yaitu waktu reaksi dan rasio molar. Faktor waktu reaksi terdiri dari tiga taraf yaitu 5 menit, 10 menit dan 30 menit, dan faktor rasio molar metanol terhadap minyak jelantah terdiri dari tiga level, yaitu 3:1, 4,5:1, dan 6:1. Semua perlakuan dilakukan dengan tiga kali ulangan. Hasil penelitian menunjukkan bahwa pemberian gelombang ultrasonik dapat menghilangkan proses pemanasan dan pengadukan pada transesterifikasi konvensional. Produksi biodiesel berkisar antara 55,67 – 70,67 % dengan
karakteristik massa jenis 0,86 – 0,94 kg/liter dan viskositas 4,16 – 8,07 cSt. Secara statistic rasio molar dan lama reaksi berpengaruh nyata terhadap rendemen dan bilangan asam biodiesel tetapi tidak berpengaruh nyata terhadap viskositas dan massa jenis biodiesel. Rasio molar 4,5:1 dan waktu raksi 10 menit menghasilkan nilai rendemen biodiesel terbaik sebesar 64,33 %. Biodiesel yang dihasilkan berpotensi dapat digunakan sebagai pengganti bahan bakar pada kompor minyak tanah.
Halaman
DAFTAR ISI ... v
DAFTAR TABEL ... vii
DAFTAR GAMBAR ... ix
DAFTAR LAMPIRAN ... xi
I. PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Tujuan Penelitian ... 3
1.3 Manfaat Penelitian ... 4
1.4 Kerangka Pemikiran ... 4
1.5 Hipotesis ... 5
II. TINJAUAN PUSTAKA ... 6
2.1 Energi Alternatif... 6
2.2 Biodiesel ... 9
2.3 Minyak Goreng Bekas atau Minyak Jelantah ... 13
2.4 Proses Produksi Biodiesel ... 17
2.4.1 Proses esterifikasi ... 18
2.4.2 Proses transesterifikasi ... 21
2.5 Pemanfaatan Gelombang Ultrasonik... 24
III. METODE PENELITIAN ... 27
3.1 Waktu dan Tempat ... 27
3.2 Alat dan Bahan ... 27
3.4.3 Pembuatan larutan metoksi untuk proses
transesterifikasi ... 30
3.4.4 Proses produksi biodiesel ... 31
3.4.5 Diagram alir ... 34
3.5 Pengujian Biodiesel ... 35
3.5.1 Analisis rendemen biodiesel ... 35
3.5.2 Analisis massa jenis ... 35
3.5.3 Analisis bilangan asam ... 36
3.5.4 Analisis viskositas ... 36
3.6 Analisis Data ... 37
IV. HASIL DAN PEMBAHASAN 4.1 Karakteristik Minyak jelantah ... 38
4.2 Jumlah Katalis NaOH ... 39
4.3 Biodiesel ... 40
4.3.1 Pengaruh rasio molar dan waktu reaksi terhadap rendemen biodiesel... 42
4.3.2 Pengaruh rasio molar dan waktu reaksi terhadap massa jenis ... 44
4.3.3 Pengaruh rasio molar dan waktu reaksi terhadap bilangan asam ... 47
4.3.4 Pengaruh rasio molar dan waktu reaksi terhadap viskositas biodiesel ... 49
1.1 Latar Belakang
Minyak jelantah merupakan salah satu bahan baku yang memiliki peluang untuk
produksi biodiesel karena minyak ini masih mengandung trigliserida. Data
statistik menunjukkan bahwa terdapat kecenderungan peningkatan konsumsi
minyak goreng (Departemen Pertanian, 2013). Peningkatan ini akan
menyebabkan jumlah minyak jelantah bertambah. Sementara untuk menekan
biaya produksi sebagian pedagang biasanya tidak membuang minyak jelantah
tersebut, tetapi menambahkannya dengan minyak yang baru atau minyak jelantah
digunakan sebagai bahan tambahan untuk membakar ayam atau ikan. Selain itu
minyak jelantah ada yang dimurnikan kembali dan dijadikan minyak goreng daur
ulang. Minyak jelantah yang digunakan kembali sebagai bahan makanan tidak
baik untuk kesehatan karena dapat mengakibatkan kerusakan pada hati, ginjal,
jantung dan bersifat karsinogenik (Hanif, 2009). Oleh karena itu perlu dilakukan
usaha-usaha lain dalam pemanfaatan minyak jelantah tersebut. Salah satunya
adalah sebagai bahan baku dalam produksi biodiesel.
Konversi langsung minyak jelantah atau minyak goreng bekas menjadi biodisel
sudah cukup lama dilakukan oleh para peneliti biodiesel (Freedman, et al., 1984;
proses produksi biodiesel dari minyak jelantah melalui tahapan penyaringan
minyak, tahapan esterifikasi dan transesterifikasi minyak menjadi biodiesel.
Untuk bahan baku yang mengandung asam lemak bebas (Free Fatty Acid, FFA)
tinggi seperti minyak jelantah, proses produksi biodiesel dilakukan dalam dua
tahap yaitu esterifikasi dan transesterifikasi. Proses produksi biodiesel dengan
menggunakan bahan baku minyak jelantah dengan metode transesterifikasi
menyimpulkan bahwa sifat-sifat ester dari minyak jelantah tidak berbeda jauh dari
sifat biodiesel dari minyak baru dan juga sifat minyak solar, kecuali kemampuan
untuk disaring yang tinggi karena titik bekunya yang tinggi. Tingginya titik beku
ini disebabkan oleh tingginya kandungan asam lemak jenuh. Selain itu, proses
transesterifikasi memerlukan suhu yang tinggi, pengadukan, waktu yang lama,
dan rasio molar yang berlebih. Pada proses pengolahan biodiesel umumnya
menggunakan pengadukan secara mekanis pada sistem batch dan menggunakan
pengadukan system orifice. Tahapan-tahapan panjang yang harus dilalui
menyebabkan rendahnya efisiensi energi dan tingginya konsumsi energi, yang
mengakibatkan tingginya biaya produksi biodiesel.
Penelitian ini harapkan dapat mencari alternatif lain pada reaksi transesterifikasi
tanpa input panas langsung dan tanpa pengadukan mekanis. Penggunaan
gelombang ultrasonik diharapkan dapat menghasilkan proses dengan input energi
lebih rendah untuk proses produksi biodiesel agar efisien, dengan suhu rendah dan
waktu proses lebih pendek dibandingkan dengan proses produksi biodiesel secara
konvensional (Susilo, 2007). Gelombang ultrasonik pada frekuensi rendah dapat
digunakan untuk menghasilkan emulsi dari cairan yang immiscible. Kavitasi
sangat ekstrim di mana suhu dan tekanan lokal sesaat dapat mencapai 10.0000C
dan 1000 atm (Santos dkk., 2009; Hendee dan Ritenour, 2002). Kondisi seperti
ini dapat menyebabkan radikal-radikal yang berpengaruh terhadap dekomposisi
pelarut, monomer, atau putusnya rantai polimer, sehingga radikal-radikal ini
mampu menginisiasi reaksi kimia (Xia et al., 2009). Untuk itu secara tidak
langsung gelombang ultrasonik mampu mempercepat reaksi dengan cara
menggetarkan molekul reaktan. Sehingga reaksi produksi biodiesel dapat
dilakukan pada suhu rendah dengan waktu yang singkat, dan dapat
menghasilkan konversi biodiesel yang optimum.
Berdasarkan uraian tersebut, penelitian ini dilakukan untuk mengamati proses
produksi biodiesel menggunakan bahan baku minyak jelantah melelui proses
transesterifikasi dengan bantuan gelombang ultrasonik. Proses transesterifikasi
dipengaruhi oleh beberapa faktor, antara lain frekuensi, suhu, waktu reaksi, dan
rasio molaritas pada pelarut yang digunakan. Oleh karena itu, penelitian ini
dilakukan untuk mengamati pengaruh rasio molar dan waktu reaksi terhadap hasil
dan mutu biodisel dari minyak jelantah melalui transesterifikasi yang dibantu
gelombang ultrasonik
1.2 Tujuan Penelitian
Tujuan penelitian yang ini adalah untuk mengetahui pengaruh rasio molar dan
waktu reaksi terhadap hasil dan mutu biodisel dari minyak jelantah melalui
1.3 Manfaat Penelitian
Pemanfaatan minyak jelantah yang merupakan limbah rumah tangga untuk
menghasilkan alternatif bahan bakar diesel yang dapat diperbaharui untuk
mengurangi ketergantungan terhadap bahan bakar fosil terutama bahan bakar
solar. Serta memberi informasi tentang alternatif penggunaan gelombang
ultrasonik pada proses transesterifikasi dalam produksi biodiesel.
1.4 Kerangka Pemikiran
Minyak jelantah (waste cooking oil) merupakan limbah dan mengandung
senyawa-senyawa yang bersifat karsinogenik, yang terjadi selama proses
penggorengan. Pemakaian minyak jelantah yang berkelanjutan dapat merusak
kesehatan manusia, menimbulkan penyakit kanker, dan akibat selanjutnya dapat
mengurangi kecerdasan generasi berikutnya. Hal ini memerlukan pemanfaatan
yang tepat agar limbah minyak jelantah ini dapat bermanfaat dan tidak
menimbulkan kerugian dari aspek kesehatan manusia dan lingkungan. Salah satu
bentuk pemanfaatan minyak jelantah agar dapat bermanfaat adalah dengan
mengubahnya menjadi biodiesel.
Proses reaksi transesterifikasi pada produksi biodiesel secara konvensional
memerlukan pemanasan dan pengadukan secara mekanis. Beberapa faktor
yang mempengaruhi kecepatan reaksi transesterifikasi pada proses produksi
biodiesel di antaranya adalah pengaruh air dan asam lemak bebas,
transesterifikasi trigliserida menjadi metil ester membutuhkan pengadukan
mekanis dengan suhu yang tinggi dalam waktu yang lama sehingga
memerlukan input energi yang tinggi. Secara konvensional, untuk
mengatasinya dengan meningkatkan suhu reaksi atau dengan menambahkan
kosolven. Alternatif pemecahan lain untuk mengatasinya yaitu dengan
menggunakan bantuan radiasi gelombang ultrasonik. Pada penelitian ini tidak
dilakuakn analisi biaya.
1.5 Hipotesis
Hipotesis yang digunakan pada penelitian ini adalah rasio molar dan waktu reaksi
pada proses produksi biodiesel dengan gelombang ultrasonik berpengaruh terhadap
II.
TINJAUAN PUSTAKA
2.1 Energi Alternatif
Konsumsi terhadap hasil olahan minyak bumi selalu mengalami peningkatan
setiap tahun seiring dengan meningkatnya populasi dan aktivitas penduduk dunia.
Di satu sisi, cadangan minyak fosil dunia yang saat ini menjadi sumber energi
terbesar justru cenderung menurun. Hal ini mendorong harga minyak mentah
terus melonjak dan ditambah dengan kondisi perekonomian dunia yang tidak
menentu menyebabkan ketidakstabilan harga minyak mentah di pasaran.
Pemakaian energi berbasis fosil juga memberikan dampak negatif terhadap
lingkungan terutama ditimbulkannya gas karbondioksida hasil pembakaran dapat
menyebabkan pemanasan global yang dikenal dengan efek rumah kaca
(Prihandana et all., 2006).
Kebutuhan energi dunia pada tahun 2008 mencapai 11.295 juta ton equivalen
minyak bumi. Bahan bakar fosil (BBF) merupakan sumber energi utama di
mana bahan bakar fosil memenuhi kebutuhan energi sebesar 88% keseluruhan
sumber energi. Bahan bakar fosil dipenuhi oleh 35% minyak bumi, 29%
batubara dan 24% gas alam. Bahan bakar non fosil (BBNF) disuplai dari
tenaga hidro 5% dan energi nuklir sebesar 6%. Bahan bakar fosil
CO2 mencapai 29 giga ton dan diasumsikan bahwa penyerapan CO2 hanya
12.000 giga ton selebihnya tidak dapat diserap dan ter-akumulasi di biosfera.
Bahan bakar fosil juga merupakan sumber energi yang tak dapat
diperbaharui. Dampak ekonomi akibat ketergantungan terhadap BBF dapat
dirasakan yaitu harga BBF naik secara eksponensial. Sebagai contoh premium
yang tahun 2004 harganya Rp 1.800,00/liter naik hingga Rp 6.000,00/liter pada
tahun 2010 (Mahreni, 2010).
Di berbagai negara sumber energi utama yang digunakan adalah minyak bumi.
Eksploitasi secara ekstensif dan berkepanjangan menyebabkan cadangan minyak
bumi semakin menipis, untuk itu harganya melonjak secara tajam dari tahun ke
tahun. Sumber daya energi yang berasal dari minyak bumi akan semakin menipis
persediaannya, seiring dengan bertambahnya industri yang akan mengakibatkan
peningkatan konsumsi bahan bakar minyak. Terjadinya krisis energi, khususnya
bahan bakar minyak (BBM) menyebabkan meningkatnya harga jual. Untuk
mengatasi semakin mahalnya harga minyak bumi, masyarakat dunia melakukan
berbagai cara untuk menghadapi kemungkinan krisis energi dan global warming
melalui berbagai pertemuan misalnya di Kyoto, Bali, Bangkok, dan sebagainya
(Prihandana et all., 2006).
Berbagai rekomendasi yang dikeluarkan adalah dengan penurunan emisi,
penurunan pertumbuhan ekonomi (zero growth), reboisasi, reforestrasi, dan
penggantian sumber energi yang ramah lingkungan. Berbagai altematif energi di
luar sumber fosil itu adalah tenaga matahari, angin, ombak/laut pasang, uap, panas
bumi, hingga bio-energi. Sumber energi ini diharapkan dapat mengurangi
akibatnya seperti perubahan iklim, bencana alam, dan sebagainya. Untuk itu
Indonesia perlu mencari sumber-sumber bahan bakar alternatif yang mungkin
dikembangkan (Kusdiana, 2008).
Energi terbaharukan merupakan energi yang dapat dihasilkan kembali, secara alami
atau dengan bantuan manusia. Sedangkan energi tidak terbaharukan merupakan
energi yang dapat habis sekali pakai. Klasifikasi ini harus memperhatikan aspek lain,
seperti aspek pemakaian (use) dan aspek komersial (commercial). Sumber energi, dilihat dari aspek pemakaian, terdiri atas energi primer dan energi sekunder. Dalam
rangka mengantisipasi kelangkaan energi di masa mendatang, perlu dikaji potensi
sumber energi lain terutama energi yang dapat diperbaharui. Indonesia diketahui
memiliki berbagai macam sumber energi yang dapat diperbaharui seperti energi air,
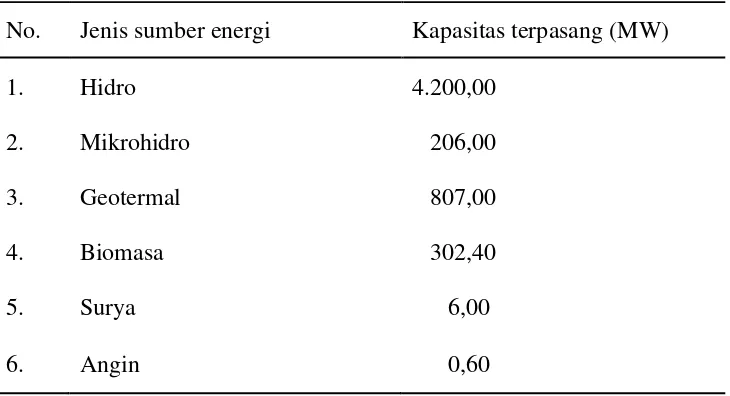
angin, matahari, panas bumi dan energi biomasa (Tabel 1). Salah satu sumber energi
biomasa yang mempunyai potensi untuk dikembangkan adalah energi biomasa yang
berasal dari minyak kelapa sawit atau disebut biodiesel, selain itu dapat juga berasal
dari jagung untuk menghasilkan bioethanol.
Tabel 1. Sumber energi terbaharukan di Indonesia
No. Jenis sumber energi Kapasitas terpasang (MW)
1. Hidro 4.200,00
2. Mikrohidro 206,00
3. Geotermal 807,00
4. Biomasa 302,40
5. Surya 6,00
6. Angin 0,60
2.2 Biodiesel
Biodiesel secara umum adalah bahan bakar mesin diesel yang terbuat dari bahan
terbaharukan atau secara khusus merupakan bahan bakar mesin diesel yang terdiri
atas ester alkil dari asam-asam lemak. Biodiesel dapat dibuat dari minyak nabati,
minyak hewani, atau dari minyak goreng bekas/daur ulang. Biodiesel merupakan
salah satu bahan bakar mesin diesel yang ramah lingkungan dan dapat
diperbaharui (renewable). Biodiesel tersusun dari berbagai macam ester asam
lemak yang dapat diproduksi dari minyak tumbuhan maupun lemak hewan.
Minyak tumbuhan yang sering digunakan antara lain minyak sawit (palm oil),
minyak kelapa, minyak jarak pagar, dan minyak biji kapuk randu, sedangkan
lemak hewani seperti lemak babi, lemak ayam, lemak sapi, dan juga lemak yang
berasal dari ikan (Handayani, 2010).
Biodiesel merupakan salah satu bahan bakar alternatif yang ramah lingkungan,
tidak mempunyai efek terhadap kesehatan yang dapat dipakai sebagai bahan bakar
kendaraan bermotor dapat menurunkan emisi bila dibandingkan dengan minyak
diesel. Biodiesel merupakan bahan bakar yang berwarna kekuningan yang
viskositasnya tidak jauh berbeda dengan minyak solar. Biodiesel memiliki
kelebihan bila dibandingkan dengan bahan bakar minyak diesel (solar) yang
diperoleh dari minyak bumi antara lain (Hanif, 2009):
1) Mempunyai sifat pelumasan yang lebih baik sehingga dapat memperpanjang
umur mesin.
2) Merupakan bahan bakar yang aman, mudah ditangani, dan tidak beracun.
Biodiesel terbuat dari minyak nabati yang berasal dari sumber daya yang dapat
diperbaharui. Beberapa bahan baku untuk pembuatan biodiesel antara lain kelapa
sawit, kedelai, bunga matahari, jarak pagar, tebu dan beberapa jenis tumbuhan
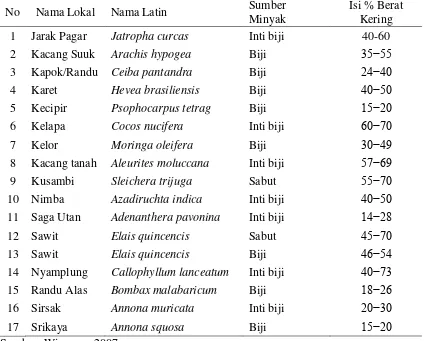
(Tabel 2) lainnya yang mengandung trigliserida (Rahayu, 2005).
Tabel 2. Tumbuhan penghasil biodiesel yang dapat dikembangkan di Indonesia
No Nama Lokal Nama Latin Sumber
Minyak
Isi % Berat Kering
1 Jarak Pagar Jatropha curcas Inti biji 40-60
2 Kacang Suuk Arachis hypogea Biji 35−55
3 Kapok/Randu Ceiba pantandra Biji 24−40
4 Karet Hevea brasiliensis Biji 40−50
5 Kecipir Psophocarpus tetrag Biji 15−20
6 Kelapa Cocos nucifera Inti biji 60−70
7 Kelor Moringa oleifera Biji 30−49
8 Kacang tanah Aleurites moluccana Inti biji 57−69
9 Kusambi Sleichera trijuga Sabut 55−70
10 Nimba Azadiruchta indica Inti biji 40−50
11 Saga Utan Adenanthera pavonina Inti biji 14−28
12 Sawit Elais quincencis Sabut 45−70
13 Sawit Elais quincencis Biji 46−54
14 Nyamplung Callophyllum lanceatum Inti biji 40−73
15 Randu Alas Bombax malabaricum Biji 18−26
16 Sirsak Annona muricata Inti biji 20−30
17 Srikaya Annona squosa Biji 15−20
Sumber: Wirawan, 2007
Biodiesel mulai mendapat perhatian dunia, terutama sebagai alternatif bahan
bakar pengganti solar yang memiliki kadar polusi yang rendah, sehingga ramah
terhadap lingkungan, dapat diperbaharui, dan mampu mendorong memberikan
nilai tambah pada sektor agribisnis. Biodiesel memiliki efek pelumasan yang
memiliki angka setana relatif tinggi, mengurangi ketukan pada mesin sehingga
mesin bekerja lebih mulus. Biodiesel juga memiliki flash point yang lebih tinggi
dibandingkan dengan solar, tidak menimbulkan bau yang berbahaya sehingga lebih
mudah dan aman untuk ditangani (Sipangkar, 2009). Biodiesel adalah salah satu
jenis biofuel (bahan bakar cair dari pengolahan tumbuhan) di samping Bioetanol.
Biofuel ramah lingkungan karena menghasilkan emisi yang lebih baik
dibandingkan dengan minyak diesel dan juga bebas belerang, memiliki
karakteristik pelumas pada mesin piston, dan juga biodegradable sehingga
menjadi energi yang tidak beracun.
Biodiesel merupakan senyawa alkil ester yang diproduksi melalui proses
alkoholisis (transesterifikasi) antara trigliserida dengan metanol atau etanol
dengan bantuan katalis basa menjadi alkil ester dan gliserol atau esterifikasi
asam-asam lemak (bebas). Biodiesel mentah (kasar) yang dihasilkan proses
transesterifikasi minyak (atau esterifikasi asam-asam lemak) biasanya masih
mengandung sisa-sisa katalis, metanol dan gliserol (air). Untuk memurnikannya,
biodiesel tersebut bisa dicuci dengan air, sehingga pengotor-pengotor tersebut
larut ke dalam dan terbawa oleh fase air pencuci yang selanjutnya dipisahkan.
Biodiesel yang sudah dicuci kemudian dikeringkan pada kondisi vakum untuk
menghasilkan produk yang jernih (pertanda bebas air) dan bertitik nyala ≥1000 C
(pertanda bebas metanol) (Musanif, 2005). Tabel 3 berikut ini memaparkan
Tabel 3. SNI-04-7182-2006: Biodiesel Quality Requirements in Indonesia
Parameter kualitas dan unit Batas Metode Uji Metode
Alternatif
Kadar Alkil ester , %-w min. 96,5 Calculated FBI-A03-03
Nilai Iodin, %-b (g-12/100g) max. 115 AOCS Cb 1-25 FBI-A04-03
Tes Halphen Negatif AOCS Cb 1-25 FBI-A06-03
Energi yang dihasilkan oleh biodiesel relatif tidak berbeda dengan petroleum
diesel (135047,149 joule vs 137157,261 joule), sehingga engine torque dan tenaga
kuda yang dihasilkan juga sama. Walaupun kandungan kalori biodiesel serupa
dengan petroleum diesel, tetapi karena biodiesel mengandung oksigen, maka flash
point yang dimiliki lebih tinggi sehingga tidak mudah terbakar. Biodiesel juga
tidak menghasilkan uap yang membahayakan pada suhu kamar, maka biodiesel
lebih aman daripada petroleum diesel dalam penyimpanan dan penggunaannya. Di
samping itu, biodiesel tidak mengandung sulfur dan senyawa bensen yang
karsinogenik, sehingga biodiesel merupakan bahan bakar yang lebih bersih dan
lebih mudah ditangani dibandingkan dengan petroleum diesel. Penggunaan
biodiesel juga dapat mengurangi emisi karbon monoksida, hidrokarbon total,
partikel, dan sulfur dioksida (Musanif, 2005).
Biodiesel dikenal sebagai bahan bakar yang ramah lingkungan dan dapat
diperbaharui. Biodiesel biasanya dibuat dengan transesterifikasi minyak
tumbuhan atau lemak hewan dengan metanol atau etanol. Biodiesel yang
diproduksi dari minyak tumbuhan atau lemak hewan biasanya lebih mahal
dibanding bahan bakar diesel konvensional dari minyak bumi. Mengingat hal
tersebut maka biodiesel dapat saja dibuat dari minyak nabati yang tidak harus
baru, seperti minyak jelantah (minyak bekas penggorengan) (Hanif, 2009).
2.3 Minyak Goreng Bekas atau Minyak Jelantah
Minyak goreng adalah minyak yang diperoleh dengan cara pemurnian minyak
tidak langsung habis dalam sekali pemakaian/penggorengan, ini lah yang
dinamakan minyak jelantah. Terkadang minyak tersisa cukup banyak terutama
pada proses penggorengan deep frying. Minyak jelantah telah mengalami
perubahan, baik sifat fisik maupun kimia, bersifat karsinogenik (racun) bagi
tubuh manusia (Ummy, 2008). Karakteristik minyak jelatah dapat dilihat pada
Tabel 4.
Tabel 4. Karakteristik dari minyak jelantah
Karakteristik Hasil analisis
Komponen non gliserida (%) 43,5
Komposisi asam lemak (%)
Minyak nabati yang dipergunakan untuk menggoreng biasanya mengandung
banyak asam lemak tidak jenuh, yaitu asam oleat dan linoleat. Minyak yang
minyak wijen, minyak bunga matahari, minyak sawit, minyak biji kapas, minyak
zaitun, dan minyak safflower. Sebagian besar minyak goreng di Indonesia berasal
dari minyak kelapa sawit. Secara umum komponen utama minyak sangat
menentukan mutu asam lemaknya, karena asam lemak dapat menentukan sifat
kimia dan stabilitas minyak. Trigliserida dari suatu minyak atau lemak
mengandung 94 96% asam lemak sehingga sebagai komponen utama yang menyusun trigliserida maka sifat fisik, kimia, dan stabilitasnya ditentukan oleh
komponen asam lemaknya. Asam lemak dominan yang terdapat pada minyak
sawit adalah asam palmitat dan asam oleat (Hanif, 2009). Struktur molekul
trigliserida dapat dilihat pada Gambar 1.
Monogliserida Digliserida Trigliserida
Gambar 1. Struktur molekul monogliserida, digliserida, dan trigliserida (Hanif, 2009)
Pemanasan minyak pada suhu tinggi dengan adanya oksigen akan mengakibatkan
rusaknya asam-asam lemak tak jenuh yang terdapat dalam minyak, seperti asam
oleat dan linoleat. Kerusakan minyak akibat pemanasan dapat dilihat dari
perubahan warna, kenaikan kekentalan, kenaikan kandungan asam lemak bebas,
esters. Kandungan FFA dan air di dalam minyak bekas berpengaruh negatif
terhadap reaksi transesterifikasi, karena Fatty Acid Methyl Ester (FAME) dan
gliserol menjadi susah untuk dipisahkan. Minyak goreng bekas lebih kental
dibandingkan dengan minyak segar disebabkan oleh pembentukan dimer dan
polimer asam dan gliserid di dalam minyak goreng bekas karena pemanasan
sewaktu digunakan. Berat molekul dan angka iodin menurun sementara berat
jenis dan angka penyabunan semakin tinggi. Selama hidrolisis, terjadi pemecahan
ikatan ester yang menghasilkan asam lemak bebas, monogliserida, dan digliserida.
Reaksi ini akan menghasilkan flavor dan bau menyengat pada minyak tersebut.
Walaupun asam lemak bebas menjadi indikator penurunan mutu pada minyak
goreng, tetapi asam lemak bebas berpotensi dalam produksi produk biokimia
dasar. Yang termasuk ke dalam produk biokimia dasar adalah fatty alcohol,
gliserol, asam lemak, dan metil ester. Semua produk biokimia tersebut
merupakan hasil dari reaksi dengan persenyawaan minyak/lemak dengan atau
tanpa bantuan katalis.
Sebagai limbah, minyak jelantah memiliki kandungan asam lemak yang cukup
tinggi. Kandungan asam lemak yang tinggi dapat menyebabkan terjadi reaksi
penyabunan. Perbedaan komposisi asam di dalam minyak bunga matahari,
minyak kedelai dan minyak goreng bekas dapat dilihat pada Tabel 5. Tabel 5
menunjukkan bahwa kandungan hampir semua asam yang ada di dalam minyak
goreng bekas lebih tinggi dibandingkan dengan di dalam minyak goreng segar
Tabel 5. Komposisi asam lemak di dalam minyak bunga matahari, minyak kedelai, dan minyak bekas.
Asam lemak Minyak Bunga
Matahari Minyak kedelai Minyak bekas
Lauric (12:0) - - 9,95
Biodiesel dapat diperoleh melalui reaksi esterifikasi asam lemak bebas atau reaksi
transesterikasi trigliserida tergantung dari kualitas minyak nabati yang digunakan
sebagai bahan baku. Transesterifikasi adalah proses yang mereaksikan trigliserida
dalam minyak nabati atau lemak hewani dengan alkohol rantai pendek seperti
metanol atau etanol (pada saat ini sebagian besar produksi biodiesel menggunakan
metanol) untuk menghasilkan metil ester asam lemak (Fatty Acids Methyl Esters /
FAME) atau biodiesel dan gliserol (gliserin) sebagai produk samping. Katalis
yang digunakan pada proses transeterifikasi adalah basa/alkali, biasanya
digunakan natrium hidroksida (NaOH) atau kalium hidroksida (KOH).
alkohol rantai pendek (metanol atau etanol) menghasilkan FAME dan air. Katalis
yang digunakan untuk reaksi esterifikasi adalah asam, biasanya asam sulfat
(H2SO4) atau asam fosfat (H3PO4). Berdasarkan kandungan FFA dalam minyak
nabati maka proses produksi biodiesel secara komersial dibedakan menjadi 2,
yaitu (Hikmah dan Zuliyana, 2010):
1) Esterifikasi dengan katalis asam (umumnya menggunakan asam sulfat) untuk
minyak nabati dengan kandungan FFA > 5% dilanjutkan dengan
transesterifikasi dengan katalis basa.
2) Transesterifikasi dengan katalis basa (sebagian besar menggunakan kalium
hidroksida) untuk bahan baku refined oil atau minyak nabati dengan
kandungan FFA < 5%.
2.4.1 Proses esterifikasi
Esterifikasi adalah reaksi di mana bahan yang mengandung asam lemak bebas
direaksikan dengan alkohol membentuk ester dan air. Esterifikasi hanya dapat
dilakukan jika umpan yang direaksikan dengan alkohol mengandung asam lemak
bebas tinggi. Selain itu, tidak diperlukan adanya tahap ekstraksi dalam proses ini
karena pada esterifikasi, alkohol berfungsi sebagai solven pengekstrak sekaligus
sebagai reaktan. Keunggulan dari proses ini adalah (Dharsono dkk., 2010):
1) Dengan memasukkan seluruh bagian ke dalam proses esterifikasi, kandungan
asam lemak dalam minyak turut berperan dalam overall yield pembentukan
2) Lemak yang teresterifikasi memiliki viskositas dan kelarutan yang berbeda
dari komponen trygliceride, sehingga dapat dengan mudah dipisahkan dari
residu padat.
3) Alkohol bertindak sebagai solven pengekstrak komponen minyak, sekaligus
reagen untuk mengesterifikasi komponen. Dengan tidak diperlukannya tahap
ekstraksi, ongkos produksi dapat ditekan seminimal mungkin dan didapatkan
produk dengan kelayakan ekonomi lebih baik.
Esterifikasi dapat dilaksanakan dengan menggunakan katalis padat (heterogen)
atau katalis cair (homogen). Berikut ini reaksi esterifikasi dengan katalis cair
berupa asam sulfat (H2SO4) menurut Dharsono dkk (2010) :
RCOOH + CH3OH RCOOCH3 + H2O
Asam lemak Metanol Metil ester Air
Faktor-faktor yang berpengaruh pada reaksi esterifikasi antara lain (Dharsono,
dkk., 2010):
1) Waktu reaksi
Semakin lama waktu reaksi maka kemungkinan kontak antar zat semakin
besar sehingga akan menghasilkan konversi yang besar. Jika kesetimbangan
reaksi sudah tercapai maka dengan bertambahnya waktu reaksi tidak akan
menguntungkan karena tidak memperbesar hasil.
2) Pengadukan
Pengadukan akan menambah frekuensi tumbukan antara molekul zat pereaksi
dengan zat yang bereaksi sehingga mempercepat reaksi dan reaksi terjadi
k = A e(-Ea/RT)……… (1) di mana: k = konstanta kecepatan reaksi (t-1)
A = faktor tumbukan (t-1)
Ea = tenaga aktivasi (cal/gmol)
R = konstanta gas umum (cal/gmol ºK)
T = suhu absolut (ºC)
Semakin besar tumbukan maka semakin besar pula harga konstanta kecepatan
reaksi, sehingga dalam hal ini pengadukan sangat penting mengingat larutan
minyak-katalis-metanol merupakan larutan yang immiscible.
3) Katalisator
Katalisator berfungsi untuk mengurangi tenaga aktivasi pada suatu reaksi
sehingga pada suhu tertentu harga konstanta kecepatan reaksi semakin besar.
Pada reaksi esterifikasi yang sudah dilakukan biasanya menggunakan
konsentrasi katalis antara 1 4 % berat sampai 10 % berat campuran pereaksi
4) Suhu reaksi
Semakin tinggi suhu yang dioperasikan maka semakin banyak konversi yang
dihasilkan, hal ini sesuai dengan persamaan Archenius. Bila suhu naik maka
nilai k makin besar sehingga reaksi berjalan cepat dan hasil konversi makin
besar.
2.4.2 Proses transesterifikasi
Reaksi transesterifikasi disebut juga dengan reaksi alkoholisis yang
gliserol sebagai produk samping. Menurut Rahayu (2005), penggunaan minyak
jelantah yang bermutu baik (kandungan asam lemak bebas lebih kecil dari 1%)
sebagai bahan baku akan mempermudah reaksi transesterifikasi. Begitu juga
sebaliknya, penggunaan minyak dengan kadar asam lemak bebas lebih dari 1%
dapat menimbulkan pembentukan sabun yang akan mempercepat proses emulsi
selama pencucian dengan air dan kandungan asam lemak bebas lebih dari 2%
maka proses tidak akan berlangsung.
Di antara alkohol-alkohol monohidrik yang menjadi kandidat sumber/pemasok
gugus alkil adalah metanol. Metanol merupakan katalis yang paling umum
digunakan, karena harganya murah dan reaktifitasnya paling tinggi (sehingga
reaksi disebut metanolisis). Jadi di sebagian besar, biodiesel praktis identik
dengan FAME. Reaksi transesterifikasi trigliserida menjadi metil ester dapat
dilihat pada gambar di bawah ini.
Gambar 2. Reaksi Transesterifikasi (Rahayu, 2005)
Transesterifikasi juga menggunakan katalis dalam reaksinya. Tanpa adanya
lambat. Katalis yang biasa digunakan pada reaksi transesterifikasi adalah katalis
NaOH, karena katalis ini dapat mempercepat reaksi. Produk yang diinginkan dari
reaksi transesterifikasi adalah ester metil asam-asam lemak. Terdapat beberapa
cara agar kesetimbangan lebih ke arah produk, yaitu (Hikmah dan Zuliyana.
2010):
1) Menambahkan metanol berlebih ke dalam reaksi.
2) Memisahkan gliserol.
3) Menurunkan temperatur reaksi (transesterifikasi merupakan reaksi eksoterm).
Tahapan reaksi transesterifikasi produksi biodiesel selalu menginginkan agar
didapatkan produk biodiesel dengan jumlah yang maksimum. Beberapa kondisi
reaksi yang mempengaruhi konversi serta perolehan biodiesel melalui
transesterifikasi adalah sebagai berikut (Freedman, et al., 1984):
1) Pengaruh air dan asam lemak bebas
Minyak nabati yang akan ditransesterifikasi harus memiliki angka asam yang
lebih kecil dari 1%. Selain itu, semua bahan yang akan digunakan harus
bebas dari air. Karena air akan bereaksi dengan katalis, sehingga jumlah
katalis menjadi berkurang. Katalis harus terhindar dari kontak dengan udara
agar tidak mengalami reaksi dengan uap air dan karbon dioksida.
2) Pengaruh perbandingan molar alkohol dengan minyak jelantah
Secara stoikiometri, jumlah alkohol yang dibutuhkan untuk reaksi adalah 3
mol untuk setiap 1 mol trigliserida untuk memperoleh 3 mol alkil ester dan 1
mol gliserol. Secara umum ditunjukkan bahwa semakin banyak jumlah
alkohol yang digunakan, maka konversi yang diperoleh juga akan semakin
adalah 98 99%, sedangkan pada 3:1 adalah 74 89%. Nilai perbandingan yang terbaik adalah 6:1 karena dapat memberikan konversi yang maksimum.
3) Pengaruh jenis alkohol
Pada rasio 6:1, metanol akan memberikan perolehan ester yang tertinggi
dibandingkan dengaan menggunakan etanol atau butanol.
4) Pengaruh jenis katalis
Alkali katalis (katalis basa) akan mempercepat reaksi transesterifikasi bila
dibandingkan dengan katalis asam. Katalis basa yang akan digunakan untuk
reaksi transesterifikasi adalah natrium hidroksida (NaOH). Katalis sejati bagi
reaksi sebenarnya adalah ion metilat (metoksida). Reaksi transesterifikasi
akan menghasilkan konversi yang maksimum dengan jumlah katalis 0,5 1,5% minyak nabati. Jumlah katalis yang efektif untuk reaksi adalah 0,5%
minyak nabati untuk natrium metoksida dan 1% minyak nabati untuk natrium
hidroksida.
5) Pengaruh jenis minyak
Perolehan metil ester akan lebih tinggi jika menggunakan minyak nabati
murni. Namun apabila produk metil ester akan digunakan sebagai bahan
bakar mesin diesel, cukup digunakan bahan baku berupa minyak yang telah
dihilangkan getahnya dan disaring.
6) Pengaruh temperatur
Reaksi transesterifikasi dapat dilakukan pada temperatur 30° 65°C (titik didih metanol sekitar 65°C). Semakin tinggi temperatur, konversi yang
2.5 Pemanfaatan Gelombang Ultrasonik
Gelombang ultrasonik adalah gelombang mekanik dengan frekuensi di atas
ambang pendengaran manusia yaitu 20 20.000 kHz. Gelombang ultrasonik merupakan rambatan energi dan momentum mekanik sehingga merambat dapat
berinteraksi dengan molekul dan sifat enersia medium yang dilaluinya.
Karakteristik gelombang ultrasonik yang melalui medium mengakibatkan getaran
partikel dengan medium amplitudo sejajar dengan arah rambat secara longitudinal
sehingga menyebabkan partikel medium membentuk rapatan (strain) dan
tegangan (stress). Hal ini disebabkan oleh getaran partikel secara periodik selama
gelombang ultrasonik melaluinya. Untuk fluida cair dan gas, osilasi partikel
searah dengan arah gelombang dan menghasilkan gelombang longitudinal
(Gambar 5.a), sedangkan pada medium padat karena memiliki regangan elastisitas
(shear elasticity), sehingga menimbulkan tegangan tangensial (tangential stress),
sehingga arah gerakan partikel tegak lurus pada arah gelombang (Gambar 5.b)
(Fajar dan Widiyawati, 2011).
(a) Longitudinal (b) Gelombang transversal
Gambar 3. Arah gelombang dan vibrasi partikel Vibrasi Partikel
Arah gelombang
Vibrasi Partikel
Gelombang ultrasonik dibangkitkan oleh suatu tranduser. Tranduser adalah
sebuah alat yang dapat mengubah satu bentuk energi ke bentuk energi lainnya,
contoh sederhananya adalah loudspeaker yang mengubah energi listrik ke energi
suara. Ultrasonik tranduser didesain untuk mengubah baik energi mekanik atau
energi listrik menjadi suara dengan frekuensi tinggi. Pada saat gelombang
ultrasonik melalui suatu medium cair, cairan tersebut akan mengalami siklus
kompresi (compression) dan ekspansi (rarefaction) (Fajar dan Widiyawati, 2011).
Gelombang ultrasonik yang dirambatkan pada cairan akan menimbulkan
gelembung mikro (microbuble). Salin itu, akan menimbulkan suatu efek yang
disebut kavitasi yaitu efek akibat ketidakseimbangan kecepatan pengadukan dan
pengembangan amplitudo. Konsekuensi normal dari pertumbuhan yang tidak
stabil dan serangkaian keruntuhan ini adalah akibat pecahnya gelembung kavitasi.
Model dinamik transestreifikasi minyak nabati dengan gelombang ultrasonik yang
dikembangkan diharapkan mampu memfasilitasi reaksi transesterifikasi. Laju
perubahan diameter gelembung diprediksi sebagai fungsi frekuensi, amplitudo,
daya, dan viskositas secara dinamik. Hasil penelitian Susilo (2007), menunjukkan
gelombang ultrasonik meningkatkan laju transesterifikasi minyak sawit menjadi
biodiesel. Konversi minyak nabati menjadi biodiesel dengan penggunaan
gelombang ultrasonik lebih tinggi dibandingkan dengan penggunaan pengaduk
mekanis. Konversi dapat mencapai 100% dengan waktu proses 1 menit.
Konversi tersebut jauh lebih tinggi dibandingkan dengan penggunaan pengaduk
mekanis yang hanya mampu pada kisaran konversi sekitar 96% dan waktu proses
ultrasonik menunjukkan waktu reaksi lebih tinggi dibandingkan dengan
penggunaan pengaduk mekanis.
Penelitian aplikasi gelombang ultrasonik untuk transesterifikasi baik dalam bentuk
eksperimen maupun pengembangan model matematika sudah banyak dilakukan
(Singh et al., 2007; Deng, at al., 2010; Fajar dan Widiyawati, 2011). Penelitian
pengolahan biodiesel sudah banyak dilakukan, tetapi penelitian yang
menggunakan bahan baku minyak jelantah dari minyak goreng yang dipakai di
Indonesia belum banyak dilakukan dalam bentuk penelitian eksperimental
khususnya untuk reaksi transesterifikasi pada proses produksi biodiesel dengan
bantuan gelombang ultrasonik. Transesterifikasi minyak nabati dengan
gelombang ultrasonik yang dikembangkan dalam penelitian ini diharapkan bisa
menerangkan efek aplikasi gelombang ultrasonik pada reaksi transesterifikasi
3.1 Waktu dan Tempat
Penelitian ini dilakukan pada bulan Juli September 2013 bertempat di
Laboratorium Pengolahan Limbah Pertanian, Jurusan Teknologi Hasil Pertanian
dan Laboratorium Teknologi Sumber Daya Air dan Lahan Jurusan Teknik
Pertanian Fakultas Pertanian Universitas Lampung, Bandar Lampung.
3.2 Alat dan Bahan
Alat-alat yang digunakan dalam penelitian ini adalah gelas ukur, timbangan,
erlenmeyer 250 ml, k o n d e n s o r , thermokopel, stopwatch, spatula,
ultrasonic cleaner (cole-parmer 8890) , falling balls viscometers, buret, stirrer,
piknometer, gelas beker, botol bening, karet silikon, pipet tetes, sentrifuser,
timbangan analitik, selang air, sarung tangan, masker, almunium foil, statif dan
klem.
Bahan yang digunakan adalah minyak jelantah yang didapat dari industri rumah
tangga pembuatan kerupuk di Sukarame, Bandar Lampung, metanol teknis, NaOH
teknis, isoprofil alkohol (IPA) teknis, air mengalir sebagai pendingin, aquadest,
3.3 Parameter Perlakuan
Penelitian ini dilakukan dengan frekuensi gelombang ultrasonik sebesar 42 KHz.
Dengan menggunakan perlakuan secara faktorial dalam rancangan kelompok
teracak lengkap dengan tiga kali ulangan (Tabel 6). Faktor pertama adalah rasio
molar* (M) yang terdiri dari tiga pebandingan yaitu volume larutan metoksi 11 ml
dengan volume minyak jelantah 100 ml untuk rasio molar 3:1 (M1), volume
larutan metoksi 16,5 ml dengan volume minyak jelantah 100 ml untuk rasio molar
4,5:1 (M2), dan volume larutan metoksi 22 ml dengan volume minyak jelantah
100 ml untuk rasio molar 6:1 (M3). Faktor kedua adalah lama waktu reaksi (L)
dengan tiga taraf yaitu 5 menit (L1), 10 menit (L2) dan 30 menit (L3).
Tabel 1. Perlakuan
Rasio molar (M)
Waktu Reaksi (L)
5 menit 10 menit 30 menit
3:1 M1L1 M1L2 M1L3
4,5:1 M2L1 M2L2 M2L3
6:1 M3L1 M3L2 M3L3
3.4 Prosedur Penelitian
Proses produksi biodiesel ini terdiri dari beberapa tahapan yaitu proses pembuatan
larutan standar 0,025 N, proses titrasi, proses pembuatan larutan metoksi untuk
reaksi transesterifikasi, dan pembuatan biodiesel.
3.4.1 Pembuatan larutan standar NaOH 0,025 N
Pembuatan larutan standar 0,025 N dilakukan dengan mencampurkan 1000 ml
aquadest ditambah dengan 1 gram NaOH. Kemudian larutan diaduk hingga
tercampur rata menggunakan stirrer. Larutan ini digunakan dalam proses titrasi
untuk menentukan kandungan asam lemak bebas yang terdapat pada minyak
jelantah maupun biodiesel. Normalitas larutan standar dihitung dengan
menggunakan rumus:
………...……… (2)
dimana: N = normalitas larutan standar NaOH (N)
V = volume air (ml)
Mr = berat molekul NaOH
3.4.2 Proses titrasi
Titrasi bertujuan untuk mengetahui banyaknya katalis yang diperlukan (X) untuk
pembuatan biodiesel dari minyak jelantah dan dihitung dari:
X = NaOHtit + 3,5 gram ………...……. (3)
Dimana NaOHtit adalah massa NaOH (gram) yang diperlukan dalam titrasi.
Sementara 3,5 gram adalah ketetapan penambahan katalis untuk minyak jelantah.
Adapun proses titrasi menurut Simanjuntak (2005) adalah:
1) Larutan standarisasi NaOH 0,025 N didapat dengan cara mencampurkan 1000
ml aquadest dengan 1 gram NaOH. Larutan diaduk hingga tercampur rata
2) Kemudian 1 ml minyak jelantah, ditambah 10 ml IPA (Isoprophyl Alcohol),
dan 2 tetes indikator dimasukkan ke dalam gelas erlenmeyer 30 ml sedangkan
larutan standar NaOH 0,025 N dimasukkan ke dalam buret yang telah
dikaitkan dengan statif dan klem.
3) Larutan pada gelas erlenmeyer dititrasi dengan menggunakan larutan standar
NaOH 0,025 N sampai larutan berwarna merah jambu dan bertahan sampai
15 detik.
4) Larutan standar NaOH yang terpakai dihitung dan dicatat hasilnya.
Proses titrasi juga bertujuan untuk menentukan kadar asam lemak bebas (FFA)
yang terkandung dalam minyak jelantah. Kadar asam lemak bebas yang
terkandung dalam minyak jelantah dapat dihitung dengan:
……. (4)
dimana: ml NaOH = jumlah ml NaOH untuk titrasi (ml)
N = normalitas larutan NaOH (mol)
BM trigliserida = bobot molekul (280,77)
= massa jenis minyak (gram/ml)
3.4.3 Pembuatan larutan metoksi untuk proses transesterifikasi
Pembuatan larutan metoksi melalui proses transesterifikasi dapat dilakukan jika
kadar FFA pada minyak jelantah lebih kecil dari 5 %, namun jika kadar FFA pada
terlebih dahulu kemudian dilanjutkan dengan proses transesterifikasi. Adapun
proses pembuatannya adalah:
1) 11 ml metanol (3 mol) dan 0,55 gram NaOH (banyaknya katalis yang
dihitung dari persamaan (3)) untuk rasio molar 3:1, 16,5 ml metanol (4,5 mol)
dan 0,55 gram NaOH untuk rasio molar 4,5:1, 22 ml metanol (6 mol) dan
0,55 gram NaOH untuk rasio molar 6:1, dimasukkan ke dalam gelas beker 50
ml yang di dalammya telah terdapat magnetic stirrer.
2) Larutan diaduk menggunakan stirrer hingga tercampur rata selama kurang
lebih 5 menit.
3) Larutan yang telah teraduk rata disimpan dalam wadah tertutup agar metanol
tidak menguap.
3.4.4 Proses produksi biodiesel
Tahapan produksi biodiesel adalah:
1) 100 ml (1 mol) minyak jelantah dimasukkan ke dalam labu erlenmeyer 250
ml (jika kandungan FFA yang terdapat dalam minyak jelantah lebih besar dari
5%, maka harus dilakukan proses esterifikasi terlebih dahulu. Larutan yang
dihasilkan dari proses esterifikasi yang akan dilanjutkan ke proses
transesterifikasi).
2) Larutan metoksi dimasukkan ke dalam minyak jelantah.
3) Labu erlenmeyer diletakkan di dalam ultrasonic cleaner. Kemudian
diatasnya ditutup menggunakan kondensor agar tidak terjadi penguapan
4) Thermokopel diletakkan di dalam lubang kondesor. Nyalakan alat ultrasonic
cleaner dengan frekuensi 42 kHz, sampai waktu yang telah dikehendaki.
Gambar 1. Rangkaian alat pada saat proses produksi biodiesel
5) Setelah proses selesai dilakukan, larutan dituangkan ke dalam botol bening
dan didiamkan selama 24 jam sampai terjadi pengendapan (pengendapan
ditandai dengan dua lapisan berbeda warna dengan lapisan gelap berada di
bawah yang disebut dengan gliserol dan lapisan atas berwarna bening yang
disebut dengan biodiesel).
Gambar 2. Hasil reaksi transesterifikasi yang telah didiamkan selama 24 jam membentuk 2 lapisan yaitu: a. Biodiesel dan b. Gliserol
6) Gliserol dan biodiesel dipisahkan dengan menggunakan pipet tetes. a
7) Biodiesel yang dihasilkan dicuci dengan menggunakan aquadest yang telah
dipanaskan dan diaduk hingga rata (pencucian bertujuan untuk membuang
sisa-sisa katalis yang masih terdapat pada biodiesel (Gerpen, 2005)).
Kemudian larutan didiamkan selama 4 12 jam. Pencucian diulangi lagi sampai air cucian berwarna bening.
8) Biodiesel dipisahkan dari air dengan menggunakan corong pemisah.
Gambar 3. Biodiesel yang telah dipisahkan dari air
9) Biodiesel yang telah dicuci diukur rendemen, massa jenis (ρ), viskositas (µ), bilangan asam, dan diuji nyalanya dengan menggunakan lampu selama 30
menit.
10) Percobaan dilakukan dengan perbandingan rasio molar dan waktu reaksi yang
bervariasi (M1L1,M1L2, M1L3, M2L1, M2L2, M2L3, M3L1, M3L2, M3L3,) dan
dilakukan masing-masing dengan 3 kali ulangan.
11) Hasil biodiesel yang diperoleh dibandingkan dengan hasil biodiesel dari
3.4.5 Diagram alir
3.5 Pengujian Biodiesel
Pengamatan yang dilakukan pada penelitian ini adalah analisis rendemen
biodiesel, analisis massa jenis, analisis viskositas, dan analisis bilangan asam
dengan prosedur pengujian sebagai berikut:
3.5.1 Analisis rendemen biodiesel
Analisis rendemen dilakukan dengan cara biodiesel dipisahkan dari gliserol yang
tersisa dalam labu pemisah selama 12 jam kemudian dicuci. Pencucian biodiesel
kotor dilakukan dengan menggunakan air hangat. Air yang masih tersisa dalam
biodiesel kemudian dipisahkan dengan menggunakan corong pemisah. Kualitas
biodiesel yang diperoleh kemudian dianalisis. Penghitungan rendemen biodiesel
dilakukan menggunakan rumus:
…… (5)
3.5.2 Analisis massa jenis
Analisis massa jenis dilakukan dengan pengukuran piknometer. Massa jenis
biodiesel dihitung dengan menggunakan rumus:
…………..……….. (6)
dimana:
ρ
Biodiesel = massa jenis biodiesel (g/ml)m = massa sampel biodiesel (g)
3.5.3 Analisis bilangan asam
1) Lakukan standarisasi NaOH 0,025 N yaitu dengan cara mencampurkan 1000
ml aquadest dengan 1 gram NaOH. Larutan diaduk hingga tercampur rata.
2) 1 ml biodiesel, ditambahkan 10 ml IPA (Isoprophyl Alcohol), dan 2 tetes
indikator PP dimasukkan ke dalam gelas erlenmeyer 30 ml sedangkan larutan
standar NaOH 0,025 N dimasukkan ke dalam buret.
3) Larutan pada gelas erlenmeyer dititrasi dengan menggunakan larutan standar
NaOH 0,025 N sampai larutan berwarna merah jambu dan bertahan sampai
15 detik (Simanjuntak, 2005).
4) Larutan standar NaOH yang terpakai dihitung dan dicatat hasilnya.
5) Dilakukan penetapan dengan rumus sebagai berikut:
…………. (7)
dimana: ml NaOH = jumlah ml NaOH untuk titrasi (ml)
N = normalitas larutan NaOH (mol)
M = berat sampel (gram)
BM NaOH = bobot molekul NaOH
3.5.4 Analisis viskositas
Alat falling ball viscometer dibersihkan dibiarkan hingga mengering. Sampel
biodiesel dimasukkan ke dalam alat tersebut secara hati-hati hingga melebihi
batas titik awal + 1 cm. Kemudian dimasukkan bola besi dengan cara
yang menetes keluar. Lalu alat diputar 180oC dan stopwatch dijalankan tepat
saat bola bergerak dari titik awal. Waktu yang dibutuhkan oleh bola tersebut
untuk bergerak hingga garis batas akhir diukur (t0). Viskositas sampel dapat
dihitung dengan rumus:
µ = –
.………... (8)
dimana: µ = viskositas (cSt)
ρbola = massa jenis bola (8,02 gram/ml)
ρbiodiesel = massa jenis biodiesel (gram/ml)
k = koefisien bola (0,01336)
t0 = waktu aliran larutan (s)
3.6 Analisis Data
Data hasil penelitian dipresentasikan ke dalam bentuk kurva dan tabel dengan
menggunakan analisis ragam dan dilakukan uji lanjut menggunakan uji beda nyata
terkecil (BNT) pada taraf 1% 5%. Pengujian yang dilakukan pada biodiesel yang dihasilan adalah analisis rendemen biodiesel, analisis massa jenis, analisis
5.1. Kesimpulan
Dari hasil penelitian yang telah dilakukan maka diperoleh kesimpulan yaitu:
1) Reaksi tranesterifikasi biodiesel dengan bantuan gelombang ultrasonik pada
frekuensi 42 kHz dapat mengurangi pengadukan dan pemanasan pada proses
produksi biodiesel.
2) Proses transesterifikasi dengan menggunakan gelombang ultasonik dengan
metanol teknis dapat menghasilkan biodiesel dengan karakteristik viskositas
dan massa jenis sesuai standar SNI.
3) Perbandingan molar metanol terhadap minyak jelantah berpengaruh nilai
rendemen biodiesel yang dihasilkan. Semakin banyak jumlah alkohol yang
digunakan, maka konversi yang diperoleh juga akan semakin bertambah.
4) Semakin lama waktu reaksi maka kontak antar zat semakin besar sehingga
akan menghasilkan konversi yang besar. Jika kesetimbangan reaksi sudah
tercapai maka dengan bertambahnya waktu reaksi tidak akan menguntungkan
karena tidak memperbesar hasil.
5) Kombinasi terbaik biodiesel berdasarkan analisis statistik didapat pada rasio
molar 4,5:1 dan waktu raksi 10 menit menghasilkan nilai rendemen biodiesel
6) Uji nyala biodiesel menghasilkan warna api orange, tidak menimbulkan asap
dan minyak dapat diserap sumbu lampu dengan baik. Daya serap sumbu
kompor pada biodiesel adalah 14 19,2 cm. Maka, biodiesel ini dapat digunakan sebagai bahan bakar penggati minyak tanah pada kompor tanpa
memodifikasi kompor tersebut.
5.2. Saran
Perlu dilakukan penelitian lebih lanjut untuk mendapatkan kondisi optimum
karakteristik biodiesel dan frekuensi yang baik untuk proses produksi biodiesel
dengan menggunakan gelombang ultrasonik. Sebaiknya dilakukan analisis lebih
lanjut terhadap parameter-parameter yang lainnya dan mengukur nilai bakar
Deng, X., Z. Fang., and Y. Liu. 2010. Ultrasonic Transesterification of Jatropha curcas L. oil to biodiesel by a two-step process. Energy conversion and management. Vol 51: 2802-2807
Departemen Pertanian. 2011. Survei Sosial Ekonomi Nasional Konsumsi Rata-rata per Kapita Setahun Beberapa Bahan Makanan di Indonesia, 2007-2011. http://www.deptan.go.id/Indikator/tabe-15b-konsumsi-rata.pdf. [22 mei 2013]
Dharsono, W., dan Y.S. Oktari. 2010. Proses Produksi Biodiesel dari Dedak dan Metanol dengan Eesterifikasi In Situ. Skripsi. Jurusan Teknik Kimia Fakultas Teknik. Universitas Diponogoro. Semarang. 64 hlm
Fajar, B., dan E. Widiyawati. 2011. Investigasi Pengaruh Kavitasi Ultrasonik pada Transesterifikasi Biodiesel (Skala Lab) untuk Pengembangan Ultrasonik Mobile Reactor. Prosiding Seminar Nasional Sains dan Teknologi ke 2. A.7 A.12
Freedman, B., E.H. Pryde., and T.L. Mounts. 1984. Variables Affecting the Yields of Fatty Esters from Transesterfied Vegetable Oils. JAOCS. Vol 61 (10). 1638-1639
Goto, S. 2008. Asia Current Status of Biodiesel Fuel in East-Asian Countries’, in Kimura, S. (ed.), Analysis on Energy Saving Potential in East Asia Region in Standardization of Biodiesel Fuel for Vehicles in East.ERIA Research Project Report 2007 6 2. 58 hlm
Handayani, P.S. 2010. Pembuatan Biodiesel dari Minyak Ikan degan Gelombang Mikro. Skripsi. Fakultas Matematika dan Ilmu Pengetahuan Alam. Universitas Sebelas Maret. 38 hlm
Hanif. 2009. Analisis Sifat Fisik dan Kimia Minyak Jelantah sebagai Bahan Bakar Alternatif Motor Diesel. Jurnal Teknik Mesin. Vol 6 (2). 92-96
Hendee, W.R., and E.R. Ritenour. 2002. Medical Imaging Physics, 4thEd., Wiley-Liss, Inc. Canada . 502 hlm
Hikmah. M.N., dan Zuliyana. 2010. Produksi Metil Ester (Biodiesel) dari Minyak Dedak dan Metanol dengan Proses Esterifikasi dan
Kheang, L.S. 1996. Recovery and Conversion Of Palm Olein Derived Used Frying Oli to Methyl Ester For Biodiesel. Jurnal of Oil Palm Research. Vol.18: 247-252
Kusdiana, D. 2008. Kondisi Riil Kebutuhan Energi di Indonesia dan Sumber-sumber Energi Alternatif Terbarukan. Direktorat Jendral Listrik dan Pemanfaatan Energi. Bogor. 37 hlm
Koran Tempo. 2009. Biodiesel Ultrasonik Agung. Edisi B4. (Rabu, 2 Desember 2009)
Mahreni. 2010. Peluang dan Tantangan Komersialisasi Biodisel-Review. Eksergi. Vol 2 (2): 15-26
Musanif, J. 2005. Biodiesel. Direktorat Pengolahan Hasil Pertanian. Ditjen Pengolahan dan Pemasaran Hasil Pertanian. 6 hlm
Nadir, D., C. Aydiner, D.Y. Ime, M. Bayramoglu, A. Tanriseven. B.
Kiskinler. 2009. Biodiesel production from sunflower, soybean, and waste cooking oils by transesterification using lipase immobilized onto a novel microporous polymer. Bioresource Technology. Vol 100: 1983–1991.
Prihandana, R., R. Hendroko dan M. Nuramin. 2006. Menghasilkan Biodiesel Murah Mengatasi Polusi dan Kelangkaan BBM. PT Agro Media Pustaka, Jakarta. 45 hlm
Putri, S.K., Supranto, dan R. Sudiyo. 2012. Studi Proses Pembuatan Biodiesel dari Minyak Kelapa (Coconut Oil) dengan Bantuan Gelombang Ultrasonik. Jurnal Rekayasa Proses. Vol. 6, (1): 147 153.
Rahayu, M. 2005. Prospek Pengembangan Bio-fuel sebagai Substitusi Bahan Bakar Minyak. Hlm 17 28
Ratno, L.J. Mawarani., dan Zulkifli. 2013. Pengaruh Ampas Tebu sebagai Adsorbent pada proses Pretreatment minyak jelantah terhadap
Karakteristik Biodiesel. Jurnal Teknik Pomits. Vol. 2 (2). 257 261 Santos, H.M., C. Lodeiro., and Capelo-Martinez J-L. 2009. The Power of
Ultrasound. In: Ultrasound In Chemistry: Analitical Applications (Editor J-L. Capelo-Martinez). Wiley-VCH Verlag GmbH & Co. KGaA, Weinheim, pp. 1-16
Setyopratomo, P., E. Purwanto., R. Hartanto., dan J. Kristianto. 2008.
Pengaruh Suhu Reaksi dan Rasio CPO/Metanol terhadap Karakteristik Produk pada Pembuatan Biodisel dengan Co-solvent Dietil Eter. Jurnal ILMU DASAR. Vol. 9(1): 72-77
Simanjuntak, M.E. 2005. Beberapa Energi Alternatif yang Terbarukan dan Proses Pembuatannya. Jurnal Teknik Simetrika. Vol. 4 (1): 287−293. Sinaga, S.V. 2013. Pengaruh Suhu dan Waktu Reaksi pada Proses Pembuatan
Biodiesel dari Minyak Jelantah. Draft Skripsi. Universitas Lampung. Bandar Lampung
Singh, A.K., S.D. Fernando., and R. Harnendez. 2007. Base –Catalyzed Fast Transesterification of Soybean Oil Using Ultrasonic. Energy and Fuels, Vol 21, (2). 1161-1164
Sipangkar, R. 2009. Analisis Pengaruh Temperatur Reaksi Dan Konsentrasi Katalis Naoh Dalam Media Etanol Terhadap Perubahan Karakteristik Fisika Biodiesel Sawit. Tesis. Sekolah Pascasarjana, Universitas Sumatra Utara. Medan. 88 hlm
Soerawidjaja, T.H. 2008. Overview of Biofuel Technologies for Indonesia. EAS Asia Biomass Seminar – Indonesia 1st Follow-up Workshop. Jakarta Sumangat, D dan T. Hidayat. 2008. Karakteristik Metil Ester Minyak Jarak Pagar
Hasil Proses Transesterifikasi Satu dan Dua Tahap. Jurnal Pascapanen. Vol 5 (2): 18-26
Susilo, B. 2007. Aplikasi Gelombang Ultrasonik untuk Pengolahan Biodiesel dari Jarak Pagar (Jatropha Curcas L.). Universitas Brawijaya. Malang. 147-153
Ummy, R.A., 2008. Kajian Proses Produksi Biodiesel dari Minyak Jelantah dengan Menggunakan Katalis Abu Tandan. Skripsi. Institut Pertanian Bogor. 71 hlm
Wirawan, S.S. 2007. Future Biodiesel Research In Indonesia. Asian Science and Technology Seminar. Institute for Engineering and Technology System Design, BPPT. 8 Maret 2007. Jakarta.
DAFTAR LAMPIRAN
Lampiran 1. Perhitungan % asam lemak bebas (FFA) dan % bilangan asam minyak jelantah
Dimana : Massa Minyak Jelantah = 1 Gram
ml NaOH = 5,23 ml
Bilangan Molekul Trigliserida = 280,77
Bilangan Molekul NaOH = 40
Maka :
1) Normalitas NaOH (N)
2) Katalis NaOH
Katalis NaOH = NaOHtit + 3,5 gram
= 1,7 + 3,5 gram
= 5,2 gram dibulatkan menjadi 5,5 gram
Karena larutan standar yang digunakan 1 liter, maka 5,5 gram katalis
NaOH yang digunakan adalah untuk 1 liter minyak jelantah. Sementara
3) Kadar Asam Lemak Bebas
4) Kadar Bilangan Asam
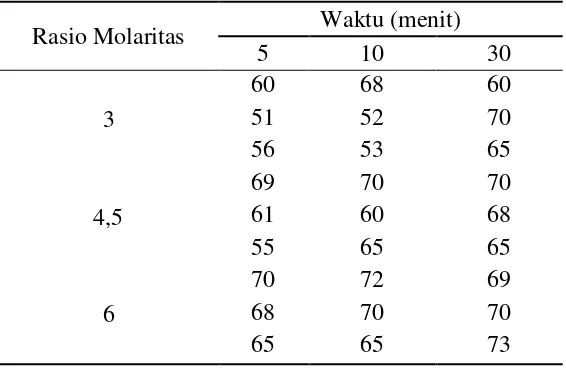
Lampiran 2. Perhitungan % rendemen biodiesel dengan menggunakan gelombang ultrasonik
Tabel 13. Hasil bobot biodiesel setelah pencucian (ml)
Rasio Molaritas Waktu (menit)
b) % Rendemen biodiesel pada M1 = 3:1 dengan T2 = 10 menit
= 68%
= 52%
= 53%
Rata-rata % rendemen biodiesel = 68% + 52% + 53%
= 57,67%
c) % Rendemen biodiesel pada M1 = 3:1 dengan T3 = 30 menit
= 60%
= 70%
= 65%
Rata-rata % rendemen biodiesel = 60% + 70% + 65%
d) % Rendemen biodiesel pada M2 = 4,5:1 dengan T1 = 5 menit
= 69%
= 58%
= 55%
Rata-rata % rendemen biodiesel = 69% + 58% + 55%
= 60,67%
e) % Rendemen biodiesel pada M2 = 4,5:1 dengan T2 = 10 menit
= 70%
= 60%
= 65%
Rata-rata % rendemen biodiesel = 70% + 60% + 65%
f) % Rendemen biodiesel pada M2 = 4,5:1 dengan T3 = 30 menit
= 70%
= 68%
= 65%
Rata-rata % rendemen biodiesel = 70% + 68% + 65%
= 67,67%
g) % Rendemen biodiesel pada M3 = 6:1 dengan T1 = 5 menit
= 70%
= 68%
= 65%
Rata-rata % rendemen biodiesel = 70% + 68% + 65%
h) % Rendemen biodiesel pada M3 = 6:1 dengan T2 = 10 menit
= 72%
= 70%
= 65%
Rata-rata % rendemen biodiesel = 72% + 70% + 65%
= 69%
i) % Rendemen biodiesel pada M3 = 6:1 dengan T3 = 30 menit
= 70%
= 69%
= 73%
Rata-rata % rendemen biodiesel = 70% + 69% + 73%
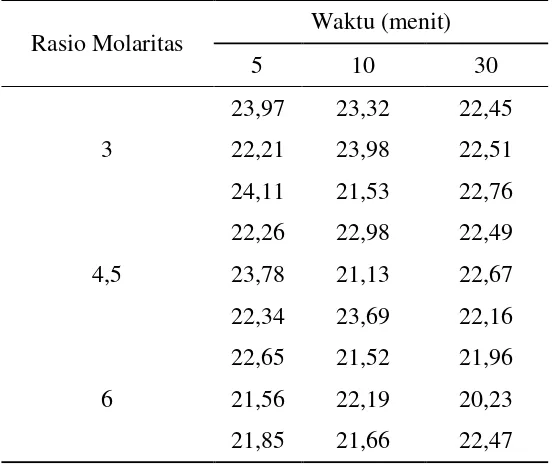
Lampiran 3. Perhitungan massa jenis biodiesel dengan menggunakan gelombang ultrasonik
Tabel 14. Hasil massa sampel biodiesel (gram)
= 0,96 gram/ml
Rata-rat massa jenis biodiesel = 0,96 gram/ml + 0,89 gram/ml + 0,96 gram/ml
= 0,94 gram/ml
Rata-rat massa jenis biodiesel = 0,93 gram/ml + 0,96 gram/ml + 0,86 gram/ml
ρBiodiesel =
Rata-rat massa jenis biodiesel = 0,90 gram/ml + 0,91 gram/ml + 0,91 gram/ml
Rata-rat massa jenis biodiesel = 0,89 gram/ml + 0,95 gram/ml + 0,89 gram/ml
Rata-rat massa jenis biodiesel = 0,92 gram/ml + 0,85 gram/ml + 0,95 gram/ml
ρBiodiesel =
Rata-rat massa jenis biodiesel = 0,90 gram/ml + 0,91 gram/ml + 0,89 gram/ml
Rata-rat massa jenis biodiesel = 0,91 gram/ml + 0,86 gram/ml + 0,87 gram/ml
Rata-rat massa jenis biodiesel = 0,86 gram/ml + 0,89 gram/ml + 0,87 gram/ml
ρBiodiesel =
=
= 0,81gram/ml
ρBiodiesel =
=
= 0,90 gram/ml
Rata-rat massa jenis biodiesel = 0,88 gram/ml + 0,81 gram/ml + 0,90 gram/ml
Lampiran 4. Perhitungan % bilangan asam dengan menggunakan gelombang ultrasonik
Tabel 15. Hasil titrasi sampel biodiesel (ml)
= 0,09%
Rata-rata % bilangan asam = 0,08% + 0,11% + 0,09%
Lampiran 5. Perhitungan viskositas biodiesel dengan menggunakan gelombang ultrasonik
Tabel 16. Lama waktu biodiesel (detik)
µ = k (ρ bola –ρ biodiesel) t0
µ = 0,01336 (8,02 g/ml – 0,89 g/ml) 89,97 s µ = 8,57 Cp / 0,89 g/ml
µ = 9,63 cSt
µ = k (ρ bola –ρ biodiesel) t0
µ = 0,01336 (8,02 g/ml – 0,96 g/ml) 76,61 s µ = 7,18 Cp / 0,96 g/ml
µ = 7,48 cSt
Rata-rata Viskositas = 7,12 cSt + 9,63 cSt + 7,48 cSt
= 8,07 cSt
b) Viskositas pada M1 = 3:1 dengan T2 = 10 menit
µ = k (ρ bola –ρ biodiesel) t0
µ = 0,01336 (8,02 g/ml – 0,93 g/ml) 71,61 s µ = 6,75 Cp / 0,93 g/ml
µ = 7,29 cSt
µ = k (ρ bola –ρ biodiesel) t0
µ = 0,01336 (8,02 g/ml – 0,96 g/ml) 61,91 s µ = 5,84 Cp / 0,96 g/ml
µ = 6,09 cSt
µ = k (ρ bola –ρ biodiesel) t0
Rata-rata Viskositas = 7,29 cSt + 6,09 cSt + 7,32 cSt
= 6,09 cSt
c) Viskositas pada M1 = 3:1 dengan T3 = 30 menit
µ = k (ρ bola –ρ biodiesel) t0
µ = 0,01336 (8,02 g/ml – 0,90 g/ml) 64,38 s µ = 4,12 Cp / 0,90 g/ml
µ = 6,80 cSt
µ = k (ρ bola –ρ biodiesel) t0
µ = 0,01336 (8,02 g/ml – 0,91 g/ml) 48,16s µ = 4,57 Cp / 0,91 g/ml
µ = 5,03 cSt
µ = k (ρ bola –ρ biodiesel) t0
µ = 0,01336 (8,02 g/ml – 0,91 g/ml) 47,73 s µ = 4,53 Cp / 0,91 g/ml
µ = 4,98 cSt
Rata-rata Viskositas = 6,80 cSt + 5,03 cSt + 4,98 cSt
= 5,60 cSt
d) Viskositas pada M2 = 4,5:1 dengan T1 = 5 menit
µ = k (ρ bola –ρ biodiesel) t0
µ = k (ρ bola –ρ biodiesel) t0
µ = 0,01336 (8,02 g/ml – 0,95 g/ml) 69,28 s µ = 6,54 Cp / 0,95 g/ml
µ = 6,89 cSt
µ = k (ρ bola –ρ biodiesel) t0
µ = 0,01336 (8,02 g/ml – 0,89 g/ml) 74,41 s µ = 7,09 Cp / 0,89 g/ml
µ = 7,96 cSt
Rata-rata Viskositas = 9,65 cSt + 6,89 cSt + 7,96 cSt
= 8,17 cSt
e) Viskositas pada M2 = 4,5:1 dengan T2 = 10 menit
µ = k (ρ bola –ρ biodiesel) t0
µ = 0,01336 (8,02 g/ml – 0,92 g/ml) 65,7 s µ = 6,23Cp / 0,92 g/ml
µ = 6,77 cSt
µ = k (ρ bola –ρ biodiesel) t0
µ = 0,01336 (8,02 g/ml – 0,85 g/ml) 63,65 s µ = 6,1 Cp / 0,85 g/ml
µ = 7,17 cSt
µ = k (ρ bola –ρ biodiesel) t0
Rata-rata Viskositas = 6,77 cSt + 7,17 cSt + 6,33 cSt
= 6,76 cSt
f) Viskositas pada M2 = 4,5:1 dengan T3 = 30 menit
µ = k (ρ bola –ρ biodiesel) t0
µ = 0,01336 (8,02 g/ml – 0,90 g/ml) 48,33 s µ = 4,60 Cp / 0,90 g/ml
µ = 5,11 cSt
µ = k (ρ bola –ρ biodiesel) t0
µ = 0,01336 (8,02 g/ml – 0,91 g/ml) 47,97s µ = 4,56 Cp / 0,91 g/ml
µ = 5,01 cSt
µ = k (ρ bola –ρ biodiesel) t0
µ = 0,01336 (8,02 g/ml – 0,89 g/ml) 53,8 s µ = 5,12 Cp / 0,89 g/ml
µ = 5,76 cSt
Rata-rata Viskositas = 5,11 cSt + 5,01 cSt + 5,76 cSt
= 5,29 cSt
g) Viskositas pada M3 = 6:1 dengan T1 = 5 menit
µ = k (ρ bola –ρ biodiesel) t0
µ = k (ρ bola –ρ biodiesel) t0
µ = 0,01336 (8,02 g/ml – 0,86 g/ml) 69,1 s µ = 6,61 Cp / 0,86 g/ml
µ = 7,69 cSt
µ = k (ρ bola –ρ biodiesel) t0
µ = 0,01336 (8,02 g/ml – 0,87 g/ml) 70,82 s µ = 6,77 Cp / 0,87 g/ml
µ = 7,78 cSt
Rata-rata Viskositas = 9,06 cSt + 7,69 cSt + 7,78 cSt
= 8,17cSt
h) Viskositas pada M1 = 6:1 dengan T2 = 10 menit
µ = k (ρ bola –ρ biodiesel) t0
µ = 0,01336 (8,02 g/ml – 0,86 g/ml) 87,98 s µ = 8,42 Cp / 0,86 g/ml
µ = 9,79 cSt
µ = k (ρ bola –ρ biodiesel) t0
µ = 0,01336 (8,02 g/ml – 0,89 g/ml) 39,8 s µ = 3,79 Cp / 0,89 g/ml
µ = 4,26 cSt
µ = k (ρ bola –ρ biodiesel) t0
Rata-rata Viskositas = 9,79 cSt + 4,26 cSt + 6,96 cSt
= 7,00 cSt
i) Viskositas pada M3 = 6:1 dengan T3 = 30 menit
µ = k (ρ bola –ρ biodiesel) t0
µ = 0,01336 (8,02 g/ml – 0,88 g/ml) 23,37 s µ = 2,83 Cp / 0,88 g/ml
µ = 2,53 cSt
µ = k (ρ bola –ρ biodiesel) t0
µ = 0,01336 (8,02 g/ml – 0,81 g/ml) 34,15 s µ = 3,29 Cp / 0,81 g/ml
µ = 4,06 cSt
µ = k (ρ bola –ρ biodiesel) t0
µ = 0,01336 (8,02 g/ml – 0,90 g/ml) 55,75 s µ = 3,30 Cp / 0,90 g/ml
µ = 5,89 cSt
Rata-rata Viskositas = 2,53 cSt + 4,06 cSt + 5,89 cSt
Lampiran 6. Perhitungan statistika rendemen bodiesel
Tabel 17. Hasil rendemen biodiesel pada masing-masing perlakuan
Perlakuan Ulangan Total Rata-rata
3. JKKelompok =
Tabel 18. Sumber keragaman rendemen biodiesel
e) Tabel Uji beda nyata
Tabel 19. Uji beda nyata rendemen biodiesel
Perlakuan
Tabel 20. Kesimpulan rendemen biodiesel
Lampiran 7. Perhitungan statistika massa jenis bodiesel
Tabel 21. Hasil massa jenis biodiesel pada masing-masing perlakuan
Perlakuan Ulangan Total Rata-rata
= 21,87 – 21,83401 = 0,04
Tabel 22. Sumber keragaman massa jenis biodiesel