PREPARASI DAN KARAKTERISASI
NANOPARTIKEL ZINK PEKTINAT MENGANDUNG
DILTIAZEM HIDROKLORIDA DENGAN METODE
GELASI IONIK
SKRIPSI
SUBHAN ASFARI
1111102000086
FAKULTAS KEDOKTERAN DAN ILMU KESEHATAN
PROGRAM STUDI FARMASI
PREPARASI DAN KARAKTERISASI
NANOPARTIKEL ZINK PEKTINAT MENGANDUNG
DILTIAZEM HIDROKLORIDA DENGAN METODE
GELASI IONIK
SKRIPSI
Diajukan sebagai salah satu syarat memperoleh gelar Sarjana Farmasi
SUBHAN ASFARI
1111102000086
FAKULTAS KEDOKTERAN DAN ILMU KESEHATAN
PROGRAM STUDI FARMASI
iv Nama : Subhan Asfari Program Studi : Farmasi
Judul Skripsi : Preparasi dan Karaterisasi Nanopartikel Zink Pektinat Mengandung Diltiazem Hidroklorida dengan Metode Gelasi Ionik.
Nanopartikel zink pektinat mengandung diltiazem hidroklorida telah dibuat dengan metode gelasi ionik. Tujuan dari penelitian ini adalah mempelajari pengaruh penambahan diltiazem hidroklorida serta perbedaan medium preparasi (akuades dan NaCl 0,05M) terhadap karakteristik fisik nanopartikel. Nanopartikel diperoleh dari tiga formula yang berbeda. Formula 1 merupakan nanopartikel zink pektinat kosong yang dipreparasi dalam medium NaCl 0,05 M. Formula 2 merupakan nanopartikel zink pektinat mengandung diltiazem hidroklorida yang dipreparasi dalam medium NaCl 0,05 M. Formula 3 merupakan nanopartikel zink pektinat mengandung diltiazem hidroklorida yang dipreparasi dalam medium akuades. Pembuatan nanopartikel dilakukan dengan menambahkan larutan ZnCl2 ke dalam
larutan pektin dan campuran pektin-diltiazem hidroklorida tetes demi tetes di bawah pengadukan ultrasonik. Ukuran partikel, potensial zeta, efisiensi penjerapan, spektrum FT-IR, dan sifat termal dari setiap formula nanopartikel dikarakterisasi. Ukuran partikel formula 1, 2 dan 3 masing-masing 433,82 nm, 502,41 nm dan 765,47 nm. Hasil penelitian menunjukkan bahwa penambahan diltiazem hidroklorida ke dalam nanopartikel dapat menyebabkan peningkatan ukuran partikel, penurunan potensial zeta dan derajat sambung silang. Sementara itu, keberadaan natrium klorida selama preparasi menyebabkan penurunan ukuran partikel, potensial zeta dan derajat sambung silang. Perbedaan medium preparasi tidak menyebabkan perbedaan dalam efisiensi penjerapan.
v Name : Subhan Asfari Program Study : Pharmacy
Title : Preparation and Characterization Zinc Pectinate Nanoparticles Containing Diltiazem Hidrochloride by Ionic Gelation
Zinc pectinate nanoparticles containing diltiazem hydrochloride had been prepared by ionic gelation method. The aim of the research was to investigate effect of diltiazem hydrochloride addition and the differences of preparation media (aquadest and NaCl 0,05M) toward physical characteristics of nanoparticles. Nanoparticles were obtained from three different formula. Formula 1 was blank zinc pectinate nanoparticles which prepared in 0,05 M NaCl media. Formula 2 was zinc pectinate nanoparticles containing diltiazem hydrochloride which prepared in 0.05 M NaCl media. Formula 3 was zinc pectinate nanoparticles containing diltiazem hydrochloride which prepared in aquadest media. Preparation of nanoparticles was done by adding ZnCl2 solution into pectin and pectin-diltiazem hydrochloride
mixture solution dropwise under ultrasonic stirring. Particle size, zeta potential, entrapment efficiency, FT-IR spectrum, and thermal properties of each nanoparticles formula were characterized. Particle size of formula 1, 2 and 3 were 433,82 nm, 502,41 nm and 765,47 nm respectively. The results showed that the addition of diltiazem hydrochloride into nanoparticles can lead to increase in particle size, decrease in zeta potential and degree of crosslinking. Meanwhile, the presence of sodium chloride during the preparation can lead to decrease in particle size, zeta potential, and degree of crosslinking. The differences of preparation media did not cause differences in entrapment efficiency.
vi
Puji dan syukur penulis panjatkan kehadirat Allah SWT karena atas rahmat dan karunia-Nya penulis dapat menyelesaikan skripsi yang berjudul “Preparasi dan Karakterisasi Nanopartikel Zink Pektinat Mengandung Diltiazem Hidroklorida dengan Metode Gelasi Ionik”. Shalawat dan salam senantiasa terlimpah kepada junjungan, Nabi Muhammad SAW, teladan bagi umat manusia dalam menjalani kehidupan.
Skripsi ini ditulis untuk memenuhi tugas akhir guna mendapatkan gelar Sarjana Farmasi pada Program Studi Farmasi, Fakultas Kedokteran dan Ilmu Kesehatan, Universitas Islam Negeri Syarif Hidayatullah Jakarta. Pada penulisan skripsi ini, penulis tidak terlepas dari bimbingan, arahan, bantuan, serta dukungan dari berbagai pihak. Oleh karena itu, dengan segenap kerendahan dan kesungguhan hati penulis ingin mengucapkan terima kasih yang sebesar-besarnya kepada: 1. Bapak Dr. Arif Sumantri S.K.M., M.Kes. selaku Dekan Fakultas Kedokteran
dan Ilmu Kesehatan, Universitas Islam Negeri Syarif Hidayatullah Jakarta. 2. Bapak Yardi, Ph.D., Apt., selaku Ketua Program Studi Farmasi Fakultas
Kedokteran dan Ilmu Kesehatan Universitas Islam Negeri Syarif Hidayatullah Jakarta.
3. Ibu Yuni Anggraeni, M.Farm., Apt. sebagai Pembimbing I dan Ibu Nelly Suryani, Ph.D., Apt. sebagai Pembimbing II yang telah memberikan bimbingan, ilmu, nasihat serta dedikasinya selama masa penelitian hingga penulisan skripsi. 4. Ibu Pricilia dari PT Rotaryana Prima yang telah membantu dalam memperoleh
bahan penelitian.
5. Seluruh dosen Program Studi Farmasi Fakultas Kedokteran dan Ilmu Kesehatan Universitas Islam Negeri Syarif Hidayatullah Jakarta atas ilmu dan pengetahuan yang telah diberikan.
vii melakukan penelitian di laboratorium.
8. Teman-teman seperjuangan teknologi farmasi yang telah saling mendukung, menyemangati, dan memberikan pertolongan selama penelitian dan penulisan skripsi.
9. Rekan-rekan Mahasiswa/i S1 Farmasi UIN Syarif Hidayatullah Jakarta angkatan 2011, yang telah menjadi bagian penting hidup penulis selama menjalankan pendidikan tinggi.
10.Semua pihak yang tidak dapat disebutkan namanya satu persatu yang telah membantu dengan ikhlas baik secara langsung maupun tidak langsung dalam proses penelitian dan penulisan skripsi ini.
Semoga semua kebaikan dan bantuan yang telah diberikan mendapatkan balasan dari Allah SWT. Penulis menyadari bahwa dalam pembuatan laporan ini masih terdapat banyak kekurangan dan kesalahan. Oleh karena itu, penulis mengharapkan kritik dan saran yang membangun.
Akhir kata, penulis berharap semoga ilmu dan pengetahuan yang penulis tuangkan dalam skripsi ini dapat memberikan manfaat bagi rekan sejawat dan semua pihak yang membutuhkan, serta menjadi keberkahan tersendiri bagi penulis.
Jakarta, Juni 2015
ix
Halaman
HALAMAN PERNYATAAN ORISINALITAS ... i
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN ... iii
ABSTRAK ... iv
ABSTRACT ... v
KATA PENGANTAR ... vi
HALAMAN PERNYATAAN PERSETUJUAN PUBLIKASI... viii
DAFTAR ISI ... ix
2.1 Diltiazem Hidroklorida ... 5
2.2 Pektin ... 6
2.3 Zink Klorida ... 9
2.4 Natrium Klorida ... 9
2.5 Nanopartikel Sebagai Sistem Penghantaran Obat ... 10
2.6 Gelasi Ionik... 12
2.7 Sifat dan Karaterisasi Fisik Nanopartikel Sambung Silang... 14
2.7.1 Analisis Spektrum FT-IR ... 14
2.7.2 Persen Efisiensi Penjerapan ... 15
2.7.3 Ukuran Partikel dan Indeks Polidispersitas... 15
2.7.4 Potensial Zeta ... 17
2.7.5 Differential Scanning Calorimetry (DSC) ... 19
BAB 3 METODOLOGI PENELITIAN ... 21
3.1 Waktu dan Tempat Penelitian... 21
3.2 Bahan dan Alat ... 21
x
3.3.1 Preparasi Larutan NaCl 0,05 M ... 21
3.3.2 Preparasi Nanopartikel Diltizem Hidroklorida ... 22
3.3.3 Pengeringan Nanopartikel ... 23
3.4 Karakterisasi Nanopartikel ... 23
3.4.1 Perubahan Transmitan (%) Suspensi Nanopartikel ... 23
3.4.2 Penetapan Ukuran Partikel dan Indeks Polidispersitas ... 24
3.4.3 Penetapan Potensial Zeta... 24
3.4.4 Penetapan Efisiensi Penjerapan (%) Diltiazem Hidroklorida ... 24
3.3.6 Analisis Spektrum Inframerah ... 25
3.3.7 Analisis Differential Scanning Calorimetry ... 25
BAB 4 HASIL DAN PEMBAHASAN ... 26
4.1 Preparasi Nanopartikel ... 26
4.2 Penurunan Transmitansi (%) ... 28
3.3 Ukuran Partikel dan Indeks Polidispersitas ... 29
4.4 Potensial Zeta ... 32
4.5 Efisiensi Penjerapan (%) Diltiazem Hidroklorida ... 35
4.6 Spektrum Inframerah ... 37
4.7 Analisis Differential Scanning Calorimetry (DSC)... 40
BAB 5 KESIMPULAN DAN SARAN ... 43
5.1 Kesimpulan ... 43
5.2 Saran ... 43
DAFTAR PUSTAKA ... 44
xi
Halaman
Gambar 2.1 Struktur molekul diltiazem hidroklorida... 5
Gambar 2.2 Struktur dasar molekul pektin... 6
Gambar 2.3 Skema struktur pektin... 7
Gambar 2.4 Mekanisme gelasi... 8
Gambar 2.5 Spektrum IR sambung silang pektin dengan ZnO... 14
Gambar 2.6 Ilustrasi diameter hidrodinamik... 16
Gambar 2.7 Skema ilustrasi percobaan DLS... 16
Gambar 2.8 Skema ilustrasi partikel bermuatan negatif pada media air... 18
Gambar 4.1 Hasil preparasi nanopartikel... 28
Gambar 4.2 Penurunan transmitan (%) suspensi nanopartikel... 29
Gambar 4.3 Hubungan pH terhadap formula... 30
Gambar 4.4 Konformasi rantai polimer pektin... 31
Gambar 4.5 Hubungan potensial zeta terhadap formula... 33
Gambar 4.6 Gugus fungsional pektin... 34
Gambar 4.6 Hubungan efisiensi penjerapan terhadap formula... 36
Gambar 4.7 Perbandingan spektrum inframerah nanopartikel kering dan pektin... 38
xii
Halaman
Tabel 3.1 Formula preparasi nanopartikel... 22
Tabel 4.1 Ukuran partikel dan indeks polidispersitas... 30
Tabel 4.2 Estimasi jumlah ion dalam 50 mL suspensi nanopartikel... 35
xiii
Halaman
Lampiran 1. Alur Penelitian ... 51
Lampiran 2. Sertifikat Analisis Diltiazem Hidroklorida ... 52
Lampiran 3. Sertifikat Analisis Pektin ... 53
Lampiran 4. Sertifikat Analisis Natrium Klorida ... 54
Lampiran 5. Perhitungan Preparasi Larutan NaCl 0,05M ... 56
Lampiran 6. Perhitungan Bahan dalam Preparasi Nanopartikel ... 56
Lampiran 7. Perhitungan Persen Transmitan ... 57
Lampiran 8. Data Distribusi Ukuran Partikel dan Indeks Polidispersitas ... 58
Lampiran 9. Data Pengukuran Potensial zeta ... 59
Lampiran 10. Data Perhitungan Jumlah Ion ... 59
Lampiran 11. Data Perhitungan pH. ... 62
Lampiran 12. Spektrum Serapan Diltiazem Hidroklorida dalam Akuades. ... 63
Lampiran 13. Spektrum Serapan Diltiazem Hidroklorida dalam NaCl 0,05 M. . 63
Lampiran 14. Kurva Kalibrasi Diltiazem Hidroklorida dalam Pelarut Akuades. 64 Lampiran 15. Kurva Kalibrasi Diltiazem Hidroklorida dalam Pelarut NaCl 0,05 M ... 64
Lampiran 16. Data Efisiensi Penjerapan ... 65
Lampiran 17. Contoh Perhitungan Persen Penjerapan Diltiazem Hidroklorida. . 65
Lampiran 18. Data Spektrum Inframerah ... 67
Lampiran 19. Data Hasil Analisa DSC ... 71
Lampiran 20. Alat-alat penelitian ... 74
Lampiran 21. Proses Sambung Silang ... 75
Lampiran 22. Suspensi Nanopartikel ... 76
Lampiran 23. Hasil Sentrifugasi Suspensi Nanopartikel ... 76
1 UIN Syarif Hidayatullah Jakarta BAB 1
PENDAHULUAN
1.1 Latar Belakang
Nanoteknologi saat ini sering digunakan untuk berbagai aplikasi, di antaranya serat dan tekstil, pertanian, elektronik, ilmu forensik, antariksa, dan terapi medis (Kumar, Yadav dan Yadav, 2010). Salah satu bidang penelitian yang paling aktif dari nanoteknologi adalah nanomedicine yang menerapkan nanoteknologi untuk intervensi medis yang sangat spesifik untuk pencegahan, diagnosis dan pengobatan penyakit (Lobatto dkk., 2011). Nanopartikel merupakan bagian studi nanomedicine dalam sistem penghantaran obat.
Nanopartikel dapat bertindak sebagai sistem penghantaran obat dengan menjerap molekul obat dalam struktur interiornya, mengadsorpsi molekul obat di permukaan, atau terikat secara kovalen dengan suatu bahan prekursor (Tiwari dkk., 2012). Teknologi nanopartikel menawarkan keuntungan besar di antaranya meningkatkan solubilisasi bahan aktif obat hidrofobik, meningkatkan bioavailabilitas, memperbaiki farmakokinetik bahan aktif obat, melindungi bahan aktif obat dari degradasi fisik, kimia atau biologis (Gupta & Kumar, 2012), dan meningkatkan waktu retensi sediaan (Petros & DeSimone, 2010).
Pembuatan nanopartikel pektin didasarkan atas kemampuan pektin untuk membentuk gel dengan penyambung silang berupa kation divalen, umumnya kalsium dan zink. Gel terbentuk karena adanya ikatan ionik antara gugus karboksil yang bermuatan negatif dari pektin dengan ion divalen (Racovita dkk.2009). Telah dilakukan penelitian bahwa zink merupakan penyambung silang yang lebih baik untuk pektin dibandingkan dengan kalsium, karena membentuk ikatan yang lebih kuat pada pektin (Das, Ng, & Ho, 2010 dan Adingsih, 2012).
Berbeda dengan pembuatan gel pektin makroskopik, pembuatan nanopartikel pektin harus dilakukan pada konsentrasi pektin encer (Vauthier & Bouchemal, 2009), yaitu di bawah konsentrasi tumpang tindih antar rantai polimer. Konsentrasi tumpang tindih dari larutan polimer tergantung pada konformasi rantai polimer dalam larutan dan pada sifat pelarut serta kondisi termodinamika (Jonassen, Treves, Kjøniksen, Smistad & Hiorth, 2013). Konformasi rantai pektin dalam media air juga tergantung pada derajat ionisasi yaitu derajat esterefikasi pektin dan pH larutan. Dalam air murni, ionisasi rantai pektin akan memiliki konformasi terentang karena tolakan elektrostatik (Sriamonsrak, 2011).
Jonassen, Treves, Kjøniksen, Smistad & Hiorth (2013) meneliti pengaruh natrium klorida terhadap konformasi rantai polimer dalam proses pembentukan nanopartikel pektin. Penambahan garam akan menyaring beberapa tolakan elektrostatik sehingga mengubah konformasi rantai polimer membentuk kumparan yang semula terentang. Partikel yang lebih kecil dan lebih kompak dapat dibentuk dalam air garam dibandingkan dengan air murni. Hal ini dipicu oleh dominasi taut silang intramolekul dibandingkan intermolekul polimer. Penambahan NaCl dalam pembuatan nanopartikel pektin juga dilakukan pada penelitian ini. Hal tersebut diharapkan dapat memicu salting-out dan meningkatkan kecenderungan agregrasi rantai polimer, sehingga nanopartikel pektin lebih mudah terbentuk.
sebagai model agen terapi yang tepat untuk dimodifikasi sebagai nanopartikel karena bioavailabilitas oral hanya 30-40% (Shukla, Kharia & Kaur, 2012), dan tablet atau kapsul konvensional perlu diberikan 3 atau 4 kali sehari karena waktu paruh biologis hanya sekitar 6 jam (Mahale & Sreenivas, 2013).
Dalam penelitian ini, akan dibuat nanopartikel pektin sambung silang dengan zink yang mengandung diltiazem hidroklorida. Sumber logam monovalen berupa NaCl ditambahkan untuk mempermudah terbentuknya nanopartikel. Tujuan dari penelitian ini adalah untuk meneliti pengaruh penambahan diltiazem hidroklorida dan NaCl terhadap karakteristik fisik dari nanopartikel serta jumlah diltiazem hidroklorida yang dapat dijerap dalam nanopartikel yang dihasilkan.
1.2 Rumusan Masalah
Rumusan masalah dari penelitian ini di antaranya;
a) Bagaimana pengaruh penambahan diltiazem hidroklorida terhadap karakteristik fisik nanopartikel sambung silang zink pektinat?
b) Bagaimana pengaruh penambahan NaCl terhadap karakterisitik fisik nanopartikel yang dibuat dan jumlah diltiazem hidroklorida yang terjerap?
1.3 Tujuan Penelitian
a) Membuat nanopartikel sambung silang zink pektinat mengandung diltiazem hidroklorida.
b) Mempelajari pengaruh penambahan diltiazem hidroklorida terhadap karakteristik fisik nanopartikel yang dihasilkan.
c) Mempelajari pengaruh penambahan NaCl terhadap jumlah diltiazem hidroklorida yang terjerap dan karakteristik fisik nanopartikel yang dihasilkan.
1.4 Manfaat Penelitian
Diharapkan hasil penelitian ini memberikan manfaat sebagai berikut: a) Meningkatkan nilai guna pektin dalam bidang farmasetik terutama dalam
sistem penghantaran obat.
5 UIN Syarif Hidayatullah Jakarta BAB 2
TINJAUAN PUSTAKA
2.1 Diltiazem Hidroklorida
Diltiazem adalah penghambat kanal kalsium golongan benzotiazepin (Golan dkk., 2011) yang biasa digunakan untuk terapi hipertensi dan angina pektoris.
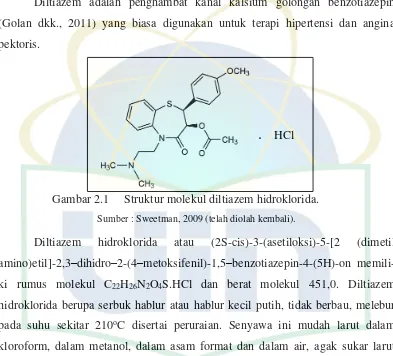
Gambar 2.1 Struktur molekul diltiazem hidroklorida.
Sumber : Sweetman, 2009 (telah diolah kembali).
Diltiazem hidroklorida atau (2S-cis)-3-(asetiloksi)-5-[2 (dimetil amino)etil]-2,3–dihidro–2-(4–metoksifenil)-1,5–benzotiazepin-4-(5H)-on memili-ki rumus molekul C22H26N2O4S.HCl dan berat molekul 451,0. Diltiazem
hidroklorida berupa serbuk hablur atau hablur kecil putih, tidak berbau, melebur pada suhu sekitar 210oC disertai peruraian. Senyawa ini mudah larut dalam kloroform, dalam metanol, dalam asam format dan dalam air, agak sukar larut etanol mutlak, dan tidak larut dalam eter (Departemen Kesehatan RI, 1995).
Obat golongan ini bekerja dengan menurunkan influks ion kalsium ke dalam sel miokard, sel‐sel dalam sistem konduksi jantung, dan sel‐sel otot polos pembuluh darah. Efek ini akan menurunkan kontraktilitas jantung, menekan pembentukan dan propagasi impuls elektrik dalam jantung dan memacu aktivitas vasodilatasi, interferensi dengan konstriksi otot polos pembuluh darah (Gormer, 2007).
Diltiazem HCl diberikan secara oral untuk pengobatan angina pektoris dan hipertensi serta perlu dikonsumsi 3–4 kali sehari untuk tetap mempertahankan tekanan darah normal dan mencegah serangan angina pektoris. Bioavailabilitas diltiazem HCl pada pemberian oral sekitar 40% dengan konsentrasi plasma yang
UIN Syarif Hidayatullah Jakarta bervariasi antar individu (Sweetman, 2009).
2.2 Pektin
Pektin merupakan satu di antara polisakarida anionik alam yang diperoleh dari ekstraksi kulit jeruk dan apel dengan asam mineral encer panas pada pH ± 2 (Sriamornsak, 2011). Pektin adalah polisakarida alami yang biasa digunakan dalam industri makanan sebagai gelling dan thickening agent (Jonassen, 2014). Pektin memiliki sifat hidrofilik, sehingga dapat digunakan sebagai matriks hidrofilik yang dapat digunakan untuk sistem penghantaran obat oral dan untuk formulasi yang pelepasannya dimodifikasi (Adiningsih, 2012 dan Bhatia dkk., 2008).
Gambar 2.2 Struktur dasar molekul pektin
Sumber: Racovita dkk., 2009
Struktur pektin sangat sulit untuk ditetapkan karena pektin dapat berubah selama isolasi, penyimpanan, dan pengolahan dari bahan tanaman (Novosel'skaya dkk., 2000). Komposisi utama pektin adalah unit-unit asam D-galakturonik (GalA) yang membentuk rantai ikatan α-(1,4) glikosidik. Asam uronat ini mempunyai kelompok gugus karboksil yaitu metil ester dan gugus lainya yang apabila direaksikan dengan amonia akan menghasilkan gugus karboksiamida. Terdapat ratusan hingga ribuan sakarida dengan bentuk konfigurasi rantai dan berat molekulnya sekitar lima puluh ribu Dalton (Srivastava dan Malviya, 2011).
Polisakarida pektin terbuat dari beberapa struktur elemen penting di antaranya homogalakturonat (HG) dan rhamnogalakturonat tipe I (RG-I), di mana daerah tersebut masing-masing digambarkan sebagai daerah "halus" dan "berbulu".
Wilayah HG terdiri dari residu (1 → 4) α-D-GalpA yang sebagian dapat termetilasi pada C-6 dan mungkin sebagian terasetil-esterifikasi di O-2 dan/atau O-3. Wilayah RG-I terdiri dari unit disakarida berulang [→ 4) -α-D-GalpA- (1 → 2) -α-LRhap-
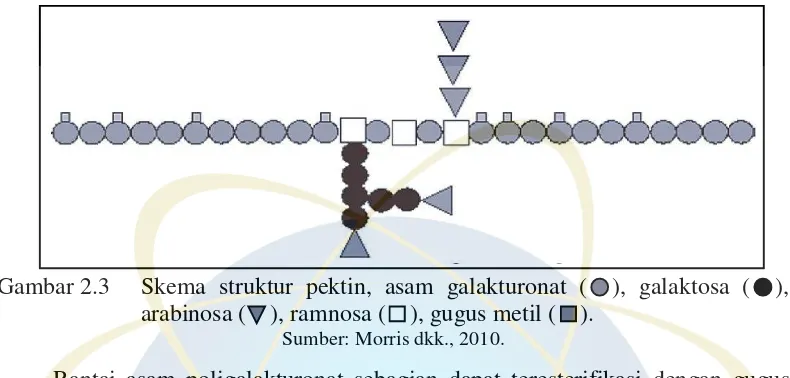
UIN Syarif Hidayatullah Jakarta galaktosa .Telah dilaporkan bahwa residu GalA di wilayah RG-I sebagian dapat terasetilasi tetapi tidak termetilasi (Morris dkk., 2010).
Gambar 2.3 Skema struktur pektin, asam galakturonat ( ), galaktosa ( ), arabinosa ( ), ramnosa ( ), gugus metil ( ).
Sumber: Morris dkk., 2010.
Rantai asam poligalakturonat sebagian dapat teresterifikasi dengan gugus metil, dan gugus asam bebas dapat sebagian atau seluruhnya dinetralkan dengan ion natrium, kalium atau amonium. Rasio gugus GalA yang teresterifikasi terhadap total gugus GalA disebut sebagai DE (derajat esterefikasi). Kelas pektin berdasarkan DE di antaranya high methoxyl (HM) pektin, dan low methoxyl (LM) baik yang secara konvensional terdemetilasi atau hasil modifikasi dengan amidasi menjadi amidated low methoxyl (AM) pektin. Nilai DE untuk HM-pektin komersial biasanya berkisar 60-75% dan untuk LM-pektin antara 20 sampai 40%. Kedua kelompok pektin membentuk gel dengan mekanisme yang berbeda (Sriamornsak, 2011)
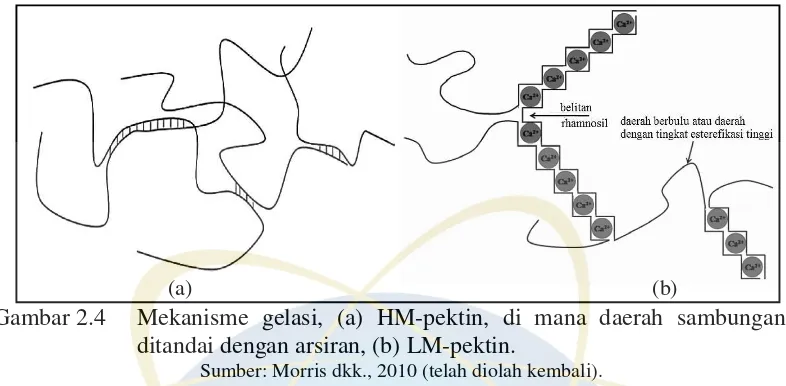
UIN Syarif Hidayatullah Jakarta Gambar 2.4 Mekanisme gelasi, (a) HM-pektin, di mana daerah sambungan
ditandai dengan arsiran, (b) LM-pektin.
Sumber: Morris dkk., 2010 (telah diolah kembali).
Kemampuan pektin dalam membentuk gel sangat bergantung dari ukuran molekul, derajat esterifikasinya, pH, konsentrasi, ion kalsium (crosslinker), kekuatan ionik larutan dan suhu, sehingga pektin yang berasal dari sumber yang berbeda tidak mempunyai kemampuan yang sama dalam membentuk gel (Ovodov, 2009). Faktor-faktor yang meningkatkan kekuatan gel akan meningkatkan kecenderungan untuk membentuk gel, menurunkan kelarutan, dan meningkatkan viskositas, serta sebaliknya. Sifat pektin ini merupakan fungsi dari struktur mereka, yang berupa polianion linear (polikarboksilat). Dengan demikian, pektin sangat terionisasi dalam larutan, dan distribusi muatan ion di sepanjang molekulnya cenderung untuk rantai polimer pektin tetap dalam bentuk terentang oleh karena tolakan Coulomb (Sriamornsak, 2011).
Tolakan Coulomb yang sama antar anion karboksilat mencegah agregasi dari rantai polimer, di mana jumlah muatan negatif ditentukan oleh DE. Selain itu, masing-masing rantai polisakarida, dan terutama setiap kelompok karboksilat akan sangat terhidrasi. Larutan pektin menunjukkan kekentalan yang sangat stabil karena setiap rantai polimer terhidrasi, diperpanjang, dan terpisah (Sriamornsak, 2011).
Pada pH rendah, ionisasi dari gugus karboksilat ditekan, dan ini mengakibatkan pengurangan hidrasi gugus asam karboksilat. Sebagai hasil dari pengurangan ionisasi, molekul polisakarida tidak lagi saling tolak di sepanjang rantai polimernya, dan pada akhirnya antar rantai polimer dapat saling mengait dan membentuk gel (Sriamornsak, 2011).
Pektin telah digunakan sebagai agen pembentuk gel untuk waktu yang lama, namun telah ada penelitian baru terhadap penggunaan gel pektin dalam
UIN Syarif Hidayatullah Jakarta penghantaran obat terkontrol. Hal ini karena sifatnya yang tidak toksik, biaya produksi yang relatif rendah dan ketersediaan tinggi. Telah diusulkan bahwa pektin dapat digunakan untuk penghantaran obat oral, nasal dan vaginal, yang umumnya diterima baik oleh pasien (Morris dkk., 2010). Pektin mempunyai beberapa sifat yang digunakan secara luas sebagai matriks untuk menjerap dan menghantarkan beberapa obat, protein dan sel (Ovodov, 2009).
2.3 Zink Klorida
Zink klorida memiliki pemerian serbuk hablur atau granul hablur, putih atau hampir putih. Dapat berupa massa seperti porselen atau berbentuk silinder. Sangat mudah mencair. Larutan (1 dalam 10) bereaksi asam terhadap lakmus. Senyawa ini mudah larut dalam air, mudah larut dalam etanol dan dalam gliserin. Larutan dalam air atau dalam etanol biasanya agak keruh, tetapi kekeruhan hilang jika ditambahkan sedikit asam klorida (Departemen Kesehatan RI, 1995). Zink klorida akan terionisasi menjadi Zn2+ dan 2Cl- di mana ion Zn2+ akan digunakan sebagai penyambung silang (crosslinker) dalam pembuatan nanopartikel zink-pektinat.
2.4 Natrium Klorida
Natrium klorida merupakan hablur bentuk kubus atau serbuk hablur putih, rasa asin. Senyawa ini mudah larut dalam air, sedikit lebih mudah larut dalam air mendidih, larut dalam gliserin, sukar larut dalam etanol (Departemen Kesehatan RI, 1995).
UIN Syarif Hidayatullah Jakarta Pada penelitian ini ion Na+ dari natrium klorida diharapkan berinteraksi dengan gugus karboksilat pektin untuk menyaring sebagian tolakan Coulomb sehingga konformasi rantai polimer pektin dapat berubah.
2.5 Nanopartikel sebagai Sistem Penghantaran Obat
Nanoteknologi adalah teknik untuk mendesain dan menyusun materi pada skala nano yang memungkinkan untuk memanfaatkan dan merekayasa struktur atom per atomnya (Yokoyama, 2007). Salah satu bidang penelitian yang paling aktif dari nanoteknologi adalah nanomedicine, yang menerapkan nanoteknologi untuk intervensi medis yang sangat spesifik untuk pencegahan, diagnosis dan pengobatan penyakit (Lobatto dkk., 2011). Nanopartikel merupakan bagian studi nanomedicine dalam sistem penghantaran obat.
Nanopartikel dapat didefinisikan sebagai partikel dengan berbagai bentuk yang memiliki ukuran dalam kisaran 1 sampai 1000 nm. (Jonassen, 2014). Nanopartikel terdiri dari nanokapsul dan nanosfer. Nanokapsul adalah sistem vesikular di mana obat hanya berada pada rongga yang dikelilingi oleh membran polimer, sedangkan nanosfer adalah sistem matriks di mana obat secara fisik tersebar merata dalam matriks polimer (Singh & Lillard, 2009). Nanopartikel harus bersifat stabil, tidak beracun, tidak trombogenik, tidak imunogenik, tidak memicu inflamasi, biodegradable, mencegah penyerapan oleh sistem retikulo endotel dan harus dapat diaplikasikan ke berbagai molekul seperti obat, protein, vaksin atau asam nukleat (Kumari, Yadaf & Yadaf, 2010)
Nanopartikel dapat terbuat baik dari unsur anorganik maupun organik (Jonassen, 2014). Dalam bidang farmasi, nanopartikel lebih banyak dibuat dari polimer alam. Polimer hidrofilik alam digunakan luas dalam berbagai industri farmasi untuk pengembangan sistem penghantaran obat baru karena sifat toksisitasnya yang rendah, biokompatibilitas dan biodegradabel (Chakraborty dkk., 2012). Polimer alam yang digunakan untuk nanopartikel penghantaran oral di antaranya kitosan, dekstran, gelatin, alginat, agar, dan di antaranya kitosan adalah yang paling populer (De Jong & Borm, 2008).
UIN Syarif Hidayatullah Jakarta dapat dimanfaatkan dalam formulasi obat hidrofobik, dengan peningkatan luas permukaan yang akan meningkatkan laju disolusi dan penyerapan obat (Merisko-Liversidge & (Merisko-Liversidge, 2008). Nanopartikel juga dapat diserap langsung oleh sel mukosa melalui endositosis (Fröhlich & Roblegg, 2012).
Selain ukuran dan bentuk, karakteristik permukaan nanopartikel juga dapat menentukan jangka hidup partikel selama sirkulasi dalam aliran darah. Salah satu kemajuan besar saat ini adalah temuan bahwa partikel yang dilapisi dengan molekul polimer hidrofilik, seperti PEG, dapat menahan adsorpsi protein serum, sehingga memperpanjang sirkulasi sistemik partikel (Bamrungsap dkk., 2012). Hal ini terjadi karena PEG memodifikasi muatan permukaan partikel. Muatan permukaan partikel mempengaruhi internalisasi oleh makrofag. Partikel bermuatan positif telah terbukti menunjukkan internalisasi yang lebih tinggi oleh makrofag dan sel dendritik, dibandingkan dengan partikel netral atau bermuatan negatif (Doshi, & Mitragotri, 2009).
Nanopartikel juga dapat berguna dalam meningkatkan stabilitas suatu agen terapeutik. Bahan farmasetik tertentu seperti protein dan peptida mudah terdegradasi ketika diberikan secara oral dan sering cepat tereliminasi setelah injeksi intravena (Balmayor, Azevedo & Reis, 2011). Penggabungan molekul obat dalam nanopartikel telah dimanfaatkan untuk melindungi bahan sejenis dari degradasi dan eliminasi fisiologis dini (Plapied, Duhem, des Rieux, & Préat 2011). Permukaan nanopartikel juga dapat dimodifikasi dengan ligan untuk penghantaran tertarget, misalnya penggabungan nanopartikel dengan folat untuk menargetkan sel kanker manusia yang mengekspresi reseptor folat berlebih (Bamrungsap dkk., 2012). Terdapat pula nanopartikel responsif rangsangan yang dapat menargetkan atau melepaskan obat di tempat yang diinginkan, atau setelah terpapar berbagai rangsangan, seperti perubahan fisiologis pada pH atau medan magnet eksternal yang diberikan (Ding & Ma, 2013).
UIN Syarif Hidayatullah Jakarta penargetan obat yang efisien. Stabilitas dispersi dan respon fisiologis primer terutama ditentukan oleh jenis surfaktan dan sifat lapisan luar. Sifat rilis dan degradasinya sangat tergantung pada komposisi dan struktur dinding kapsul (Gupta & Kumar, 2012).
Nanopartikel dalam sistem penghantaran obat memang telah memberikan banyak keuntungan. Namun demikian, masih terdapat kelemahan dalam nanopartikel sebagai nanocarrier (pembawa nano). Keterbatasan pembawa nano di antaranya:
a) Pembawa nano masih sulit dibuat, disimpan dan diberikan karena rentan terhadap agregasi.
b) Nanocarrier tidak cocok untuk obat yang efikasinya belum jelas.
c) Hal utama yang menjadi perhatian terkait dengan ukurannya yang kecil sebagai nanocarrier yaitu dapat masuk ke bagian tubuh yang tidak diinginkan dengan
konsekuensi berbahaya, misalnya dapat menyeberangi selubung nukleus sel dan menyebabkan kerusakan genetik dan mutasi yang tidak diinginkan (Gupta & Kumar, 2012).
2.6 Gelasi Ionik
Gelasi ionik merupakan metode pembuatan nanopartikel yang melibatkan proses sambung silang antar polielektrolit dengan adanya pasangan ion multivalennya. Gelasi ionik seringkali diikuti dengan kompleksasi polielektrolit dengan polielektrolit yang berlawanan. Pembentukan ikatan sambung dapat meningkatkan kekuatan mekanis dari partikel yang terbentuk (Iswandana, Effionora & Jufri, 2013).
Gelasi ionik adalah teknik sederhana dan cepat untuk pembuatan dispersi nanopartikel (Jonassen, Treves, Kjøniksen, Smistad & Hiorth, 2013). Penemu fenomena gelasi ionik adalah seorang ilmuwan koloid Jerman, Heinrich Thiele yang menggagas mekanisme pemisahan fase segregasi droplet. Proses gelasi;
Larutan Polimer + Elektrolit ↔ Gelisfer + Elektrolit + Air
UIN Syarif Hidayatullah Jakarta dapat merilis obat melalui kesatuan tersebut yang dikendalikan oleh relaksasi polimer (Patil, Chavanke, & Wagh, 2012).
Metode gelasi ion telah banyak digunakan pada proses enkapsulasi polisakarida alam seperti alginat, pektin, kitosan, dan karboksimetil selulosa (Patil, Chavanke, & Wagh, 2012). Penaut silang yang digunakan untuk gelasi ionik dapat dibagi menjadi dua macam yaitu penyambung silang dengan bobot molekul rendah misalnya kalsium klorida, barium klorida, magnesium klorida, zink asetat, pirofosfat, tripolifosfat, tetrapolifosfat, serta penyambung silang bobot molekul tinggi seperti lauril dan setilstearil sulfat (Racovita dkk., 2009).
Faktor-faktor yang mempengaruhi metode gelasi ionik: a) Konsentrasi polimer dan elektrolit sambung silang.
Konsentrasi polimer dan elektrolit memiliki pengaruh besar pada formulasi partikel dengan metode gelasi ionik. Konsentrasi keduanya harus dalam rasio tertentu yang dihitung dari jumlah unit sambung silang. Variasi persen efisiensi penjerapan berasal dari jenis elektrolit dan konsentrasi elektrolit.
b) Suhu
Suhu juga memainkan peran pada ukuran partikel yang dibentuk oleh metode gelasi ionik. Selain itu, waktu reaksi juga berpengaruh, yaitu waktu yang dibutuhkan untuk terbentuk ikatan silang.
c) pH larutan sambung silang
pH larutan sambung silang juga faktor yang dipertimbangkan selama formulasi karena menunjukkan efek pada laju reaksi, bentuk dan ukuran partikel.
d) Konsentrasi Obat
Obat yang akan terperangkap dalam partikel harus dalam rasio yang tepat dengan polimer, karena konsentrasi obat sangat mempengaruhi efisiensi penjerapan, jika rasio obat-polimer melebihi kisaran maka dapat dilihat efek bursting, densitas partikel meningkat serta ukuran dan bentuk dari partikel juga
meningkat.
e) Konsentrasi zat pembentuk gas
UIN Syarif Hidayatullah Jakarta membentuk partikel berpori, lapisan partikel rusak dan hasilnya permukaan tidak teratur (Patil, Chavanke, & Wagh, 2012).
Pektin memiliki kemampuan untuk membentuk gel dengan penyambung silang berupa kation divalen (ion zink atau ion kalsium) (Racovita dkk., 2009). Kalsium klorida adalah penyambung silang yang biasa digunakan untuk preparasi gel makroskopik pektin. Mekanisme sambung silang biasanya digambarkan oleh model egg-box, di mana Ca2+ yang bermuatan positif berinteraksi dengan dua gugus asam yang terpisah pada rantai polimer secara paralel (Sriamornsrak, 2011). Pembentukan gel pektin dengan dua mekanisme yaitu reaksi sambung silang berdasarkan model egg box dan ikatan hidrogen non ionik. (Chambin dkk., 2006).
2.7 Sifat dan Karaterisasi Fisik Nanopartikel Sambung Silang
2.7.1 Analisis Spektrum FT-IR
FTIR (Fourier Transform Infrared) merupakan metode analisis dengan memanfaatkan spektroskopi sinar inframerah yang dapat digunakan untuk mengidentifikasi kandungan gugus kompleks pada senyawa dengan melihat ikatan-ikatan yang dihasilkan. Pada FTIR radiasi inframerah ditembakkan pada sampel. Sebagian dari radiasi inframerah diserap oleh sampel dan sebagian lainnya diteruskan. Frekuensi dari suatu vibrasi akan menentukan spektrum yang dihasilkan dengan penggambaran transmitan. Dari spektrum inilah dilihat ikatan-ikatan apa saja yang berubah maupun yang dihasilkan dari sampel (Harahap, 2012).
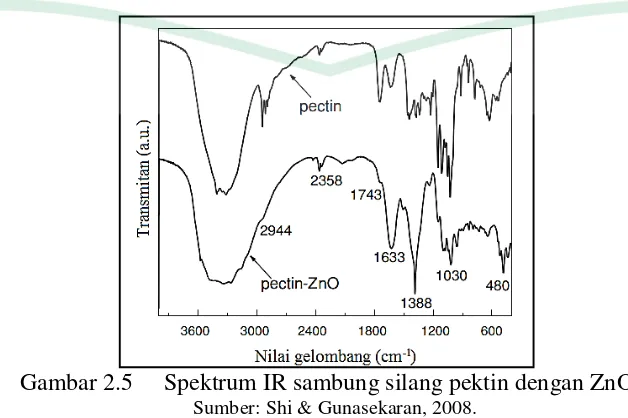
Gambar 2.5 Spektrum IR sambung silang pektin dengan ZnO.
UIN Syarif Hidayatullah Jakarta 2.7.2 Persen Efisiensi Penjerapan
Istilah efisiensi penjerapan berhubungan dengan jumlah obat yang terkandung dalam nanopartikel. Kandungan obat menyatakan persen berat bahan aktif terjerap dengan berat nanopartikel, sedangkan efisiensi penjerapan adalah rasio persentase eksperimen dari jumlah obat yang ditentukan dibanding dengan jumlah obat yang diberikan, atau massa teoritis obat yang digunakan untuk penyusunan nanopartikel (Kharia, Singhai, & Verma, 2012).
Efisiensi penjerapan bergantung pada kombinasi obat polimer dan metode yang digunakan. Polimer hidrofobik menjerap jumlah yang lebih besar dari obat hidrofobik, sedangkan polimer hidrofilik menjerap jumlah yang lebih besar dari obat yang lebih hidrofilik. Beberapa parameter formulasi, seperti jenis emulsifier, rasio berat polimer terhadap obat, dan rasio organik fase berair, akan mempengaruhi tingkat muatan obat (Kharia, Singhai, & Verma, 2012).
2.7.3 Ukuran Partikel dan Indeks Polidispersitas
Ukuran partikel dan distribusi ukuran partikel merupakan faktor penting dalam nanopartikel, di mana nanopartikel dengan distribusi ukuran partikel luas menunjukkan variasi yang signifikan dalam pemuatan dan pelepasan obat, bioavailabilitas, serta efikasi (Kharia, Singhai, & Verma, 2012). Menurut Jonassen (2014), suatu partikel dapat disebut nanopartikel jika memiliki kisaran ukuran 10-1000 nm.
Indeks polidispersitas adalah parameter yang menyatakan distribusi ukuran partikel dari sistem nanopartikel (Nidhin dkk., 2008), di mana rentang nilai 0,1-0,25 menunjukkan distribusi ukuran yang sempit, sementara nilai lebih dari 0,5 menunjukkan distribusi yang luas (Lu dkk., 2011). Nilai ini menunjukan hasil perhitungan dari berat rata-rata berat molekul dibagi dengan jumlah rata-rata berat molekul. Semakin mendekati nol berarti distribusinya semakin baik (Haryono, Restu & Harmami, 2012).
UIN Syarif Hidayatullah Jakarta Light Scattering /DLS) (Cho dkk., 2013). Hamburan cahaya dinamis adalah teknik
non-invasif dan baik untuk mengukur ukuran dan distribusi ukuran partikel di wilayah submikron, dan juga dapat digunakan untuk mempelajari perilaku cairan kompleks, seperti konsentrat larutan polimer (Jonnasen, 2014).
Ukuran partikel yang diukur menggunakan DLS merupakan nilai dari diameter lingkaran partikel yang terdifusi dengan kecepatan yang sama pada saat pengukuran (Shabrina, 2011). Diameter tersebut disebut juga diameter hidrodinamik. Diameter yang diperoleh dengan teknik ini merujuk pada asumsi bentuk sferik partikel yang memiliki koefisien difusi translasi sama dengan partikel yang diukur (Malvern Instruments Worldwide, 2012).
Gambar 2.6 Ilustrasi diameter hidrodinamik
Sumber: Malvern Instruments Worldwide, 2012
Ukuran partikel dihitung dari koefisien difusi translasi dengan menggunakan persamaan Stokes-Einstein;
d =
πηT (2.1)di mana dh merupakan diameter hidrodinamik, k adalah konstanta
Boltzman, T adalah temperature dalam satuan Kelvin, D merupakan koefisien difusi translasi dan merupakan viskositas medium pendispersi.
Gambar 2.7 Skema ilustrasi percobaan DLS.
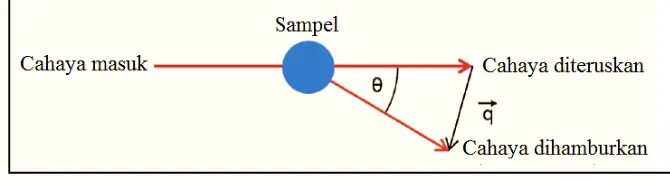
UIN Syarif Hidayatullah Jakarta Penentuan ukuran partikel dengan DLS juga memanfaatkan pemendaran cahaya akibat gerak Brown yang terjadi pada partikel submikron dalam medium pendispersi tertentu. Pada saat pengukuran, pancaran berkas cahaya monokromatik dari alat ke larutan berpartikel sferis dalam gerak Brown menyebabkan pergeseran Doppler, sehingga mengubah panjang gelombang cahaya yang masuk (Sartor, 2003).
Perbedaan besaran antara cahaya yang diteruskan dengan cahaya yang dihamburkan disebut vektor gelombang (q). Vektor gelombang didefinisikan sebagai;
q =
πn sinθ
λL (2.2)
di mana λL adalah panjang gelombang cahaya insiden dalam ruang hampa,
di mana adalah sudut hamburan, dan n adalah indeks bias sampel (Jonnasen dkk., 2014).
Oleh karena partikel terus bergerak intensitas cahaya yang diterima detektor berfluktuasi konstan. Tingkat di mana fluktuasi intensitas terjadi bergantung pada ukuran partikel. Partikel-partikel kecil menyebabkan intensitas berfluktuasi lebih cepat daripada yang besar. Sistem dari instrumen akan mengukur tingkat fluktuasi intensitas dan kemudian menggunakan hal tersebut untuk menghitung ukuran partikel.
Berkaitan dengan fluktuasi intensitas yang diterima, maka dibuat sebuah autokorelator sebagai pembanding sinyal. Hal ini dirancang untuk mengukur tingkat kesamaan antara dua sinyal, atau satu sinyal dengan dirinya sendiri pada interval waktu yang berbeda-beda. Autokorelator ini berguna untuk menafsirkan ukuran partikel dari data fluktuasi sinyal yang diterima.
2.7.4 Potensial Zeta
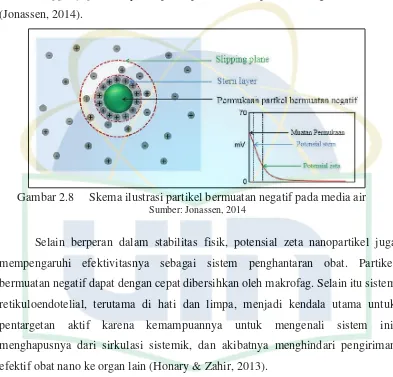
UIN Syarif Hidayatullah Jakarta Partikel bermuatan dalam dispersi cair dikelilingi oleh ion dalam lapisan ganda listrik. Lapisan ganda cair ini terdiri dari bagian dalam (stern layer) dengan ion berlawanan (dari permukaan partikel) yang terikat relatif kuat, dan wilayah luar dengan ion yang terikat kurang kuat. Potensial zeta adalah potensial listrik di bidang terluar (slipping plane), yaitu pada permukaan lapisan cair ganda stationer (Jonassen, 2014).
Gambar 2.8 Skema ilustrasi partikel bermuatan negatif pada media air
Sumber: Jonassen, 2014
Selain berperan dalam stabilitas fisik, potensial zeta nanopartikel juga mempengaruhi efektivitasnya sebagai sistem penghantaran obat. Partikel bermuatan negatif dapat dengan cepat dibersihkan oleh makrofag. Selain itu sistem retikuloendotelial, terutama di hati dan limpa, menjadi kendala utama untuk pentargetan aktif karena kemampuannya untuk mengenali sistem ini, menghapusnya dari sirkulasi sistemik, dan akibatnya menghindari pengiriman efektif obat nano ke organ lain (Honary & Zahir, 2013).
UIN Syarif Hidayatullah Jakarta karbohidrat yang ditemukan di sel mamalia mengandung gugus bermuatan negatif (Honary & Zahir, 2013).
Nanopartikel dengan muatan positif lebih cenderung diserap oleh sel tumor dan waktu retensi yang lebih lama dibandingkan dengan partikel bermuatan negatif atau netral karena fosfatidil serin, residu bermuatan negatif, ditranslokasikan ke permukaan sel kanker dan nanopartikel dengan muatan positif dapat ditranslokasikan oleh sel-sel tumor baik melalui endositosis, atau interaksi muatan dan penambatan ligan-reseptor (Honary & Zahir, 2013).
2.7.5 Differential Scanning Calorimetry (DSC)
DSC adalah teknik analisis termal yang paling sering digunakan. Teknik ini dikembangkan oleh E. S. Watson dan M. J. O'Neill pada tahun 1962 dan diperkenalkan secara komersial pada 1963 dalam Konferensi Kimia Analitik dan Spektroskopi Terapan Pittsburgh (O’Neill & Watson, 1966). Sejak saat itu, DSC banyak digunakan pada berbagai disiplin ilmu.
Analisis DSC digunakan untuk mengukur perubahan entalpi atau perubahan kapasitas panas dalam sampel sebagai fungsi temperatur atau waktu. Selain itu, DSC dapat menentukan kapasitas panas (heat capacity), suhu perubahan dari keadaan kaku ke keadaan elastis (Tg), suhu pembentukan kristal (Tc), suhu perubahan dari padat menjadi cair (Tm), dan derajat pengkristalan (cristallinity) (Jumadi & Sari, 2014).
UIN Syarif Hidayatullah Jakarta Hasil percobaan DSC adalah kurva fluks panas terhadap suhu atau terhadap waktu. Selain dapat digunakan untuk mengidentifikasi parameter yang telah disebutkan sebelumnya, kurva ini juga dapat digunakan untuk menghitung entalpi transisi. Hal tersebut dapat dilakukan dengan mengintegrasikan puncak sesuai dengan transisi yang diberikan. Entalpi transisi dapat dinyatakan dengan menggunakan persamaan berikut:
∆H = KA
21 UIN Syarif Hidayatullah Jakarta BAB 3
METODOLOGI PENELITIAN
3.1 Waktu dan Tempat Penelitian
Penelitian dilaksanakan di Laboratorium Penelitian II, Laboratorium Kimia Obat, Laboratorium Farmakologi, Laboratorium Formulasi Sediaan Padat, dan Laboratorium Kesehatan Lingkungan Fakultas Kedokteran dan Ilmu Kesehatan, Universitas Islam Negeri Syarif Hidayatullah Jakarta, dalam kurun waktu Januari -Juni 2015.
3.2 Bahan dan Alat
3.2.1 Bahan
Pektin (Grindsted Pectin LA 415, Danisco, Amerika), diltiazem hidroklorida (Dr. Reddy's, India), zink klorida (Merck, Jerman), natrium klorida (Merck, Jerman), akuades.
3.2.2 Alat
Neraca analitik (GH-202, AND, Jepang), pengaduk magnetik (Nuova Strirrer, Thermolyne, Amerika), overhead stirrers (RW 20 Digital, IKA) buret (50 ml, Pyrex), sonicator bath (Bransonic 5510J-MT, Branson Ultrasonic, Amerika) spektrofotometer inframerah (IRPrestige-21, Shimadzu, Jepang), spektrofotometer UV-VIS (U-2900, Hitachi, Amerika), particle size analyzer (VASCO-Particle Size Analyzer, Particulate Systems, Amerika), zeta analyzer (Delsa Nano C, Beckman Coulter, Amerika), sentrifus (EBA 20, Hettich Zentrifugen, Inggris), vortex (Wiggen Houser), differential scanning calorimeter (DSC 60, Shimadzu, Jepang), dan alat gelas.
3.3 Prosedur Kerja
3.3.1 Preparasi Larutan NaCl 0,05 M
UIN Syarif Hidayatullah Jakarta 3.3.2 Preparasi Nanopartikel Diltizem Hidroklorida
Optimasi jumlah bahan dalam preparasi nanopartikel berdasarkan penelitian Jonassen, Treves, Kjøniksen, Smistad & Hiorth (2013). Preparasi dilakukan pada konsentrasi awal pektin 0,0875% dan ZnCl2 0,062%. Perbandingan jumlah pektin
dengan diltiazem hidroklorida adalah 1:1 (b/b) (Adiningsih, 2012). Gelasi dilakukan pada medium akuades dan NaCl 0,05 M. Perbandingan jumlah larutan ZnCl2 dan larutan pektin yang akan dicampurkan adalah 1:4 (v/v). Proses gelasi
yang pada umumnya dilakukan di bawah pengaduk magnetik dimodifikasi dengan ultrasonikasi selama 60 menit
Tabel 3.1 Formula preparasi nanopartikel.
a) Formula 1
Sebanyak 87,5 mg pektin didispersikan dalam 100 mL larutan NaCl 0,05 M di bawah pengaduk magnetik. Setelah terdispersi sempurna, pengadukan larutan pektin dilanjutkan dengan overhead stirrers selama 1 jam. Dalam wadah lain, zink klorida sebanyak 31 mg dilarutkan dalam 50 mL larutan NaCl 0,05 M. Masing-masing larutan disaring terpisah menggunakan membran penyaring berpori 0,45 µm. Larutan zink klorida dimasukkan ke dalam buret yang ujungnya telah diberi jarum suntik 23G. Sementara itu 40 mL larutan pektin ditempatkan didalam gelas beacker 250 mL yang telah diberi pelampung dari bahan sterefoam.
Sebanyak 10 mL larutan ZnCl2 tetes demi tetes ditambahkan ke dalam
larutan pektin di bawah pengaruh ultrasonikasi menggunakan alat sonicator bath. Kecepatan rata-rata tetesan larutan ZnCl2 0,17 mL/menit. Setelah penambahan
larutan ZnCl2 selesai, campuran didiamkan dalam pengaruh ultrasonikasi selama 1
jam. Selama proses preparasi suhu dijaga 25oC.
b) Formula 2
UIN Syarif Hidayatullah Jakarta terdispersi sempurna, pengadukan campuran diltiazem hidroklorida-pektin dilanjutkan dengan overhead stirrers selama 1 jam. Dalam wadah lain, zink klorida sebanyak 31 mg dilarutkan dalam 50 mL larutan NaCl 0,05 M. Masing-masing larutan disaring terpisah menggunakan membran penyaring berpori 0,45 µm. Prosedur selanjutnya sama seperti pada formula 1.
c) Formula 3
Prosedur yang dilakukan pada formula 3 sama dengan formula 2. Perbedaan dilakukan pada medium pendispersi di mana pada formula 3 diganti menjadi akuades.
3.3.3 Pengeringan Nanopartikel (Shi & Gunasekaran, 2008)
Sebanyak 13 mL suspensi nanopartikel disentrifugasi pada 6000 rpm selama 15 menit. Kemudian supernatan dan sedimen hasil sentrifugasi dipisahkan. Supernatan akan digunakan untuk pengukuran persen efisisensi penjerapan sementara sedimen digunakan untuk analisis spektrum inframerah dan differential scanning calorimetry.
Sedimen nanopartikel didispersikan kembali dalam akuades dengan alat vortex. Dispersan disentrifugasi lagi untuk memperoleh kembali sedimen. Perlakuan tersebut dilakukan dua kali untuk menghilangkan pengotor pada sedimen nanopartikel. Kemudian sedimen diliofilisasi selama 12 jam untuk mendapatkan nanopartikel kering dengan menggunakan alat freeze dryer.
3.4 Karakterisasi Nanopartikel
3.4.1 Perubahan Transmitan (%) Suspensi Nanopartikel
Sebanyak 3 mL suspensi nanopartikel diukur persen transmitan dengan menggunakan spektrofotometer UV-Vis pada panjang gelombang 600 nm. Pengukuran dilakukan secara triplo. Larutan pektin dan campuran pektin-diltiazem hidroklorida sebelum disambung silang menjadi pembanding. Penurunan transmitan dihitung sebagai berikut:
RT % = T −TT × % (4.1)
UIN Syarif Hidayatullah Jakarta 3.4.2 Penetapan Ukuran Partikel dan Indeks Polidispersitas (Sharma, Ahuja
& Kaur, 2012 dan Yurika, 2012)
Tiga tetes suspensi nanopartikel ditentukan ukuran dan indeks polidispersitas partikelnya menggunakan teknik Dynamic Light Scattering (DLS) dengan alat Particle Size Analyzer (PSA).
3.4.3 Penetapan Potensial Zeta (Jonassen, Treves, Kjøniksen, Smistad & Hiorth, 2013)
Sebanyak 0,7 mL suspensi nanopartikel ditempatkan ke dalam flow cell lalu dikarakterisasi sifat elektrokinetiknya pada 25oC menggunakan alat zeta analyzer.
3.4.4 Penetapan Efisiensi Penjerapan (%) Diltiazem Hidroklorida
Pengukuran persen efisiensi penjerapan dilakukan pada formula B dan C untuk mempelajari pengaruh penambahan NaCl terhadap jumlah obat terjerap dalam nanopartikel.
3.4.4.1 Pembuatan Spektrum Serapan dan Penentuan Panjang Gelombang Maksimum Diltiazem
Larutan diltiazem hidroklorida dengan konsentrasi 9 ppm dibuat dalam larutan NaCl 0,05 M dan akuades, kemudian diukur serapannya pada panjang gelombang 200-400 nm.
3.4.4.2 Pembuatan Kurva Kalibrasi
UIN Syarif Hidayatullah Jakarta 3.4.4.3 Pengukuran Efisiensi Penjerapan (%) Diltiazem Hidroklorida (Sahu,
Kumar & Jain, 2014)
Jumlah diltiazem hidroklorida bebas dalam supernatan hasil sentrifugasi dihitung dengan mengukur absorbansinya dalam spektofotometer UV-Vis. Efisiensi penjerapan nanopartikel dihitung sebagai rasio diltiazem hidroklorida yang terjerap ke dalam nanopartikel dibandingkan dengan jumlah total diltiazem klorida yang digunakan dalam pembuatan nanopartikel. Secara matematis persen efisiensi penjerapan sebagai berikut;
EE % = J J − J × % (4.2)
Dimana EE (%) adalah efisiensi penjerapan (%).
3.3.6 Analisis Spektrum Inframerah (Shi & Gunasekaran, 2008)
Spektrum inframerah dari nanopartikel kering dilihat pada daerah 4000-400 cm dengan menggunakan spektofotometer FT-IR. Serbuk disiapkan menggunakan KBr dalam bentuk pellet. Sebagai pembanding, spektrum FT-IR pektin juga dianalisis.
3.3.7 Analisis Differential Scanning Calorimetry (Hu dkk., 2015)
Sifat termal dari nanopartikel kering dikarakterisasi menggunakan differential scanning calorimeter (DSC). Tujuh miligram nanopartikel kering
26 UIN Syarif Hidayatullah Jakarta BAB 4
HASIL DAN PEMBAHASAN
4.1 Preparasi Nanopartikel
Preparasi nanopartikel dibuat dengan tiga formula, yaitu formula 1, 2 dan 3. Formula 1 merupakan nanopartikel zink pektinat kosong yang dibuat dalam medium NaCl 0,05 M. Formula ini dijadikan sebagai acuan (blanko) untuk mengetahui perubahan karakteristik nanopartikel akibat penambahan diltiazem hidroklorida. Formula 2 merupakan nanopartikel zink pektinat mengandung diltiazem hidroklorida yang dibuat dalam medium NaCl 0,05 M. Perbedaan karakteristik fisik antara formula 1 dan 2 akibat penambahan diltiazem hidroklorida menjadi parameter yang akan diteliti dalam penelitian ini. Formula 3 merupakan nanopartikel zink pektinat mengandung diltiazem hidroklorida yang dibuat dalam medium akuades. Perbandingan karakteristik fisik antara formula 2 dan 3 juga akan menjadi parameter yang akan diteliti sebagai akibat perbedaan medium preparasi nanopartikel.
Metode yang digunakan dalam preparasi nanopartikel adalah metode gelasi ionik. Metode ini dipilih dalam preparasi nanopartikel karena dinilai sebagai metode yang paling mudah dilakukan. Proses gelasi utamanya terjadi karena sambung silang antara gugus COO- pektin dengan ion Zn2+. Sambung silang yang terbentuk ini disebut model egg-box, di mana rantai galakturonat terikat bersama dengan ion penyambung silang yang berada di antara rantai tersebut, sehingga diibaratkan seperti telur dalam sebuah kotak telur (Chambina, Dupuis, Champion, Voilley & Pourcelot, 2006). Interaksi hidrofobik dan ikatan hidrogen yang diinduksi gugus amida juga berkontribusi pada proses gelasi (Jonassen dkk., 2013) Terdapat dua fase cair dalam preparasi, di antaranya fase polimer-obat dan fase penyambung silang. Fase polimer-obat berisi pektin dan diltiazem hidroklorida sedangkan fase penyambung silang berisi ZnCl2. Kedua fase tersebut dibuat
UIN Syarif Hidayatullah Jakarta diltiazem diadaptasi sesuai dengan penelitian Adiningsih (2012), yaitu setara dengan jumlah pektin (b/b).
Larutan polimer pada formula 1 serta larutan polimer-obat pada formula 2 dan 3 terlebih dahulu diaduk dengan overhead strirrers selama 1 jam sebelum dicampurkan dengan larutan penyambung silang. Hal ini dilakukan untuk memaksimalkan semua komposisi larutan polimer-obat agar terdispersi sempurna. Selain itu pada formula 2 dan 3, perlakuan ini diharapkan dapat mendorong molekul diltiazem hidroklorida agar terperangkap dalam kumparan rantai polimer pektin. Selanjutnya, kedua larutan tersebut disaring secara terpisah menggunakan membran filter berpori 0,45 µm untuk menghilangkan pengotor dan komponen lain yang tidak larut.
Proses gelasi dilakukan dengan mencampurkan fase penyambung silang ke dalam fase polimer-obat tetes demi tetes. Kecepatan tetesan dibuat konstan dengan harapan distribusi ukuran partikel yang dihasilkan homogen. Biasanya reaksi antara polimer dan penyambung silang dibantu dengan pengadukan kecepatan tinggi menggunakan pengaduk magnetik. Akan tetapi, pengadukan tersebut dapat menimbulkan buih yang berpotensi mengganggu proses gelasi (Iswandana, Anwar & Jufri, 2013). Pengadukan dengan pengaduk magnetik juga dapat menyebabkan hasil gelasi menempel pada magnet pengaduk. Berdasarkan pertimbangan tersebut, reaksi gelasi dilakukan dengan bantuan ultrasonikasi.
Penggunaan ultrasonik pada dasarnya memanfaatkan sifat kuvitasi akustik gelombang ultrasonik yang dapat merambat melalui medium yang dilewati. Pada saat gelombang merambat, medium yang dilewati akan mengalami getaran. Getaran tersebut akan memberikan pengadukan yang intensif terhadap proses gelasi. Suhu gelasi dijaga 25oC untuk menghindari efek hidrotermal saat sonikasi yang dapat mengoyak partikel dan mengganggu kristalinitas sehingga memberikan partikel lebih amorf (Sahroni, Darmawan & Sumarno, 2014).
UIN Syarif Hidayatullah Jakarta berupa pengukuran penurunan transmitansi (%) untuk menilai perbedaan kekeruhan yang dihasilkan pada tiap formula.
Gambar 4.1 Hasil preparasi nanopartikel (a) formula 1, (b) formula 2, dan (c) formula 3.
4.2 Penurunan Transmitansi (%)
Pengukuran penurunan transmitansi (%) dilakukan sebagai pengujian awal untuk memastikan sistem telah membentuk suspensi nanopartikel. Selain itu, pengujian ini bertujuan untuk menilai perbedaan tingkat kekeruhan tiap formula. Pengujian ini memanfaatkan aktivitas pemendaran cahaya oleh partikel akibat efek Tyndall-Faraday. Transmitan larutan sebelum dan setelah proses sambung silang ditentukan, serta selisih antara keduanya didefinisikan sebagai penurunan transmitan. Adanya penurunan transmitan menjadi indikator perubahan fase sistem dari dispersi molekuler menjadi dispersi partikulat (koloid).
UIN Syarif Hidayatullah Jakarta Gambar 4.2 Penurunan transmitan (%) suspensi nanopartikel
Besar penurunan transmitansi (%) formula 3 > formula 1 > formula 2. Formula 3 memiliki penurunan transmitansi paling besar yang dapat memprediksi kemungkinan ukuran atau jumlah partikel yang dihasilkan lebih besar dibandingkan formula 1 dan 2, serta seterusnya pada formula 1.
3.3 Ukuran Partikel dan Indeks Polidispersitas
Penentuan ukuran partikel dan distribusi ukuran partikel merupakan faktor penting dalam preparasi nanopartikel. Ukuran partikel berpengaruh terhadap pelepasan obat dan kestabilan nanopartikel. Semakin kecil ukuran partikel dapat memberikan pelepasan obat yang lebih baik. Sementara itu, ukuran partikel yang semakin kecil biasanya menunjukkan kestabilan yang semakin rendah. Penentuan ukuran partikel dilakukan secara tidak langsung menggunakan prinsip hamburan cahaya dinamis dengan alat particle size analyzer (PSA).
Menurut Jonassen (2014), suatu partikel dapat disebut nanopartikel jika memiliki kisaran ukuran 10-1000 nm. Dari penentuan ukuran partikel dengan PSA diketahui bahwa semua formula telah memasuki rentang ukuran nanopartikel. Ukuran partikel yang berbeda ditunjukkan pada tiap formula di mana formula 1 memiliki rentang ukuran partikel terkecil sedangkan formula 3 yang terbesar. Hasil tersebut disebabkan adanya beberapa parameter preparasi yang berbeda di tiap formula yang dapat menunjukkan pengaruhnya terhadap ukuran partikel.
9,37 6,53
8,60
4 5 6 7 8 9 10
UIN Syarif Hidayatullah Jakarta Tabel 4.1 Ukuran partikel dan indeks polidispersitas.
Konsentrasi polimer, penyambung silang, obat dan pH medium pendispersi (Patil, Chavanke, & Wagh, 2012), merupakan parameter umum yang dapat mempengaruh preparasi nanopartikel dengan metode gelasi ionik. Selain itu, kekuatan ion pelarut juga dapat mempengaruhi ukuran nanopartikel yang dihasilkan (Jonassen, Kjøniksen & Hiorth, 2013). Pada tahap pengujian ini, dipelajari pengaruh penambahan obat dan kekuatan ion pelarut terhadap ukuran nanopartikel. Formula 2 memiliki ukuran nanopartikel yang lebih besar dibandingan dengan formula 1. Parameter yang berbeda antara formula 1 dan 2 adalah keberadaan obat, di mana formula 2 mengandung diltiazem hidroklorida sedangkan formula 1 tidak. Pada formula 2, keberadaan molekul dilitazem hidroklorida dalam kumparan rantai polimer pektin mungkin dapat meningkatkan ruang geometri kumparan rantai polimer sehingga dihasilkan ukuran partikel yang lebih besar dibanding formula 1.
Gambar 4.3 Grafik ubungan pH terhadap formula.
Penambahan diltiazem hidroklorida juga dapat menurunkan pH formula akhir. Oleh karena pH diturunkan, ionisasi dari gugus karboksilat pada pektin ditekan, dan hal ini menyebabkan pengurangan hidrasi gugus asam karboksilat.
Formula Ukuran Partikel (nm) PDI
1 433,82 0,2580
2 502,41 0,0030
3 765,47 0,0070
4.919 4.434
4.676
4.0 4.2 4.4 4.6 4.8 5.0
pH
UIN Syarif Hidayatullah Jakarta Sebagai hasil dari pengurangan ionisasi, antarmolekul polisakarida tidak lagi saling tolak disepanjang rantai polimernya (Sriamornsak, 2003). Penurunan tolakan ini meningkatkan potensi sambung silang intermolekul yang dapat menyebabkan peningkatan ukuran partikel. Meskipun perbedaan pH antara formula 1 dan 2 tidak signifikan, hal ini menunjukkan perubahan sedikit pH masih dapat merubah karakteristik fisik nanopartikel yang dihasilkan.
Gambar 4.4 Konformasi rantai polimer pektin, (a) dalam akuades sebelum sambung silang, (b) dalam NaCl 0,05 M sebelum sambung silang, (c) dalam akuades setelah sambung silang dan (d) dalam NaCl 0,05 M setelah sambung silang.
UIN Syarif Hidayatullah Jakarta Formula 3 memiliki ukuran partikel yang lebih besar dibanding formula 2. Medium preparasi sistem nanopartikel formula 3 berupa akuades sedangkan formula 2 berupa NaCl 0,05 M. Polimer pektin yang berada dalam medium air akan terionisasi, sehingga memiliki konformasi terentang karena tolakan elektrostatik. Sementara itu, keberadaan garam NaCl 0,05 M pada formula 2 akan menyaring beberapa tolakan elektrostatik di antara rantai polimer yang mendorong pengurangan muatan. Kondisi ini menyebabkan berkurangnya konformasi rantai polimer yang terentang dan lebih banyak kumparan polimer kompak dalam larutan, serta mencegah pembentukan jaringan polimer (Jonassen, Treves, Kjøniksen, Smistad, & Hiorth, 2013). Perbedaan konformasi rantai polimer ini menyebabkan perbedaan ukuran partikel yang dihasilkan formula 2 dan 3.
Pengukuran distribusi ukuran partikel menunjukkan indeks polidispersitas formula 1 sebesar 0,258, formula 2 sebesar 0,003, dan formula 3 sebesar 0,007. Formula 2 dan 3 menghasilkan indeks polidispersitas di bawah 0,25 yang menunjukkan hasil preparasi memberikan distribusi ukuran yang sempit. Formula 1 yang memiliki indeks polidispersitas sedikit diatas 0,25 juga masih dianggap memiliki distribusi ukuran yang sempir. Hal ini berarti semua hasil preparasi memiliki homogenitas ukuran partikel yang baik.
Informasi mengenai ukuran partikel dapat melengkapi penjelasan besarnya penurunan transmitan yang berbeda pada setiap formula. Formula 1 memiliki ukuran partikel yang lebih kecil namun menghasilkan penurunan transmitansi (%) lebih besar dibandingkan formula 2. Hal ini disebabkan jumlah nanopartikel yang dihasilkan pada formula 2 lebih sedikit dibandingkan formula 1. Sementara itu, formula 3 yang memiliki ukuran partikel paling besar mendukung data yang menyatakan bahwa penurunan transmitansi (%) pada formula tersebut juga paling besar.
4.4 Potensial Zeta
UIN Syarif Hidayatullah Jakarta terdispersi, karena potensial ini mengatur derajat tolak-menolak antara partikel-partikel terdispersi yang bermuatan sama dan saling berdekatan (Sinko, 2006).
Potensial zeta sistem nanopartikel diukur menggunakan alat zeta analyzer. Dari hasil pengukuran, potensial zeta formula 1, 2 dan 3 masing-masing sebesar +80,13 mV,-16,72 mV, dan +76,51 mV. Nanopartikel dengan nilai potensial zeta lebih dari ±30 mV telah terbukti stabil dalam suspensi sebagai muatan permukaan yang mencegah agregasi (Mohanraj & Chen, 2006). Dalam hal ini berarti formula 1 dan 3 memiliki sistem nanopartikel yang stabil sedangkan formula 2 tidak.
Gambar 4.5 Hubungan potensial zeta terhadap formula
Formula 1 dan 3 memiliki potensial zeta bernilai positif. Nilai positif atau negatif potensial zeta dipengaruhi oleh muatan permukaan partikel dari pektin yang mengandung gugus fungsional yang dapat terionisasi (Doymus, 2007). Dalam penelitian ini, pektin yang digunakan memiliki gugus fungsional COOH yang ketika terioniasi bermuatan negatif, serta gugus NH2 yang ketika terionisasi
bermuatan positif. Semua sistem nanopartikel yang dibuat memiliki pH rendah berkisar 4 yang menyebabkan ionisasi gugus karboksil pektin ditekan (Sriamornsak, 2003) sedangkan gugus amida ditingkatkan sesuai kaidah pH-partisi. Selain itu, gugus bermuatan negatif juga mengalami netralisasi oleh ion Zn2+ melalui proses sambung silang. Oleh karena jumlah muatan negatif lebih sedikit, resultan muatan permukaan partikel menjadi positif sehingga menyebabkan potensial zeta nanopartikel bernilai positif.
80.13
UIN Syarif Hidayatullah Jakarta Gambar 4.6 Gugus fungsional pektin.
(Sumber: Kral dkk., 2011)
Berbeda dengan formula 1 dan 3, nanopartikel formula 2 memiliki potensial zeta bernilai negatif. Hal ini mungkin disebabkan karena pengaruh kekuatan ion pelarut pada potensial zeta sistem nanopartikel. Kekuatan ion pelarut formula 2 meningkat dengan penambahan NaCl dan diltiazem hidroklorida. Hal ini berpengaruh pada potensial zeta sebagai akibat dari berubahnya komposisi dan jumlah kation dan anion dalam sistem nanopartikel. NaCl akan menyumbangkan ion Na+ dan Cl-, sedangkan diltiazem akan menyumbangkan ion Cl-.
Pengaruh ion terhadap potensial zeta berhubungan dengan Hukum Schultze-Hardy yang menyatakan muatan-muatan yang berlawanan dapat menghasilkan netralisasi muatan permukaan koloid sehingga mengakibatkan potensial zeta menuju nol (Sukardjo, 1997). Pengaruh ion terhadap potensial zeta suatu partikel hidrofilik tergambar dalam suatu deret Hofmeister, di mana untuk anion CO32- >
SO42- > HPO42- > OH- > F- > HCOO- > CH3COO- > Cl- > Br- > NO3- > ClO3- > I- >
ClO4-> SCN-, dan untuk kation Ca2+ > Mg2+ > Li+ > Na+ >K+ > Rb+ > Cs+> NH4+ (Salgin, Salgin & Bahadir, 2012). Berdasarkan deret Hofmeister, ion Na+ dan Cl -diprediksi memiliki pengaruh yang moderat terhadap perubahan potensial zeta, sedangkan ion Zn2+ tidak dapat diprediksi dengan deret Hofmeister.
UIN Syarif Hidayatullah Jakarta yang berlebih dapat diserap dibandingkan dengan kebutuhan untuk menetralkan muatan permukaan. Hal ini dapat menyebabkan perubahan potensial zeta nanopartikel dari positif ke negatif. Penurunan nilai potensial zeta oleh anion berkorelasi dengan data yang menunjukkan bahwa estimasi ion Cl- pada formula 2 lebih banyak dibandingkan formula 1 dan 3.
Tabel 4.2 Estimasi jumlah ion dalam 50 mL suspensi nanopartikel
Aktivitas penurunan potensial zeta oleh anion diperkuat dengan menurunnya pH sistem nanopartikel. Semakin asam pH medium, maka jumlah gugus basa (NH2)
yang terionisasi akan semakin banyak (Sinko, 2006). Peningkatan gugus basa yang terionisasi meningkatkan muatan positif permukaan partikel, sehingga meningkatkan kecendurungan ion dengan muatan berlawanan untuk diserap. Aktivitas penurunan potensial zeta oleh anion pada formula 2 paling besar karena pH sistem pelarutnya paling kecil dibanding formula lain.
4.5 Efisiensi Penjerapan (%) Diltiazem Hidroklorida
Pengujian efisiensi penjerapan (%) dilakukan untuk mengetahui jumlah diltiazem hidroklorida yang terjerap dalam matriks nanopartikel. Selain itu, evaluasi ini juga bertujuan untuk mengetahui pengaruh perbedaan medium preparasi nanopartikel terhadap efisiensi penjerapan (%) diltiazem hidroklorida. Pengujian dilakukan pada formula 2 dengan medium preparasi NaCl 0,05 M dan formula 3 dengan medium preparasi akuades.
Efisiensi penjerapan (%) dari nanopartikel ditentukan secara tidak langsung melalui pemisahan nanopartikel dengan sentrifugasi 6000 rpm selama 15 menit dari medium yang mengandung diltiazem hidroklorida bebas. Selanjutnya jumlah diltiazem hidroklorida bebas pada supernatant dihitung dengan spektofotometri pada panjang gelombang 236 nm. Efisiensi penjerapan nanopartikel dihitung sebagai rasio jumlah diltiazem terjerap terhadap jumlah diltiazem hidroklorida yang ditambahkan ketika preparasi (Sharma, Ahuja & Kaur, 2012). Jumlah diltiazem
Formula Jumlah Ion (mEq)
Na+ Zn2+ Cl
-1 2,5 0,049 2,5910
2 2,5 0,049 2,6686
UIN Syarif Hidayatullah Jakarta hidroklorida yang terjerap sendiri merupakan selisih dari jumlah diltiazem hidroklorida yang ditambahkan ketika preparasi dengan jumlah diltiazem hidroklorida bebas.
Sistem nanopartikel yang sukses memiliki penjerapan obat yang tinggi sehingga dapat menurunkan jumlah komponen matriks saat pemberian (Mohanraj & Chen, 2006). Penjerapan dapat dikatakan tinggi jika efisiensinya mendekati 100%. Dari hasil pengujian, diketahui efisiensi penjerapan diltiazem hidroklorida pada formula 2 dan formula 3 masih rendah, di mana masing-masing hanya sebesar 64,13% dan 64,29%.
Gambar 4.6 Hubungan efisiensi penjerapan terhadap formula
Efisiensi penjerapan (%) yang rendah juga mungkin disebabkan oleh rendahnya konsentrasi obat. Semakin rendah konsentrasi obat, maka kemungkinan terjadinya interaksi obat dan polimer semakin kecil sehingga peristiwa penjerapan molekul obat dalam rantai polimer juga sedikit. Namun demikian, jumlah diltiazem hidroklorida yang ditambahkan harus setara dengan jumlah pektin. Jika diltiazem hidroklorida ditingkatkan maka jumlah pektin juga harus ditingkatkan. Sementara itu, untuk menjaga partikel yang dihasilkan masih dalam rentang ukuran nano, maka pektin harus dijaga pada konsentrasi 0,07% (Jonassen dkk., 2013).
Di samping itu, persen efisiensi penjerapan yang rendah pada penelitian ini diakibatkan karena tidak adanya pengaturan tingkat keasaman (pH) pada saat pembentukkan nanopartikel dilakukan, sehingga tingkat disosiasi antara molekul obat, polimer, dan bahan penyambung silang yang digunakan tidak diatur. Hal ini
UIN Syarif Hidayatullah Jakarta akan berdampak pada pembentukan gugus ionik antara obat, polimer, dan bahan penyambung silang yang memungkinkan terjadinya ikatan menjadi sedikit, sehingga efisiensi penjerapan menjadi rendah (Iswandana, Anwar & Jufri, 2013).
Efisiensi penjerapan (%) formula 2 dan 3 menghasilkan nilai yang hampir sama. Hasil yang setara ini menunjukkan bahwa tidak ada perbedaan pada jumlah obat yang terjerap dalam nanopartikel yang dipreparasi dalam medium NaCl 0,05 M maupun dalam akuades.
4.6 Spektrum Inframerah
Spektrum inframerah memberikan informasi mengenai kelompok gugus fungsi serta struktur dari nanopartikel yang dihasilkan. Analisis spektrum inframerah dilakukan terhadap serbuk nanopartikel zink pektinat dan pektin sebagai pembanding untuk mengetahui perubahan yang terjadi pada pektin sebelum dan sesudah dibuat nanopartikel. Serbuk nanopartikel dan pektin dianalisis pada bilangan gelombang 4000-400 cm-1.
Tabel 4.3 Daftar ikatan dan bilangan gelombang spektrum inframerah
No Ikatan Bilangan Gelombang (cm
-1)
1010,95 1017,50 1014,84 1018,10
3 C-O regang, dalam
ROR' 1149,91 1095,51 1147,41 1149,67
4 C-H tekuk 1424,58 1412,64 1416,65 1418,85 5 NH2 out of plane,
dalam RCONH2
1597,16 1617,59 1619,24 1624,95
6
C=O regang dalam RCO-OH atau RCOOR'
1727,40 1733,16 1740,78 1740,86
7 C-H regang 2935,66 2924,61 2937,80 2943,51
8 O-H 3412,54 3437,64 3408,74 3427,68