KADAR FENOLIK DAN AKTIVITAS ANTIOKSIDAN LIMA
AKSESI TANAMAN KUNYIT (
Curcuma domestica
) PADA
LOKASI BUDIDAYA KECAMATAN NAGRAK, SUKABUMI
JANUAR ANNISAS
DEPARTEMEN BIOKIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI SKRIPSI DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA
Dengan ini saya menyatakan bahwa skripsi berjudul Kadar fenolik dan aktivitas antioksidan lima aksesi tanaman kunyit (Curcuma domestica) pada lokasi budidaya kecamatan Nagrak, Sukabumi adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam daftar pustaka di bagian akhir disertasi ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, Juni 2013
Januar Annisas
iii
ABSTRAK
JANUAR ANNISAS. Kadar fenolik dan aktivitas antioksidan lima aksesi tanaman kunyit (Curcuma domestica) pada lokasi budidaya kabupaten Nagrak. Dibimbing oleh WARAS NURCHOLIS dan EDI DJAUHARI.
Kunyit telah diketahui memiliki kandungan fenolik yang berkhasiat sebagai antioksidan. Penelitian ini bertujuan menganalisis kandungan senyawa fenolik dan aktifitas antoksidan yang terkandung pada tanaman kunyit yang berasal dari lima aksesi dan dua varietas yang ditanam di lokasi pertanian Nagrak. Bioaktivitas antioksidan ditentukan dengan menggunakan metode DPPH (1,1-diphenyl-2-picryl-hydrazyl), sedangkan untuk total fenolik menggunakan metode metode FCA (Folin-Ciocalteau assay). Kunyit yang berasal dari varietas Nagrak memiliki kandungan fenolik dan aktifitas antioksidan tertinggi dibandingkan dengan sampel lainnya yaitu sebesar 479.20 mg/g dan 39.36 µg/mL. Selain itu kunyit varietas Nagrak merupakan kunyit terbaik dibandingkan dengan aksesi dari 6 lokasi lainnya. Berdasarkan parameter agrobiofisik kondisi lingkungan lokasi pertanian Nagrak tidak baik untuk budidaya kunyit dikarenakan suhunya hanya 18-26oC, curah hujan ± 231.98 mm tahun-1, dan tanahnya tidak berpasir.
Kata kunci : antioksidan, kunyit, senyawa fenolik.
ABSTRACT
JANUAR ANNISAS. The Fenolik’s level and the antioxidant’s activity of five promicing lines of turmeric (curcuma domestica) in cultivating location at Nagrak regency. Under direction WARAS NURCHOLIS and EDI DJAUHARI.
Turmeric is well known have the fenolik content that can be as antioxidant. The purpose of this research is for analyzing the fenolik’s compound and the antioxidant’s activity of turmeric that comes from five promicing lines and two varieties in Nagrak’s agricultural. The activity of antioxidant is depent on DPPH (1,1-diphenyl-2-picryl-hydrazyl)’s method. Wereas for the total of fenolik is used FCA (Folin-Ciocalteau assay)’s method. Nagrak’s promicing lines has the highest fenolik’s level and the activity antioxidant’s level of all it is 479.20 mg/g and 39.36 µg/mL. Turina’s 2 is a better tumeric than the other promicing lines from six location. Besides the agrobiofisik’s parameter, the environment of Nagrak is not good for the Tumeric because the temperature is only 18-26oC, the rainfall is ± 231.98 mm year1 and the land has no sand
KADAR FENOLIK DAN AKTIVITAS ANTIOKSIDAN LIMA
AKSESI TANAMAN KUNYIT (
Curcuma domestica
) PADA
LOKASI BUDIDAYA KECAMATAN NAGRAK, SUKABUMI
JANUAR ANNISAS
Skripsi
sebagai salah satu syarat memperoleh gelar Sarjana Sains pada
Departemen Biokimia
DEPARTEMEN BIOKIMIA
v
Disetujui oleh
Waras Nurcholis, S.Si., M.Si Ketua
Drs. Edi Djauhari P, M.Si Anggota
Diketahui oleh
Dr Ir I Made Artika. M.App.Sc Ketua Departemen
Tanggal Lulus :
Judul Skripsi : Kadar Fenolik dan Aktivitas Antioksidan Lima Aksesi Tanaman Kunyit (Curcuma domestica) pada Lokasi Budidaya Kecamatan Nagrak, Sukabumi.
Nama : Januar Annisas
vii
PRAKATA
Alhamdulillah, segala puji dan syukur penulis panjatkan kepada Allah SWT atas segala karunia-Nya. Shalawat dan salam semoga selalu tercurah kepada Nabi Muhammad SAW dan para pengikutnya sampai akhir zaman sehingga penulis dapat menyelesaikan penelitian ini. Penelitian ini berjudul “Kadar fenolik dan aktivitas antioksidan lima aksesi tanaman kunyit (Curcuma domestica) pada lokasi budidaya kecamatan Nagrak, Sukabumi”. Kegiatan penelitian ini dilakukan dari bulan November 2012 hingga Februari 2013, bertempat di Laboratorium Pusat Studi Biofarmaka (PSB), Taman Kencana, Bogor.
Terima kasih penulis ucapkan kepada semua pihak yang telah membantu dalam penyelesaian penelitian ini, terutama kepada Waras Nurcholis, S.Si., M.Si. selaku ketua pembimbing dan Edi Djauhari, S.Si., M.Si selaku anggota pembimbing yang telah memberikan saran, kritik, dan bimbingannya serta mempercayai saya dalam mengerjakan penelitian ini. Terima kasih kepada orang tua dan keluarga yang selalu memberikan doa, dukungan, motivasi, dan semangat bagi penulis untuk menyelesaikan penelitian ini. Terima kasih pula kepada Mbak ina, Ibu Nunuk, Antonio, Endi, Bapak taufik dan Bapak Zaim selaku peneliti di Laboratorium Pusat Studi Biofarmaka (PSB), serta rekan-rekan yang membantu selama penelitian ini yaitu Kartika, Febri, Syifa, Andin, Eko, Irma, teman teman rumah kopi dan biokimia 46 yang telah memberikan bantuan, kritik, dan saran bagi penulis. Semoga penelitian ini mampu memberikan informasi dan manfaat bagi yang memerlukan.
Bogor, Juni 2013
DAFTAR ISI
DAFTAR TABEL IX
DAFTAR GAMBAR IX
DAFTAR LAMPIRAN IX
PENDAHULUAN 1
METODE 2
BAHAN 2
ALAT 2
PROSEDUR 2
HASIL DAN PEMBAHASAN 4
HASIL 4
Ekstrak Rimpang Kunyit 4
Kadar Senyawa Fenolik Ekstrak Rimpang Kunyit 4
Aktivitas Antioksidan (IC50)Ekstrak Rimpang Kunyit 5
Hasil Analisis Agroklimat Lokasi Pertanian 5
PEMBAHASAN 6
Ekstrak Rimpang Kunyit 6
Korelasi Total Fenolik dan Aktifitas Antioksidan 7
Kondisi Agroklimat Lokasi Pertanian 9
SIMPULAN DAN SARAN 10
SIMPULAN 10
SARAN 10
DAFTAR PUSTAKA 11
LAMPIRAN 18
ix
DAFTAR TABEL
1. Karakteristik agroklimat lokasi pertanian 5
DAFTAR GAMBAR
1. Rendemen ekstrak rimpang kunyit 4
2. Senyawa Fenolik Ekstrak Rimpang Kunyit 4
3. Aktifitas antioksidan ekstrak rimpang kunyit 5
4. Perubahan warna DPPH dalam micro plate 8
5. Hasil uji antioksidan ekstrak kunyit 8
6. Grafik korelasi antara total fenolik dengan IC50 9
DAFTAR LAMPIRAN
1. Rendemen hasil ekstraksi 14
2. Absorban standar asam tanat pada panjang gelombang ( ) 725 nm 15 3. Total fenolik kunyit pada panjang gelombang ( ) 725 nm 16 4. Data absorban dan nilai IC50 kunyit dari tujuh asal yang berbeda 16
5. Grafik pengaruh sampel terhadap % inhibisi 18
6. Hasil uji IC50 sampel kunyit 22
PENDAHULUAN
Tanaman kunyit merupakan jenis Curcuma yang banyak dikonsumsi masyarakat. Kunyit (Curcuma domestica Val.) merupakan salah satu jenis tanaman obat dari famili Zingiberaceae yang potensial untuk dikembangkan dan merupakan salah satu dari sembilan jenis tanaman unggulan dari Ditjen POM yang memiliki banyak manfaat sebagai bahan obat (Hadipoentyanti & Syahid 2007). Rimpang Kunyit mempunyai berbagai komponen bioaktif seperti kurkuminoid, minyak atsiri, pati, protein, lemak, selulosa, mineral serta berbagai senyawa fenolik (Permadi 2008).
Rimpang kunyit mengandung senyawa bioaktif yang berkhasiat sebagai obat yakni, senyawa kurkuminoid yang terdiri atas tiga senyawa yaitu: kurkumin, demetoksikurkumin dan bisdemetoksikurkumin. Beberapa kandungan senyawa lainnya dari rimpang kunyit adalah resin, oleoresin, dan minyak atsiri yang terdiri atas senyawa monoterpen, dan sesquiterpen meliputi zingiberin, α-tumeron, β -tumeron, tumerol, α-atlanton, dan linalool. Menurut Rustam et al. (2007), kurkuminoid yang terkandung di dalam kunyit sebagai senyawa isolasi maupun kurkuminnya mempunyai aktivitas yang sangat luas, diantaranya sebagai antioksidan (Hudayani 2008).
Radikal bebas merupakan penyebab beberapa penyakit degeneratif contohnya kanker dan antioksidan senantiasa dibutuhkan untuk melawan keberadaan radikal bebas. Tumbuhan herbal seperti kunyit diketahui memiliki aktifitas antioksidan terhadap radikal bebas. Namun untuk mengetahui aktivitas komponen bioaktif kunyit dan kandungan antioksidan yang lebih baik, maka perlu dilakukan uji mengenai kandungan senyawa bioaktif yang terkandung dalam kunyit, dalam hal ini kurkuminoid yang berpotensi sebagai antioksidan (Narlawar 2008).
Pada penelitian bertujuan untuk mengukur kemampuan aktifitas antioksidan dan kandungan kadar fenolik yang terdapat pada tanaman kunyit. Penentuan total fenolik ditentukan dengan menggunakan metode folin-ciocalteau
assay (FCA), sedangkan penentuan aktifitas antioksidan menggunakan metode 1,1 difenil-2-pikrihidrazil (DPPH). Penelitian ini bermanfaat sebagai sumber informasi mengenai keanekaragaman kunyit dan senyawa bioaktifnya, manakah dari ketujuh sampel yang memiliki data yang terbaik.
Hipotesis pada penelitian ini, umumnya kunyit memiliki aktivitas antioksidan. Aktifitas antioksidan pada tanaman kunyit disebabkan oleh senyawa kurkumioid yang terdapat di kunyit. Kurkuminoid termasuk kedalam golongan senyawa fenolik. Semakin banyak kadar fenolik yang dimiliki maka akan semakin tinggi pula aktivitas antioksidan yang dimiliki.
2
METODE
Bahan
Bahan yang digunakan adalah sampel rimpang tanaman kunyit (5 aksesi dan 2 varietas (turina 1 dan turina 2) sebagai varietas pembanding), 96 well plate, aqua tridestillata, DMSO (E. Merck), etanol absolut (E. Merck), alumunium foil, metanol, reagen Folin-Ciocalteau 10%, Na2CO3 7.5%, asam tanat dan DPPH (2,2 difenil-1-pikril hidrazil).
Alat
Alat yang digunakan dalam penilitian diantaranya microplate reader (Lab
System Multiscan Ascent), mikro pipet (Socorex), neraca digital, shaker (Labnet Orbit 1000), vortex, dan mikro plate, vial, labu takar, gelas ukur, tabung reaksi, spatula, neraca digital, vorteks, oven, penggiling 100 mash, pipet tetes, pipet volumetrik, pipet mikro, tip, pisau.
Prosedur Persiapan Sampel
Kunyit diambil dari lokasi pertanian Nagrak, Sukabumi. Kunyit berasal dari 5 aksesi (Nagrak, Ngawi, BPTO, Ciemas, Wonogiri) dan 2 varietas asal Balitro (Turina 1 dan 2) yang digunakan sebagai kontrol positif pada penelitian ini. Masing-masing kunyit dibersihkan dan dicuci menggunakan air mengalir sampai semua tanah dan kotoran yang menempel pada kunyit hilang. Semua kunyit yang telah bersih dipotong, selanjutnya dikeringkan di bawah sinar matahari selama 5 hari. Setelah kunyit menjadi simplisia, masing-masing kunyit digiling dengan ukuran 100 mesh. Selanjutnya dipilih simplisia yang kadar airnya ≤ 10 %.
Ekstraksi Rimpang Kunyit.
Simplisia dengan kadar air ≤ 10 % yang telah didapat diekstraksi menggunakan metode maserasi. Proses ekstraksi menggunakan pelarut etanol 70% dengan perbandingan simplisia dengan pelarut adalah 1: 10 yang dimasukkan ke dalam maserator dan direndam selama 6 jam sambil sekali-kali diaduk, kemudian didiamkan sampai 24 jam. Maserat dipisahkan, dan proses diulang 2 kali dengan jenis dan jumlah pelarut yang sama. Semua maserat dikumpulkan dan diuapkan dengan penguap vakum hingga diperoleh ekstrak kental. Proses ekstraksi dilakukan dengan ulangan sebanyak 5 kali.
Penentuan Bilangan Total Fenolik
Analisis Aktivitas Antioksidan dengan Metode DPPH
Berdasarkan penelitian Udenigwe et al. (2009), estrak kental sampel kunyit yang berasal dari lima aksesi dan dua varietas hasil maserasi dilarutkan dengan 3ethanol dan dimasukkan ke dalam tabung reaksi. Modifikasi metode dilakukan dengan mengubah konsentrasi ekstrak yang digunakan untuk analisis yaitu 12,5, 25, 50, 100, 200 ppm. Larutan induk untuk masing-masing sampel kunyit Sukabumi yaitu 200 ppm dibuat dengan menimbang 1 mg sampel dan ditambahkan dengan 5 ml 3ethanol. Pembuatan larutan DPPH dilakukan dengan menimbang 1,23 mg DPPH kemudian diencerkan dengan 3ethanol hingga 25 ml menggunakan labu takar. Larutan sampel dengan konsentrasi 12,5 ppm, 25 ppm, 50 ppm, 100 ppm dan 200 ppm dimasukkan ke dalam masing-masing sumur (well plate) dan dilakukan masing-masing tiga kali ulangan sebanyak 100 L setiap sampel dengan masing-masing konsentrasi tersebut.
Pada masing-masing sumur ditambahkan 100 L larutan DPPH 0,1 M hingga volume akhir yang terdapat pada sumur yaitu 200 L. Selanjutnya, diinkubasi pada suhu 370C selama 30 menit dan diukur serapannya menggunakan
Micro plate reader dengan panjang gelombang 517 nm. Nilai absorbansi yang diperoleh selanjutnya digunakan untuk mendapatkan persen penangkapan radikal bebas dan digunakan untuk mendapatkan persamaan regresi linier dengan rumus yaitu y = a + b ln x. Nilai IC50 dihitung dengan menggunakan rumus persamaan regresi tersebut (Lampiran 11). Nilai IC50 yang paling rendah menunjukkan aktivitas antioksidan yang paling tinggi.
Penentuan IC50
Inhibition concentration 50 atau IC50 merupakan nilai konsentrasi minimal ekstrak yang dapat menginhibisi enzim sampai 50%. Nilai IC50 diperoleh dari masing-masing kurva ekstrak sampel dengan memasukkan nilai Y=50.
Y = a + bx (fungsi linier)
Langkah selanjutnya yaitu dipilih satu persamaan yang paling sesuai untuk masing-masing sampel dengan melihat nilai r2 tertinggi yang diperoleh.
Analisis Kadar Tanah
Penentuan anlisis kadar tanah dilakukan di laboratorium ilmu tanah IPB, menggunakan jasa analis untuk penentuan kadar tanah yang terdapat di lokasi pertanian
Analisis Statitik
Data dianalisis menggunakan Statistical Package Social Science (SPSS)
4
HASIL DAN PEMBAHASAN
Hasil
Ekstrak Rimpang Kunyit
Hasil ekstraksi rimpang kunyit yang berasal dari tujuh sampel menghasilkan data rendemen yang terkandung berkisar antara 16.97-21.37% (Gambar 1). Kunyit yang berasal dari daerah Ngawi memiliki rendemen yang lebih tinggi dibandingkan kunyit yang lain dengan nilai rendemen sebesar 21.37% dan kunyit yang berasal dari wonogiri memiliki rendemen terkecil dengan nilai rendemen sebesar 16.97%.
Gambar 1 Rendemen ekstrak rimpang kunyit
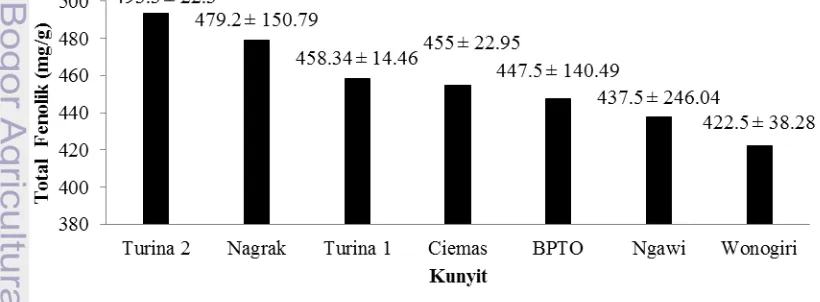
Kadar Senyawa Fenolik Ekstrak Rimpang Kunyit
Gambar 2 Senyawa Fenolik Ekstrak Rimpang Kunyit
Aktivitas Antioksidan (IC50)Ekstrak Rimpang Kunyit
Hasil pengukuran senyawa antioksidan yang terdapat pada ekstrak rimpang kunyit diperoleh hasil kadar IC50 berkisar antara 39.36-73.47 µg/mL (Gambar 3). Kunyit yang berasal dari daerah Nagrak memiliki kadar IC50 yang paling baik yaitu sebesar 44.09 µg/mL, sedangkan kunyit yang berasal dari daerah Wonogiri memiliki kadar IC50 paling rendah yaitu sebesar 73.47 µg/mL. Varietas turina 1 dan turina 2 merupakan varietas pembanding pada penelitian ini.
Gambar 3 Aktifitas antioksidan ekstrak rimpang kunyit
Hasil Analisis Agroklimat Lokasi Pertanian
Keadaan agroklimat lokasi pertanian Nagrak, Sukabumi memiliki suhu 18-26, ketinggian 550-750 dpl, curah hujan 231,98 mm (tahun-1), sedangkan kandungan senyawa kimia seperti C organik dan N bernilai 1.67 dan 0.17. Analisis kadar tanah dilakukan di laboratorium departemen ilmu tanah, fakultas pertanian IPB dengan menggunakan jasa analis.
Tabel 1. Karakteristik agroklimat lokasi pertanian
Agroklimat Lokasi Budidaya Nagrak (Sukabumi)
Kondisi iklim
Suhu (oC) 18-26
Ketinggian tempat (m dpl) 550-750
Curah Hujan (mm tahun-1) 231.98
Sifat fisik atau kimia tanah : Kandungan komponen (%) :
Basa yang dapat dipertukarkan (me 100 g-1)
6 (Nagrak, Ngawi, Tawamangu, Wonogiri, dan Ciemas) dan 2 varietas yang berasal dari Bogor (Turina 1 & 2 )yang bertindak sebagai varietas pembanding. Penanaman sampel dilakukan di tempat yang sama yaitu di Kabupaten Nagrak, Sukabumi. Ekstraksi dilakukan menggunakan pelarut etanol 70 % dengan metode maserasi. Penggunaan etanol sebagai pelarut disebabkan beberapa hal di antaranya, kepolaran, toksisitas, dan mudah diperoleh. Sifat dari pelarut etanol yang tidak beracun menyebabkan etanol ditetapkan standar sebagai pelarut yang aman oleh Badan Pengawas Obat dan Makanan (BPOM).
Etanol 70% digunakan karena memiliki dua gugus fungsi yang berbeda tingkat kepolarannya, yaitu gugus hidroksil (OH) yang bersifat polar dan gugus alkil (-R) yang bersifat non polar. Adanya kedua gugus tersebut diharapkan agar senyawa-senyawa kimia dengan tingkat kepolaran yang berbeda dalam simplisia sampel akan terekstrak ke dalam etanol (Khopkar 2003). Seperti halnya, kurkuminoid merupakan senyawa yang bersifat polar, kepolarannya disebabkan oleh gugus –OH yang terdapat pada struktur senyawa kurkuminoid. Kurkuminoid larut dalam pelarut yang mempunyai kepolaran hampir sama. Etanol memiliki kepolaran yang mirip dengan kurkuminoid sehingga cocok digunakan sebagai pelarut dalam proses ekstraksi rimpang \ kunyit.
Metode maserasi dilakukan selama 3 x 24 jam. Menurut hasil penelitian yang dilakukan Suwiah (1991) rendemen yang dihasilkan dari suatu proses ekstraksi akan meningkat seiring dengan peningkatan waktu ektraksi. Hal ini disebabkan semakin lama waktu ekstraksi, semakin lama waktu kontak antara pelarut dan bahan baku sehingga proses penetrasi pelarut ke dalam sel bahan (sampel) akan semakin baik yang menyebabkan semakin banyaknya senyawa yang berdifusi keluar sel. Perbedaan jumlah rendemen pada ekstrak kunyit dikarenakan pada ekstrak dengan rendemen tertinggi mengandung lebih banyak senyawa yang mudah larut dalam pelarut etanol 70%, sedangkan ekstrak dengan rendemen yang lebih rendah mengandung sejumlah senyawa yang kurang larut dalam pelarut etanol 70%.
yang digunakan. Hal inilah yang menentukan besar kecilnya rendemen yang dihasilkan dalam suatu proses ekstraksi secara maserasi. Ketebalan dinding sel sangat dipengaruhi faktor genetik dari ketujuh sampel tersebut.
Korelasi Total Fenolik dan Aktifitas Antioksidan
Senyawa kurkuminoid merupakan senyawa hasil dari metabolit sekunder yang termasuk kedalam golongan senyawa fenolik umumnya terdapat pada tanaman jenis Curcuma dan telah dilaporkan memiliki aktivitas biologis seperti antioksidan dan antiinflamasi (Itokawa et al. 2008). Senyawa fenolik yang terdapat pada kunyit diantaranya adalah kurkuminoid, kurkuminoid merupakan senyawa hasil metabolit sekunder yang mempunyai fungsi sebagai antioksidan dan antiinflamasi.
Penentuan total fenolik didasarkan pada prinsip kolorimetri menggunakan metode Folin-Ciocalteau assay (FCA). Metode FCA yang digunakan untuk menentukan jumlah total fenolik dinilai lebih baik dibandingkan beberapa metode penentuan total fenolik lainnya seperti Folin-Denis assay (FDA). Prinsip penentuan total fenolik menggunakan metode Folin-Ciocalteau assay yaitu adanya transfer elektron dalam kondisi medium basa dari senyawa fenolik ke asam fosfomolibdat (H3PMo12O40) atau fosfotungstat (H3PW12O40) yang terdapat di dalam reagen Folin-Ciocalteau membentuk kompleks warna biru yang diukur nilai absorbannya. Pembentukan kompleks warna biru ini sebanding dengan jumlah senyawa fenolik yang terkandung dalam suatu sampel (Dai & Mumper 2010). Kadar senyawa fenolik dari varietas Nagrak adalah 479.20 mg/g paling besar dibandingkan dengan kadar senyawa fenolik dari sampel lainnya.
Pemilihan pelarut juga sangat mempengaruhi terhadap jumlah senyawa fenolik yang terekstrak. Pelarut polar seperti air dan etanol sangat efektif untuk mengekstraksi senyawa fenolik. Hal inilah yang menyebabkan total fenolik terbesar ekstrak rimpang kunyit terdapat pada ekstrak dengan pelarut polar (air dan etanol). Ekstraksi senyawa fenolik dengan pelarut etanol akan lebih efektif karena tingkat kepolaran etanol lebih rendah dibandingkan air. Hal ini akan mengakibatkan dinding sel tumbuhan yang bersifat kurang polar lebih mudah didegradasi dan senyawa fenolik akan lebih mudah keluar dari sel tanaman (Tiwari et al. 2011). Pelarut lainnya yang sering digunakan untuk mengekstraksi senyawa fenolik diantaranya adalah metanol yang cocok digunakan untuk mengekstraksi polifenol dengan berat molekul rendah dan aseton yang cocok digunakan untuk mengekstraksi senyawa fenolik dengan berat molekul yang lebih besar seperti flavanol (Dai & Mumper 2010)
8
Berdasarkan data yang diperoleh yakni kunyit asal Nagrak memiliki aktifitas antioksidan tertinggi sebesar 44.09 µg/mL. Sesuai dengan hipotesis awal yang menyatakan bahwa semakin tinggi kadar senyawa fenolik yang terkandung maka semakin tinggi pula aktifitas antioksidannya (Nurcholis 2008). Cara menentukan aktifitas antioksidan yang terbaik dilihat dari nilai IC50 yang semakin kecil, sesuai dengan kunyit asal Turina 2 yang mempunyai nilai IC50 yang kecil. Sampel dapat dikatakan memiliki aktifitas antioksidan yang baik karena nilai IC50 yang didapat kurang dari 200 µg/mL (Blois 1985).
Pada pengujian aktivitas antioksidan terjadi perubahan warna pada larutan DPPH yang awalnya berwarna ungu menjadi berubah kekuningan setelah penambahan ekstrak kunyit (Gambar 5). Berdasarkan hasil pengukuran serapan dengan micro plate reader diperoleh data absorban, semakin tinggi konsentrasi sampel yaitu dimulai dari 12.5 ppm, 25 ppm, 50 ppm, 100 ppm, 200 ppm akan menghasilkan nilai absorban yang semakin rendah (Gambar 5).
Gambar 4 Perubahan warna DPPH dalam micro plate
Gambar 5 Hasil uji antioksidan ekstrak kunyit
menghambat radikal bebas lebih banyak. Penghambatan radikal bebas ini ditandai dengan peluruhan warna ungu. Penurunan nilai absorban karena yang diukur oleh
micro plate reader adalah warna ungu DPPH yang semakin pudar seiring dengan meningkatnya konsentrasi sampel.
Hal ini disebabkan satu molekul dari senyawa antioksidan disumbangkan kepada senyawa DPPH dan mekanisme ini dibuktikan dengan perubahan warna DPPH (Naik et al. 2003). Perubahan warna DPPH diukur pada panjang gelombang 517 nm dengan menggunakan micro plate reader. Pemilihan panjang gelombang 517 nm disebabkan warna ungu larutan DPPH memiliki serapan yang kuat pada panjang gelombang 517 nm dalam bentuk teroksidasi (Masuda et al.
1999).
Gambar 6 Grafik korelasi antara total fenolik dengan IC50
Hasil uji menunjukan bahwa senyawa fenolik yang dihasilkan berbanding lurus dengan nilai IC50 yang didapat, yakni semakin tinggi kadar fenolik yang didapat maka nilai IC50 akan semakin kecil, dengan kata lain aktifitas antioksidan akan semakin tinggi dengan kadar fenolik yang semakin tinggi pula. Hal ini sesuai dengan korelasi positif yang didapatkan berdasarkan analisis statistik menggunakan perangkat komputer SPSS dengan metode one way ANOVA. Nilai r2 yang didapat sebesar 0.962. Kunyit yang berasal dari Nagrak memiliki kadar fenolik dan aktifitas anioksidan yang terbaik dibandingkan dengan kunyit lainnya. Kondisi Agroklimat Lokasi Pertanian
Data agroklimat tiga lokasi penelitian dari kondisi iklim, sifat fisik dan kimia tanah tersaji pada Tabel 1. Kondisi tanah pada lokasi penelitian akan mempengaruhi produksi rimpang dan banyaknya jumlah rimpang. Kondisi tanah kabupaten Nagrak Sukabumi memiliki kadar pasir yang tidak terlalu besar yaitu 7.98%, sehingga pertumbuhan kunyit kurang optimal. Kondisi yang berpasir merupakan kondisi optimal untuk pertumbuhan kunyit dibandingkan dengan kondisi tanah yang liat yang menyebabkan pertumbuhan tidak maksimal dan lebih memperbanyak jumlah percabangan dibandingkan dengan besarnya rimpang (Nurcholis 2008).
10
matahari, suhu udara, lingkungan atmosfer (CO2, O2 dan kelembaban) dan lingkungan perakaran (sifat kimia dan fisika tanah) serta ketersediaan air di dalam tanah (Nitisapto dan Siradz, 2005)
Selain itu faktor penentu pembentukan senyawa metabolit sekunder lainnya yaitu stimulasi faktor lingkungan biotik maupun abiotik, keseimbangan nutrisi karbon, genotipe, dan ontogenesis (Kliebenstein 2004; Laitinen et al 2005; Lerdau 2002; Lila 2006). Masing masing faktor memiliki suatu mekanisme biokimiawi kompleks tertentu yang menyebabkan kunyit dari setiap daerah memproduksi kurkuminoid yang berbeda-beda. Kondisi lingkungan yang ekstrim dapat meningkatkan kandungan metabolit sekunder tanaman (Kirakosyan et al.,
2004; Zobayed et al., 2005; zobayed et al., 2007). Kondisi curah hujan (mm tahun-1) di lokasi pertanian 231.98. Hal ini pula yang menyebabkan produksi metabolit sekunder berbeda, cekaman kekeringan menyebabkan meningkatnya kandungan metabolit sekunder jenis atsiri dalam kunyit. Unsur hara juga dimungkinkan dapat meningkatkan cekaman lingkungan terutama unsur hara N. Ketersediaan N yang rendah merupakan induksi transkripsi gen-gen yang berkaitan dengan metabolisme fenolik (Peneulas dan Estiarte 1998).
Produksi suatu senyawa bioaktif dalam tanaman dipengaruhi oleh adanya prekursor yang diperoleh dari hasil metabolisme primer (Tumova et al., 2006). Metabolit primer akan tinggi jika terdapat CO2 sebagai sumber karbon untuk fotosintesis yang melimpah dalam sesuatu lingkungan di tempat tanaman itu tumbuh. Molekul CO2 merupakan molekul yang dapat meningkatkan suhu udara (Soon et al., 1999). Suhu udara di lokasi pertanian Nagrak berkisar antara 18-26oC berbeda dengan suhu yang terdapat pada daerah aksesi seperti di Wonogiri 24-320C, Tawamangu 22-250C, Ngawi 26-380C, dan Ciemas 23-320C.
SIMPULAN DAN SARAN
Simpulan
Kunyit varietas Nagrak memiliki kadar total fenolik dan aktifitas antioksidan paling tinggi dibandingkan dengan rimpang kunyit lainnya yaitu sebesar 493.3 mg/g dan 39.36 µg/mL. Hal ini membuktikan bahwa semakin tinggi kadar fenolik yang didapat maka kadar aktifitas antioksidannya juga semakin tinggi, sehingga penentuan senyawa fenolik sudah dapat dijadikan senyawa penciri dalam penentuan aktifitas antioksidan.
Saran
DAFTAR PUSTAKA
Apak R. et al. 2007. Comparative Evaluation of Various Total Antioxidant Capacity Assay Applied to Phenolic Compounds with the CUPRAC Assay.
Molecules 12: 1496-1547.
[BPOM] Badan Pengawas Obat dan Makanan. 2005. Peraturan Kepala Badan Pengawas Obat dan Makanan Nomor HK.00.05.41.1384 Tahun 2005 tentang Kriteria dan Tata Laksana Pendaftaran Obat Tradisional, Obat Herbal Terstandar, dan Fitofarmaka. BPOM, Jakarta.
Blois MS. 1958. Antioxidant determination by the use of stable free radical.
Nature 181: 1191-1200.
Dai J, Mumper RJ. 2010. Plant phenolic: extraction, analysis and their antioxidant and anticancer properties. Molecules 15 : 7313-7352.
Hadipoentyanti E, Syahid SF. 2007. Respon Temulawak (Curcuma xanthorriza Roxb.) Hasil Rimpang Kultur Jaringan Generasi Kedua Terhadap Pemupukan. Jurnal Littri 13: 106-110
Itokawa H, Shi Q, Akiyama T, Morris-Natschke SL, Lee KH. 2008. Recent advances in the investigation of curcuminoids. Chinese Medicine 3 (11): 13. Javanmardi J, Stushnoff C, Locke E, Vivanco JM. 2003. Antioxidant activity and
total phenolic content of Iranian Ocimum accessions. J Food Chem 83: 547-550.
Jayaprakasha GK. Rao LJM. Sakariah KK 2006. Antioxidant activities of curcumin, demethoxycurcumin and bisdemethoxycurcumin. Food Chemistry. 98:720-724
Kirakosyan, A.P., Kaufman, S. Warber, S. Zick, K. Aaronson, S. Bolling, S.C. Chang. 2004. Applied environmental stresses to enhance the levels of polyphenolics in leaves of hawthorn plants. Physiol. Plant. 121:182-186. Khaerana, M., Ghulamahdi, E.D., Purwakusumah. 2008. Pengaruh cekaman
kekeringan dan umur panen yang berbeda terhadap kandungan xanthorrhizol tanaman temulawak (Curcuma xanthorrhiza Roxb.). Bul. Agron. 36:241-247. Khopkar M. 2003. Konsep Dasar Kimia Analitik. Penerjemah: Saptorahardjo A.
Jakarta: Universitas Indonesia Press. Terjemahan dari: Analytical Chemistry Basic Concept.
Kliebenstein, D.J. 2004. Secondary metabolites and plant environment interactions: a view through Arabidopsis thaliana tinged glasses. Plant Cell. Environ. 27: 675-684.
Kristina, N., N., R., Noveriza, S., F., Syahid dan M., Rizal. 2007. Peluang peningkatan kadar kurkumin pada tanaman kunyit dan temulawak. Buletin Perkembangan Teknologi Tanaman Rempah dan Obat. 18 (1) :1-12
12
Lerdau, M. 2002. Benefits of the carbon-nutrient balance hypothesis. OIKOS 98:534-536.
Lila, M.A. 2006. The nature-versus-nurture debate on bioactive phytochemicals: the genome versus terroir. J. Sci. Food Agric. 86:2510-2515.
Masuda T, Isoke J, Jitoe A, Nakatani N. 1992. Antioxidative curcuminoids from rhizomes of Curcuma xanthorrhiza. Phytochemistry 31 (10): 3645-3647. Naik GH, Priyadarsini K I, Satav JG, Banavalikar M M, Sohoni D P, Biyani, M
K, Mohan H. 2003. Comparative antioxidant activity of individual herbal components used in ayurvedic medicine. Phytochemistry 63 (1): 97-104 Narlawar, J., et al. 2008. “Curcumin-derived Pyrazoles and Isoxazoles : Swiss
Army Knives or Blunt Tools for Alzheimer’s Disease”, Bioorganic & Medicinal chemistry Letters Vol 3:165-172.
Nitisapto, M., dan S., A., Siradz. 2005. Evaluasi kesesuaian lahan untuk pengembangan jahe pada beberapa daerah di Jawa Tengah dan Jawa Timur.
Jurnal Ilmu Tanah dan Lingkungan. 5 (2) : 15-19
Nurcholis W. 2008. Profil Senyawa Penciri Bioaktifitas Tanaman Kunyit pada Agrobiofisik Berbeda [tesis]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Pahaditya D. 2012. Analisis Keragaman Genetika Tanaman Kunyit Dan Temulawak Secara Random Amplified Polymorphic Dna-Polymerase Chain Reaction (Rapd-Pcr) Menggunakan Primer Opa-Opd 6-10 [Skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor. Permadi A. 2008. Membuat Kebun Tanaman Obat. Jakarta: Pustaka Bunda. Penuelas, J., M. Estiarte. 1998. Can elevated CO2 affect secondary metabolism
and ecosystem function?. Tree 13:20-23.
Rahmat R. 1995. Temulawak : Tanaman Rempah dan Obat. Yogyakarta: Kanisius Rustam E., Atmasari I., Yanwirasti. 2007. Efek Antiinflamasi Ekstrak Etanol Kunyit (Curcuma domestica Val.) Pada Tikus putih Jantan Galur Wistar. Jurnal sains dan Teknologi farmasi, Vol 12, No 2: 112-115.
Soon, W., S.L. Baliunas, A.B. Robinson, Z.W. Robinson. 1999. Environmental effects of increased atmospheric carbon dioxide. Climate Res. 13:149-164. Suwiah A. 1991. Pengaruh perlakuan bahan dan jenis pelarut yang digunakan
pada pembuatan temulawak instant terhadap rendemen dan mutunya [skripsi]. Bogor: Fakultas Teknologi Pertanian, Institut Pertanian Bogor.
Tiwari P, Kumar B, Kaur G, Kaur H, Kaur M. 2011. Phytochemical screening and extraction : A review. J Int Pharm Sci 1 : 98-106.
Tumova, L., J. Rimakova, J. Tuma, J. Dusck. 2006. Silybum marianum in vitro-flavolignan production. Plant Cell Environ. 52:454-458.
Wadiyati, et al. 2012. Koleksi dan identifikasi temulawak (curcuma xanthorrhiza,
roxb. ) dan kunyit (curcuma domestica) di jawa dan madura : 1. pengaruh lingkungan terhadap bobot rimpang dan kadar kurkumin. Universitas Brawijaya. Malang.
Zobayed, S.M.A., F. Afreen, T. Kozai. 2005. Temperature stress can alter the photosynthetic efficiency and secondary metabolite concentrations in St. John’s wort. Plant Physiol. Biochem. 43:977-984.
Zobayed, S.M.A., F. Afreen, T. Kozai. 2007. Phytochemical and physiological changes in the leaves of St. John’s wort plants under a water stress condition.
LAMPIRAN
Lampiran 1 Rendemen hasil ekstraksi
Tanaman Varietas Varietas
ulangan
Rendemen rata-rata kunyit (%) = =
Lampiran 2 Absorban standar asam tanat pada panjang gelombang ( ) 725 nm
Konsentrasi Tanat (mg/L) Absorban
10 0.258
30 0.676
50 1.043
70 1.665
100 2.437
Lampiran 3 Total fenol kunyit pada panjang gelombang ( ) 725 nm
Ulangan Absorban Kunyit
Ciemas Ngawi BPTO Wonogiri Turina 2 Nagrak Turina 1
1 0.497 0.281 0.493 0.426 0.746 0.442 0.478
2 0.517 0.493 0.495 0.481 0.414 0.275 0.549
3 0.464 0.641 0.464 0.456 0.529 0.849 0.463
Rata-Rata 0.493 0.472 0.484 0.454 0.539 0.522 0.497 Bobot
Ekstrak(mg) 0.01 0.01 0.01 0.01 0.01 0.01 0.01
Total Fenol
(mg/L) 22.750 21.875 22.375 21.125 24.667 23.958 22.917 Total Fenolik
TAE (mg/g) 455 437.5 447.5 422.5 493.3 479.2 458.34
Contoh Perhitungan :
Persamaan garis kurva standar asam galat: Y = 0.024x-0.053
A rata-rata = = = 0.493
Y (Absorban) = 0.024 x (Total Fenol)-0.053 0.493 = 0.024(x)-0.053
0.024 (x) = 0.546 x = 22.75
Total Fenolik TAE (C)= c. (V/m)
C = konsentrasi total fenolik dari kurva standar, V = volume ekstrak
M = berat ekstrak
Lampiran 4 Data absorban dan nilai IC50 kunyit dari tujuh asal yang berbeda Sampel Ulangan Konsentrasi
Lampiran 5 Grafik pengaruh sampel terhadap % inhibisi Kunyit asal Nagrak
Kunyit asal Wonogiri
Konsentrasi (ppm)
Konsentrasi (ppm) Konsentrasi (ppm)
% Inhibisi % Inhibisi % Inhibisi
Ulangan 1 Ulangan 2 Ulangan 3
% Inhibisi
Ulangan 1
Konsentrasi (ppm)
% Inhibisi
Konsentrasi (ppm)
Ulangan 2 Ulangan 3
Konsentrasi (ppm) % Inhibisi
Kunyit asal Ciemas
Kunyit asal Ngawi
Konsentrasi (ppm) % Inhibisi
Ulangan 1 Ulangan 2
% Inhibisi
Konsentrasi (ppm)
% Inhibisi
Konsentrasi (ppm) Ulangan 3
Konsentrasi (ppm) Ulangan 1
% Inhibisi % Inhibisi
Konsentrasi (ppm) Ulangan 2
% Inhibisi
Kunyit asal Bogor (Turina 1)
Kunyit asal Bogor (Turina 2)
Konsentrasi (ppm) Konsentrasi (ppm) Konsentrasi (ppm)
% Inhibisi % Inhibisi
% Inhibisi
Ulangan 1 Ulangan 2 Ulangan 3
Konsentrasi (ppm) Konsentrasi (ppm) Konsentrasi (ppm)
% Inhibisi % Inhibisi % Inhibisi
Ulangan 1 Ulangan 2 Ulangan 3
Kunyit asal Tawamangu (BPTO)
Konsentrasi (ppm) Konsentrasi (ppm) Konsentrasi (ppm)
% Inhibisi
% Inhibisi % Inhibisi
Ulangan 1 Ulangan 2
Lampiran 6 Hasil uji IC50 sampel kunyit
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta, pada tanggal 14 Januari 1992 dari ayah Abdur Rachman dan ibu Nina Rukuhati. Penulis merupakan anak kedua dari tiga bersaudara dengan kakak perempuan bernama Lia Agturani Tudaryati dan adik laki-laki bernama Maha fadillah Rachman. Pendidikan penulis dimulai dari SDN CIBULUH I Kota Bogor, melanjutkan pendidikan ke SMPN 5 Kota Bogor dan melanjutkan pendidikan ke SMAN 6 Kota Bogor. Penulis lulus tahun 2009 dari SMAN 6 Bogor dan pada tahun yang sama lulus seleksi masuk IPB melalui jalur Seleksi Nasional Masuk Perguruan Tinggi Negeri Undangan atau dahulu yang lebih dikenal dengan nama PMDK. Penulis memilih mayor Departemen Biokimia, Fakultas Matematika dan Ilmu Pengetahuan Alam.
Selama mengikuti perkuliahan, penulis pernah menjadi asisten responsi Sosiologi Umum selama dua tahun (2011-2013). Penulis pernah melakukan Praktik Lapangan (PL) di Balai Pusat Studi Biofarmaka, Taman Kencana, Bogor selama periode Juli 2012 hingga Agustus 2012 dengan judul “Analisis Tanaman Kunyit Asal Ngawi, Nagrak dan Tawamangu”.
Beberapa organisasi yang diikuti penulis selama perkuliahan yakni Himpunan Profesi Mahasiswa Biokimia (CREBs) tahun 2010-2011 sebagai anggota dan Badan Pengawas CREBs tahun 2011-2012 sebagai ketua. Penulis juga pernah mengikuti berbagai kepanitiaan seperti Seminar Kesehatan dan Keselamatan Kerja tahun 2010, Lomba Karya Ilmiah Populer tahun 2010, Masa Pengenalan Departemen tahun 2011, Masa Pengenalan Fakultas 2011, SPIRIT 2011, Gebyar Nusantara 2011, Biokimia Expo tahun 2010-2011, Seminar Kesehatan Biokimia tahun 2011, Biochemistry Champions League tahun 2011 dll.
Penulis dalam bidang karya ilmiah pernah mendapat hibah dana bersaing dari Direktorat Jenderal Pendidikan Tinggi (DIKTI) dalam Program Kreativitas Mahasiswa (PKM) untuk kategori Bidang Penelitian pada tahun 2011 untuk dua buah proposal dengan judul “Identifikasi Bakteri Resisten Merkuri Pada Paerah Penambangan Emas dan Biofiltrasi Dari Kulit Pisang Sebagai Solusi Penciptaan Air Sehat dan Bersih ”. Penulis juga pernah mengikuti pelatihan Good Laboratory Practices (GLP) di departemen Ilmu dan Teknologi Pangan pada tahun 2010, Pelatihan Keamanan dan Keselamatan Kerja (K3) yang diselenggarakan oleh