ISOLASI SENYAWA TERPENOIDA DARI EKSTRAK
METANOL BIJI BUAH DUKU
(Lansium domesticum L.)
SKRIPSI
BELDINA E NABABAN
050802024
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
ISOLASI SENYAWA TERPENOIDA DARI EKSTRAK
METANOL BIJI BUAH DUKU
(Lansium domesticum L.)
SKRIPSI
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar Sarjana sains
BELDINA E NABABAN
050802024
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
PERSETUJUAN
Judul : ISOLASI SENYAWA TERPENOIDA DARI EKSTRAK METANOL BIJI BUAH DUKU
(Lansium domesticum L.)
Kategori : SKRIPSI
Nama : BELDINA E NABABAN
Nomor Induk Mahasiswa : 050802024
Program Studi : SARJANA (S1) KIMIA
Departemen : KIMIA
Fakultas : MATEMATIKA DAN ILMU PENGETAHUAN
ALAM (FMIPA) UNIVERSITAS SUMATERA UTARA
Disetujui di
Medan, Januari 2010
Komisi Pembimbing :
Pembimbing 2 Pembimbing 1
Lamek Marpaung, M.Phil, Ph.D. Drs. Phillipus H. Siregar,M.Si
NIP. 131 126 697 NIP. 130 517 489
Diketahui/Disetujui oleh
Departemen Kimia FMIPA USU
Ketua,
Dr. Rumondang Bulan Nst., MS
PERNYATAAN
ISOLASI SENYAWA TERPENOIDA DARI EKSTRAK METANOL BIJI BUAH DUKU
( Lansium domesticum L. )
SKRIPSI
Saya mengakui bahwa skripsi ini adalah hasil karya saya sendiri, kecuali beberapa kutipan dan ringkasan yang masing – masing disebutkan sumbernya.
Medan, Januari 2010
PENGHARGAAN
Segala puji dan syukur penulis panjatkan kepada Tuhan Yang Maha Kuasa, yang sudah memberikan kasih dan karunia-Nya bagi penulis sehingga dapat menyelesaikan penelitian dan penyusunan skripsi ini guna melengkapi syarat dalam memperoleh gelar sarjana kimia di FMIPA USU Medan.
Keberhasilan dalam menyelesaikan penelitian dan penyusunan skripsi ini juga tidak luput dari perhatian dan bantuan dari berbagai pihak. Dalam kesempatan ini, penulis dengan segala kerendahan hati mengucapkan terima kasih yang sebesar – besarnya kepada :
1. Bapak Drs. Phillipus H. Siregar, MSi selaku Dosen Pembimbing Pertama dan Bapak Lamek Marpaung,M.Phil,Ph.D. selaku Dosen Pembimbing Kedua yang telah meluangkan waktu dalam memberikan pemikiran, pengarahan, petunjuk, serta saran kepada penulis dari awal hingga akhir penelitian dan penyusunan skripsi ini.
2. Bapak Drs Johannes Simorangkir, MS selaku Kepala Laboratorium Kimia Bahan Alam beserta para stafnya atas fasilitas yang telah diberikan kepada penulis selama melakukan penelitian sampai tersusunnya skripsi ini.
3. Ibu DR. Rumondang Bulan, MS selaku Ketua Departemen Kimia dan Bapak Drs. Firman Sebayang, MS selaku Sekretaris Departemen Kimia FMIPA USU yang turut memberikan pengarahan dan mengesahkan skripsi ini
4. Bapak dan Ibu Staf Dosen jurusan Kimia FMIPA USU yang telah mendidik selama penulis dalam masa perkuliahan. Khususnya kepada Drs.Adil ginting,M.Sc sebagai dosen wali Penulis yang selalu mendukung perkuliahan penulis.
5. Rekan – rekan kuliah dan asisten laboratorium Kimia Bahan Alam Eva,Whendy,Saulina, Rony, Qiting, Albi dan sobat – sobat ku Eviyoana, Novri, Winda, Ajeng, Haposan, Vera, Jubel,Eviana, Tresna, Ocha, Donald dan semua stambuk 05 serta teman terdekat saya Herbet Manik,dan yang lain yang tidak dapat saya tuliskan yang telah membantu dan memberikan perhatiannya kepada penulis selama penelitian dan pengerjaan skripsi ini. Akhirnya penulis mengucapkan rasa terima kasih yang sedalam – dalamnya kepada kedua orang tuaku, Ayahanda tercinta A.Nababan dan Ibunda R.Sianipar serta Abang,Kakak dan kepada adik-adikku yang terbaik ,tersayang dan seluruh Keluargaku yang telah memberikan doa, semangat serta dorongan baik secara materi maupun moril sehingga penulis dapat menyelesaikan perkuliahan, penelitian dan penyusunan skripsi ini. Penulis menyadari sepenuhnya bahwa skripsi ini masih jauh dari sempurna, oleh karena itu penulis mengharapkan saran – saran dan kritik yang membangun dari berbagai pihak agar skripsi ini dapat bermanfaat bagi kita semua.
Medan, Januari 2010 Penulis
ISOLASI SENYAWA TERPENOIDA DARI EKSTRAK METANOL
BIJI BUAH DUKU
(Lansium domesticum L. )
ABSTRAK
THE ISOLATION TERPENOIDA COMPOUND OF EXTRACT METHANOL WHICH CONTAINED IN THE SEED OF DUKU
( Lansium domesticum L. )
ABSTRACT
DAFTAR ISI
Halaman
PERSETUJUAN ii
PERNYATAAN iii
PENGHARGAAN iv
ABSTRAK v
ABSTRACT vi
DAFTAR ISI vii
DAFTAR LAMPIRAN ix
BAB I. PENDAHULUAN
1.1. Latar Belakang 1
1.2. Permasalahan 3
1.3. Tujuan Penelitian 3
1.4. Manfaat Penelitian 3
1.5. Lokasi Penelitian 3
1.6. Metodologi Penelitian 3
BAB II. TINJAUAN PUSTAKA
2.1. Tumbuhan duku 5
2.1.1. Pengenalan Morfologi Dari Tanaman Duku 5
2.1.2. Sifat dan khasiat Tumbuhan Duku 5
2.1.3. Sistematika tumbuhan Duku 5
2.2. Senyawa Terpenoida 6
2.2.1. Klasifikasi Senyawa Terpenoida 6
2.3. Senyawa Triterpenoida 7
2.3.1. Klasifikasi Senyawa Triterpenoida 7
2.3.2. ... Biosintesis senyawa Triterpenoida 12
2.4.Teknik Pemisahan 14
2.4.1. Ekstraksi 14
2.4.2. Kromatografi 15
2.4.2.1. Kromatografi Lapis Tipis 15
2.4.2.1. Kromatografi Kolom 16
2.5.Teknik Spektroskopi
2.5.1. Spektrofotometri Inframerah ( FT – IR ) 19 2.5.2. Spektrometer Resonansi Magnetic Inti
Proton (1H-NMR) 20
BAB III. BAHAN DAN METODOLOGI PENELITIAN
3.1. Alat – alat 22
3.2. Bahan – bahan 23
3.3. Prosedur Penelitian
3.3.1. ... Penyediaan Sampel 23
3.3.2. ... Uji Pendahuluan Terhadap Ekstrak Tumbuhan
Biji Duku 23
3.3.2.1.
3.3.2.2.
Analisis Kromatografi Lapisan Tipis 24
3.3.3. ... Prosedur Untuk Memperoleh Senyawa Kimia dari
Ekstrak biji Duku 25
3.3.4. ... Isolasi Senyawa Terpenoida Dengan Kromatografi
Kolom 25
3.3.5. ... Pemurnian 26
3.3.6. ... Uji Kemurnian Hasil Isolasi Dengan Kromatografi
Lapis Tipis 26
3.3.7. ... Analisis Spektroskopi Kristal Hasil Isolasi 3.3.7.1.
Uji Kristal Hasil Isolasi Dengan
Spektrofotometer InfraMerah (FT-IR)32 27 3.3.7.2.
Uji Kristal Hasil Isolasi Dengan Spektroskopi Resonansi Magnetik Inti Proton (1H-NMR) 27
Bagan Penelitian 28
BAB IV. HASIL DAN PEMBAHASAN
4.1. Hasil Penelitian 29
4.2. Pembahasan 30
BAB V. KESIMPULAN DAN SARAN
5.1. Kesimpulan 36
5.2. Saran 36
DAFTAR PUSTAKA
DAFTAR LAMPIRAN
Lampiran 1. Determinasi Tumbuhan Duku Lampiran 2. Gambar Tumbuhan Duku
Lampiran 3. Kromatografi Lapisan Tipis Ekstrak Metanol biji buah Duku (Lansium domesticum L. )
Lampiran 4. Kromatogram Lapisan Tipis Senyawa Hasil Isolasi Melalui
Penampakan Noda dengan sinar Ultraviolet. Lampiran 5. Spektrum FT – IR Senyawa Hasil Isolasi.
ISOLASI SENYAWA TERPENOIDA DARI EKSTRAK METANOL
BIJI BUAH DUKU
(Lansium domesticum L. )
ABSTRAK
THE ISOLATION TERPENOIDA COMPOUND OF EXTRACT METHANOL WHICH CONTAINED IN THE SEED OF DUKU
( Lansium domesticum L. )
ABSTRACT
BAB 1 PENDAHULUAN
1.1 Latar Belakang
Bangsa Indonesia telah lama mengenal pengobatan secara tradisional, misalnya dengan tumbuhan, binatang dan mineral. Penggunaan tumbuh-tumbuhan tersebut adalah sebagai ramuan obat untuk penyakit-penyakit tertentu, ini merupakan suatu bukti bahwa di dalam ramuan obat tersebut terdapat senyawa-senyawa kimia yang berkhasiat. Dan salah satu senyawa kimia tersebut adalah senyawa triterpenoida (Arief, H. 2004).
Kebanyakan senyawa terpenoida terdapat bebas dalam jaringan tanaman, tidak
terikat dengan senyawa – senyawa lain, tetapi banyak diantara senyawa terpenoida
tersebut yang terdapat sebagai glikosida, ester dari asam organik dan dalam beberapa
hal terikat dalam protein. Senyawa terpenoida dengan berat molekul yang rendah
(senyawa C10 dan C15 ) sering dapat diperoleh dengan cara destilasi uap dari tanaman yang segar atau kering, sedangkan senyawa terpenoida dengan berat molekul yang
lebih tinggi ( C20 atau lebih ) biasanya diisolasi dengan cara ekstraksi dengan pelarut kemudian dipisahkan dan dimurnikan dengan cara kristalisasi, destilasi, dan
kromatografi (Sastrohamidjojo, H. 1996).
Salah satu tumbuhan tumbuhan yang biasa digunakan oleh masyarakat sebagai
obat adalah duku.Duku (Lansium Domesticum L.) biasanya digunaskan sebagai obat
tradisional misalnya biji duku yang berasa pahit digunakan sebagai obat cacing dan
demam yaitu dengan cara menumbuknya dan mencampurnya dengan air,kulit kayunya
digunakan sebagai obat disentri dan malaria,dan dapat digunakan untuk mengobati
gigitan kalajengking. Kulit buahnya juga dapat digunakan untuk mengobati diare
Dari kulit buah duku (Lansium domesticum L) telah diisolasi senyawa triterpen oleh
Magio Nishizawa,dkk pada tahun 1983.seperti dalam gambar berikut:
(Nishizawa.M,, 1983).
Dan sebelumnya telah dilakukan penelitian oleh K.Nakanishi dan K.Kabagashi pada tahun
1967 dan menghasilkan senyawa triterpenoida yang sering disebut dengan asam
langsat
H
CO2CH3
H H
H H
(Kiang.A.K,1967)
Dari uraian diatas maka penulis berminat untuk meneliti biji duku dan ingin
mengetahui kandungan dari biji duku, apakah juga mengandung senyawa terpenoida.
OH
CO
2CH
3 2029
22 30 8
3
23
27 24
28
H
H
H
H
1.2 Permasalahan
Permasalahan dalam penelitian ini adalah apakah di dalam biji duku (Lansium
domesticum L) juga mengandung senyawa terpenoida?
1.3 Tujuan Penelitian
Tujuan penelitian ini adalah untuk memperoleh senyawa terpenoida dari biji buah
duku (Lansium domesticum L.)
1.4 Manfaat Penelitian
Hasil penelitian diharapkan dapat memberi informasi terhadap pengembangan zat-zat
kimia dari biji buah duku (Lansium domesticum L.) berkhasiat dan memberikan
dukungan ilmiah pada bidang kimia bahan alam hayati.
1.5 Lokasi Penelitian
Sampel yang digunakan diambil dari Jl.Gadjah Mada, Medan, Sumatera Utara.
Penelitian dilakukan di Laboratorium Kimia Bahan Alam FMIPA Universitas
Sumatera Utara. Analisis Spektrofotometri Inframerah (FT – IR) dilakukan dibea
cukai Belawan dan Spektrometri Resonansi Magnetik Inti Proton (1H – NMR) dilakukan di Laboratorium Dasar FMIPA UNAIR Surabaya.
1.6 Metodologi Penelitian
Dalam penelitian ini, isolasi senyawa terpenoida digunakan biji buah duku (Lansium
domesticum.L) berupa serbuk halus yang kering sebanyak 1000 g. Langkah awal yang
dilakukan adalah dengan uji skrining fitokimia dengan menggunakan pereaksi –
pereaksi pada senyawa terpenoida yaitu dengan menggunakan pereaksi Salkowsky
Kemudian tahapan Isolasi yang dilakukan adalah :
a. Ekstraksi maserasi
b. Analisis Kromatografi Lapisan Tipis
c. Analisis Kromatografi Kolom
d. Pemurnian
e. Analisis Senyawa
Tahapan analisis senyawa hasil isolasi yang dilakukan mencakup :
a. Analisis Kromatografi Lapisan Tipis
b. Identifikasi dengan menggunakan Spektrofotometer Inframerah (FT – IR)
BAB 2
TINJAUAN PUSTAKA
2.1. Tumbuhan Duku (Lansium domesticum L.)
2.1.1. Pengenalan Morfologi Tumbuhan Duku
Duku (Lansium domesticum L.) merupakan tanaman berupa pohon yang berasal dari
Indonesia.Tanaman ini dapat tumbuh baik di dataran rendah sampai pada ketinggian
500 m dpl. Dengan tipe iklim basah sampai agak basah dengan curah hujan antara
1500-2500mm pertahun dan merata sepanjang tahun. pH tanaman yang baik adalah
6-7 dan tanaman ini relatif lebih toleran terhadap keadaan tanah. ( Setiawan.I.A., 2001 )
2.1.2. Sifat dan Khasiat Tumbuhan Duku (Lansium domestikum L.)
Tanaman duku selain buahnya dapat dimakan, masyarakat juga menggunakan biji
duku sebagai obat tradisional misalnya sebagai obat cacing dan demam yaitu dengan
cara menumbuknya dan mencampurnya dengan air,kulit kayunya dapat digunakan
sebagai obat disentri dan malaria.
2.1.3. Sistematika Tumbuhan Duku
Sistematika tumbuhan Duku adalah sebagai berikut :
Kingdom : Plantae
Divisi : Spermatophyta
Kelas : Dicotylledoneac
Ordo : Rutales
Familia : Meliaceae
Genus : Lansium
2.2Senyawa Terpenoida
Senyawa terpenoida berasal dari molekul isoprene CH2=C(CH3)-CH=CH2 dan kerangka karbonnya dibangun oleh penyambungan dua atau lebih satuan C5 ini. Kedua senyawa – senyawa itu dibagi – bagi menjadi beberapa golongan berdasarkan
jumlah satuan yang terdapat di dalam senyawa tersebut; dua (C10), tiga (C15), empat (C20), enam (C30), atau delapan (C40) satuan. Terpenoida terdiri atas beberapa macam senyawa, mulai dari komponen minyak atsiri, yaitu monoterpenoida dan
seskuiterpenoida yang mudah menguap (C10 dan C15), diterpena yang lebih sukar menguap (C20), sampai senyawa yang tidak menguap, yaitu triterpenoida dan sterol (C30), serta pigmen karotenoida (C40 ) (Harborne,J.B.1987).
Senyawa terpenoida dikaitkan terhadap bentuk strukturnya.Komposisi
senyawa terpenoida (C10, C15, C20, C30, dan sebagainya) dapat dipandang merupakan kelipatan satuan lima atom dan satuan tersebut mempunyai kerangka karbon isopentil
(Sastrohamidjojo,H.1996).
Unit-unit isoprena ganda dalam suatu terpen berfungsi untuk klasifikasi:C10 (monoterpen), C15 (seskuiiterpen), C20 (diterpena), C30 (Triterpena) yang berkaitan erat dengan steroida,C25 (sesterpena) adlah suatu hal yang mengherankan untuk diperhatikan bahwa aturan isoprena yang sangat berguna tidak saja untuk
mengungkapakan struktur,memiliki landasan yang tidak alami.Meskipun demikian
banyak terpena yang memiliki struktur yang tidak dapat dikategorikan sebagai satuan
lima karbon dengan kerangka isoprena.Sekarang diketahui bahwa senyawa terpenoida
tidak diturunkan dari isoprena sendiri, dan isoprena sendiri merupakan senyawa yang
2.2.1. Klasifikasi Senyawa Terpenoida
Senyawa terpenoida dapat terbagi ke dalam beberapa golongan utama terpenoida,
yaitu : Jumlah satuan isoprena Jumlah karbon
Golongan Jenis utama dan sumbernya
1 2 3 4 6 8 N C5 C10 C15 C20 C30 C40 Cn isoprena monoterpenoida seskuiterpenoida diterpenoida triterpenoida tetraterpenoida poliisoprena
Dideteksi dalam daun Hamammelis japonica
Monoterpena dalam minyak atsiri tumbuhan
Seskuiterpenoida dalam minyak atsiri
Seskuiterpenoida dalam lakton ( dalam
Compositae )
Abisin ( mis : asam abisat )
Asam diterpena dalam dammar tumbuhan
Giberalin ( mis : asam giberelat )
Sterol ( mis : sitosterol )
Triterpena ( mis : β - amirin ) Saponin ( mis : yamogenin )
Glikosida jantung
Rubber contohnya tumbuhan Hevea
brasilliensis
Karotyenoid ( mis : β - karotena )
2.3. Senyawa Triterpenoida
Senyawa triterpenoida yang dijumpai di alam terdapat dalam dua bentuk yaitu bentuk
asiklik dan siklik. Di alam, senyawa ini terdapat pada tumbuhan dan hewan, senyawa
ini terdapat dalam bentuk ester dari senyawa glikosida atau membentuk suatu senyawa
yang kerangka dasarnya mempunyai persekutuan dengan senyawa glikosida, berarti
senyawa – senyawa triterpenoida dialam mempunyai bentuk – bentuk yang berbeda
Triterpenoida merupakan salah satu golongan senyawa terpenoida yang
mempunyai atom karbon sebanyak (C30) pada kerangka dasarnya, dan secara teoritis rantainya dibentuk oleh enam unit molekul isoprena.Senyawa ini berstruktur
siklik,kebanyakan berupa alkohol, aldehid atau asam karboksilat,berupa senyawa
tidak berwarna, berbentuk kristal, seringkali bertitik leleh tinggi dan optis aktif, yang
umumnya sukar dicirikan karena tidak ada kereaktifan kimianya.Uji yang banyak
digunakan ialah reaksi Lieberman-Bouchard (anhidrida asetat-H2SO4) yang dengan kebanyakan triterpen dan sterol memberikan warna hijau biru (Harborne J.B. 1987).
2.3.1. Klasifikasi Senyawa Triterpenoida
Berdasarkan bentuk dan keadaan senyawa triterpenoida, maka senyawa ini dapat
diklasifikasikan sebagai berikut :
1. Senyawa steroida
Merupakan salah satu golongan senyawa triterpenoida yang struktur dasarnya
mempunyai cincin tetrasiklik yang tak jenuh. (Robinson,T., 1995)
Contoh : Stigmasterol
H3C
CH3 C2H5
H3C
HO
CH3
2. Senyawa triterpena
Triterpena tersebar sangat luas pada tumbuhan dan hewan.Terdapat dalam
keadaan bebas sebagai ester atau glikosida
1. Triterpena asiklik, yaitu senyawa triterpena yang tidak mempuinyai cincin tertutup pada strukturnya, misalnya skualena, senyawa ini berupa kristal yang
tidak berwarna, mempunyai titik leleh tinggi, dan bersifat optis aktif.
Contoh : Skualena
2. Triterpena trisiklis, yaitu senyawa triterpena yang mempunyai tiga cincin tertutup pada struktur molekulnya, misalnya Ambrein.
H3C CH3
CH3 CH3
CH3
CH3
3. . Triterpena tetrasiklis, yaitu senyawa triterpena yang mempunyai empat cincin
tertutup pada struktur molekulnya, misalnya Lanosterol. Dimana senyawa ini
merupakan golongan tetrasiklis yang memiliki rangka
perhidroksiklopentanofenantren dan dapat dianggap sebagai intermediate, dan
senyawa ini berhubungan erat dengan struktur sterol.
Contoh : Lanosterol
4. . Triterpena pentasiklis, yaitu triterpena yang mempunyai lima cincin tertutup pada struktur molekulnya. Senyawa ini terdapat pada tumbuh – tumbuhan
yang terikat dengan senyawa – senyawa gula yang disebut dengan triterpen
glikosida.
3. Saponin
Saponin adalah salah satu golongan triterpenoida glikosida, dimana kerangka dasarnya
berhubungan erat dengan struktur senyawa sterol dan triterpenoida. Bila senyawa ini
dihidrolisis akan menghasilkan suatu senyawa aglikon ( saponin steroida ) dan
glikosida ( gula ). Aglikon yang membentuk senyawa saponin ini adalah merupakan
senyawa triterpenoida, sterol dan sapogenin steroida. Senyawa saponin dapat
menurunkan tegangan permukaan cairan dan dapat menghemolisi darah. Saponin larut
dalam air, biasanya berasa pahit. Contohnya : Helogenin (Harborne.J.B.,1987).
O
O CH3
CH3 O
CH3
4. Kardiak glikosida
Kardiak glikosida adalah salah satu golongan triterpenoida, dimana kerangka dasarnya
sama dengan triterpenoida dan steroida. Akan tetapi pada atom C17 berikatan langsung dengan senyawa glikosida atau senyawa turunan furan. Senyawa kardiak glikosida ini
sukar dihidrolisa sebab ikatan ikatan glikosida tadi tidak sama dengan ikatan glikosida
pada senyawa saponin. Senyawa saponin adalah suatu senyawa ester dari suatu
glikosida dengan aglikon. Contoh : Digitoksigenin (Makin,H.L. 1975) .
O
O CH3
OH CH3
OH
2.3.2.Biosintesa Senyawa Triterpenoida
Biosintesa Senyawa Triterpenoida
Telah lama diduga bahwa penggulungan dari unit Isoprena dalam molekul Terpenoida
menunjukkan bahwa proses biosintesa molekul-molekul tersebut merupakan suatu
kesatuan akan tetaspi senyawa dasar dalam biosintesa Terpenoida ialah asam
CH
3COOH
Asam asetat
CoA-SH
CH
3COSCoA
Asetil Ko-A
2CH
3COSCoA
Asetil Ko-A
CH
3COCH
2COSCoA
+
CoASH
Asetoasetil Ko-A
H
3C C
O
CH2COSCoA
Asetoasetil Ko-A
+
CH
3COSCoA
Asetil Ko-A
HOOCCH
2C
H
3C
CH
2COSCoA
OH
Turunan asam glutarat
HOOCCH
2C
H
3C
OH
[ H ]
H
2O
CH
2CH
2asam mevalonat
Asam mevalonat dibentuk dari kondisi aldol asam asetat dan membentuk
rantai cabang. Perubahan selanjutanya menjadi Isopentenil pirofosfat yakni Isoprene
biologis yang sesungguhnya aktif untuk melakukan penggabungan yang berturut-turut
HOOC-CH
2C
H
3C
OH
CH
2CH
2OH
Asam mavalonat
ATP
2 tahap
H
3C
OP
C
CH2 CH2 OP CH2COO
-ATP
H
3C
C OPH2C
CH2 OP CH2 C=O O
-dekarboksilasi
CH
2=C-CH
2-CH
2-OP
CH3
isopentenil
pirofosfat
CH
3-C=CH-CH
2-OP
CH3
Triterpenoida (C20) dan warna karotenoida (C40) berasal dari dimerisasi C15 dan C20 pirofosfat dan bukan dari polimerisasi terus-menerus dari unit C5. Yang banyak diketahui ialah dimerisasi Farnesil pirofosfat menjadi skualena yang
merupakan Triterpenoida dasar dan sumber dari Triterpenoida lainnya dan Steroida.
Siklisasi dari skualena menghasilkan tetrasiklis triterpenoida Lanosterol. Reaksi
OP
isopentil pirofosfat
3 X C5
OP O
Farnesil pirofosfat (FPP)
FPP
skualena CH3
CH3
OH CH3
Protosterol karbonium ion
LANOSTEROL
2.4. Teknik Pemisahan
Berdasarkan pemisahan fasanya teknik pemisahan ada dua yaitu:
1) Pemisahan kimia adalah suatu teknik pemisahan berdasarkan perbedaan dari
sifat campuran yang hendak dipisahkan. Contohnya proses ekstraksi.
2) Pemisahan fisika merupakan pemisahan yang didasarkan pada perbedaan –
perbedaan kecil dari sifat – sifat fisika antara beberapa campuran senyawa.
Misalnya daya penguapan, kemampuan adsorpsi, polaritas, dan ukuran
molekul (Edward,J. dan Stevenson,R. 1991).
2.4.1. Ekstraksi
Ekstraksi dapat dilakukan dengan metode maserasi, perkolasi, dan sokletasi. Sebelum
ekstraksi dilakukan, biasanya serbuk tumbuhan dikeringkan lalu dihaluskan dengan
Ekstraksi dengan metode sokletasi dapat dilakukan secara bertingkat dengan berbagai
pelarut berdasarkan kepolarannya, misalnya : n – heksana, eter, benzene, kloroform,
etil asetat, etanol. metanol, dan air.
Ekstraksi dianggap selesai bila tetesan ekstrak yang terakhir memberikan
reaksi negatif terhadap senyawa yang diekstraksi. Untuk mendapatkan larutan ekstrak
yang pekat biasanya pelarut ekstrak diuapkan dengan menggunakan alat rotary
evaporator (Mulja,M.dan Suharman,H. 1995).
2.4.2. Kromatografi
Kromatografi didefenisikan sebagai pemisahan campuran dari dua atau lebih senyawa
atau ion dengan mendistribusikannya diantara dua fasa yaitu fasa diam dan fasa
bergerak. Dasar dari pemisahan ini adalah perbedaan daya serap atau daya larut pada
kedua fasa tersebut (Gritter,R.J. dan James. 1991).
Kromatografi adalah proses melewatkan sampel melalui suatu
kolom,perbedasan kemampuan adsorbsi terhadap zat-zat yang sangat mirip
mempengaruhi resolusi zat terlarut dan menghasilkan apa yang disebut dengan
kromatogram (Khopkar,S. 1990).
2.4.2.1. Kromatografi Lapisan Tipis
Kromatografi merupakan metoda pilihan untuk pemisahan semua kandungan yang
larut dalam lipid, steroid, karotenoid, kuinon sederhana dan klorofil. Satu kekurangan
kromatografi lapis tipis yang asli adalah kerja penyaputan plat kaca dengan penyerap.
Bila kromatografi lapis tipis dibandingkan dengan kromatografi kertas, kelebihan
kromatografi lapis tipis adalah keserbagunaan, kecepatan dan kepekaannya.
Keserbagunaan kromatografi lapis tipis disebabkan oleh kenyataan bahwa di samping
selulosa, sejumlah penyerap yang berbeda-beda dapat disaputkan pada plat kaca atau
Teknik dasar dalam melaksanakan pemisahan dengan kromatografi lapis tipis
adalah sebagai berikut. Pertama kali lapisan tipis adsorben dibuat pada permukaan plat
kaca atau plat lain, misalnya berukuran 5 x 20 cm. Tebal lapisan adsorben dapat
bervariasi tergantung penggunaannya. Larutan campuran senyawa yang akan
dipisahkan diteteskan pada kira-kira 1,5 cm dari bagian bawah plat dengan
menggunakan pipet mikro atau syringe. Zat pelarut yang terdapat pada sampel yang
diteteskan tersebut kemudian diuapkan dahulu Selanjutnya plat kromatografi
dikembangkan dengan mencelupkannya pada chamber yang berisi campuran zat
pelarut. Tinggi permukaan zat pelarut dalam chamber harus lebih rendah dari letak
tetesan sampel pada plat kromatografi. Dengan pengembangan tersebut
masing-masing komponen senyawa dalam sampel; akan bergerak ke atas dengan kecepatan
yang berbeda Perbedaan kecepatan gerakan ini merupakan akibat dari terjadinya
pengaruh proses dengan kromatografi lapis tipis, mulai pemilihan adsorben sampai
identifikasi masing-masing komponen yang telah terpisah.
Kromatografi lapis tipis merupakam kromatografi adsorbsi dan adsorben bertindak
sebagai fasa tetap. Empat macam adsorben yang umum dipakai adalah silika gel
(asam silikat), alumina (aluminium oksida), kieselgur (diatomeus earth), dan selulosa
(Hosttetman,dan Marston. 1950).
Kromatogram pada kromatografi lapis tipis merupakan noda-noda yang terpisah
setelah divisualisasi dengan cara fisika atau kimia. Visualisasi cara fisika yaitu dengan
melihat noda kromatogram yang mengadsorbsi radiasi ultraviolet atau berfluoresensi
dengan radiasi ultraviolet pada λ = 254 nm. Visualisasi dengan cara kimia adalah
dengan mereaksikan kromatogram dengan pereaksi warna yang memberikan warna
atau fluoresensi sensitif. Visualisasi cara kimia ini dilakukan dengan cara
penyemprotan dengan atomizer atau memberikan zat uap kimia pada kromatogram
atau dengan pencelupan ke dalam pereaksi penampak warna
2.4.2.2. Kromatografi Kolom
Pada kromatografi kolom, campuran yang dipisahkan diletakkan berupa pita bagian
atas kolom penyerap yang berada dalam tabung kaca, tabung logam atau bahkan
tabung plastik. Pelarut (fasa gerak) dibiarkan mengalir melalui kolom karena aliran
yang disebabkan oleh gaya berat atau didorong dengan tekanan. Pita senyawa linarut
bergerak melalui kolom dengan laju yang berbeda, memisahkan dan dikumpulkan
berupa fraksi ketika keluar dari atas kolom.
Ada empat perubahan utama yang dilakukan pada kolom klasik. Pertama,
dipakai penyerap yang lebih halus dengan ukuran kisaran mesh lebih sempit tercapai
kesetimbangan yang lebih baik di dalam sistem. Kedua, sistem tekanan biasanya
pompa mekanis dipakai untuk mendorong pelarut melalui penyerap yang halus.
Ketiga, detektor telah dikembangkan sehingga diperoleh analisis senyawa, ketika
senyawa itu keluar dari kolom. Keempat, penyerap baku dan penyerap cara kemasan
kolom baru dapat dikembangkan sehingga memungkinkan derajat daya pisah yang
tinggi tercapai (Edward,J.dan Stevenson,R.1991).
Kolom hanya berupa tabung kaca yang dilengkapi dengan keran pada salah
satu ujungnya dan ukurannya sedemikian rupa sehingga nisbah garis tengah terhadap
panjang kolom dalam rentang 1 : 10 sampai 1 : 30. Ukuran volume yang diperlukan
untuk suatu pemisahan dapat dihitung sacara kasar bila bobot campuran
diketahui.Mengemas kolom harus dilakukan dengan hati-hati agar hasil kolom kemas
yang serba sama. Jika kolom tidak mempunyai penyaring, mula - mula kita harus
menyumbat leher kolom dengan segumpal kaca wool atau kapas.
Pengisian kolom harus dikerjakan dengan seragam, setelah adsorben
dimasukkan dapat diseragamkan kerapatannya dalam kolom dengan menggunakan
vibrator atau dengan plunger. Selain itu dapat juga dikerjakan dengan memasukkan
Pengisian kolom yang tidak seragam akan menghasilkan rongga-rongga di tengah –
tengah kolom. Cara memecahkan masalah ini dapat dikerjakan dengan mengadakan
back flushing, sehingga terjadi pengadukan yang seterusnya dibiarkan lagi
mengendap. Pada bagian bawah (dasar) dan atas dari isian kolom diberi wool karena
(glass wool) atau sintered glass diss untuk menyangga isian. Bila kolom telah diisi
bahan isian permukaan cairan tidak boleh dibiarkan turun di bawah permukaan bahan
isian bagian atas, karena akan memberikan peluang masuknya gelembung-gelembung
udara masuk ke dalam kolom (Hosttetman.dan Marston.1995).
Pemilihan pertama dari pelarut ialah bagaimana sifat kalarutannya. Tetapi
sering lebih baik untuk memilih suatu pelarut yang tak tergantung daripada tekanan
kekuatan elusi sehingga zat-zat elusi yang lebih kuat dapat dicoba. Yang dimaksud
dengan kekuatan dari zat elusi adalah daya penyerapan pada penyerap dalam kolom.
Biasanya untuk penyerap-penyerap yang polar seperti alumina dan silika gel maka
kekuatan penyerap naik dengan kenaikan polaritas zat-zat yang diserap
(Sastohamidjojo H. 1995).
2.5. Teknik Spektroskopi
Teknik spektroskopik adalah salah satu teknik analisis kimia – fisika yang mengamati
tentang interaksi atom atau molekul dengan radiasi elektromagnetik.Untuk
pelaksanaan teknik analisis spektroskopik dipakai instrument sebagai pengukur dan
perekam sinyal interaksi molekul dengan radiasi elektromagnetik.Ada dua macam
instrumen pada teknik spektroskopik yaitu spektrometer dan spektrofotometer.
Instrumen yang memakai monokromator celah tetap pada bidang fokus disebut
sebagai spektrometer. Apabila spektrometer tersebut dilengkapi dengan detektor yang
bersifat fotoelektrik maka disebut spektrofotometer
(Muldja,M.,dan Suharman.H. 1955).
Informasi Spektroskopi Inframerah menunjukkan tipe – tipe dari adanya gugus
bilangan dari setiap tipe dari atom hidrogen. Ini juga memberikan informasi yang
menyatakan tentang alam serta lingkungan dari setiap tipe dari atom hidrogen.
Kombinasinya dan data yang ada kadang – kadang menentukan struktur yang lengkap
dari molekul yang tidak diketahui (Pavia L. D. 1979).
2.5.1.Spektrofotometri Inframerah ( FT-IR )
Bila sinar infra merah dilewatkan melalui cuplikan senyawa organik, maka sejumlah
frekuensi diserap sedangkan frekuensi yang lain diteruskan atau ditransmisikan tanpa
diserap. Jika kita menggambar antara persen absorbansi atau persen transmitansi
lawan frekuensi maka akan dihasilkan suatu spektrum infra merah. Ikatan-ikatan yang
berbeda (C-C, C=C, C≡C, C-O, C=O, O-H, N-H) mempunyai frekuensi vibrasi yang berbeda dan kita dapat mendeteksi adanya ikatan-ikatan tersebut dalam molekul
organik dengan mengidentifikasi frekuensi-frekuensi karakteristiknya sebagai pita
serapan dalam spektrum infra merah.Spektrum infra merah alkohol pada konsentrasi
yang rendah menunjukkan sebuah pita yang tajam pada 3650 cm-1 di samping adanya pita lebar tambahan pada 3350 cm-1 (Noerdin,D. 1985).
Dalam molekul sederhana beratom dua atau beratom tiga tidak sukar untuk
menentukan jumlah dan jenis vibrasinya dan menghubungkan vibrasi – vibrasi
tersebut dengan dengan energy serapan.tetapan untuk molekul – molekul beratom
banyak, analisa jumlah dan jenis vibrasi itu menjadi sukar sekali atau tidak mungkin
sama sekali karena bukan saja disebabkan besarnya jumlah pusat – pusat vibrasi,
melainkan juga karena harus diperhitubgkan terjadinya saling mempengaruhi
(interaksi) beberapa pusat vibrasi.
Vibrasi molekul dapat dibagi dalam dua golongan yaitu vibrasi regang (stretching)
dan vibrasi lentur ( bending vibrations ).
1.Vibrasi Regang
Terjadi perubahan jarak antara dua atom dalam suatu molekul secara terus – menerus.
2.Vibrasi Lentur
Terjadi perubahan sudut antara dua ikatan kimia. Ada dua macam vibrasi lentur yaitu
vibrasi lentur dalam bidang dan vibrasi luar bidang.
Jelaslah sekarang bahwa Spektrometer Infra-merah ditujukan untuk penentuan gugus
– gugus fungsi molekul. Radiasi IR dapat dibagi ke dalam dua daerah, yaitu :
-. Daerah gugus fungsi pada pada rentang vibrasi antara 4000 hingga 1600 cm-1. -. Daerah sidik jari pada rentang vibrasi antara 1600 hingga 670 cm-1.
Radiasi IR yang dipakai harus berada pada rentang frekuensi yang sesuai
dengan rentang getaran alamiah dari molekul agar diperoleh informasi gugus – gugus
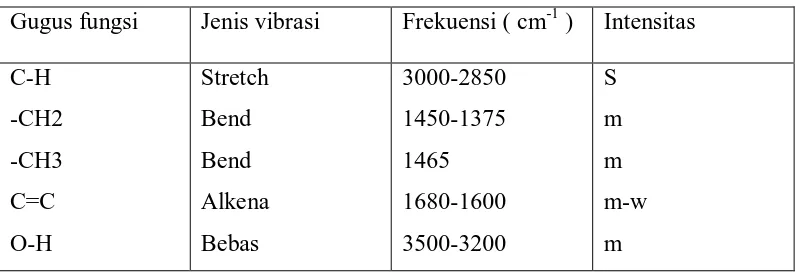
[image:32.595.108.508.392.528.2]molekul dari zat yang dianalisis. ( Muldja M. Dan Suharman,H. 1995).
Tabel : Absorpsi karakteristik infra-merah dari gugus – gugus fungsi molekul.
Keterangan :
S = kuat, m = sedang, w = lemah
Gugus fungsi Jenis vibrasi Frekuensi ( cm-1 ) Intensitas
C-H -CH2 -CH3 C=C O-H Stretch Bend Bend Alkena Bebas 3000-2850 1450-1375 1465 1680-1600 3500-3200 S m m m-w m
2.5.2. Spektrometer Resonansi Magnetik Inti ( 1H-NMR )
Spektrometri Resonansi Magnetik Inti (Nuclear Magnetic Resonance, NMR)
merupakan alat yang berguna pada penentuan struktur molekul organik. Teknik ini
memberikan informasi mengenai berbagai jenis atom hidrogen dalam molekul.
Struktur NMR memberikan informasi mengenai lingkungan kimia atom hidrogen,
jumlah atom hidrogen dalam setiap lingkungan dan struktur gugusan yang berdekatan
Pergeseran kimia adalah pengukuran medan dalam keadaan bebas. Semua
proton – proton dalam satu molekul yang ada dalam lingkungan kimia yang serupa
kadang – kadang menunjukkan pergeseran kimia yang sama. Setiap senyawa
memberikan penaikan menjadi puncak absorpsi tunggal dalam spektrum NMR.
(Silverstein.R.M. 1981).
Dalam spektroskopi NMR, suatu contoh senyawa ditaruh di antara
kutub-kutub sebuah magnet yang cukup kuat untuk mensearahkan sebagian dari inti-inti
yang mempunyai momen magnet. Contoh itu kemudian disinari dengan radiasi
elektromagnet, biasanya dalam jangkau frekuensi radio 107 - 108 Hz. Sebuah inti yang berpusing yang disearahkan dengan medan magnet itu dapat dibalikkan arahnya
dengan cara menyerap sebuah proton yang energinya tepat sesuai. Inti yang berlainan
atau inti yang serupa tetapi terikat pada lingkungan yang berlainan, menyerap foton
pada panjang gelombang yang berlainan. Pola frekuensi radio yang diserap
merupakan spektrum NMR dari senyawa itu. (Cresswell,C.J.R dan Campbell.1982).
Di dalam medan magnet , perputaran elektron – elektron valensi dari proton
menghasilkan medan magnet yang melawan medan magnet yang digunakan. Hingga
setiap proton dalam molekul dilindungi dari medan magnet yang digunakan mengenai
dan bahwa besarnya perlindungan ini tergantung pada kerapatan elektron yang
mengelilinginya.Makin besar kerapatan elektron yang mengelilingi inti, maka makin
besar pula medan yang dihasilkan yang melawan medan magnet yang digunakan.
Akibat secara keseluruhan/proton merasakan adanya pengurangan medan yang
mengenainya. Karena inti merasakan medan magnet yang dirasakan lebih kecil, maka
ia akan mengalami presesi pada frekuensi yang lebih rendah. Setiap proton dalam
molekul mempunyai lingkungan kimia yang sedikit berbeda yang akan
BAB 3
BAHAN DAN METODE PENELITIAN
3.1. Alat – alat
- Kolom kromatografi Pyrex 20 / 40
- Rotary evaporator Buchi B - 480
- Gelas Erlenmeyer Pyrex 250 ml
- Gelas Beaker Pyrex 250 ml
- Gelas ukur Pyrex 100 ml
- Neraca analitis Mettler PM 480
- Oven Memmers
- Corong pisah Duran 500 ml
- Labu alas Pyrex 500 ml
- Blender
- Bejana
- Plat skrining
- Plat kromatografi lapisan tipis ( KLT )
- Pipet tetes
- Statif dan Klem
- Batang pengaduk
- Bejana Kromatografi Lapisan Tipis
- Lampu UV
- Botol vial
- Spektrofotometer FT-IR ( Jasco FT / IR – 5300 )
3.2. Bahan – bahan
- Biji duku(Lansium domesticum L)
- Metanol
- n- Heksana
- Etil asetat
- Silika gel 60 G ( E. Merck. Art. 7734 )
- Silika gel 60 GF 254 ( E. Merck. Art. 10180 ) - Aseton
- CeSO4 1% - Aquadest
- H2SO4 (p)
3.3. Prosedur Penelitian
3.3.1. Penyediaan sampel
Sampel yang diteliti adalah biji buah duku (Lansium domesticum L.) yang diperoleh
dari pasar Jl. Gajah Mada Medan, Sumatera Utara. Biji buah duku dikeringkan di
udara terbuka, lalu dihaluskan sampai diperoleh serbuk biji buah duku (Lansium
domesticum L.) sebanyak 1000 g.
3.3.2. Uji Pendahuluan Terhadap Ekstrak Biji Buah Duku
Serbuk biji buah duku (Lansium domesticum L) yang telah diperoleh diidentifikasi
dengan menggunakan cara :
1. Skrining Fitokimia senyawa kimia bahan alam
3.3.2.1. Skrining Fitokimia
Untuk mengetahui adanya senyawa Terpenoida yang terdapat pada biji buah duku
(Lansium domesticum L.) maka dilakukan uji pendahuluan secara kualitatif dengan
pereaksi warna yaitu uji skrining fitokimia, dimana ditimbang 10 g serbuk biji duku
dan dimaserasi dengan 50 ml metanol selama 24 jam, disaring. Filtrat yang diperoleh
dibagi ke dalam tiga bagian :
1. Filtrat pertama ditambahkan 2 tetes pereaksi salkowsky yaitu larutan H2SO4 (p) menghasilkan larutan berwarna merah. Hal ini menunjukkan adanya
senyawa terpenoida
2. Filtrat kedua ditambahkan 2 tetes pereaksi Lieberman – Bouchard yaitu
campuran antara H2SO4 (p) dan CH3COOH anhidrid dengan perbandingan (1 : 20 v/v) menghasilkan larutan berwarna hijau kebiruan. Hal ini menunjukkan
adanya senyawa terpenoida.
3. Filtrat ketiga ditambahkan aquades tidak menghasilkan buih yang stabil.Hal ini
menunjukkan tidak adanya terpenoid glikosida.
3.3.2.2.Analisis Kromatografi Lapisan Tipis ( KLT )
Analisis Kromatografi Lapisan Tipis dilakukan terhadap ekstrak pekat n – heksana
dengan menggunakan fasa diam silika gel 60 GF254 ( E. Merck. Art. 10180 ). Fasa gerak yang digunakan adalah n- heksana 100 %, dan campuran n – heksana : aseton
dengan perbandingan ( 90 : 10 v/v ), ( 80 : 20 v/v ), dan ( 70 : 30 v/v )
Prosedur :
Dimasukkan 10 ml larutan fasa gerak n – heksana 100 % ke dalam bejana
kromatografi. Ditotolkan ekstrak pekat metanol pada plat KLT yang telah diaktifkan.
Dimasukkan plat ke dalam bejana yang telah berisi pelarut, lalu ditutup rapat dan
dielusi. Plat yang telah dielusi dikeluarkan dari bejana, dan dikeringkan. Diamati
warna bercak yang timbul dan dihitung harga Rf yang diperoleh. Perlakuan yang sama
dilakukan untuk perbandingan pelarut n- heksana : aseton (90 : 10 v/v), (80 : 20 v/v),
duku (Lansium domesticum L.) terdapat senyawa Terpenoida,dan hasil pemisahan
yang baik diberikan pada fasa gerak n – heksana : aseton ( 80 : 20 v/v ).
3.3.3. Prosedur untuk Memperoleh Senyawa Kimia dari Eksrak Serbuk biji
duku ( Lansium DomesticumL.)
Serbuk dari biji buah duku (Lansium domesticum L.) diekstraksi maserasi dengan
menggunakan pelarut metanol.
Prosedur :
Serbuk halus biji buah duku (Lansium domesticum L.) ditimbang sebanyak
1000 g, dimasukkan ke dalam bejana dan ditambahkan pelarut metanol sampai semua
sampel terendam oleh pelarut dan dibiarkan selama 48 jam. Maserat disaring dan
diperoleh ekstrak berwarna coklat. Maserasi dilakukan kembali secara berulang –
ulang dengan menggunakan pelarut metanol. Ekstrak metanol yang diperoleh
dikumpulkan dan dipekatkan dengan menggunakan alat rotary evaporator pada suhu
65oC sehingga diperoleh ekstrak pekat metanol. Dilanjutkan dengan ekstraksi partisi dengan menggunakan n - heksana : air ( 1 : 1 v/v ), dimana akan terbentuk lapisan n –
heksana dan lapisan metanol/air. Kedua lapisan diskrining fitokimia. Lapisan
metanol/air memberikan hasil yang positif terhadap senyawa Triterpenoid. Diambil
fraksi – metanol yang memberikan hasil positif. Fraksi metanol tersebut dipekatkan
dengan menggunakan alat rotary evaporator, sehingga diperoleh ekstrak pekat metanol
sebanyak 50 ml
3.3.4. Isolasi Senyawa Terpenoida Dengan Kromatografi Kolom
Isolasi senyawa terpenoida dengan cara Kromatografi Kolom dilakukan
terhadap ekstrak pekat metanol biji buah duku (Lansium domesticum L.). Fasa diam
yang digunakan adalah silika gel 60 G ( E. Merck. Art. 7734 ) dan fasa geraknya
adalah n- heksana 100 % dan campuran n – heksana : aseton dengan perbandingan (
Prosedur :
Dirangkai seperangkat alat kolom kromatografi. Terlebih dahulu dibuburkan
silika gel 60 G ( E. Merck. Art. 7734 ) dengan menggunakan n – heksana 100 %
diaduk – aduk hingga homogen lalu dimasukkan ke dalam kolom kromatografi.
Kemudian dielusi dengan n – heksana 100 % hingga bubur silika gel padat dan
homogen. Dimasukkan 7 g ekstrak pekat metanol biji buah duku ke dalam kolom
kromatografi yang telah berisi bubur silika gel. Sampel dibiarkan turun dan terserap
dengan baik pada silika gel di puncak kolom, lalu ditambahkan fasa gerak n – heksana
100 % secara perlahan – lahan, dan diatur sehingga aliran fasa yang keluar dari kolom
sama banyaknya dengan penambahan fasa gerak dari atas. Lalu dinaikkan kepolaran
dari pelarut pengelusi dengan mencampurkan n – heksana : aseton dengan
perbandingan ( 80 : 20 v/v). Hasil yang diperoleh ditampung ke dalam beberapa botol
vial, lalu diuapkan di udara terbuka sampai pelarutnya habis sehingga terbentuk pasta.
3.3.5. Pemurnian
Pasta yang diperoleh masih bercampur dengan pengotor sehingga perlu dilakukan
pemurnian terhadap pasta.
Prosedur :
Pasta yang diperoleh terdapat pada perbandingan pelarut n – heksana : aseton
( 80 : 20 v/v ). Pasta tersebut dikolom kembali dengan menggunakan silika gel 60G
dengan pelarut n-heksana:etil asetat (60 : 40 v/v) hingga dihasilkan pasta yang lebih
murni
3.3.6. Uji Kemurnian Hasil Isolasi Dengan Kromatografi Lapisan Tipis
Uji kemurnian pasta dilakukan dengan kromatografi Lapisan Tipis dengan
Prosedur :
Dimasukkan 10 ml larutan fasa gerak ke dalam bejana kromatografi, lalu
dijenuhkan. Ditotolkan kristal pada plat KLT yang telah diaktifkan. Dimasukkan plat
KLT tersebut ke dalam bejana kromatografi yang telah jenuh. Setelah pelarut fasa
gerak merembes ke atas, plat KLT dikeluarkan dari bejana, dikeringkan, dan difiksasi
dengan pereaksi 1% cerium sulfat dalam 10 % asam sulfat, menghasilkan bercak
berwarna coklat yang menunjukkan adanya senyawa Terpenoida. ( Lampiran 3 ).
3.3.7. Analisis Spektroskopi Hasil Isolasi.
3.3.7.1. Uji Hasil Isolasi Dengan Spektrofotometer Inframerah
Analisis spektrum inframerah dengan alat Spektrofotometer FT-IR diperoleh dari
Laboratorium Bea Cukai bagian identifikasi barang, Belawan ( Lampiran 4 ).
3.3.7.2. Uji Hasil Isolasi Dengan Spektroskopi Resonansi Magnetik Inti Proton 1
H – NMR.
Analisis ini dilakukan di Laboratorium Dasar Bersama FMIPA UNAIR Surabaya
3.4.Bagan Penelitian
←Diekstraksi dengan metanol sebanyak (3 liter) ←Didiamkan selama ± 48 jam
←Diulangi sebanyak 4 x
←Diskrining Fitokimia
←Dipekatkan dengan rotarievaporator
← Difraksinasi dengan n-heksana secara berulang-ulang
←Dipekatkan dengan rotarievaporator
←Diuji dengan pereaksi Lieberman bouchardat,salkowsky
←Dianalisis KLT untuk menentukan eluen pada pemisahan kromatografi kolom ←Dibuburkan dengan silica gel sebanyak 140 g
←Dipisahkan dengan kromatografi kolom dengan fasa diam silica gel 60 GE netral dan gerak
(eluen) n-heksana:Aseton
←Ditampung setiap fraksi di dalam botol vial sebanyak 15 ml
←diuji pereaksi ←diuji pereaksi ←diKLT ←diuji pereaksi
← digabungkan Rf sama
←diuapkan
←dimurnikan ←dianalisis KLT
←dianalisis
1000 g serbuk kering biji duku
Ekstrak methanol Residu
Ekstrak pekat metanol
Fraksi Metanol Fraksi n-heksana
Ekstrak pekat metanol
Fraksi 1-28 n-heksan 100% Fraksi 29-147 n-heksan: aseton 8:2 v/v Fraksi 148-190 n-heksan-aseton 7:3 v/v Fraksi 191-226 n-heksan-aseton 6:4 v/v
Hasil negatif Hasil positif Hasil positif
Fraksi 148-190
residu putih kekuningan
pasta
BAB 4
HASIL DAN PEMBAHASAN
4.1. Hasil Penelitian
Dari hasil skrining pendahuluan terhadap ekstrak metanol dari biji buah duku
(Lansium domesticum L.) dengan menggunakan pereaksi Salkowsky dan Lieberman –
Bouchard menunjukkan bahwa di dalam buah tumbuhan Biji buah duku mengandung
senyawa Terpenoida.Dan dari hasil isolasi berupa pasta disimpulkan bahwa senyawa
tersebut bukanlah berupa monoterpen karena monoterpen biasanya berbentuk
cairan.Dan tidak dapat ditentukan jenis terpenoida apa yang diperoleh karena kami
tidak menggunakan 13C-NMR sehingga jumlah atom C-nya tidak dapt dihitung,dan juga tidak menggunkan Mass Spektro sehingga berat molekul tidak dapat ditentukan.
Dari hasil analisa kromatografi lapisan tipis dengan menggunakan adsorben
silika gel 60 GF254, dapat diketahui bahwa pelarut yang baik untuk mengisolasi senyawa terpenoida dari biji buah duku (Lansium domesticum L.) adalah pada
perbandingan pelarut n – heksana : aseton ( 80 : 20 v/v ). Dimana metode penggunaan
pelarut ini yaitu metode polar-nonpolar,dimana dalam hal ini yag paling baik
digunakan adalah n-heksan : aseton.
Dari hasil isolasi buah tumbuhan biji buah duku (Lansium domesticum L.)
diperoleh pasta berwarna kuning putih sebanyak 20 mg .
Hasil analisis Spektrofotometri FT – IR dari pasta hasil isolasi menghasilkan
pita – pita serapan pada daerah bilangan gelombang diperoleh sebagai berikut :
1. Pada bilangan gelombang 3438,44 cm-1 puncak melebar menunjukkan adanya vibrasi ulur (stretching) –OH.
2. Pada bilangan gelombang 2921,49 cm-1 puncak kuat menunjukkan adanya vibrasi ulur (stretching) –CH.
4. Pada bilangan gelombang 1260,46 – 1161,75 dan 1027,74 cm-1 puncak sedang menunjukkan adanya vibrasi uluran –C-O.
5. Pada bilangan gelombang 960,56 cm -1 puncak sedang menunjukkan adanya ikatan rangkap –C=CH.
6. Pada bilangan gelombang 875,48 cm-1 puncak sedang menunjukkan adanya vibrasi furan.
7. Pada bilangan gelombang 772,47 dan 603,4 cm-1 puncak sedang menunjukkan adanya getaran tekuk –OH.
Hasil analisis Spektrometer Resonansi Magnetik Inti Proton (1H-NMR) memberikan pergeseran kimia pada daerah ( ppm ) sebagai berikut :
1. Pergeseran kimia pada daerah δ = 0,827 – 0,986 ppm terdapat puncak
multiplet
2. Pergeseran kimia pada daerah δ = 1,020 – 1,062 ppm terdapat puncak triplet
3. Pergeseran kimia pada daerah δ = 1,259 – 1,330 ppm terdapat puncak doublet
4. Pergeseran kimia pada daerah δ = 1,425 – 1,655 ppm terdapat puncak
multiplet
5. Pergeseran kimia pada daerah δ = 3,690 – 3,842 ppm terdapat puncak doublet
6. Pergeseran kimia pada daerah δ = 4,8 – 5,3 ppm terdapat puncak triplet
7. Pergeseran kimia pada daerah δ = 7,244 -7,481 ppm terdapat puncak multiplet
Spektrum resonansi magnetik inti proton dapat dilihat pada Lampiran 5
4.2. Pembahasan
Biji buah duku (Lansium domesticum L.) dinyatakan mengandung senyawa
Terpenoida berdasarkan hasil skrining fitokimia yang dilakukan. Dimana dengan
menggunakan pereaksi Salkowsky menunjukkan adanya larutan berwarna merah.
Dengan menggunakan pereaksi Lieberman – Bouchard menunjukkan adanya larutan
Dari hasil kromatografi lapisan tipis, diketahui bahwa perbandingan pelarut
yang baik untuk mengisolasi senyawa Terpenoida dari biji buah duku (Lansium
domesticum L.) adalah n – heksana : aseton ( 80 : 20 v/v ). Hal ini disebabkan karena
pada perbandingan pelarut tersebut noda yang timbul lebih banyak dibandingkan
dengan perbandingan pelarut yang lain, dimana pelarut tersebut dapat memisahkan
senyawa – senyawa yang terkandung di dalam sampel secara sempurna.
Dari hasil interpretasi spektrum FT – IR dan spektrum resonansi magnetik inti
proton (1H – NMR) senyawa hasil isolasi dengan menggunakan pelarut CDCl3 dalam standart TMS diperoleh bahwa :
1. Pada bilangan gelombang 3438,44 cm-1 puncak melebar menunjukkan adanya vibrasi ulur (stretching) –OH.
2. Pada bilangan gelombang 2921,49 cm-1 puncak kuat menunjukkan adanya vibrasi ulur (stretching) –CH.
3. Pada bilangan gelombang 1717,75 cm-1 puncak sedang menunjukkan adanya vibrasi ikatan rangkap –C=O.
4. Pada bilangan gelombang 1260,46 – 1161,75 dan 1027,74 cm-1 puncak sedang menunjukkan adanya vibrasi uluran –C-O.
5. Pada bilangan gelombang 960,56 cm-1 puncak sedang menunjukkan adanya ikatan rangkap –C=CH.
6. Pada bilangan gelombang 875,48 cm-1 puncak sedang menunjukkan adanya vibrasi furan.
7. Pada bilangan gelombang 772,47 dan 603,4 cm-1 puncak sedang menunjukkan adanya getaran tekuk –OH.
Hal ini didukung oleh Spektrum Resonansi Magnetik Inti Proton ( 1H – NMR), yang terdapat pada :
1. Pergeseran kimia pada daerah 0,827ppm – 0,986ppm terdapat puncak multiplet dari proton –CH3.
2. Pergeseran kimia pada daerah 1,020ppm – 1,062ppm terdapat puncak triplet
3. Pergeseran kimia pada daerah 1,259ppm – 1,330ppm terdapat puncak doublet
dari proton –CH3.
4. Pergeseran kimia pada daerah 1,425ppm – 1,655ppm terdapat puncak
multiplet dari proton –CH2.
5. Pergeseran kimia pada daerah 3,690ppm – 3,842ppm terdapat puncak doublet
dari proton –O-CH3.
6. Pergeseran kimia pada daerah 4,8ppm – 5,3ppm terdapat puncak triplet dari
proton –OH.
7. Pergeseran kimia pada daerah 7,244ppm – 7,481ppm terdapat puncak
multiplet dari proton furan.
Berdasarkan data – data yang diperoleh dari hasil analisis Spektrofotometer
Resonansi Magnetik Inti Proton ( 1H – NMR ) yang menunjukkan adanya Furan dan Spektrometer Infra-merah ( FT – IR ) yang menunjukkan adanya gugus karbonil
(C = O ) pada pasta hasil isolasi dan berdasarkan hasil skrining fitokimia terhadap
ekstrak metanol biji buah duku (Lansium domestikum L.) adalah senyawa terpenoida.
Dimana kemungkinan struktur terpenoida dari hasil isolasi terhadap biji duku adalah
seperti gambar berikut:
COOH
O
O O
O H
H
Andirobin
O O
O COOMe
O O
O
Odoratin
Dan sebagai senyawa pembanding yang mendukung adanya furan dalam senyawa
hasil isolasi adalah sebagai berikut:
Dari hasil 1H-NMR diperoleh pada pergesaran kimia 7,33 ppm(H-23) terdapat puncak multiplet yang menunjukan adanya –CH2-(metilen) dari cincin siklo, dan pada pergeseran kimia pada daerah 7,25 ppm (H-21) terdapat puncak multiplet yang
menunjukan adanya furan (Cui Baoliang,Chai Heebyung,Constant,L.W,1997). Pada
hasil 1H-NMR dari senyawa hasil isolasi terdapat puncak multiplet pada pergeseran kimia 7,244- 7,481 yang menyatakan adanya furan.Dari hasil perbandingan tersebut
BAB 5
KESIMPULAN DAN SARAN
5.1. Kesimpulan
1. Dari hasil skrining fitokimia terpenoida menunjukkan bahwa biji buah duku
(Lansium domesticum L.) mengandung senyawa terpenoida.
2. Hasil isolasi yang diperoleh dari 1000 g biji buah duku (Lansium domesticum
L.) merupakan pasta berwarna kuning, sebanyak 20 mg.
3. Hasil identifikasi infra merah (FT-IR) dan spektroskopi magnetic inti proton
(1H-NMR) menunjukkan bahwa pasta hasil isolasi dari bii duku (Lansium
domesticum L.) adalah senyawa terpenoida.
5.2. Saran
1. Perlu dilakukan penentuan jumlah atom karbon dengan menggunakan 13 C – NMR, dan menentukan massa dengan MS, untuk menentukan struktur dari
DAFTAR PUSTAKA
Arief. H., 2004. Tumbuhan Obat dan khasiatnya (seri Agri sehat). Seri pertama.
Jakarta : Penerbit Penebar Swadaya.
Cresswell ,C. J.,Runquist dan Campbell. 1982. Analisis Spektrum Senyawa Organik. .
Edisi kedua. Bandung: Penerbit ITB.
Cui Baoliang,Chai.H, dan Constant Howard.L. 1997. Phytochemistry. Volume 47
no.7.
Elsevier Science Ltd. Bangkok
Dalimartha, S. 2008. Atlas Tumbuhan Obat Indonesia. Jilid 5. Jakarta : Pustaka
Bunda.
Edward, J. Dan Stevenson. R. 1991. Dasar Kromatografi Cair. Bandung: Penerbit
ITB.
Gritter, R. B. dan James. 1991. Pengantar Kromatografi. Terjemahan Kosasih
Padmawinata. Bandung : Penerbit ITB.
Harborne, J .B. 1987. Metode Fitokimia penentuan Cara Modern Menganalisa
Tumbuhan. Terbitan kedua. Terjemahan kosasih Padmawinata dan Iwan
soediro.
Bandung: Penerbit ITB.
Herbert,B, dan Richard. 1995. Biosintesa Metabolit Sekunder. Edisi Kedua. Cetakan
pertama. Terjemahan Bambang Srigandono. Semarang : Penerbit IKIP Press
Semarang.
Heftmann, E. 1960. Biochemistry Of Steroids. First Printing. New York : Reinhold
Hosttetmann ,M. 1995. Cara Kromatografi Preparatif. Bandung : Penerbit ITB.
Khopkar, S. M. 1990. Konsep Dasar Kimia Analitik. Cetakan Pertama. Jakarta :
Penerbit UI Press.
Kiang, A. K .,. 1967. Tertrahedron Letter no 37. Pergamon Press Ltd. Singapura.
Makin, H.L. 1975. Biochemistry Of Steroid Hormones .London : Chapman and Hall
Ltd.
Manitto, P. 1992. Biosintesis Produk Alami. Terjemahan Koensomardiyah.Semarang :
Penerbit IKIP Press Semarang.
Mulja.M ,dan Suharman.H. 1995. Analisis Instrumental. Cetakan pertama.
Surabaya : Penerbit IKIP Press Semarang.
Nishizawa ,M. 1983. Natural Product Chemistry. Kodansha Ltd. New York.
Noerdin, D. 1985. Elusidasi Struktur Ultralembayung dan inframerah. Bandung :
Penerbit Angkasa
Pavia, L. D. 1979. Introduction To Spektroscpoy A Gide For Student Of Organic
Chemistry. Philadelphia: Saunders Collage.
Pinder ,A.R. 1960. The Chemistry of Terpenes. London: Chapmann and Hall Ltd.
Robinson, T. 1995. Kandungan Organik Tumbuhan Tinggi. Edisi Keenam. Bandung :
Penerbit ITB.
Sastrohamidjojo, H. 1985. Kromatografi. Cetakan Pertama. Yongyakarta : Penerbit
Sastrohamidjojo, H. 1996. Sintesis Bahan Alam. Cetakan Pertama. Yongyakarta :
Penerbit Liberty.
Setiawan, I. A. 2001. Kiat memilih Tanaman Buah. Jakarta : Penebar Swadaya.
Silverstein, R. M. 1984. Penyidikan Spektometrik senyawa Organik. Jakarta : Penerbit
Erlangga.
Lampiran 3. Kromatogram Lapisan Tipis Ekstrak metanol Biji Duku
I II III
cokelat
cokelat
cokelat
cokelat
cokelat
cokelat
cokelat
cokelat
E E E
Keterangan :
E : Ekstrak Metanol Biji Duku
I : Fase gerak n-heksan : aseton (9:1 v/v)
II : Fase gerak n-heksan : aseton (8: 2 v/v)
III : Fase gerak n-heksan : aseton (7 : 3 v/v)
Lampiran 4. Kromatogram Lapisan Tipis Senyawa Hasil Isolasi Melalui Penampakan Noda Dengan Sinar Ultraviolet
I II
S S
Keterangan :
Fasa diam : Kieselgel 60 F 254 (E. Merck. Art 554)
S : Senyawa hasil isolasi
I : Fiksasi dengan pereaksi Serium Sulfat