11 BAB III DASAR TEORI 3.1 Karbon aktif
Arang adalah padatan berpori hasil pembakaran bahan yang mengandungkarbon. Arang tersusun dari atom-atom karbon yang berikatan secara kovalenmembentuk struktur heksagonal datar dengan sebuah atom pada setiap sudutnya. Susunan kisi-kisi heksagonal datar ini tampak seolah-olah seperti pelat-pelat datar yang saling bertumpuk dengan sela-sela di antaranya (Sudarman, 2001).
Gambar 1. Struktur Grafit Karbon Aktif
Karbon aktif adalah bentuk umum dari berbagai macam produk yang mengandung karbon yang telah diaktifkan untuk meningkatkan luaspermukaannya. Karbon aktif adalah bentuk umum dari berbagai macam produk yang mengandung karbon yang telah diaktifkan untuk meningkatkan luas permukaannya. Karbon aktif berbentuk kristal mikro karbon grafit yang pori-porinya telah mengalami pengembangan
kemampuan untuk mengadsorpsi gas dan uap dari campuran gas dan zat-zat yang tidak larut atau yang terdispersi dalam cairan (Murdiyanto, 2005). Luas permukaan, dimensi, dan distribusi karbon aktif bergantung pada bahan baku, pengarangan, dan proses aktivasi.Berdasarkanukuran porinya, ukuran pori karbon aktif diklasifikasikan menjadi 3, yaitu mikropori(diameter <2 nm), mesopori (diameter 2 –50 nm), dan makropori (diameter >50 nm)(Kustanto, 2000).
Karbon aktif merupakan padatan berpori yang mengandung 85% -95% karbon.Bahan-bahan yang mengandung unsur karbon dapat menghasilkan karbon aktif dengan cara memanaskannya pada suhu tinggi.Pori-pori tersebut dapatdimanfaatkan sebagai agen penyerap (adsorben). Karbon aktif dengan luas permukaan yang besar dapat digunakan untuk berbagai aplikasi yaitu sebagai penghilang warna, penghilang rasa, penghilang bau dan agen pemurni dalam industri makanan. Selain itu juga banyak digunakan dlaam proses pemurnian air baik dalam proses produksi air minum maupun dalam penanganan limbah (Wu,2004).
Luas permukaan karbon aktif berkisar antara 300-3500 m2/g dan ini berhubungan dengan struktur pori internal yang menyebabkan karbon aktif mempunyai sifat sebagai adsorben. Pada karbon aktif berupa bubuk, semakin besar luas area permukaan pori adsorben makadaya adsorpsinya juga semakin besar (Abdi, 2008).
3.2 Fenol
Fenol atau asam karbolat atau benzenol adalah zat kristal tak berwarna yang memiliki bau khas. Rumus kimianya adalahC6H5OH dan strukturnya memiliki gugus hidroksil (-OH) yang berikatan dengan cincin fenil.Fenol memiliki kelarutan terbatas dalam air, yakni 8,3 gram/100 ml. Fenol memiliki sifat yang cenderung asam, artinya dapat melepaskan ion H+ dari gugus hidroksilnya. Pengeluaran ion tersebut menjadikan anion fenoksida C6H5O− yang dapat dilarutkan dalam air (Aditya, 2009).
Fenol merupakan salah satu senyawa organik yang bersifat karsinogenik dan merusak kesehatan manusia berupa kerusakan hari dan ginjal hingga kematian meskipun dalam konsentrasi yang rendah. Salah satu limbah yang mengandung senyawa fenol adalah limbah rumah sakit yang berasal dari hasil cucian sterilisasi alat, bahan kimia laboratorium yang sangat berbahaya jika dibuang begitu saja ke lingkungan. Oleh karena itu, fenol perlu dihilangkan dari air limbah sebelum dibuang (Wardhani, 2008).
3.3 Katalis Heterogen
Katalis heterogen merupakan katalis yang memiliki fasa yang berbeda dengan reaktannya atau dapat didefinisikan bahwa katalis heterogen merupakan katalis yang fasanya tidak sama dengan reaktan dan produk. Katalis heterogen secara umum berbentuk padat dan banyak digunakan reaktan berwujud cair atau gas. Katalis dapat bekerja dengan membentuk senyawa antara atau mengadsorpsi zat yang direaksikan.
Sehingga katalis dapat meningkatkan laju reaksi, sementara katalis itu sendiri tidak mengalami perubahan secara permanen (Fajariyah,2013).
3.4 Fotokatalisis
Teknologi fotokatalis merupakan kombinasi dari proses fotokimia dan katalis yang terintegrasi sehingga reaksi transformasi kimia dapat berlangsung. Reaksi transformasi tersebut berlangsung pada permukaan bahan katalis semikonduktor yang diinduksi oleh sinar (Holikin, 2011).
Fotokatalisis menghasilkan permukaan yang bersifat sebagai pengoksidasi yang kuat sehingga dapat digunakan untuk mengurangi zat-zat berbahaya seperti senyawa organik atau bakteri ketika dikenakan cahaya matahari atau lampu yang berpijar (Hutabarat, 2012).
Mekanisme fotokatalis adalah jika katalis semikonduktor dikenai sinar dengan energi yang lebih besar, maka elektron (e-) pada pita valensi bereksitasi menuju pita konduksi dan akan meninggalkan hole (h+) pada pita valensi. Hole (h+) akan berinteraksi dengan H2O dan OH- yang berada pada permukaan katalis membentuk OH radikal (•OH) yang bersifat sebagai oksidator kuat. Elektron (e-) akan bereaksi dengan O2 yang berada pada katalis membentuk radikal superoksida (•O2) yang bersifat sebagai reduktor (Andari, 2014).
Semikonduktor adalah bahan yang memiliki daerah energi kosong (voidenergy region) yang disebut celah pita (band gap) yang berada diantara konduktor dan isolator.Banyak jenis bahan semikonduktor yang tersedia secara komersial tetapi hanya sedikit yang cocok dipakai sebagai fotokatalis dalam menguraikan berbagai polutan organik. Kriteria yang diperlukan bahan semikonduktor sebagai katalis adalah (Litter, 1999):
1. Bersifat fotoaktif
2. Mampu memanfaatkan cahaya tampak atau ultraviolet dekat 3. Bersifat inert secara biologis dan kimiawi
4. Bersifat fotostabil (stabil terhadap cahaya) 5. Murah dan mudah didapatkan
6. Tidak larut dalam reaksi
Fotodegradasi adalah proses peruraian suatu senyawa (biasanya senyawa organik) dengan bantuan energi foton. Proses fotodegradasi memerlukan suatu
fotokatalisis, yang umumnya merupakan bahan semikonduktor. Prinsip fotodegradasi adalah adanya loncatan elektron dari pita valensi ke pita konduksi pada logam semikonduktor jika dikenai suatu energi foton. Loncatan elektron ini menyebabkan timbulnya hole(lubang elektron) yang dapat berinteraksi dengan pelarut (air) membentuk •OH. Radikal bersifat aktif dan dapat berlanjut untuk menguraikan senyawa organik target (Fatimah et al., 2005).
3.5 SurfaceArea Analyzer (SAA)
Surface Area Analyzer (SAA) merupakan salah satu alat utama dalam karakterisasi material yang memerlukan sampel dalam jumlah yang kecil biasanya berkisar 0,1 sampai 0,01 gram. Alat ini khususnya berfungsi untuk menentukan luas permukaan material, distribusi pori dari material dan isoterm adsorpsi suatu gas pada suatu bahan (Gregg, 1982).
Luas permukaan merupakan luasan yang ditempati satu molekul adsorbat/zat terlarut yang merupakan fungsi langsung dari luas permukaan sampel. Dengan demikian dapat dikatakan bahwa luas permukaan merupakan jumlah pori disetiap satuan luas dari sampel dan luas permukaan spesifiknya merupakan luas permukaan per gram. Luas permukaan dipengaruhi oleh ukuran partikel/pori,bentuk pori dan susunan pori dalam partikel (Martin et al.,1993).
Pengukuran luas permukaan zat padat dengan alat Surface Area Analyzer
dan merupakan jenis adsorpsi sistem gas padat. Adsorpsi gas dengan zat padat berlangsung pada temperatur nitrogen cair (-196°C) (Nurwijayadi,1998).
Proses adsorpsi dipengaruhi oleh lima faktor yaitu:
a. Karakteristik fisik dan kimiawi adsorben (luas permukaan dan ukuran pori)
b. Karakteristik fisik dan kimiawi adsorbat (ukuran molekul dan polaritas molekul)
c. Konsentrasi adsorbat dalam larutan d. Karakteristik larutan (pH dan temperatur) e. Lama adsorpsi (Jankwoska et al., 1991).
Secara garis besar alat Surface Area Analyzer bekerja berdasarkan metode BET yaitu adsorpsi dan desorpsi isotermis gas nitrogen(N2) oleh sampel padatan pada kondisi temperatur nitrogen cair sebagai lapisan tunggal (monolayer) (Rianto, 2007). 3.6 Spektrofotometer UV-Visible
Prinsip metode spektrofotometer UV-Visible adalah sampel menyerap radiasi (pemancar) elektromagnetik yang pada panjang gelombang tertentu dapat terlihat.Spektrofotometri UV-Visible menggunakan dua buah sumber cahaya berbeda, sumber cahaya UV dan sumber cahaya visible. Penggunaan utama spektroskopi
UV-Visibleadalah dalam analisis kuantitatif. Penentuan kadar senyawa organik yang mempunyai struktur kromofor atau senyawa kromofor. Penentuan kadar dilakukan dengan mengukur absorbsi pada panjang gelombang maksimum (puncak kurva), agar dapat memberikan adsorbsi tertinggi untuk setiap konsentrasi (Manurang, 2012).
Keuntungan utama pemilihan metode spektrofotometri ini adalah bahwa metode ini ini memberikan metode yang sangat sederhana untuk menentukan kuantitas zat yang sangat kecil. Spektrofotometri menyiratkan pengukuran jauhnya penyerapan energi cahaya oleh suatu sistem kimiaitu sebagai fungsi dari panjang gelombang radiasi, demikian pula pengukuran penyerapan yang menyendiri pada suatu panjang gelombang tertentu. Analisis spektrofotometri digunakan suatu sumber radiasi yang menjorot ke dalam daerah ultraviolet spektrum tersebut. Dari spektrum ini, dipilih panjang-panjang gelombang tertentu dengan lebar pita kurang dari 1 nm (Sastrohamidjojo, 1999).
Teknik spektroskopi pada daerah ultraviolet dan sinar tampak disebut spektroskopi UV-Visible. Spektrofotometri ini merupakan gabungan antara spektrofotometri UV dan Visible. Spektrofotometer UV-Visible merupakan alat dengan teknik spektrofotometer pada daerah ultra-violet dan sinar tampak. Alat ini digunakan guna mengukur serapan sinar ultraviolet atau sinar tampak oleh suatu materi dalam bentuk larutan. Konsentrasi larutan yang dianalisis sebanding dengan jumlah sinar yang diserap oleh zat yang terdapat dalam larutan tersebut. Metode penyelidikan dengan bantuan spektrometer disebut spektrometri. Dalam spektrometer modern, sinar yang datang pada sampel diubah panjang gelombangnya secara kontinu. Hasil percobaan diungkapkan dalam spektrum dengan absisnya menyatakan panjang gelombang (atau bilangan gelombang atau frekuensi) sinar datang dan ordinatnya menyatakan energi yang diserap sampel (Kunanto, 2013).
3.7 Kromatografi Gas
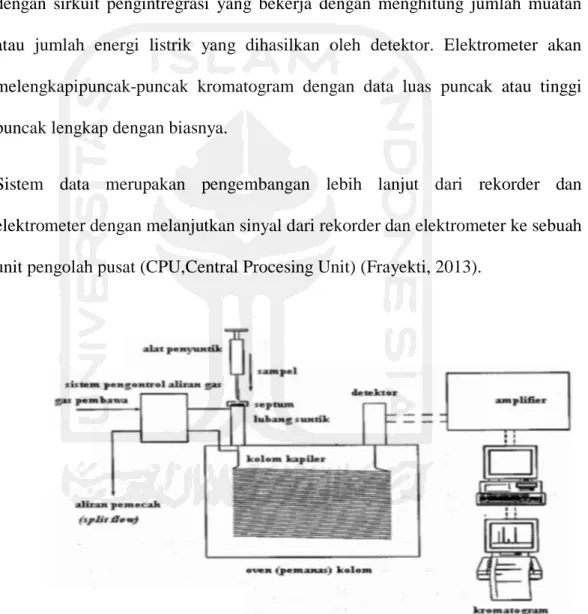
Kromatografi gas merupakan suatu cara kromatografi dimana sampel diuap dan diinjeksikan ke dalam bagian atas dari kolom. Sampel kemudian dibawa melalui kolom oleh gas pembawa yang bersifat inert. Di dalam kolom sendiri telah ada fasa diam. Baik kromatografi gas padat maupun kromatografi gas cair mempunyai komponen-komponen alat yang hampir sama. Prinsip kromatografinya adalah:
Dasar kerja: adsorpsi
Fase gerak : gas (helium, nitrogen dan lain-lain)
Fase diam : padatan (silika, alumina, grafit) dan bahan polimer berpori (Rubiyanto,2013).
Cara pemisahan dari sistem GC, cuplikan yang akan dipisahkan diinjeksikan kedalam injektor, aliran gas pembawa yang inert akan membawa uap cuplikan kedalam kolom. Kolom akan memisahkan komponen-komponen cuplikan tersebut. Komponen-komponen yang telah terpisah tadi dapat dideteksi oleh detektor sehingga memberikan sinyal yang kemudian dicatat pada rekorder dan berupa puncak-puncak (kromatogram).
1. Gas Pembawa
Gas pembawa ditempatkan dalam tabung bertekanan tinggi. Biasanya tekanan dari silinder sebesar 150 atm. Tetapi tekanan ini sangat besar untuk digunakan secara Iangsung. Untuk memperkecil tekanan tersebut agar memenuhi kondisi pemisahan maka digunakan drager yang dapat mengurangi tekanan dan
mengalirkan gas dengan laju tetap. Aliran gas akan mengelusi komponen-komponen dengan waktu yang karaterisitik terhadap komponen-komponen tersebut (waktu retensi). Karena kecepatan gas tetap maka komponen juga mempunyai volume yang karateristik untuk gas pembawa (volume retensi).
Adapun persyaratan-persyaratan yang harus dipenuhi oleh gas pembawa adalah : 1. Inert, agar tidak terjadi interaksi dengan pelarut.
2. Murni, mudah didapat dan murah harganya. 3. Dapat mengurangi difusi dari gas
4. Cocok untuk detektor yang digunakan.
Gas-gas yang sering dipakai adalah : helium, argon, nitrogen, karbon dioksida dan hidrogen.Gas helium dan argon sangat baik, tidak mudah terbakar, tetapi sangat mahal. H2 mudah terbakar, sehingga harus berhati-hati dalam pemakaiannya. Kadang-kadang digunakan juga CO2.
Pemilihan gas pengangkut atau pembawa ditentukan oleh detektor yang digunakan. Tabung gas pembawa dilengkapi dengan pengatur tekanan keluaran dan pengukur tekanan. Sebelum masuk ke kromatografi, harusnya ada pengukur kecepatan aliran gas serta sistem penapis molekuler untuk memisahkan air dan pengotor gas lainnya. Pada dasarnya kecepatan alir gas diatur melalui pengatur tekanan dua tingkat yaitu pengatur kasar (coarse) pada tabung gas dan pengatur halus (fine) pada kromatografi. Tekanan gas masuk ke kromatografi(yaitu tekanan dari tabung gas) diatur pada 10 s.d 50 psi (di atas tekanan ruangan) untuk
memungkinkan aliran gas 25 s.d 150 mL/menit pada kolom terpaket dan 1 s.d 25 mL/menit untuk kolom kapiler. Laju alir gas pembawa mempengaruhi resolusi. Laju alir yang minimum diperlukan untuk resolusi maksimum. Namun, perlu diketahui bahwa pada laju alir yang sangat lambat resolusinya secara dramatis menurun oleh karena faktor-faktor: packing tidak teratur, ukuran partikel, diameter kolom, dan lain-lain.
2. Tempat Injeksi
Dalam pemisahan dengan GLC (Gas Liquid Chromatography) cuplikan harus dalam bentuk fase uap. Gas dan uap dapat dimasukkan secara langsung. Tetapi kebanyakan senyawa organik berbentuk cairan dan padatan. Hingga dengan demikian senyawa yang berbentuk cairan dan padatan pertama-tama harus diuapkan. Ini membutuhkan pemanasan sebelum masuk dalam kolom. Tempat injeksi dari alat GLC selalu dipanaskan. Dalam kebanyakan alat, suhu dari tempat injeksi dapat diatur. Aturan pertama untuk pengaturan suhu ini adalah bahwa suhu tempat injeksi sekitar 50°C lebih tinggi dari titik didih campuran dari cuplikan yang mempunyai titik didih yang paling tinggi. Bila kita tidak mengetahui titik didih komponen dari cuplikan maka kita harus mencoba-coba. Sebagai tindak lanjut suhu dari tempat injeksi dinaikkan. Jika puncak-puncak yang diperoleh lebih baik, ini berarti bahwa suhu percobaan pertama terlalu rendah. Namun demikian suhu tempat injeksi tidak boleh terlalu tinggi, sebab
kemungkinan akan terjadi perubahan karena panas atau penguraian dari senyawa yang akan dianalisa.
3. Kolom
Kolom merupakan jantung dari kromatografi gas. Bentuk dari kolom dapat lurus, bengkok, misal berbentuk V atau W, dan kumparan/spiral. Biasanya bentuk dari kolom adalah kumparan. Kolom ini dapat terbuat dari :
a. Tembaga (murah dan mudah diperoleh)
b. Plastik (teflon), dipakai pada suhu yang tidak terlalu tinggi. c. Baja (stainless steel), (mahal)
d. Alumunium
e. Gelas Panjang kolom dapat dari 1 m sampai 3 m.
Diameter kolom mempunyai berbagai ukuran, biasanya pengukuran berdasarkan diameter dalam dari kolom gelas yaitu antara 0,3 mm hingga 5 mm. Kebanyakan kolom yang digunakan berupa stainless steel dengan diameter luar (OD) dari I/S atau 1/4 inch (0,3 atau 0,6 cm). Pada GSC (Gas Solid Chromatography) kolom diisi dengan penyerap (adsorbent), sedangkan pada GLC kolom diisi dengan "solid support" (padatan pendukung) yang diikat oleh fase diam. Instrumen GC didisain supaya kolom dapat diganti secara mudah dengan melepaskan fitting di dalam oven. Fitting ini tidak hanya memudahkan penggantian fasa diam yang berbeda, tetapi juga mengijinkan operator mengganti kolom yang lebih panjang yang berisi fasa diam yang sama. Ide penggantian kolom yang lebih panjang adalah memberikan kesempatan kontak lebih lama antara campuran komponen
dengan fasa diam yang pada gilirannya memperbaiki pemisahan. Interaksi campuran komponen dengan cairan fasa diam memainkan peran kunci dalam proses pemisahan sehingga sifat-sifat fasa diam menjadi penting. Berbagai jenis kolom biasanya menyebutkan nama komersialnya, komposisi, dan klasifikasi senyawa untuk penggunaannya (kaitannya dengan polaritas).
4. Detektor
Detektor berfungsi sebagai pendeteksi komponen-komponen yang telah dipisahkan dari kolom secara terus-menerus, cepat, akurat, dan dapat melakukan pada suhu yang lebih tinggi. Detektor harus dapat dipercaya dan mudah digunakan. Fungsi umumnya mengubah sifat-sifat molekul dari senyawa organik menjadi arus listrik kemudian arus listrik tersebut diteruskan ke rekorder untuk menghasilkan kromatogram. Detektor yang diinginkan adalah detektor yang mempunyai sensitifitas yang tinggi, noisenya rendah, responnya linear, dapat memberikan respon dengan setiap senyawa, tidak sensitif terhadap perubahan temperatur dan kecepatan aliran dan juga tidak mahal harganya. Detektor dalam GC digunakan untuk memunculkan sinyal listrik hasil elusi gas pembawa dari kolom. Berbagai jenis detektor dibuat untuk melakukan deteksi. Tidak hanya berupa variasi disain, tapi juga variasi sensitivitas dan selektivitas. Sensitivitas mengacu pada kuantitas terkecil komponen campuran di mana sensitivitas menghasilkan sinyal yang masih teramati. Sementara, selektivitas mengacu pada jenis senyawa di mana sinyalnya dapat dimunculkan. Detektor yang umum digunakan:
a. Detektor hantaran panas (Thermal Conductivity Detector/TCD)
Prinsip kerja TCD : Berdasarkan perbedaan daya hantar panas, relatif terhadap gas pembawa. Filament dipanaskan, dimana suhu filament
tergantung pada konduktivitas panas gas di sekelilingnya. Konduktivitas panas efluen kolom lebih rendah (karena adanya sampel). Adanya sampel melewati kolom menyebabkan jembatan Wheatstone tak seimbang sehingga terjadi signal. TCD berdasar atas prinsip, suatu benda yang panas akan kehilangan panasnya pada suatu kecepatan yang tergantung kepada komposisi gas di sekitarnya. Jadi, kecepatan hilangnya panas itu dapat digunakan sebagai ukuran tentang komposisi gas. Gas pembawa yang mengandung sampel atau analit masuk ke dalam kolom, maka konduktivitas gas akan turun dan suhu filament akan meningkat serta resistansi. Lewatnya sampel melalui kolom menyebabkan Jembatan Wheatstone yang tak seimbang sehingga terjadi signal yang terbaca pada detektor.
b. Detektor ionisasi nyala (Flame Ionization Detector/FID)
Prinsip kerja detektor FID : Senyawa yang terbawa fasa gerak diionisasi dengan nyala (H2 + O2/udara). Perubahan arus akibat ionisasi diukur sebagai respon analit. Tidak senstif terhadap karbon yang teroksidasi penuh. FID merupakan detektor yang paling luas penggunaannya, bahkan dianggap sebagai detektor yang universal untuk analisis obat dalam cairan biologis menggunakan GLC. Pada detector ini, komponen-komponen sampel yang
keluar dari kolom dibakar dalam nyala (campuran gas hidrogen dan udara atau oksigen). Sejumlah besar ion yang terbentuk dalam nyala masuk ke dalam celah elektroda dan menurunkan tegangan listrik dari celah elektroda mula-mula. Penurunan tegangan ini yang kemudian dicatat sebagai sinyal oleh rekorder. Intensitas sinyal ini berbanding lurus dengan konsentrasi solute dalam gas pembawa.
c. Detektor penangkap elektron (Electron Capture Detector/ECD)
Prinsip kerja detektor ECD : Mekanisme deteksi melibatkan emisi partikel radioaktif (β) dari 63Ni. Partikel β menghasilkan elektron termal dari gas pembawa. Berdasarkan penangkapan elektron termal oleh molekul sampel. Pada ECD terdapat pemancar radioaktif β, seperti 3
H atau 63Ni yang akan mengionisasi gas pembawa. Aliran elektron sebagai hasil ionisasi gas pembawa (nitrogen atau argon/methan) dalam ECD memberikan sinyal yang berupa baseline suatu kromatogram. Bila kemudian suatu senyawa masuk ke dalam detektor, sebagian dari elektron tersebut akan ditangkap oleh senyawa sebelum mereka mencapai plat detektor. Ini mengakibatkan aliran arus listrik dalam detektor berkurang, yang oleh rekorder akan dicatat sebagai suatu peak.
1. Detektor fotometrik nyala (Flame Photomertic Detector/FPD) 2. Detektor nyala alkali
3. Detektor spektroskopi massa Detektor yang peka terhadap senyawa organik yang mengandung fosfor adalah FID, ECD, dan FPD. Detektor
penangkap elektron (ECD). Pada penetapan ini, digunakan detektor penangkap elektron. Detektor ini merupakan modifikasi dari FID yaitu pada bagian tabung ionisasi. Dasar dari ECD ialah terjadinya absorbsi e- oleh senyawa yang mempunyai afinitas terhadape- bebas (senyawa-senyawa elektronegatif). Dalam detektor gas terionisasi oleh partikel yang dihasilkan dari 3H atau 63Ni. Detektor ini mengukur kehilangan sinyal ketika analit terelusi dari kolom kromatografi. Detektor ini peka terhadap senyawa halogen, karbonil terkonjugasi, nitril, nitro, dan organo logam, namun tidak peka terhadap hidrokarbon, ketone, dan alkohol.
5. Pencatat (Recorder)
Recorder berfungsi sebagai pengubah sinyal dari detektor yang diperkuat melalui elektrometer menjadi bentuk kromatogram. Dari kromatogram yang diperoleh dapat dilakukan analisis kualitatif dan kuantitatif. Analisis kualitatif dengan cara membandingkan waktu retensi sampel dengan standar. Analisis kuantitatif dengan menghitung luas area maupun tinggi dari kromatogram. Sinyal analitik yang dihasilkan detektor dikuatkan oleh rangkaian elektronik agar bisa diolah oleh rekorder atau sistem data. Sebuah rekorder bekerja dengan menggerakkan kertas dengan kecepatan tertentu. di atas kertas tersebut dipasangkan pena yang digerakkan oleh sinyal keluaran detektor sehingga posisinya akan berubah-ubah sesuai dengan dinamika keluaran penguat sinyal detektor. Hasil rekorder adalah
sebuah kromatogram berbentuk puncak-puncak dengan pola yang sesuai dengan kondisi sampel dan jenis detektor yang digunakan.
Recorder biasanya dihubungkan dengan sebuah elektrometer yang dihubungkan dengan sirkuit pengintregrasi yang bekerja dengan menghitung jumlah muatan atau jumlah energi listrik yang dihasilkan oleh detektor. Elektrometer akan melengkapipuncak-puncak kromatogram dengan data luas puncak atau tinggi puncak lengkap dengan biasnya.
Sistem data merupakan pengembangan lebih lanjut dari rekorder dan elektrometer dengan melanjutkan sinyal dari rekorder dan elektrometer ke sebuah unit pengolah pusat (CPU,Central Procesing Unit) (Frayekti, 2013).
3.9 Hipotesis
Dari uraian di atas, maka hipotesis untuk penelitian ini bahwa preparasi ZnO/C, dapat diaplikasikan sebagai fotokatalis yang memberikan pengaruh aktivitas fotokatalitik yang baik terhadap degradasi fenol.