6
BAB II
LANDASAN TEORI
A. Tinjauan Pustaka
1. Degradasi Fotokatalitik
Degradasi fotokatalitik merupakan proses reaksi yang melibatkan cahaya (foton) dan katalis. Dalam media air, senyawa organik dapat dioksidasi menjadi karbondioksida dan air, berarti proses tersebut dapat membersihkan air dari pencemar organik. Senyawa-senyawa anorganik seperti sianida dan nitrit dapat diubah menjadi senyawa lain yang relatif tidak beracun (Hoffmann et al., 1995).
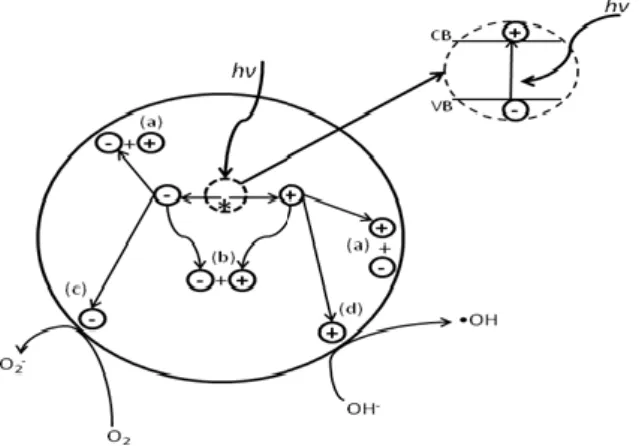
Semikonduktor tipe n apabila dikenai cahaya (hv) dengan energi yang sesuai, maka elektron (e-) pada pita valensi akan berpindah ke pita konduksi dan meninggalkan lubang positif (hole atau disimbolkan h+) pada pita valensi. Elektron dan hole pada permukaan semikonduktor, masing-masing berperan sebagai reduktor dan oksidator. Pasangan elektron-hole dapat berekombinasi, yaitu kembali ke keadaan awal dengan melepas panas atau bermigrasi ke permukaan dan bereaksi dengan senyawa teradsorbsi (Macias, 2003).
Gambar 1. Skema fotokatalitik (Macias, 2003)
Pada skema fotokatalitik (Gambar 1) memperlihatkan reaksi rekombinasi elektron-hole dapat terjadi pada permukaan semikonduktor atau disebut Surface Recombination (reaksi A) dan dapat terjadi pada bulk semikonduktor yang disebut Volume Recombination (reaksi B). Pada permukaan partikel, elektron fotogenerasi dapat mereduksi oksigen menjadi anion super-oksida (reaksi C) dan hole
7
fotogenerasi dapat mengoksidasi OH- atau air untuk membentuk radikal hidroksil (reaksi D) (Macias, 2003).
Ketika terjadi penyerapan foton dengan energi hv yang besarnya sesuai atau melebihi perbedaan energi Eg dari semikonduktor, maka elektron (e-) berpindah dari pita valensi ke pita konduksi, meninggalkan hole yang bermuatan positif di pita valensi. Peristiwa eksitasi elektron ini diikuti beberapa proses selanjutnya, yaitu:
a. Rekombinasi elektron dan hole dalam semikonduktor atau di permukaan, masing-masing disertai dengan pembebasan energi panas
b. Pemerangkapan elektron dan hole dalam keadaan permukaan metastabil c. Reduksi suatu akseptor elektron oleh elektron pada pita konduksi d. Oksidasi suatu donor elektron oleh hole pada pita valensi
Jika energi yang diperoleh cukup besar untuk terjadinya pemerangkapan, maka rekombinasi bisa dicegah dan reaksi redoks dapat terjadi (Linsebigler et al., 1995)
Hole merupakan oksidator yang kuat, sedangkan elektron merupakan reduktor yang baik. Sebagian besar reaksi fotodegradasi senyawa organik menggunakan kekuatan hole untuk mengoksidasi baik secara langsung maupun tidak langsung, sehingga untuk mempertahankan muatan perlu ditambahkan spesies lain yang dapat tereduksi oleh elektron. Oleh karena itu tingkat keefektifan semikonduktor meningkat dengan modifikasi permukaan semikonduktor dengan logam tertentu (Hoffman et al., 1995).
Lama waktu penyinaran saat proses degradasi fotokatalis akan menghasilkan banyak radikal hidroksil. Radikal hidroksil dihasilkan dari hole positif (h+) dari uap air yang teradsorp pada permukaan katalis semikonduktor. Pembentukan h+ dipengaruhi oleh energi (hv) yang dipancarkan oleh sinar. Semakin besar hv yang dipancarkan oleh sinar visible, maka h+ yang terbentuk akan semakin banyak (Linsebigler et al., 1995).
2. Material Semikonduktor
Semikonduktor dapat dikarakterisasi melalui 2 tipe pita energi, yaitu pita valensi dan pita konduksi. Di antara 2 pita tersebut, terdapat band gap.
8
Semikonduktor merupakan bahan yang memiliki energi celah (Eg) antara 0,5 – 5,0 eV. Eksitasi cahaya dari semikonduktor menyebabkan elektron dari pita valensi meloncat ke pita konduksi (Andi, 2007).
Energi band gap terjadi karena adanya overlaping orbital atom yang akan memberikan pelebaran dan penyempitan pita. Hal ini menyebabkan bahan tersebut dapat menyerap energi radiasi sebesar Eg yang dimiliki sehingga dapat meningkatkan kepekaan reaksi oksidasi reduksi yang diinduksi oleh cahaya. Pada saat terjadi eksitasi yang melewati Eg diperlukan waktu tenggang dalam skala nanosekon untuk menghasilkan pasangan elektron-hole sebagai hasil eksitasi elektron dari pita valensi ke pita konduksi (Noqueira et al, 1993).
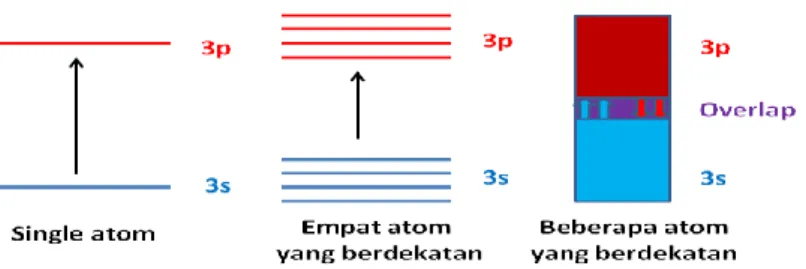
Material logam memiliki Energy Gap yang saling tumpang tindih (overlap), sehingga atom-atom dapat dengan sangat mudah bergerak ke daerah pita konduksi. Sehingga, material ini memiliki sifat yang sangat konduktif dan dikenal dengan bahan konduktor. Gambar 2 di bawah ini mengilustrasikan pita energi dan energy gap pada material konduktor.
Gambar 2. Pita energi dan energy gap pada material logam (Andi, 2007)
Pada sisi yang lain, terdapat material yang memiliki Energy Gap yang berdekatan. Oleh karena itu, pada kondisi normal atom-atom sulit untuk bergerak ke daerah pita konduksi dan bersifat isolator. Namun, dengan sedikit tambahan energi, atom-atom tersebut dapat bergerak ke daerah pita konduksi sehingga menjadi bersifat konduktor. Karena sifatnya yang demikian, material ini dikenal dengan nama bahan semikonduktor. Ilustrasi pita energi dan energy gap pada material semikonduktor ditampilkan pada Gambar 3 di bawah ini.
9
Gambar 3. Pita energi dan energy gap pada material semikonduktor
3. Doping Logam Transisi pada Semikonduktor TiO2
TiO2 merupakan bahan semikonduktor yang memiliki fotoaktivitas dan
stabilitas kimia tinggi serta tahan terhadap fotokorosi dalam semua kondisi larutan, kecuali pada larutan yang sangat asam atau mengandung fluoride. TiO2
juga bersifat nontoksik, memiliki sifat redoks, yaitu mampu mengoksidasi polutan organik dan mereduksi sejumlah ion logam dalam larutan (Brown, 1992).
Titanium dioksida (TiO2) merupakan semikonduktor yang terdiri dari
padatan ionik yang tersusun dari ion Ti4+ dan O2- dalam konfigurasi oktahedron. Ada tiga struktur kristal dari Titanium dioksida ini, yaitu:
a. Rutile
Titanium(IV) oksida rutile mempunyai struktur tetragonal dan mengandung 6 atom per unit sel. Bentuk oktahedron TiO2 sedikit menyimpang (Chen et al.,
2007; Thompson et al., 2006; Diebold, 2003). Rutile memiliki tiga bentuk, yaitu TiO2 II (mempunyai struktur seperti α-PbO2), TiO2 (H) yang memiliki struktur
hollandite, dan TiO2 (B) yang memiliki struktur monoklinik. Bentuk rutile stabil
pada berbagai temperatur dan tekanan lebih dari 60 kbar, dimana TiO2 (II)
menjadi fase termodinamis yang menguntungkan. Zhang et al (2000) menemukan struktur anatase dan brokit menjadi bentuk bentuk rutile setelah mencapai ukuran partikel khusus, dengan bentuk rutile menjadi lebih stabil daripada anatase untuk ukuran partikel lebih besar dari 14 nm. Ketika bentuk rutile telah terbentuk, terbentuknya lebih cepat daripada anatase. Aktivitas dari bentuk rutile pada fotokatalis buruk. Sclafani et al (1990) menyimpulkan bentuk rutile dapat aktif atau tidak aktif, tergantung pada kondisi preparasinya.
Pita Konduksi
Pita Valensi
Beberapa atom yang berdekatan
10 b. Anatase
Struktur anatase dapat diamati pada pemanasan sol TiO2 dari 120 oC dan
mencapai sempurna pada 500 oC. Anatase titanium(IV) oksida berbentuk struktur tetragonal tetapi mengalami distorsi dari bentuk octahedron TiO2 menjadi sedikit
lebih besar dari bentuk anatase (Linsebigler et al., 1995). Bentuk anatase lebih stabil daripada rutile pada suhu 0 K, tetapi perbedaan energi antara dua bentuk tersebut kecil (~ 2 sampai 10 kJ/mol). Anatase lebih disukai daripada bentuk polimorf lainnya untuk aplikasi sel tenaga surya karena mobilitas tinggi dari elektronnya, tetapan dielektriknya rendah dan berat jenisnya lebih rendah (Carp et al, 2004).
c. Brookite
Brookite memiliki struktur kristal ortorombik. Panjang ikatan antara titanium dan oksigen semuanya berbeda. Band gap dari brokite sekitar 3,14 eV berdasarkan persamaan Huckel. Band gap dari brokite berada diantara anatase (3,23 eV) dan rutile (3,02 eV). Kesukaran dalam proses sintesis brokite yang mempunyai kemurnian tinggi dan luas permukaan yang besar menjadi satu alasan brokite kurang dipelajari untuk sifat fotokatalisnya (Di Paola et al, 2013).
Gambar 4 menunjukkan tiga struktur yang berbeda dari semikonduktor TiO2. Struktur titanium(IV) oksida yang cukup stabil ada dua, yaitu anatase dan
rutile. Struktur dari anatase dan rutile dapat digambarkan sebagai rantai oktahedron titanium(IV) oksida. Oktahedral pada struktur rutile dikelilingi oleh 10 oktahedron tetangga, sedangkan pada struktur anatase setiap oktahedronnya dikelilingi 8 oktahedron lainnya (Cherepy et al, 1997).
Gambar 4. Struktur TiO2 : (a) rutil, (b) anatase , (c) brookit (Hazama et al.,
11
Perbedaan struktur anatase dan rutile menyebabkan perbedaan massa jenis dan struktur pita elektroniknya antara dua bentuk titanium(IV) oksida, yaitu anatase mempunyai daerah aktivasi yang lebih luas dari pada rutil. Hal ini menyebabkan titanium(IV) oksida jenis anatase lebih reaktif dibandingkan dengan jenis rutile (Ramdhani, 2012).
Penambahan logam transisi telah dipelajari untuk aktivitas fotokatalitik dari titanium(IV) oksida. Ion-ion logam tersebut diyakini menempel pada kisi-kisi kristal titanium(IV) oksida. Tingkat energi pada band gap titanium(IV) oksida terbentuk berdasarkan persamaan (Ni et al., 2007) :
Mn+ + hv M(n+1)+ + e-ch
Mn+ + hv M(n-1)+ + h+vb
untuk M dan Mn+ adalah dopan logam dan ion logam.
Elektron (hole) ditransfer dari titanium(IV) oksida ke ion-ion logam. Perpindahan elektron tersebut dapat meminimalkan rekombinan elektron-hole.
Elektron trap : Mn+ + e-cb M(n-1)+
Hole trap : Mn+ + h+vb M(n+1)+
Potensial reduksi dari Mn+/M(n-1)+ harus lebih tinggi daripada pita konduksi dari titanium(IV) oksida, tingkat energi dari Mn+/M(n+1)+ harus lebih rendah dari pita valensi titanium(IV) oksida. Pada reaksi fotokatalitik, proses transfer menjadi sangat penting untuk penjebakan elektron. Jika elektron ditransfer ke permukaan reaksi fotokatalitik dapat terjadi. Oleh karena itu, ion-ion logam di tambah di permukaan dari titanium(IV) oksida untuk proses transfer elektron. Penambahan logam kepermukaan titanium(IV) oksida menjadi objek penelitian yang penting untuk meneliti aktivitas fotokatalitik dari titanium(IV) oksida (Ni et al, 2007).
Penambahan logam pada material TiO2 mampu meningkatkan respon
spektra sampai dengan daerah visible mengakibatkan efek perubahan band gap. Pada proses fotoeksitasi, elektron dapat ditransfer dari pita konduksi dari titanium(IV) oksida ke partikel logam pada permukaan titanium(IV) oksida. Ion dopan dapat menciptakan trap elektron yang mana akan meminimalkan proses rekombinan elektron dan hole (El Bahy et al., 2008).
12
Gambar 5. Mekanisme fotokatalis TiO2 (hv1 = TiO2 murni, hv2 = TiO2 dengan
doping ion logam, hv3 = TiO2 dengan doping non logam) (Zaleska, 2008)
Pada Gambar 5 memperlihatkan setelah foton dengan energi yang sesuai atau melebihi celah energi TiO2 menghasilkan pasangan elektron-hole di
permukaan semikonduktor, elektron kemudian dieksitasi ke pita konduksi, sedangkan hole terbentuk di pita valensi. Elektron yang tereksitasi ini dapat bergabung kembali dengan hole dengan melepaskan panas, terperangkap dalam kondisi stabil di permukaan atau bereaksi dengan donor elektron dan akseptor elektron teradsorpsi di permukaan semikonduktor atau di sekitar lapisan ganda listrik partikel yang bermuatan (Zaleska, 2008).
Aktivitas fotokatalis TiO2 yang didoping dengan logam tertentu dapat
dijelaskan dengan adanya tingkat energi baru TiO2 akibat dispersi logam yang
dimasukkan dalam matriks TiO2. Elektron tereksitasi dari pita valensi ke tingkat
energi tertentu di bawah pita konduksi TiO2 akibat mengabsorpsi cahaya dengan
energi hv2. Keuntungan adanya penambahan logam transisi ke dalam matriks
TiO2 adalah pemerangkapan elektron diperbaiki sehingga rekombinasi
elektron-hole dapat diperkecil selama iradiasi. Selain menghasilkan band gap yang baru, doping logam juga dapat mempercepat aktivitas fotokatalis (Zaleska, 2008).
Mekanisme migrasi elektron pada permukaan semikonduktor doping logam melalui tahap eksitasi elektron dari pita valensi ke pita konduksi, kemudian elektron bermigrasi menuju logam dan terperangkap dalam logam sehingga rekombinasi electron-hole dapat ditekan. Hole dapat berdifusi ke permukaan semikonduktor di mana pada permukaan tersebut terjadi oksidasi senyawa-senyawa yang didegradasi (Linsebigler et al., 1995).
13
Modifikasi elektronik permukaan semikonduktor melalui deposisi logam dapat dilakukan dengan menggunakan beberapa logam mulia (logam yang tidak mudah teroksidasi). Pemilihan logam yang digunakan sebagai penjebak elektron didasarkan pada sifatnya yang tidak mudah teroksidasi atau yang memiliki potensial reduksi tinggi, sehingga logam-logam tersebut bertindak sebagai akseptor elektron (Rahmawati et al., 2003).
Energi cahaya daerah visible yang mengenai ion logam akan menyebabkan elektron pada ion logam tereksitasi menuju pita konduksi TiO2 (charge-transfer).
Spektra serapan modifikasi TiO2 dalam daerah visible dikarenakan adanya
kecacatan kristal yang disebabkan adanya kekosongan oksigen yang menimbulkan pusat-pusat berwarna (Choi et al., 2009).
Logam yang digunakan dalam penelitian ini yaitu Cadmium (Cd), Cobalt (Co) dan Mangan (Mn) dengan karakteristik masing-masing pada Tabel 1.
Tabel 1. Logam cadmium (Cd), cobalt (Co) dan mangan (Mn).
Mn (Mangan) Co (Cobalt) Cd (Cadmium)
Nomor atom 25 27 48
Golongan 7 9 12
Periode 4 4 5
Massa atom (g/mol) 54,938 58,93 112,41
Bilangan oksidasi 7, 6, 5, 4, 3, 2, 1,
-1, -2, -3 5, 4, 3, 2, 1, -1 2, 1
Elektronegativitas 1,55 1,88 1,69
Energi ionisasi I (kJ/mol) 717,3 760,4 867,8
Energi ionisasi II (kJ/mol) 1509,0 1648 1631,4
Energi ionisasi III (kJ/mol) 3248 3232 3616
Jari-jari atom (pm) 127 125 151
Jari-jari ion (A) 0,46 0,74 0,97
Potensial reduksi (V) 1,5415 -0,28 -0,403
Jari-jari kovalen (pm) 161±8 150±7 144±9
Penambahan logam ke dalam semikonduktor TiO2 dengan konsentrasi
semakin besar menyebabkan energi band gap semakin rendah menuju daerah serapan cahaya visible (Ganesh et al., 2012; Tian et al., 2012).
14
Tabel 2. Penurunan band gap semikonduktor TiO2 doping logam
Co (%) dalam TiO2 Ebg (eV) Co (%) dalam TiO2 Ebg (eV)
0,1 3,24 0,01 3,24
0,5 3,17 0,03 3,26
1 3,12 0,05 3,23
5 2,45 0,07 3,18
10 2,45 0,10 3,10
(Ganesh et al., 2011) (Tian et al., 2011)
Perbedaan logam yang ditambahkan dalam semikonduktor TiO2 akan
memperkecil ukuran partikel semikonduktor terdoping dibandingkan semikonduktor TiO2 murni (Siwinska et al., 2013).
Doping logam Mn terhadap semikonduktor TiO2 yang diaplikasikan
terhadap metilen biru menunjukkan hasil optimal pada doping Mn 0,2%. Semakin besar konsentrasi Mn yang ditambahkan, ukuran kristal semakin menurun. Doping Mn dapat menurunkan band gap sehingga mampu menyerap cahaya tampak, namun semakin besar konsentrasi Mn yang ditambahkan akan memperbanyak cacat kristal yang terbentuk sehingga pusat rekombinasi akan mengurangi aktivitas fotokatalisnya (Deng et al., 2011). Papadimitriou et al. (2011) melakukan sintesis doping Mn (0,1%, 1%, dan 5%) terhadap semikonduktor TiO2 yang selanjutnya dilanjutkan oleh Binas et al. (2011)
diaplikasikan pada degradasi metilen biru menggunakan cahaya tampak. Hasil optimal diperoleh menggunakan doping Mn 0,1% pada menit ke 30 sebesar 70% metilen biru terdegradasi. Wang et al. (2015) menunjukkan hasil optimal pada doping Mn 6% terhadap TiO2 dan bila konsentrasi logam yang didopingkan
semakin tinggi maka dapat menumbuhkan fasa rutil sehingga dapat mengurangi sensitivitas fotokatalis dari TiO2.
4. Sifat Kimia Senyawa Berwarna
Senyawa berwarna banyak digunakan dalam berbagai industri termasuk industri tekstil. Molekul senyawa berwarna merupakan gabungan dari zat organik tidak jenuh dengan kromofor sebagai pembawa warna dan auksokrom sebagai pengikat warna dengan serat. Gugus kromofor merupakan gugus yang
15
menyebabkan molekul menjadi berwarna. Pada umumnya, senyawa berwarna mempunyai struktur kimia aromatik yang sederhana hingga kompleks, dilengkapi gugus-gugus yang dapat memberikan sifat-sifat tertentu pada senyawa berwarna tersebut, seperti kemampuan bereaksi dengan serat (daya ikat), daya larut, intensitas warna dan tahan luntur (Can et al, 2003).
Senyawa berwarna dapat digolongkan menurut cara diperolehnya, yaitu senyawa berwarna alam dan sintetik. Berdasarkan pencelupannya, senyawa berwarna dapat digolongkan sebagai senyawa berwarna substantif, yaitu senyawa berwarna yang memerlukan zat pembantu pokok untuk dapat mewarnai serat. Penggolongan lainnya adalah berdasarkan struktur kimianya, yaitu senyawa berwarna nitroso, introazo, poliazo, indigoida, antrakinon, ptalosianina dan lain-lain.
Senyawa berwarna berdasarkan aplikasinya pada bahan yaitu, senyawa berwarna basa atau kationik, asam atau anionik, direk, mordan, belerang, bejana, dispersi dan reaktif (Isminingsih et al,1982).
a. Senyawa berwarna asam
Senyawa berwarna asam merupakan garam-garam natrium dari asam sulfonat dan nitrofenol. Biasanya digunakan dalam media asam. Senyawa berwarna asam merupakan senyawa berwarna yang relatif murah dan mudah didapatkan. Contoh : Methyl Orange dan Panceau B.
b. Senyawa berwarna basa
Senyawa berwarna basa merupakan turunan dari azin, azo, tioazin, tiazol maupun akridin dan umumnya berupa garam dari HCl dan ZnCl2 untuk
membentuk warnanya. Senyawa berwarna ini banyak digunakan untuk pencelupan dari pencetakan. Contoh : Crystal Violet dan Rosalin.
c. Senyawa berwarna direct
Kebanyakan dari senyawa berwarna ini adalah tiazol atau turunan dari senyawa azo dari benzidin, toluidin, diamino dan gugus yang sejenis. Senyawa berwarna direk digunakan untuk serat-serat tumbuhan pada media netral atau alkalis dan membentuk lapisan warna. Contoh : Direct Green B.
16 d. Senyawa berwarna mordan
Senyawa berwarna yang dibuat tak larut dalam suatu tekstil dengan mengkomplekskan dengan suatu ion logam yang disebut mordan. Salah satu contoh senyawa berwarna ini adalah Alizarin yang membentuk warna berbeda tergantung dari logam yang digunakan. Alizarin membentuk warna merah dengan logam Al3+ dan warna biru dengan logam Ba2+.
e. Senyawa berwarna belerang
Biasanya diproduksi dengan mereaksikan senyawa amino aromatik dengan sulfur. Senyawa berwarna ini menghasilkan warna-warna gelap seperti biru, coklat, hijau dan hitam. Penggunaan secara luas adalah untuk pencelupan serat kapas atau pembungkus kapas, wol, lynen atau rayon.
f. Senyawa berwarna bejana
Senyawa berwarna yang diaplikasikan pada tekstil dalam bentuk terlarut dan kemudian dibiarkan bereaksi menjadi suatu bentuk tak terlarut. Contoh yang umum pada jenis senyawa berwarna ini adalah senyawa berwarna Indigo yang mengandung gugus indoksil yang apabila bereaksi dengan udara akan teroksidasi menghasilkan indigo yang tidak larut dan berwarna biru.
g. Senyawa berwarna dispersi
Senyawa berwarna dispersi merupakan senyawa berwarna organik yang digunakan secara koloid dari dispersi senyawa berwarna tersebut dalam air pada serat tekstil. Untuk menghasilkan warna yang baik biasanya digunakan sebagai senyawa berwarna rayon asetat. Golongan ini merupakan turunan dari azo, azometin, dan antrakinon. Contoh : Zapon Fast Yellow G dan Disperse Red 9. h. Senyawa berwarna reaktif
Senyawa berwarna reaktif adalah suatu senyawa berwarna yang dapat mengadakan reaksi dengan serat, sehingga senyawa berwarna tersebut merupakan bagian dari serat. Oleh karena itu hasil celupan senyawa berwarna reaktif mempunyai ketahanan cuci yang sangat baik. Berat molekul senyawa berwarna reaktif relatif kecil, maka kilapnya akan lebih baik daripada senyawa berwarna direk (Rasjid, 1976).
17
Methylene blue (metilen biru) merupakan senyawa hidrokarbon aromatik yang memiliki rumus kimia C16H18ClN3S yang beracun dan merupakan dye
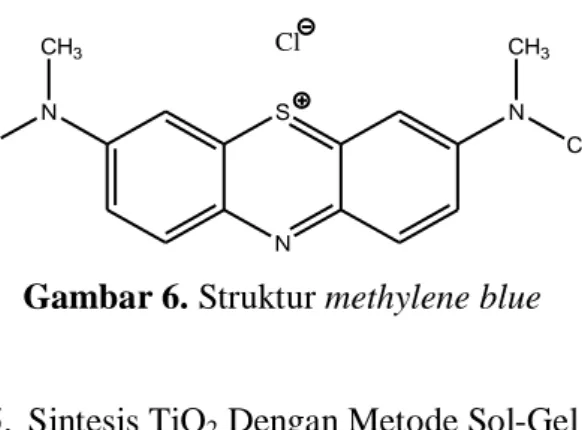
kationik dengan daya adsorpsi yang sangat kuat. Senyawa berwarna ini termasuk salah satu senyawa berwarna thiazine yang sering digunakan karena harganya yang ekonomis dan mudah diperoleh. Pada umumnya digunakan sebagai pewarnaan kulit, kain mori dan kain katun. Penggunaan metilen biru dapat menimbulkan beberapa efek, seperti iritasi saluran pencernaan jika tertelan, menimbulkan sianosis jika terhirup dan iritasi pada kulit jika tersentuh oleh kulit (Hamdaoui et al., 2006). Senyawa ini berupa kristal berwarna hijau gelap. Pada suhu ruang senyawa ini berbentuk padatan dan tidak berbau. Ketika dilarutkan dalam air atau alkohol akan menghasilkan larutan berwarna biru. Bentuk hidratnya mengandung 3 molekul air per molekul metilen biru. Memiliki berat molekul 319,86 g/mol, dengan titik lebur pada 105 oC dan daya larut sebesar 4,36 x 104 mg/L (Palupi, 2006). Metilen biru merupakan salah satu senyawa berwarna yang dapat didegradasi dengan proses fotokatalis.
Gambar 6. Struktur methylene blue
5. Sintesis TiO2 Dengan Metode Sol-Gel
Metode sol-gel merupakan salah satu metode yang dapat digunakan untuk mensintesis TiO2. Keuntungan dari penggunaan metode sol-gel yaitu mudah,
pencampuran dapat terjadi sempurna, fase yang dihasilkan homogen, diperolehnya kristal bubuk nanosized dengan kemurnian tinggi pada temperatur rendah dan lebih praktis, tidak memerlukan suhu tinggi (Liqun et al., 2005).
Pada proses sol-gel, prekursor molekuler diubah menjadi partikel berukuran nano untuk membentuk suspensi koloid atau sol, selanjutnya nano partikel koloid tersebut berikatan satu sama lain melalui polimerisasi membentuk gel.
N S N N CH3 H3C CH3 CH3 Cl
18
Polimerisasi membuat proses difusi kimia terus meningkat, kemudian gel tersebut dikeringkan dan dikalsinasi untuk menghasilkan bubuk. Reaksi sol-gel adalah:
Sol merupakan suspensi koloid yang fasa terdispersinya berbentuk padat dan fasa pendispersinya berbentuk cairan. Reaksi hidrolisis merupakan reaksi suspensi dari partikel padat atau molekul-molekul koloid dalam larutan yang menghasilkan partikel padatan metal hidroksida dalam larutan.
Hidrolisis:
(OR)3M – OR + H2O → (OR)3M – OM + ROH (1)
Pada reaksi ini terjadi pertukaran ion dari grup OH yang bermuatan parsial negatif ke logam (M) yang bermuatan parsial positif. Kemudian terjadi parsial positif. Kemudian terjadi tranfer proton terhadap grup alkoksi bersamaan dengan eliminasi ROH.
Gel (gelation) merupakan jaringan partikel atau molekul, baik padatan dan cairan, dimana polimer yang terjadi di dalam larutan digunakan sebagai tempat pertumbuhan zat anorganik. Pertumbuhan anorganik terjadi pada gel point yang memiliki energi ikat lebih rendah. Reaksi kondensasi adalah reaksi alkohol atau air yang menghasilkan oxygen bridge (jembatan oksigen) untuk mendapatkan metal oksida.
Kondensasi:
-M – OH + OX – M → -M – O – M - + XOH (2)
Kondensasi molekul hidroksida dengan proses eliminasi air membentuk terjadinya struktur gel dari logam hidroksida dengan reaksi dehidrasi.
Dehidrasi:
(OR)3M – OH + (OR)3M – OH → (OR)3M – O – M(OR)3 + H2O (3)
Dealkoholisasi:
(OR)3M – OH + (OR)3M – OR → (OR)3M – O – M(OR)3 + ROH (4)
M adalah Ti dan R adalah gugus alkil (Heung, 2000).
Kualitas bubuk menggunakan sol-gel sangat berkaitan dengan kecepatan proses hidrolisis dan kondensasi. Proses hidrolisis yang lebih lambat dan terkontrol akan menghasilkan ukuran partikel yang lebih kecil dan karakteristik yang unik. Parameter-parameter yang perlu dikontrol yaitu konsentrasi air/
19
alkohol/ prekursor, pH larutan, temperatur proses, pemilihan prekursor (struktur molekul, karakteristik ikatan).
Sintesis TiO2 doping Mn menggunakan metode sol-gel diperoleh struktur
fase anatase dan dengan bertambahnya konsentrasi Mn yang ditambahkan peak (puncak) melebar pada 2θ = 25,4o
. Ukuran kristal semakin menurun dengan bertambahnya konsentrasi Mn yang didopingkan dengan rata-rata ukuran kristal 7 nm (Deng et al., 2011).
6. Kinetika Laju Reaksi
Konstanta laju reaksi (k) untuk mengetahui aktivitas kinetika fotokatalis yang terjadi mengikuti reaksi orde satu, orde dua atau orde tiga. Menurut Triyono et al. (2000), reaksi orde satu adalah reaksi yang lajunya berbanding langsung dengan konsentrasi reaktan dan harga k dapat dihitung dengan persamaan (5) dan (6).
(5)
(6)
Dari persamaan diatas, nilai k dapat ditentukan dari grafik hubungan ln C terhadap waktu penyinaran (t). Selanjutnya dibuat garis lurus (y=a+bx) sehingga akan diperoleh nilai slope (b) yang merupakan konstanta laju reaksi (k).
Pada reaksi orde dua, laju reaksi berbanding langsung dengan kuadrat konsentrasi dari satu reaktan atau dengan hasil kali konsentrasi yang meningkat sampai pangkat satu atau dua dari reaktan-reaktan tersebut dan harga k dapat dihitung dengan persamaan (7) dan (8).
(7)
(8)
Dari persamaan diatas, nilai k dapat ditentukan dari grafik hubungan 1/C terhadap waktu penyinaran (t). Selanjutnya dibuat garis lurus (y=a+bx) sehingga akan diperoleh nilai slope (b) yang merupakan konstanta laju reaksi (k).
20
Pada reaksi orde tiga, laju reaksi berbanding lurus dengan pangkat tiga konsentrasi dari suatu reaktan dan harga k dapat dihitung dengan persamaan (9) dan (10).
(9)
(10)
Dari persamaan diatas, nilai k dapat ditentukan dari grafik hubungan 1/C2 terhadap waktu penyinaran (t). Selanjutnya dibuat garis lurus (y=a+bx) sehingga akan diperoleh nilai slope (b) = 2k sehingga k = ½ dari slope.
7. Metode Karakterisasi
a. Spektrofotometer Ultraviolet-Visible (UV-Vis)
Pada spektrofotometer UV-Vis, sinar kontinyu dihasilkan oleh lampu awan muatan hidrogen atau deuterium (D2), sedangkan sinar visible dihasilkan oleh
lampu Wolfram. Panjang gelombang cahaya UV-Vis jauh lebih pendek daripada panjang gelombang radiasi IR. Panjang gelombang UV-Vis berada pada kisaran 180-800 nm. Prinsip dasar spektroskopi UV-Vis adalah terjadinya transisi elektronik yang disebabkan penyerapan sinar UV-Vis yang mampu mengeksitasi elektron dari orbital yang kosong. Umumnya, transisi yang paling mungkin adalah transisi pada tingkat tertinggi (HOMO) ke orbital molekul yang kosong pada tingkat terendah (LUMO).
Intensitas penyerapan dijelaskan dengan hukum Lambert-Beer, dimana fraksi cahaya yang diabsorbsi tidak tergantung pada kekuatan sumber cahaya mula-mula, dan fraksi yang diabsorbsi tergantung pada banyaknya mol (ketebalan/ konsentrasi) yang dapat mengabsorbsi. Oleh karena itu, absorbsi cahaya merupakan fungsi dari molekul yang mengabsorbsi, maka cara yang tepat untuk menyatakan absorbansi adalah:
A = ε.b.c (11)
Dimana,
ε adalah absorptivitas molar (mol-1
. cm-1 L) b adalah tebal lintasan (cm)
21 c adalah konsentrasi larutan (mol L-1)
Dengan menggunkaan metode kurva kalibrasi, yaitu dengan membuat grafik absorbansi versus konsentrasi dapat diperoleh suatu kurva linier. Melalui pengukuran absorbansi suatu sampel dan menginterpolasikannya ke kurva kalibrasi, maka konsentrasi sampel dapat ditentukan (Underwood, 1980).
Penentuan band gap energi menggunakan metode perhitugan Tauc Plot dengan mengikuti persamaan sebagai berikut:
(hvα)1/n = A(hv – Eg) (12) Dimana, h : konstanta Planck v : frekuensi vibrasi α : koefisien absorpsi Eg : band gap A : konstanta proporsional
n = ½ (mengikuti transisi yang diperbolehkan). Nilai hv ditentukan menggunakan persamaan:
(13)
Dengan
h = 6,63x10-34 J.s c = 3x108 m/s.
Penentuan band gap dilakukan dengan melakukan ekstrapolasi dari grafik hubungan E (hv) sebagai absis dan (hvα)1/n sebagai ordinat hingga memotong sumbu energi sehingga diperoleh nilai band gap (Bilalodin, 2004; Tauc et al., 1966).
b. X-Ray Diffraction (XRD)
XRD digunakan untuk menganalisis komposisi senyawa pada material dan juga karakterisasi kristal. Prinsip dasar XRD adalah mendifraksi cahaya yang melalui celah kristal. Difraksi cahaya oleh kisi-kisi atau kristal ini dapat terjadi apabila difraksi tersebut berasal dari radius yang memiliki panjang gelombang
22
yang setara dengan jarak antar atom, yaitu sekitar 1 Angstrom. Radiasi yang digunakan berupa radiasi sinar-X, elektron dan neutron.
Sinar-X merupakan foton dengan energi yang memiliki panjang gelombang berkisar antara 0,5 sampai 2,5 Angstrom. Ketika berkas sinar-X berinteraksi dengan suatu material, maka sebagian berkas akan diabsorbsi, ditransmisikan, dan sebagian dihamburkan terdifraksi. Hamburan terdifraksi inilah yang dideteksi oleh XRD.
Berkas sinar-X yang dihamburkan tersebut ada yang saling menghilangkan karena fasanya berbeda dan ada juga yang saling menguatkan karena fasanya sama. Berkas sinar-X yang saling menguatkan itulah yang disebut sebagai berkas difraksi. Hukum Bragg merumuskan tentang persyaratan yang harus dipenuhi agar berkas sinar-X yang dihamburkan tersebut merupakan berkas difraksi. Ilustrasi difraksi sinar-X pada XRD dapat dilihat pada Gambar 7.
Gambar 7. Ilustrasi hukum Bragg (Settle, 1997)
Menurut Hukum Bragg, kristal terdiri atas bidang-bidang datar (kisi kristal) yang masing-masing berfungsi sebagai cermin semi transparan. Jika sinar-X ditembakkan pada tumpukan bidang datar tersebut, maka beberapa akan dipantulkan oleh bidang tersebut dengan sudut pantul yang sama dengan sudut datangnya, seperti pada ilustrasi diatas. Sedangkan sisanya akan diteruskan menembus bidang. Perumusan secara matematik dapat dikemukakan dengan menghubungkan panjang gelombang sinar-X, jarak antar bidang dalam kristal dan sudut difraksi (Park et al., 2004):
(14)
Dimana,
Lamda (λ) : panjang gelombang sinar-X d : jarak antar kisi kristal
θ θ
θ d
23 θ : sudut datang sinar
n = 1, 2, 3, dan seterusnya adalah orde difraksi.
Persamaan Bragg tersebut digunakan untuk menentukan parameter sel kristal. Sedangkan untuk menentukan struktur kristal, dengan menggunakan metoda komputasi kristalografik, data intensitas digunakan untuk menentukan posisi-posisi atomnya (Settle, 1997).
Dalam penelitian yang telah dilakukan Mugundan et al. (2015) pada kristal Co-TiO2 dengan variasi 4%, 8%, 12%, 16%. Penambahan Co dengan konsentrasi
rendah tidak menunjukkan fase kobalt, hal ini mengindikasikan ion kobalt tertutup oleh TiO2. Sedangkan pada penambahan Co dengan konsentrasi tinggi (12% dan
16%) diperoleh puncak baru. Kemudian dilakukan pengukuran kristal menggunakan persamaan Debye-Scherrer:
(15)
Dimana,
D : ukuran kristal K : faktor pengukuran λ = 0,154 nm
β : setengah lebar maksimum (FWHM) θ : derajat reflektansi
Diperoleh hasil pada Tabel 3, menunjukkan semakin besar konsentrasi kobalt yang ditambahkan maka ukuran kristal semakin meningkat. Hal ini terjadi karena ukuran ion Co2+ (0,74A) lebih besar daripada Ti4+ (0,60A).
Tabel 3. Ukuran kristal TiO2 dan TiO2-Co (Mugundan et al.,2015)
Sampel Ukuran kristal (nm)
TiO2 murni 15,31
4% Co-doped TiO2 19,91
8% Co-doped TiO2 20,91
12% Co-doped TiO2 23,44
24
c. Scanning Electron Microscopy with Energy Dispersive X-Ray Spectroscopy (SEM-EDX)
SEM merupakan suatu mikroskop elektron yang menerapkan prinsip difraksi elektron, yang prinsip kerjanya sama dengan mikroskop optik. Pada SEM, lensa yang digunakan merupakan lensa elektromagnetik, yaitu kumparan medan magnet dan medan listrik yang dibuat dengan adanya tegangan tinggi sehingga elektron yang melewatinya dibelokkan seperti cahaya oleh lensa elektromagnetik tersebut.
Sebagai pengganti sumber cahaya digunakan suatu pemicu elektron (electron gun) yang berfungsi sebagai sumber elektron. SEM dapat menyediakan suatu hasil gambar dari permukaan dan memberikan perbesaran yang cukup tinggi, serta kedalaman medan yang cukup baik.
Panjang gelombang (λ) dari sumber cahaya yang digunakan untuk pencahayaan berpengaruh pada daya resolusi yang tinggi. Besarnya energi elektron (E) menentukan besarnya momentum (P) sesuai dengan rumus.
(15)
Besarnya momentum menetapkan nilai panjang gelombang sesuai dengan persamaan de Broglie.
λ = = (16)
Pada SEM, sampel diletakkan di ruang vakum, dimana sebelumnya udara yang ada dipompa keluar, lalu suatu pemicu elektron akan memancarkan sinar dari elektron berenergi tinggi. Sinar elektron ini turun melewati suatu lensa magnetik yang dibuat untuk memfokuskan elektron pada tempat yang tepat. Sinar elektron yang terfokus ini digerakkan ke seluruh permukaan sampel dengan menggunakan deflection coil. Sinar elektron ini mengenai setiap permukaan pada sampel. Suatu detektor kemudian mengumpulkan elektron sekunder tersebut dan mengubahnya menjadi suatu sinyal yang dikirim ke layar. Hasil gambar yang terbentuk ini disusun dari sejumlah elektron yang dipancarkan dari permukaan sampel tersebut (Abdullah et al., 2010).
Energi spesifik sinar X yang dipancarkan oleh setiap atom dalam senyawa dapat dideteksi dengan Energy Dispersive X-Ray Spectroscopy (EDX). EDX
25
adalah suatu teknik analitik yang digunakan untuk menganalisis unsur-unsur atau mengkarakterisasi kandungan unsur kimia dari suatu sampel. EDX menganalisis emisi sinar X oleh unsur dalam partikel.
Untuk mendorong terjadinya emisi karakteristik sinar X dari suatu sampel, sebuah energi yang tinggi dari partikel yang bermuatan seperti elektron atau proton, atau pancaran sinar X difokuskan pada sampel untuk dikarakterisasi. Sisanya, suatu atom dengan sampel yang mengandung elektron pada keadaan dasar (tidak tereksitasi) berada pada tingkat energi yang diskrit atau kulit elektron bergerak ke inti. Pancaran yang terjadi mungkin mengeksitasi sebuah elektron di dalam kulit yang terdalam. Sebuah elektron dari kulit terluar, tingkat energi yang lebih tinggi kemudian mengisi kekosongan itu dan adanya perbedaan energi antara tingkat energi tertinggi dengan tingkat energi terendah dibentuk dalam bentuk sinar X. Sinar X yang terbentuk oleh elektron kemudian dideteksi dan dianalisis dengan EDX (Mauritz, 2008).
Hasil SEM-EDX pada penelitian menggunakan Co-TiO2 16%
menunjukkan bentuk bulatan-bulatan yang tersebar pada kristal TiO2-Co. Bentuk
bulatan tersebut tidak hanya mempengaruhi area permukaan saja, tetapi juga meningkatkan struktur elektronik yang membuat lebih aktif pada spektra cahaya daerah visible untuk aktivitas fotokatalisnya (Mugundan et al., 2015).
d. Spektrofotometer Fourier Transform Infra Red (FTIR)
FTIR merupakan metode analisis material dengan menggunakan spektroskopi sinar infra merah. Sinar inframerah memiliki rentang panjang gelombang dari 2,5 μm sampai 25 μm. Adapun frekuensi sinar merah memiliki rentang panjang gelombang dari 400 cm-1 sampai 4000 cm-1. Dalam spektroskopi sinar infra merah, radiasi sinar infra merah ditembakkan ke arah sebuah molekul. Sebagian radiasi sinar infra merah tersebut diserap (diadsorpsi) oleh molekul dan sebagian lagi diteruskan (ditransmisikan) melalui molekul tersebut yang menghasilkan sebuah spektrum. Hasil spektrum tersebut mewakili nilai adsorpsi dan transmisi dari molekul. Seperti sidik jari manusia, tidak ada molekul yang
26
memiliki nilai spektrum atau vibrasi yang sama. Hal ini menyebabkan spektroskopi inframerah sangat bermanfaat untuk menganalisis dari molekul.
Pengujian FTIR dilakukan untuk menentukan intensitas suatu komponen dalam sebuah campuran. FTIR merupakan pengujian kuantitatif untuk sebuah sampel. Ukuran puncak (peak) data FTIR menggambarkan jumlah atau intensitas senyawa yang terdapat di dalam sampel. FTIR menghasilkan data berupa grafik intensitas dan frekuensi. Intensitas menunjukkan tingkatan jumlah senyawa, sedangkan frekuensi menunjukkan jenis senyawa yang terdapat dalam sebuah sampel.
B. Kerangka Pemikiran
Doping logam pada TiO2 dapat mempengaruhi pertumbuhan kristal TiO2
karena aglomerasi partikel. Doping logam yang ditambahkan pada struktur kristal TiO2 dapat mempengaruhi struktur kristal. Jika logam yang ditambahkan memiliki
jari-jari ionik lebih besar dari jari-jari ionik Ti4+ (0,60 A) maka akan menyebabkan peningkatan ukuran partikel kristal. Sehingga semakin banyak konsentrasi yang ditambahkan ke dalam TiO2 ukuran kristalnya semakin
meningkat. Penambahan logam Mn, Co dan Cd ke dalam TiO2 dengan komposisi
berbeda juga dapat mempengaruhi band gap energi.
Mekanisme migrasi elektron TiO2-M melalui tahap eksitasi elektron dari
pita valensi ke pita konduksi, kemudian elektron bermigrasi menuju logam dan terperangkap dalam logam. Logam yang bertindak sebagai electron trapper dapat meminimalisir rekombinasi electron-hole, sehingga hole akan bebas berdifusi ke permukaan semikonduktor dan melakukan oksidasi senyawa-senyawa yang didegradasi. Electron trapper dapat memperlambat rekombinasi electron-hole sehingga waktu hidup semakin lama dan meningkatkan reaksi redoks terhadap senyawa berwarna. Ion logam juga dapat meningkatkan aktivitas katalitik dan memodifikasi sifat fotokatalitik semikonduktor dengan meningkatkan serapan cahaya TiO2-M menuju ke daerah visible (380 – 750 nm) karena adanya
27
menyebabkan elektron pada ion logam tereksitasi menuju pita konduksi TiO2
(charge-transfer).
Proses fotodegradasi pada TiO2-M dipicu oleh energi cahaya menyebabkan
elektron pada M tereksitasi dari pita valensi ke pita konduksi TiO2. Reaksi
fotoeksitasi dari material TiO2-M kemungkinan akan melewati tahapan berikut:
TiO2-M + hν → eCB‾ + hVB+ eCB- + O2 → O2•‾ 2O2•‾ + 2H+ → O2 + H2O2 O2•‾ + 2H+ + 2eCB‾ → H2O2 H2O2 + eCB‾ → •OH + OH‾ H2O + hVB+ → •OH + H+
Semakin besar konsentrasi logam yang ditambahkan pada TiO2 maka akan
menghasilkan ukuran kristal yang lebih besar dan energi band gap semakin menurun. Semakin banyak ion logam dopan yang menempel pada permukaan TiO2 maka akan lebih banyak electron trapped dan menekan laju rekombinasi dan
kemungkinan penyerapan cahaya pada daerah visible semakin besar, sehingga aktivitas fotokatalis meningkat.
Lama waktu penyinaran saat proses degradasi fotokatalis akan menghasilkan banyak radikal hidroksil. Radikal hidroksil dihasilkan dari hole positif (h+) dari uap air yang teradsorp pada permukaan katalis semikonduktor. Pembentukan h+ dipengaruhi oleh energi (hv) yang dipancarkan oleh sinar. Semakin besar hv yang dipancarkan oleh sinar visible, maka h+ yang terbentuk akan semakin banyak. Sehingga radikal hidroksil yang dihasilkan juga semakin banyak. Semakin banyak radikal hidoksil yang terbentuk maka semakin banyak reagen pengoksidasi senyawa organik dan akan meningkatkan degradasi senyawa tersebut.
C. Hipotesis
1. Penambahan logam terhadap TiO2 akan mempengaruhi struktur kristal dan
28
2. Perubahan band gap dapat meningkatkan penyerapan cahaya semikonduktor TiO2 ke daerah sinar tampak (visible) dan meningkatkan aktivitas fotokatalis
dari TiO2 dan semakin lama penyinaran maka aktivitas fotokatalis akan