REAKSI ESTERIFIKASI Α-PINENA MENJADI
Α-TERPENIL ASETAT DENGAN KATALIS ZEOLIT
ALAM
Nanik Wijayati1, Ristia Purwodiningsih2, Nuni Widiarti3, Ella Kusumastuti4
1234Jurusan Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Negeri Semarang
Email: nanikanang@mail.unnes.ac.id
Abstract. Turpentine is one of the oil obtained from pine tree with composition
of 82% α- pinene. Turpentin oil has a high sales value is to make the esterification reaction α-pinene to get α-terpinyl. Usually esterification α-pinene is carried out with homogeneous catalysts are corrosive and unreusable. The purpose of the research are to know the optimum reaction time(2, 3, 4 jam), optimum reaction temperature (30, 40, 60ºC)and optimum mol ratio of reactants (1:5, 1:15, 1:20) between α-pinene and acetic anhydride for esterification α-pinene to α-terpinyl acetate using natural zeolite. Characterization of catalyst involve X- ray Diffraction, spectroscopy IR and Scanning Electron Microscopy. Product of esterification reaction analyzed using spectroscopy IR, gas chromatography, and gas chromatography-mass spectroscopy. Result of the analysis using spectrocopy IR show absorption of C-H at 2923 cm-1, C=O at 1725 cm-1, C=C at 1617 cm-1 and C-O at 1254 cm-1. The reaction time effect the conversion of α-pinena while reaction temperature and mol ratio of reactants effect on the increased levels of reaction products produced. The optimum conditions for esterification reaction α-pinene to α-terpinyl acetate is at temperature of 40ºC during 3 hours with mol ratio of reactants between α-pinene and acetic anhydride is 1:15 to produce α-terpenyl acetate amewweounted to 21,40%. Keywords: α-pinena, esterification, α-terpinyl acetate
Keywords : α-pinena, esterification, α-terpinyl acetate. PENDAHULUAN
Sebagian besar pohon pinus di Indonesia adalah jenis Pinus merkusii yang menghasilkan terpentin dengan komposisi 82% α-pinena dan komponen lain seperti kamfen, α-pinena, dan limonen (Utami, 2009). Upaya untuk mendapatkan nilai tambah minyak terpertin adalah melalui proses penyulingan yang menghasilkan komponen- komponen dari minyak terpentin. Salah satu upaya agar minyak terpentin mempunyai nilai jual tinggi adalah dengan melakukan reaksi esterifikasi α-pinena untuk menghasilkan α- terpenil asetat yang digunakan secara luas dalam industri pewangi, terutama pada sabun (Gainsford et al, 2000).Namun demikian, keberadaan terpenil asetat dialam sedikit dan kebutuhannya sangat kurang ekonomis sehingga
untuk memperolehnya dilakukan dengan mengisolasi dari tanaman (Rasmita, 2011).
Untuk memperoleh selektivitas tinggi dengan aktivitas yang baik akan menjadi sulit karena α-pinena mudah diisomerisasi menjadi beberapa produk. Dengan mengontrol variabel reaksi, memungkinkan untuk membuatnya selektivitas lebih tinggi terhadap produk yang diinginkan (Wijayati, 2013).
Zeolit alam merupakan zeolit yang banyak terdapat pada gunung berapi dan ditambang langsung dari alam sehingga harganya jauh lebih murah daripada zeolit sintesis (Yuanita, 2010). Kandungan utama zeolit alam Malang adalah mineral morderit yang memiliki rasio Si/ Al yang tinggi sehingga memiliki stabilitas termal yang tinggi (Rianto et al, 2012).
Reaksi esterifikasi antara α-terpineol dan anhidrida asetat dengan rendemen 5,57% dan kemurnian 67,50% pada suhu kamar (Rasmita, 2011). Gainsford et al (2000) melangsungkan konversi α-pinena menjadi α-terpenil asetat dengan H-zeolit beta pada suhu kamar dalam 24 jam menghasilkan rendemen 29%. Li et al (2012) melakukan sintesis terpenil asetat menggunakan cairan ionik oktadesil amina etoksilat sebagai katalis, kondisi optimum dicapai pada perbandingan pinena) : n(cairan ionik) : n(asam asetat) = 5:0,3:20, dimana n(α-pinena) = 0,05 mol, dilakukan pada temperatur 30ºC dengan waktu reaksi 10 jam sehingga didapatkanrendemen terpenil asetat sebesar 35,70%. Liu et al (2008) melakukan reaksi esterifikasi α-pinena menjadi α-terpenil asetat dengan selektivitas α-terpenil asetat tertinggi 27,8% menggunakan katalis cairan ionik asam yaitu [HSO3- (CH2)3-NEt3]H2PO4.
Berdasarkan uraian diatas, penelitian ini bertujuan untuk mengubah komponen minyak terpentin berupa α-pinena menjadi senyawa α-terpenil asetat melalui reaksi esterifikasi menggunakan katalis zeolit alam teraktivasi dengan waktu reaksi, temperatur, dan rasio mol reaktan optimum.
METODE
Alat yang digunakan dalam penelitian yaitu satu set alat destilasi fraksinasi pengurangan tekanan, Spektrofotometer IR, Difraktometer Sinar X, Scanning Electron Microscopy (SEM) Kromatografi Gas dan Kromatografi Gas-Spektrometer Massa. Sedangkan bahan yang digunakan yaitu minyak terpentin, aquades, zeolit alam, gas amonia, gas piridin, Na2SO4
anhidrat, anhidrida asetat, kertas saring, diklorometana, natrium bikarbonat jenuh, dan MgSO4 anhidrat.
Serbuk zeolit alam sebanyak 100 g direndam dengan 150 mL HF 1% selama 30 menit kemudian dicuci dengan aquades. Zeolit bebas HF dikeringkan dalam oven pada temperatur 120ºC selama 3 jam. Kemudian direndam dengan 150 mL HCl 6M selama 30 menit kemudian dicuci dengan aquademin sampai ion Cl- hilang (uji dengan AgNO3 1%) selanjutnya zeolit dikeringkan dalam oven pada temperatur 120ºC selama 3 jam. Kemudian direndam dengan
NH4Cl 1N kemudian dicuci dengan aquademin sampai ion Cl- hilang (uji dengan AgNO3), dikeringkan. Zeolit dipanaskan pada temperatur 450ºC selama 4 jam. Zeolit hasil aktivasi diayak kembali dengan ukuran 100 mesh dan dianalisis menggunakan XRD dan SEM.
Penentuan jumlah situs asam yaitu dengan menginkubator 0,5 g serbuk zeolit dengan aliran gas amonia dan piridin selama 24 jam kemudian dikarakterisasi menggunakan FTIR.
Isolasi α-pinena dari minyak terpentin, minyak terpenyin sebanyak 500 mL dimasukkan ke dalam erlenmeyer dan disaring menggunakan kertas saring. Selanjutnya ditambahkan Na2SO4
anhidrat untuk mengikat air didalam minyak sampai Na2SO4 anhidrat tidak menggumpal lagi
dan disaring untuk memisahkan endapan dengan minyak. Minyak terpentin yang sudah bebas air dalam erlenmeyer dipasang dengan alat destilasi fraksinasi pengurangan tekanan kemudian dipanaskan pada temperatur 50ºC. Kemudian hasil destilasi diuji dengan Spektrofotometer IR dan Kromatografi Gas.
Esterifikasi α-pinena, α-pinena seberat 0,5 g dicampurkan dalam 10 mL anhidrida asetat dan 5 mL aquades serta 10 mL diklorometana kemudian diaduk dengan menggunakan pengaduk mekanik selama 3 jam pada temperatur 40ºC dengan 0,5 g zeolit. alam teraktivasi dalam labu tertutup dilengkapi termometer. Hasil reaksi diekstraksi dengan 9 mL diklorometana. Setelah pemisahan, fase organik dicuci dengan aquades dan larutan natrium bikarbonat jenuh untuk menetralkan campuran. Kemudian ditambahkan dengan Na2SO4 anhidrat kemudian disaring
untuk memperoleh larutan organik yang murni lalu dialiri gas N2 untuk menguapkan sisa
pelarut. Selanjutnya hasil reaksi diuji dengan GC, FTIR dan GC-MS.
HASIL DAN PEMBAHASAN
Zeolit alam yang berbentuk bongkahan dihancurkan kemudian dihaluskan dan diayak dengan ayakan 100 mesh agar ukuran zeolit alam menjadi sama dan luas permukaannya menjadi lebih besar. Aktivasi zeolit alam dengan perlakuan asam dan garam bertujuan untuk meningkatkan kinerja zeolit alam. Zeolit alam yang sudah dilakukan perlakuan awal kemudian diaktivasi menggunakan HF 1% yang bertujuan untuk melarutkan oksida-oksida pengotor dalam zeolit. Zeolit alam yang sudah diaktivasi dengan HF 1% kemudian dilakukan perendaman dengan larutan HCl 6M bertujuan untuk dealuminasi zeolit alam yang dapat menaikkan rasio Si/Al. Perendaman dengan NH4Cl 1N bertujuan untuk menggantikan kation penyeimbang
dalam zeolit.
Hasil analisis zeolit alam teraktivasi dengan XRD pada Gambar 1 menunjukkan terdapat 3 puncak tertinggi pada H/ZA yaitu pada 2θ = 27,21º; 21,34º dan 25,09º. Menurut Rianto et
al (2012), puncak-puncak spesifik yang merupakan puncak dari morderit yaitu pada 2θ
= 20,9º; 25,63º; 26º; 26,25º; 27,67º. Sedangkan puncak khas untuk morderit terdapat pada puncak tertinggi yaitu pada 2θ = 25,631º dan 27,651º (JCPDS No 700232). Kesesuaian pola
difraktogra H/ZA dengan morderit dapat disimpulkan bahwa sampel H/ZA mempunyai struktut zeolit tipe Morderit.
Gambar 1. Difraktogram dari katalis H/ZA
Berdasarkan hasil scanning menggunakan SEM pada Gambar 2, maka diperoleh gambaran mengenai morfologi dari H/ZA pada perbesaran 5.000x menunjukkan bahwa sebaran ukurannya mencapai skala 20 mikrometer sedangkankan pada perbesaran 10.000x menunjukkan bahwa sebaran ukurannya mencapai skala 10 mikrometer. Ukuran molekul H/ ZA tidak merata dan bentuknya tidak teratur
Gambar 2. Foto mikro sampel H/ZA (a) perbesaran 5.000x (b) perbesaran 10.000x
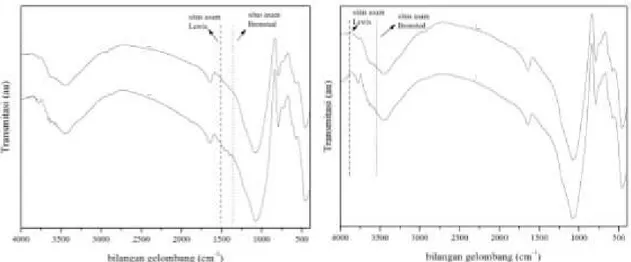
Penentuan jumlah situs asam katalis H/ZA dyang diperoleh dengan amonia (total) sebesar 0,809 mol/gram sedangkan jumlah situs asam dengan piridin (permukaan) sebesar 0,787 mol/gram.Berdasarkan hasil analisis menunjukkan bahwa jumlah situs asam total dengan amonia pada katalis H/ZA lebih tinggi dari jumlah situs asam permukaan dengan piridin. Hal ini disebabkan karena amonia merupakan basa lebih kuat dibandingkan piridin. Disamping itu, ukuran molekul basa amonia relatif lebih kecil dibanding piridin sehingga basa amonia
teradsorpsi sampai ke permukaan dalam (pori-pori) sementara piridin hanya teradsorpsi pada permukaan luar (mulut pori).
Gambar 3. Spektrum IR katalis H/ZA (a) setelah adsorpsi uap piridin (b) setelah adsorpsi uap amonia
Hasil indentifikasi fisik senyawa α-pinena yaitu berwujud cair, berwarna jernih dan berbau khas seperti terpentin. Berdasarkan hasil analisis menggunakan FTIR, α-pinena mengadung gugus C=C pada bilangan gelombang 1650 cm-1 menunjukkan bahwa α-pinena termasuk senyawa alkena. Dari data kromatografi gas pada Gambar 4kadar α-pinena hasil isolasi minyak terpentin sebesar 98,10%, hal ini sesuai menurut Utami (2009) Kandungan terbesar dalam minyak terpentin adalah senyawa α-pinena sekitar 82%.
Gambar 4. Kromatogram GC α-pinena
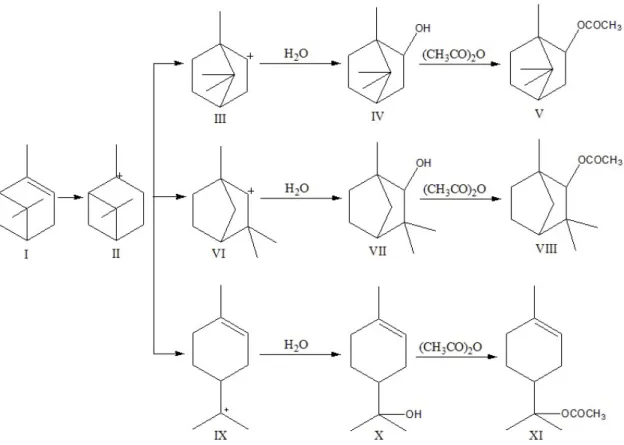
Reaksi esterifikasi α-pinena berlangsung secara insitu yaitu terjadi dalam satu reaksi melaui reaksi hidrasi terlebih dahulu dengan penambahan aquades sehingga terbentuk α- terpineol kemudian α-terpineol yang terbentuk akan mengalami reaksi esterifikasi dengan anhidrida asetat membentuk α-terpenil asetat. Dalam hal ini memungkinkan adanya produk lain dalam
reaksi esterifikasi α-pinena seperti fensil asetat, bornil asetat, fensil alkohol dan borneol.Reaksi esterifikasi α-pinena disajikan pada Gambar 5.
Gambar 5. Reaksi esterifikasi α-pinena (I) α-pinena (II) ion karbonium (III) ion karbonium (IV) borneol (V) bornil asetat (VI) ion karbonium (VII) fensil alkohol (VIII) fensil asetat (IX) ion karbonium (X) α-terpineol (XI) α-terpenil
asetat
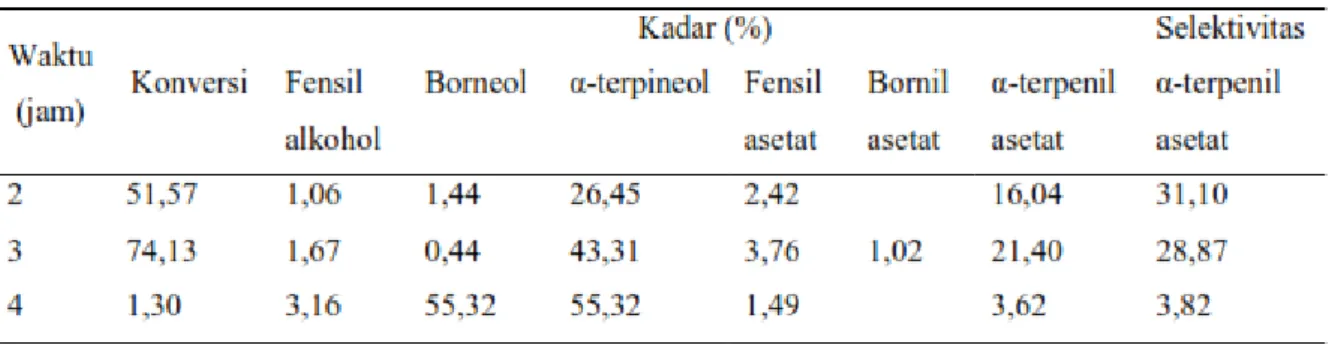
Berdasarkan tabel 1 kadar senyawa α-terpenil asetat dengan variasi waktu reaksi 2, 3 dan 4 jam didapatkan hasil yang optimum dengan waktu reaksi 3 jam dengan kadar sebesar 21,40%. Berdasarkan hasil analisis variasi waktu reaksi akan mempengaruhi konversi α- pinena terhadap produk yang dihasilkan. Dalam hal ini, konversi α-pinena semakin tinggi sedangkan kadar α-terpenil asetat yang dihasilkan dan selektivitasnya menurun pada waktu reaksi 4 jam
Tabel 1. Hasil reaksi esterifikasi α-pinena variasi waktu
Kondisi reaksi: 0,5 g pinena, 10 mL anhidrida asetat, 5 mL aquades, 10 mL diklorometana, T= 40ºC
Berdasarkan tabel 2 analisis hasil esterifikasi α-pinena variasi temperatur 30, 40 dan 60ºC dengan waktu reaksi optimum 3 jam dan rasio mol α-pinena dengan anhidrida asetat 1:15 didapatkan senyawa α-terpenil asetat dengan kadar tinggi pada temperatur reaksi 40ºC sebesar 21,40%. Kadar senyawa α-terpenil asetat pada temperatur 30ºC sebesar 0,18% kemudian pada temperatur 40ºC kadar α-terpenil asetat naik sebesar 1,40%. Pada temperatur reaksi 60ºC kadar α-terpenil asetat turun menjadi 14,72% sehingga temperatur optimum untuk melangsungkan reaksi esterifikasi α-pinena yaitu 40ºC. Dalam hal ini, temperatur reaksi mempengaruhi peningkatan kadar hasil reaksi dengan temperatur optimum pada 40ºC.
Tabel 2. Hasil reaksi esterifikasi α-pinena variasi temperatur
Kondisi reaksi: 0,5 g pinena, 10 mL anhidrida asetat, 5 mL aquades, 10 mL diklorometana, t= 3 jam
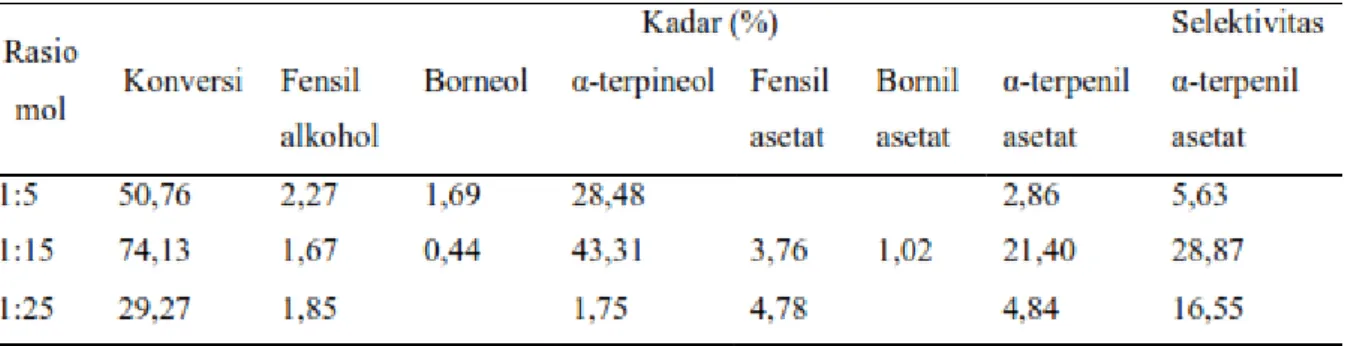
Berdasarkan tabel 3analisis hasil esterifikasi α-pinena rasio mol α-pinena dan anhidrida asetat 1:5, 1:15 dan 1:25 pada waktu reaksi optimum 3 jam dan temperatur optimum 40ºC didapatkan kadar senyawa α-terpenil asetat pada rasio mol 1:5 sebesar 2,86% kemudian pada
rasio mol 1:15 kadar α-terpenil asetat naik sebesar 21,40%. Pada rasio mol 1:25 kadar α-terpenil asetat turun menjadi 14,72% sehingga rasio mol antara α- pinena dengan anhidrida asetat optimum untuk melangsungkan reaksi esterifikasi α-pinena yaitu 1:15. Pada variasi mol reaktan juga akan mempengaruhi kadar hasil reaksi dengan rasio mol reaktan optimum 1 (0,007 mol) : 15 (0,105 mol).
Tabel 3. Hasil reaksi esterifikasi α-pinena variasi rasio mol antara α-pinena dengan anhidrida asetat
Kondisi reaksi: 5 mL aquades, 10 mL diklorometana, T= 40ºC, t= 3 jam
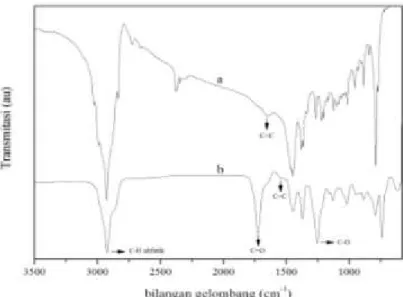
Hasil analisis esterifikasi α-pinena menggunakan FTIR pada Gambar 6 yaitu adanya serapan gugus C-H alifatik pada bilangan gelombang 2923 cm-1, gugus C=C pada bilangan
gelombang 1617 cm-1, gugus C=O pada bilangan gelombang antara 1735-1750 cm-1 dan
puncak gugus C-O pada bilangan gelombang antara 1050-1300 cm-1 dapat disimpulkan bahwa
senyawa yang dihasilkan merupakan senyawa ester. Dari senyawa α-pinena yang tidak adanya gugus C-O dan C=O menunjukkan bahwa senyawa hasil esterifikasi menghasilkan senyawa ester dari senyawa alkena.
Gambar 6. Spektrum IR (a) senyawa α-pinena (b) hasil esterifikasi hasil reaksi esterifikasi α-pinena waktu reaksi 3 jam, temperatur 40ºC dan rasio mol
antara α-pinena dengan anhidrida asetat 1:15 SIMPULAN
Kondisi optimum untuk melangsungkan reaksi esterifikasi α-pinena menggunakan zeolit alam teraktivasi yaitu pada temperatur 40ºC selama 3 jam dengan rasio mol reaktan antara α-pinena dengan anhidrida asetat 1:15 menghasilkan α-terpenil asetat sebesar 21,40% dan selektivitas sebesar 28,87%.Waktu reaksi berpengaruh terhadap konversi α-pinena yang semakin tinggi sedangkan temperatur reaksi dan rasio mol reaktan berpengaruh terhadap peningkatan kadar hasil reaksi yang dihasilkan.
DAFTAR PUSTAKA
Gainsford, G.J., C.F. Hosie, & R.J. Wetson. 2000. Conversion of α-pinene To Terpinyl Acetate Over H-Beta Zeolites. Applied Catalysis A: General, 209: 269–277.
Li, L., S. Liu, Y Shi, S. Yu, C. Xie, & C. Qi. 2012. Synthesis of Terpinyl Acetate Using Octadecylamine Ethoxylate Ionic Liquids as Catalysts. Res Chem Intermed 39:2095– 2105.
Liu, S., C. Xie, S. Yu, F. Liu, & K. Ji. 2008. Esterification of α-Pinene and Acetic Acid Using Acidic Ionic Liquids as Catalysts. Catalysis Communications, 9: 1634–1638.
Rasmita, I. 2011. Sintesis Terpenil Asetat dari Terpineol dan Anhidrida Asetat. Skripsi. Jurusan Kimia FMIPA Universitas Negeri Malang.
Utami, H. 2009. Kinetika Reaksi Terpineol dari Terpentin. Fakultas Teknik UGM.
Wijayati, N., H.D. Pranowo, Jumina, & Triyono. 2013. The Acid Catalyzed Reaction of α- Pinene Over Y-Zeolit. Indo. J. Chem, 13(1): 59-65.
Yuanita, D. 2009. Hidrogenasi Katalitik Metil Oleat menjadi Stearil Alkohol menggunakan Katalis Ni/Zeolit Alam. Prosiding Seminar Nasional Kimia. Yogyakata: Universitas Negeri Yogyakata.