Streptomyces erythreus. Pada determinasi mula-mula, ia di klasifikasikan sebagai anggota dari genus Streptomyces. Namun pada penelitian selanjutnya atas komponen penyusun dinding selnya, memperlihatkan bahwa asam amino yang terdapat pada dinding sel mikroba ini adalah meso-DAP, sedangkan pada genus Streptomyces komponen yang ada adalah L-DAP yang terikat pada residu glisin. Oleh karena itu, pada retaksonomi berikutnya Streptomyces erythreus dimasukkan ke dalam genus Saccharopolyspora.
Eritromisin yang terutama aktif terhadap bakteri Gram-positif, mempunyai spektrum antibiotika yang sempit dan kegunaan kliniknya mirip dengan penisilin (Frobisher et al., 1974). Spektrum aktivitas eritromisin yang mirip dengan penisilin dapat digunakan sebagai obat pilihan yang tepat untuk pasien yang sensitif terhadap penisilin, contohnya untuk melawan Mycoplasma sp, Haemophylus influenzae, Streptococcus pyogenes, dan Staphylococci. Mekanisme kerja eritromisin sebagai antimikroba adalah dengan menghambat sintesis protein bakteri, dengan menyekat reaksi translokasi asil amino dalam ribosomal (Jawetz et al., 1974), dengan pengikatan ribosom bakteri yang kekuatannya bergantung pada struktur antibiotik dan RNA ribosom bakteri.
Eritromisin tersebut termasuk dalam golongan makrolid, yang terdiri dari bagian aglikon berupa cincin lakton dengan anggota 14 atom, yang terikat pada molekul gula, yakni desosamin dan L-kladinosa / L-mikarosa (Omura dan Tanaka, 1984) seperti pada Gambar 5.
Eritromisin A merupakan produk akhir dalam biosintesis eritromisin oleh mikroba penghasil, sedangkan pada eritromisin B dan C merupakan bentuk
intermediet dalam biosintesis eritromisin. Gugus-gugus fungsional pada eritromisin seperti 12-hidroksi dan 9-keton pada cincin lakton, 2-hidroksi dan
3’-dimetilamino pada desosamin, dan 3”-metoksi kladinosa akan berikatan dengan
ribosom bakteri sub unit 50 S, sehingga akan mengganggu sintesis protein (Seno dan Hutchinson, 1986). O O 0 O OR2 CH3 OH CH3 O O N H3C CH3 CH3 HO CH3 H3C HO H3C R1 CH3 CH2R3 CH3 HO R1 R2 R3 Eritromisin A OH CH3 H Eritromisin B H CH3 H Eritromisin C OH H H Eritromisin D H H H Eritromisin F OH CH3 OH
Gambar 5. Struktur Antibiotik Eritromisin (Omura, 1984)
4. Jalur Biosintesis Eritromisin
Jalur biosintesis dari eritromisin terdiri dari dua jalur utama, yaitu 1. Sintesis dari cincin makrolakton, eritronolid
2. Sintesis dari D-desosamin dan L-mikarosa atau L-kladinosa yang akan bergabung dengan cincin makrolakton.
Biosintesis eritromisin diawali dengan kondensasi tipe Claisen antara 1 unit propionil-Koenzim A dan 6 unit metilmalonil-Koenzim A (Corcoran, 1981;
Donadio et al., 1991). Dengan demikian, propionil koenzim A disebut sebagai prekursor utama biosintesis eritromisin. Penambahan bahan-bahan yang mampu meningkatkan ketersediaan prekursor tersebut akan dapat meningkatkan produksi eritromisin (Mulyani, 2013). Propionil koenzim A dan metilmalonil koenzim A dapat diperoleh dari hasil katabolisme asam amino L-valin dan L-isoleusin (Corcoran, 1981; Luckner, 1984; Greenberg, 1961).
Eritronolid merupakan hasil kondensasi antara satu unit propionil koenzim A dengan enam unit metilmalonil koenzim A. Gula amino D-desosamin dan L-mikarosa serta L-kladinosa dibentuk dari D-glukosa tanpa pemecahan rantai karbon (Corcoran, 1981). Ada perbedaan pendapat antara Corcoran (1967), Manitto (1981) dan Donadio et al. (1991) mengenai biosintesis 6-deoksieritronolid, yang merupakan senyawa antara pada proses biosintesis eritromisin.
Menurut Corcoran (1967), pembentukan eritronolid diawali dengan kondensasi secara serempak satu unit propionil koenzim A sebagai unit pemula dengan enam unit metilmalonil koenzim A sebagai unit pengembang. Kondensasi ini membentuk poliketida asam heksametilheksaoksopentadekanoat. Asam tersebut mengalami laktonisasi membentuk polioksolakton, kemudian diikuti reduksi spesifik gugus karbonil yang terdapat pada atom C pada nomor 3, 5, 7, 11 dan 13 hingga diperoleh 6-deoksieritronolida B.
Menurut Manitto (1981), reduksi spesifik terjadi segera setelah poliketida terbentuk, baru kemudian poliketida tereduksi ini mengalami laktonisasi
membentuk 6-deoksieritronolida B. Hal ini berkebalikan dengan pendapat Corcoran, dimana reduksi spesifik terjadi lebih dahulu daripada laktonisasi.
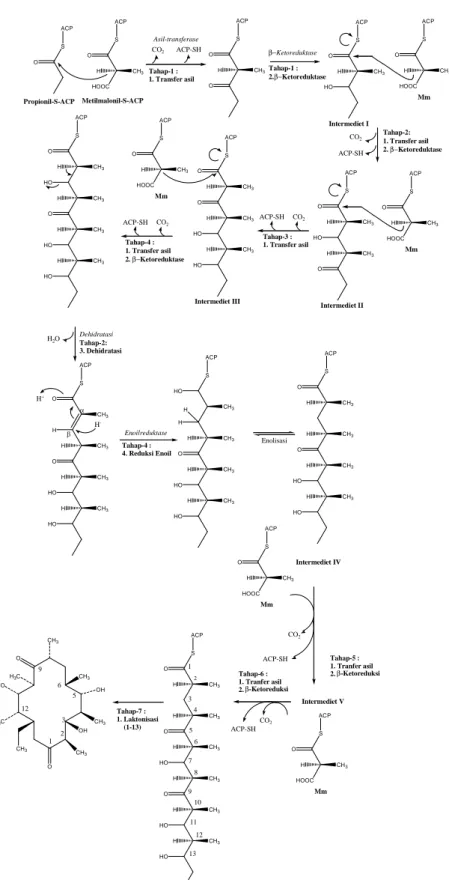
Menurut Donadio et al. (1991), aglikon eritronolida disintesis dengan kondensasi secara bertahap dengan bantuan enzim kompleks yang bekerja seperti sintase asam lemak (Fatty Acid Synthase/FAS) yang disebut dengan FAS-like. Penggabungan antara satu unit propionil koenzim A dan eenam unit metil malonil koenzim A terjadi secara tahap demi tahap dan tidak melalui zat antara berupa asam heksametilheksaoksopentadekanoat. Di setiap tahap kondensasinya, akan melibatkan satu unit metilmalonil koenzim A. Setiap tahap kondensasi yang terjadi akan segera diikuti dengan reaksi reduksi β-keto kecuali pada tahap ketiga, sehingga gugus keto tetap terdapat pada ato C-9. Pada tahap ke-empat, selain
reduksi β-keto, juga terjadi dehidrasi dan reduksi enoil. Yang kemudian setelah
ke-enam tahap kondensasi selesai, baru terjadi laktonisasi antara C-1 dengan C-13 membentuk 6-deoksieritronolida B, seperti terlihat pada gambar 6.
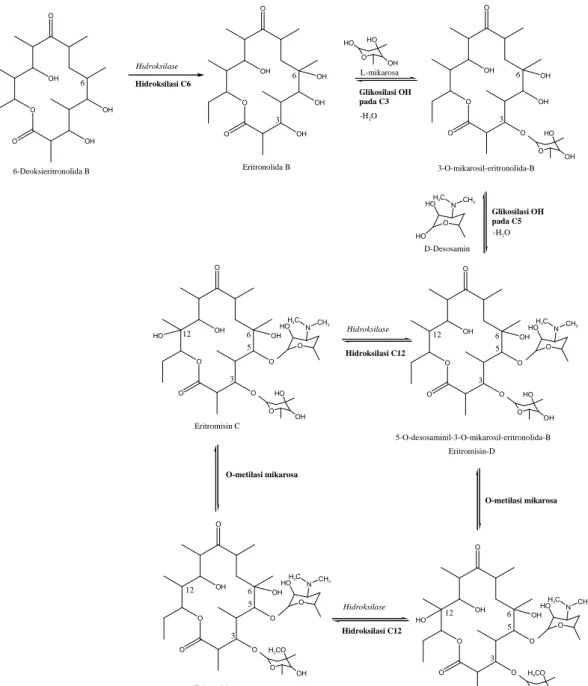
Selanjutnya, dilakukan pengikatan eritronolida B dengan L-mikarosa pada atom C-3 membentuk monoglikosida, yaitu 3-O-mikarosil eritronolida B. Kemudian D-desosamin berikatan pada C-5 untuk membentuk glikosida yang merupakan percabangan dalam biosintesis eritromisin, yaitu eritromisin D. Reaksi O metilasi pada gula netralnya akan menghasilkan eritromisin B, sedangkan hidroksilasi aglikon pada posisi 12 akan membentuk eritromisin C (Corcoran 1981). Eritromisin B dan C dapat diubah menjadi eritromisin A masing-masing melalui oksidasi C-12 dan O-metilasi pada C-3 (Omura & Tanaka, 1984).
Propionil-S-ACP O S ACP O S HOOC ACP H CH3 Metilmalonil-S-ACP ACP-SH CO2 Asil-transferase Tahap-1 : 1. Transfer asil O S ACP H CH3 O Ketoreduktase Tahap-1 : 2.Ketoreduktase O S ACP H CH3 HO O S HOOC ACP H CH3 Intermediet I Mm CO2 ACP-SH Tahap-2: 1. Transfer asil 2.Ketoreduktase O S ACP H CH3 HO O CH3 H O S HOOC ACP H CH3 Mm Intermediet II ACP-SH CO2 Tahap-3 : 1. Transfer asil O S ACP H CH3 O HO CH3 H Intermediet III HO H CH3 O S HOOC ACP H CH3 Mm ACP-SH CO2 Tahap-4 : 1. Transfer asil 2.Ketoreduktase O S ACP H CH3 HO O CH3 H HO H CH3 HO H CH3 Tahap-2: 3. Dehidratasi Dehidratasi H2O O S ACP CH3 H O CH3 H HO H CH3 HO H CH3 H+ H -Enoilreduktase Tahap-4 : 4. Reduksi Enoil HO S ACP CH3 H O CH3 H HO H CH3 HO H CH3 H Enolisasi O S ACP CH3 O CH3 H HO H CH3 HO H CH3 H Intermediet IV Tahap-5 : 1. Tranfer asil 2.-Ketoreduksi Intermediet V O S HOOC ACP H CH3 Mm Tahap-6 : 1. Tranfer asil 2. -Ketoreduksi ACP-SH CO2 O S ACP CH3 O CH3 H HO H CH3 O H CH3 H CH3 H HO HO H CH3 1 2 3 4 5 6 7 8 9 10 11 12 13 Tahap-7 : 1. Laktonisasi (1-13) O CH3 CH3 OH CH3 OH CH3 O CH3 H3C HO H3C 1 2 3 5 6 9 12 ACP-SH CO2 O S HOOC ACP H CH3 Mm
Gambar 6. Hipotesis Mekanisme dari Biosintesis 6-Deoksieritronolida B berdasarkan Studi Genetik oleh Donadio (1991)
O OH O OH OH O 6 Hidroksilase Hidroksilasi C6 O OH O OH OH O 6 OH 6-Deoksieritronolida B Eritronolida B Glikosilasi OH pada C3 -H2O 3 O HO OH HO L-mikarosa O OH O OH O O 6 OH 3 O HO OH Glikosilasi OH pada C5 -H2O O N CH3 H3C HO HO D-Desosamin O OH O O O O 6 OH 3 O HO OH 5 O N CH3 H3C HO 5-O-desosaminil-3-O-mikarosil-eritronolida-B Eritromisin-D 3-O-mikarosil-eritronolida-B O OH O O O O 6 OH 3 O HO OH 5 O N CH3 H3C HO Hidroksilase Hidroksilasi C12 12 12 HO Eritromisin C O-metilasi mikarosa O OH O O O O 6 OH 3 O H3CO OH 5 O N CH3 H3C HO 12 Eritromisin A O OH O O O O 6 OH 3 O H3CO OH 5 O N CH3 H3C HO 12 O-metilasi mikarosa Hidroksilase Hidroksilasi C12 HO
5. Minyak Jelantah
Minyak goreng merupakan salah satu kebutuhan pokok manusia sebagai alat pengolah bahan-bahan makanan yang biasa digunakan untuk menggoreng. Minyak goreng nabati biasa di produksi dari kelapa sawit, kelapa atau jagung. Penggunaan minyak nabati lebih dari empat kali sangat membahayakan kesehatan.
Minyak goreng bekas (jelantah) adalah minyak goreng yang sudah digunakan beberapa kali pemakaian (Satriana, 2013). Selain warnanya yang tidak menarik dan berbau tengik, minyak jelantah juga mempunyai potensi bersar dalam membahayakan kesehatan tubuh. Minyak jelantah mengandung radikal bebas yang dapat mengoksidasi organ tubuh secara perlahan (Pakpahan, 2013). Minyak jelantah mengandung asam-asam lemak jenuh maupun tak jenuh yang sebagian telah terdegradasi karena adanya hidrolisis. Minyak jelantah merupakan limbah dari minyak kelapa sawit yang telah mengalami hidrolisis selama proses memasak. Kandungan yang terdapat pada minyak jelantah tergantung pada jenis makanan apa yang telah digunakan pada saat memasak dengan menggunakan minyak tersebut.
Minyak jelantah telah mengalami berbagai perubahan struktur. Suhu penggorengan telah menyebabkan berbagai perubahan ikatan kimia dari minyak. Salah satu perubahan yang terjadi adalah terjadinya perubahan struktur asam lemak. Minyak jelantah mengandung lebih banyak asam lemak trans (trans fatty acid) (IFST, 2007). Lemak trans, merupakan asam lemak tak jenuh yang
mempunyai minimal sebuah ikatan rangkap dua dengan konfigurasi trans, yang terbentuk selama proses hidrogenasi parsial dari minyak nabati (Mozaffarian, 2006).
Banyaknya asam lemak baik jenuh maupun tak jenuh akan sangat digunakan dalam proses fermentasi yang membutuhkan asam lemak jenuh dan tak jenuh sebagai praprekursornya.
Menurut Kasanah (1993), minyak kelapa sawit dimetabolisme oleh mikroorganisme menjadi asetil koenzim A. Asetil koenzim A tersebut akan memasuki siklus asam sitrat dan menghasilkan zat antara berupa suksinil koenzim A. Suksinil koenzim A akan berinterkonversi menjadi propionil koenzim A yang merupakan prekursor dalam biosintesis eritromisin.
C. Landasan Teori
Fermentasi merupakan suatu cara untuk mengubah suatu substrat menjadi produk tertentu yang dikehendaki dengan menggunakan bantuan mikroba. Dalam fermentasi dapat dilakukan beberapa cara untuk meningkatkan produk yang dihasilkan, salah satunya adalah dengan melakukan optimasi pada media fermentasi. Hal ini dapat dilakukan dengan menambahkan senyawa-senyawa yang dapat digunakan sebegai prekursor.
Penggunaan minyak jelantah pada media yang telah diberi molase dan ampas tahu sebelumnya akan dapat meningkatkan produksi eritromisin yang dihasilkan. Menurut Sudibyo (1990), metilmalonil koenzim A yang merupakan senyawa pembentuk eritronolida B yang juga merupakan pembentuk antibiotika
eritromisin, dapat dibuat dengan beberapa cara. Cara tersebut adalah dengan melalui siklus asam sitrat dan melalui pembentukan propionil koenzim A. Pada minyak jelantah yang mengandung asam lemak, asam lemak yang terdapat pada minyak jelantah tersebut dapat turut serta dalam siklus asam sitrat. Selain itu dapat juga turut serta dalam pembentukan propionil koenzim A.
Dengan adanya asam lemak yang ditambahkan pada media, maka pembentukan eritromisin yang dihasilkan dari fermentasi Sac. erythraea akan meningkat.
D. Hipotesis
Eritromisin dapat diproduksi melalui fermentasi menggunakan media yang sesuai. Berdasarkan uraian pustaka sebelumnya, dapat dikumpulkan hipotesis sebagai berikut :
1. Penambahan minyak jelantah pada media, dapat meningkatkan produksi eritromisin.
2. Penambahan kombinasi ampas tahu, molase dan minyak jelantah dapat meningkatkan jumlah biomassa yang dihasilkan.