PRODUKSI BIOFLOKULAN DARI LUMPUR AKTIF
INDUSTRI UNTUK AIR SUNGAI DAN
AIR LIMBAH INDUSTRI
WENNY AYUNISA
DEPARTEMEN TEKNOLOGI INDUSTRI PERTANIAN FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR BOGOR
PERNYATAAN MENGENAI SKRIPSI DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA
Dengan ini saya menyatakan bahwa skripsi berjudul Produksi Bioflokulan dari Lumpur Aktif Industri untuk Air Sungai dan Air Limbah Industri adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, Desember 2014 Wenny Ayunisa NIM F34100093
ABSTRAK
WENNY AYUNISA. Produksi Bioflokulan dari Lumpur Aktif Industri untuk Air Sungai dan Air Limbah Industri. Dibimbing oleh SUPRIHATIN.
Bioflokulan merupakan flokulan alami yang diperoleh dari hasil sekresi mikroorganisme berupa polisakarida, protein, glikoprotein dan asama nukleat. Sumber bioflokulan yang digunakan pada penelitian ini adalah lumpur aktif industri hasil proses produksi kecap, PT. XXX. Penelitian ini bertujuan untuk menganalisis metode isolasi mikroorganisme dan metode sintesis polisakarida menggunakan asam berdasarkan efektivitas flokulasi, waktu produksi dan biaya produksi. Metode isolasi mikrooganisme menghasilkan isolat potensial yang dapat mengendapkan suspensi kaolin hingga lebih dari 60% dalam waktu 10 menit yaitu isolat CMC-1 (78.36%). Isolat CMC-1 diketahui adalah bakteri selulolitik. Metode produksi bioflokulan dengan sintesis polisakarida menggunakan asam menghasilkan efektivitas flokulasi sebesar 53.92% tetapi waktu produksinya lebih cepat, lebih murah, dan lebih mudah sehingga lebih dapat diaplikasikan di industri. Selanjutnya bioflokulan dengan metode terpilih diujikan ke air limbah. Air limbah yang digunakan adalah air sungai dan air limbah industri kecap, PT. XXX. Hasil uji efektivitas flokulasi bioflokulan menyatakan bahwa bioflokulan dapat membantu flokulasi air sungai sebesar 43.49% dan air limbah industri sebesar 29.93%. Penambahan koagulan alum dan FeCl3 dengan dosis tertentu dapat membantu meningkatkan efektivitas flokulasi.
Kata kunci: bioflokulan, isolasi bakteri, koagulan, efektivitas flokulasi
ABSTRACT
WENNY AYUNISA. Production of Bioflocculant from Activated Sludge for River Water and Industrial Wastewater. Supervised by SUPRIHATIN.
Bioflocculant is a natural flocculant from secretion product of microorganism that is polysaccharide, protein, glycoprotein, and nucleic acid. Source of bioflocculant used in this study is activated sludge from soy sauce industry PT. XXX. This study aims to analyze produce bioflocculant from industrial activated sludge with the isolation microb method and polysaccharide synthesis using acid method. The isolation microb method revealed that there are potential isolates that could floculate the suspension of kaolin by more than 60% in ten minutes which is isolates CMC-1 (78.36%). Isolate CMC-1 is identified as cellulolytic bacteria. Bioflocculant production using acid to catch polysaccharide resulted in only 53.92% flocculation effectivity but it is lower cost, more quickly, and easy to apply in industry. The selected bioflocculant is then tested for water and wastewater treatment. Research results showed the bioflocculant flocculation effectivity of 43.49% for river water and of 29.93% for wastewater. Addition of coagulant with specific dose can help bioflocculant increase flocculating effectivity.
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Teknologi Pertanian
pada
Departemen Teknologi Industri Pertanian
PRODUKSI BIOFLOKULAN DARI LUMPUR AKTIF
INDUSTRI UNTUK AIR SUNGAI DAN
AIR LIMBAH INDUSTRI
WENNY AYUNISA
DEPARTEMEN TEKNOLOGI INDUSTRI PERTANIAN FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR BOGOR
Judul Skripsi : Produksi Bioflokulan dari Lumpur Aktif Industri untuk Air Sungai dan Air Limbah Industri
Nama : Wenny Ayunisa NIM : F34100093
Disetujui oleh
Prof Dr-Ing Ir Suprihatin Pembimbing
Diketahui oleh
Prof Dr Ir Nastiti Siswi Indrasti Ketua Departemen
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah subhanahu wa ta’ala atas segala karunia-Nya sehingga skripsi ini berhasil diselesaikan. Tema yang dipilih dalam penelitian yang dilaksanakan sejak bulan April 2014 ini ialah flokulasi dan koagulasi, dengan judul Produksi Bioflokulan dari Lumpur Aktif Industri untuk Air Sungai dan Air Limbah Industri.
Terima kasih penulis ucapkan kepada Bapak Prof Dr-Ing Ir Suprihatin selaku pembimbing yang telah banyak memberi solusi dan saran selama pelaksanaan penelitian, Bapak Arie Budiawan Suryadiredja beserta staff PT. XXX bagian pengelolaan air limbah yang telah memberikan dukungan moril dan material selama penulis melaksanakan penelitian, dan staf dan laboran departemen Teknologi Industri Pertanian yang telah membantu selama pengumpulan data. Ungkapan terima kasih juga penulis sampaikan kepada ayah, ibu, adik serta seluruh mahasiswa Teknologi Industri Pertanian angkatan 47 atas segala bantuan, doa dan kasih sayangnya.
Semoga karya ilmiah ini bermanfaat.
Bogor, Desember 2014 Wenny Ayunisa
DAFTAR ISI
DAFTAR TABEL viii
DAFTAR GAMBAR viii
DAFTAR LAMPIRAN viii
PENDAHULUAN 1
Latar Belakang 1
Perumusan Masalah 2
Tujuan Penelitian 2
Manfaat Penelitian 3
Ruang Lingkup Penelitian 3
METODE 3
Waktu dan Tempat 3
Bahan 3
Alat 3
Metode 4
HASIL DAN PEMBAHASAN 6
Karakteristik Sampel Bioflokulan 6
Metode A (Isolasi Mikroorganisme) 7
Metode B (Sintesis Polisakarida menggunakan Asam) 9
Efektivitas Flokulasi Bioflokulan 9
Analisis Biaya Produksi 13
Analisis Metode Produksi Bioflokulan A dan B 13
Pengujian Efektivitas Flokulasi Air Sungai dan Air IPAL 14
SIMPULAN DAN SARAN 20
Simpulan 20
Saran 20
DAFTAR PUSTAKA 20
LAMPIRAN 22
DAFTAR TABEL
1 Karakteristik Lumpur Aktif 6
2 Penampakan visual isolat lumpur aktif 8
3 Efektivitas flokulasi isolat lumpur aktif 10
4 Perbandingan metode produksi bioflokulan 13
DAFTAR GAMBAR
1 Diagram alir pembuatan bioflokulan dari lumpur aktif industri 4 2 Proses destabilisasi partikel oleh polimer 11
3 Nilai kekeruhan kaolin 12
4 Persentase efektivitas flokulasi 12
5 Efektivitas koagulan pada air sungai 15
6 Nilai kekeruhan air sungai 16
7 Persentase efektivitas flokulasi air sungai 16 8 Pengaruh penambahan koagulan dan bioflokulan pada air sungai 17
9 Nilai kekeruhan air IPAL 18
10 Persentase efektivitas flokulasi air IPAL 19
11 Pengaruh penambahan koagulan dan bioflokulan pada air IPAL 19
DAFTAR LAMPIRAN
1 Efektivitas flokulasi isolat mikroba dari lumpur aktif industri 22 2 Nilai kekeruhan dan efektivitas flokulasi kaolin 23 3 Perbandingan rincian biaya produksi bioflokulan 24
4 Dosis koagulan untuk air sungai 26
5 Nilai kekeruhan dan efektivitas flokulasi air 27 6 Perbandingan flokulasi air berkoagulan dengan dan tanpa bioflokulan 28
1
PENDAHULUAN
Latar Belakang
Air baku pada umumnya mengandung partikel tersuspensi berupa partikel bebas dan koloid dengan ukuran yang sangat kecil. Koloid adalah campuran zat heterogen antara dua fasa atau lebih yang memiliki ukuran partikel sangat kecil (10-7-10-5) sehingga sulit terpisah secara alami dan menyebabkan kekeruhan. Pemisahan koloid dilakukan untuk memisahkan air dengan polutannya sehingga diperoleh air yang bersih. Terdapat berbagai macam cara pengolahan air limbah diantaranya nutrient removal, presipitasi, screening, filtrasi, adsorpsi, dan koagulasi-flokulasi. Pengolahan air limbah secara koagulasi-flokulasi dipilih karena proses tersebut dapat mengubah partikel koloid yang sangat kecil (lebih kecil dari 10-3) menjadi partikel yang ukurannya lebih besar. Selain itu, prosesnya lebih mudah dan sederhana serta mempermudah proses sedimentasi. Flokulan dan koagulan merupakan senyawa kimia yang digunakan dalam proses flokulasi. Flokulan adalah polimer yang berfungsi untuk menggabungkan flok-flok sehingga berukuran lebih besar dan mudah mengendap (Siregar 2005). Flokulan diklasifikasikan menjadi tiga yaitu flokulan sintetik anorganik (aluminium, feri sulfat, dan feri klorida), flokulan sintetik organik (poliakrilamid, polivinilpirimidin, dan polietilenimin), dan flokulan alami yang disebut bioflokulan. Flokulan yang paling sering digunakan adalah flokulan organik sintetik yaitu poliakrilamid. Penggunaan flokulan organik sintetik diketahui bersifat nonbiodegredable atau meninggalkan residu di lingkungan. Monomer poliakrilamid bersifat neurotoksik dan karsinogen kuat terhadap tubuh manusia (Salehizadeh dan Shokaosadati 2001). Maka dicari alternatif penggunaan flokulan yang aman dan tidak meninggalkan residu pada lingkungan. Penggunaan bioflokulan dapat menjadi alternatif pilihan flokulan yang aman untuk kesehatan manusia dan mengurangi pencemaran lingkungan secara sekunder.
Bioflokulan merupakan flokulan yang diperoleh secara biologis yaitu dari tumbuhan dan bakteri. Contoh bioflokulan yang diperoleh dari tumbuhan adalah bioflokulan dari biji kelor sedangkan bioflokulan dari bakteri diperoleh dari hasil sekresi mikroorganisme berupa polisakarida, protein, glikoprotein dan asam nukleat. Komponen tersebut yang berperan sebagai flokulan yang berfungsi untuk mengendapkan bahan cemaran air limbah. Lumpur aktif hasil pengolahan air limbah industri diketahui juga mengandung polisakarida dan protein yang dapat dijadikan sebagai sumber bioflokulan (Lauda 2013). Jika lumpur aktif tersebut dapat mengendapkan bahan cemaran dalam air limbah maka perusahaan dapat mengurangi penggunaan flokulan organik sintetik dan mengurangi pencemaran lingkungan.
Metode produksi bioflokulan dari lumpur aktif industri ada dua macam yaitu isolasi mikroorganisme (Wang et al. 1995) dan sintesa polisakarida menggunakan asam (Sun et al. 2012). Penggunaan lumpur sebagai bioflokulan telah banyak dilakukan sebelumnya. Wang et al.. (1995) telah berhasil mengisolasi Sporolactobacillus sp., Arthrobacter sp., Pseudomonas sp., dan Aeromonas sp dari lumpur aktif pengolahan air limbah kota di Cina dengan efektivitas flokulasi yang tinggi. Purnama (2007) juga dapat mengisolasi bakteri
2
dari lumpur aktif industri tekstil. Isolat tersebut diketahui adalah Pseudomonas diminuta yang mempunyai efektivitas flokulasi sebesar 71.23%. Produksi bioflokulan yang menggunakan media seperti glukosa, sukrosa, pepton dan ekstrak khamir membutuhkan biaya yang mahal sehingga akan berpengaruh terhadap efisiensi biaya produksi.
Bezawada et al. (2012) berhasil mengisolasi Serratia sp. dari lumpur aktif. Media yang digunakan sebagai substitusi glukosa, sukrosa, pepton dan ekstrak khamir adalah lumpur aktif yang telah dinetralkan terlebih dahulu. Hasil efektivitas Serratia sp. yang telah diinokulasikan pada media lumpur adalah 76.4%. Sun et al. (2012) menemukan metode yang lebih mudah dan murah untuk memproduksi bioflokulan yaitu dengan cara mensintesa polisakarida menggunakan asam. Pasangan elektron tunggal yang terdapat pada amida dalam polisakarida akan menarik ion H+ dalam larutan asam dan saling berikatan. Ikatan hidrogen antarmolekul akan dihancurkan oleh gaya tarik-menarik elektrostatik dan kemudian polisakarida akan larut dalam larutan asam (Guang et al. 2009). Berdasarkan teori tersebut maka digunakan asam klorida untuk memecah lumpur aktif dan memisahkan komponen bioflokulan yang disebut crude bioflokulan. Lumpur aktif yang digunakan Sun et al. adalah lumpur hasil dari pengolahan air limbah domestik secara biologis di Tiongkok. Lumpur aktif tersebut diketahui mengandung komponen makromolekul berupa polisakarida, protein, selulosa, asam lemak dan lain-lain sehingga sesuai dengan komponen bioflokulan. Oleh karena itu pada penelitian ini dilakukan analisis metode produksi bioflokulan yaitu dengan metode isolasi mikroorganisme dan sintesis polisakarida menggunakan asam berdasarkan efektivitas flokulasi, biaya produksi, dan waktu produksinya. Setelah itu bioflokulan terbaik diuji efektivitas flokulasinya terhadap air sungai dan air limbah industri serta pengaruh penambahan koagulan terhadap efektivitas flokulasi.
Perumusan Masalah
Berdasarkan penjabaran diatas, masalah yang diteliti dalam penelitian ini adalah lumpur aktif yang diperoleh dari industri kecap PT. XXX dilihat karakteristiknya kemudian dilakukan produksi bioflokulan dengan dua cara yaitu isolasi mikroorganisme dan sintesis polisakarida menggunakan asam. Kemudian dilakukan analisis terhadap efektivitas flokulasi, waktu dan biaya produksi dari kedua metode tersebut.
Tujuan Penelitian
Tujuan penelitian ini adalah untuk menganalisis metode isolasi mikroorganisme dan sintesis polisakarida menggunakan asam berdasarkan efektivitas flokulasi, biaya produksi, dan waktu produksinya. Menguji efektivitas flokulasi bioflokulan untuk menjernihkan air sungai dan air dari Instalasi Pengolahan Air Limbah (IPAL) serta mengetahui pengaruh penambahan koagulan terhadap efektivitas flokulasi bioflokulan.
3
Manfaat Penelitian
Penelitian ini diharapkan dapat memberikan ilmu pengetahuan baru tentang produksi bioflokulan ramah lingkungan dari lumpur aktif industri dengan proses yang lebih mudah dan flokulasi yang efektif. Memberikan informasi dan pengembangan terhadap industri yang memiliki lumpur aktif untuk mengurangi pemakaian flokulan sintetik dan menggunakan flokulan biologis. Bagi institusi hasil penelitian ini dapat dijadikan sebuah karya ilmiah dengan inovasi baru.
Ruang Lingkup Penelitian
Penelitian ini difokuskan untuk menganalisis metode produksi bioflokulan yaitu dengan metode isolasi mikroorganisme dan sintesis polisakarida menggunakan asam berdasarkan efektivitas flokulasi, biaya produksi, dan waktu produksinya. Setelah itu bioflokulan terbaik diuji efektivitas flokulasinya terhadap air sungai dan air Instalasi Pengolahan Air Limbah (IPAL) serta pengaruh penambahan koagulan terhadap efektivitas flokulasi.
METODOLOGI
Waktu dan Tempat
Penelitian dilaksanakan pada bulan April hingga Oktober 2014. Pengambilan data, analisis, dan perhitungan dilakukan di Laboratorium Dasar Ilmu Terapan, Laboratorium Bioindustri, dan Laboratorium Teknik Manajemen Lingkungan, Departemen Teknologi Industri Pertanian, Institut Pertanian Bogor.
Bahan
Bahan utama yang digunakan pada penelitian ini yaitu lumpur aktif yang dihasilkan oleh industri pembuatan kecap PT. XXX. Selain itu digunakan juga akuades, media nutrient agar (NA), CMC agar, skimmed milk agar, dan starch agar, alkohol 70%, larutan Alum, FeCl3, NaOH 4% dan HCl 3%. Media produksi bioflokulan yaitu glukosa, sukrosa, yeast ekstrak, pepton, urea, MgSO4, KH2PO4, (NH4)2SO4 dan NaCl.
Alat
Alat yang digunakan pada penelitian ini adalah neraca analitik, loop, labu erlenmeyer, mikropipet, pipet volumetrik, bulp, cawan petri, tabung ulir, tabung reaksi, gelas ukur, inkubator, pH meter, stopwatch,kapas, aluminium foil, clean bench, bunsen, batang pengaduk, alat jar test, sentrifuge dan rotary shaker, dan spektrofotometer DR 2000.
4
Metode
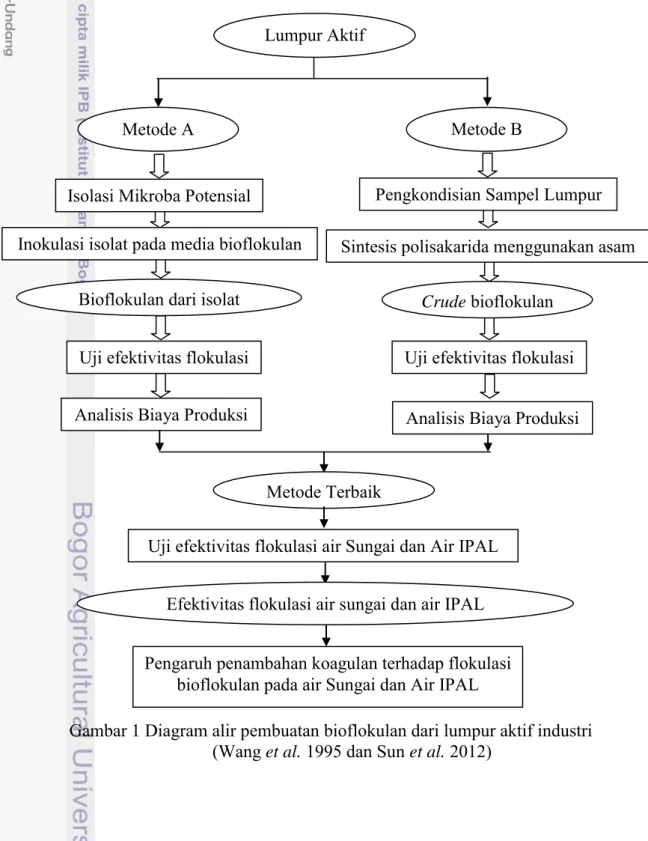
Metode yang dilakukan pada penelitian ini dapat dilihat pada Gambar 1. Lumpur aktif yang telah diketahui karakterisasinya dijadikan sebagai sumber bioflokulan. Produksi bioflokulan dilakukan dengan dua cara yaitu isolasi mikroorganisme dan sintesis polisakarida menggunakan asam. Analisis kedua metode adalah berdasarkan lama waktu produksi, efektivitas flokulasi dan biaya produksi bioflokulan. Setelah terpilih metode terbaik, maka bioflokulan diuji efektivitas flokulasinya pada air sungai dan air Instalasi Pengolahan Air Limbah (IPAL). Penambahan koagulan alum dan FeCl3 dilakukan untuk membantu bioflokulan mengendapkan bahan cemaran yang terdapat pada air.
Gambar 1 Diagram alir pembuatan bioflokulan dari lumpur aktif industri (Wang et al. 1995 dan Sun et al. 2012)
Metode Terbaik
Crude bioflokulan Uji efektivitas flokulasi Uji efektivitas flokulasi
Bioflokulan dari isolat
Inokulasi isolat pada media bioflokulan Sintesis polisakarida menggunakan asam Pengkondisian Sampel Lumpur Isolasi Mikroba Potensial
Lumpur Aktif
Metode A Metode B
Analisis Biaya Produksi Analisis Biaya Produksi
Uji efektivitas flokulasi air Sungai dan Air IPAL
Pengaruh penambahan koagulan terhadap flokulasi bioflokulan pada air Sungai dan Air IPAL Efektivitas flokulasi air sungai dan air IPAL
5
Isolasi Mikroba Potensial
Lumpur aktif diambil sebanyak 1 mL dan ditambahkan ke dalam 9 mL garam fisiologis. Diambil sebanyak 1 mL dari larutan tersebut kemudian dilakukan pengenceran bertingkat hingga 10-3. Sebanyak 100 µL suspensi larutan ditumbuhkan dalam media dengan metode cawan sebar kemudian diinkubasi selama 24 jam pada suhu 37 oC. Koloni yang muncul pada cawan diambil dan diisolasi pada agar miring kemudian diinkubasi kembali selama 24 jam pada suhu 37oC.
Produksi Bioflokulan A
Koloni terpilih yang telah diisolasi kemudian ditumbuhkan pada media produksi bioflokulan. Komposisi media produksi bioflokulan sebagai berikut: glukosa 10 g, sukrosa 10 g, yeast ekstrak 0.5, pepton 0.5 g, urea 0.5 g, MgSO4 0.2 g, KH2PO4 5.0 g, (NH4)2SO4 0.5 g dan NaCl 0.1 g dalam 1 L akuades (Wang et al. 1995). Koloni terpilih diinokulasikan dalam 50 mL media di dalam labu erlenmeyer 100 mL dan diinkubasi pada suhu 27 oC untuk persiapan inokulasi. Contoh medium diambil pada jam ke 72 dan diuji efektivitas flokulasinya. Menurut Parwono (1998) waktu kultivasi yang cukup lama bertujuan untuk memperoleh jumlah bioflokulan yang lebih banyak, dikarenakan adanya kemungkinan terdapat jenis bakteri yang lebih lambat dalam mensintesis bioflokulan. Menurut Lauda (2013) bakteri yang terdapat pada lumpur aktif industri kecap, PT. XXX memiliki fase stasioner saat berumur 2 hari hingga 15 hari dan akan memasuki fase kematian setelah 20 hari.
Pengujian Efektivitas Flokulasi
Pengujian efektivitas flokulasi kultur bakteri terhadap larutan kaolin sebagai model limbah dan dilakukan dalam gelas ukur 100 mL. Sebanyak 80 mL larutan kaolin dicampur dengan 10 mL koagulan FeCl3 0.05% dan 1.0 mL cairan kultur, kemudian ditambahkan air destilata hingga volume total 100 mL. Campuran kemudian diaduk pada suhu 27 oC dan dibiarkan tegak selama 10 menit. Pembentukan agregat diamati untuk menentukan terbentuk atau tidaknya flok dalam campuran reaksi. Dengan mengukur penurunan turbiditas lapisan atas campuran maka dapat dihitung derajat flokulasi. Kekeruhan lapisan atas campuran diukur pada panjang gelombang 450 nm menggunakan turbidimetri. Efektivitas flokulasi dihitung menurut persamaan : (A – B)/A x 100% dimana A adalah kekeruhan kontrol dan B adalah kekeruhan sampel.
Pengkondisian Sampel Lumpur Aktif
Sampel lumpur aktif diperoleh dari industri yang memproduksi kecap yaitu PT XXX. Sampel tersebut telah melewati proses pengolahan air limbah secara biologis. Sebelum digunakan untuk pembuatan bioflokulan, sebanyak 30 g sampel lumpur direndam dalam 100 ml larutan NaOH (4% w/w). Natrium hidroksida berfungsi untuk menghilangkan komponen mikromolekul dan inorganik flokulan yang terdapat pada lumpur aktif. Selama proses perendaman, sampel diaduk cepat selama 40 menit kemudian disentrifugasi pada kecepatan 4 000 rpm selama 15 menit. Sedimen hasil proses sentrifugasi kemudian dibilas dengan air destilata. Sedimen tersebut didefinisikan sebagai sampel lumpur yang sudah netral.
6
Produksi Crude Bioflokulan
Sebanyak 60 ml HCl (3% v/v) dicampurkan dengan sampel lumpur netral kemudian diaduk selama 15 menit. Suspensi tersebut disentrifugasi dengan kecepatan 4 000 rpm selama 15 menit. pH supernatan hasil dari proses sentrifugasi diatur menjadi 2. Supernatan tersebut disebut sebagai crude bioflokulan.
Pengujian Efektivitas Flokulasi
Pengujian efektivitas flokulasi kultur bakteri terhadap larutan kaolin sebagai model limbah dan dilakukan dalam gelas ukur 100 mL. Sebanyak 95 mL larutan kaolin dicampur dengan 3.0 mL cairan kultur ditambahkan air destilata hingga volume total 100 mL. Campuran kemudian diaduk pada suhu 27 oC dan dibiarkan tegak selama 10 menit. Pembentukan agregat diamati untuk menentukan terbentuk atau tidaknya flok dalam campuran reaksi. Dengan mengukur penurunan turbiditas lapisan atas campuran maka dapat dihitung derajat flokulasi. Kekeruhan lapisan atas campuran diukur pada panjang gelombang 450 nm menggunakan turbidimetri. Efektivitas flokulasi dihitung menurut persamaan : (A – B)/A x 100 % dimana A adalah kekeruhan kontrol dan B adalah kekeruhan sampel.
Efektivitas Bioflokulan terhadap Air Limbah
Bioflokulan terpilih akan diuji efektivitas flokulasinya pada air limbah. Caranya dengan mengganti kaolin sebagai bahan dasar uji flokulasi dengan air limbah. Sebanyak 80 ml air limbah dicampur dengan bioflokulan. Larutan diaduk perlahan kemudian dibiarkan 10 menit. kekeruhan dari air limbah diukur dengan menggunakan turbidimetri pada panjang gelombang 450 nm.
HASIL DAN PEMBAHASAN
Karakteristik Sampel Bioflokulan
Bioflokulan berasal dari sekresi alami mikroorganisme selama proses pertumbuhannya berupa polisakarida, protein, glikoprotein dan asam nukleat. Berdasarkan hasil analisis proksimat yang telah dilakukan oleh Lauda (2013) diketahui bahwa karakteristik sampel lumpur dapat dilihat pada Tabel 1.
Tabel 1 Karakteristik Lumpur Aktif
Parameter Satuan Hasil
Air % b/b 82.24 Abu % b/b 6.11 Protein Kasar % b/b 4.12 Lemak Kasar % b/b 0.016 Serat Kasar % b/b 5.82 Karbohidrat % b/b 1.69 Sumber : Lauda 2013
7 Tabel 1 menunjukkan bahwa sampel lumpur aktif industri mempunyai komponen yang sesuai untuk dijadikan bahan baku bioflokulan yaitu mikroorganisme yang menghasilkan protein, serat, dan karbohidrat (polisakarida) sebagai hasil sekresi hidupnya. Hasil sekresi polisakarida dan protein dari mikroba yang terkandung pada lumpur aktif, dapat digunakan sebagai bahan baku bioflokulan. Setelah diketahui bahwa sampel sesuai maka dilanjutkan dengan produksi bioflokulan dengan dua metode yaitu metode A (isolasi mikroorganisme) menurut Wang et al. (1995) dan metode B (sintesis polisakarida menggunakan asam) menurut Sun et al. (2012) yang dimodifikasi.
Metode A (Isolasi Mikroorganisme) Isolasi Mikroba Potensial
Sampel lumpur aktif diberi perlakuan pengenceran bertingkat hingga 10-3 kemudian diinokulasikan pada empat jenis media yaitu NA, CMC agar, Starch agar, dan Skimmed Milk agar. Penggunaan media CMC agar, Skimmed Milk agar dan Starch agar bertujuan untuk mempermudah mengetahui jenis bakteri yang terkandung dalam lumpur aktif. CMC agar adalah media spesifik yang dapat digunakan untuk mengisolasi bakteri selulolitik. Skimmed Milk agar digunakan untuk mengisolasi bakteri proteolitik, dan Starch agar untuk mengisolasi bakteri amilolitik.
Metode cawan sebar digunakan untuk mengisolasi bakteri. Metode cawan sebar berfungsi untuk mengisolasi bakteri yang bersifat aerobik. Menurut Davis (2010) populasi terbesar dalam pengolahan air limbah secara biologis adalah bakteri dengan sifat aerobik kemoheterotrof. Aerobik kemoheterotrof adalah bakteri yang memerlukan oksigen dan senyawa organik untuk pertumbuhannya. Setelah dilakukan inokulasi media diinkubasi pada suhu 37 oC selama 24 jam. Koloni dominan yang terbentuk selanjutnya diinokulasikan pada agar miring untuk diinkubasi kembali pada suhu 37 oC selama 24 jam.
Jumlah koloni dominan yang dapat diisolasi yaitu 11 koloni dengan kode NA-1, NA-2, NA-3, SA-1, SA-2, SA-3, SA-4, SA-5, SM-1, SM-2, SM-3, CMC-1, CMC-2 dan CMC-3. Penulisan kode disesuaikan dengan media tumbuhnya. Pada media nutrient agar terdapat 3 koloni dominan maka ditulis dengan kode NA-1, NA-2, dan NA-3. Berdasarkan uji efektivitas flokulasi pada Lampiran 1, diketahui bahwa tidak semua koloni mempunyai kekuatan flokulasi. Dari 11 koloni yang ada, hanya 8 koloni yang mempunyai kekuatan flokulasi. Menurut Salehizadeh dan Yan (2014) konsentrasi dan valensi logam seperti Al3+, Ca2+, Mg2+, dan Fe3+ akan berperan pada destabilisasi sistem koloid tetapi tidak semua logam dapat meningkatkan efektivitas flokulasi. Penampakan visual koloni yang mempunyai kekuatan flokulasi tersebut dapat dilihat pada Tabel 2.
8
Tabel 2 Penampakan visual isolat lumpur aktif
Kode
Isolat Warna
NA-1 Kuning tebal NA-2 Putih tipis SA-2 Kuning tebal SA-4 Kuning tebal SA-5 Kuning tebal SM-1 Putih tipis CMC-1 Putih tipis CMC-2 Putih tipis
Media Produksi Bioflokulan
Koloni yang telah diisolasi diinokulasikan ke dalam larutan media bioflokulan. Media bioflokulan yang digunakan adalah sebagai berikut: glukosa 10 g, sukrosa 10 g, ekstrak khamir 0.5, pepton 0.5 g, urea 0.5 g, MgSO4 0.2 g, KH2PO4 5.0 g, (NH4)2SO4 0.5 g dan NaCl 0.1 g dalam 1 L akuades (Wang et al. 1995). Media produksi bioflokulan tidak hanya berguna untuk memenuhi kebutuhan nutrisi bagi mikroorganisme tetapi juga menstimulasi bakteri mengeluarkan bioflokulan yang diproduksi oleh mikroorganisme selama proses pertumbuhannya (Gao et al. 2006).
Setiap bahan yang digunakan dalam media bioflokulan mempunyai fungsi masing-masing. Glukosa dan sukrosa digunakan sebagai energi bagi bakteri. Jumlah glukosa dan sukrosa yang digunakan lebih banyak dibanding bahan lain dalam medium. Hal ini memiliki tujuan agar bakteri terus mengkonsumsi sumber karbon tersebut selama pertumbuhan sehingga produk hasil metabolisme mikroba juga semakin banyak. Ekstrak khamir berguna sebagai sumber nitrogen organik yang paling baik dalam pembentukan bioflokulan dibanding sumber nitrogen organik lain. Jumlah ekstrak khamir yang sesuai menurut Nohata dan Kurane (1994) adalah 0.5 gram. Urea dan (NH4)2SO4 berfungsi sebagai sumber nitrogen anorganik karena kombinasi keduanya dapat memacu aktivitas sel dalam pembentukan bioflokulan. Senyawa KH2PO4 merupakan media kultivasi yang mengandung buffer sehingga selain berfungsi sebagai sumber energi, KH2PO4 juga berfungsi mempertahankan pH media tetap netral.
Koloni dominan yang berhasil diisolasi disebut kultur bioflokulan. Kultur bioflokulan diambil 1 ose kemudian diinokulasikan ke dalam media bioflokulan. Produksi bioflokulan dilakukan selama 72 jam pada suhu 27 oC dengan kecepatan 180 rpm menggunakan alat rotary shaker. Menurut Parwono (1998) waktu kultivasi yang cukup lama bertujuan untuk memperoleh jumlah bioflokulan yang lebih banyak, dikarenakan adanya kemungkinan terdapat jenis bakteri yang lebih lambat dalam mensintesis bioflokulan. Kecepatan 180 rpm digunakan agar kultur homogen dan bakteri memiliki aerasi yang baik.
Penambahan kultur pada media mempengaruhi pertumbuhan dan produksi bioflokulan. Pertumbuhan bakteri dapat dilihat dari warna media bioflokulan yang berubah menjadi keruh. Semakin keruh media maka semakin banyak jumlah bakteri yang tumbuh. Warna media sebelum diinokulasikan kultur adalah kuning
9 jernih sedangkan setelah kultivasi selama 72 jam akan berubah menjadi kuning keruh yang menunjukkan tumbuhnya bakteri.
Metode B (Sintesis Polisakarida menggunakan Asam) Produksi Crude Bioflokulan
Sampel lumpur aktif direndam terlebih dahulu menggunakan natrium hidroksida (4% w/w). Natrium hidroksida berfungsi untuk menghilangkan komponen mikromolekul dan inorganik flokulan yang terdapat pada lumpur aktif. Setelah itu dilakukan pemecahan komponen lumpur dengan menggunakan larutan HCl (3% v/v). Menurut Sun et al. (2012) jumlah HCl (3% v/v) yang efektif adalah sebanyak 60 ml untuk memecah 5 gram lumpur aktif. Efektivitas flokulasinya dapat mencapai 95.4%. Bioflokulan diperoleh dengan cara memisahkan lumpur dengan HCl menggunakan alat sentrifugasi. Supernatan hasil sentrifugasi digunakan untuk pengujian selanjutnya dan disebut sebagai crude bioflokulan. Crude bioflokulan terdiri dari air, polisakarida, protein, dan lain lain. Terbentuknya crude bioflokulan pada supernatan hasil sentrifugasi disebabkan karena pasangan elektron tunggal yang terdapat pada amida dalam polisakarida akan menarik ion H+ dalam larutan asam dan saling berikatan. Ikatan hidrogen antarmolekul akan dihancurkan oleh gaya tarik-menarik elektrostatik dan kemudian polisakarida akan larut dalam larutan asam (Guang et al. 2009).
Crude bioflokulan yang telah terbentuk memiliki nilai pH lebih kecil dari 1.0 akibat proses sebelumnya yaitu pemecahan oleh asam kuat HCl (3% v/v). Selanjutnya crude bioflokulan disesuaikan nilai pHnya menjadi 2.0 menggunakan larutan NaOH (4% w/w). Menurut penelitian Sun (2012) diketahui bahwa terdapat fenomena pengendapan ketika crude bioflokulan diatur pH menjadi diatas 3.0 yaitu terbentuk dua lapisan bioflokulan terdiri dari supernatan dan flok. Fenomena pengendapan pada crude bioflokulan akan berpengaruh terhadap penurunan efektivitas flokulasi ketika diuji pada suspensi kaolin. Oleh karena itu pH yang digunakan untuk crude bioflokulan ini disesuaikan menjadi 2.0 agar mencegah terjadinya pengendapan crude bioflokulan.
Efektivitas Flokulasi Bioflokulan
Pengujian efektifitas flokulasi dilakukan dengan menggunakan kaolin (5.5 g/L). Kaolin merupakan bahan uji standar dalam penentuan efektivitas flokulasi (Purnama 2007). Kultur bioflokulan yang telah terbentuk di media bioflokulan diambil sebanyak 1 ml kemudian dilarutkan dalam 80 mL larutan kaolin (5.5 g/L). Menurut Parwono (1998) penambahan dosis bioflokulan paling efektif adalah sebanyak 1 mL. Apabila ditambahkan dalam dosis yang berlebih maka akan mengakibatkan koloid menjadi stabil kembali. Selain itu ditambahkan juga 10 mL FeCl3 dengan konsentrasi 0.05% dan sisanya ditambah akuades sampai volumenya mencapai 100 mL (Susanti 2007). Semua bahan diaduk hingga homogen kemudian dibiarkan tegak selama 10 menit. Hasil pengujian efektivitas flokulasi dengan metode A dapat dilihat pada Tabel 3.
10
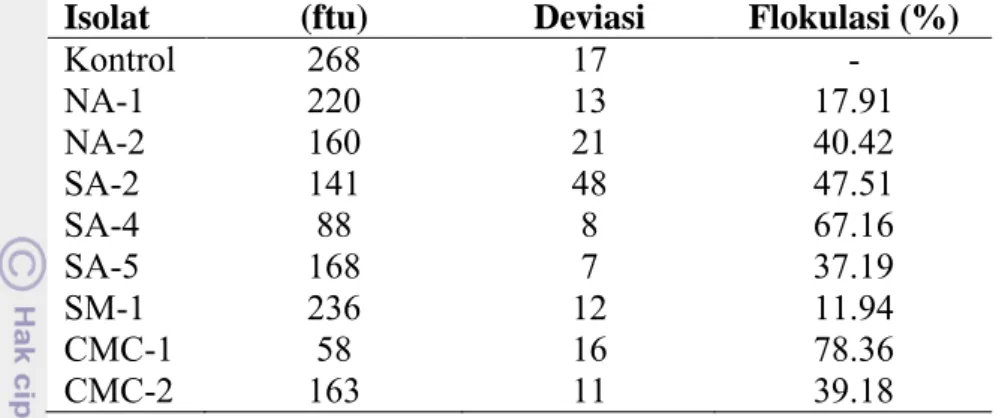
Tabel 3 Efektivitas flokulasi isolat lumpur aktif
Kode Isolat Kekeruhan (ftu) Standar Deviasi Efektivitas Flokulasi (%) Kontrol 268 17 - NA-1 220 13 17.91 NA-2 160 21 40.42 SA-2 141 48 47.51 SA-4 88 8 67.16 SA-5 168 7 37.19 SM-1 236 12 11.94 CMC-1 58 16 78.36 CMC-2 163 11 39.18
Simbol NA, SM, SA, dan CMC telah dijelaskan sebelumnya bahwa simbol tersebut dibagi berdasarkan media yang digunakan. NA merupakan media umum yang dapat menumbuhkan berbagai jenis bakteri, SA media spesifik untuk bakteri amilolitik, SM media untuk bakteri proteolitik, dan CMC merupakan media untuk bakteri selulolitik. Nomer yang berbeda menandakan bakteri berasal dari koloni yang berbeda dari media sejenis. Berdasarkan hasil uji tersebut diketahui masing-masing isolat memiliki efektivitas flokulasi yang berbeda. Isolat yang memiliki kemampuan flokulasi tertinggi yaitu isolat kode CMC-1 dan SA-2 sebesar 78.36% dan 67.16%. Isolat CMC-1 diketahui adalah bakteri dengan jenis selulolitik. Sedangkan isolat kode SA-2 diketahui adalah isolat bakteri dengan jenis amilolitik. Efektivitas flokulasi terendah yaitu isolat dengan kode SM-1 sebesar 11.94%. Menurut Salehizadeh dan Yan (2014) konsentrasi dan valensi logam seperti Al3+, Ca2+, Mg2+, dan Fe3+ akan berperan pada destabilisasi sistem koloid tetapi tidak semua logam dapat meningkatkan efektivitas flokulasi. Konsorsium bioflokulan Cobetia sp. dan Bacillus sp. meningkat efektivitas flokulasinya setelah dilakukan penambahan logam. Hampir semua jenis logam dapat meningkatkan efektivitas flokulasi kecuali Li+ dan K+. Penambahan Li+ dan K+ pada konsorsium mengganggu proses pengendapan sehingga efektivitas flokulasinya menurun (Nwodo et al. 2014). Selain itu, menurut Lu et al. (2005) karakteristik penting flokulan adalah mengandung polisakarida yang tinggi karena polisakarida lebih tahan panas dibandingkan dengan flokulan yang mengandung protein tinggi.
Kemampuan isolat-isolat dalam memflokulasi dapat diketahui dengan adanya endapan yang terbentuk hingga menit kesepuluh. Flok-flok yang terbentuk merupakan ikatan antara bioflokulan dengan FeCl3 0.05% dalam mengikat partikel koloid. Flokulasi bertujuan untuk membuat gumpalan lebih besar dengan penambahan polimer sehingga mempercepat proses pengendapan. Semakin besar agregat yang terbentuk berarti semakin banyak kaolin yang terflokulasi akibatnya lapisan atas larutan kaolin akan lebih bening dibanding kontrol sehingga dapat diukur dengan turbidimetri pada λ 450 nm.
Proses mekanisme terjadinya flokulasi dapat dilihat pada Gambar 2. Gambar 2 menjelaskan molekul polimer yang ditambahkan dalam suspensi berinteraksi dengan partikel koloid. Terjadi penyerapan polimer pada permukaan partikel sehingga terjadi persilangan antara segmen polielektrolit untuk
11 membentuk jembatan antara partikel koloid. Proses terjadinya jembatan ini yang akan menghasilkan partikel flok yang dapat mengendap.
Apabila cabang polimer tidak dapat berikatan dengan sisi aktif partikel koloid lain, polimer tersebut akan berbalik dan berikatan pada sisi aktifnya semula dan kembali stabil. Proses flokulasi yang tidak efisien dapat terjadi akibat dosis polimer yang berlebih atau proses pengadukan terlalu cepat dan terlalu lama. Jika dosis polimer yang ditambahkan terlalu berlebih maka molekul polimer akan menutupi seluruh permukaan partikel koloid sehingga tidak ada lagi sisi aktif yang dapat digunakan sebagai jembatan. Sementara pengaruh pengadukan akan mengakibatkan putusnya jembatan yang telah terbentuk sehingga partikel akan stabil kembali (Crittenden et al. 2012).
Reaksi 1
Destabilisasi koloid pada dosis polimer optimum
+
Polimer Partikel Partikel koloid terdestabilkan
Reaksi 2 Pembentukan flok
Partikel koloid terdestabilkan Flok
Gambar 2 Proses destabilisasi partikel oleh polimer (Crittenden et al. 2012 yang dimodifikasi)
Pengujian efektivitas flokulasi pada crude biflokulan dilakukan dengan cara yang sama yaitu menggunakan larutan kaolin kemudian ditambahkan crude bioflokulan sebanyak 3 mL dan diukur kekeruhannya menggunakan alat turbidimetri. Menurut Sun et al. (2012) persentase efektivitas flokulasi dapat diperoleh hingga 98% ketika jumlah bioflokulan yang digunakan sebanyak 2.7 – 3.3% (v/v). Penggunaan dosis crude bioflokulan yang lebih tinggi dari 3 mL mengakibatkan penurunan efektivitas flokulasi. Menurut Yim et al. (2007) diketahui bahwa dosis bioflokulan dapat meningkatkan efektivitas flokulasi hingga mencapai batas maksimum dan kemudian akan mengalami penurunan. Gambar 3 dan Gambar 4 menunjukkan hasil nilai kekeruhan dan persentase efektivitas flokulasi terhadap crude bioflokulan.
12
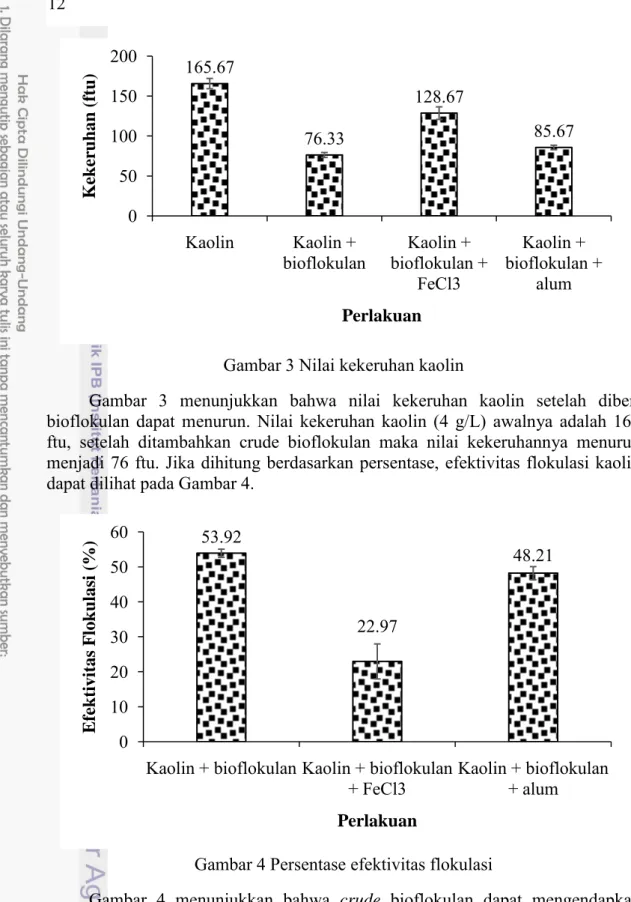
Gambar 3 Nilai kekeruhan kaolin
Gambar 3 menunjukkan bahwa nilai kekeruhan kaolin setelah diberi bioflokulan dapat menurun. Nilai kekeruhan kaolin (4 g/L) awalnya adalah 165 ftu, setelah ditambahkan crude bioflokulan maka nilai kekeruhannya menurun menjadi 76 ftu. Jika dihitung berdasarkan persentase, efektivitas flokulasi kaolin dapat dilihat pada Gambar 4.
Gambar 4 Persentase efektivitas flokulasi
Gambar 4 menunjukkan bahwa crude bioflokulan dapat mengendapkan kaolin lebih cepat yaitu sebesar 53.92% dibandingkan tanpa crude bioflokulan. Penambahan FeCl3 dan alum berfungsi untuk mengetahui koagulan yang dapat membantu mempercepat proses pengendapan. Menurut Siregar (2005) valensi ion akan berpengaruh terhadap proses koagulasi. Semakin besar valensi koagulan, efektivitas koagulasi juga semakin besar. Dengan demikian digunakan koagulan FeCl3 dan Alum yang memiliki valensi ion 3 namun berdasarkan data yang
165.67 76.33 128.67 85.67 0 50 100 150 200 Kaolin Kaolin +
bioflokulan bioflokulan + Kaolin + FeCl3 Kaolin + bioflokulan + alum K ek er u h an (f tu) Perlakuan 53.92 22.97 48.21 0 10 20 30 40 50 60
Kaolin + bioflokulan Kaolin + bioflokulan
+ FeCl3 Kaolin + bioflokulan + alum
E fe k tivitas F lok u lasi ( % ) Perlakuan
13 diperoleh ternyata koagulan alum dan FeCl3 tidak dapat membantu meningkatkan efektivitas flokulasi. Penurunan efektivitas flokulasi saat dilakukan penambahan koagulan dapat terjadi karena larutan dosis koagulan yang ditambahkan terlalu sedikit atau terlalu banyak sehingga proses destabilisasi menjadi tidak efisien (Crittenden et al. 2012).
Analisis Biaya Produksi
Analisis biaya produksi bioflokulan perlu diketahui untuk membandingkan biaya produksi bioflokulan dari metode A ataupun metode B. Asumsi yang digunakan adalah jumlah air limbah yang akan diolah adalah sebanyak 1 000 Liter. Metode A membutuhkan bioflokulan isolat CMC-1 sebanyak 10 L ditambah FeCl3 100 L untuk mengolah 1 000 L air limbah. Sedangkan untuk metode B jumlah crude bioflokulan yang dibutuhkan adalah sebanyak 30 L untuk 1 000 L air limbah. Rincian biaya produksi bioflokulan dapat dilihat pada Lampiran 3.
Perbandingan dilakukan dengan menghitung biaya investasi dan biaya operasional dari masing-masing metode. Metode A dapat menghabiskan biaya investasi sebesar 86 050 000 sedangkan metode B hanya 49 430 000. Begitu juga dengan biaya operasional, untuk memproduksi 10 L bioflokulan dibutuhkan biaya sebanyak 217 479 rupiah sementara metode B hanya membutuhkan dana sebesar 105 537 rupiah untuk menghasikan 30 L crude bioflokulan. Untuk membandingkannya maka diubah satuan biayanya menjadi per liter. Maka metode A membutuhkan Rp 31 992 per liter bioflokulan. Sementara metode B hanya membutuhkan Rp 3 975 per liter bioflokulan. Jika dihitung berdasarkan 1 liter air limbah maka metode A membutuhkan 320 rupiah per liter air limbah dan metode B 120 rupiah per liter air limbah. Kesimpulan dari perhitungan biaya kedua metode produksi bioflokulan adalah biaya produksi bioflokulan dengan metode B lebih murah dibandingkan dengan metode A.
Analisis Metode Produksi Bioflokulan A dan B
Setelah diketahui efektivitas flokulasi, waktu produksi, dan biaya produksi dari masing-masing metode maka selanjutnya adalah pemilihan metode terbaik. Faktor yang dibandingkan adalah waktu produksi, efektivitas flokulasi, dan biaya produksi. Ketiga faktor tersebut dipilih karena apabila metode tersebut akan diaplikasikan, diperlukan cara yang mudah dan sederhana, biaya produksi yang murah dan efektivitas flokulasinya yang tinggi hingga dapat bersaing dengan flokulan organik sintetik. Tabel 4 menunjukkan hasil pengujian ketiga faktor dari masing-masing metode.
Tabel 4 Perbandingan metode produksi bioflokulan
Faktor Inokulasi CMC-1 Crude bioflokulan
Waktu Produksi 4 hari 1 hari
Efektivitas Flokulasi 78.36% 53.92%
14
Berdasarkan data yang tertera pada Tabel 4, maka diketahui bahwa crude bioflokulan unggul dalam waktu produksi yang lebih cepat dan biaya yang lebih murah. Sementara pada efektivitas flokulasi, metode inokulasi CMC-1 pada media bioflokulan unggul dengan 78.36%. Efektivitas flokulasi pada crude bioflokulan, dapat disebabkan oleh ikatan antara asam dan polisakrida belum terikat secara sempurna. Menurut penelitian Guang et al. (2009) produksi bioflokulan dengan sampel TB-EBS menghasilkan efektivitas flokulasi yang lebih baik dibanding SB-EBS dan supernatan. Perbedaan TB-SB-EBS, SB-SB-EBS, dan supernatan adalah putaran sentrifugasinya yaitu 20 kHz, 5 000 g, dan 2 000 g. Berdasarkan penelitian tersebut, diketahui bahwa putaran sentrifugasi yang semakin tinggi akan membuat polisakarida terikat sempurna pada larutan asam yang disebut dengan TB-EBS (Tightly-Bond Extracellular Biopolymer Flocculant) dan hasil flokulasinya semakin tinggi. Penelitian Sun et al. (2012) juga menggunakan kecepatan sentrifugasi yang tinggi yaitu 8 000 rpm selama 15 menit dan menghasilkan efektivitas flokulasi mencapai 99.5%. Oleh karena itu efektivitas flokulasi dari metode crude bioflokulan dapat ditingkatkan dengan meningkatkan putaran sentrifugal saat pembuatan bioflokulan. Peningkatan kecepatan sentrifugasi menjadi 8 000 rpm dapat digunakan sebagai saran penelitian selanjutnya.
Efektivitas flokulasi dapat diteliti kembali untuk menghasilkan persentase flokulasi yang tinggi tetapi waktu dan biaya produksi adalah variabel yang dapat menjadi penentu metode terbaik. Maka metode B dipilih sebagai metode produksi bioflokulan terbaik. Selanjutnya pengujian dilakukan dengan menggunakan crude bioflokulan
Pengujian Efektivitas Flokulasi Air Sungai dan Air IPAL Dosis Koagulan
Koagulasi adalah proses yang biasa digunakan untuk menghilangkan pengotor pada pengolahan air. Koagulan yang paling umum digunakan adalah aluminium dan garam besi (Siregar 2005). Pada penelitian ini, koagulan digunakan untuk membantu bioflokulan mendestabilkan koloid. Koagulan yang ditambahkan diharapkan berikatan dengan larutan yang terdestabilisasi sehingga terbentuk gumpalan partikel yang lebih besar. Uji pendahuluan dilakukan untuk menentukan dosis koagulan pada air limbah. Koagulan yang digunakan adalah alum dan FeCl3. Alasan pemilihan jenis koagulan adalah karena koagulan tersebut memiliki valensi ion 3 sehingga kekuatan koagulasinya semakin baik. Menurut Siregar (2005) efektivitas koagulasi alum dan FeCl3 besar karena koagulan tersebut merupakan kation multivalen yang memiliki ion valensi lebih tinggi (+3) dibanding koagulan lainnya. Kemampuan Al3+ dan Fe3+dalam mengikat koloid-koloid bermuatan negatif dalam suspensi kaolin semakin besar karena sifat muatannya yang lebih positif sehingga terbentuklah gumpalan-gumpalan. Semakin besar gumpalan yang terbentuk berarti semakin besar pula flok dan bobot yang dihasilkan sehingga mempermudah pengendapan.
Setelah ditentukan jenis koagulan yang akan digunakan selanjutnya adalah menentukan dosis koagulan. Metode yang digunakan adalah dengan menggunakan metode jar test. Air limbah yang digunakan adalah air sungai yang
15 diambil disekitar kampus IPB Dramaga. Hasil jar test dari kedua koagulan dapat dilihat pada Gambar 5.
Gambar 5 Efektivitas koagulan pada air sungai
Berdasarkan gambar 5 diketahui bahwa dosis optimum untuk koagulan alum adalah 0.023 g/L air sungai. Hasil efektivitas koagulasi dari koagulan tersebut dapat mencapai 92.86%. Hal ini menandakan bahwa air sungai menjadi lebih jernih jika dicampurkan dengan koagulan alum. Penggunaan koagulan lebih dari 0.023 g/L tidak banyak berpengaruh terhadap efektivitas koagulasi. Sementara itu untuk koagulan FeCl3 dosis optimum untuk mengkoagulasi air sungai adalah sebesar 0.02 g/L air sungai. Diketahui pula saat dosis 0.033 g/L, efektivitas koagulasi menurun karena dosis yang berlebih. Dosis koagulan ini yang selanjutnya akan digunakan untuk menguji flokulasi air sungai dan air IPAL.
Air Sungai
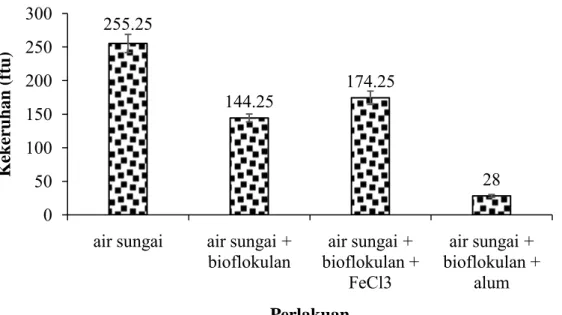
Air sungai yang digunakan pada penelitian ini diperoleh dari sungai di sekitar kampus IPB Dramaga. Air sungai berwarna coklat muda dan keruh. Kekeruhan air sungai menandakan bahwa air tersebut bersifat memendarkan cahaya. Pemendaran cahaya adalah sifat dari larutan tersuspensi koloid maka air sungai memerlukan pengolahan koagulasi-flokulasi. Hasil uji efektivitas flokulasi crude bioflokulan terhadap air sungai tertera pada Gambar 6. Pada Gambar 6 diketahui bahwa crude bioflokulan sendiri dapat menjernihkan air sungai dalam waktu 10 menit. Nilai kekeruhan air sungai yang awalnya 225 ftu, setelah ditambahkan bioflokulan kekeruhannya berkurang menjadi 144 ftu. Selanjutnya dilakukan uji pengaruh koagulan terhadap efektivitas flokulasi air sungai. Koagulan yang digunakan adalah alum dan FeCl3 dengan dosis sesuai yang telah diteliti sebelumnya. Nilai kekeruhan air sungai setelah dicampur dengan koagulan FeCl3 dan bioflokulan adalah 174 ftu. Sedangkan nilai kekeruhan air sungai yang ditambahkan koagulan alum dan bioflokulan nilai kekeruhannya berkurang cukup drastis selama 10 menit yaitu sebesar 28 ftu.
0 20 40 60 80 100 E fe k tivitas K oagu lasi ( % ) Dosis koagulan (g/L) Alum FeCl3
16
Gambar 6 Nilai kekeruhan air sungai
Persentase efektivitas flokulasi bioflokulan pada air sungai dapat dilihat pada Gambar 7. Efektivitas flokulasi bioflokulan saat digunakan pada air sungai persentasenya lebih rendah dibanding pada saat diuji dengan air standar (kaolin). Hal ini dapat disebabkan oleh kompleksitas komponen yang terkandung oleh air sungai. Hasil penambahan koagulan FeCl3 dan bioflokulan pada air sungai memperoleh efektivitas flokulasi sebesar 31.73%. Efektivitas flokulasi air sungai dengan penambahan koagulan FeCl3 lebih rendah dibanding hanya menggunakan bioflokulan saja. Hal ini dapat terjadi karena ketidaksesuaian jenis koagulan yang digunakan. Koagulan tersebut dapat menghambat atau menurunkan efektivitas flokulasi (Salehizadeh dan Yan 2014). Selain itu, koagulan FeCl3 mudah terionisasi, cairan koagulan mudah berikatan dengan senyawa lain seperti oksigen dan air sehingga menjadi berwarna coklat. Warna tersebut mempengaruhi warna air sungai menjadi lebih keruh. Efektivitas flokulasi air sungai yang diberi campuran alum dan bioflokulan memperoleh hasil sebesar 88.9%. Hasil ini membuktikan bahwa koagulan alum dapat membantu bioflokulan dalam pengendapan dan dapat membuat air sungai menjadi lebih jernih.
Gambar 7 Persentase efektivitas flokulasi air sungai 255.25 144.25 174.25 28 0 50 100 150 200 250 300
air sungai air sungai +
bioflokulan bioflokulan + air sungai + FeCl3 air sungai + bioflokulan + alum K ek er u h an (f tu) Perlakuan 43.49 31.73 88.9 0 20 40 60 80 100 air sungai +
bioflokulan bioflokulan + air sungai + FeCl3 air sungai + bioflokulan + alum E fe k tivitas F lok u lasi (% ) Perlakuan
17 Gambar 8 menunjukkan perbandingan efektivitas flokulasi antara campuran air sungai, koagulan, dan bioflokulan dengan air sungai dan koagulan saja. Percobaan ini bertujuan untuk mengetahui apakah pencampuran koagulan dan bioflokulan dapat lebih baik dibanding hanya ditambahkan koagulan. Berdasarkan hasil penelitian, diketahui bahwa penambahan bioflokulan pada air sungai yang dicampur koagulan FeCl3 menghasilkan air yang lebih jernih dibanding air sungai yang hanya ditambahkan koagulan FeCl3 saja. Bioflokulan dan FeCl3 yang ditambahkan ke air sungai, efektif memflokulasi sebanyak 39% lebih jernih dibanding hanya ditambahkan koagulan FeCl3. Koagulan alum juga mempunyai hasil serupa yaitu pencampuran koagulan alum dan bioflokulan dapat menghasilkan air sebesar 37% lebih jernih dibanding air sungai yang hanya dicampur koagulan alum saja. Hasil ini membuktikan bahwa bioflokulan membantu proses flokulasi dan koagulasi air sungai menjadi lebih baik.
Gambar 8 Pengaruh penambahan koagulan dan bioflokulan pada air sungai
Air IPAL
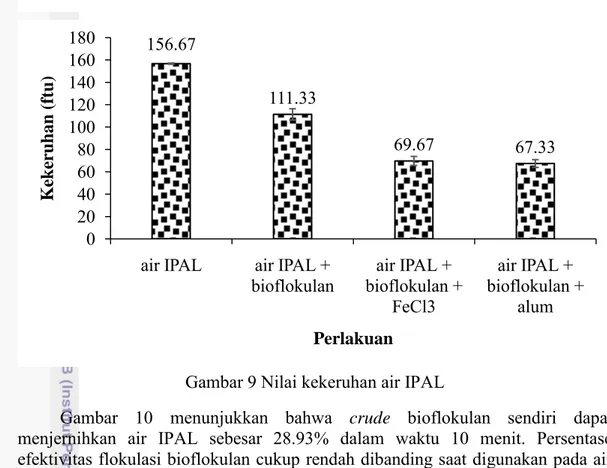
Selain air sungai, air limbah lain yang juga diuji kekeruhan dan efektivitas flokulasinya adalah air dari Instalasi Pengolahan Air Limbah (IPAL) sebuah industri. Industri tersebut adalah industri kecap PT. XXX, industri yang sama dengan tempat pengambilan sampel lumpur aktif industri untuk dijadikan bioflokulan pada penelitian ini. Air IPAL berwarna cokelat tua dengan banyak partikel didalamnya. Gambar 9 menunjukkan nilai kekeruhan air IPAL. Awal kekeruhannya adalah 156 ftu, setelah ditambahkan 3 ml bioflokulan nilai kekeruhannya berkurang menjadi 111 ftu. Selanjutnya dilakukan uji pengaruh penambahan koagulan. Uji tersebut menghasilkan bahwa koagulan FeCl3 dan alum dapat menjernihkan air IPAL sebesar 69 dan 67 ftu.
288 173 45 28 0 100 200 300 400 K ek er u h an (f tu) Perlakuan
air sungai+FeCl3 air sungai+bioflokulan+FeCl3 air sungai+alum air sungai+bioflokulan+alum
18
Gambar 9 Nilai kekeruhan air IPAL
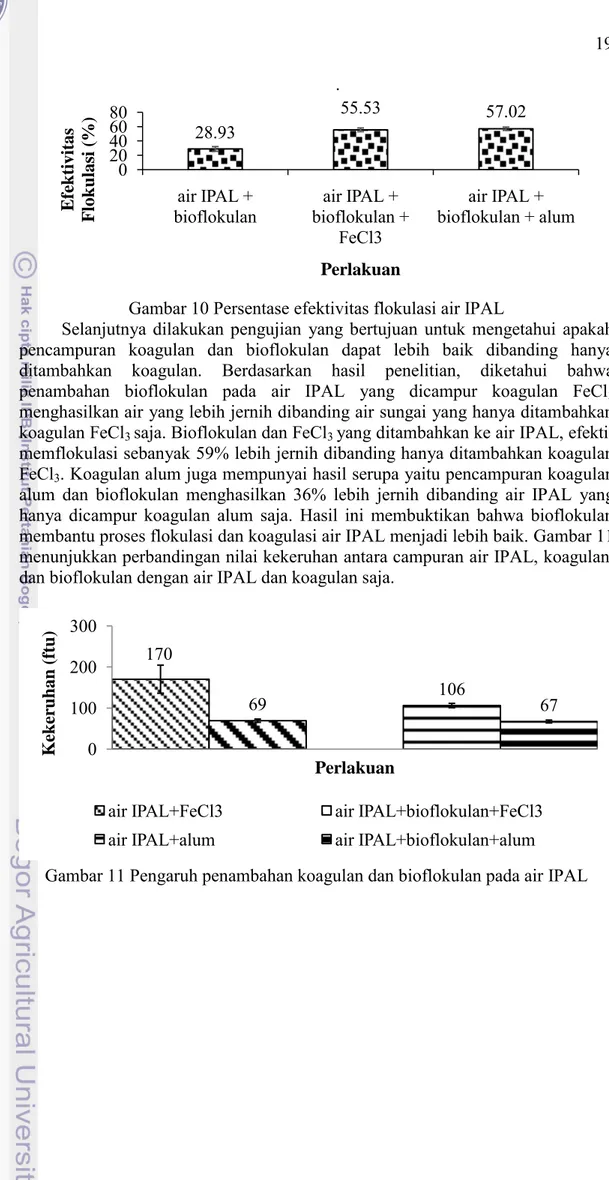
Gambar 10 menunjukkan bahwa crude bioflokulan sendiri dapat menjernihkan air IPAL sebesar 28.93% dalam waktu 10 menit. Persentase efektivitas flokulasi bioflokulan cukup rendah dibanding saat digunakan pada air sungai dan air kaolin. Hal ini membuktikan bahwa jenis air yang berbeda menghasilkan efektivitas flokulasi yang berbeda pula. Hasil uji efektivitas flokulasi crude bioflokulan terhadap air IPAL tertera pada Gambar 10.
Penambahan koagulan dilakukan untuk mengetahui pengaruh koagulan terhadap efektivitas flokulasi air IPAL. Koagulan yang digunakan tetap sama yaitu alum dan FeCl3 dengan dosis sesuai yang telah diteliti sebelumnya. Hasil penambahan koagulan FeCl3 dan bioflokulan pada air IPAL memperoleh efektivitas flokulasi sebesar 55% lebih jernih dibanding kontrol. Hal ini menunjukkan bahwa koagulan yang digunakan sesuai dan dapat membantu bioflokulan dalam menjernihkan air IPAL. Walaupun koagulan FeCl3 mudah terhidrolisis hingga cairan koagulan menjadi berwarna coklat, tetapi warna asli dari air IPAL hampir sama dengan cairan koagulan. Kontrol yang digunakan mempunyai warna yang mirip tetapi saat ditambahkan koagulan FeCl3, air IPAL menjadi lebih jernih sehingga nilai kekeruhan menjadi lebih rendah. Efektivitas flokulasi air IPAL yang diberi campuran alum dan bioflokulan memperoleh hasil sebesar 57% lebih jernih dibanding kontrol.
156.67 111.33 69.67 67.33 0 20 40 60 80 100 120 140 160 180
air IPAL air IPAL +
bioflokulan bioflokulan + air IPAL + FeCl3 air IPAL + bioflokulan + alum K ek er u h an (f tu) Perlakuan
19 .
Gambar 10 Persentase efektivitas flokulasi air IPAL
Selanjutnya dilakukan pengujian yang bertujuan untuk mengetahui apakah pencampuran koagulan dan bioflokulan dapat lebih baik dibanding hanya ditambahkan koagulan. Berdasarkan hasil penelitian, diketahui bahwa penambahan bioflokulan pada air IPAL yang dicampur koagulan FeCl3 menghasilkan air yang lebih jernih dibanding air sungai yang hanya ditambahkan koagulan FeCl3 saja. Bioflokulan dan FeCl3 yang ditambahkan ke air IPAL, efektif memflokulasi sebanyak 59% lebih jernih dibanding hanya ditambahkan koagulan FeCl3. Koagulan alum juga mempunyai hasil serupa yaitu pencampuran koagulan alum dan bioflokulan menghasilkan 36% lebih jernih dibanding air IPAL yang hanya dicampur koagulan alum saja. Hasil ini membuktikan bahwa bioflokulan membantu proses flokulasi dan koagulasi air IPAL menjadi lebih baik. Gambar 11 menunjukkan perbandingan nilai kekeruhan antara campuran air IPAL, koagulan, dan bioflokulan dengan air IPAL dan koagulan saja.
Gambar 11 Pengaruh penambahan koagulan dan bioflokulan pada air IPAL 28.93 55.53 57.02 0 20 40 60 80 air IPAL +
bioflokulan bioflokulan + air IPAL + FeCl3 air IPAL + bioflokulan + alum E fe k tivitas F lok u lasi (% ) Perlakuan 170 69 106 67 0 100 200 300 K ek er u h an (f tu) Perlakuan
air IPAL+FeCl3 air IPAL+bioflokulan+FeCl3 air IPAL+alum air IPAL+bioflokulan+alum
20
SIMPULAN DAN SARAN
Simpulan
Hasil analisis metode produksi bioflokulan berdasarkan efektivitas flokulasi, waktu produksi dan biaya produksi telah diketahui. Metode A (isolasi mikroorganisme) menghasilkan bioflokulan potensial yaitu isolat bakteri selulolitik CMC-1 yang memiliki efektivitas flokulasi sebesar 78.36%, lama waktu produksi 4 hari dan biaya produksi sebesar 217 480 rupiah. Metode B (sintesis polisakarida menggunakan asam) menghasilkan crude bioflokulan dengan efektivitas flokulasi 53.92%, lama waktu produksi 1 hari, dan biaya produksi 105 538 rupiah. Metode B terpilih karena faktor waktu produksi dan biaya produksi menjadi faktor utama dalam efisiensi pembuatan bioflokulan. Setelah diuji pada air sungai dan air IPAL diketahui bahwa crude bioflokulan dapat menjernihkan air sebesar 43% dan 29% dari kontrol. Penambahan koagulan dengan valensi (3+) yaitu alum dan FeCl3 dapat membantu bioflokulan dalam menjernihkan air.
Saran
Penelitian ini dapat memberikan hasil bahwa metode produksi bioflokulan yang lebih mudah dan terjangkau adalah dengan pembuatan crude bioflokulan. Metode terpilih masih menghasilkan efektivitas flokulasi yang lebih rendah dari metode tandingannya. Oleh karena itu perlu dilakukan peningkatan kecepatan sentrifugasi menjadi 8 000 rpm. Peningkatan kecepatan sentrifugasi diharapkan dapat menghasilkan proses flokulasi yang lebih jernih sehingga efektivitas flokulasinya meningkat.
DAFTAR PUSTAKA
Bezawada J, Hoang NV, More TT, Yan S, Tyagi N, Tyagi RD, Surampalli RY. 2013. Production of Extracellular Polymeric Subtances (EPS) by Serratia sp.using Wastewater Sludge as Raw Material and Flocculation Activity of the EPS Produced. J Environm Man. 128:83-91
Crittenden JC, Trussel RR, Hand DW, Howe KJ, Tchobanoglous G. 2012. Water Treatment: Principles and Design (Third Ed.). United States of America : John Wiley & Sons, Inc.
Davis ML. 2010. Water and Wastewater Engineering – Design Principles and Practice (Profesional Ed.). United States of America : McGraw-Hill Companies, Inc.
Gao et al.. 2006. Characterization of a bioflocculant from a newly isolated Vagococcus sp. W31. J Zheijiang Univ Sci. 7(3):186-192
Guang HY, Pin JH, Li MS. 2009. Characteristics of extracellular polymeric substances (EPS) fractions from excess sludge and their effects on bioflocculability. J Bioresour Technol. 100:3193-3198
21 Lauda RD. 2013. Stabilisasi Sludge dari Instalasi Pengolahan Air Limbah (IPAL) menggunakan Starter Bakteri Indigenous pada Aerobic Sludge Digester [skripsi]. Bogor (ID) : Institut Pertanian Bogor
Lu WY, Zhang T, Zhang DY, Li CH, Wen JP, Du LX. 2005. A novel bioflocculant produced by Enterobacter aerogenes and its use in defecating the trona suspension. J Biochem Engin 27:1-7
Nohata Y, Kurane. 1994. Culture condition for production and purification of bioabsorbent from Alcaligenes B-16. J Ferment Bioengin. 77(4):390-393 Nwodo UU, Green E, Mabinya LV, Okaiyeto K, Rumbold K, Obi LC. 2014.
Bioflocculant production by a consortium of Streptomyces and Cellulomonas species and media optimization via surface response model. JCSBB. 116:257–64.
Parwono A. 1998. Uji kemampuan flokulasi dan kajian aktivitas flokulasi isolat bakteri potensial penghasil bioflokulan pada suspensi kaolin [skripsi]. Bogor (ID) : Institut Pertanian Bogor
Purnama D. 2007. Isolasi dan Optimasi Flokulasi Mikrob Potensial Penghasil Bioflokulan dari Lumpur Aktif Industri [skripsi]. Bogor (ID) : Institut Pertanian Bogor
Salehizadeh H, Shakaosadati SA. 2001. Extracellular Biopolymeric Flocculant: recent trends and biotechnological importance. J Biotechnol Adv. 19: 371-385
Salehizadeh H, Yan N. 2014. Recent advance in Extracellular Biopolymer Flocculants. J Biotechnol Adv. 32:1506-1522
Siregar SA. 2005. Instalasi Pengolahan Air Limbah. Yogyakarta: Kanisius
Sun J, Zhang X, Miao X, Zhou J. 2012. Preparations and Characteristics of Bioflocculant from Excess Biological Sludge. J Bioresour Technol. 126:362-366
Susanti HE. 2007. Isolasi dan Optimasi Flokulasi Bakteri Penghasil Bioflokulan dari Sumber Perairan di Daerah Bogor [skripsi]. Bogor (ID) : Institut Pertanian Bogor
Yim JH, Kim SJ, Ahn SH, Lee HK. 2007. Characterization of a novel bioflocculant p-KG03 from a marine dinoflagellate Gyrodinium impudicum KG03. J Bioresour Technol. 98:361-367
Wang Z, Wang KXY, Yao Y. 1995. Studies on Bioflocculant-Producing Microorganisms. J Saf Env. 70:53-62
22
LAMPIRAN
Lampiran 1. Efektivitas flokulasi isolat mikroba dari lumpur aktif industri
Kode
Kekeruhan (ftu)
Rata-Rata
(ftu) Standar Deviasi
Efektivitas Flokulasi (%) 1 2 3 Kontrol 288 256 260 268 17 - NA-1 229 205 226 220 13 17.91 NA-2 136 166 177 160 21 40.42 NA-3 221 355 260 279 69 -3.98 SA-1 280 226 294 267 36 0.50 SA-2 92 143 187 141 48 47.51 SA-3 244 275 203 241 36 10.20 SA-4 95 90 79 88 8 67.16 SA-5 160 173 172 168 7 37.19 SM-1 222 228 258 236 19 11.94 SM-2 252 349 460 354 104 -31.97 SM-3 323 280 323 309 25 -15.17 CMC-1 42 58 74 58 16 78.36 CMC-2 156 176 157 163 11 39.18 CMC-3 288 254 309 284 28 -5.85
23 Lampiran 2 Nilai kekeruhan dan efektivitas flokulasi kaolin
a. Nilai kekeruhan kaolin
Perlakuan Kekeruhan (ftu) Rata-rata
(ftu) Standar deviasi (ftu) 1 2 3 4 5 6 Kaolin 163 161 173 165.67 6.42 Kaolin + bioflokulan 75 80 78 76 78 71 76.33 3.14 Kaolin + bioflokulan + FeCl3 135 137 119 120 127 134 128.67 7.86 Kaolin + bioflokulan + alum 89 88 86 81 85 85 85.67 2.81
b. Persentase efektivitas flokulasi kaolin
Perlakuan Efektivitas Flokulasi (%) Rata-rata
(%) Standar deviasi (%) 1 2 3 4 5 6 Kaolin + bioflokulan 54.72 51.71 52.91 54.12 52.91 57.14 53.92 1.17 Kaolin + bioflokulan + FeCl3 18.51 17.30 28.16 27.56 23.34 19.11 22.97 5.01 Kaolin + bioflokulan + alum 46.27 46.88 48.08 51.10 48.69 48.69 48.21 1.88
24 Lampiran 3 Perbandingan rincian biaya produksi bioflokulan
a. Biaya pembuatan bioflokulan dengan cara isolasi mikroorganisme
Komponen Unit Harga (Rp) Jumlah (Rp)
Investasi
Inkubator 1 buah 15 000 000 15 000 000
Ose 2 buah 10 000 20 000
Bunsen 1 buah 30 000 30 000
Timbangan Analitik 1 buah 3 000 000 3 000 000
Autoclave 1 buah 40 000 000 40 000 000
Rotary Shaker 2 buah 13 000 000 26 000 000
Kultur isolat CMC-1 1 kultur 2 000 000 2 000 000
Total 86 050 000
Biaya Operasional
Kapas 1 buah 30 000 / buah 30 000
Alumium Foil 1 buah 20 000 / buah 20 000
Alkohol 70% 100 ml 5 400 / 100 ml 5 400 Spiritus 100 ml 6 000 / L 600 CMC Powder 2 g 70 000 / kg 140 Glukosa 100 g 78 000 / kg 7 800 Sukrosa 100 g 32 500 / kg 3 250 Ekstrak Khamir 5 g 1 989 000 / 500 g 19 890 Pepton 5 g 910 000 / 500 g 9 100 Urea 5 g 1 352 000 / 500 g 13 520 MgSO4 2 g 9 100 / g 18 200 KH2PO4 50 g 58 500 / kg 2 925 (NH4)2SO4 5 g 19 500 / 500 g 195 FeCl3 50 g 30 000 / kg 1 500 NaCl 1 g 39 000 / 500 g 78 Aquades 10 L 1 300 / L 13 000
Gaji Operator 1 orang 65 000 / orang 65 000
Pemakaian Inkubator 1 buah 5.76 kWh x Rp 796 4 584.96 Pemakaian Autoclave 1 buah 0.45 kWh x Rp 796 358.2 Pemakaian Rotary Shaker 2 buah 1.2 kWh x 2 x Rp 796 1 910.4
Adapter Neraca 1 buah 0.035 kWh x Rp 796 27.86
Total 217 479.42
Penyusutan Investasi 102 440
25
b. Biaya pembuatan bioflokulan dengan cara penghancuran dengan asam
Komponen Unit Harga (Rp) Jumlah (Rp)
Investasi
Sentrifugasi 1 buah 40 000 000 40 000 000
pH meter 1 buah 430 000 430 000
Stirer 1 buah 6 000 000 6 000 000
Timbangan Analitik 1 buah 3 000 000 3 000 000
Total 49 430 000
Biaya Operasional
NaOH 4% 400 g 23 400 / kg 9 360
HCl 18% 500 ml 32 500 / L 16 250
Aquades 10.5 L 1 300 / L 13 650
Gaji Operator 1 orang 65 000 / orang 65 000
Pemakaian Sentrifugasi 1 buah 1.54 kWh x Rp 796 1 225.84 Pemakaian Stirrer 1 buah 0.03 kWh x Rp 796 23.88
Adapter Neraca 1 buah 0.035 kWh x Rp 796 27.86
Total 105 538
Penyusutan Investasi 13 730
Total 119 268
c. Biaya bioflokulan untuk 1 Liter air limbah Metode isolasi CMC-1 adalah 31 992/L maka
= 31 992/L
= 31.992/mL x 10 mL = Rp 320 /L air limbah
Metode isolasi CMC-1 adalah 31 992/L maka = 3 975/L
= 3.975/mL x 30 mL = Rp 120 /L air limbah
26 Lampiran 4. Dosis koagulan untuk air sungai
1. Koagulan alum Dosis
Alum (g/L)
Kekeruhan (ftu) Rata-Rata (ftu) SD Efektivitas Koagulasi (%) 1 2 3 Kontrol 24 32 28 28.00 4.00 - 0.006 17 16 17 16.67 0.58 40.48 0.01 15 17 13 15.00 2.00 46.43 0.013 14 13 10 12.33 2.08 55.95 0.016 4 7 5 5.33 1.53 80.95 0.02 4 2 3 3.00 1.00 89.29 0.023 1 2 3 2.00 1.00 92.86 0.026 1 2 2 1.67 0.58 94.05 0.03 2 1 1 1.33 0.58 95.24 0.033 1 1 2 1.33 0.58 95.24 2. Koagulan FeCl3 Dosis FeCl3 (g/L) 1 2 3 Rata-Rata (ftu) SD Efektivitas Koagulasi (%) Kontrol 32 23 28 27.67 4.51 - 0.006 17 16 15 16 1.00 42.17 0.01 15 12 13 13.33 1.53 51.81 0.013 6 8 9 7.67 1.53 72.29 0.016 3 4 6 4.33 1.53 84.34 0.02 3 2 3 2.67 0.58 90.36 0.023 3 2 2 2.33 0.58 91.57 0.026 2 2 1 1.67 0.58 93.98 0.03 2 1 1 1.33 0.58 95.18 0.033 5 12 8 8.33 3.51 69.88
27 Lampiran 5 Nilai kekeruhan dan efektivitas flokulasi air
1. Air Sungai
c. Nilai kekeruhan air sungai
Perlakuan Kekeruhan (ftu) Rata-rata (ftu) Standar deviasi (ftu)
1 2 3 4
air sungai 261 249 271 240 255.25 13.57
air sungai + bioflokulan 142 138 152 145 144.25 5.91 air sungai + bioflokulan + FeCl3 186 172 162 177 174.25 10.01 air sungai + bioflokulan + alum 28 31 26 27 28.00 2.16
d. Persentase efektivitas flokulasi air sungai
Perlakuan Efektivitas Flokulasi (%) Rata-rata (%)
Standar deviasi
(%)
1 2 3 4
air sungai + bioflokulan 44.37 45.94 40.45 43.19 43.49 2.31 air sungai + bioflokulan + FeCl3 27.13 32.62 36.53 30.66 31.73 3.40 air sungai + bioflokulan + alum 89.03 87.86 89.81 89.42 88.90 0.99
2. Air IPAL
a. Nilai kekeruhan air IPAL
Perlakuan Kekeruhan (ftu) Rata-rata (ftu) Standar deviasi (ftu)
1 2 3
air IPAL 157 157 156 156.67 0.57
air IPAL + bioflokulan 116 106 112 111.33 5.03 air IPAL + bioflokulan + FeCl3 66 69 74 69.67 4.04 air IPAL + bioflokulan + alum 67 71 64 67.33 3.51 b. Persentase efektivitas flokulasi air IPAL
Perlakuan Efektivitas Flokulasi (%) Rata-rata (%) Standar deviasi (%)
1 2 3
air IPAL + bioflokulan 25.95 32.34 28.51 28.93 3.21 air IPAL + bioflokulan + FeCl3 57.87 55.95 52.76 55.53 2.57 air IPAL + bioflokulan + alum 57.23 54.68 59.14 57.02 2.24
28
Lampiran 6 Perbandingan flokulasi air berkoagulan dengan dan tanpa bioflokulan 1. Air Sungai
Perlakuan Kekeruhan (ftu) Rata-rata (ftu) Standar deviasi (ftu)
1 2 3 4
air sungai + FeCl3 284 283 297 288 288.00 6.38 air sungai + bioflokulan + FeCl3 186 172 162 177 174.25 10.01
air sungai + alum 48 45 42 45 45.00 2.45
air sungai + bioflokulan + alum 28 31 26 27 28.00 2.16
2. Air IPAL
Perlakuan Kekeruhan (ftu) Rata-rata (ftu) Standar deviasi (ftu)
1 2 3
air IPAL + FeCl3 132 183 197 170.67 34.21
air IPAL + bioflokulan + FeCl3 66 69 74 69.67 4.04
air IPAL + alum 112 102 104 106 5.29
29
RIWAYAT HIDUP
Penulis bernama Wenny Ayunisa dilahirkan di Jakarta pada tanggal 8 Oktober 1992 dari ayah Yuliarto S.Sos dan ibu Novri Yenni. Penulis merupakan anak pertama dari tiga bersaudara. Pendidikan formal ditempuh dari Taman Kanak-Kanak Alodia, SDN Pejuang VII dan SLTP N 19 Bekasi. Pada tahun 2010 penulis menamatkan pendidikan SMA di SMA Negeri 4 Bekasi. Kemudia pada tahun yang sama diterima di IPB melalui jalur USMI (Undangan Seleksi Masuk IPB) dengan program studi Teknologi Industri Pertanian, Fakultas Teknologi Pertanian.
Selama mengikuti perkuliahan, penulis aktif berpartisipasi dalam kepanitiaan beberapa acara, seperti Fateta Annual English Competition (FALCON) 2011, Techno-F 2012, Hari Warga Industri 2012, Sekretaris Reds Cup 2012, dan Sekretaris To Get Himalogin Better (TOGETHER) 2013.
Penulis melaksanakan Praktik Lapangan pada tahun 2013 di PT. Goodyear Indonesia Tbk, Bogor, Jawa Barat dengan tema “Uraian Proses Produksi dan Analisis Jaminan Kualitas melalui Audit Harian pada Industri Ban PT Goodyear Indonesia Tbk”. Selanjutnya pada tahun 2014 penulis melaksanakan penelitian dengan judul “Produksi Bioflokulan dari Lumpur Aktif Industri untuk Air Sungai dan Air Limbah Industri” di bawah bimbingan Prof Dr Ing Ir Suprihatin.