III
BAHAN DAN METODE PENELITIAN
3.1 Bahan dan Alat Penelitian 3.1.1 Bahan Penelitian
Bahan yang digunakan dalam penelitian pengomposan adalah sebagai berikut:
1. Feses sapi perah 12,24 kg 2. Jerami padi 36,5 kg 3. Air 152,36 liter
Bahan yang digunakan untuk analisis nisbah C/N adalah sebagai berikut: 1. 1 gram sampel campuran feses sapi perah dan jerami padi
2. 11,5 mL H2SO4 pekat 3. 5 mL K2CrO4-2 1N 4. 20 mL NaOH 40% 5. 50 mL HCl 0,01N 6. Aquades
7. 1 gram katalis (Selenium Mixture) 8. 5 mL asam borat 2%
9. 3 tetes indikator
Bahan yang digunakan dalam penelitian analisis N, P, dan K adalah sebagai berikut:
1. Analisis N Total
a. 1 mL larutan sampel pupuk organik cair b. H2SO4 0,0479 N
c. Aquades d. Asam borat 2% e. NaOH 40% f. HCl 25% 2. Analisis P2O5
a. 0,5 mL sampel pupuk organik cair b. Aquades
c. Reagent P 3. Analisis K2O
a. 1 mL sampel pupuk organik cair b. Aquades
c. HNO3 5 mL d. HClO4 0,5 mL 3.1.2 Alat Penelitian
Peralatan yang digunakan dalam penelitian dekomposisi ini adalah sebagai berikut:
1. Timbangan kapasitas 10 kg dengan ketelitian 0,05 kg untuk menimbang bahan dekomposisi.
2. Karung plastik sebanyak 18 buah.
3. Penutup untuk inkubasi padat dengan diameter 45 cm.
4. Thermometer alkohol untuk mengukur suhu fermentasi padat.
5. Bak plastik sebanyak 18 buah dengan ukuran panjang 30 cm; lebar 20 cm; dan tinggi 10 cm untuk proses fermentasi cair.
6. Saringan untuk memisahkan padatan (filtrat) dan cairan (ekstrak). 7. Aerator yang digunakan untuk aerasi cairan hasil ekstraksi.
Peralatan yang digunakan untuk analisis nisbah C/N adalah sebagai berikut: 1. Labu ukur 100 mL 2. Kjehdahltherm 3. Penangas air 4. Stirrer magnetik 5. Botol semprot 6. Kertas lakmus 7. Kertas saring berabu 8. Spektrofotometer 9. Labu Kjehdahl 100 mL 10. Neraca analitik 11. Alat destruksi 12. Erlenmeyer 250 mL 13. Buret 50 mL
Peralatan yang digunakan dalam penelitian uji N, P, dan K ini adalah sebagai berikut:
1. Labu Kjehdahl 2. Kjehdahltherm 3. Bunsen
4. Pipet ukur volume 5 mL 5. Labu Erlenmeyer
6. Timbangan analitik kapasitas 300 gr dengan ketelitian 0,005 gr 7. Labu ukur 25 mL
8. Spektrofotometer tipe Genesys 20
3.2 Metode Penelitian
Penelitian ini dilakukan secara eksperimental dengan Rancangan Acak Lengkap (RAL) dengan tiga macam perlakuan dan masing-masing pengulangan sebanyak enam kali, sehingga diperoleh 18 sampel perlakuan. Ketiga perlakuan tersebut adalah:
T1 = campuran feses sapi perah dan jerami padi dengan nisbah C/N 25 T2 = campuran feses sapi perah dan jerami padi dengan nisbah C/N 30 T3 = campuran feses sapi perah dan jerami padi dengan nisbah C/N 35
Untuk menguji pengaruh antar perlakuan dilakukan analisis sidik ragam. Untuk mengetahui perbedaan antar perlakuan dilakukan dengan Uji Jarak Berganda Duncan. Model matematik yang digunakan adalah:
Yij= µ + 𝜶i + 𝜺ij
Dimana:
Yij : Variabel yang diamati µ : Rataan Umum
𝛼I : Pengaruh perlakuann (i= 1,2,3)
𝜀ij : Pengaruh pengacakan pada perlakuan ke I ulangan ke j (j= 1,2,3,4,5,6)
Asumsi:
1. Nilai 𝜺ij menyebar normal dan bebas satu sama lain 2. Nilai harapan dari 𝜀ij = 0
Hipotesis yang diamati adalah sebagai berikut:
𝐻0 : T1 = T2 = T3; perlakuan tidak berpengaruh nyata terhadap respon yang diamati.
𝐻1 : T1 ≠ T2 ≠ T3; perlakuan berpengaruh nyata terhadap respon yang diamati.
Hasil pengaruh antar perlakuan dapat dilihat dalam table sidik ragam. Tabel 1. Sidik Ragam
Sumber
Keragaman DB JK KT Fhit Ftabel0,05
Perlakuan (P) (t-1) = 2 JKP KTP
KTP/KTG Galat (G) t(r-1) = 15 JKG KTG
Total (tr-1) = 17 JKT
Kaidah keputusan:
1. Apabila 𝐹ℎ𝑖𝑡 ≤ Ttab 0,05, maka perlakuan tidak berpengaruh nyata (non signifikan), terima 𝐻0
2. Apabila 𝐹ℎ𝑖𝑡 > Ttab 0,05, maka perlakuan berpengaruh nyata (signifikan), tolak
𝐻0
Untuk menguji tingkat perbedaan setiap perlakuan nisbah C/N maka dilakukan Uji Jarak Berganda Duncan:
Sẍ = √𝑲𝑻 𝑮𝒂𝒍𝒂𝒕𝒓 LSRa = SSRa . S 𝐗̅
Keterangan:
S X̅ : Galat Baku
KT Galat : Kuadrat Tengah Galat r : Ulangan
LSRa : Jarak beda nyata terkecil (Least Significant Range)
SSRa : Studentized Significant Range
Apabila selisih antara perlakuan (d) dibandingkan dengan LSRa , kaidah keputusannya adalah sebagai berikut:
1. Bila d ≤ LSRa : Tidak berbeda nyata 2. Bila d > LSRa : Berbeda nyata
d adalah selisis rata-rata perlakuan
Tata letak percobaan dapat dilihat pada ilustrasi 1. 1 T2 2 T3 3 T1 4 T1 5 T1 6 T2 7 T3 8 T3 9 T1 10 T1 11 T1 12 T2 13 T3 14 T3 15 T2 16 T2 17 T2 18 T3 Ilustrasi 1. Tataletak Percobaan
Keterangan:
T1: Perlakuan nisbah C/N 25 antara feses sapi perah dan jerami padi (r; 1,2,3,4,5,6) T2: Perlakuan nisbah C/N 30 antara feses sapi perah dan jerami padi (r; 1,2,3,4,5,6) T3: Perlakuan nisbah C/N 35 antara feses sapi perah dan jerami padi (r; 1,2,3,4,5,6)
3.3 Prosedur Penelitian 3.3.1 Persiapan Penelitian
Persiapan penelitian adalah sebagai berikut:
1. Mengumpulkan feses sapi perah dan jerami padi 2. Menyiapkan alat dan bahan
3. Analisis kandungan nisbah C/N feses sapi perah dan jerami padi a. Analisis C total dengan metode Walkley and Black.
- Menimbang 0,5 gram feses sapi perah dan jerami padi yang dipotong halus 0,5mm, kemudian masukkan ke dalam tabung reaksi/labu ukur 100ml.
- Memasukkan 7,5 ml H2SO4 pekat, kemudian menambahakan 5 ml K2CrO4−2 IN.
- Memanaskan campuran tersebut dengan penangas air mendidih selama 1,5 jam atau dapat juga dengan menggunakan stirrer magnetic.
- Mendinginkan dan mengencerkan dengan air suling menjadi 100 ml atau sampai tanda batas kemudian kocok.
- Membiarkan sampai jernih lalu menyaring dengan menggunakan kertas saring.
- Mengukur dengan alat kalorimetri dengan panjang gelombang 561 mm, sebagai pembanding gunakan deret standar dengan kepekatan antara 0-250 ppm C.
- Mencatat hasil pembacaan trasmittance (T) pada alat lembaran data, kemudian mengkonversikan kembali absorbance (A).
Membuat kurva baku berdasarkan kepekaan C glukosa baku dari 0-250 ppm C.
- Menghitung kadar C – organic, contoh: %C + (X-kurva) / (gram contoh)x 100% = Dimana A = -log% T/100
% bahan organic (KU) = 1,72 x C-organik (KU) % bahan organic (KM) = % BO (KU) x F KA
Keterangan: x kurva (mg) dicari dengan menggunakan persamaan regresi.
b. Analisis kandungan N total dengan metode kjeldahl (Titrasi). - Menimbang 0,5 gram sampel yang telah dihaluskan dan
memasukkan sampel ke dalam labu kjeldahl 100 ml. - Menambahkan 1 gram katalis, 4 ml H2SO4 lalu dikocok.
- Kemudian memanaskan dengan api kecil selama ± 2 menit (timbul warna hitam), pemanas dilanjutkan dengan memperbesar api sedikit demi sedikit, dan mendestruksi sampai jernih.
- Mendinginkan labu kjeldahl, menambahkan 15 ml aquades setelah labu kjehldahl dingin.
- Pipet 5 ml asam borat 2% yang telah mengandung indikator ke dalam labu Erlenmeyer 100 ml kemudian menempatkannya untuk menampung hasil destruksi.
- Memasang Labu Kjeldahl yang berisi hasil destruksi pada alat destilasi.
- Menambahkan 20 ml NaOH 40% pada labu kjeldahl secara hati-hati kemudian menghubungkan dengan alat destilasi.
- Destilasi sampai NH3 habis (memeriksa dengan kertas lakmus) - Membilas alat destilasi kemudian membilas larutan di dalam
labu Erlenmeyer.
- Menitrasi dengan H2SO4 0,0479 N sampai berubah warna menjadi kemerahan.
4. Hitungan perbandingan feses sapi perah dan jerami padi dengan nisbah C/N perlakuan yang diinginkan (25, 30, 35)
a. Perhitungan C/N
Untuk menentukan komposisi cairan yang dibutuhkan, maka dilakukan dengan rumus sebagai berikut:
C/N = C feses+C jerami N feses+N Jerami Keterangan:
C/N = Nisbah C/N bahan campuran yang diinginkan 25, 30, 35 Cfeses = % kandungan C feses sapi perah
Cjerami = %kandungan jerami padi
NFeses = %kandungan N total feses sapi perah NJerami = % kandungan N total jerami padi
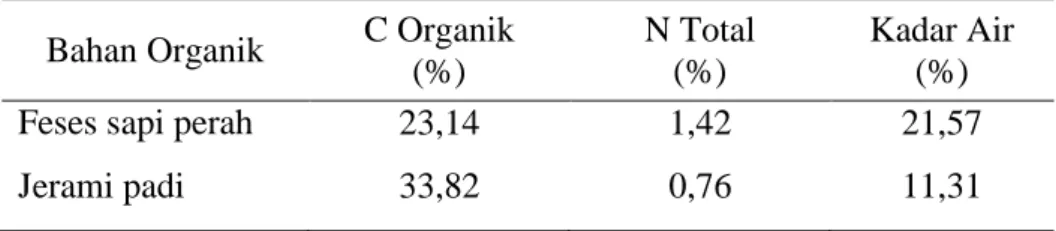
Tabel 2. Komposisi C dan N Feses Sapi Perah dan Jerami Padi Bahan Organik C Organik
(%)
N Total (%)
Kadar Air (%)
Feses sapi perah 23,14 1,42 21,57
Contoh perhtungan nisbah C/N 25 dan kadar air: 1) 𝐶/𝑁 =%𝑁1+%𝑁2%𝐶1+%𝐶2 2) 25 = 23,14𝑆+33,82𝐽1,42𝑆+0,76𝐽 3) 25(1,42S + 0,76J) = (23,14S + 33,82J) 4) 35,5S + 19J = 23,14S + 33,82J 5) 35,5S-23,14S = 33,82J – 19J 6) 12,36S =14,82J 7) Jika J = 1 kg, maka: 12,36S = 14,82(1) 12,36S = 14,82 S=14,8212,36 S= 1,2 kg
Jadi, untuk setiap 1,2 kg feses sapi perah dibutuhkan 1 kg jerami. Penambahan Air
1) Kadar Air Campuran (KAC) Kadar Air (KA) C/N 25: Jerami = 1 kg 15% x 1 = 0,15 kg
Feses sapi perah = 1,2 kg + 85% x 1,2 = 1,02 kg +
2,2 kg 1,17 kg 𝐾𝐴𝐶(25) =1,17 2,2 𝑥 100% 𝐾𝐴𝐶(25) = 53,2% 2) Penambahan Air (x): 1,17 + 𝑥 2,2 + 𝑥 = 60 100 100 ( 1,17 + 𝑥) = 60( 2,2 + 𝑥) 117 + 100𝑥 = 130,2 + 60𝑥 130,2 − 117 = 100𝑥 − 60𝑥
13,2 = 40𝑥 𝑥 = 13,2
40 𝑥 = 0,33 𝑘𝑔
Jadi, penambahan air pada campuran feses sapi perah dan jerami untuk nisbah C/N 25 adalah 0,33 kg, nisbah C/N 30 0,78 kg, dan nisbah C/N 35 0,95 kg.
Tabel 3. Campuran Bahan Penelitian Nisbah C/N Feses Sapi Perah (kg) Jerami Padi (kg) Penambahan Air (kg) 25 1,2 1 0,33 30 0,57 1 0,78 35 0,27 1 0,95 3.3.2 Pelaksanaan Penelitian
Pelaksanaan penelitian adalah sebagai berikut:
1. Menimbang feses sapi perah dan jerami padi sesuai dengan hasil perhitungan perbandingan bahan sesuai nisbah C/N perlakuan.
2. Mencampurkan kedua bahan, kemudian menambahkan air sesuai hasil perhitungan dan mengaduk sampai rata.
3. Menyusun hasil campuran bahan ke dalam karung. 4. Menginkubasi padat bahan secara aerob selama 14 hari.
5. Mengeringkan substrat hasil dekomposisi padat sampai kadar airnya <15%.
6. Melakukan proses ekstraksi dan filtrasi. Hasil filtrasi yaitu filtrate dan padatan.
7. Mengomposkan filtrat selama 14 hari. 8. Menganalisis kandungan N, P, dan K.
- Mengambil sampel sebanyak 1 mL menggunakan pipet dan memasukkannya ke dalam labu Kjehdahl 100 mL.
- Menambahkan 1 g katalis, 4 mL H2SO4, kemudian mengocoknya.
- Memanaskan campuran tersebut dengan api kecil selama dua menit atau sampai muncul warna kehitaman, lalu memperbesar api sedikit demi sedikit, dan mendestruksi sampai jernih. - Mendinginkan labu Kjehdahl, setelah dingin, menambahkan
aquadest sebanyak 15 mL.
- Mengambil 5 mL asam borat 2% yang telah mengandung indikator dan memasukkan ke labu erlenmeyer 100 mL kemudian ditempatkan untuk menampung hasil destruksi. - Memasang labu Kjehdahl yang berisi hasil destruksi pada alat
destilasi.
- Menambahkan 20 mL NaOH 40% secara hati-hati kemudian menghubungkan dengan alat destilasi.
- Destilasi sampai NH3 habis (memeriksanya dengan kertas lakmus).
- Membilas alat destilasi dan larutan di labu erlenmeyer. - Mentitrasi dengan H2SO4 0,0479 N sampai berubah warna. - Perhitungan N:
% N = (mL HCl x N HCl x 14) / 9 g tanah x 1000) x 100 = % N kering mutlak
= % N x faktor kadar air
b. Analisis kandungan P2O5 dengan menggunakan metode Spektrofotometri
- Memasukkan 0,5 mL sampel ke dalam labu ukur 25 mL, kemudian mengencerkannya sampai tanda batas dan mengocok sampai homogen.
- Mengambil 5 mL larutan dari labu erlenmeyer dan memasukkan ke dalam tabung reaksi, menambahkan 5 mL reagent P (asam vanadate molibdat), mengocok sebentar dan diamkan selama 15 menit.
- Membaca intensitasnya pada panjang gelombang 600 nm (%T) dengan spektrofotoneter tipr Genesys 20. 0,5; 1; 2; 4; 6; 8 ppm P2O5 ke dalam tabung reaksi. Mencatat hasil pengukurannya.
- Perhitungan P:
P2O5 potensial dalam tanah (mg/10 g) (KU) = 100/3 x 12,5/1000 x ppm dalam larutan P2O5 potensial dalam tanah (mg/100 g) (KM) = P2O5 potensial (KU) x KFA
c. Analisis kandungan K2O dengan menggunakan metode Spektrofotometri
- Memasukkan 1 mL sampel ke dalam labu Kjehdahl, menambahkan asam nitrat (HNO3) 5 mL dan asam perklorat (HClO4) 0,5 mL.
- Melakukan proses destruksi dengan Kjehdahltherm suhu 700oC sampai uap putih hilang.
- Mengencerkan sampel yang telah didestruksi dengan volume pengenceran 100 mL dan homogenkan.
- Menganalisis kandungan K menggunakan Automatic Absorption Spectrometer tipe AA240FS, dengan deret standar 0 – 10 ppm K, 0 – 20 ppm K, 0 – 40 ppm K, 0 – 80 ppm K, dan 0 – 100 ppm K, sebagai pembanding.
- Perhitungan K:
Mg K2O potensial per 100 g tanah (KU) = 100/5 x 25/1 x 12,5/1000 x ppm K2O potensial (mg/100 g) (KM) = k2o potensial (KU).
POC
Filtrat
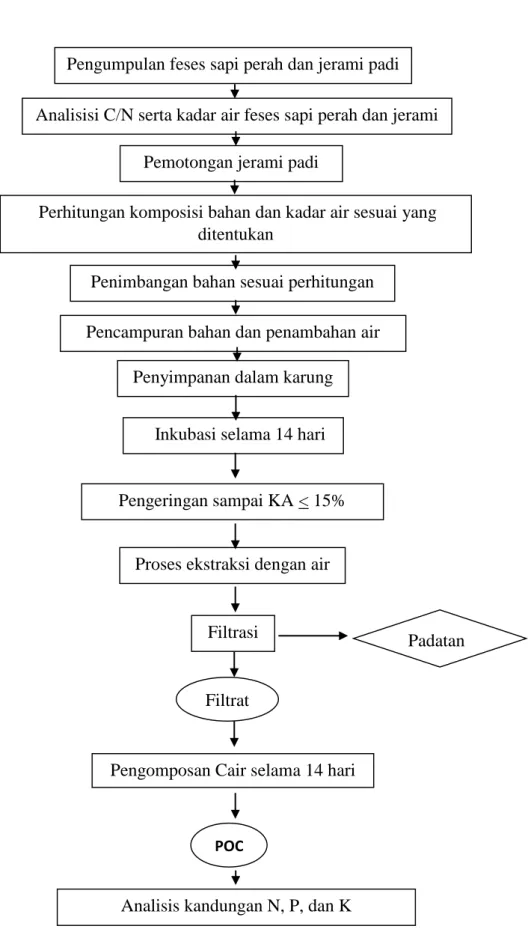
Ilustrasi 2. Diagram Alir Proses Pembuatan Pupuk Organik Cair Pengumpulan feses sapi perah dan jerami padi
Analisisi C/N serta kadar air feses sapi perah dan jerami padi
Pemotongan jerami padi
Perhitungan komposisi bahan dan kadar air sesuai yang ditentukan
Penimbangan bahan sesuai perhitungan Pencampuran bahan dan penambahan air
Inkubasi selama 14 hari
Pengeringan sampai KA < 15%
Proses ekstraksi dengan air
Filtrasi Filtrasi
Pengomposan Cair selama 14 hari
Analisis kandungan N, P, dan K
Padatan Penyimpanan dalam karung
3.4 Peubah yang Diamati
Peubah yang diamati dalam penelitian ini adalah sebagai berikut: 1. Kandungan N pupuk organik cair
2. Kandungan P pupuk organik cair 3. Kandungan K pupuk organik cair