i
PERBANDINGAN SIFAT FISIS BEDAK TABUR BERBAHAN DASAR
AMILUM SOLANI (Solanum tuberosum L.) DAN AMILUM MANIHOT
(Manihot utilisima L.) DENGAN PEWARNA KAROTENOID
DARI BUAH LABU KUNING (Cucurbita moschata Duch.)
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S. Farm.)
Program Studi Farmasi
Oleh :
Arum Mangastuti Poernomo NIM : 08 8114 116
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA
YOGYAKARTA
iv
Halaman Persembahan
Karya ini aku persembahkan kepada : Tuhan Yesus Kristus Papahku Soekotjo Poernomo dan Mamahku Laurentia Koh Harry Keluargaku dan sahabat-sahabatku Teman-temanku Farmasi dan Almamaterku tercinta
Filipi 4:13 Segala perkara dapat kutanggung
di dalam Dia yang memberi kekuatan kepadaku…
Pengkotbah 3:11 IA membuat segala sesuatu Indah Pada waktunya…
Belajarlah dari keberhasilan dan kesalahan diri sendiri dan orang lain…
vii
KATA PENGANTAR
Puji dan syukur penulis haturkan kepada Tuhan Yang Maha Esa karena atas berkat, cinta kasih, dan penyertaan-Nya penulis dapat menyelesaikan skripsi yang berjudul “PERBANDINGAN SIFAT FISIS BEDAK TABUR BERBAHAN DASAR AMILUM SOLANI (Solanum tuberosum L.) DAN AMILUM MANIHOT
(Manihot utilisima L.) DENGAN PEWARNA KAROTENOID DARI BUAH
LABU KUNING (Cucurbita moschata Duch.)” sebagai tugas akhir untuk memenuhi salah satu syarat memperoleh gelar Sarjana Strata satu Farmasi (S. Farm), Program Studi Farmasi Fakultas Farmasi Universitas Sanata Dharma, Yogyakarta.
Pada kesempatan ini, penulis ingin mengucapkan terima kasih kepada berbagai pihak yang telah memberikan doa, bimbingan, dukungan dan bantuan yang penulis terima secara langsung maupun tidak langsung sehingga akhirnya penulis dapat menyelesaikan skripsi ini dengan baik. Ucapan terima kasih tersebut penulis tujukan kepada :
1. Tuhan Yesus Kristus, atas segala sesuatu yang telah penulis terima dalam hidupnya.
2. Bapak Ipang Djunarko, M,Sc., Apt. selaku Dekan Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
viii
meluangkan waktu untuk berdiskusi bersama penulis hingga akhirnya skripsi ini dapat selesai dengan baik.
4. Ibu Prof. Dr. Sri Noegrohati, Apt selaku Dosen Penguji Skripsi yang telah meluangkan waktu, memberikan saran dan masukan yang membangun serta atas bimbingannya selama perkuliahan.
5. Bapak Yohanes Dwiatmaka, M.Si selaku Dosen Penguji Skripsi yang telah meluangkan waktu, memberikan saran dan masukan yang membangun serta atas bimbingannya selama perkuliahan.
6. Ibu Phebe Hendra, Ph. D., Apt dan Bapak Jeffry Julianus, M.Si atas bimbingan selama perkuliahan dan penyusunan proposal.
7. Segenap Dosen Fakultas Farmasi Universitas Sanata Dharma Yogyakarta atas segala bimbingan selama perkuliahan.
8. Pak Musrifin, Mas Kayat, Mas Kunto, Mas Pardjiman, Mas Heru, Mas Ottok, dan segenap staf laboratorium atas bantuan dan kerja samanya selama penelitian.
9. Segenap karyawan Fakultas Farmasi Universitas Sanata Dharma Yogyakarta atas bantuannya.
10. Papah dan Mamah tercinta atas doa, dukungan, nasehat sehingga penulis dapat menyelesaikan skripsi ini dengan baik.
11. Koh Harry, terima kasih atas dukungannya.
ix
13. Cik Nancy dan Fenny Anggraeni, terima kasih atas dukungan, saran, dan nasehatnya.
14. Intan Chintya Dewi, terima kasih atas kebersamaan, semangat dan kerja samanya selama penelitian di laboratorium dan ujian.
15. Budiastuti Nurrochmah, terima kasih atas semangat, kerja sama selama mempersiapkan ujian dan saat ujian tertutup.
16. Dessy, Elen, Dewi, teman-teman “lipbalm Buah Naga”, terima kasih atas kebersamaan dan bantuannya. Dian, Mariana, Tika, Ana, Pius, Agnes, Silvia, Eddie, Lala, Sin Lie, Yessy, Dea, Noveli, Nanda, teman-teman satu laboratorium, terima kasih atas kebersamaan dan bantuannya.
17. Melly, Citra, Vivi, Vithe, Riana, Cinthya Wijayani, terima kasih atas masukan, dan bantuannya.
18. Teman-teman FST B 2008, teman kelas B 2008, dan semua teman-teman Farmasi terima kasih atas segala kebersamaannya.
19. Semua pihak dan teman-teman yang tidak dapat disebutkan satu-persatu oleh penulis yang telah berpartisipasi dalam menyelesaikan skripsi ini.
Penulis menyadari masih banyak ketidaksempurnaan dan kekurangan dalam penyusunan skripsi ini oleh karena keterbatasan pengetahuan dan kemampuan penulis. Untuk itu, penulis sangat mengharapkan kritik dan saran yang dapat membuat karya ini menjadi lebih baik. Akhir kata, semoga skripsi ini dapat bermanfaat bagi pembaca dan perkembangan ilmu pengetahuan khususnya ilmu kefarmasian.
x
DAFTAR ISI
HALAMAN JUDUL ... i
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN ... iii
HALAMAN PERSEMBAHAN ... iv
PERNYATAAN KEASLIAN KARYA ... v
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH UNTUK KEPENTINGAN AKADEMIS... vi
xi
3. Uji kandungan lembab/moisture content ... 16
4. Uji stabilitas warna ... 16
5. Uji daya lekat ... 17
I. Uji Keamanan/Uji Iritasi ... 17
J. Landasan Teori ... 19
xii
BAB III METODOLOGI PENELITIAN ... 21
A. Jenis Rancangan Penelitian ... 21
B. Variabel Penelitian ... 21
1. Variabel bebas ... 21
2. Variabel tergantung ... 21
3. Variabel pengacau terkendali ... 21
4. Variabel pengacau tak terkendali ... 21
C. Definisi Operasional ... 22
D. Alat Penelitian ... 22
E. Bahan Penelitian ... 23
F. Tata Cara Penelitian ... 23
1. Determinasi ... 23
2. Pengambilan sampel buah labu kuning ... 23
3. Pembuatan sari buah labu kuning ... 23
4. Formulasi bedak tabur ... 24
5. Uji sifat fisis ... 25
a. Uji mikromeritik ... 25
b. Uji pengetapan ... 25
c. Uji kandungan lembab/moisture content ... 25
d. Uji stabilitas warna ... 25
e. Uji daya lekat ... 26
f. Uji sifat fisis bedak tabur yang beredar di pasaran ... 26
xiii
G. Analisis Hasil ... 27
BAB IV HASIL DAN PEMBAHASAN ... 28
A. Formulasi ... 28
B. Uji Sifat Fisis ... 33
1. Uji mikromeritik ... 34
2. Uji pengetapan ... 38
3. Uji kandungan lembab/moisture content ... 42
4. Uji stabilitas warna ... 47
5. Uji daya lekat ... 51
C. Uji Keamanan/uji iritasi ... 53
BAB V KESIMPULAN DAN SARAN ... 56
DAFTAR PUSTAKA ... 57
LAMPIRAN ... 61
xiv
DAFTAR TABEL
Tabel I. Hasil analisis kandungan gizi buah labu kuning/waluh per 100 gram ... 9
Tabel II. Evaluasi reaksi iritasi kulit ... 18
Tabel III. Indeks iritasi ... 18
Table IV. Formula acuan bedak tabur (Menurut Riley, 2000) ... 24
Table V. Formula bedak tabur berbahan dasar Amylum Solani ... 24
Table VI. Formula bedak tabur berbahan dasar Amylum Manihot ... 24
Tabel VII. Hasil uji normalitas persentil ... 36
Tabel VIII. Hasil uji R Paired t-test pengukuran mikromeritik hari ke-0 dan ke-30 37 Tabel IX. Hasil uji normalitas pengetapan hari ke 0, 2, 10, 20 dan 30 ... 40
Tabel X. Hasil uji R t -test pengetapan hari ke 0, 2, 10, 20 dan 30 ... 40
Tabel XI. Hasil uji normalitas pengetapan 2 jenis amilum dan bedak “M” .. 41
Tabel XII. Hasil uji normalitaskandungan lembab 2 jenis amilum ... 44
Tabel XIII. Hasil uji R t-test kandungan lembab 2 jenis amilum ... 45
Tabel XIV. Hasil uji normalitas 2 jenis amilum dan bedak “M”... 46
xv
DAFTAR GAMBAR
Gambar 1. Struktur Kulit ... 6
Gambar 2. Labu kuning (Cucurbita moschata Duch.) ... 8
Gambar 3. Diagram distribusi ukuran partikel amylum solani ... 34
Gambar 4. Diagram distribusi ukuran partikel amylum manihot ... 35
Gambar 5. Persentil hari ke-0 dan ke-30... 36
Gambar 6. Pengetapan hari ke 0, 2, 10, 20 dan 30 ... 39
Gambar 7. Struktur Amylose dan Amylopectin ... 43
Gambar 8. Kandungan lembab pada ke-2 jenis amilum ... 44
Gambar 9. Skala Munsell ColorChart ... 47
Gambar 10. Struktur α-caroten, β-caroten, β-cryptocanthin, lutein, zeaxanthine.. 49
xvi
DAFTAR LAMPIRAN
Lampiran 1. Data hasil uji mikromeritik ... 62
Lampiran 2. Data hasil uji stabilitas warna, kandungan lembab, pengetapan, daya lekat dan uji iritasi... 65
Lampiran 3. Data hasil uji normalitas dan signifikansi ... 77
Lampiran 4. Komposisi bedak pasaran merk “M” yang digunakan sebagai pembanding... 91
Lampiran 5. Dokumentasi ... 92
Lampiran 6. Alur penelitian dalam bentuk skema ... 95
Lampiran 7. Surat Pengesahan Determinasi ... 96
xvii
INTISARI
Penelitian ini merupakan formulasi dan uji sifat fisis bedak tabur berbahan dasar Amylum Solani dan Amylum Manihot dengan pewarna karotenoid dari buah labu kuning (Cucurbita moschata Duch.). Penelitian ini bertujuan untuk mengetahui pengaruh penggunaan jenis amilum yang berbeda sebagai bahan dasar bedak akan memberikan sifat fisis yang berbeda pada bedak tabur.
Penelitian ini merupakan penelitian eksperimental. Sifat fisis bedak tabur yang diteliti meliputi ukuran partikel, sifat alir, kandungan lembab, daya lekat dan stabilitas warna bedak tabur. Selain itu, dilakukan juga uji iritasi dengan metode
Draize Skin Test pada kulit kelinci. Untuk perbandingan 2 jenis amilum diuji
menggunakan uji R t-test. Untuk pergeseran ukuran partikel digunakan uji R
paired-t test. Untuk perbandingan 2 jenis amilum dan kontrol menggunakan uji R
One Way Anova (uji parametrik) atau uji R Kruskal-Wallis (uji non-parametrik)
dengan taraf kepercayaan 95%.
Hasil penelitian menunjukkan bahwa penggunaan jenis amilum yang berbeda akan memberikan sifat fisis yang berbeda, meliputi ukuran partikel, sifat alir, kandungan lembab dan stabilitas warna bedak tetapi tidak memberikan perbedaan dalam hal daya lekat dan uji iritasi (uji keamanan).
Kata kunci : bedak tabur, Amylum Solani, Amylum Manihot, buah labu kuning
xviii
ABSTRACT
This research is about formulation and physical properties comparison on loose powder with amylum manihot and amylum solani as basic materials with carotenoid pigment as colour from pumpkin fruit (Cucurbita moschata Duch.). This study aims to know whether different amylum as basic material would give different physical properties on loose powder or not.
This study is an experimental research. Physical properties that would be observed were particle size, flow ability, moisture content, adhesion ability and colour stabilization of loose powder. Besides, it was also done an iritation test with Draize Skin Test method on a rabbit’s skin. As a comparison, two kinds of amylum were analyzed with R t-test. R paired t-test was used on the movement of particle size. The comparison of two kinds of amylum and standart were analyzed using R One Way Anova (parametric test) and R Kruskal-Wallis (nonparametric test) with 95% level of confidence.
The results showed that the use of different amylum would give different physycal properties, include particle size, flow ability, moisture content and colour stabilization of loose powder, but wouldn’t give different on adhesion ability and iritation test (safety test).
Key words: loose powder, amylum solani, amylum manihot, pumpkin fruit
1
BAB I
PENGANTAR
A. Latar Belakang
Setiap wanita mendambakan mempunyai wajah yang cantik dan menarik maka tidak heran para wanita akan mencoba berbagai kosmetik yang dapat membuat wajah mereka menjadi lebih menarik. Menurut penelitian yang dilakukan oleh Nair dan Pillai (2007), terdapat 62% dari 300 responden wanita yang menggunakan produk kosmetik. Hal ini menjadi peluang usaha yang sangat baik bagi produsen kosmetik.
Menurut Kepala Badan Pengawas Obat dan Makanan (BPOM), Husniah Rubiana Thamrin, bahan pewarna Merah K.10 (Rhodamin B) dan Merah K.3 adalah zat warna sintetis yang umumnya digunakan sebagai zat warna kertas, tekstil atau tinta. Zat warna ini merupakan zat karsinogenik yang dapat menyebabkan kanker, dan apabila digunakan pada konsentrasi tinggi dapat mengakibatkan kerusakan hati (Saputri, 2008).
Pada umumnya, buah labu kuning (Cucurbita moschata Duch.) digunakan sebagai bahan pangan. Buah labu kuning dapat diolah menjadi berbagai jenis masakan, seperti kolak, jenang, sayur, dan lain-lain. Di dalam buah labu kuning mengandung beberapa senyawa, antara lain vitamin A, vitamin C,
betacaroten, zat besi dan kalium (Maryani, 2011). Senyawa betacaroten inilah
yang membuat buah labu kuning berwarna kuning, sehingga buah labu kuning dapat digunakan sebagai pewarna dalam makanan. Oleh karena itu, dalam penelitian ini akan dibuat bedak tabur dengan pewarna dari buah labu kuning. Dengan digunakannya buah labu kuning sebagai pewarna dalam kosmetik bedak tabur diharapkan dapat meningkatkan nilai guna dan nilai ekonomis di masyarakat.
Pada umumnya, bedak tabur yang beredar di pasaran menggunakan
talcum sebagai bahan dasar bedak, tetapi ada beberapa produk kosmetik yang
menambahkan amilum sebagai bahan dasar bedak. Amilum yang biasa digunakan untuk bahan dasar bedak adalah AmylumMaydis dan AmylumOryzae. Di pasaran terdapat beraneka ragam jenis amilum, antara lain AmylumMaydis (dari jagung),
Amylum Oryzae (dari beras), Amylum Solani (dari kentang), Amylum Manihot
(dari singkong), Amylum Tritici (dari gandum). Oleh karena itu, dalam penelitian ini akan dibuat bedak tabur dengan bahan dasar dari amilum, yaitu Amylum
Manihot dan Amylum Solani. Dengan digunakannya Amylum Manihot dan
Amylum Solani sebagai bahan dasar bedak diharapkan dapat menambah variasi
Menurut Voigt (1994), amilum mempunyai sifat slip dan absorbency yang baik. Kemampuan slip (daya sebar) dapat dilihat dari pengujian sifat alir, daya lekat dan ukuran partikel. Amilum dengan ukuran partikel yang besar akan mempunyai sifat alir yang baik, tetapi mempunyai daya lekat yang buruk. Uji kandungan lembab yang dilakukan bertujuan untuk mengetahui apakah bedak tabur dapat menyerap lembab dari lingkungan karena hal ini akan berpengaruh terhadap stabilitas bedak tabur selama penyimpanan.
Amylum Manihot mempunyai ukuran partikel yang kecil jika
dibandingkan dengan Amylum Solani. Ukuran partikel Amylum Manihot yaitu sekitar 5-35 µm sedangkan ukuran partikel Amylum Solani yaitu sekitar 10-100 µm (Rowe, Sheskey, Quinn, 2009). Ukuran partikel akan berpengaruh terhadap sifat alir dan daya lekat bedak tabur. Ukuran partikel yang kecil akan mempunyai daya lekat yang bagus dan mempunyai sifat alir yang buruk sedangkan ukuran partikel yang besar akan mempunyai sifat alir yang bagus dan mempunyai daya lekat yang buruk. Ukuran partikel yang kecil mempunyai luas permukaan spesifik yang besar, semakin besar kontak partikel dengan kulit, sehingga bedak akan melekat dengan baik di kulit wajah. Ukuran partikel yang besar mempunyai kohesivitas yang kecil antarpartikel, sehingga partikel akan cenderung berpisah satu sama lain, hal ini akan mempermudah partikel bedak untuk mengalir.
penggunaan bahan baku alam adalah dapat meminimalkan resiko efek samping yang tidak diharapkan. Pembuatan kosmetik yang berasal dari bahan baku alam sesuai dengan fenomena sekarang ini yaitu Back to Nature.
1. Perumusan masalah
Apakah penggunaan Amylum Manihot dan Amylum Solani sebagai bahan dasar bedak akan memberikan sifat fisis yang berbeda pada bedak tabur?
2. Keaslian penelitian
Sejauh penelusuran yang dilakukan peneliti, penelitian terhadap buah labu kuning (Cucurbita moschata Duch.) telah banyak dilakukan, antara lain Pengaruh Jumlah Bubur Labu Kuning dan Konsentrasi Kitosan terhadap Mutu
Mie Basah oleh Andriyani (2008); Ekstraksi dan Pengeringan Waluh untuk
Mendapatkan Produk Fine Powder oleh Perdanianti dan Pratiwi (2004). Tetapi
penggunaan buah labu kuning sebagai pewarna dalam kosmetik serta amylum
solani dan amylum manihot sebagai bahan dasar dalam kosmetik belum pernah
dilakukan.
3. Manfaat penelitian
a. Manfaat teoritis. Dengan penelitian ini, diharapkan dapat menambah pengetahuan dalam formulasi bedak tabur dengan pewarna dari buah labu kuning.
B. Tujuan Penelitian
Mengetahui apakah penggunaan jenis amilum yang berbeda (Amylum
Manihot dan Amylum Solani) sebagai bahan dasar bedak akan memberikan sifat
6
BAB II
PENELAAHAN PUSTAKA
A. Kulit
1. Struktur Kulit
Kulit merupakan organ yang terluas yang menutupi seluruh permukaan tubuh. Daerah yang paling kaku dan tebal adalah telapak kaki dan telapak tangan serta sela-sela jari. Sel kulit yang paling tipis terdapat pada kulit muka (Young, 1972).
Gambar 1. Struktur Kulit (American Medical Association, 1998)
Kulit tersusun atas 2 lapisan, yaitu epidermis dan dermis. Epidermis merupakan lapisan kulit yang paling tipis dan berfungsi sebagai penghalang
(barrier) dari senyawa asing yang masuk ke dalam tubuh. Sel dasar epidermis
disebut keratinosit. Epidermis dibagi menjadi 5 lapisan, yaitu stratum
germinativum, stratum spinosum, stratum granulosum, stratum lusidum, dan
Dermis merupakan kulit sejati dan tersusun atas protein fibrin, kolagen yang merupakan jaringan yang bersifat elastis. Pada lapisan dermis kaya akan pembuluh darah dan syaraf. Selain itu, pada lapisan dermis terdapat kelenjar keringat, kelenjar lemak dan folikel rambut (Young, 1972). Kelembaban kulit yang rendah menyebabkan kulit kering, kasar dan tidak menarik. Pada tingkatan yang lebih buruk menyebabkan kulit pecah-pecah dan mudah teriritasi (Rawling, 2002).
2. Fungsi Kulit
a. Proteksi. Kulit menutupi tubuh dan merupakan barier atau rintangan fisik yang melindungi jaringan di bawahnya dari abrasi fisik, invasi bakteri, dehidrasi dan radiasi ultraviolet.
b. Pengindera (sensori). Kulit terdiri dari berbagai ujung saraf dan reseptor yang menerima rangsang suhu, sentuhan, tekanan dan sakit.
c. Pengatur suhu tubuh dan ekskresi. Kulit mengatur suhu tubuh tidak hanya dengan mengeluarkan keringat, tetapi juga dengan ekskresi sisa-sisa metabolisme tubuh, misalnya air, garam dan beberapa senyawa organik.
B. Labu Kuning (Cucurbita moschata Duch.)
1. Deskripsi
a. b.
Gambar 2. a. Berbagai macam bentuk buah labu kuning (Ferriol, Nuez, and Pico (2007).
b.Labu kuning (BISI Internasional, 2010)
Buah labu kuning termasuk dalam famili Cucurbitaceae, genus
Cucurbita dan nama spesiesnya yaitu Cucurbita moschata Duch. dengan nama
umum labu kuning dan nama daerah labu parang (Melayu), labu kuning (Sunda dan Jawa Tengah) (Anonim, 2011a).
Buah labu kuning berbentuk bulat, berdaging dengan diameter 25-35 cm dan berwarna kuning. Bijinya keras, pipih dengan panjang ±1,5 cm dan lebar ±5 mm, berwarna coklat muda (Anonim, 2011a).
2. Kandungan
Buah labu kuning mengandung saponin, flavonoida dan tanin. (Anonim, 2011a). Selain itu, buah labu kuning juga mengandung vitamin A, vitamin C,
betacaroten, zat besi dan kalium (Maryani, 2011). Warna oranye pada labu
merupakan provitamin A yang terdapat dalam tanaman. Tubuh manusia memiliki kemampuan secara fisiologis mengubah sejumlah besar betacaroten ini menjadi vitamin A. Sedangkan vitamin C merupakan antioksidan dan diduga dapat menangkal berbagai jenis kanker akibat pembentukan radikal bebas (Anonim, 2008).
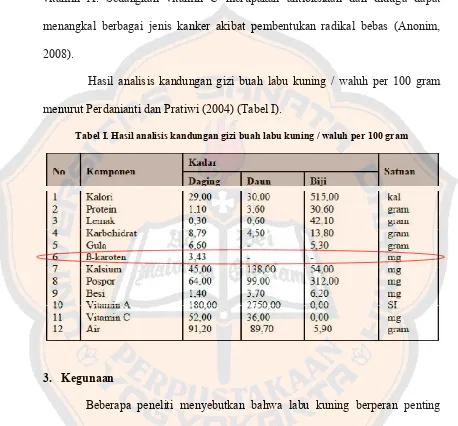
Hasil analisis kandungan gizi buah labu kuning / waluh per 100 gram menurut Perdanianti dan Pratiwi (2004) (Tabel I).
Tabel I. Hasil analisis kandungan gizi buah labu kuning / waluh per 100 gram
3. Kegunaan
Beberapa peneliti menyebutkan bahwa labu kuning berperan penting dalam mencegah penyakit degeneratif seperti diabetes mellitus (kencing manis),
arterosclerosis (penyempitan pembuluh darah), jantung koroner, tekanan darah
tinggi, bahkan bisa pula mencegah kanker (Perdanianti dkk, 2004). Kandungan
betacaroten yang cukup tinggi pada labu kuning efektif untuk mengatasi
Buah labu kuning terdiri dari lapisan kulit luar yang keras dan lapisan daging buah. Dalam daging buah inilah terkandung beberapa vitamin, antara lain
betacaroten, vitamin A dan vitamin C. Selain daging buahnya, daun dan pucuk
ranting yang masih muda dapat digunakan sebagai bahan untuk sayuran. Komponen lain buah labu kuning yang masih mengandung nilai gizi tinggi adalah bijinya. Biji labu kuning mengandung bahan pencahar laksatif dan antelmintik yang dapat digunakan untuk peluruh cacing (Perdanianti dkk, 2004).
C. Bedak
Kosmetik berasal dari kata Yunani ‘kosmetikos’ yang mempunyai arti keterampilan menghias atau mengatur (Prihatin, 2010). Berdasarkan keputusan Kepala Badan Pengawas Obat dan Makanan Republik Indonesia No. HK.00.05.4.1745 tentang kosmetik, pengertian kosmetik adalah sebagai berikut: kosmetik adalah bahan atau sediaan yang dimaksudkan untuk digunakan pada bagian luar tubuh manusia (epidermis, rambut, kuku, bibir dan organ genital bagian luar) atau gigi dan mukosa mulut terutama untuk membersihkan, mewangikan, mengubah penampilan dan atau memperbaiki bau badan atau melindungi atau memelihara tubuh pada kondisi baik (Direktorat Jenderal Pengawas Obat dan Makanan RI, 2003).
menyembunyikan noda (kerusakan) yang terlihat di kulit (Rieger, 2000), membuat kulit menjadi lebih bercahaya, melindungi kulit dari radiasi sinar ultraviolet (Mitsui, 1998).
Ciri-ciri bedak wajah (face powder) yang baik harus memiliki karakteristik berikut, antara lain :
1. Covering power, yaitu kemampuan menyembunyikan cacat pada kulit wajah,
seperti bekas luka, noda di kulit wajah (flek), pori-pori kulit yang besar, bekas jerawat, dan sebagainya
2. Absorbency, yaitu kemampuan bedak wajah (face powder) untuk
menghilangkan kulit berminyak di sekitar area wajah dengan mengabsorbsi sekresi kelenjar sebaceous
3. Slip, yaitu kualitas kemudahan dari substansi bedak untuk dapat menyebar dengan baik pada kulit wajah dan mempermudah pengaplikasian
4. Adhesion, yaitu kemampuan dari substansi bedak untuk melekat dengan baik
pada kulit wajah (Rieger, 2000).
D. Amilum
Amilum sebagai salah satu komposisi bedak mempunyai fungsi sebagai
absorbency dan slip yang baik (Voigt, 1994). Absorbency yaitu kemampuan
bedak wajah (face powder) untuk menghilangkan kulit berminyak di sekitar area wajah dengan mengabsorbsi sekresi kelenjar sebaceous dan slip yaitu kualitas kemudahan penyebaran dan pengaplikasian serbuk untuk menghasilkan hasil yang lembut pada kulit wajah (Rieger, 2000). Selain itu, amilum mempunyai fungsi untuk memperhalus permukaan kulit (Schlossman, 2006).
1. Amylum Solani
Amylum Solani didapatkan dari umbi Solanum tuberosum L. Amylum
Solani berupa serbuk putih, jika ditekan di antara jari akan menimbulkan suara
creaks (seperti suara engsel); praktis tidak larut di air dingin dan alkohol. Amylum
Solani mempunyai bentuk yang tidak beraturan, oval (European Pharmacopoeia,
2002). Ukuran partikel Amylum Solani sekitar 10-100 µm, dengan diameter rata-rata partikel adalah 46 µm dan kandungan lembabnya sebesar 18% (Jackson, 1968; Rowe et al, 2009).
Amylum Solani sudah banyak digunakan di industri makanan sebagai
pengental (thickener), pengikat (binder). Amylum Solani juga digunakan sebagai bahan tambahan pada industri kosmetik dan industri farmasi (Anonim, 2010b).
2. Amylum Manihot
Amylum Manihot mempunyai ukuran partikel dengan diameter sekitar
Manihot telah banyak digunakan di industri farmasi dan industri kosmetik. Amilum tersebut relatif mudah didapat dan harganya lebih murah (Wahyu, 2009). Penggunaan Amylum Manihot dapat memberikan rasa halus dan lembut (Riley, 2000).
E. Titanium Diokside
Fungsi utama bedak (face powder) adalah untuk menutupi kulit wajah secara visual. Oleh karena itu, dalam formulasi bedak (face powder) berisi bahan-bahan dasar dengan sifat penutup yang paling efektif. Bahan-bahan-bahan tersebut antara lain zinc oxide dan titanium dioxide, yang daya penutupnya tidak menurun jika terkena air (Tranggono dan Latifah, 2007).
Titanium diokside berupa serbuk berwarna putih, amorf, tidak berbau dan
tidak berasa (Rowe et al, 2009). Titanium diokside secara luas digunakan pada kosmetik dan sediaan topikal sebagai pigmen pemutih dan opacifier. Titanium
diokside juga dapat digunakan sebagai pelindung sinar ultraviolet (sunscreen)
pada sediaan kosmetik dan sediaan topikal (Rowe et al, 2009 dan Mitsui, 1998). Konsentrasi maksimum untuk penggunaan titanium diokside adalah 25% (SCCNFP, 1998).
F. Magnesium Stearat
Konsentrasi magnesium stearat dalam bedak yaitu 0,1-2,0 % (Sakai Chemical Industry, 2010). Pada level yang terlalu tinggi dapat menyebabkan efek blotchy pada kulit dan akan menurunkan kemampuan slip (daya penyebaran bedak) (Riley, 2000).
G. Metil Paraben
Pengawet adalah bahan untuk mencegah tumbuhnya mikroorganisme yang bisa merusak produk atau tumbuh pada produk. Alasan diperlukan bahan pengawet pada kosmetik adalah untuk melindungi produk-produk yang sudah terformulasi. Kontaminan dengan mikroorganisme dapat menyebabkan timbulnya bau yang tidak sedap, perubahan warna, penurunan daya kerja bahan aktif, perubahan perasaan atas pemakaian produk atau gangguan kesehatan (Tranggono dkk, 2007).
Metil paraben secara luas digunakan sebagai pengawet dan antimikroba pada kosmetik, produk makanan, dan sediaan farmasi. Metil paraben memiliki spektrum aktivitas antimikroba yang luas. Metil paraben paling efektif terhadap ragi dan kapang. Metil paraben berupa kristal tidak berwarna atau serbuk kristalin putih, tidak berbau, dan berasa sedikit membakar. Konsentrasi metil paraben untuk penggunaan sediaan topikal adalah 0,02-0,3 % (Rowe et al, 2009).
H. Uji Sifat Fisis
1. Uji mikromeritik
dan pengendalian ukuran partikel dalam bidang farmasi sangatlah penting. Hal ini berhubungan dengan sifat fisika, kimia dan efek farmakologis suatu obat. Ukuran partikel suatu obat dapat mempengaruhi pelepasan zat aktif dari bentuk sediaannya, yang diberikan melalui oral, parenteral, rektal dan topikal (Martin, Swarbrick, Cammarata, 1983).
Kerugian dari metode mikroskopik adalah hanya diperoleh garis tengah dari dua dimensi dari partikel tersebut, yaitu dimensi panjang dan lebar. Tidak ada perkiraan untuk mengetahui ketebalan dari partikel dengan memakai metode ini. Jumlah partikel yang harus dihitung adalah 300-500 partikel agar mendapatkan suatu perkiraan yang baik dari distribusi partikel (Martin et al, 1983).
2. Uji pengetapan
Pengukuran sifat alir dengan metode pengetapan yaitu dengan melakukan penghentakan (tapping) terhadap sejumlah serbuk dengan menggunakan alat volumenometer (mechanical tapping device) (Dewi, 2010).
Pengurangan volum serbuk akibat pengetapan dinyatakan sebagai harga %T. Serbuk mempunyai sifat alir bagus bila nilai %T tidak lebih dari 20% .
%T = x 100%
Keterangan : V0=volum serbuk sebelum pengetapan
Vt=volum serbuk setelah pengetapan (Anshory, Syukri, Malasari, 2006).
densitas serbuk. Serbuk mempunyai sifat alir bagus bila nilai %C tidak lebih dari 16%.
%C= x100
Keterangan : Df=densitas serbuk sebelum pengetapan
D0=densitas serbuk setelah pengetapan (Aulton, 1988). 3. Uji kandungan lembab
Kadar air adalah banyaknya hidrat yang terkandung di dalam suatu zat atau banyaknya air yang terserap oleh zat. Alatnya menggunakan moisture
balance dan oven (Direktorat Jenderal Pengawasan Obat dan Makanan RI, 1979).
Metode gravimetri didasarkan pada perhitungan susut pengeringan dengan menimbang bahan sebelum dan sesudah pengeringan. Selisihnya merupakan kadar air yang diselidiki (Direktorat Jenderal Pengawasan Obat dan Makanan RI, 1995).
Salah satu cara untuk mengetahui kelembaban suatu bahan padat adalah dengan perhitungan menggunakan data berdasarkan bobot keringnya. Angka hasil perhitungan ini dianggap sebagai kandungan lembab (moisture content / MC). Persamaan untuk menghitung MC yaitu:
%MC = 100% (Rankell, 1989).
4. Uji stabilitas warna
Tujuan dari uji stabilitas produk kosmetik adalah untuk memastikan bahwa produk baru atau produk modifikasi yang dibuat memenuhi standar kualitas fisika, kimia dan mikrobiologi sehingga akan tetap memiliki fungsionalitas yang baik selama dalam kondisi penyimpanan (The European
Metode untuk menentukan warna ditemukan oleh Albert Henry Munsell (1858-1976). Beliau adalah guru dan seniman di Massachusetts College of Art,
Boston
.
Oleh karena itu, metode ini dinamakan Munsell Color System (Anonim,2011c).
5. Uji daya lekat
Uji daya lekat berhubungan dengan kemampuan sediaan untuk dapat menempel dengan baik pada kulit wajah. Uji ini dilakukan dengan menimbang berat bedak yang menempel pada gelas obyek, dimana semakin banyak jumlah bedak yang menempel pada gelas obyek, daya lekatnya semakin buruk.
I. Uji Keamanan/Uji iritasi
Iritasi adalah suatu reaksi pada kulit oleh zat kimia, misalnya alkali kuat, asam kuat, pelarut dan detergen. Beratnya bermacam-macam dari hyperemia, edema dan vesikulasi sampai pemborokan. Iritasi primer terjadi di tempat kontak dan umumnya pada sentuhan pertama (Lu, 1995).
Reaksi iritasi dapat terjadi pada 1-10% dari pemakai kosmetik dan terutama terjadi pada wajah. Reaksi iritasi yang terjadi dapat berupa :
a. Reaksi iritasi subyektif : pada reaksi iritasi ringan, penderita mengeluh rasa terbakar, gatal tanpa disertasi gejala di kulit.
Uji iritasi kulit dilakukan dengan mengoleskan sediaan pada punggung kelinci yang telah dibersihkan dari bulu, kemudian diamati eritema dan edema yang terbentuk setelah 24, 48 dan 72 jam (Tarini, Dewi, Immaculata, 2007). Setelah 24, 48 dan 72 jam pemejanan, tempelan dilepas dan reaksi yang timbul dievaluasi berdasarkan skor dalam tabel berikut ini (Lu, 1995).
Tabel II. Evaluasi reaksi iritasi kulit (Lu, 1995)
Jenis iritasi Skor
Eritema Tanpa eritema 0
Eritema hampir tidak nampak 1
Eritema berbatas jelas 2
Eritema moderat sampai berat 3 Eritema berat (merah bit) sampai sedikit
membentuk kerak
4
Edema Tanpa edema 0
Edema hampir tidak nampak 1
Edema tepi berbatas jelas 2
Edema moderat (tepi naik ±1 mm) 3 Edema berat (tepi naik lebih dari 1 mm dan
meluas ke luar daerah pejanan)
4
Setelah pengamatan selesai dilakukan, kemudian dilakukan perhitungan indeks iritasi primer berdasarkan jumlah eritema dan jumlah edema yang mungkin terdapat pada kulit hewan uji dengan rumus di bawah ini :
Indeks iritasi primer =
, , , ,
Berdasarkan indeks iritasi primer yang diperoleh dapat diketahui kriteria iritasi dari senyawa kimia yang dapat dilihat pada tabel di bawah ini :
Tabel III. Indeks iritasi (Maibach and Patrick, 2001)
Indeks iritasi Kriteria iritasi senyawa kimia
0 Tidak mengiritasi
<2 Kurang merangsang
2-5 Iritan moderat
J. Landasan Teori
Bedak tabur (loose powder) adalah suatu produk kosmetik dimana sebagian besar bahan dasarnya berupa serbuk (Mitsui, 1998). Amilum telah banyak digunakan sebagai bahan dasar untuk pembuatan bedak. Penggunaan amilum untuk bedak dapat memperhalus kulit wajah karena amilum mempunyai kemampuan absorbency dan slip yang baik (Voigt, 1994). Absorbency dan slip merupakan karakteristik bedak wajah yang penting.
Jenis amilum yang berbeda akan mempunyai karakteristik yang berbeda. Perbedaan ukuran partikel amilum dapat berpengaruh terhadap sifat alir, dan daya lekat bedak. Partikel dengan ukuran yang lebih kecil akan mempunyai sifat alir yang buruk, tetapi mempunyai daya lekat yang baik, sebaliknya partikel dengan ukuran yang besar akan mempunyai sifat alir yang bagus, tetapi mempunyai daya lekat yang buruk. Sifat alir akan berpengaruh terhadap slip, yaitu kemampuan bedak untuk dapat menyebar secara merata di kulit wajah.
Oleh karena itu, penelitian ini dilakukan untuk mengetahui apakah penggunaan jenis amilum yang berbeda sebagai bahan dasar bedak akan memberikan sifat fisis yang berbeda, meliputi ukuran partikel, sifat alir, kandungan lembab, daya lekat, stabilitas warna dan iritasi pada kulit. Bahan dasar yang digunakan pada penelitian ini adalah Amylum Manihot dan Amylum Solani.
Sifat fisis bedak tabur ini juga dibandingkan dengan sifat fisis bedak yang telah beredar di pasaran, hal ini bertujuan untuk mengetahui apakah bedak yang diformulasikan memiliki potensi untuk diterima oleh konsumen.
K. Hipotesis
21
BAB III
METODE PENELITIAN
A. Jenis Rancangan Penelitian
Penelitian ini termasuk jenis penelitian eksperimental. Penelitian ini dilakukan di Laboratorium Formulasi Teknologi Sediaan Solid Universitas Sanata Dharma Yogyakarta.
B. Variabel Penelitian
1. Variabel bebas
Variabel bebas dalam penelitian ini adalah Amylum Solani dan
Amylum Manihot.
2. Variabel tergantung
Variabel tergantung dalam penelitian ini adalah sifat fisis dari bedak meliputi ukuran partikel, sifat alir serbuk, kandungan lembab serbuk, stabilitas warna bedak, daya lekat bedak, iritasi pada kulit.
3. Variabel pengacau terkendali
Variabel pengacau terkendali dalam penelitian ini adalah lama pencampuran serbuk, suhu pengeringan serbuk (oven), alat dan bahan yang digunakan, lama penyimpanan bedak.
4. Variabel pengacau tak terkendali
C. Definisi Operasional
1. Bedak tabur adalah salah satu tipe kosmetik yang bahan utamanya berupa serbuk dan digunakan pada bagian wajah manusia untuk memperbaiki penampilan.
2. Amylum Solani adalah serbuk pati berwarna putih yang berasal dari umbi
kentang (Solanum tuberosum L.).
3. Amylum Manihot adalah serbuk pati berwarna putih yang berasal dari umbi
singkong (Manihot utilissima L.).
4. Sari buah labu kuning adalah sari buah yang diperoleh dari buah labu kuning
(Cucurbita moschata Duch.) yang dijuice menggunakan juice extractor.
5. Sifat fisis adalah sifat bedak tabur yang dapat dilihat kenampakan fisiknya dan dapat diukur secara kuantitatif, meliputi uji mikromeritik, uji pengetapan, uji kandungan lembab (moisturecontent), uji stabilitas warna, dan uji daya lekat. 6. Uji keamanan adalah pengujian yang bertujuan untuk menjamin keamanan
dari bedak yang dibuat, menggunakan metode Draize skin test.
D. Alat Penelitian
Alat yang digunakan dalam penelitian ini adalah neraca analitik (Mettler AE 260 Delta Range®), neraca analitik (Mettler PL 300), juicer extractor (Miyako JE-507), oven (Memmert), moisture balance (Mettler Toledo HG53 Halogen Moisture Analyzer), pengetapan/volumenometer (Erweka SVM), motic
pengayak, saringan teh, loyang, alat-alat gelas, wadah plastik, gunting, kandang kelinci yang terbuat dari bambu.
E. Bahan Penelitian
Bahan yang digunakan dalam penelitian ini adalah Amylum Solani (PT. Adimitra Prima Lestari) distributor Tunas Sumber Idea Kreasi Kimia Jakarta Barat, Amylum Manihot (PT. Brataco Chemica Yogyakarta), titanium diokside (PT. Brataco Chemica Yogyakarta), buah labu kuning (Cucurbita moschata Duch.) yang diperoleh dari LotteMart Yogyakarta, metil paraben (PT. Brataco Chemica Yogyakarta), magnesium stearat (PT. Brataco Chemica Yogyakarta), kelinci jenis albino, kain kasa, plester.
F. Tata Cara Penelitian
1. Determinasi
Determinasi tanaman dilakukan dengan mengacu pustaka menurut Ferriol, Nuez, and Pico (2007) dari European Central Cucurbits database.
2. Pengambilan sampel buah labu kuning
Buah labu kuning yang digunakan dalam penelitian ini diperoleh dari LotteMart Wholesale, Maguwoharjo, Yogyakarta yang ditanam di daerah Kopeng, Kabupaten Salatiga, Jawa Tengah.
3. Pembuatan sari buah labu kuning
sampai didapatkan sarinya. Sari buah labu kuning yang telah didapat kemudian disaring menggunakan saringan teh kemudian disaring lagi menggunakan saringan dengan diameter lubang yang lebih kecil.
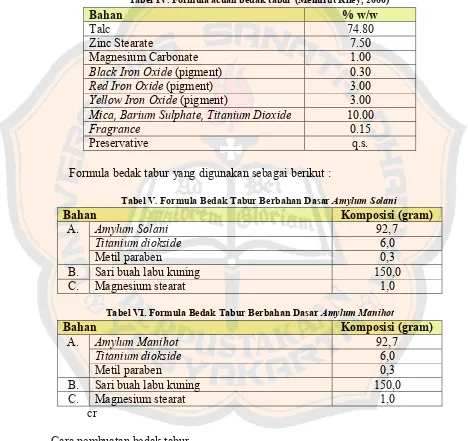
4. Formulasi bedak tabur
Tabel IV. Formula acuan bedak tabur (Menurut Riley, 2000)
Bahan % w/w
Talc 74.80
Zinc Stearate 7.50
Magnesium Carbonate 1.00
Black Iron Oxide (pigment) 0.30
Red Iron Oxide (pigment) 3.00
Yellow Iron Oxide (pigment) 3.00
Mica, Barium Sulphate, Titanium Dioxide 10.00
Fragrance 0.15
Preservative q.s.
Formula bedak tabur yang digunakan sebagai berikut :
Tabel V. Formula Bedak Tabur Berbahan Dasar Amylum Solani
Bahan Komposisi (gram)
Tabel VI. Formula Bedak Tabur Berbahan Dasar Amylum Manihot
Bahan Komposisi (gram)
Campuran tersebut didiamkan selama 6 hari di dalam lemari pendingin. Kemudian campuran dikeringkan di dalam oven sampai kering. Kemudian ditambahkan bahan C ke dalam serbuk bedak yang sudah kering, lalu diblender. Serbuk dituang ke dalam wadah. Pembuatan bedak tabur dilakukan sebanyak 3 replikasi.
5. Uji sifat fisis
a. Uji mikromeritik. Sebelum motic microscope digunakan, dilakukan kalibrasi terlebih dahulu. Air diambil secukupnya, lalu diletakkan di atas gelas objek, beri sedikit bedak, diratakan lalu ditutup dengan kaca penutup. Lalu diamati menggunakan motic microscope, kemudian diukur diameter partikelnya. Pengujian dilakukan pada hari ke 0 dan 30 dengan replikasi sebanyak 3 kali.
b. Uji pengetapan. Seratus gram bedak dituang pelan-pelan ke dalam gelas ukur sehingga didapat volum tertentu (Vo). Gelas ukur dipasang pada alat dan motor dihidupkan. Perubahan volum pada hentakan ke 5, 10, 25 dan seterusnya sampai volum konstan dicatat sebagai Vt. Pengujian dilakukan pada hari ke 0, 2, 10, 20 dan 30 dengan replikasi sebanyak 3 kali
c. Uji kandungan lembab/moisture content. Bedak dengan berat ±5 gram ditempatkan secara merata pada krus, lalu dilakukan siklus pemanasan mengikuti panduan alat gravimetri. Pengujian dilakukan pada hari ke 0, 2, 10, 20 dan 30 dengan replikasi sebanyak 3 kali.
dicatat. Pengujian dilakukan pada hari ke 0, 2, 10, 20 dan 30 dengan replikasi sebanyak 3 kali.
e. Uji daya lekat. Bedak sebanyak 0,01 gram ditempelkan pada kulit di bagian tangan, lalu diratakan. Gelas obyek ditimbang sebagai M0, lalu
diletakkan gelas objek di atas tangan yang sudah diberi bedak. Kemudian diberi beban seberat 50 gram, dan dibiarkan selama 1 menit. Kemudian gelas obyek ditimbang sebagai Mt. Dihitung selisih M0 dan Mt. Pengujian
direplikasi sebanyak 3 kali.
f. Uji sifat fisis bedak tabur yang beredar di pasaran. Diambil 3 buah bedak tabur merk “M” dengan nomor batch yang sama. Lalu dilakukan uji sifat fisis meliputi uji mikromeritik, uji pengetapan, uji kandungan lembab, uji stabilitas warna, uji daya lekat dan uji iritasi pada bedak tabur merk “M” (pengujian yang dilakukan sama dengan pengujian yang dilakukan terhadap bedak tabur formulasi dari laboratorium).
6. Uji keamanan/uji iritasi
Kelinci yang digunakan untuk penelitian berjenis albino dengan mata berwarna merah. Kelinci tersebut diperoleh dari Desa Sumberharjo, Prambanan, Yogyakarta pada tanggal 2 November 2011.
G. Analisis Hasil
Analisis hasil menggunakan program uji R versi 2.14.0. Untuk pengujian normalitas data digunakan program komputer, digunakan uji Shapiro-Wilk jika jumlah data kurang dari 50, dan digunakan uji Kolmogorov-Smirnov jika jumlah data lebih dari 50.
Untuk menghitung persentil dari 300 partikel digunakan program
Microsoft Excel 2007. Untuk mengetahui signifikansi ukuran partikel hari ke-0
dan hari ke-30 setelah pembuatan digunakan uji R Paired t-test untuk masing-masing jenis amilum. Untuk data berdistribusi normal digunakan uji R Paired t-test, sedangkan untuk data berdistribusi tidak normal digunakan uji R Wilcoxon. Penarikan kesimpulan menggunakan taraf kepercayaan (Confidence Interval) 95%.
28
BAB IV
HASIL DAN PEMBAHASAN
A. Formulasi
Formula bedak yang digunakan pada penelitian ini merupakan hasil modifikasi dari formula bedak standar menurut Riley (2000). Bahan-bahan yang digunakan dalam pembuatan bedak antara lain Amylum Solani, Amylum Manihot,
titanium diokside, metil paraben, magnesium stearat, dan sari buah labu kuning
(Cucurbita moschata Duch.).
Determinasi terhadap buah labu kuning yang digunakan pada penelitian ini dilakukan di Laboratorium Kebun Tanaman Obat Fakultas Farmasi Universitas Sanata Dharma Yogyakarta dengan mengacu pustaka menurut Ferriol, Nuez, and Pico (2007) dari European Central Cucurbits database, dengan hasil buah yang digunakan adalah Cucurbita moschata Duch.
Amylum Solani dan Amylum Manihot berfungsi sebagai bahan dasar
pembuatan bedak. Selain itu amilum juga berfungsi sebagai slip dan absorbency. Slip yaitu kemampuan bedak untuk dapat menyebar merata pada kulit wajah dan
absorbency yaitu kemampuan bedak untuk dapat menyerap keringat dan minyak
Titanium diokside berfungsi sebagai opacifier dan covering power yang baik, karena salah satu fungsi dari penggunaan bedak wajah adalah untuk menutupi kulit wajah secara visual, menutupi noda-noda di kulit wajah, sehingga dapat memperbaiki penampilan. Selain itu, titanium diokside dapat juga berfungsi sebagai sunscreen.
Metil paraben berfungsi sebagai bahan pengawet. Pada formula bedak yang digunakan dalam penelitian ini banyak menggunakan bahan-bahan yang berasal dari alam, seperti amilum dan sari buah labu kuning, sehingga peran bahan pengawet sangat penting dalam formula ini, untuk mencegah tumbuhnya mikroorganisme yang dapat mengganggu stabilitas bedak. Adanya kontaminasi mikroorganisme dapat menyebabkan timbulnya bau yang tidak sedap dan dapat menurunkan fungsi dari bedak.
Magnesium stearat berfungsi sebagai peningkat adhesivitas, yaitu meningkatkan daya lekat bedak pada kulit wajah. Selain itu, magnesium stearat juga dapat memperbaiki adhesi bedak pada puff (Tranggono dan Latifah, 2007).
pembentukan kolagen yang dapat mempercepat pembentukan sel kulit baru sehingga dapat mencegah terjadinya keriput di kulit wajah.
Pada proses pencampuran bahan-bahan yang meliputi amilum (Amylum
Manihot atau Amylum Solani), titanium diokside dan metil paraben dilakukan
dengan cara diblender, hal ini bertujuan supaya lebih cepat homogen dan lebih praktis dibandingkan dengan penggerusan menggunakan mortir dan stamper. Urutan pencampuran bahan dimulai dari kuantitas bahan yang kecil hingga kuantitas yang besar dalam formula, yaitu metil paraben, titanium diokside, dan amilum. Urutan ini berdasarkan atas jumlah bahan yang sedikit hingga jumlah bahan yang banyak, tujuannya adalah untuk mempermudah pencampuran bahan sehingga didapatkan campuran yang homogen. Penambahan sari buah labu kuning dilakukan setelah semua bahan telah tercampur.
Sari buah labu kuning berasal dari daging buah labu kuning yang dijuicer menggunakan juice extractor. Buah labu kuning yang digunakan dalam penelitian ini diambil yang kulitnya berwarna hijau dengan bintik-bintik coklat, kemudian daging buahnya berwarna kuning tua. Buah labu kuning ini diperoleh dari LotteMart Wholesale, Maguwoharjo, Yogyakarta, dan buah labu kuning ini ditanam di daerah Kopeng, Kabupaten Salatiga, Jawa Tengah.
tua. Hal ini dikarenakan pada buah labu kuning yang daging buahnya berwarna kuning tua mengandung senyawa karotenoid yang lebih tinggi sehingga dapat menghasilkan bedak dengan warna kuning yang lebih menyala dan stabil.
Pada penelitian ini, tidak digunakan ekstrak (hasil ekstraksi) tetapi menggunakan sari buah yang berasal dari buah yang dijuicer, karena senyawa karotenoid tidak stabil pada pemanasan. Apabila buah labu kuning diekstraksi menggunakan ekstraksi pada suhu tertentu, hal ini dapat menyebabkan senyawa karotenoid menjadi tidak stabil karena terjadi peristiwa degradasi senyawa karotenoid yang disebabkan oleh panas. Selain itu, dalam proses pembuatan bedak masih melalui tahap pengeringan, yang akan terpapar panas dari oven, sehingga apabila dibuat dalam bentuk ekstrak tidak dapat dijamin kestabilan senyawa karotenoid tersebut karena mengalami pemanasan berulang kali. Jadi, pada penelitian ini digunakan sari buah untuk meminimalkan terjadinya degradasi senyawa karotenoid yang disebabkan oleh pemasanan.
Pada penelitian ini menggunakan sari buah labu kuning dalam jumlah yang banyak (yaitu 150 mL sari buah labu kuning untuk 100 gram bahan) karena dari hasil orientasi jumlah tersebut yang dapat menghasilkan warna yang bagus dan stabil.
memberikan hasil yang hampir sama, sehingga untuk mengefektifkan waktu digunakan yang 6 hari, sedangkan pendiaman selama 3 hari warna yang terbentuk belum bagus dan tidak stabil.
Setelah serbuk kering, kemudian digerus dan diblender untuk memperkecil ukuran partikel dan menghomogenkan warna. Tetapi sewaktu
memblender tidak boleh terlalu lama karena proses blender akan menghasilkan
energi panas. Apabila terlalu lama dalam proses blender, energi panas tersebut dapat mendegradasi senyawa karotenoid yang ada di dalam bedak, sehingga dapat menyebabkan warna bedak menjadi pudar.
Penambahan magnesium stearat dilakukan di akhir pembuatan bedak yaitu setelah bedak selesai dikeringkan karena magnesium stearat di sini berfungsi sebagai peningkat adhesivitas bedak terhadap kulit wajah sehingga penambahannya setelah didapatkan serbuk kering bedak. Selain itu, magnesium stearat bersifat nonpolar (hidrofob), apabila ditambahkan bersamaan dengan bahan-bahan lain dan sari buah labu kuning, maka magnesium stearat tidak dapat bercampur dengan bahan lain. Magnesium stearat akan mengapung di atas permukaan sehingga bahan yang sudah dicampur tidak dapat digunakan.
B. Uji Sifat Fisis
Sifat fisis merupakan salah satu unsur penting yang digunakan untuk menentukan kualitas suatu sediaan. Dalam penelitian ini, parameter sifat fisis bedak yang diuji antara lain ukuran partikel, sifat alir, kandungan lembab, stabilitas warna, dan daya lekat serta uji keamanan yaitu uji iritasi.
luas. Bedak pasaran yang digunakan sebagai pembanding adalah bedak merk “M”. Bedak pasaran yang digunakan sebagai pembanding diambil dari nomor batch yang sama untuk menjamin bedak yang digunakan memiliki kualitas yang sama. Uji sifat fisis yang dilakukan meliputi:
1. Uji mikromeritik
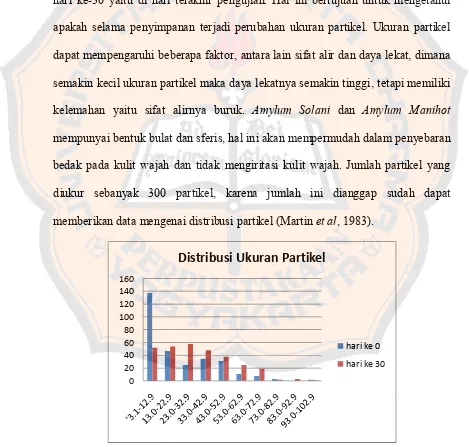
Uji mikromeritik dilakukan pada hari ke-0 yaitu di awal pembuatan dan hari ke-30 yaitu di hari terakhir pengujian. Hal ini bertujuan untuk mengetahui apakah selama penyimpanan terjadi perubahan ukuran partikel. Ukuran partikel dapat mempengaruhi beberapa faktor, antara lain sifat alir dan daya lekat, dimana semakin kecil ukuran partikel maka daya lekatnya semakin tinggi, tetapi memiliki kelemahan yaitu sifat alirnya buruk. Amylum Solani dan Amylum Manihot mempunyai bentuk bulat dan sferis, hal ini akan mempermudah dalam penyebaran bedak pada kulit wajah dan tidak mengiritasi kulit wajah. Jumlah partikel yang diukur sebanyak 300 partikel, karena jumlah ini dianggap sudah dapat memberikan data mengenai distribusi partikel (Martin et al, 1983).
Gambar 3. Diagram distribusi ukuran partikel Amylum Solani
Pada gambar 3 dapat dilihat bahwa pada hari ke-0 bedak berbahan dasar
Amylum Solani lebih banyak berada pada ukuran yang kecil, yaitu ukuran yang
paling dominan adalah 3,1-12,9 µm. Pada hari ke-30 bedak berbahan dasar
Amylum Solani ukuran partikelnya lebih merata, yaitu paling dominan berada di
ukuran 3,1-72,9 µm. Hal ini menunjukkan selama penyimpanan selama 30 hari, terjadi penurunan jumlah ukuran partikel berukuran kecil, dan terjadi pertambahan jumlah ukuran partikel berukuran besar.
Gambar 4. Diagram distribusi ukuran partikel Amylum Manihot
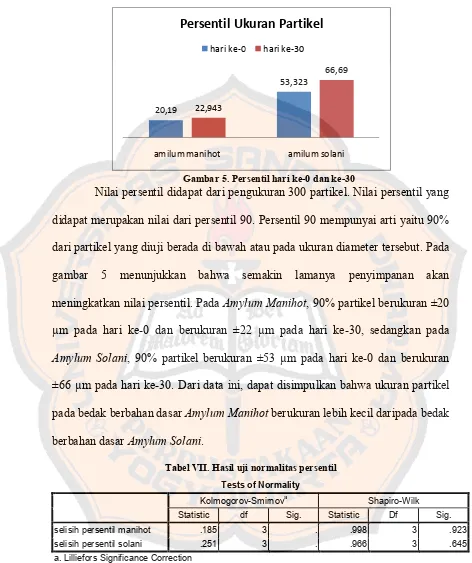
Gambar 5. Persentil hari ke-0 dan ke-30
Nilai persentil didapat dari pengukuran 300 partikel. Nilai persentil yang didapat merupakan nilai dari persentil 90. Persentil 90 mempunyai arti yaitu 90% dari partikel yang diuji berada di bawah atau pada ukuran diameter tersebut. Pada gambar 5 menunjukkan bahwa semakin lamanya penyimpanan akan meningkatkan nilai persentil. Pada Amylum Manihot, 90% partikel berukuran ±20 µm pada hari ke-0 dan berukuran ±22 µm pada hari ke-30, sedangkan pada
Amylum Solani, 90% partikel berukuran ±53 µm pada hari ke-0 dan berukuran
±66 µm pada hari ke-30. Dari data ini, dapat disimpulkan bahwa ukuran partikel pada bedak berbahan dasar Amylum Manihot berukuran lebih kecil daripada bedak berbahan dasar Amylum Solani.
Tabel VII. Hasil uji normalitas persentil
Tests of Normality
Untuk uji normalitas karena jumlah data yang digunakan kurang dari 50, maka digunakan uji Shapiro-Wilk. Untuk data Amylum Manihot, data yang didapat berdistribusi normal karena nilai p>0,05 yaitu p=0,923. Untuk data
Amylum Solani, data yang didapat berdistribusi normal karena nilai p>0,05 yaitu p=0,645. Oleh karena data yang didapat berdistribusi normal, maka untuk mengetahui perbedaan atau signifikansi antara 2 kelompok, dilakukan uji R Paired t-test.
Tabel VIII. Hasil uji R Paired t-test pengukuran mikromeritik hari ke-0 dan ke-30
Jenis amilum df Confidence Interval p-value
Manihot 2 95% 0.024
Solani 2 95% 0.2703
Dari tabel VIII dapat disimpulkan bahwa pada bedak berbahan dasar
Amylum Manihot, ukuran partikel bedak saat pembuatan yaitu hari ke-0 berbeda
signifikan dengan ukuran partikel bedak pada akhir pengujian yaitu hari ke-30, hal ini dikarenakan nilai p<0,05 yaitu p=0,024, sedangkan pada bedak berbahan dasar
Amylum Solani, ukuran partikel bedak saat pembuatan yaitu hari ke-0 tidak
berbeda signifikan dengan ukuran partikel bedak pada akhir pengujian yaitu hari ke-30, hal ini dikarenakan nilai p>0,05 yaitu p=0,2703.
Pada uji signifikansi menggunakan uji R Paired t-test, untuk bedak berbahan dasar Amylum Solani ukuran partikel bedak pada hari ke-0 tidak berbeda signifikan dengan ukuran partikel pada hari ke-30, hal ini berarti partikel bedak berbahan dasar Amylum Solani stabil selama penyimpanan, sedangkan untuk bedak berbahan dasar Amylum Manihot ukuran partikel bedak pada hari ke-0 berbeda signifikan dengan ukuran partikel pada hari ke-30, hal ini berarti partikel bedak berbahan dasar Amylum Manihot tidak stabil selama penyimpanan.
16,063-16,498. Ukuran diameter partikel bedak hasil formulasi lebih besar daripada ukuran diameter partikel bedak “M”.
2. Uji pengetapan
Tujuan dilakukan uji pengetapan yaitu untuk mengetahui sifat alir serbuk (secara metode tidak langsung) dan mengetahui nilai kompresibilitas dari serbuk. Salah satu syarat bedak yang baik yaitu bedak dapat menyebar dengan merata pada kulit wajah. Daya sebar bedak dipengaruhi oleh kemampuan bedak untuk dapat mengalir dengan baik.
Ada beberapa cara untuk menguji sifat alir serbuk, antara lain dengan metode langsung yaitu dengan metode corong (hopper flow rate), dan metode tidak langsung yaitu dengan metode sudut diam (angel of repose), uji pengetapan
(bulk density measurement) (Aulton, 1988). Pada penelitian ini digunakan uji
pengetapan untuk menguji sifat alir serbuk. Uji pengetapan menggunakan alat volumenometer.
Selama proses pengetapan terjadi mekanisme penataulangan
(rearrangement) karena partikel serbuk akan mengisi ruang atau celah kosong
yang ada di bawahnya. Partikel serbuk akan bergerak karena ada pengaruh hentakan dan tekanan dari partikel di atasnya. Hal ini menyebabkan terjadinya reduksi volum.
Persentase pengetapan (% C) dibandingkan antara ke-2 jenis amilum serta dibandingkan dengan bedak pasaran :
a. Perbedaan % C antara bedak berbahan dasar Amylum Manihot dengan Amylum Solani
Gambar 6. Pengetapan hari ke 0, 2, 10, 20 dan 30
Dari gambar 6 dapat dilihat bahwa semakin lama penyimpanan maka nilai % C semakin besar. Semakin besar nilai % C, semakin besar reduksi volum yang terjadi, sifat alir semakin buruk karena semakin banyak partikel yang berukuran kecil. Partikel yang berukuran kecil mempunyai sifat alir yang buruk karena partikel kecil mempunyai kohesivitas yang tinggi, yang mempunyai kecenderungan untuk mengelompok.
Dari perolehan nilai % C, dapat disimpulkan bahwa bedak berbahan dasar Amylum Solani mempunyai sifat alir yang lebih baik daripada bedak berbahan dasar Amylum Manihot, karena nilai % C pada bedak berbahan dasar
Amylum Solani lebih kecil dari pada % C pada bedak berbahan dasar Amylum
Manihot. Serbuk mempunyai sifat alir yang bagus apabila nilai % C kurang
dari 21% (Aulton, 1988), sehingga dapat disimpulkan bahwa bedak berbahan dasar Amylum Solani mempunyai sifat alir yang bagus. Serbuk dengan rentang % C 23-28% (Aulton, 1988) mempunyai sifat alir yang buruk, sehingga dapat disimpulkan bahwa bedak berbahan dasar Amylum Manihot mempunyai sifat alir yang buruk.
Tabel IX. Hasil uji normalitas pengetapan hari ke 0, 2, 10, 20 dan 30 Tests of Normality
Kolmogorov-Smirnova Shapiro-Wilk
Statistic df Sig. Statistic df Sig.
pengetapan .139 30 .145 .952 30 .189
a. Lilliefors Significance Correction
Untuk uji normalitas, karena jumlah data yang digunakan kurang dari 50, maka digunakan uji Shapiro-Wilk. Dari tabel IX data yang didapat berdistribusi normal karena nilai p>0,05 yaitu p=0,189. Oleh karena data yang didapat berdistribusi normal, maka untuk mengetahui perbedaan atau signifikansi antara 2 kelompok, dilakukan uji R t-test.
Tabel X. Hasil uji R untuk pengetapan
Pengujian Jenis uji p-value
Dari tabel X dapat disimpulkan bahwa selama penyimpanan bedak berbahan dasar Amylum Manihot dan Amylum Solani tidak mengalami perubahan sifat alir, karena nilai p>0,05 yang berarti tidak terdapat perbedaan yang signifikan. Dan apabila diperbandingkan antara kedua jenis amilum, terdapat perbedaan yang signifikan antara sifat alir untuk bedak berbahan dasar Amylum Manihot dan Amylum Solani, karena nilai p<0,05 yang berarti terdapat perbedaan yang signifikan.
Apabila dilihat dari nilai % C yang ditunjukkan pada grafik pada gambar 4 dapat dinyatakan bahwa bedak berbahan dasar Amylum Solani mempunyai sifat alir yang lebih baik daripada bedak berbahan dasar Amylum
Manihot.
b. Perbedaan % C antara ke-2 jenis amilum dengan bedak “M”
Tabel XI. Hasil uji normalitas pengetapan 2 jenis amilum dan bedak “M” Tests of Normality
Kolmogorov-Smirnova Shapiro-Wilk
Statistic df Sig. Statistic df Sig.
pengetapan .197 9 .200* .844 9 .064
a. Lilliefors Significance Correction
*. This is a lower bound of the true significance.
Untuk uji normalitas, karena jumlah data yang digunakan kurang dari 50, maka digunakan uji Shapiro-Wilk. Dari tabel XI data yang didapat berdistribusi normal karena nilai p>0,05 yaitu p=0,064. Oleh karena data yang didapat berdistribusi normal, maka untuk mengetahui perbedaan atau signifikansi dilakukan uji R One Way Anova. Dari pengujian uji R One Way
Anova diperoleh nilai p<0,05 yaitu p=0.0005495, yang berarti terdapat
Apabila dilihat dari nilai % C, dapat dinyatakan bahwa bedak berbahan dasar Amylum Solani mempunyai nilai % C yang lebih kecil daripada bedak berbahan dasar Amylum Manihot. Bedak berbahan dasar
Amylum Solani mempunyai perbedaan yang signifikan dengan bedak berbahan
dasar Amylum Manihot dan bedak M, sehingga dapat dinyatakan bahwa bedak berbahan dasar Amylum Solani mempunyai sifat alir yang paling bagus dibandingkan dengan bedak berbahan dasar Amylum Manihot dan bedak M. Dalam hal ini, bedak M yang digunakan sebagai pembanding mempunyai sifat alir yang buruk, karena bedak M tidak berbeda signifikan dengan bedak berbahan dasar Amylum Manihot.
3. Uji kandungan lembab/moisture content
Gambar 7. Struktur Amylose dan Amylopectin (Rowe et al, 2009).
Kandungan lembab amilum dipengaruhi oleh jumlah amylopectin dan
amylose dalam amilum. Menurut Rowe et al (2009), di dalam Amylum Solani
terdapat 20-23% amylose, sedangkan di dalam Amylum Manihot terdapat 17-20%
amylose. Pada gambar 7, apabila dilihat dari struktur amylose banyak mengikat
gugus –OH, semakin tinggi persentase amylose maka kandungan lembabnya semakin tinggi pula. Jadi, apabila dilihat dari persentase amylose kandungan lembab pada Amylum Solani lebih tinggi daripada kandungan lembab pada Amylum Manihot
Persentase kandungan lembab (%MC) dibandingkan antara ke-2 jenis amilum serta dibandingkan dengan bedak pasaran :
Gambar 8. Kandungan lembab pada ke-2 jenis amilum
Dari gambar 8 dapat dilihat bahwa pada bedak berbahan dasar
Amylum Solani, semakin lama penyimpanan maka jumlah persentase
kandungan lembab semakin menurun, hal ini berarti selama penyimpanan bedak tidak menyerap lembab dari lingkungan, sedangkan pada bedak berbahan dasar Amylum Manihot, semakin lama penyimpanan jumlah persentase kandungan lembab lebih stabil. Pada bedak berbahan dasar Amylum
Manihot terjadi peningkatan persentase kandungan lembab pada hari ke 2 dan
30. Bila dilihat dari grafik pada gambar 7 kandungan lembab pada bedak berbahan dasar Amylum Solani lebih tinggi daripada kandungan lembab pada bedak berbahan dasar Amylum Manihot, tetapi selama penyimpanan bedak berbahan dasar Amylum Solani tidak menyerap lembab dari lingkungan.
Tabel XII. Hasil uji normalitas kandungan lembab 2 jenis amilum
Untuk uji normalitas, karena jumlah data yang digunakan kurang dari 50, maka digunakan uji Shapiro-Wilk, data yang didapat berdistribusi tidak normal karena p<0,05 yaitu p=0,018. Oleh karena data yang didapat berdistribusi tidak normal, maka untuk mengetahui perbedaan atau signifikansi dilakukan uji R t-test.
Tabel XIII. Hasil uji R kandungan lembab
Pengujian Jenis uji p-value
Manihot hari ke 0, 2, 10, 20, 30 Anova 0.002741 Solani hari ke 0, 2, 10, 20, 30 Anova 0.2443 Perbandingan ke-2 jenis amilum Unpaired t-test 0.001458
Dari tabel XIII dapat disimpulkan bahwa selama penyimpanan bedak berbahan dasar Amylum Solani tidak mengalami perubahan kandungan lembab, karena nilai p>0,05 yang berarti tidak terdapat perbedaan yang signifikan, sedangkan untuk bedak berbahan dasar Amylum Manihot mengalami perubahan kandungan lembab, karena nilai p<0,05 yang berarti terdapat perbedaan yang signifikan. Dan apabila diperbandingkan antara kedua jenis amilum, terdapat perbedaan yang signifikan antara sifat alir untuk bedak berbahan dasar Amylum Manihot dan Amylum Solani, karena nilai p<0,05 yang berarti terdapat perbedaan yang signifikan.
Dari hasil pengujian, diperoleh data bahwa bedak berbahan dasar
Amylum Solani mempunyai persentase kandungan lembab yang lebih tinggi,
penyimpanan mengalami peningkatan jumlah persentase kandungan lembab, yang berarti selama penyimpanan bedak menyerap lembab dari lingkungan. Kesimpulannya adalah bedak berbahan dasar Amylum Solani lebih stabil daripada bedak berbahan dasar Amylum Manihot, karena bedak berbahan dasar Amylum Solani lebih rendah dalam menyerap lembab daripada bedak berbahan dasar Amylum Manihot, yang berarti bedak berbahan dasar Amylum
Solani lebih stabil dalam penyimpanan.
b. Perbedaan %MC antara ke-2 jenis amilum dengan bedak “M” Tabel XIV. Hasil uji normalitas 2 jenis amilum dan bedak “M”
Tests of Normality
Kolmogorov-Smirnova Shapiro-Wilk
Statistic df Sig. Statistic df Sig.
MC .275 9 .049 .833 9 .049
a. Lilliefors Significance Correction
Untuk uji normalitas, karena jumlah data yang digunakan kurang dari 50, maka digunakan uji Shapiro-Wilk, data persen kandungan lembab yang didapat berdistribusi tidak normal (p<0,05). Karena data yang diperoleh berdistribusi tidak normal, maka untuk mengetahui perbedaan dilakukan uji R
Kruskal-Wallis. Hasil dari pengujian menggunakan uji R Kruskal-Wallis
4. Uji stabilitas warna
Tujuan dilakukannya uji stabilitas warna adalah untuk mengetahui kestabilan senyawa karotenoid yang berasal dari buah labu kuning setelah diformulasikan sebagai bahan pewarna dalam bentuk sediaan bedak tabur.
Pengujian stabilitas warna menggunakan Munsell Color Chart yang diambil 7 skala warna untuk mempermudah dalam pengamatan selama pengujian. Cara pengujiannya adalah dengan membandingkan warna sediaan bedak hasil formulasi dengan skala Munsell ColorChart yang dipilih.
Skala Munsell ColorChart yang digunakan adalah sebagai berikut:
Gambar 9. Skala Munsell ColorChart
Skala paling besar menunjukkan intensitas warna yang paling tua, dan skala yang paling kecil menunjukkan intensitas warna yang paling muda. Rentang kestabilan apabila perubahan warnanya antara skala 4-7. Apabila perubahan warnanya menuju skala yang lebih kecil dari skala 4 berarti warna sudah tidak stabil.
peristiwa degradasi senyawa karotenoid, yang dimungkinkan disebabkan oleh panas dan oksigen. Pada saat pengeringan, menggunakan loyang yang terbuat dari aluminium. Aluminium merupakan penghantar panas yang baik, sehingga panas akan terserap ke aluminium, sehingga setelah selesai pengeringan bedak yang dihasilkan warnanya sudah tidak stabil, karena senyawa karotenoid telah terdegradasi oleh panas. Selain itu, menurut Ruwanti (2010), senyawa karotenoid akan mengikat oksigen dari udara bebas dan dapat meningkatkan percepatan perubahan warna yang lebih pucat. Peristiwa autooksidasi karotenoid ini dimulai setelah beberapa hari kontak dengan udara.
Untuk meminimalkan terjadinya peristiwa degradasi senyawa karotenoid oleh panas, dibuat alternatif lain yaitu menggunakan loyang yang terbuat dari kaca. Kaca mempunyai struktur yang lebih rigid, dan kaca bukan penghantar panas yang baik, sehingga pengeringan menggunakan loyang kaca diharapkan dapat meminimalkan terjadinya degradasi senyawa karotenoid yang disebabkan oleh panas, sehingga diharapkan dapat menghasilkan bedak dengan warna yang lebih stabil dan optimum. Dari pengujian stabilitas warna dengan membandingkan warna bedak yang dibuat dengan skala warna pada Munsell Color Chart, didapat bedak yang dibuat dengan loyang kaca mempunyai stabilitas warna yang lebih baik.
senyawa karotenoid karena panas. Senyawa karotenoid akan rusak pada suhu di atas 60 0C (Ruwanti, 2010). Oleh karena itu, untuk meminimalkan terjadinya degradasi senyawa karotenoid oleh panas, pada saat pengeringan menggunakan oven, suhu dijaga antara 40-450 C.
Senyawa karotenoid yang terdapat pada buah labu kuning antara lain α
-caroten, β-caroten, β-cryptocanthin, lutein, dan zeaxanthin. Berikut adalah
struktur dari senyawa karotenoid tersebut: (gambar 10)
Gambar 10. Struktur α-caroten, β-caroten, β-cryptocanthin, lutein, zeaxanthine