i
PERBANDINGAN SIFAT FISIS BEDAK TABUR BERBAHAN DASAR
AMILUM SOLANI (Solanum tuberosum L.) DAN AMILUM MANIHOT
(Manihot utilissima L.) DENGAN PEWARNA KAROTENOID DARI UMBI WORTEL (Daucus carota L.)
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S. Farm.)
Program Studi Farmasi
Oleh:
Intan Chintya Dewi
NIM : 088114096
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
iii
iv
“If You Don't Stand for Something,
You'll Fall for Anything”
Dr. Alan Zimmerman
Karya ini kupersembahkan untuk orang-orang yang
kukasihi dan mengasihiku tanpa batas…
vi
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah Yang Maha Kuasa atas berkat dan rahmat-Nya, sehingga penulis dapat menyelesaikan skripsi yang berjudul “Perbandingan Sifat Fisis Bedak Tabur Berbahan Dasar Amylum Solani
(Solanum tuberosum L.) dan Amylum Manihot (Manihot utilisima L.) dengan
Pewarna Karotenoid dari Umbi Wortel (Daucus carota L.)” Skripsi ini disusun guna memenuhi salah satu syarat memperoleh gelar Sarjana Farmasi (S.Farm.) di
Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
Selama perkuliahan, penelitian, dan penyusunan skripsi, Penulis telah banyak mendapatkan bantuan, sarana, dukungan, nasehat, bimbingan, saran dan
kritik dari berbagai pihak. Oleh karena itu, Penulis ingin mengucapkan terima kasih yang sebesar-besarnya kepada:
1. “Jesus Christ” yang selalu setia menemani, membimbing dan mencurahkan berkat-berkatnya setiap hari
2. Papi, Mami, Cie Evi sekeluarga, Cie Feny sekeluarga, Ko Wawan sekeluarga atas segala dukungan doa, semangat, perhatian, nasehat dan
materi yang selalu menyertai Penulis sehingga skripsi ini dapat terselesaikan.
vii
4. Rini Dwiastuti, S. Farm, M. Sc., Apt, selaku dosen pembimbing atas ide judul skripsi, bimbingan, bantuan, kesabaran, selama penyusunan proposal hingga selesainya skripsi ini
5. Prof. Dr. Sri Noegrohati, Apt. dan Yohanes Dwiatmaka S.Si., M.Si. selaku dosen penguji atas segala masukkan dan bimbingannya
6. Agatha Budi Susiana L, M.Si., Apt. atas masukan, pinjaman buku dan informasi yang telah diberikan.
7. Segenap dosen atas kesabarannya dalam mengajar dan membimbing Penulis
selama perkuliahan di Fakultas Farmasi Universitas Sanata Dharma
8. Ponakan-ponakanku: Axel, Elvano, Zivanna, Jessica, Jevanny yang selalu
memberikan keceriaan saat penulis jenuh.
9. Arum Mangastuti selaku partner skripsi yang selalu setia dan mendukung penulis untuk menyelesaikan skripsi ini.
10. “Tung-Tung” girls: Ratih (Ratman), SariJo, Vita yang memberikan semangat, perhatian dan bantuan.
11. DIGIEE team: Erika, Tanyuk, Devichi, Evelyn, Geta atas kebersamaan dan motivasi penulis selama ini.
viii
13. Teman-teman “lantai 1”: Asti, Dian, Mariana, Tika, Anna, Agnes, Pius, Noveli, Nanda, Edi, Silvia, Sisca, Nindi, Ellen, Desy, Dewi, Yessy, Sisca, Lala, Dea atas dukungan, semangat dan kerja samanya.
14. Teman-teman FST 2008 B yang telah memberikan saran, dukungan, dan semangat bagi Penulis untuk menyelesaikan skripsi ini
15. Pak Musrifin, Mas Agung, Mas Ottok, Pak Iswandi, Mas Kayat, dan segenap laboran lain atas segala bantuannya selama ini
16. Semua pihak yang tidak dapat disebutkan satu per satu yang telah membantu
penulis menyelesaikan skripsi ini.
Penulis menyadari penelitian ini masih belum sempurna mengingat
keterbatasan pengetahuan dan kemampuan penulis. Oleh karena itu, penulis sangat mengharapkan adanya kritik dan saran yang dapat berguna bagi ilmu pengetahuan.
Yogyakarta, 28 Desember 2011
ix
x
DAFTAR ISI
HALAMAN JUDUL ………... i
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN ………. iii
HALAMAN PERSEMBAHAN ... iv
PERNYATAAN PERSETUJUAN PUBLIKASI ... v
PRAKATA ... vi
PERNYATAAN KEASLIAN KARYA ... ix
DAFTAR ISI ... x
DAFTAR TABEL ... xiv
DAFTAR GAMBAR ... xv
DAFTAR LAMPIRAN ... xvii
INTISARI ... xviii
ABSTRACT ... xix
BAB I PENGANTAR ... 1
A. Latar Belakang ……… 1
1. Perumusan masalah ……….. 3
2. Keaslian Penelitian ……… 4
3. Manfaat Penelitian ……….. 4
B. Tujuan Penelitian ………. 4
BAB II PENELAAHAN PUSTAKA ……….. 5
xi
1. Keterangan Botani..………... 5
2. Kandungan Wortel ……… 6
B. Kulit ……….. 6
1. Epidermis ……….... 7
2. Corium(Dermis) ………... 8
3. Hipodermis ………... 8
C. Bedak ……… 8
D. Bedak Tabur ………. 9
E. Komponen Penyusun Bedak ……… 9
1. Daya Penutupan Bedak (Covering powder)………. 9
2. Daya Serap (Abrosrbency) ……….. 10
3. Daya Lekat ( Adhesion )……….. 11
4. Pewarna ………... 12
5. Pengawet ………. 13
F. Uji Sifat Fisis ……… 14
1. Pengujian Mikromeritik ………... 14
2. Pengujian Pengetapan ………... 14
3. Pengujian Kandungan Kelembapan ………... 14
4. Pengujian Stabilitas Warna ………. 15
5. Pengujian Iritasi Primer ………. 15
6. Pengujian Daya Lekat ……….... 16
xii
H. Landasan Teori ……… 17
I. Hipotesis ……….... 19
BAB III METODOLOGI PENELITIAN ……… 20
A. Jenis dan rancangan Penelitian ………... 20
B. Variabel Penelitian ………. 20
C. Definisi Operasional ………... 21
D. Bahan Penelitian ………... 22
E. Alat Penelitian ……….... 22
F. Tata Cara Penelitian ………... 23
1. Formulasi Bedak Tabur ………..……….. 23
2. Pengumpulan dan Penyiapan Sari Umbi Wortel ………... 23
3. Penghomogenan dan Pewarnaan Bedak Tabur ……… 23
4. Pengambilan Sampel ……….... 24
5. Pengujian Mikromeritik ……….... 24
6. Pengujian Pengetapan ………... 24
7. Pengujian Kandungan Kelembaban ……….. 25
8. Pengujian Stabilitas Warna ………... 26
9. Pengujian Iritasi ……… 26
10.Pengujian Daya Lekat ………... 27
G. Analisis Hasil ……….. 27
BAB IV PEMBAHASAN ………... 28
xiii
B. Pembuatan Bedak Wajah ……….... 33
C. Uji Sifat Fisis Bedak Tabur ……….... 38 1. Karakteristik Ukuran Partikel ……….. 38
2. Kandungan Lembab Bedak Tabur ……….... 42
3. Bulk Density ………... 45
4. Daya Lekat Bedak Tabur ……….. 48
5. Uji Iritasi Bedak Tabur ………... 50
6. Stabilitas Warna Bedak Tabur ……….. 51
BAB V KESIMPULAN DAN SARAN ………... 55
A. Kesimpulan ………... 55
B. Saran ………... 55
DAFTAR PUSTAKA ………. 56
LAMPIRAN………. 60
xiv
DAFTAR TABEL
Tabel I. Formula Acuan ... 23
Tabel II. Formula Modifikasi ... 23
Tabel III. Hubungan sifat alir dan kompresibilitas berdasarkan indeks Carr 25
Tabel IV. Evaluasi Reaksi Iritasi Kulit ... 26
Tabel V. Kriteria Iritasi ... 27
Tabel VI. Rata-rata Percentile 90% ... 39
Tabel VII. Hasil Uji Paired T Test nilai Percentile hari ke o dan 30 ... 39
Tabel VIII. Uji Signifikasi Kandungan Lembab hari ke 0, 2, 10,20,30 ... 44
Tabel IX. Hubungan sifat alir dan kompresibilitas berdasarkan indeks Carr 46
Tabel X. Uji Signifikasi Persentase Indeks Carr hari ke 0-30 ... 47
Tabel XI. Perbandingan Rata-rata Bedak Tabur ... 49
Tabel XII. Skor Indeks Iritasi Primer Bedak Tabur pada Kelinci Albino 50
xv
DAFTAR GAMBAR
Gambar 1. Wortel (Daucus Carota L.) ... 5
Gambar 2. Diagram epidermis dengan perbedaan lapisan epidermis dan komponen penyusunnya ... 7
Gambar 3. Bedak Tabur ... 9
Gambar 4. Struktur amilopektin pada amilum ... 11
Gambar 5. Struktur amilosa pada amilum ... 11
Gambar 6. Struktur Magnesium Stearat ... 12
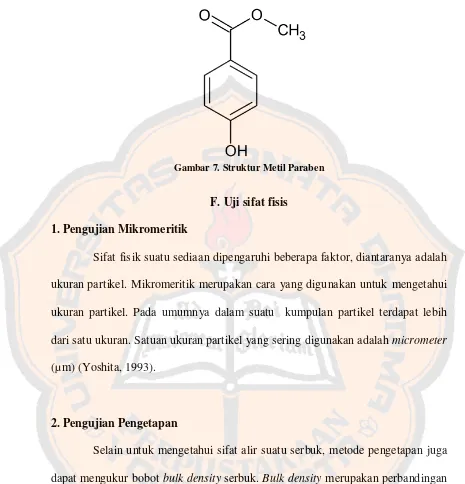
Gambar 7. Struktur Metil Paraben ………. 14
Gambar 8.Interaksi hidrogen antara amilum dan kandungan air pada keringat ... 30
Gambar 9. Interaksi hidrogen antara amilum dan komponen minyak pada wajah ... . 31
Gambar 10. Tipe Kerusakan Pada amilum ……… 36
Gambar 11. Kerusakan pada Amylum Manihot (kiri) dan Amylum Solani (kanan)………..….. 36
Gambar 12. Kurva nilai tengah diameter partikel vs frekuensi formula I .... 40
Gambar 13. Kurva nilai tengah diameter partikel vs frekuensi formula II .. 41
Gambar 14. Grafik persentase pertambahan kandungan lembab bedak tabur ……… ... 42
xvi
xvii
DAFTAR LAMPIRAN
Lampiran 1. Data Penimbangan Wortel ... 60
Lampiran 2. Data Kandungan Lembab ... 61
Lampiran 3. Data Stabilitas Warna ... 67
Lampiran 4. Data Uji Pengetapan ... 69
Lampiran 5. Data Ukuran Partikel…….. ………... 78
Lampiran 6 Data Uji Daya Lekat ... 82
Lampiran 7. Data Uji Iritasi Primer ... 85
Lampiran 8 Dokumentasi Pembuatan Bedak Tabur ... 86
Lampiran 9. Dokumentasi Karakteristik Ukuran Partkel Hari ke 0 Dan 30 pada tiap formula ……… 88
Lampiran 10. Dokumentasi Uji Iritasi Primer……….. 89
Lampiran 11 Dokumentasi Uji Stabilitas Warna ……… 91
Lampiran 12. Bahan dan Alat ... 94
Lampiran 13. Keterangan Determinasi ... 96
xviii
INTISARI
Tujuan dari penelitian yang bersifat eksperimental ini adalah untuk mengetahui stabilitas dan perbedaan sifat fisis bedak tabur berbahan dasar
Amylum Solani dan Amylum Manihot dengan menggunakan pewarna karotenoid dari umbi wortel. Stabilitas sifat fisis dari bedak tabur akan mempengaruhi mutu, keamanan, dan kualitas, baik selama penyimpanan ataupun pemakaian. Stabilitas sangat dipengaruhi oleh sifat fisika kimia komponen dalam bedak tabur. Sifat fisis yang diamati dalam penelitian ini adalah kandungan air, stabilitas warna, bulk density, daya lekat, ukuran partikel dan uji iritasi primer untuk melihat keamanannya.
Untuk mengevaluasi perbedaan yang signifikan pada sifat fisis bedak tabur pada tiap formula, maka digunakan analisis statistik menggunakan Oneway
ANOVA atau T test untuk data berdistribusi normal dan uji Kruskal-Wallis atau
Mann-Whitney untuk data berdistribusi tidak normal. Tingkat kepercayaan yang digunakan untuk analisis statistik adalah 95%.
Dari hasil uji didapatkan terjadi perubahan ukuran partikel, kandungan lembab, bulk density, warna yang signifikan (p<0,050) pada kedua formula selama penyimpanan. Dari hasil uji statistik didapatkan bahwa terdapat perbedaan ukuran partikel, kandugan lembab, stabilitas warna, bulk density yang berbeda pada kedua formula, yang dinyatakan dengan nilai p< 0,050. Sedangkan pada uji daya lekat tidak terjadi perbedaan yang signifikan antar kedua formula (p>0,050). Pada uji iritasi primer didapatkan nilai total respon adalah nol, sehingga bedak tabur bersifat kurang merangsang iritasi
xix
ABSTRACT
The purpose of this experimental study is to determine the stability and the differences seen in physical properties of loose powder based potato starch and cassava starch by using carotenoid pigments from the carrot. The physical properties of loose powder will affect the quality, security, and good quality during storage or usage. The stability is affected by the physical properties of chemical components in the powder. The physical properties which are observed in this research are moisture content, color stability, bulk density, particle size, adhesion of loose powder and irritation test for safety.
To evaluate the significant difference in the physical properties of each loose powder formula, the writer used statistical analysis using One way ANOVA or T test for normal distribution and Kruskal-Wallis test or the Mann-Whitney for abnormal distribution. The confident interval that is used for the statistical analysis is 95%.
The results obtained from the research are the significant changing of particle size, moisture content, bulk density, colors (p < 0,050) in both formulas. During the storage, statistical test proves that there are differences in particle size, moisture content, color stability, bulk density, for each formula which is indicated by p<0,050. Meanwhile, in adhesion test there is no significant difference occurred between the two formula (p>0,050). In primary irritation test brings the total value in all formula is zero, thus the loose powder are less in stimulating irritation.
1
BAB I PENGANTAR
A. Latar Belakang
Setiap wanita pasti berkeinginan untuk terlihat cantik dan menarik. Seorang wanita akan merasa lebih percaya diri apabila terlihat cantik. Kecantikan tersebut dapat diperoleh dari beberapa cara, salah satunya adalah dengan memakai
kosmetik.
Peneliti memilih bedak dengan pertimbangan bedak adalah salah satu
alat rias yang hampir dimiliki oleh semua wanita. Seorang wanita akan menggunakan bedak untuk menutupi segala kekurangan yang ada di permukaan
kulit dan memberi kesan terlihat mendekati sempurna (Fabricant, Stacey and Gould, 1993).
Akhir-akhir ini banyak kosmetik berbahaya yang beredar di pasaran.
BPOM menarik peredaran 27 merk kosmetik yang mengandung bahan berbahaya, salah satunya adalah bahan pewarna berbahaya. Bedak yang mengandung bahan
pewarna yang berbahaya akan mengakibatkan iritasi dan kanker (Anonim. 2009). Pemerintah Indonesia membatasi peredaran kosmetik mengandung pewarna berbahaya melalui Peraturan Menteri Kesehatan No.
239/Menkes/Per/V/85 yang menetapkan 30 zat pewarna berbahaya, dan menyarankan untuk menggunakan pewarna alami. Pada penelitian digunakan
Carotenoid memiliki warna kuning, orange, dan merah (Mortensen, 2009). Pada juice wortel mengandung 62,5 µg mL-1 β-karoten; 27,6 µg mL-1 α -karoten; 6,0 µg mL-1 lutein; 3,4 µg mL-1 13-cis-β-karoten; 1,3 µg mL-1
13,15-di-cis-β-karoten; 1,1 µg mL-115-cis-β-karotem; 1,1 µg mL-19-cis-β-karoten; 0,6 µg mL-113-cis-lutein; 0,4 µg mL-19 cis-lutein, 0,2 µg mL-113-cis-α-karoten; 0,2 µg
mL-19-cis-β-karoten (Chen, Peng and Chen, 1995).
Bedak biasanya menggunakan bahan dasar yang disebut talkum. Kelemahan Talkum adalah mudah pudar oleh keringat, tidak melekat baik pada
kulit dan terlalu mengkilat (Board, 2000). Dari kelemahan penggunaan Talkum ini maka perlu dilakukan upaya formulasi dengan menambah variasi bahan dasar
bedak, yaitu dengan menggunakan Amylum Manihot dan Amylum Solani menjadi pengganti Talkum sebagai bahan dasar bedak.
Amilum adalah bahan alami yang tidak larut dalam air dingin, bewarna
putih, tidak berasa, dan tidak berbau. Amilum beras adalah amilum yang pernah digunakan pada bedak traditsional (bedak dingin). Karena pemakaian bedak
dingin tidak praktis dan hasilnya tidak baik maka bedak dingin ditinggalkan dan digantikan oleh bedak tabur atau bedak padat (Anonim, 2010).
Penelitian ini menggunakan bahan dasar amilum dikarenakan amilum tidak berbahaya, dapat menjaga kelembapan kulit, dan tidak mengiritasi kulit (David, 2007). Amylum Manihot memiliki ukuran granul rata-rata 15µm. Amylum
pengganti talkum karena keduanya memenuhi kriteria basis bedak yaitu ukuran partikel tidak lebih dari 74µ m tidak larut dalam air dan minyak dan dapat menyerap sekresi minyak dan air pada wajah (Wilkinson and Moore, 1997: Singh,
2010).
Dalam penelitian ini amilum yang digunakan yaitu Amylum Manihot dan
Amylum Solani yang akan mempengaruhi sifat fisis bedak yang dihasilkan, seperti kandungan lembab, kompresibilitas (bulk density), daya lekat, ukuran partikel, stabilitas warna. Bedak yang dihasilkan selanjutnya akan diuji sifat fisisnya
meliputi bulk density, perubahan ukuran partikel, kandungan lembab, daya lekat, stabilitas warna, uji iritasi. Data yang diperoleh dibandingkan dengan
menggunakan uji Oneway ANOVA untuk lebih dari dua kelompok dan memiliki distribusi normal dan Kruskall-Wallis untukdata yang tidak berdistribusi normal. Untuk dua kelompok data menggunakan Pairet T test atau independent T test
untuk data berdistribusi normal dan Mann-Whitney untuk data berdistribusi tidak normal.
1. Perumusan Masalah
Berdasarkan latar belakang, rumusan masalah pada penelitian di atas adalah : apakah ada perbedaan sifat fisis (sifat alir, kompresibilitas (bulk density), kandungan lembab, mikromeritik, daya lekat, dan stabilitas warna) pada bedak
tabur berbahan dasar Amylum Manihot dan Amylum Solani dengan pewarna
2. Keaslian Penelitian
Sejauh penelusuran yang telah dilakukan oleh penulis, amilum telah digunakan sebagai bahan dasar sediaan bedak dingin, namun penggunaan Amylum
Manihot dan Amylum Solani sebagai bedak tabur dan pewarna carotenoid dari umbi wortel (Daucus Carota L.) belum pernah dilakukan.
3. Manfaat Penelitian
a. Manfaat teoritis. Dengan adanya penelitian ini, diharapkan dapat
diketahui apakah jenis amilum berbeda sebagai bahan dasar bedak mempengaruhi sifat fisis dari sediaan bedak tabur yang akan dibuat.
b. Manfaat praktis. Dengan adanya penelitian ini, diharapkan dapat menambah variasi bedak tabur yang telah ada dan memeberikan kemungkinan untuk dikembangkan menjadi sebuah peluang usaha.
B. Tujuan Penelitian
Untuk mengetahui apakah penggunaan jenis amilum yang berbeda sebagai bahan dasar bedak akan memberikan sifat fisis yang berbeda, meliputi
5
BAB II
PENELAAHAN PUSTAKA
A. Wortel
Gambar 1. Wortel (Daucus carota L.)
(Anonim, 2010)
1. Keterangan Botani
Wortel (Daucus carota L.) tumbuh di daerah sejuk bertemperatur 20°C, dapat tumbuh baik pada ketinggian 500-1000 m, dan dapat tumbuh disepanjang
tahun (Setiawan, 2001).
Umbi wortel terbentuk dari akar tunggang yang berubah fungsi menjadi tempat penyimpanan cadangan makanan (karbohidrat, protein, lemak, vitamin,
berdiameter 3.5 cm. Berat umbi dapat mencapai 300 g sedangkan yang berukuran kecil mempunyai berat 100 g (Mumun,2011).
Wortel dengan jenis Nantes merupakan jenis wortel dengan panjang
15-17cm. Ujung umbi wortel nantes tumpul. Bagian xylem hampir memiliki warna yang sama dengan bagian cortex (Masley,2010).
2. Kandungan Wortel
Wortel merupakan umbi yang telah diketahui mengandung banyak
kandungan pigmen carotenoid. Pada juice wortel mengandung 62,5 µg mL-1 β -karoten; 27,6 µg mL-1 α-karoten; 6,0 µg mL-1 lutein; 3,4 µg mL-1 13-cis-β
-karoten; 1,3 µg mL-1 13,15-di-cis-β-karoten; 1,1 µg mL-1 15-cis-β-karotem; 1,1 µg mL-1 9-cis-β-karoten; 0,6 µg mL-1 13-cis-lutein; 0,4 µg mL-1 9 cis-lutein, 0,2 µg mL-1 13-cis-α-karoten; 0,2 µg mL-1 9-cis-β-karoten (Chen, Peng, and Chen,
1995).
B. Kulit
Kulit merupakan organ terluas yang menutupi seluruh permukaan tubuh.
Gambar 2. Diagram epidermis dengan perbedaan lapisan epidermis dan komponen
penyusunnya.
(Draelos, 2010).
1. Epidermis
Merupakan lapisan kulit terluar yangyang tersusun dari stratum corneum,
stratum licudum, Rein’s barrier, stratum granulosum, stratum spinosum, dan
stratum germinativum. Stratum corneum berada pada lapisan paling luar dari
epidermis (Jellinek, 1970).
Stratum corneum merupakan lapisan sel tanpa inti sel sehingga disebut
sel mati yang terdiri dari keratin, protein tidak larut air dan mempunyai kelembapan yang rendah (sekitar 10%). Walaupun kelembapannya rendah, tapi berperan penting dalam menentukan kelembutan dan fleksibilitas kulit.
Permukaan stratum corneum tertutup oleh sebum dan keringat yang berfungsi menjaga fleksibilitas kulit dan mengatur kelembapan lapisan kulit yang berada di
2. Corium (dermis)
Terdiri dari jaringan pengikat dan serabut kolagen yang menentukan elastisitas kulit. Antara epidermis dan corium dihubungkan dengan lapisan kapiler
yang akan menjadi pipih seiring bertambahnya usia sehingga elastisitas kulit berkurang. Pembuluh darah kapiler dan ujung saraf terdapat pada vagan corium.
Tepatnya pada lapisan retikuler (Jellinek, 1970).
3. Hipodermis
Terdiri atas jaringan pengikat yang mengandung sel lemak yang berfungsi sebagai pelindung getaran mekanik dan cadangan lemak (Jellinek,
1970).
C. Bedak
Bedak wajah (face powder) merupakan kosmetik yang telah lama digunakan dengan tujuan membuat wajah lebih menarik dan cantik dengan cara
menutupi bintik hitam (liver spots), menutupi kilauan akibat adanya sekresi kelenjar sebaseus dan kelenjar keringat. Bedak wajah harus bersfat tahan lama
D. Bedak Tabur (loose powder)
Gambar 3. Bedak tabur
(Anonim, 2011). Bedak tabur adalah bedak kering yang hampir semua bahan bakunya
terbuat dari serbuk bahan bedak. Pembuatan bedak tabur cukup mudah, yaitu dengan cara mencampurkan bahan bedak dan pigmen dengan blender. Kemudian
penambahan pewangi (perfume). Pencampuran bedak harus homogen dan tahap terakhir adalah tahap pengayakan bedak untuk mencapai ukuran yang ditentukan (Matsui, 1997).
E. Komponen penyusun bedak
1. Daya penutupan bedak (Covering powder)
Bedak harus dapat menyembunyikan berbagai cacat pada wajah, misalnya belang, kerutan diwajah, pori-pori besar dan juga dapat menutupi
dalah satunya dapat diperoleh dari titanium dioksida (Wilkinson and Moore, 1997).
Titanium dioksida (titanium dioxide). Titanium dioksida merupakan
pigmen putih yang memiliki kemampuan yang baik dalam menutupi noda atau cacat oleh karena mimiliki opacity yang baik. Bersifat inert, stabil terhadap panas
dan cahaya, serta mudah diformulasikan dalam semua jenis produk kosmetik (Butler, 2000).
2.Daya serap (Absorbency)
Kemampuan bedak wajah untuk mengeliminasi kilauan pada kulit
melalui proses penyerapan sekresi minyak dan keringat merupakan hal penting. Sehingga pada formulasi bedak wajah diperlukan bahan-bahan yang memiliki kapasitas serapan tinggi. Biasanya bahan yang digunakan adalah amilum (starch)
(Butler, 2000).
Amilum (starch). Amilum merupakan serbuk putih tidak berbau,
memiliki kelarutan yang rendah dalam air (Depkes RI., 1995). Selain itu memiliki daya serap sekresi minyak dan keringat yang baik sehingga akan menutupi
kekurangan seperti kilauan pada wajah. Ukuran partikel amilum yang kecil (µ m) akan memberikan kelembutan ketika diaplikasikan pada kulit (Wilkinson and Moore,1997). Amilum tersusun dari amilosa dan amilopektin. Tiap-tiap tanaman
rata-rata sebesar 27 µ m dan mengandung 20-23% amilosa. Pada Amylum Manihot mengandung amilosa sebesar 17-20%, dengan diameter granul sekitar 4-35 µm, diameter rata-rata sebesar 15 µm (BeMiller and Whistler, 2009).
Gambar 4. Struktur amilopektin pada amilum
Gambar 5. Struktur amilosa pada amilum
(Bowen, 2006).
3. Daya lekat (Adhesion)
Daya lekat menggambarkan seberapa baik bedak melekat pada wajah. Daya lekat ini diperoleh dari penggunaan magnesium stearat.
Magnesium stearat. Magnesium Stearat sering disebut dengan garam magnesium yang mengandung dua stearat (anion dari asam stearat) dan satu
kation (Mg 2+), dengan rumus [CH3(CH2)16COO]2Mg.. Sifat dari magnesium stearat adalah tidak larut dalam air , etanol (95%), eter dan meleleh pada sekitar
Gambar 6. Struktur magnesium stearat
( Anonim, 2011). 4. Pewarna
Pewarna merupakan bahan tambahan dalam sebuah produk kosmetik
dekoratif, seperti bedak. Fungsi utama pewarna adalah menyamarkan bintik atau noda serta menghasilkan warna yang indah untuk menciptakan daya tarik. Pewarna diklasifikasikan menjadi pewarna bahan organik sintetik, pigmen
inorganik dan pewarna alami (Matsui, 1997).
a. Organik Sintetik. Dyes dan lakes merupakan contoh dari jenis pewarna
organik sintetik. Dyes merupakan pewarna yang larut pada air, minyak, alcohol. Dyes sering digunakan pada lipstick, tetapi tidak cocok digunakan pada bedak
karena akan meninggalkan noda pada kulit. Lakes merupakan pewarna tidak larut pada air dan biasa digunakan pada cat kuku (Butler, 2000).
b. Pigmen inorganik. Pigmen innorganik lebih stabil pada panas dan
cahaya dari pada pigmen organik. Pigmen ini sangat sering digunakan dalam produk kosmetik seperti bedak dan rias mata. Contoh dari pigmen innorganik
adalah titanium dioxide, zinc oxide, alumina, dan sebagainya (Butler, 2000). c. Pewarna alami. Pewarna alami berasal dari tumbuhan dan hewan, serta dari mikroorganisme. Dibandingkan dengan warna sintetis, mereka memiliki
digunakan. Tetapi karena dasar keamanan, akhir-akhir ini dipertimbangkan untuk memakai pewarna alami. Contoh pewarna alami adalah senyawa carotenoid
(Matsui, 1997).
d. Carotenoid. Carotenoid merupakan pigmen yang disintesis oleh tanaman, alga, bakteri fotosintetik, yang berwarna kuning, orange, dan merah dan
larut dalam minyak (Asgar and Musaddad, 2006). Karoten dapat terdegradasi cepat mulai pada suhu 60oC, cahaya, dan oksigen. Contoh karoten adalah α -carotene, β-carotene, β-cryptoxanthin, lutein, lycopene, zeaxanthin (Mortensen,
2009).
5. Pengawet
Bahan pengawet adalah bahan yang digunakan untuk mencegah kerusakan kosmetik yang disebabkan oleh mikroorganisme. Mikroorganisme
dapat mengkontaminasi kosmetik dan menyebabkan timbulnya bau yang tak sedap, perubahan warna dan gangguan kesehatan pada konsumen (Tranggono,
Iswari and Latifah, 2007)
Metil paraben. Metil paraben banyak digunakan sebagai pengawet dalam
kosmetik, produk makanan dan formulasi farmasi. Pada kosmetik, metil paraben adalah pengawet yang paling sering digunakan. Paraben paling efektif terhadap ragi dan kapang. Aktifitas antimikrobia paraben meningkat seiring dengan rantai
Gambar 7. Struktur Metil Paraben
F. Uji sifat fisis
1. Pengujian Mikromeritik
Sifat fisik suatu sediaan dipengaruhi beberapa faktor, diantaranya adalah ukuran partikel. Mikromeritik merupakan cara yang digunakan untuk mengetahui
ukuran partikel. Pada umumnya dalam suatu kumpulan partikel terdapat lebih dari satu ukuran. Satuan ukuran partikel yang sering digunakan adalah micrometer
(µm) (Yoshita, 1993).
2. Pengujian Pengetapan
Selain untuk mengetahui sifat alir suatu serbuk, metode pengetapan juga dapat mengukur bobot bulk density serbuk. Bulk density merupakan perbandingan
antara berat massa dan volume massa. Bulk density tergantung pada bentuk dan ukuran partikel penyusun bedak. Partikel berbentuk bulat maka bobot jenisnya meningkat. Bila ukuran granul besar bobot jenisnya menurun. Pengujian
Pengetapan dilakukan hingga mencapai volume akhir yang kosntan. Pengujian ini menggunakan tabung silinder yang dinamai volumeter (Board, 2000).
3. Pengujian Kandungan Lembab
Tujuan uji ini untuk mengetahui kandungan lembab bedak seiring dengan
bertambahnya waktu penyimpanan. (Tranggono, Iswari and Latifah , 2007). Uji tersebut menggunakan metode gravimetri yaitu salah satu metode analisis kandungan air dalam serbuk (Basser, Denney, Jeffery and Mendham, 1994).
Amilum memiliki sifat higroskopis yang mengabsorbsi air 10-17 % pada kondisi temperature ruangan (Akade, 1988).
4. Pengujian Stabilitas Warna
Uji Stabilitas warna bertujuan untuk mengetahui kesetabilan warna jika
ditempatkan pada kondisi lingkungan yang berbeda (tingkat cahaya,suhu, dan sebagainya) untuk jangka waktu tertentu. Warna tersebut dapat dikatakan stabil
apabila perubahan tersebut tidak jauh dari warna semula (Perry, 2009). Pengukuran intensitas dan stabilitas warna menggunakan Munsell Color Charts.
5. Pengujian Iritasi primer
Iritasi primer adalah suatu reaksi kulit terhadap zat kimia misalnya alkali
pemborokan. Iritasi primer terjadi di tempat kontak dan umumnya pada sentuhan pertama (Lu, 1995).
Suatu rangsanagan kimia langsung pada jaringan disebabkan oleh zat
yang mudah bereaksi dengan berbagai bagian jaringan. Biasanya zat ini tidak mencapai peredaran darah, karena langsung bereaksi dengan tempat jaringan yang
pertama berhubungan. Organ tubuh yang terlibat terutama mata, hidung, tenggorokan, trakea, epitel, alveolus, esophagus dan kulit (Ariens, Simons dan Mutschler, 1985). Bila zat ujinya berupa zat padat, maka zat itu dilarutkan dalam
suatu pelarut misalnya minyak nabati atau aquadest (Loomis, 1978).
6. Pengujian Daya Lekat
Daya lekat merupakan gambaran penting dari komponen bedak tabur yang menggambarkan kemampuan bedak tabur melekat pada wajah. Daya lekat
dapat ditimbulkan oleh zinc stearat atau magnesium stearat dengan penggunaan berkisar 3-10% (Wilkinson and Moore, 1997).
G. Analisis hasil
Analisis ragam atau analysis of variance (ANOVA) adalah suatu metode untuk menguraikan keragaman total data menjadi komponen komponen yang mengukur berbagai sumber keragaman. Secara aplikatif, ANOVA digunakan
distribusi normal dan varians data yang sama. Jika tidak memenuhi syarat, maka dilakukan transformasi data supaya distribusi menjadi normal dan varians menjadi sama. Apabila variabel hasil transformasi tidak berdistribusi normal atau varians
tetap tidak sama, maka dipilih alternatifnya dengan menggunakan uji Kruskal-Wallis. Jika pada uji ANOVA atau Kruskal-wallis menghasilkan nilai p< 0,05
maka dilanjutkan dengan melakukan analisis Post hoc (Dahlan, 2011).
Uji-t merupakan uji untuk menilai signifikansi dua sampel. jika dihubungkan dengan kebebasan (independency) sampel yang digunakan, maka
uji-t dibagi lagi menjadi 2, yaitu uji-t untuk sampel bebas (independent) dan uji-t untuk sampel berpasangan (paired). Untuk menilai signifikansi dua sempel tidak
berpasangan dan berdata normal digunakan unpaired T test (untuk data normal) dan Mann-Whitney (untuk data yang tidak normal). Untuk data berpasangan dan bedistribusi normal digunakan paired T test, dan untuk data berdistribusi tidak
normal digunakan Mann Whitney (Dahlan, 2011).
H. Landasan Teori
Amilum secara luas telah digunakan pada industri kosmetik, sedangkan
pewarna carotenoid belum dikembangkan pada industri kosmetik seperti bedak tabur. Bedak tabur merupakan salah satu kosmetik yang banyak digunakan. Untuk membuat suatu bedak tabur harus mempertimbangkan aspek formulasi dan
Amilum bersifat higroskopis, tidak larut dalam minyak dan air dingin. Pada Amylum Solani diameter granul sekitar 5-100 µ m dengan diameter rata-rata sebesar 27 µ m sedangkan pada Amylum Manihot memiliki ukuran partikel 4-35
µ m dengan ukuran partikel rata-rata 15 µm. Dilihat dari sifat tersebut, maka amilum cocok untuk menjadi suatu bahan dasar bedak wajah. Dilihat dari
komposisinya, amilum merupakan suatu kompleks karbohidrat yang tersusun dari 2 komponen, yaitu amilosa dan amilopektin. Pada Amylum Manihot terdapat 17-20% amilosa dan pada Amylum Solani terdapat sekitar 21% amilosa. Perbedaan
kedua amilum tersebut akan memberikan kestabilan fisis (kandungan lembab pada bedak, bulk density, ukuran partikel) yang berbeda antar kedua bahan dasar bedak.
Pewarna merupakan salah satu bahan tambahan yang digunakan pada sediaan bedak tabur. Untuk memilih jenis pewarna, perlu dipertimbangkan dari segi keamanan dan dan sifat kimia dari pewarna yang digunakan. Carotenoid
merupakan jenis pewarna alami yang telah disetujui oleh Food and Drug Administration dalam hal keamananya. Carotenoid dapat terdegradasi oleh
adanya oksigen, cahaya dan panas diatas 60oC. Dilihat dari kepolarannya,
carotenoid cenderung memiliki sifat non polar.
Dari sifat fisika dan kimia yang dimiliki amilum dan carotenoid maka dilakukan formulasi dan uji kesetabilan sifat fisis. Dari penelitian ini dilakukan untuk mengetahui dan membandingkan sifat fisis bedak dengan bahan dasar
pada tiap formula, maka digunakan analisis statistik menggunakan One Way Anova dan uji paired T untuk data berdistribusi normal dan uji Kruskal Wallis dan uji Mann-Whitney untuk data berdistribusi tidak normal.
Sifat fisis bedak tabur ini juga akan dibandingkan dengan sifat fisis bedak tabur yang telah beredar dipasaran. Apabila sifat fisis bedak tabur secara
statistik tidak berbeda dengan sifat fisis bedak tabur yang ada dipasaran, maka dapat diasumsikan bedak tabur yang telah dibuat dapat diterima oleh masyarakat luas. Pembandingan dengan bedak tabur yang telah beredar dipasaran ini
dilakukan guna mengetahui apakah bedak tabur yang diformulasikan ini memiliki potensi untuk diterima oleh konsumen jika produk ini dipasarkan.
I. Hipotesis
Bedak tabur berbahan dasar Amylum Solani memiliki sifat fisis yang
20
BAB III
METODOLOGI PENELITIAN
A. Jenis Rancangan Penelitian
Penelitian dengan judul Formulasi dan Perbandingan Sifat Fisis Bedak
Tabur Berbahan Dasar Amylum Solani (Solanum tuberosum L.) dan Amylum Manihot (Manihot utilissima L.) dengan Pigmen Carotenoid dari Umbi Wortel (Daucus carota L.) sebagai pigmen alami ini merupakan jenis penelitian
eksperimental.
B. Variabel Penelitian
1. Variabel bebas dalam penelitian ini adalah jenis amilum yaitu Amylum
Manihot , Amylum Solani serta intensitas cahaya (terang dan gelap pada uji stabilitas warna)
2. Variabel tergantung dalam penelitian ini adalah sifat fisis bedak tabur yang
meliputi kandungan air, stabilitas warna, bulk density, daya lekat, ukuran partikel dan iritasi.
3. Variabel pengacau terkendali yaitu suhu oven dan suhu lemari pendingin 4. Variabel pengacau tak terkendali adalah panas akibat putaran blender,
C. Definisi Operasional
1. Bedak Wajah (face powder) merupakan kosmetik dekoratif yang digunakan untuk pemakaian pada wajah
2. Bedak Tabur (loose powder) merupakan bedak berbentuk serbuk yang digunakan untuk pemakaian pada wajah.
3. Umbi wortel yang digunakan merupakan jenis wortel nantes.
4. Sari wortel (juice wortel) diperoleh dari wortel dengan menggunakan juice extractor tanpa ada pengenceran.
5. Cake bedak adalah bentuk padatan bedak yang diperoleh setelah pengeringan komponen bedak dengan oven.
6. Mikromeritik merupakan metode yang digunakan untuk mengukur ukuran partikel bedak dengan mikroskop Motic B3 Proffesional Series.
7. Pengetapan (bulk density test) merupakan metode pengukuran yang digunakan
untuk mengetahui sifat alir bedak tabur.
8. Pengujian kandungan lembab adalah menyatakan jumlah lembab (air) yang
terabsorbsi pada komponen bedak dengan menggunakan alat Moisture Balance.
9. Absorbency adalah kemampuan bahan bedak dalam menyerap kandungan lembab atau sekresi keringat dan minyak
10.Uji stabilitas warna digunakan untuk mengetahui kesetabilan warna yang
11.Iritasi primer adalah suatu reaksi kulit terhadap zat kimia yang terjadi di tempat kontak dan umumnya pada sentuhan pertama
12.Respon adalah besaran yang diamati, dalam penelitian ini adalah sifat fisis
bedak yang meliputi kandungan air, stabilitas warna, bulk density, daya lekat, ukuran partikel dan respon iritasi primer
D. Bahan Penelitian
Bahan-bahan yang digunakan dalam penelitian ini adalah Amylum
Manihot (Manihot utilissima L.), titanium dioksida, metil paraben, Mg stearat (Bratachem®), Amylum Solani (Solanum tuberosum L.) dan sari umbi wortel
nantes (panjang umbi 15-17cm, diameter umbi 2,5-3,5cm dan diameter xylem
±1cm cortex dan xylem berwarna orange).
E. Alat Penelitian
Alat yang digunakan dalam penelitian ini adalah Juicer (Miyako),
blender (Sanyo), mikroskop (Motic, B3 Proffesional Series), Munsell Color System Chart, alat-alat gelas pada umumnya, sofware Motic Image Plus 2.0.,
F. Tata Cara Penelitan 1. Formulasi Bedak Tabur
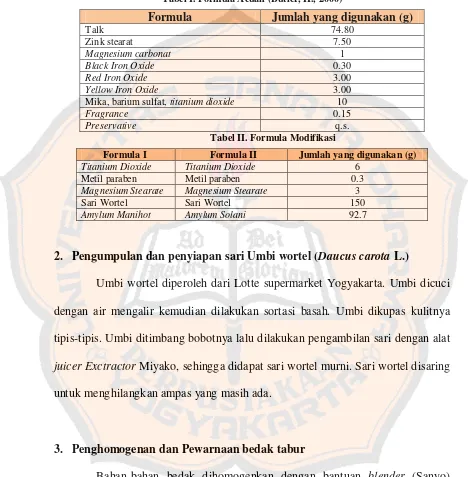
Tabel I. Formula Acuan (Butler, H., 2000)
Formula Jumlah yang digunakan (g)
Talk 74.80
Zink stearat 7.50
Magnesium carbonat 1
Black Iron Oxide 0.30
Red Iron Oxide 3.00
Yellow Iron Oxide 3.00
Mika, barium sulfat, titanium dioxide 10
Fragrance 0.15
Preservative q.s.
Tabel II. Formula Modifikasi
Formula I Formula II Jumlah yang digunakan (g)
Titanium Dioxide Titanium Dioxide 6 Metil paraben Metil paraben 0.3
Magnesium Stearate Magnesium Stearate 3 Sari Wortel Sari Wortel 150
Amylum Manihot Amylum Solani 92.7
2. Pengumpulan dan penyiapan sari Umbi wortel (Daucus carota L.)
Umbi wortel diperoleh dari Lotte supermarket Yogyakarta. Umbi dicuci dengan air mengalir kemudian dilakukan sortasi basah. Umbi dikupas kulitnya tipis-tipis. Umbi ditimbang bobotnya lalu dilakukan pengambilan sari dengan alat
juicerExctractor Miyako, sehingga didapat sari wortel murni. Sari wortel disaring untuk menghilangkan ampas yang masih ada.
3. Penghomogenan dan Pewarnaan bedak tabur
dikeringkan dengan oven pada suhu 40-45OC. Dilakukan pengecilan ukuran serbuk bedak dengan menggunakan blender kering (Sanyo) dan serbuk bedak diayak dengan ayakan dengan nomer Mesh 400.
4. Pengambilan sampel
Dalam penelitian ini dibuat 3 kali replikasi pada tiap setiap formula percobaan yaitu formula I dan II. Masing-masing replikasi tersebut kemudian diuji dan diamati stabilitas fisiknya melalui uji bulk density, kandungan air,
stabilitas warna, ukuran partikel serta uji tabahan yaitu uji iritasi dan daya lekat.
5. Pengujian mikromeritik
Microscope disiapkan dan dikalibrasi. Bedak disiapkan dalam bentuk suspensi cair, dipreparasi pada gelas objek, lalu dilihat dibawah mikroskop.
Digunakan pengambilan gambar partikel bedak tabur sebanyak 300 partikel. Pengujian dilakukan pada bedak pada hari ke 0 dan ke 30. Pengukuran ukuran
partikel menggunakan sofware Motic Image Plus 2.0.
6. Pengujian Pengetapan
Kerapatan nyata. 110 g bedak tabur ditimbang, kemudian dimasukkan ke dalam tabung volumenometer dan volume dicatat sebagai vo. Kerapatan nyata
adalah bobot bedak tabur dibagi dengan volume awal bedak tabur.
Kerapatan mampat. 110 g bedak tabur ditimbang, kemudian dimasukkan ke dalam tabung volumenometer dan volume dicatat sebagai vo. Tabung dihentakkan hingga volume bedak tabur konstan (vt). Kerapatan mampat adalah
bobot bedak tabur dibagi dengan volume bedak tabur konstan.
Kerapatan mampat= (g/mL)
Kompresibilitas. Pengujian kompresibilitas digunakan untuk mengetahui sifat alir bedak tabur yang dibuat. Kompresibilitas dilihat dari indeks Carr yang
sangat bergantung pada kerapatan nyata maupun kerapatan mampat. Kompresibilitas dinyatakan dalam persen. Semakin besar harga indeks Carr (C%) maka sifat alir bedak tabur semakin buruk.
Indeks Carr= x 100%
Hubungan antara indeks Carr dengan sifat alir granul dapat dilihat pada tabel III.
Tabel III. Hubungan sifat alir dan kompresibilitas berdasarkan indeks Carr
Kompresibilitas (%) Sifat Alir
5-15 Excellent (free flowing granules)
12-16 Good (free flowing powdered granules)
18-21 Fair (powdered granules)
23-28 Poor (very fluid powder)
28-35 Poor (fluid cohesive powder)
35-38 Very poor
>40 Extremely poor
(Aulton, 2002). 7. Pengujian kandungan lembab
Bedak dengan berat sekitar 5 gram ditempatkan secara merata pada krus,
(Zhang, Law and Chakrabarti, 2003). Uji dilakukan pada hari ke 0, 2, 10, 20 dan 30 dengan replikasi 3 kali tiap formula
8. Pengujian Stabilitas Warna
Pada uji stabilitas warna, tiap replikasi formula dikondisikan dengan
terpapar cahaya (tidak terbungkus aluminium foil) dan tidak terpapar cahaya (dibungkus aluminium foil). Penilaian stabilitas warna dilakukan observasi secara visual, yang dideterminasi dengan menggunakan Munsell colour charts.
Pengujian ini dilakukan pada hari ke 0,2,10,20,30.
9. Pengujian iritasi
Ditaburkan 0.5 gram bedak pada kulit punggung kelinci yang telah dicukur bulunya. Kasa diikatkan dengan cermat pada bagian yang ditaburi bedak
selama 48 jam. Reaksi kulit yang terlihat diamati dan diberi angka sesuai dengan tingkat (1) eritema dan pembentukan kerak (eschar) dan (2) pembentukan edema.
Pembacaan reaksi kulit juga dilakukan pada jam ke 48 (Lu, 1995).
Tabel IV. Evaluasi Reaksi Iritasi Kulit (Lu, 1995)
Jenis Iritasi Skor
Eritema
Tanpa eritema 0
Eritema hampir tidak tampak 1
Eritema berbatas jelas 2
Eritema moderat sampai berat 3 Eritema berat (merah bit) sampai sedikit membentuk kerak 4
Edema
Tanpa edema 0
Edema hampir tidak tampak 1
Edema tepi berbatas jelas 2
Rata-rata skor eritrema dan edema keseluruhan dicari selama 48 jam. Akan didapatkan indeks iritasi primer.
Tabel V. Kriteria Iritasi (Lu, 1995)
Indeks Iritasi Kriteri Iritasi senyawa Kimia < 2 Kurang merangsang
2-5 Iritan Moderat >6 Iritan Berat
10. Pengujian daya lekat
Ditaburkan 0,1 g bedak pada kulit seluas 5cm2. Gelas objek ditimbang
sehingga memperoleh bobot mula. Gelas objek seluas 5 cm2 ditempel pada daerah yang telah ditaburi bedak dan diberi beban pada atasnya seberat 5 g (3 menit).
Gelas objek yang telah ditempeli bedak ditimbang sebagai bobot akhir.
G. Analisis Hasil
Data yang dihasilkan adalah berupa data hasil pengamatan uji stabilitas dan uji keamanan kedua formula bedak wajah yang meliputi kandungan air,
stabilitas warna, bulk density, daya lekat, ukuran partikel. Hasil tiap uji stabilitas sifat fisis kedua formula serta bedak yang telah beredar dipasaran dibandingkan. Hasil yang diperoleh dianalisis secara statistik dengan menggunakan Oneway
ANOVA (lebih dari dua kelompok) dan Ttest (dua kelompok) untuk data berdistribusi normal. Untuk data yang berdistribusi tidak normal digunakan
metode Kruskal-Walis (lebih dari dua kelompok) atau Mann-Whitney (dua kelompok). Penarikan kesimpulan dilakukan dengan menggunakan taraf
28
BAB IV
HASIL DAN PEMBAHASAN
A. Formulasi
Formula yang digunakan pada penelitian ini adalah modifikasi formula
bedak tabur yang diperoleh pada acuan Butler (2000). Bahan-bahan yang digunakan dalam pembuatan bedak tabur ini antara lain Titanium dioksida, metil paraben, magnesium stearat, sari wortel, dan amilum. Pada penelitian ini, peneliti
membuat dua formula, dimana antara formula I dengan formula II terdapat perbedaan pada bahan dasar bedak tabur yang digunakan. Pada formula I
menggunakan bahan dasar Amylum Manihot dari umbi singkong, dan pada formula II menggunakan bahan dasar Amylum Solani dari umbi kentang.
Bahan pewarna merupakan bahan yang penting bagi suatu sediaan
kosmetik. Selain dapat menambah nilai keindahan pada bentuk sediaan, pewarna juga dapat digunakan untuk menambah kesan warna natural dan menutupi cacat
seperti pori-pori besar dan luka pada wajah atau noda pada wajah (daya covering) (Wilkinson and Moore, 1997). Pada kosmetik digunakan pewarna yang
menyerupai warna kulit untuk menambah kesan warna natural pada wajah. Pada penelitian ini digunakan pewarna alami yang didapat dari sari wortel dan daya penutupan (covering) didapatkan dari titanium dioksida.
adalah bedak wajah (Butler, 2000). Sifat opac pada titanium dioksida ini membantu dalam hal penutupan noda dan cacat (daya covering) yang baik pada kulit wajah. Selain itu, titanium dioksida juga bersifat inert, stabil terhadap cahaya
dan panas sehingga tahan terhadap proses pembuatan kosmetik yang terkadang membutuhkan panas (Butler, 2000). Titanium dioksida bukanlah suatu astringent,
sehingga kerap kali digunakan untuk bedak wajah yang digunakan untuk kulit normal tanpa sekresi minyak yang berlebihan. Untuk membantu penyerapan keringat dan minyak pada wajah biasanya ditambahkan bahan absorbency, yang
salah satunya adalah amilum (starch).
Salah satu fungsi penting dari bedak wajah adalah dapat mengeliminasi
kilauan pada kulit akibat adanya sekresi keringat dan minyak. Sehingga pada formulasi bedak wajah perlu ditambahkan bahan absorben yang dapat menyerap keberadaan minyak dan keringat pada wajah. Amilum (starch) telah diketahui
memiliki daya serap minyak dan keringat yang baik.
Pada penelitian ini digunakan Amylum Solani dan Amylum Manihot.
Amylum Solani memiliki bentuk partikel yang oval dan sferis sedangkan Amylum Manihot memiliki bentuk partikel bulat sehingga jika digunakan pada formulasi
bedak tabur tidak akan melukai dan mengiritasi kulit wajah. Amylum Solani
diameter ± 5-100µ m dengan diameter rata-rata sebesar 27µ m, sedangkan Amylum Manihot memiliki diameter partikel 4-35µ m dan rata-rata diameter 15µ m dilihat
Amilum memiliki daya absorbency yang baik, sehingga dapat menyerap sekresi keringat dan minyak pada wajah. Daya absorbency ini berperan dalam mengurangi kilauan pada wajah sehingga akan diperoleh wajah yang fresh.
Interaksi hidrogen antara amilum dan kandungan air pada keringat, serta interaksi antara amilum dan komponen minyak (fatty acid, triglyseride, wax esters) pada
wajah berperan dalam mekanisme penyerapan sekresi keringat dan minyak.
O
Gambar 8. Interaksi hidrogen antara amilum dan kandungan air pada keringat
Amilum memiliki sifat yang higroskopis sehingga dapat menyerap
kandungan air (pada ruangan dan keringat) (daya absorbency). Sifat higroskopis tersebut dikarenakan oleh gugus hidroksi (-OH) pada amilum yang dapat
O H
Sekresi minyak (sebum) merupakan salah satu penyebab kilauan pada wajah sehingga akan mengurangi penampilan. Komposisi sebum adalah
triglycerides, fatty acids, diglycerides sebanyak 57%, wax esters sebanyak 25%,
squalene sebanyak 13% dan 2 % cholesterol (Huang, Lin and Fang, 2009). Adanya interaksi hidrogen antara gugus hidroksil (-OH) pada amilum dan
komponen penyusun sebum akan membuat sebum terserap pada amilum.
Dalam formulasi suatu bedak, juga digunakan bahan adhesif. Bahan adhesif ini sangat penting untuk menjamin bedak akan dapat menempel dengan
baik pada kulit wajah. Daya adhesif ini dapat didapatkan dengan menambahkan
magnesium stearate sebanyak 3-10% (Rowe, Sheskey, and Quinn, 2009). Rantai
panjang hidrofobik pada Mg stearate akan berinteraksi dengan membran kulit yang juga memiliki sifat nonpolar, sedangkan bagian polar akan berinteraksi dengan gugus polar komponen bedak sehingga dapat membantu pelekatan antara
komponen bedak dengan kulit wajah. Mg stearate juga dapat digunakan sebagai
lubricant atau bahan pelicin yang dapat memperbaiki sifat alir sehingga
memberikan kemudahan untuk bedak tabur mengalir pada saat proses filling. Untuk mengurangi atau mencegah terjadinya kontaminasi mikrobia,
maka dalam suatu formulasi sediaan kosmetik perlu ditambahkan bahan pengawet. Batasan bahan pengawet adalah ≤ 3%. Bahan pengawet yang
B. Pembuatan Bedak Wajah (Loose Powder)
Sediaan yang dibuat dalam penelitian ini adalah bedak tabur dekoratif yang diaplikasikan pada wajah. Pada bedak wajah yang dibuat digunakan pewarna
alami yang diperoleh dari sari umbi wortel. Pewarna alami digunakan karena lebih aman dari pada pigmen sintetis.
Wortel merupakan umbi yang telah diketahui mengandung banyak kandungan carotenoid. Pada juice wortel mengandung 62,5 µg mL-1 β-karoten; 27,6 µg mL-1α-karotene; 6,0 µg mL-1 lutein; 3,4 µg mL-113-cis-β-karoten; 1,3 µg
mL-1 13,15-di-cis-β-karoten; 1,1 µg mL-1 15-cis-β-karoten; 1,1 µg mL-1 9-cis-β -karoten; 0,6 µg mL-113-cis-lutein; 0,4 µg mL-19 cis-lutein, 0,2 µg mL-113-cis-α
-karoten; 0,2 µg mL-19-cis-β-karoten (Chen, Peng and Chen, 1995).
Semakin tua intensitas warna wortel (jingga-merah) maka semakin banyak proporsi β-karotennya. Intensitas warna ini meningkat seiring dengan
pertambahan usia umbi wortel. Konsentrasi carotenoid pada jaringan luar (cortex) lebih besar dari pada bagian core (xylem) (Britton, Jensen and Pfander, 2009).
Pada penelitian ini digunakan wortel nantes berdiameter 2,5-3,5cm dengan panjang 15-17cm dan diameter xylem ±1cm untuk mendapatkan kandungan
carotenoid yang hampir sama pada tiap buah.
Apabila pigmen carotenoid ini diaplikasikan pada formula bedak akan menghasilkan warna orange muda (peach) yang akan membuat kesan pewarnaan
carotenoid tidak dapat masuk stratum corneum dan tidak dapat memberikan efek antioksidan. Suatu zat akan dapat terpenetrasi pada lapisan stratum corneum apabila memiliki bobot molekul kecil yaitu <500 dalton, memiliki sifat lipofilik
dan memiliki koefisien partisi antara 10-1000. Untuk membantu penetrasi kedalam kulit dapat dilakukan menambahkan enhancer pada formula
(Daniels,2004). Pada penelitian ini efek daya antioksidan tidak diteliti lebih lanjut dan carotenoid yang digunakan hanya sebagai pewarna dalam formulasi bedak.
Hal pertama yang dilakukan adalah pembuatan sari wortel. Sari wortel
didapatkan dengan alat juice extractor yang akan memeras umbi wortel. Digunakan alat juice extractor karena dengan alat ini tidak dibutuhkan
penambahan air (pengenceran) untuk mengambil sari wortel. Sari wortel dihomogenkan dengan cara diaduk.
Sari wortel ini dicampurkan pada bahan bedak lainnya (kecuali Mg
stearat) yang sebelumnya telah dihomogenkan. Sari wortel yang digunakan untuk 100 g bedak tabur adalah 150 g. Penghomogenan serbuk dilakukan dengan
bantuan blender selama 1 menit (waktu penghomogenan optimal serbuk). Penghomogenan serbuk bedak ini berguna untuk memperkecil ukuran partikel
serta menghomogenkan semua komponen serbuk bedak.
Setelah sari wortel ditambahkan dilakukan juga penghomogenan warna. Penghomogenan warna dilakukan untuk membasahi semua serbuk bedak oleh
orentasi,) dimana pada waktu 6 hari itu didapat pewarnaan bedak yang paling baik. Waktu 6 hari ini menggambarkan bahwa kandungan carotenoid telah terserap sempurna pada komponen serbuk bedak.
Untuk menghasilkan bedak yang kering, maka dilakukan pengeringan bedak dengan oven pada temperature 40-45oC. Temperatur ini dipilih karena
carotenoid dapat terdegradasi dengan cepat pada suhu 60oC (Mortensen, 2009). Selain itu bila digunakan suhu terlalu tinggi, maka akan menyebabkan amilum tergelatinisasi. Pada Amylum Manihot memiliki suhu gelatinisasi 65-70oC dan
pada Amylum Solani 60-65oC (BeMiller and Whistler, 2009) sehingga dipilih temperature 40-45oC untuk mencegah terdegradasinya carotenoid dan mencegah
gelatinisasi amilum. Pengeringan selesai pada waktu 3 hari.
Carotenoid merupakan pigmen yang tidak larut dalam air, sehingga kemungkinannya kecil untuk menimbulkan suatu migrasi warna yang membuat
pewarnaan tidak merata tetapi dalam aplikasinya tetap terdapat pewarnaan yang tidak merata pada permukaan cake bedak. Pewarnaan yang tidak merata pada
permukaan cake bedak juga dapat disebabkan oleh degradasi pigmen carotenoid
saat proses pengeringan, yang mengakibatkan hilangnya warna pada bagian
permukaan cake bedak.
Untuk menjadikan sebuah bedak tabur, maka cake bedak dihaluskan (milling) dengan menggunakan mortir dan stamper. Digunakan penghalusan
intensitas warna komponen bedak oleh karena panas yang dihasilkan oleh putaran
blender yang akan mendegradasi carotenoid.
Pada tahap milling, memungkinkan terjadinya kerusakan mekanis
komponen bedak, yaitu amilum. Amilum yang berukuran lebih besar akan memiliki peluang yang besar untuk rusak (Dubat, 2004). Kerusakan komponen
bedak dapat dilihat pada gambar 1.
Gambar 10. Tipe Kerusakan pada amilum ( Dubois, 1949).
Kerusakan amilum dapat berupa break atau crack. Break merupakan
hilangnya sedikit bagian amilum, jika proses milling tidak dihentikan maka akan terjadi Crack. Crack merupakan kerusakan amilum yang parah yang disebabkan
oleh proses milling yang terlalu kuat dan lama, sehingga antar partikel amilum atau partikel amilum dengan alat akan saling berbenturan hingga patah (Dubat,
2004).
Gambar 11. Kerusakan pada Amylum Manihot (kiri) dan Amylum Solani (kanan) Break
Terlihat terdapat kerusakan amilum pada kedua formula. Kerusakan komponen bedak ini dikarenakan benturan saat penghalusan cake bedak. Pecahan ini dapat mengiritasi kulit bila pecahan yang dihasilkan bersifat tajam sehingga
perlu dilakukan proses milling yang tidak terlalu kuat dan tidak terlalu lama untuk menghindari kerusakan komponen bedak.
Mg stearat dicampurkan setelah dilakukan penghalusan komponen bedak, karena bila magnesium stearat dicampurkan bersama-sama dengan sari wortel akan mempersulit pencampuran dan tercapainya homogenitas komponen
bedak dengan sari wortel. Magnesium stearat merupakan komponen yang tidak larut air sehingga sulit untuk terbasahi oleh sari wortel. Pencampuran dilakukan
dengan menggunakan blender selama 1 menit agar panas blender tidak mendegradasi pigmen carotenoid.
Umumnya, sebuah bedak tabur dapat diterima apabila dapat lolos pada
pengayak dengan ukuran 200 mesh (Singh, 2010), tetapi dalam penelitian ini dilakukan pengayakan dengan pengayak ukuran 400 mesh, sehingga didapatkan
tekstur bedak yang halus. Tekstur bedak yang halus ini akan memberikan kesan yang lebih natural pada kulit. Tetapi apabila ukuran partikel bedak tabur terlalu
kecil (sekala nanometer), akan membuat penyumbatan pada pori-pori kulit wajah sehingga menimbulkan komedo. Dari sediaan bedak yang didapat akan diuji sifat fisisnya meliputi kandungan lembab, bulk density, stabilitas warna, daya lekat,
C. Uji Sifat Fisis Bedak Tabur
Bedak tabur yang telah dibuat juga dilakukan uji sifat fisis dan stabilitasnya. Uji sifat fisis dan stabilitas ini cukup penting karena akan
mempengaruhi mutu dan penerimaan konsumen terhadap suatu sediaan. Karena dalam beberapa uji dalam penelitian ini tidak ada persyaratan baku, maka dalam
penelitian ini, bedak tabur yang telah dibuat akan dibandingkan dengan salah satu merek bedak yang telah beredar di pasaran. Bedak yang telah beredar di pasaran diasumsikan memiliki sifat fisis yang baik sehingga dapat diterima oleh
masyarakat. Apabila nantinya bedak tabur yang dibuat oleh peneliti ini tidak berbeda signifikan dengan bedak tabur pasaran maka dapat disimpulkan bedak
cukup stabil dan dapat diterima oleh masyarakat bila produk bedak dipasarkan. Komposisi bedak tabur pasaran yang digunakan adalah Talcum, Amylum Maydis,
zinci oxydum, zinci stearas, acidium salicylicum 0,08 g, pigment yellow iron oxide, pigment yellow FCF (37-39%) dan parfume Marks bedak.
1. Karakteristik Ukuran Partikel
Pengujian ukuran partikel dilakukan pada hari ke 0 dan ke 30, hal ini
dilakukan untuk melihat adanya suatu perubahan ukuran partikel pada saat penyimpanan. Untuk melihat karakteristik ukuran partikel serbuk bedak digunakan software Motic Image plus 2.0 (perbesaran 4x10 kali). Jumlah partikel
distribusi yang baik pada suatu populasi (Martin, 1990). Sebelum pengukuran dilakukan kalibrasi dengan menggunakan skala objektif micrometer 0.01 mm.
Dari 300 partikel tiap replikasi tersebut dicari nilai percentile 90 dengan
menggunakan Microsoft Excel. Nilai Percentile 90 ini mewakili distribusi ukuran partikel pada sediaan bedak tabur. Percentile 90 merupakan suatu parameter nilai
yang menunjukkan sejumlah 90% populasi dari partikel yang diamati memiliki ukuran kurang dari nilai yang tertera. Hasil pengukuran nilai rata-rata percentile
90 pada tiap formula dapat dilihat pada tabel berikut ini.
Tabel VI. Rata-Rata Percentile 90
Formula Rata-rata percentile 90
Hari 0 Hari 30
I (manihot) 19,313 20,164
II (solani) 64,261 70,121
Apabila rata-rata percentile 90 dalam sebuah formula semakin kecil, maka ukuran partikel dalam formula tersebut juga cenderung lebih kecil
dibandingkan dengan formula yang memiliki nilai percentile 90 yang lebih besar. Dilihat dari nilai percentile 90, formula satu memiliki nilai percentile 90 yang lebih kecil dari pada formula dua, hal ini menandakan ukuran partikel pada
formula satu lebih kecil dibandingkan formula dua. Pada kedua formula terjadi kenaikan nilai percentile 90 selama penyimpanan (hari ke 30), dari sini didapat
kesimpulan terjadi penambahan ukuran partikel selama waktu penyimpanan. Nilai percentile 90 tiap formula diuji dengan Paired T Test (karena kedua formula berdistribusi normal) untuk menilai signifikansi perbedaan ukuran pada
saat penyimpanan. Uji statistik nilai percentil 90 dapat dilihat pada tabel II.
Formula Df Confidence Interval Asymp. Sig
I
2 95% 0,04199
II 0,02649
Karena Convidence Interval (tingkat kepercayaan) yang digunakan
adalah 95%, maka perbedaan ukuran partikel saat penyimpanan pada kedua formula berbeda signifikan apabila didapat nilai p < 0,050. Dari tabel II pada
kedua formula menghasilkan p<0,050 sehingga disimpulkan perbedaan ukuran partikel pada hari 0 dan 30 berbeda signifikan atau dengan kata lain terjadi pertambahan ukuran partikel yang signifikan untuk kedua formula. Walaupun
terjadi pertambahan ukuran, kedua formula tetap memenuhi standar ukuran partikel bedak, yaitu kurang dari 74 µ m.
Gambar 12. Kurva nilai tengah diameter partikel vs frekuensi formula I
terlihat adanya penurunan frekuensi pada ukuran partikel kecil, dan terjadi kenaikan frekuensi pada ukuran partikel besar.
Gambar 13. Kurva nilai tengah diameter partikel vs frekuensi formula II
Berdasarkan gambar 13, ukuran partikel bedak tabur pada formula II berada pada rentang 11,03-105,94 µm. Dimana terlihat terjadi peningkatan
frekuensi ukuran partikel bedak tabur yang lebih besar setelah waktu penyimpanan satu bulan.
Perbedaan formula I dan II adalah pada bahan dasar (amilum) yang digunakan, sehingga diperkirakan pertambahan ukuran partikel pada kedua formula terjadi pada amilum yang digunakan. Amilum dapat mengabsorbsi
kandungan lembab pada temperatur ruangan (20-30oC) (Darkwa, Jetuah and Sekyere, 2003). Gugus hidroksil pada komponen amilosa dan amilopektin
kohesif, sehingga partikel cenderung bergabung dan memberikan diameter yang lebih besar.
2. Kandungan lembab bedak tabur
Uji kandungan lembab dilakukan pada hari ke 0,2,10,20 dan 30. Pada penelitian ini uji kandungan lembab dilakukan untuk mengetahui adanya
perubahan kandungan lembab pada bedak tabur seiring dengan bertambahnya waktu penyimpanan. Uji kandungan lembab dilakukan dengan metode
gravimetric dengan alat Moisture Balance dengan suhu 110 OC. Digunakan suhu
110 OC karena titik didih air adalah 100 OC, dengan memakai suhu 110 OC proses penguapan air akan berlangsung lebih cepat. Kandungan lembab dalam formula
bedak tabur digambarkan dengan persentase bobot yang hilang saat pengeringan (lost of drying) (Olayemi, Oyi, Allagh, 2008). Bobot bedak tabur yang hilang pada saat pengeringan dikarenakan adanya kandungan air yang menguap saat
pengeringan. Semakin banyak bobot bedak tabur yang hilang saat pengeringan menggambarkan semakin banyak juga kandungan air dalam bedak tabur.
Pada gambar 14 terlihat terjadi pertambahan persentase kandungan lembab seiring dengan waktu penyimpanan pada kedua formula. Kandungan
lembab yang terus meningkat seiring dengan bertambahnya waktu penyimpanan ini dapat menggambarkan stabilitas sifat fisis bedak tabur. Pertambahan
kandungan lembab ini dikarenakan oleh bahan dasar bedak, yaitu amilum yang merupakan komponen terbesar dari komposisi bedak tabur yang dibuat. Amilum bersifat higroskopis, yang dapat mengabsorbsi kandungan lembab pada ruangan
hingga mencapai equilibrium humidity (Rowe, Sheskey, dan Quinn, 2009). Kandungan lembab pada bedak tabur ini dapat menggambarkan
kemampuan menyerap sekresi keringat pada wajah. Semakin besar kandungan lembab yang dapat diabsorbsi maka akan semakin baik pula daya absorbsi sekresi keringat pada kulit. Namun, apabila terus terjadi pertambahan kandungan lembab
pada bedak selama waktu penyimpanan, maka akan mencapai titik equilibrium humidity, yang akan membuat komponen bedak tidak dapat lagi mengabsorbsi
sekresi minyak. Apabila bedak tabur ini digunakan pada saat telah mencapai titik
equilibrium humidity¸ maka bedak tabur tidak dapat mengabsorbsi sekresi
keringat, sehingga diperlukan repowdering (pembedakan berulang kali) untuk membantu menutupi sekresi keringat tersebut. Untuk mencegah terjadinya titik
equilibrium humidity pada komponen bedak tabur, bedak tabur dapat disimpan
Kandungan lembab pada formula I lebih rendah daripada formula II (gambar 14). Hal ini dikarenakan ukuran partikel granul Amylum Manihot (pada formula I) dan Amylum Solani (formua II) berbeda. Semakin besar ukuran partikel
dapat menggambarkan semakin banyak kandungan amilopektin dan amilosa sehingga semakin banyak kandungan lembab yang dapat terserap. Molekul air dan
amilum berinteraksi dengan interaksi hidrogen (gambar 12).
Molekul air pada udara dapat kontak pada lapisan monomolecular
partikel dan membentuk interaksi hidrogen. Semakin banyak molekul air pada
bagian surface partikel, menyebabkan air akan tertransfer kedalam material (Nokhodchi, 2005), sehingga semakin bertambahnya kandungan air dalam
material tersebut.
Gambar 15. Keberadaan kandungan lembab pada partikel (Nokhodchi, 2005).
Tabel VIII. Uji signifikansi kandungan lembab hari ke 0,2,10,20,30
Formula Sig.
I 8.022e-8