Pengaruh Suplementasi Besi pada Tuberkulosis Paru dengan
Anemia Defisiensi Besi
(Kajian Respon Kesembuhan, Respon Imun, dan Resistensi)
The Influence of Iron Supplement on Lung Tuberculosis
with Iron Deficiency Anemia
(Review on The Recovery Responses, Immune Responses, and Resistance)
Djoko Trihadi Lukmono Subagyo1*, Soeharyo Hadisaputro2, dan Hadiarto Mangunnegoro3
ABSTRACT
Background: Prevalence of Lung Tuberculosis (TB) in Indonesia is about 0.15% - 0.26%. Iron supplement on the TB patients with iron deficiency anemia (IDA) has several effects such as activating macrophage derived monocyt (MDM) and interferon-gamma (IFN- ), with a positive feed-back mechanism pushing interleukin-12 (IL-interleukin-12). The objective of this research is to find out the influence of iron supplement on recovery responses, immune responses, and resistance on the TB patients with IDA without chronic disease anemia, no acute or chronic infections, and good nutrition status.
Design and method: The method of this study was Randomized Clinical Trial with Simple Randomized Pre-test – Post-Pre-test Control Group Design on 252 respondents in a triple blind manner. The respondents are those having the category 1 active pulmonary TB with IDA according the World Health Organization (WHO) standard, receiving the Directly Observed Treatment Shortcourse (DOTS) strategy treatment. The experimental group consists of 126 respondents, treated with a therapy of 2 RHZE / 4 R3H3 and 3 x 200 mg sulfate ferrosus containing 60 mg ferro-sulfate hepta-hydrate for the first 2 months, and 3 times a week for the next 4 months. The control group consists of 126 respondents, treated with a therapy of 2 RHZE / 4 R3H3 and placebo. Independent variable was iron supplementation, while dependent variable were Acid FastBaccili (AFB) smears, IFN-γ, IL-12, MDR-TB, hemoglobin, serum tranferrin Receptor (sTfR), and Body Mass Index (BMI). Data analysis is conducted with SPSS t-test Version 15 (2007).
Result: The analysis results of delta data of study variables between the control group vs. experimental group are: 1) increased sputum AFB conversion in the experimental group +100% (p<0,05). 2) increased
IFN-γ in the experimental group +324,84% (p<0,05). 3) increased IL-12 in the experimental group +364,42% (p<0,05). 4) decreased MDR-TB in the experimental group -100% (p<0,05). 5) increased haemoglobin in the experimental group +47,96% (p<0,05). 6) decreased sTfR in the experimental group -68,54% (p<0,05). 7) increased BMI in the experimental group +45,63% (p<0,05). 8) inhibited single - basa mutation CCT-Arginin, and multiple - basa mutation histidin-leusin GGC TGA DNA MTB. 9) haemoglobine threshold for MDR-TB risk was 9,5gr%, sTfR 60,26 pg/ml, IFN-γ 14,58 pg/ml, IL-12 15,56 pg/ml, and BMI less than 18,5 kg/m2. 10)
haemoglobine highest risk threshold was 15 gr% to prevent infection MTB worsening. The results of logarithmic data t-test of all variables are highly significant (p<0.00), except BMI was significantly increases (p<0.05); Mann-Whitney test of delta data, highly significant differences were found (p<0.00).
Conclusion: In the control group 9 multiple-basa mutations as the causes of MDR-TB were found. We conclude that iron supplement on the TB with IDA increases: sputum AFB conversion, IFN- , IL-12, hemoglobin, BMI, decreases sTfR and MDR-TB. In other group which no iron supplementation there are 9 multiple-basa mutations as the causes of MDR-TB (Sains Medika, 2 (1):57-69).
Key words: interferon-gamma, interleukin-12, iron supplementation, tuberculosis
ABSTRAK
Pendahuluan: Prevalensi Tuberkulosis Paru (TBP) di Indonesia sekitar 0,15%-0,26%. Suplementasi besi pada penderita TBP dengan anemia defisiensi besi (ADB) mempunyai efek antara lain mengaktivasi macrophage derived monocyt (MDM), dan interferon-gamma (IFN-γ), dengan mekanisme umpan balik positif memacu interleukin-12 (IL-12). Tujuan penelitian ialahuntuk mengetahui pengaruh suplementasi besi terhadap respon kesembuhan, respon imun, dan resistensi pada pasien TB dengan ADB tanpa anemia
1 Bagian Penyakit Dalam RSUD Kota Semarang * Email: [email protected]
penyakit khronis, tidak ada infeksi akut atau kronis, dan status gizi baik.
Metode penelitian: Metode penelitian ini adalah Randomized Clinical Trial dengan Simple randomized the Pre test-Post test Control Group Design pada 252 responden secara tersamar ganda (triple blind). Responden yaitu penderita TBP aktif kategori 1 dengan ADB sesuai dengan standar WHO yang mendapat pengobatan strategi Directly Observed Treatment Shortcourse (DOTS). Kelompok eksperimen 126 responden diterapi 2 RHZE / 4 R3H3 dan sulfas ferrosus 3 x 200 mg yang mengandung ferro-sulfat heptahidrat 60 mg selama 2 bulan pertama, dan 3 kali seminggu selama 4 bulan selanjutnya. Kelompok kontrol 126 responden diterapi 2 RHZE / 4 R3H3 dan plasebo. Variabel bebas adalah suplementasi besi, variabel tergantung adalah konversi Bakteri Tahan Asam (BTA), IFN-γ, IL-12, Multi Drug-Resistant TB (MDR-TB), hemoglobin, serum Transferrin Receptor (sTfR), dan Indeks Massa Tubuh (IMT). Analisis data dengan uji-t SPSS Version 15.0 (2007).
Hasil Penelitian: Hasil analisis data delta variabel penelitian antara kelompok kontrol dibandingkan dengan kelompok eksperimen adalah: 1) peningkatan konversi BTA dahak pada kelompok eksperimen sebesar +100% (p<0,05), 2) peningkatan IFN-γ pada kelompok eksperimen sebesar +324,84% (p<0,05), 3) peningkatan IL-12 pada kelompok eksperimen sebesar +364,42% (p<0,05), 4) penurunan MDR-TB pada kelompok eksperimen sebesar –100% (p<0,05), 5) peningkatan hemoglobin pada kelompok eksperimen sebesar +47,96% (p<0,05), 6) penurunan kadar sTfR pada kelompok eksperimen sebesar –68,54% (p<0,05), 7) peningkatan IMT pada kelompok eksperimen sebesar +45,63% (p<0,05), 8) menghambat mutasi basa-tunggal CCT-Arginin, dan mutasi basa-berganda histidin–leusin GGC TGA DNA MTB, 9) batas nilai ambang risiko terjadi MDR-TB pada kadar hemoglobin 9,5 gr%, sTfR 60,26 pg/ml, IFN-γ 14,58 pg/ml, IL-12 15,56 pg/ml, dan IMT kurang 18,5 kg/m2,10) batas nilai ambang kadar hemoglobin tertinggi 15 gr% untuk mencegah makin
beratnya infeksi MTB.Hasil uji test data logaritma semua variabel berbeda sangat bermakna (p<0,00), kecuali IMT meningkat bermakna (p<0,05), dan pada uji Mann-Whitney data delta didapatkan perbedaan sangat bermakna (p<0,00).
Kesimpulan: Pada kelompok kontrol didapatkan 9 mutasi basa-ganda sebagai penyebab MDR-TB. Jadi dapat disimpulkan bahwa suplementasi besi pada TB dengan ADB meningkatkan: konversi BTA sputum, IFN- , IL-12, hemoglobin, IMT, menurunkan sTfR, dan MDR-TB. Pada kelompok yang tidak diberi suplementasi besi didapatkan 9 mutasi basa-ganda sebagai penyebab MDR-TB (Sains Medika, 2 (1):57-69).
Kata kunci: interferon-gama, interleukin-12, resistensi, suplementasi besi, tuberkulosis.
PENDAHULUAN
Tuberkulosis Paru (TBP) telah menyebabkan angka kematian lebih dari 1,97 juta
orang per tahun. Case Fatality Rate 27%; kasus baru tahun 2005 sebesar 10,4 juta. Angka
Multidrug-resistant (MDR) bervariasi antara 1,2 – 8,7%. Populasi yang telah terinfeksi antara
lain di Afrika 35%; Amerika 18%; Asia Tenggara, termasuk Indonesia 44% ( prevalensi TB di
Indonesia 0,15% - 0,26%) (Achmadi, 2004). Salah satu faktor risiko TB adalah anemia
defisiensi besi (ADB). Diperkirakan tahun 2020 TB menyerang 1 miliar populasi dengan 70
juta kematian, bila tidak dilakukan pengendalian (Soemantri et al., 2007; Lemery et al.,
2004).
Pengaruh ADB pada TB antara lain adalah: 1) menurunkan respon imun seluler,
dimana aktivitas interleukin-12 (IL-12) dan interferon-gamma (IFN-γ) memacu makrofag
yang mempunyai dua efek, yaitu membunuh MTB dan memacu produksi IL-12, atau disebut
umpan-balik positif (positive-feedback) (Viane et al., 2005; Johnson et al., 2005); 2)
menurunkan konversi bakteri tahan asam (BTA) dahak; 3) meningkatkan re-infeksi dan
Vosskuill et al., 2006).
Penelitian meta analisis melaporkan masih ada beda pendapat tentang
suplementasi besi pada TBP dengan ADB. Kelompok yang setuju suplementasi besi pada
infeksi MTB dengan alasan yaitu: 1) infeksi laten MTB menimbulkan defisiensi Magnesium
(Rv 1811, mgtc), dan menyebabkan afinitas Fe-Mg-S berkurang (Kuhn et al., 2005); 2)
Mycobactin (Mbt-RV 2383c) dan carboxymycobactin yang berfungsi sebagai penyandi
protein MTB aktivitasnya berkurang (De Voss et al., 2004); 3) inang membutuhkan monosit
lebih banyak dari suplementasi besi untuk membentuk macrophage derived monocyt
(MDM) dan diharapkan fagositosis lebih baik (Matos et al., 2006).
Kelompok yang tidak setuju suplementasi besi pada TBP dengan ADB beralasan: 1)
virulensi MTB karena faktor Sigma A (Rv 2703, sig A) yang menimbulkan mutasi
arginin-histidin pada kodon 515 terminal C (Yang et al., 2007); 2) TBP dengan ADB terjadi
hiperekspresi TNF (Washent et al., 2006); 3) Overblown-infection TBP disebabkan oleh
Streptomycinresistant (Richardon et al., 2007). Selain TBP keadaan yang harus diperhatikan
didalam suplementasi besi adalah infeksi malaria, diare khronis, meningitis, anemia infeksi
khronis, dan status gizi (Gerraldino et al., 2006). Dilaporkan bahwa pada infeksi MTB yang
sangat berat, kadar IFN-γ sangat rendah. Disisi lain, IFN-γ dengan IL-12 berperan sangat
penting pada pematangan hematopoisis(Smulders et al., 2005). Secara umum hanya 7%
zat besi atau 1 mg yang dapat memasuki plasma dari perkiraan asupan sehari 15 mg.
Pengukuran ADB menggunakan parameter sTfR dengan pertimbangan: tidak menyakitkan,
tidak membahayakan, tidak memerlukan tenaga khusus, dan tidak mahal bila dibandingkan
dengan biopsi sumsum tulang (Fitzsimon dan Brock, 2003).
Penelitian terdahulu menemukan bahwa MDR-TB dapat disebabkan oleh adanya
mutasi basa-tunggal pada gen rpoB pada Rif, gen katG pada resistensi INH (Word et al.,
2006; Qunnonew dan Irjala, 2004). Perbedaan penelitian ini dibandingkan dengan
penelitian lain adalah memberikan gambaran tentang pengaruh suplementasi besi
terhadap adanya: 1) mutasi basa ganda pada TBP dengan ADB yang mengalami MDR
-TB; 2) mekanisme resistensi genotip MDR--TB; dan 3) titik potong ( cutoff point ) kadar
hemoglobin, sTfR, IFN-γ, dan IL-12 sebagai deteksi dini resistensi Mycobacterium
tuberculosis (MTB) (Ravligione & Maher, 2006; Vosskuill et al., 2006).
Penelitian ini bertujuan untuk mengetahui pengaruh suplementasi besi terhadap
respon kesembuhan, respon imun, dan resistensi pada pasien TBP dengan ADB. Tujuan
kesembuhan yang diukur dengan konversi BTA dahak, respon imun yang diukur dengan
IFN-γ dan IL-12, kadar hemoglobin, sTfR, MDR-TB yang diukur dengan skuensing urutan
DNA MTB, dan IMT.
METODE PENELITIAN
Desain yang digunakan adalah Uji Klinis Randomized Clinical Trial dengan Simple
randomized The Pre test-Posttest Control Group, tersamar ganda (triple blind) terhadap
126 penderita TBP dengan ADB yang diterapi OAT dan suplementasi besi sebagai kelompok
eksperimen, dan 126 penderita TBP dengan ADB yang diterapi OAT dan plasebo sebagai
kelompok kontrol.
Sampel ditentukan dengan cara acak sederhana, objektivitas penelitian pemberian
obat dilakukan dengan teknik buta-berganda. Kelompok eksperimen diterapi dengan OAT
standar 2RHZE/4R3H3 dan sulfas ferrosus besi 3×200 mg mengandung ferro-sulfat
heptahidrat 60 mg selama 2 bulan pertama-fase awal, dilanjutkan 3 kali seminggu selama
4 bulan-fase lanjutan. Kelompok kontrol diterapi dengan OAT standar 2RHZE/4R3H3 dan
plasebo. Tempat penelitian di Poliklinik Penyakit Dalam RSUD Semarang, waktu penelitian
antara 3 Januari 2003 sampai 31 Mei 2007. Kriteria inklusi yaitu: 1) TBP kategori 1-BTA
dahak positif; 2) pria atau wanita usia 15-55 tahun; 3) bersedia menjadi responden
sampai penelitian selesai; 4) belum pernah mendapat OAT dan suplementasi besi; 5)
anemia ringan sampai sedang sesuai jenis kelamin: hemoglobin antara 8 sampai 11
gr%; sTfR lebih dari 50 pg/ml; CRP negatif; 6) IMT antara 18 sampai 25 Kg/m2;7) patuh
minum OAT dan suplementasi besi minimal 90% obat yang ditentukan. Kriteria eksklusi
yaitu : 1) DM; 2) gagal ginjal akut atau gagal ginjal khronis; 3) gagal jantung/ aritmia
kordis; 4) penyakit hati akut atau khronis; 5) tumor paru atau keganasan lain; 6)
Thalasemia, leukemia, koagulasi intravaskuler disseminata, dan anemia penyakit
khronis; 7) penyakit degeneratif; 8) menghentikan terapi; 9) penyakit saluran cerna; 10)
hamil atau laktasi, dan kontrasepsi hormonal. Variabel tergantung adalah tingkat
konversi BTA dahak, kadar IFN-γ, kadar IL-12, MDR-TB, hemoglobin, sTfR, dan IMT
sedangkan variabel bebas yaitu suplementasi besi.
Analisis data menggunakan SPSS 15.0 untuk membuktikan pengaruh suplementasi
besi terhadap respon kesembuhan, respon imun, dan resistensi. Dilakukan analisis
berdistribusi normal, sedangkan data yang tidak berdistribusi normal dianalisis dengan
uji non-parametrik menggunakan uji Mann-Whitney. Untuk membuktikan hipotesis
dilakukan uji t tes data delta konversi BTA sputum, IFN-γ, dan IL-12 sedangkan hemoglobin,
sTfR, dan IMT kedua kelompok dengan uji Mann-Whitney.
HASIL PENELITIAN
Berdasarkan hasil penelitian terhadap 1276 orang tersangka TBP didapatkan 843
orang dengan BTA dahak +3. Setelah pemeriksaan hemoglobin dan sTfR didapatkan 347
sampel memenuhi kriteria, karena beberapa faktor penyulit 74 sampel dikeluarkan dari
penelitian. Sampel yang memenuhi kriteria sebesar 273 orang, pada akhir 6 bulan terapi
21 sampel dikeluarkan dari penelitian. Sampel yang benar diteliti adalah 252 orang yang
terdiri dari kelompok eksperimen 126 orang dan kelompok kontrol 126 orang.
Hasil pengujian data penelitian antara kelompok kontrol dan kelompok eksperimen
disajikan pada Tabel 1, 2 dan 3. Secara keseluruhan terdapat berbedaan yang bermakna
pada setiap variabel antara kelompok kontrol dan kelompok terapi (p<0,05). Bila
dikonfirmasikan dengan data deskriptif (Mean atau Median) menunjukkan bahwa nilai
yang jauh lebih besar pada kelompok eksperimen dibandingkan pada kelompok kontrol.
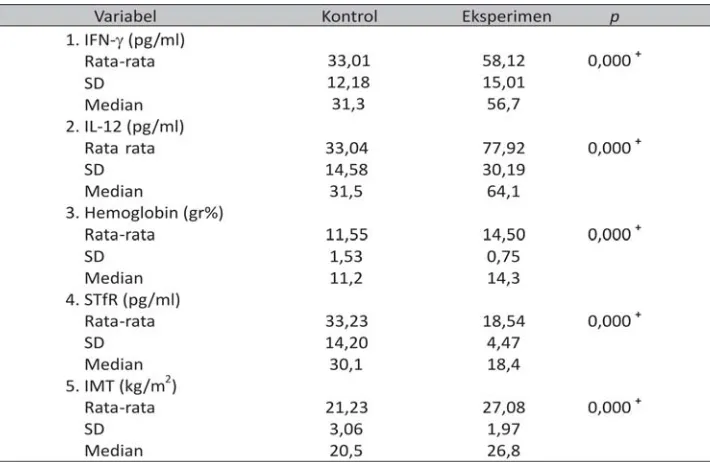
Tabel 1. Uji signifikansi data pascaterapi antara kelompok kontrol (n = 126) dan kelompok
eksperimen (n = 126)
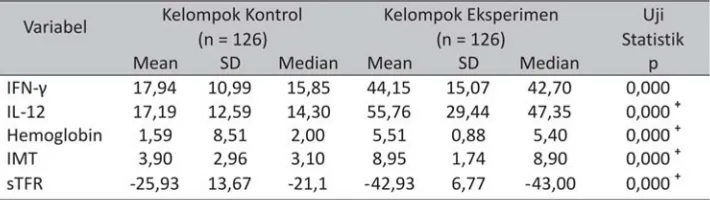
Tabel 2. Hasil analisis data delta variabel penelitian antara kelompok kontrol (n=126) dan kelompok eksperimen (n=126)
Keterangan : +Mann Whitney test
Konversi BTA (+) yang berhasil yaitu dari keadaan BTA (+) ke BTA (-) lebih banyak
terdapat pada kelompok eksperimen dibandingkan pada kelompok kontrol. Sebaliknya
konversi BTA (+) yang tidak berhasil lebih banyak terdapat pada kelompok kontrol
dibandingkan pada kelompok eksperimen, dan secara statistik terdapat perbedaan yang
bermakna tentang keberhasilan konversi BTA (+) antara kedua kelompok.
Untuk mengetahui variabel yang menjadi penyebab perbedaan diantara dua
kelompok subyek dilakukan analisis multivariat yaitu Analisis Deskriminan. Adapun variabel
yang diduga menjadi pembeda adalah perubahan (delta) IFN- , IL-12 , hemoglobin, IMT
dan sTFR. Hasil analisis ini menunjukkan bahwa semua variabel yang diduga telah terbukti
menjadi pembeda pengelompokan kelompok subyek. Jadi variabel perubahan IFN- ,
IL-12, hemoglobin, IMT, sTFR secara bersama-sama menunjukkan perbedaan di antara
kelompok eksperimen dan kelompok kontrol. Keadaan dalam kelompok sebagian besar
sangat bervariasi kecuali hemoglobin yang relatif homogen (Wilk’s Lambda mendekati 1).
Hasil Reaksi PCR DNA-MTB
Hasil PCR pada 22 ekstrak dilusi dari suspensi kultur galur MTB, 9 dari 22
pemeriksaan (9/22) dapat dideteksi satu pita DNA spesifik dengan ukuran molekul
157-bp yang disesuaikan dengan standar ukuran molekul marka digesti DNA pUC 19 Hae III,
pada gel elektroforesis. Pada isolat 7B posisi + 19 diisi C, sedangkan nukleotida
seharusnya Arginin. Isolat 13A dan 13B posisi + 4 nukleotida G menggantikan Timin dan
Sitosin, juga isolat 15A dan 15B nukleotida G dan T menggantikan susunan Histidin. Hal
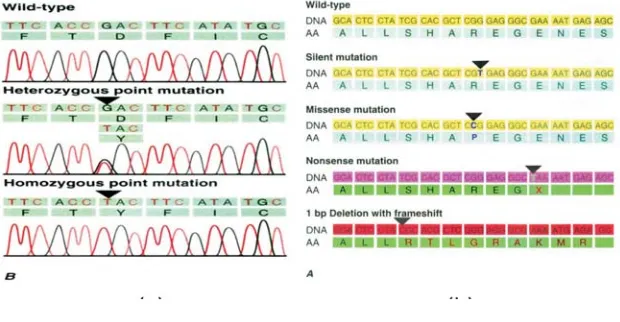
Gambar 1. (a) Hasil analisis titik mutasi basa – ganda pada MDR – TB dan (b) Hasil analisis perubahan nukleotida DNA – MTB yang mengalami MDR – TB
Keterangan:
(a) Hasil analisis homologi urutan nukleotida gen KatG isolat 5, 8, 10, dan 12
ditemukan adanya perubahan urutan nukleotida (mutasi titik) pada daerah regulasi gen, dari nukleotida G pada isolat 7A menjadi C pada isolat 7B pada posisi +28 daerah urutan RBS sebelum ATG (awal translasi pada posisi +36).
Dibandingkan wild-type sebagai pembanding standar MDR-TB, pada
penelitian ini didapatkan mutasi basa-ganda ACC GAC TTC ATA TGC pada
area kodon heterozygous point mutation. Mutasi basa-tunggal terdapat pada
TAC area kodon homozygous point mutation.
(b) Hasil analisis perubahan urutan nukleotida DNA MDR-TB yang menyebabkan
mutasi basa-ganda, yaitu insersi-basa TGC CAT, delesi-basa CGG TGA, dan
transkripsi-basa TGC GGA. Silent mutation didapatkan pada area kodon CGT,
missense mutation pada kodon CCG, nonsense mutation pada kodon TCG, dan deletion with frameshift pada kodon CGC.
Pengaruh suplementasi besi terhadap peningkatan konversi BTA dahak
Delta konversi BTA dahak kedua kelompok yang diteliti, didapatkan peningkatan
konversi BTA dahak kelompok eksperimen (+100%) lebih besar daripada kelompok kontrol
(+76,2%) (p< 0,05).
Pengaruh suplementasi terhadap peningkatan IFN-γγγγγ dan IL-12
Delta IFN- dan IL-12 kedua kelompok yang diteliti didapatkan peningkatan pada
kelompok eksperimen IFN- (+324,84%) dan IL-12 (+364,42%), lebih besar dibandingkan
Pengaruh suplementasi besi terhadap peningkatan hemoglobin dan IMT
Delta hemoglobin dan IMT kedua kelompok yang diteliti didapatkan peningkatan
pada kelompok eksperimen yaitu hemoglobin (+47,96 %) dan IMT (+45,63 %), lebih besar
dibandingkan dengan kelompok kontrol yaitu hemoglobin (+22,69 %) dan IMT (+22,68 %).
Menggunakan uji Mann-Whitney terhadap hemoglobin dan IMT didapatkan perbedaan
bermakna pada variabel hemoglobin dan IMT (p<0,05).
Pengaruh suplementasi besi terhadap penurunan MDR-TB dan sTfR
Delta sTfR dan MDR-TB pada kedua kelompok yang diteliti didapatkan penurunan
pada kelompok eksperimen yaitu sTfR (–68,54%) dan MDR-TB (–100 %) lebih besar
dibandingkan dengan kelompok kontrol yaitu sTfR (–43,45%) dan MDR-TB (–76,40%).
Menggunakan uji Mann Whitney terhadap sTfR dan MDR-TB didapatkan perbedaan
bermakna (p<0,05).
PEMBAHASAN
Angka konversi BTA kelompok ekperimen pada penelitian ini sebesar 100% lebih
tinggi dibandingkan dengan target P2TB Nasional tetapi pada kelompok kontrol hanya
76,2%. Hal ini berarti masih ada sekitar 23,8% kasus yang berpotensi menjadi sumber
penularan aktif dan sulit untuk memutus rantai penularan (Van Klose et al., 2007; Depkes
RI, 2002).
Suplementasi besi meningkatkan konversi BTA sputum dengan mekanisme sebagai
berikut: 1) Menghambat delayed hipersensitivity yang memicu aktivitas seluler MTB,
sehingga banyak MTB dorman dan semi-dorman yang mati (Wu and Cotes, 2007); 2)
Meningkatkan Monocyt Derived Macrophage sehingga fagositosis terhadap MTB lebih
kuat (Marshal and Bates, 2007). Peningkatan IFN-γ pascaterapi 74% pada penelitian ini
lebih tinggi dibandingkan peneliti terdahulu. Suplementasi besi meningkatkan IFN-γ dengan mekanisme yaitu: 1) Memacu IFN-γ mengurangi ketersediaan besi intraseluler
yang digunakan MTB (Ambrosino et al., 2008); 2) Mengaktivasi MDM pada reaksi dengan
IL-12 secara umpan balik positif (Cockeril et al., 2006). Batas ambang terjadi MDR-TB
adalah bila kadar IFN- lebih kecil dari 14,46 pg/ml. Peningkatan IL-12 pascaterapi
2007). Pengaruh suplementasi besi terhadap IL-12 yaitu: 1) Mengaktivasi pematangan,
jumlah dan fungsi MDM, sehingga jumlah IL-12 meningkat; 2) Mengubah fase tenang
menjadi fase aktif IL-12 (Piilatek et al., 2008). Batas nilai ambang terjadi MDR-TB adalah
bila kadar IL-12 lebih kecil dari 15,56 pg/ml. Penurunan MDR-TB sebesar 12,4% pada
penelitian ini lebih tinggi dari penelitian terdahulu (Aisen et al., 2007). Pengaruh
suplementasi besi terhadap penurunan resistensi MTB yaitu: 1) Menghambat fungsi
mannose-receptor, maka fagositosis terhadap MTB semi dorman dan dorman lebih aktif;
2) Memperkuat daerah rawan mutasi sehingga menghambat mutasi basa-tunggal maupun
basa-berganda (Xematery et al., 2007); 3) Mengaktifkan NRAMP 1 yang bermuatan
makrofag pada fase “immune-macrophage cell-line”, sehingga efek fagositosis lebih kuat.
Fenomena baru penelitian ini adalah didapatkannya mutasi basa-ganda DNA MTB yang
belum pernah dilaporkan di Indonesia selama ini dengan beberapa bentuk mutasi.
Pengaruh suplementasi besi terhadap perubahan urutan nukleotida yaitu. 1) Mengubah
sifat genomik dan fenomik MTB yang patogen melalui proses “host extracellular iron
chelates accesible” sehingga urutan nukleotida DNA tidak berubah (Chin et al., 2007). 2)
Menghambat virulensi MTB yang bersifat “non-viable strains” sehingga dimensi sel yang
tersusun oleh nukleotida tertentu menjadi lebih kuat. 3) Memperkuat ikatan awal
intraseluler pada asam amino AAT GCG atau AAT CGT, sehingga menghambat terjadinya
mutasi basa-tunggal maupun basa-ganda (Wilner et al., 2006).
Peningkatan hemoglobin pascaterapi sebesar 54%, lebih tinggi dibandingkan dengan
penelitian sebelumnya. Hal ini disebabkan oleh pengaruh suplementasi terhadap 2 hal
yaitu: 1) Meningkatkan jumlah eritrosit, besi simpanan, dan besi fungsional (Hansen et
al., 2007); 2) Meningkatkan hematopoisis. Batas nilai ambang risiko terjadi MDR-TB
pada kadar hemoglobin 9,5 gr%. Sedangkan batas nilai ambang hemoglobin tertinggi 15
gr% untuk mencegah makin beratnya infeksi TB.
Penurunan sTfR pascaterapi sebesar 69,7%, lebih tinggi dibandingkan penelitian
terdahulu. Hal ini merupakan efek peningkatan simpanan besi enterosit akibat
suplementasi besi dan berkurangnya reseptor di plasma membran (Dennerry et al., 2008).
Batas nilai ambang risiko terjadi MDR-TB bila kadar sTfR lebih besar dari 60,26 pg/ml.
Peningkatan IMT pascaterapi sebesar 64,2%, lebih tinggi dibandingkan penelitian
ikatan mioglobin, sehingga massa otot bertambah besar melalui aktivasi RAB 5
-Recycling-antigen-binding dan Lamp-12 - lipid associated macrophage protein-1; 2) Mengaktifkan
Reactive Oxygen Intermediate sehingga terjadi penimbunan masa otot tubuh; 3)
Meningkatkan ekspresi Inducible Nitric Oxid Syntethase (INOS) sehingga metabolisme
intraseluler karbohidrat, lemak, protein meningkat, dan menimbulkan penambahan jaringan
lemak tubuh (anabolik). Batas nilai ambang terjadi MDR-TB adalah bila IMT lebih kecil dari
18,5 kg/m2.
KESIMPULAN
Berdasarkan hasil penelitian terhadap 252 responden TBP dengan anemia defisiensi
besi, tanpa anemi penyakit khronis, dengan staus gizi baik, kelompok eksperimen diterapi
OAT standar strategi DOTS 2 RHZE / 4 R3 H3 dan sulfas ferrosus heptahydrat 3 × 200 mg zat
besi elemental standar hayati, kelompok kontrol diterapi 2 RHZE / 4 R3 H3 dan plasebo,
masing-masing selama 6 bulan, maka disimpulkan bahwa suplementasi besi:
1) Meningkatkan konversi BTA dahak pada kelompok eksperimen sebesar +100%
dibandingkan dengan kelompok kontrol +76,2% (p<0,05).
2) Meningkatkan IFN-γγγγγ pada kelompok eksperimen sebesar +324,84% dibandingkan
dengan kelompok kontrol +117,27% (p<0,05).
3) Meningkatkan IL-12 pada kelompok eksperimen sebesar +364,42% dibandingkan
dengan kelompok kontrol +103,51% (p<0,05).
4) Menurunkan MDR-TB pada kelompok eksperimen sebesar –100% dibandingkan
dengan kelompok kontrol –76,4% (p<0,05).
5) Meningkatkan hemoglobin pada kelompok eksperimen sebesar +47,96% dibandingkan
dengan kelompok kontrol +22,69% (p<0,05).
6) Menurunkan kadar sTfR pada kelompok eksperimen sebesar –68,54% dibandingkan
dengan kelompok kontrol –43,45% (p<0,05).
7) Meningkatkan IMT pada kelompok eksperimen sebesar +45,63% dibandingkan
dengan kelompok kontrol +22,68% (p<0,05).
Pengaruh suplementasi besi adalah menghambat mutasi basa-tunggal CCT-Arginin,
dan mutasi basa-berganda histidin–leusin GGC TGA DNA MTB. Batas nilai ambang risiko
terjadi MDR-TB pada kadar hemoglobin 9,5 gr%, sTfR 60,26 pg/ml, IFN-γ 14,58 pg/ml,
SARAN
Untuk klinisi perlu mempertimbangkan menyingkirkan faktor anemia penyakit
khronis, infeksi akut, dan inflamasi khronis sebelum memberikan suplementasi besi pada
pasien TBP dengan ADB. Hal ini mengingat prevalensi TBP di masyarakat masih tinggi, cara
pemberian sederhana, harga murah, tetapi indikasi kontra harus diperhatikan.
DAFTAR PUSTAKA
Achmadi, U.F., 2004, The Global Burden of Tuberculosis and Curent Control Strategies in
Indonesia, Simposium Nasional TB Update, Eds: Palilingan JF. Surabaya, Maret 2004:
164 – 69.
Aisen, H., Resnick, M.W., and Leibold, H., 2007, Role of Mannose Receptor Focusing in Iron Alternate and Acquisition for Tuberculosis Resistance : From Facts and Acts? Circulation, April 2007: 5 – 9.
Ambrosino, F.G., Palzkill T, and Charles F., 2008, Systematic Mutagenesis of IL-12 and
IFN-gamma Associated with MDR-TB: In vitro Mycobacterium tuberculosis, CHEST, 38:
182 – 87.
Bellamy, R., Cuwende, C., and Mc Adam, K.P., 2007, Variations in the NRAMP 2, IL-12,
Iron-gene, and Susceptibility to Tuberculosis in West Africans, The New England Journal
of Medicine, August; 19: 640 – 44.
Chin, K.L., Grace, Y., and Haley, T., 2007, Correlations of Host Extra-Cellular Iron chelates
with treatment of Iron Deficiency Anemia in Active and MDR-TB Patients, CHEST;53:
146 – 53.
Cockeril, F.R., Vardeniz, K., and Van Lakkens, D., 2006, IL-12 and IFN-gamma Genetic Methods
for Assesing Resistance-Focusing in Mycobacterium tuberculosis. TUBERCLE, May
2006: 45 – 52.
De Voss, J.J., Rutter, K., Schroder, B.G., and Cliffon, 2004, Iron Acquisition and Mycobactin
(Mbt-Rv 2383c) Hyper expression, Journal of Bacteriology, August: 443-51.
Dennerry, G., Visner, T., Weng, Y.H., and Nguyen, X.L., 2008, Increasing Recycling-Antigen Binding 5 (RAB-5) Activity in Myoglobin Expression : Role in Body Mass Index
Tuberculosis Patients, American Journal of Respiratory Cell And Molleculer Biology,
95: 47 – 53.
Departemen Kesehatan Republik Indonesia, 2002, Program Penanggulangan Tuberkulosis, Pedoman Nasional Penanggulangan Tuberkulosis Terpadu, 1 – 16.
Fitzsimon, E.J., and Brock, J.H., 2003, Serum Transferrin receptor in The Anemia of Chronic
Disease. Remains Hard to Distinguís, BLOOD, May; 17(24): 39 - 43.
Gerraldino, T., Wolkow, D., van Syss, G., Lung, K., and Schultz, R., 2006, Limitation of Iron Intake In Acute And Chronic Diseases: Prospects And Warning on IL-12 and IFN-γ. CHEST, May: 247 – 54.
Hansen, S., Loo, B., Evans, D., and Neophyton, K., 2007, Surfactant Protein-D interconection
with Serum Transferrin Receptor: In vivo Case in resistance MDR-TB. NATURE74:
Johnson, B., Catherine, G., Brook, R., and Viery, P., 2005, Nutritional Status, Comorbidity,
And Influencing Factors In Human Tuberculosis. Infection and Immunity, 37: 76 –
82.
Kuhn, M.G., Goebel, W., Philpot, D.J., and Sansonetti, P.J., 2005, Overview of the Bacterial
Pathogens: Mycobacterium tuberculosis and Magnesium Deficiency. In: Immunology
of Infectious Diseases, Eds: Kaufmann SHE, Sher A, Ahmed R. ASM Press, Washington DC: 16-18.
Lemery, G., Ferguso, B..J, Skine, B.S, 2004, Simpson, K.M., Baynes, R.D., and Look, J.D., Correlation between Anemia of Chronic Disease with Iron Deficiency Anemia, Journal of Laboratory And Clinical Medicine; 119: 385 – 90.
Marshal, K.J., and Bates, J.F., 2006, An Essential Macrophage Activity: Positive-Feedback
Mechanism Between IFN-gamma and IL-12 in Active Tuberculosis, TUBERCLE, May:
536 – 43.
Matos, E.B., Lemos, A.C., and Moreirera, H., 2006, Association Between Tuberculosis and
Macrophage Derived Monocy, International Journal of Tuberculosis and Lung
Diseases, March 10 (12): 1360 – 66.
Piilatek, A.S., Tyagi, S., Pol, A.C., Tellenti, A., and Miller, L.P., 2008, Molecular Beacon Sequence Analysis for Detecting Drugs Resistance in Mycobacterium tuberculosis. NATURE, March: 27 – 35.
Qunnonew, K., and Irjala, M., 2004, Iron deficiency is Associated with High Concentration
of Transferrin Receptor in serum and MDR-TB Multiple-Basa Mutation, Clinical
Chemistry 2004: 74 – 76.
Ravligione, M.C., and Maher, D., 2006, Hyperexpression of rpoB gene Associated with
Single-Basa Mutation in Pulmonary Tuberculosis, TUBERCLE, 10(3): 240-42.
Richardson, F., Nelly, T., Hubert, C., and Luang, L., 2007, Overblown Severity Lung Tuberculosis Precipitated By Streptomycin Resistant Strains: Risk Factor For MDR-TB? CHEST, May: 69 – 76.
Smulders, M.J., Keer, J., Speight, R.A., and Williams, H.D., 2005, Adaptation of Mycobacterium
tuberculosis to Iron Acquisition, Interferon-g and IL-12 in MDR-TB Basa Mutation
Pattern, Infection and Immunity, December 5: 914 – 19.
Soemantri, S., Senewe, F.P., Tjandrarini, D.H., Day, R., Basri, C., Manissero, D., et al., 2007,
Three-fold reduction in the prevalence of Tuberculosis over 25 years in Indonesia
and Risk Factors, International Journal of Tuberculosis and Lung Diseases, 11(4):
398-404.
Van Klose, A., Klapper, F., Heinke, N.M., and Bald, M.S., Iron Mediated Plasmids to Mannose Receptor Surface and targeting of sTfR Stimulation. BLOOD, May 2007; 92: 68 – 72.
Viane, K.W., Smith, G.F., Bruce, R., and Hamilton, K., 2005, Interferon-gamma and Il-12:
Positive-Feedback Mechanism in Tuberculosis Infection, Infection and Immunity,
January: 327-36.
Vosskuill, M., Garther, H.F., and Smith, C., 2006, Oxygen-bridged Iron in Mycobacterium
tuberculosis in Iron –dependent gene expresión, iron metabolism, and Argynine
Washent, G.F., Gross, B., Armadoz, H.G., and Cecilia, N., 2006, TNF Hyper Expresión Along
C Terminal Codon in Latency Tuberculosis, TUBERCLE, 25: 148 – 54.
Willner, J.J., Hirsech, C.S., and Whallen, K., 2006, Impacts of Secondary Hemoglobinopathies In Severity And MDR-TB Strains: Obsession for Preventive
cases, TUBERCLE, October 85: 25 – 31.
Word, D., Snack, R.C., and Meter, J.F., 2006, Bacterial Pathogenicity: Iron Acquisition And Pattern of Basa-mutation in MDR-TB: A Guide to Microbial Infections, In: Patogénesis, Immunity, Laboratory Diagnosis and Control, Churchil Livingstone, Edinburg, 3th Eds: 138 – 43.
Wu Y and Cotes, R.M., 2007, Cytokines Stimulations: IL-12, TNF, and IFN-gamma Related to
Immune responses of Tuberculosis Infection, Journal of Bacteriology, March: 1380
– 87.
Xematery, H., Stroganoff, W., and Pernott, K., 2007, Characterization of New Multiple Basa Mutation in Pyrazinamide and Rifampicin Resistant Strains of Severe Pulmonary
Tuberculosis, TUBERCLE, June; 43: 95 – 100.
Yang, H.K., Shiou, L..M, Kimoto, F.J., and Lie, Y.T., 2007, Rv 2703, sigA Recognition And Single
Mutation in MDR-TB: Focus on Alternated Iron Level, Infection and Immunity, April: