1. Penentuan Berat Molekul Polimer
A. Pengertian Berat Molekul Polimer
Berat molekul merupakan variabel yang teristimewa penting sebab berhubungan langsung dengan sifat kimia polimer. Umumnya polimer dengan berat molekul tinggi mempunyai sifat yang lebih kuat. Polimer – polimer diangggap memiliki berat molekul yang berkisar antara ribuan hingga jutaan dengan berat molekul optimum yang bergantung pada struktur kimia dan penerapannya.
Berat molekular polimer merupakan salah satu sifat yang khas bagi polimer yang penting untuk ditentukan. Berat molekular (BM) polimer merupakan harga rata-rata dan jenisnya beragam yang akan dijelaskan kemudian. Dengan mengetahui BM kita dapat memetik beberapa manfaat, antara lain :
1. Menentukan aplikasi polimer tersebut
2. Sebagai indikator dalam sintesa dan proses pembuatan produk polimer 3. Studi kinetika reaksi polimerisasi
4. Studi ketahanan produk polimer dan efek cuaca terhadap kualitas produk
Polimer sendiri biasa disebut juga polidispersi. Polidispersi adalah banyaknya hamburan yang artinya satu molekul yang dibentuk dari molekul yang sama tetapi berat molekul tidak sama. Nilai berat molekul suatu polimer bergantung pada besarnya ukuran yang digunakan dalam metode pengukurannya.
Nilai berat molekul yang diperoleh bergantung pada besarnya ukuran dalam metode pengukurannya. Sampel suatu polimer sesungguhnya terdiri atas sebaran ukuran molekul dan sebaran massa molekul. Oleh karena itu setiap penentuan massa molekul akan menghasilkan harga rata – rata.
B. Derajat Polimerisasi
Derajat polimerisasi adalah nomor unit dari suatu monomer yang bergabung dengan rantai polimer selama masa rantai tersebut masih ada. Pada polimerisasi terdapat transfer reaksi yang berpengaruh terhadap temperatur (derajat polimerisasi) polimer dan berat molekulnya. Jika transfer reaksi terkontrol dengan baik maka akan ditemukan pemotongan berat molekul suatu polimer dan adanya peningkatan temperatur.
Faktor yang mempengaruhi transfer reaksi polimer salah satunya karena lebih tingginya aktivitas energi pada transfer reaksi menyebabkan lamanya penggabungan rata-
rata transfer yang akan digunakan dalam penambahan monomer, sehingga mempengaruhi berat molekul.
C. Sifat Dan Konsep Berat Molekul Polimer
Hal yang membedakan polimer dengan spesies berat molekul rendah adalah adanya distribusi panjang rantai dan untuk itu derajat polimerisasi dan berat molekular dalam semua polimer yang diketahui juga terdistribusi (kecuali beberapa makromolekul biologis). Distribusi ini dapat digambarkan dengan Mem”plot” berat polimer (BM diberikan) lawan BM, seperti terlihat pada gambar di bawah.
Panjang rantai polimer ditentukan oleh jumlah unit ulangan dalam rantai, yang disebut derajat polimerisasi (DPn). Berat molekular polimer adalah hasil kali berat molekul unit ulangan dan DPn.
. M0
DP Mn n
Mn = berat molekul rata-rata polimer
M0 = berat molekul unit ulangan ( sama dengan berat molekul monomer) DP = derajat polimerisasi
Contoh :
polimer poli(vinil klorida), PVC memiliki DP = 1000 maka berat molekulnya (Mn) adalah :
M0 (– CH2CHCl - ) = 63, DP = 1000 Mn = DP x M0
Mn = 63 x 1000 = 63000.
D. Metode Pengukuran
Ada beberapa metode pengukuran yang digunakan untuk menentukan berat molekul suatu polimer, dalam hal ini adalah berat molekul rata-rata jumlah dan berat molekul rata-rata berat.
Sebelum mencari nilai rata-ratanya, terlebih dahulu mencari berat total dari suatu polimer yang dirumuskan sebagai berikut :
W : Jumlah berat dari setiap bagian molekul polimer N : Jumlah mol
M : Berat molekul
Dari rumus diatas dapat dicari berat molekul rata-rata suatu polimer.
1. Berat Molekul Rata-Rata Jumlah (𝑴𝒏 )
Berat molekul rata – rata jumlah (𝑀 𝑛 ), diperoleh dari perhitungan bilangan atau jumlah molekul dari setiap berat dalam sampel bersangkutan. Berat total suatu sampel polimer adalah jumlah berat dari setiap spesies molekul yang ada. Dalam pengukuran berat molekul rata – rata jumlah semua molekul yang terdispersi dianggap memiliki berat yang sama pada suatu rantai polimer, namun antara rantai polimer yang satu dengan rantai polimer yang lain memiliki jumlah molekul yang berbeda sesuai dengan derajat polimerisasi dari suatu proses polimer.
Secara matematis dapat ditulis:
Dimana:
Mi : Jumlah mol setiap spesies i.
Ni : Jumlah molekul etiap spesies i.
Jadi berat molekul rata-rata jumlah (𝑀 𝑛 ) adalah berat sampel per mol.
2. Berat Molekul Rata-Rata Berat (𝑴𝒘)
Berat molekul rata – rata berat (𝑀 𝑤) dihitung berdasarkan pada massa dan polarisibilitas spesies polimer yang ada. Polimer dengan masa yang lebih besar maka kontribusinya ke pengukuran menjadi lebih besar. Berbeda dengan berat molekul rata – rata jumlah (yang merupakan jumlah fraksi mol masing – masing spesies dikalikan dengan molekulnya). Metode ini menjumlahkan fraksi berat masing – masing spesies dikalikan jumlah molekulnya. Nilai ini dikenal dengan berat molekul rata-rata berat (𝑀 𝑤).
Secara matematis diekspresikan sebagai berikut:
Polimer terdiri dari berbagai macam jenis, dan masing-masing jenis polimer tersebut tentunya memiliki berat molekul yang berbeda-beda.
Contoh soal :
1. Suatu sampel polimer yang terdiri dari 3 mol dengan berat molekul 20.000 dan 2 mol dengan berat molekul 70.000, hitunglah nilai dari:
a. Berat molekul rata - rata jumlah dan b. Berat molekul rata - rata berat
2. Suatu sampel polimer yang terdiri atas 9 mol dengan berat molekul 30.000 dan 5 mol dengan berat molekul 50.000. Hitunglah :
a. Berat molekul rata – rata jumlah b. Berat molekul rata-rata berat
Dari kasus tersebut terlihat bahwa 𝑀 𝑤 lebih besar dari pada 𝑀 𝑛 . Hal ini terjadi karena dalam pengukuran sifat koligatif, setiap molekul mempunyai kontribusi yang sama berapapun beratnya sedangkan dengan metode hamburan cahaya., molekul
efektif. Jika molekul – molekul polimer terdispersi dalam ruang luas, maka masing – masing molekul dalam satu rantai polimer memiliki bobot yang berbeda semakin banyak, namun jumlahnya sama sehingga menyebabkan 𝑀 𝑤 dalam suatu sampel lebih besar dari 𝑀 𝑛 . Atau dengan kata lain sistem yang memiliki suatu daerah berat molekul dikatakan sebagai polidispersi (𝑀 𝑤 > 𝑀 𝑛 ). Jika berat masing – masing berat molekul yang terdispersi dalam suatu sistem adalah sama, maka 𝑀 𝑤 = 𝑀 𝑛 , disebut sistim monodispersi.
E. Penentuan Berat Molekul Polimer Dengan Metoda Lain
Banyak sekali bahan polimer yang tergantung pada massa molekulnya. Misalnya kelarutan, ketercetakan, larutan serta lelehan. Karena itu perlu diketahui cara menentukan bobot molekul polimer.
Untuk menghitung nilai Mn dan Mw dapat dilakukan dengan berbagai metode pengukuran, dimana masing-masing memiliki metode yang berbeda-beda. Metode- metode tersebut yaitu:
1. Berat Molekul Rata-rata Jumlah (Mn) a. Osmometri
b. Analisis Gugus Ujung
2. Berat Molekul Rata-rata Berat (Mw) a. Hamburan Cahaya
b. Ultrasentrifugasi c. Viskositas
Berikut ini akan disajikan secara mendalam mengenai kelima metode tersebut:
1. Berat Molekul Rata-rata Jumlah (Mn)
a. Pengukuran Sifat Koligatif Larutan (Osmometri)
Osmometri adalah metode penentuan bobot yang didasarkan pada peristiwa Osmosis. Diantara berbagai metode penetapan berat molekul rata – rata jumlah yang didasarkan pada sifat – sifat koligatif, osmometri membran merupakan metode yang paling bermanfaat dalam menentukan jumlah partikel terlarut yang ada dengan menghasilkan harga rata-rata massa molekul relatif.
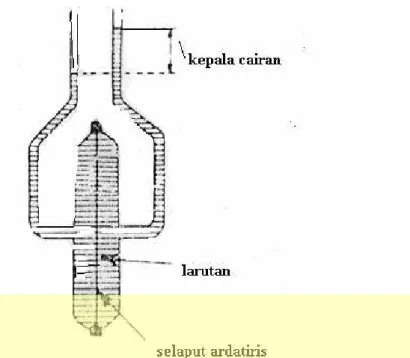
Osmosis dapat dikatakan sebagai pelewatan pelarut melalui selaput ardatiris atau semipermiabel dan pelarut murni ke dalam larutan atau larutan encer ke larutan yang lebih pekat. Selaput ini biasanya terdiri atas selofan atau pun bahan berselulosa lainnya. Selaput ini hanya melewatkan pelarut saja sedangkan zat terlarut tidak dapat dilewatkan.
Gambar 2. Membran Semipermeabel
Prinsip Kerja Osmometer :
Tekanan osmotik merupakan sifat koligatif yang bergantung kepada jumlah partikel terlarut yang ada, maka osmometri menghasilkan harga rata-rata berat molekul. Tekanan osmotik (P) suatu larutan adalah tekanan luar yang harus digunakan untuk mencegah lewatnya pelarut berlebih melalui selaput ardatiris ke dalam larutan.
Selaput ardatiris hanya dapat melewatkan pelarut sedangkan zat terlarut tidak dapat tembus. Berikut adalah gambar dari sebuah osmometri
Gambar 3. Osmometri
Mula-mula tinggi larutan pelarut sama, setelah dibiarkan beberapa saat osmosis terjadi ketika pelarut pindah ke larutan melalui membrane semi permiabel, sehingga tinggi larutan naik, tetapi pada suatu saat kenaikan berhenti karena sistem mengalami keseimbangan.
Pada keadaan ini selisih ketinggian pelarut dan larutan ialah massa molekul relatif polimer dapat dihitung dengan menggunakan persamaan:
𝝅
𝒄′= 𝑹𝑻
(𝑴)+𝑩𝒄′ Dimana:
π = Tekanan osmosis c’ = Konsentrasi larutan
R = Tetapan gas ideal 0,082 L atm mol-1K-1 = 8,314 Jmol-1K-1 T = Suhu (°Kelvin)
B = Koofesien visial
(M) = Massa molekul relative polimer
Kelemahan metode osmometri ialah ada beberapa jenis polimer yang tidak ikut terukur, yakni jenis yang memiliki berat molekul yang rendah, dikarenakan polimer dengan berat molekul rendah tersebut akan terdifusi melewati membran.
Akibatnya, jumlah berat molekul rata - rata jumlah yang terukur bukan menyatakan harga keseluruhan dari berat molekul polimer sampel. Kelemahan
lain dari metode ini adalah sulit untuk memilih selaput yang cocok, dan harga osmometer yang mahal.
b. Metode Analisis Gugus Ujung
Analisis gugus ujung merupakan teknik analisis polimer untuk mengetahui massa molekul satu sampel atau sistem dengan menghitung jumlah rantainya.
Dalam proses polarisasi pada suatu monomer awal dan akhir rantai, akan terdapat gugus fungsi yang tidak berkaitan dengan satuan monomer lain. Jika suatu polimer diketahui mengandung jumlah tertentu gugus ujung per molekulnya, maka jumlah gugus itu dapat ditentukan dalam jumlah massa polimer dengan metode analisis gugus ujung. Dengan demikian jika massa 1 mol polimer dapat ditentukan, maka molekul atau bobot molekul polimer juga dapat ditentukan.
Hal – hal yang harus diperhatikan dalam penerapan analisis gugus ujung:
1) Gugus ujung harus dapat dianalisis secara kuantitatif.
2) Jumlah gugus ujung yang dapat dianalisis harus diketahui dengan pasti.
3) Gugus fungsi lain yang mengganggu analisis harus ditiadakan.
4) Konsentrasi gugus ujung harus cukup besar.
5) Metode ini tidak dapat diterapkan pada polimer bercabang.
6) Dalam 1 polimer linier terdapat gugus ujung sebanyak dua kali molekul linier.
Metode analisis gugus ujung dapat dilakukan melalui beberapa cara yakni titrasi, penerapan spektroskopi UV, IR dan NMR, pengukuran aktivitas gugus ujung yang radioaktif serta analisis gugus ujung yang mengandung unsur tertentu.
Contoh analisis gugus ujung, dengan cara titrasi, prosedur kerjanya adalah sebagai berikut:
a) Sampel Poliester (gugus karboksil dan hidroksil), masing – masing ditimbang dan dilarutkan dalam pelarut yang cocok (aseton untuk karboksil dan dititrasi dengan basa NaOH dengan indicator penolftalein (titik akhir titrasi).
b) Untuk hidroksil sampel diasetilasi dengan anhidrat asetat berlebih untuk membebaskan asam asetat, bersama dengan gugus ujung distribusi dengan cara yang sama.
c) Dari kedua titrasi tersebut diperoleh milligram ekivalen karboksil dan
d) Jumlah mol polimer per gram dapat dihitung dengan persamaan : Mol polimer per gram = 𝑴𝒆𝒌𝑪𝑶𝑶𝑯+𝑴𝒆𝒌𝑶𝑯
𝟐 ×𝟏𝟎𝟎𝟎 ×𝑩𝒆𝒓𝒂𝒕 𝑺𝒂𝒎𝒑𝒆𝒍
C2, dinyatakan bahwa 2 gugus ujung dihitung per molekul.
e) Hitung berat molekul = 𝒎𝒐𝒍𝒑𝒐 𝐥𝐢𝐦 𝒆𝒓𝒑𝒆𝒓 𝒈𝒓𝒂𝒎𝟏
Gugus ujung lain yang dapat dititrasi adalah gugus amino dalam polisakarida, gugus asetil dalam poliamida bergugus asetil, isosianat dalam polistirena dan epoksida dalam polimer epoksi.
Contoh soal:
Andaikan 1 gram poliester yang diambil mengandung 1 gugus –COOH per molekul polimer. Jika CM2 larutan baku natrium hidroksida 0,01 mol dm3 diperlukan untuk menetralkan sampel tersebut. Berapa massa molekul relatif poliester tersebut?
Jawab:
Mol NaOH yang digunakan = 𝟏𝟎
𝟏𝟎𝟎×𝟎, 𝟎𝟏 = 𝟏𝟎−𝟒𝒎𝒐𝒍
Maka jumlah mol gugus –COOH = 10-4, karena tiap molekul polimer mengandung 1 gugus –COOH, jumlah mol polimer yang ada = 10-4 mol. Berat 10-
4 mol polimer tersebut adalah 1 gram. Maka 1 mol polimer beratnya 1/10-4 gram = 104 gram. Dengan demikian massa molekul polimer = 10.000.
Kelemahan dari metode ini adalah sebagai berikut:
Harus mengandaikan struktur molekul.
Tidak dapat dipakai untuk polimer bercabang.
Hanya dapat dipakai untuk polimer dengan daerah berat molekul < 10.000.
Keunggulan dari metode ini adalah:
Bisa dipakai untuk polimer kondensasi. Dipakai untuk menentukan bobot molekul yang mempunyai gugus fungsi.
Bisa dipakai untuk menentukan polimer poliamida, insiator, polyester dan radikal bebas.
2. Berat Molekul Rata-rata Berat (Mw) a. Hamburan Sinar / Cahaya
Hamburan cahaya (light scatering) adalah metode analisis polimer untuk menentukan berat molekul satu contoh dengan melihat jumlah cahaya yang dihamburkan oleh partikel – partikel dalam larutan. Hamburan cahaya dapat dipakai untuk mendapatkan berat molekul mutlak. Prinsip kerjanya didasarkan pada fakta bahwa cahaya, ketika melewati suatu pelarut atau larutan melepaskan energi yang diakibatkan oleh absorbsi, konversi ke panas dan hamburan.
Jika seberkas sinar ditembuskan kedalam cairan yang tak menyerap sinar, maka sebagian sinar dihamburkan. Jika cairan pelarut dibuat tak homogen oleh penambahan molekul nisbi maka hamburan tambahan akan terjadi.
Peningkatan hamburan dapat dihubungkan dengan konsentrasi larutan dan massa molekul nisbi zat terlarut, dibuat dalam persamaan Debye:
Dimana :
Skema alat penghamburan sinar sederhana :