PEMBIBITAN BENIH JAGUNG MENJADI BIOETHANOL
Oleh :
Adinda Gitawati
NPM : 0831010054
PROGRAM STUDI TEKNIK KIMIA FAKULTAS TEKNOLOGI INDUSTRI
UNIVERSITAS PEMBANGUNAN NASIONAL “VETERAN” JAWA TIMUR
KATA PENGANTAR
Puji syukur penyusun panjatkan ke hadirat Tuhan Yang Maha Esa atas Karunia dan rahmat-Nya sehingga penyusun dapat menyelesaikan laporan skripsi ini.
Penelitian ini merupakan salah satu syarat yang harus dipenuhi oleh mahasiswa tingkat akhir sebelum dinyatakan lulusan sebagai Sarjana Program Studi Teknik Kimia, Fakultas Teknologi Industri, Universitas Pembangunan Nasional “VETERAN” Jawa Timur.
Pada kesempatan ini penyusun melakukan penelitian dengan judul “Pemanfaatan Limbah Biji Jagung dari Industri Pembibitan Benih Jagung Menjadi Bioethanol”. Terima kasih sebesar – besarnya penyusun tujukan kepada semua pihak yang telah membantu penelitian hingga tersusunnya laporan ini, terutama kepada :
1. Bapak Ir. Sutiyono, MT. selaku Dekan Fakultas Teknologi Industri,
Universitas Pembangunan Nasional “VETERAN” Jawa Timur, serta selaku Dosen penguji.
2. Ibu Ir. Retno Dewati, MT. selaku Ketua Program Studi Teknik Kimia,
Fakutas Teknologi Industri, Universitas Pembangunan Nasional “VETERAN” Jawa timur.
3. Ibu Dr. Ir. Ni Ketut Sari, MT. selaku Dosen pembimbing dalam
penelitian ini.
4. Bapak Ir. Sukamto NEP, MT. selaku Dosen penguji.
5. Ibu Ir. Nurul Widji Triana, MT. Selaku Dosen Penguji.
6. Semua pihak yang tidak dapat dituliskan terperinci yang telah
Penyusun mengucapkan terima kasih yang sebesar – besarnya atas segala bantuan, fasilitas, yang telah diberikan kepada kami. Penyusun menyadari masih banyak kekurangan pada penyusunan laporan ini. Oleh karena itu kami mengharapkan saran dan kritik yang membangun atas laporan ini
Akhir kata, penyusun mohon maaf yang sebesar – besarnya kepada semua pihak, apabila dalam melaksanakan penelitian dan dalam penyusunan laporan ini penyusun melakukan kesalahan baik yang disengaja maupun tidak di sengaja.
Surabaya, Agustus 2011
DAFTAR ISI
HALAMAN JUDUL ... i
HALAMAN PENGESAHAN ... ii
KATA PENGANTAR ... iv
BAB II. TINJAUAN PUSTAKA 2.1. Tinjauan Umum ... 3
2.1.11. Saccharomyces Cereviceae... 19
2.3. Landasan Teori ... 22
BAB III. PELAKSANAAN PENELITIAN 3.1. Bahan - Bahan yang diperlukan ... 26
3.2. Alat – Alat yang Digunakan ... 26
3.3. Gambar dan susunan alat ... 26
3.4. Kondisi... 27
3.4.1. Hidrolisa ... 27
3.4.2. Fermentasi ... 28
3.5. Skema dan Prosedur Penelitian ... 29
BAB IV. HASIL DAN PEMBAHASAN 4.1. Hasil Analisa Kadar Glukosa, Pati Sisa, Bioethanol dan yield ... 34
4.2. Grafik dan Pembahasan 4.2.1. Grafik Analisa Kadar Glukosa dan Pati pada Proses Hidrolisa ... 35
4.2.2. Grafik Analisa Kadar Bioethanol pada Proses Fermentasi ... 38
BAB V. KESIMPULAN DAN SARAN 5.1 Kesimpulan ... 41
5.2 Saran ... 41
DAFTAR PUSTAKA ... 42
LAMPIRAN A ... 43
DAFTAR TABEL
Tabel 2.1 Kandungan Gizi Jagung per 100 gram Bahan ... 6
Tabel 2.2 Klasifikasi Jagung ... 6
Tabel 2.3 Produksi Bahan Bakar Ethanol Tahunan ... 11
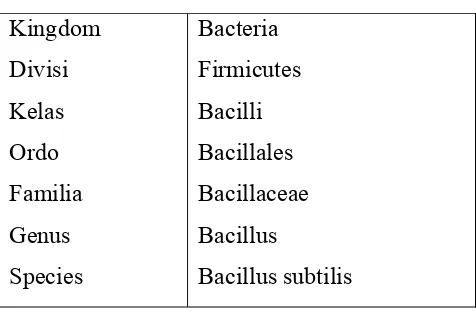
Tabel 2.4 Klasifikasi Bacillus Subtilis ... 19
Tabel 2.5 Klasifikasi Saccharomycess Cereviceae... 20
Tabel 4.1 Analisa Hasil Penelitian Kadar Glukosa dan Pati Sisa pada Proses Hidrolisa ... 34
DAFTAR GAMBAR
Gambar 2.1 Struktur Jagung... 6
Gambar 2.2 Limbah Biji Jagung ... 7
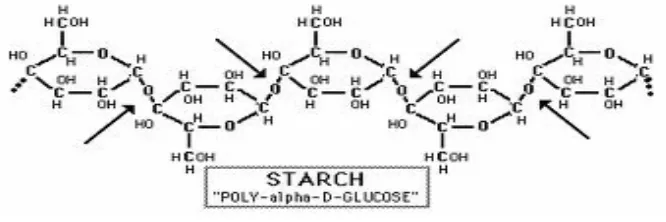
Gambar 2.3 Rantai Pati ... 9
Gambar 2.4 Kurva Pertumbuhan Jasad Renik ... 15
DAFTAR GRAFIK
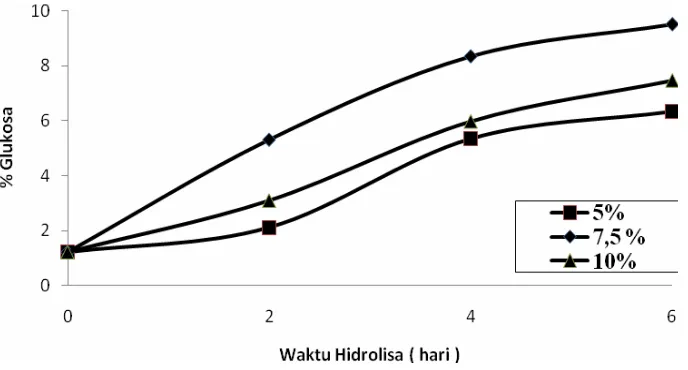
Gambar 4.1 Pengaruh Waktu Hidrolisa Terhadap % Glukosa
pada Perbandingan 1 : 3 ... 35
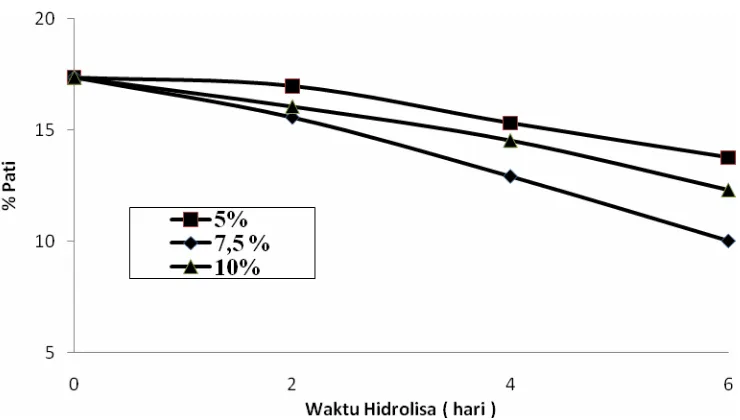
Gambar 4.2 Pengaruh Waktu Hidrolisa Terhadap % Pati Sisa
pada Perbandingan 1 : 3 ... 36
Gambar 4.3 Pengaruh Waktu Hidrolisa Terhadap % Glukosa
pada Perbandingan 1 : 5 ... 36
Gambar 4.4 Pengaruh Waktu Hidrolisa Terhadap % Pati Sisa
pada Perbandingan 1 : 5 ... 37
Gambar 4.5 Pengaruh Waktu Fermentasi Terhadap % Bioethanol
pada Perbandingan 1 : 5 dan Waktu 2 hari Hidrolisa ... 38
Gambar 4.6 Pengaruh Waktu Fermentasi Terhadap % Bioethanol
pada Perbandingan 1 : 5 dan Waktu 4 hari Hidrolisa ... 39
Gambar 4.7 Pengaruh Waktu Fermentasi Terhadap % Bioethanol
INTISARI
Alkohol atau sering disebut dengan ethanol (ethyl alcohol) yang didalam dunia industri sering digunakan sebagai bahan pelarut, dapat diproduksi dengan cara proses fermentasi menggunakan khamir Saccharomyces cereviceae.
Adapun bahan dasar yang dapat difermentasikan antara lain bahan – bahan yang mengandung sakarin, pati, dan sellulose. Produksi Bioethanol untuk penelitian saat dilakukan dengan menggunakan bahan dasar Pati yang berasal dari limbah biji jagung dari industri pembibitan benih jagung (PT. BISI INTERNASIONAL, Tbk) yang kadarnya 63%.
Sebelum dilakukan proses fermentasi, terlebih dahulu dilakukan proses
hidrolisa dengan menggunakan bakteri penghasil enzim α-amilase yaitu Bacillus
subtilis hingga diperoleh suatu larutan yang mengandung gula (glukosa). Larutan hasil hidrolisa yang mengandung kadar glukosa 15,22 ini kemudian difermentasi selama selang waktu yang telah ditentukan dengan menggunakan khamir jenis Saccharomyces cereviceae.
BAB I
PENDAHULUAN
1.1. Latar Belakang
Ethanol atau ethyl alcohol kadang disebut juga ethanol spiritus. Ethanol digunakan dalam beragam industri, bidang kesehatan dan pendidikan seperti bahan baku farmasi, kosmetika, dan campuran bahan bakar kendaraan, peningkat oktan, bensin ethanol (gasohol) dan sebagai sumber oksigen untuk pembakaran yang lebih bersih pengganti methyl tertiary-butyl ether/MTBE.
Pertumbuhan konsumsi ethanol di dunia mengalami pertumbuhan pesat dalam kurun waktu beberapa tahun terakhir. Pertumbuhan konsumsi ethanol selama tahun 2001 hingga 2009 rata-rata 17,8% per tahun. Pertumbuhan ini dikarenakan banyaknya negara di dunia yang mendorong penggunaan ethanol sebagai bahan bakar. Hal ini dapat dilihat melalui kebijakan negara-negara di dunia. Pada tahun 2010, konsumsi ethanol di dunia diperkirakan mencapai 21,7 juta galon dan ditahun 2015 diperkirakan meningkat 45,24 juta galon. Di Indonesia, industri ethanol kurang berkembang karena terkendala bahan baku yang pada umumnya menggunakan tetes atau molase. Selain karena factor tetes merupakan bahan yang dibutuhkan untuk industri lain seperti pembuatan bir dan pembuatan bumbu masak, kapasitas produksi dari industri atau pabrik gula di Indonesia juga semakin menurun.
Karena konsumsi ethanol Indonesia serta dunia semakin meningkat, maka dibutuhkan inovasi bahan baku alternatif yang bersifat renewable yang mampu menjadi ethanol dan lebih ramah lingkungan yaitu bioethanol, sehingga dapat menopang kebutuhan yang tinggi tersebut. Untuk itu dipilih pemanfaatan limbah biji jagung dari industri pembibitan benih jagung menjadi bioethanol.
Limbah biji jagung dihasilkan dari limbah industri pembibitan benih jagung yang berlokasi di sidoarjo, jawa timur. Biji jagung yang tidak dapat tumbuh ( afkir ) akan terbuang menjadi limbah industri. Berdasarkan hasil analisa awal, limbah ini mengandung kadar pati yang sangat tinggi yaitu kurang lebih 63%, sangat memungkinkan untuk diproses menjadi bioethanol. Pada limbah biji jagung terdapat kandungan berbahaya seperti pestisida, warna, bahan pengawet. Pemanfaatannya untuk menjadi bioethanol diperlukan beberapa proses, yaitu hidrolisis, fermentasi dan distilasi. Limbah biji jagung apabila diolah menjadi pakan ternak dan pupuk dilarang pemerintah, karena dalam proses pembuatan benih biji jagung unggulan dilakukan penambahan pestisida. Limbah biji jagung non benih saat ini tersedia 20 ton yang belum dimanfaatkan dan rata-rata produksi limbah biji jagung ini mencapai 2-4 ton/ bulan. Dengan potensi tersebut dipastikan sumber bahan baku pembuatan bioethanol akan tersedia dalam jumlah yang cukup besar (PT.Bisi Internasional Tbk, 2010).
1.2. Tujuan
Tujuan dari penelitian ini adalah meningkatkan nilai ekonomi limbah biji jagung dari industri pembibitan benih jagung, dan mencari kondisi terbaik pada proses hidrolisa, fermentasi dan distilasi sehingga diperoleh hasil biethanol yang optimal.
1.3. Manfaat
1. Memberikan nilai tambah untuk limbah biji jagung dari industri
2. Memanfaatkan limbah biji jagung dari industri pembibitan benih jagung sebagai bahan baku alternatif dalam produksi bioethanol.
3. Bioethanol dapat digunakan sebagai pengganti bahan bakar, pelarut, dan
bahan dasar pembuatan asetaldehyde, ethyl acetate dan sebagainya.
BAB II
TINJAUAN PUSTAKA
2.1.
Tinjauan Umum
2.1.1. Jagung
Berdasarkan temuan-temuan genetik, antropologi, dan arkeologi diketahui bahwa daerah asal jagung adalah Amerika Tengah (Meksiko bagian selatan). Budidaya jagung telah dilakukan di daerah ini 10.000 tahun yang lalu, teknologi ini dibawa ke Amerika Selatan (Ekuador) sekitar 7000 tahun yang lalu, dan mencapai daerah pegunungan di selatan Peru pada 4.000 tahun yang lalu. Kajian filogenetik menunjukkan bahwa jagung budidaya (Zea mays ssp. mays) merupakan keturunan langsung dari teosinte (Zea mays ssp. parviglumis). Dalam proses domestikasinya, yang berlangsung paling tidak 7.000 tahun oleh penduduk asli setempat, masuk gen-gen dari subspesies lain, terutama Zea mays ssp.
mexicana. Istilah teosinte sebenarnya digunakan untuk menggambarkan semua spesies dalam genus Zea, kecuali Zea mays ssp. mays. Proses domestikasi menjadikan jagung merupakan satu-satunya spesies tumbuhan yang tidak dapat hidup secara liar di alam. Hingga kini dikenal 50.000 kultivar jagung, baik yang terbentuk secara alami maupun dirakit melalui pemuliaan tanaman (Anonimous,2010).
Jagung merupakan tanaman semusim (annual). Satu siklus hidupnya diselesaikan dalam 80-150 hari. Paruh pertama dari siklus merupakan tahap pertumbuhan vegetatif dan paruh kedua untuk tahap pertumbuhan generatif.
Akar jagung tergolong akar serabut yang dapat mencapai kedalaman 8 m meskipun sebagian besar berada pada kisaran 2 m. Pada tanaman yang sudah cukup dewasa muncul akar adventif dari buku-buku batang bagian bawah yang membantu menyangga tegaknya tanaman.
Batang jagung tegak dan mudah terlihat, sebagaimana sorgum dan tebu, namun tidak seperti padi atau gandum. Terdapat mutan yang batangnya tidak tumbuh pesat sehingga tanaman berbentuk roset. Batang beruas-ruas, ruas terbungkus pelepah daun yang muncul dari buku, batang jagung cukup kokoh namun tidak banyak mengandung lignin.
Daun jagung adalah daun sempurna. Bentuknya memanjang, antara pelepah dan helai daun terdapat ligula. Tulang daun sejajar dengan ibu tulang daun. Permukaan daun ada yang licin dan ada yang berambut. Stoma pada daun jagung berbentuk halter, yang khas dimiliki familia Poaceae. Setiap stoma dikelilingi sel-sel epidermis berbentuk kipas. Struktur ini berperan penting dalam respon tanaman menanggapi defisit air pada sel-sel daun.
Jagung yang dibudidayakan memiliki sifat bulir/biji yang bermacam-macam. Menurut data Anonimous di dunia terdapat enam kelompok kultivar jagung yang dikenal hingga sekarang, berdasarkan karakteristik endosperma yang membentuk bulirnya:
1. Indentata (Dent, "gigi-kuda") 2. Indurata (Flint, "mutiara") 3. Saccharata (Sweet, "manis") 4. Everta (Popcorn, "berondong") 5. Amylacea (Flour corn, "tepung") 6. Glutinosa (Sticky corn, "ketan")
Dipandang dari bagaimana suatu kultivar ("varietas") jagung dibuat dikenal berbagai tipe kultivar :
1. Galur murni, merupakan hasil seleksi terbaik dari galur-galur terpilih
2. Komposit, dibuat dari campuran beberapa populasi jagung unggul yang
diseleksi untuk keseragaman dan sifat-sifat unggul
3. Sintetik, dibuat dari gabungan beberapa galur jagung yang memiliki
keunggulan umum (daya gabung umum) dan seragam
4. Hibrida, merupakan keturunan langsung (F1) dari persilangan dua, tiga, atau empat galur yang diketahui menghasilkan efek heterosis.
Table 2.1. Kandungan Gizi Jagung Per 100 Gram Bahan
Kalori Protein Lemak Pati Kalsium Fosfor Ferrum Vitamin
A
Tabel 2.2. Klasifikasi Jagung
Kingdom
2.1.2. Limbah Biji Jagung
beracun. Kandungan bahan organik dalam limbah biji jagung ini sangat tinggi, maka pengolahan yang paling sesuai adalah secara biologi.
Gambar 2.2. Limbah Biji Jagung
(PT.Bisi Internasional Tbk,2010)
2.1.3. Karbohidrat
Karbohidrat merupakan sumber kalori utama bagi manusia selain protein dan lemak. Karbohidrat yang mempunyai rumus empiris (CH2O)n ini juga
mempunyai peranan penting dalam menentukan karakteristik bahan makanan, misalnya rasa, warna, tekstur, dan lain – lain. Sedangkan dalam tubuh, karbohidrat berguna untuk mencegah timbulnya pemecahan protein tubuh yang berlebihan, kehilangan mineral dan berguna untuk membantu metabolisme lemak dan protein. Di alam, karbohidrat dibentuk dari reaksi CO2 dan H2O dengan bantuan sinar
matahari melalui proses fotosíntesis dalam sel tanaman yang berklorofil, bahan – bahan yang merupakan sumber karbohidrat diperoleh dari umbi – umbian dan batang tanaman misalnya sagu. Sumber karbohidrat yang merupakan bahan makanan pokok di berbagai daerah di Indonesia adalah biji – bijian, khususnya beras dan jagung.
Pada umumnya karbohidrat dapat dikelompokkan menjadi tiga bagian yaitu :
a) Monosakarida
Sedangkan ketosa mempunyai satu gugus keton. Monosakarida dengan 6 atom C disebut heksosa, misal glukosa (dekstrosa/gula anggur). Sedangkan yang mempunyai 5 atom C disebut pentosa, misal xilosa, arabinosa, dan ribose.
b) Oligosakarida
Merupakan polimer dari 2 – 10 monosakarida. Biasanya bersifat larut dalam air. Oligosakarida yang terdiri dari 2 molekul monosakarida disebut disakarida. Contoh dari disakarida adalah sukrosa. Oligosakarida diperoleh dari hasil hidrolisis polisakarida dengan bantuan enzim tertentu atau hidrolisis dengan asam.
c) Polisakarida
Disusun oleh banyak molekul monosakarida. Polisakarida dalam bahan makanan berfungsi sebagai bahan penguat tekstur (selulosa, hemiselulosa, pektin, dan lignin). Dan sebagai sumber energi (pati, glikogen, fruktan) (Winarno, 1994).
2.1.4. Pati
Pati atau amilum adalah karbohidrat kompleks yang tidak larut dalam air, berwujud bubuk putih, tawar dan tidak berbau. Pati merupakan bahan utama yang dihasilkan oleh tumbuhan untuk menyimpan kelebihan glukosa (sebagai produk fotosintesis) dalam jangka panjang. Hewan dan manusia juga menjadikan pati sebagai sumber energi yang penting.
Pati tersusun dari dua macam karbohidrat, amilosa dan amilopektin, dalam komposisi yang berbeda-beda. Amilosa memberikan sifat keras (pera) sedangkan amilopektin menyebabkan sifat lengket. Amilosa memberikan warna ungu pekat pada tes iodin sedangkan amilopektin tidak bereaksi. Penjelasan untuk gejala ini belum pernah bisa tuntas dijelaskan (Anonimous, 2010).
Gambar 2.3. Rantai Pati
(http://wikipedia-pati.jpg)
2.1.5. Glukosa
Glukosa adalah monosakarida yang paling banyak terdapat di alam sebagai produk dari proses fotosíntesis. Dalam bentuk bebas terdapat didalam buah – buahan, tumbuh – tumbuhan, madu, darah. Dalam bentuk ikatan terdapat sebagai glikosida didalam tubuh binatang, sebagai disakarida, dan polisakarida didalam tubuh tumbuhan. Glukosa juga dapat dihasilkan melalui hidrolisis polisakarida atau disakarida, dengan asam atau enzim. Sebagai aldoheksosa, glukosa memiliki 6 atom karbon didalam rantai molekulnya. Salah satu ujung rantai tersebut merupakan gugus aldehid. Atom – atom karbon nomor 2 sampai nomor 5 didalam rantai adalah gugus chiral. Dengan demikian terdapat 16 kemungkinan konfigurasi isomer pada glukosa. Semua konfigurasi isomer tersebut telah dikenal sebagian. Terdapat bebas dialam, sebagian yang lain harus dibuat secara sintesis (Soebijanto, 1986).
2.1.6. Ethanol
Ethanol atau etil alkohol (CH3CH2OH) dikenal dengan nama alkohol.
Paling sering digunakan sebagai bahan bakar motor, terutama sebagai biofuel aditif untuk bensin. Dunia produksi ethanol untuk bahan bakar transportasi meningkat tiga kali lipat antara tahun 2000 dan 2007 dari 17 miliar menjadi lebih dari 52 miliar liter. Dari 2007 hingga 2008, pangsa pasar ethanol dalam penggunaan bahan bakar jenis bensin global meningkat dari 3,7% menjadi 5,4%. Pada tahun 2009 produksi bahan bakar etanol di seluruh dunia mencapai 19,5 milyar galon (73,9 miliar liter).
Ethanol digunakan secara luas di Brazil dan di Amerika Serikat, dan bersama-sama kedua negara bertanggung jawab atas 89 % bahan bakar ethanol produksi dunia pada tahun 2009. Kebanyakan mobil di AS dapat berjalan pada campuran sampai dengan 10 % ethanol, dan penggunaan bensin ethanol 10% yang diamanatkan di beberapa negara bagian Amerika Serikat dan kota-kota. Sejak tahun 1976 pemerintah Brazil telah membuatnya menjadi wajib untuk mengkombinasikan ethanol dengan bensin, dan sejak 2007, hukum campuran sekitar 25 % ethanol dan 75% bensin (E25). Selain itu, pada 2010 Brasil memiliki armada lebih dari 10 juta fleksibel-bahan bakar kendaraan secara teratur menggunakan bahan bakar ethanol rapi (dikenal sebagai E100 ) (Anonimous,2010).
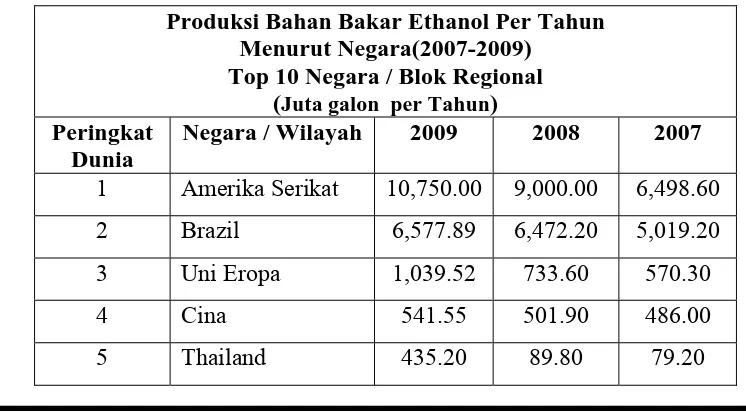
Table 2.4. Produksi Bahan Bakar Ethanol Tahunan.
Produksi Bahan Bakar Ethanol Per Tahun
1 Amerika Serikat 10,750.00 9,000.00 6,498.60 2 Brazil 6,577.89 6,472.20 5,019.20 3 Uni Eropa 1,039.52 733.60 570.30
6 Kanada 290.59 237.70 211.30 7 India 91.67 66.00 52.80 8 Kolumbia 83.21 79.30 74.90 9 Australia 83.21 26.40 26.40 10 Lainnya 247.27 - -
Total Dunia 19,534.99 17,335.29 13,101.70
(http://en.wikipedia.org/wiki/Ethanol_fuel).
Ethanol mempunyai sifat – sifat fisik sebagai berikut :
1. Cairan tidak berwarna
2. Berbau khas, menusuk hidung 3. Mudah menguap
4. Titik didih 78,32 oC 5. Larut dalam air dan eter
6. Densitas pada 15 oC adalah 0,7937
7. Spesifik panas pada 20 oC adalah 0,579 cal/groC 8. Panas pembakaran pada keadaan cair adalah 328 Kcal 9. Viskositas pada 20 oC adalah 1,17 cp
10.Flash point adalah sekitar 70 oC.
Sifat – sifat kimia ethanol :
1. Berat molekul adalah 46,07 gr/mol
2. Terjadi dari reaksi fermentasi monosakarida
Didalam perdagangan dikenal tingkat – tingkat kualitas ethanol sebagai berikut :
a. Alkohol teknis (96,5 oGL)
Digunakan terutama untuk kepentingan industri. Sebagai pelarut organik, bahan bakar, dan juga sebagai bahan baku ataupun untuk produksi berbagai senyawa organik lainnya.
b. Spiritus (88 oGL)
Bahan ini biasa digunakan sebagai bahan bakar untuk alat pemanas ruangan dan alat penerangan.
c. Alkohol absolute (99,7 – 99,8 oGL)
Banyak digunakan dalam pembuatan sejumlah besar obat – obatan dan juga sebagai bahan pelarut atau sebagai bahan didalam pembuatan senyawa – senyawa lain pada skala laboratorium.
d. Alkohol murni (96,0 – 96,5 oGL)
Alkohol jenis ini terutama digunakan untuk kepentingan farmasi dan konsumsi (minuman keras dan lain – lain) (Soebijanto, 1986).
2.1.7. Bioethanol
Bioethanol merupakan produk fermentasi yang dapat dibuat dari substrat yang mengandung karbohidrat (gula, pati/sukrosa) ataupun selulosa. Fermentasi bioethanol terjadi pada kondisi anaerob dengan menggunakan khamir tertentu yang dapat mengubah glukosa menjadi etanol (Othmer, 1953).
kayu dan beberapa limbah pertanian. Selain ketiga jenis bahan tersebut, etanol dapat juga dari bahan bukan asli pertanian tetapi dari bahan yang merupakan hasil proses lain. Sebagai contohnya adalah ethylene (Sa’id, 1987).
Bioethanol biasanya diperoleh dari konversi karbon berdasarkan bahan baku. Pertanian dianggap terbarukan karena mereka mendapatkan energi dari matahari menggunakan fotosintesis, dengan syarat semua mineral yang dibutuhkan untuk pertumbuhan (seperti nitrogen dan fosfor) dikembalikan ke tanah (Anonimous, 2010).
2.1.8. Hidrolisis
Hidrolisis, merupakan proses pemecahan suatu senyawa menjadi senyawa yang lebih sederhana dengan bantuan molekul air (Othmer, 1967).
Jenis hidrolisis ada lima macam yaitu sebagai berikut : 1. Hidrolisis murni
Pada proses ini hanya melibatkan air saja. Proses ini tidak dapat menghidrolisis secara efektif karena reaksi berjalan lambat. Hidrolisis murni ini biasanya hanya untuk senyawa yang sangat reaktif dan reaksinya dapat dipercepat dengan memakai uap air.
2. Hidrolisis dengan larutan asam
Menggunakan larutan asam sebagai katalis. Larutan asam yang digunakan dapat encer atau pekat, seperti H2SO4 atau HCl.
3. Hidrolisis dengan larutan basa
4. Alkali fusion
Hidrolisis ini dilakukan tanpa menggunakan air pada suhu tinggi, misalnya dengan menggunakan NaOH padat.
5. Hidrolisis dengan enzym
Hidrolisis ini dilakukan dengan menggunakan enzym sebagai katalis. Enzym yang digunakan dihasilkan dari mikroba seperti enzym α-amylase yang dipakai untuk hidrolisis pati menjadi glukosa dan maltosa (Groggins, 1958).
α-amylase yang diperoleh dari bacillus subtilis menghidrolisis pati dengan hasil utama maltoheksosa, maltopentaosa, dan sedikit glukosa 4-5% (Sari, 2010).
2.1.9. Fermentasi
Kata fermentasi berasal dari bahasa latin “Fervere” yang berarti merebus (to boil). Arti kata dari bahasa latin tersebut dapat dikaitkan dengan kondisi cairan bergelembung atau mendidih. Keadaan ini disebabkan adanya aktivitas ragi pada ekstraksi buah-buahan atau biji-bijian. Gelembung-gelembung karbondioksida dihasilkan dari katabolisme anaerobic terhadap kandungan gula. Fermentasi pada umumnya mempunyai pengertian suatu proses terjadinya perubahan kimia pada suatu substrat organic melalui aktivitas enzim yang dihasilkan oleh mikroba, walaupun dalam beberapa hal dapat juga terjadi tanpa adanya sel-sel hidup(mikroba).
Pertumbuhan Mikroorganisme
Pertumbuhan sel merupakan puncak aktivitas fisiologik yang saling mempengaruhi secara beraturan. Proses pertumbuhan ini sangat kompleks mencakup pemasukan nutrient dasar dari lingkungan ke dalam sel, konversi bahan – bahan nutrient menjadi energi dan berbagai konstituen sel yang vital serta perkembangbiakan. Pertumbuhan mikroorganisme dapat ditandai dengan peningkatan jumlah dan masa sel, sedangkan kecepatan pertumbuhan tergantung pada lingkungan fisik dan kimianya.
Pertumbuhan mikroorganisme dapat digambarkan sebagai kurva berikut :
Gambar 2.4. Kurva Pertumbuhan Jasad Renik
Keterangan gambar : a. Fase adaptasi
Fase ini adalah waktu penyesuaian suatu mikroorganisme yang dipindahkan ke media lain yang berbeda dari media asalnya. Lamanya fase ini dipengaruhi oleh beberapa faktor, diantaranya : 1. Medium dan lingkungan pertumbuhan
penyesuaian untuk mensintesa enzim – enzim yang dibutuhkan untuk metabolisme.
2. Jumlah inokulum
Jumlah awal sel yang semakin tinggi akan mempercepat fase adaptasi.
b. Fase pertumbuhan awal
Setelah mengalami fase adaptasi, sel mulai membelah dengan kecepatan yang masih rendah karena baru selesai tahap penyesuaian diri.
c. Fase pertumbuhan logaritmik
Sel jasad renik membelah dengan cepat dan konstan, dimana pertumbuhan sangat dipengaruhi oleh medium tempat tumbuhnya, seperti pH, kandungan nutrient, suhu dan kelembaban udara. Pada fase ini sel membutuhkan energi lebih banyak dari fase lainnya dan juga paling sensitive terhadap keadaan lingkungan.
d. Fase pertumbuhan lambat
Pada fase ini pertumbuhan populasi jasad renik diperlambat karena beberapa sebab :
1. Zat nutrisi didalam medium sudah sangat berkurang.
2. Adanya hasil – hasil metabolisme yang mungkin beracun atau dapat menghambat pertumbuhan jasad renik.
e. Fase pertumbuhan statis
f. Fase menuju kematian dan Fase kematian
Pada fase ini sebagian populasi jasad renik mulai mengalami kematian karena beberapa sebab, yaitu :
1. Nutrient didalam medium sudah habis
2. Enargi cadangan didalam sel habis (Yuliana, 2005).
Pembuatan Starter
Starter adalah susunan bakteri dalam jumlah yang cukup banyak untuk ditambahkan dalam suatu larutan bahan mentah yang sudah disiapkan untuk proses fermentasi. Banyaknya starter adalah sekitar 3 – 10 % dari bahan yang akan difermentasi. Faktor – faktor yang mempengaruhi pembuatan starter diantaranya adalah :
a. Temperature b. Waktu
c. Adanya penambahan pupuk d. Vitamin
Penyiapan Starter antara lain : a. Regenerasi kultur
Pertumbuhan optimum dapat dicapai bila kultur dalam keadaan segar sebelum diinokulasi. Untuk itu kultur yang akan digunakan diinokulasikan pada media agar miring selama 48 jam. Selain itu regenerasi memungkinkan untuk mendapatkan kultur atau starter di fase ekponensial. Hal ini akan dapat mempersingkat masa adaptasi dan laju pertumbuhan optimal yang mungkin diperoleh dalam waktu relative cepat.
b. Starter dalam media cair
ini dibuat dengan basis konsentrasi substart yang lebih encer (Rahman, 1989).
2.1.10 Bacillus subtilis
Jika keadaan lingkungan tidak menguntungkan seperti suhu tinggi, kekeringan atau zat-zat kimia tertentu, beberapa spesies dari Bacillus yang aerob dapat mempertahankan diri dengan spora. Spora tersebut dibentuk dalam sel yang disebut endospora. Endospora dibentuk oleh penggumpalan protoplasma yang sedikit sekali mengandung air. Oleh karena itu endospora lebih tahan terhadap keadaan lingkungan yang tidak menguntungkan dibandingkan dengan bakteri aktif. Apabila keadaan lingkungan membaik kembali, endospora dapat tumbuh menjadi satu sel bakteri biasa. Letak endospora di tengah-tengah sel bakteri atau pada salah satu ujungnya. Bacillus subtilis juga merupakan bakteri penghasil antibiotic, yang mempunyai daya hambat terhadap kegiatan mikroorganisme lain (Anonimous, 2010).
Banyak spesies Bacillus dapat mengeluarkan sejumlah besar enzim.
Amyloliquefaciens Bacillus merupakan spesies Bacillus yang merupakan sumber protein alami antibiotik barnase (a ribonuklease ), alfa amilase yang digunakan dalam hidrolisis pati, yang protease subtilisin digunakan dengan deterjen, dan BamH1 enzim restriksi yang digunakan dalam penelitian DNA. Bacillus subtilis
merupakan salah satu prokariota terbaik, dari segi biologi molekuler dan biologi sel.
Cara mudah untuk mengisolasi Bacillus adalah dengan menempatkan tanah non steril dalam tabung reaksi dengan air, getarkan, lalu tempatkan di media agar - agar, dan inkubasi pada suhu kamar selama minimal sehari. Koloni biasanya besar, menyebar dan berbentuk tidak teratur. Di bawah mikroskop,
endospora pada salah satu ujungnya, sehingga berbentuk tonjolan (Anonimous,
2010).
Tabel 2.5. Klasifikasi Bacillus subtilis
Kingdom
2.1.11. Saccharomyces cereviceae
Istilah khamir umunya digunakan untuk menyebutkan bentuk-bentuk mikroorganisme yang menyerupai jamur dari kelompok Ascomycetes yang tidak berfilamen tetapi uniseluler dengan bentuk ovoid atau spheroid. Saccharomycess cerevisiae merupakan khamir yang paling popular dalam pengolahan makanan. Khamir ini telah lama digunakan dalam industry wine dan bir. Dalam bidang pangan, khamir digunakan dalam pengembangan adonan roti dan dikenal sebagai ragi roti. Penggunaan dalam produksi etanol secara fermentasi telah banyak dikembangkan di beberapa negara, seperti Brasil, Afrika Selatan, dan Amerika Serikat. Hal ini disebabkan karena Saccharomycess cerevisiae dapat memproduksi etanol dalam jumlah besar dan mempunyai toleransi terhadap alkohol yang tinggi. Selain Saccharomycess cerevisiae, Zymomonas mobilis
Saccharomycess cerevisiae adalah mikroorganisme penghasil ethanol yang paling dikenal saat ini (Anonimous,2010).
Adapun sifat – sifat dari Saccharomyces Cereviceae antara lain adalah :
a. Berbentuk bulat (ellips).
b. Tidak berflagella.
c. Tidak mempunyai klorofil.
d. Dapat membentuk spora.
Tabel 2.6. Klasifikasi Saccharomycess Cereviceae
Kingdom c. Bau menyengat dan beracun d. Freezing point : -114’C
e. Boiling point : 110 °C(383K) untuk larutan 20,2% ; 48 °C(321K) untuk larutan 38%.
b. Berat molekul : 36,4609 c. Spesifik gravity : 1,268 d. Sangat larut dalam air
Larutan asam klorida atau yang biasa kita kenal dengan larutan HCl dalam air, adalah cairan kimia yang sangat korosif dan berbau menyengat. HCl termasuk bahan kimia berbahaya atau B3. Di dalam tubuh HCl diproduksi dalam perut dan secara alami membantu menghancurkan bahan makanan yang masuk ke dalam usus. Dalam skala industri, HCl biasanya diproduksi dengan konsentrasi 38%. Ketika dikirim ke industri pengguna, HCl dikirim dengan konsentrasi antara 32~34%. Pembatasan konsentrasi HCl ini karena tekanan uapnya yang sangat tinggi, sehingga menyebabkan kesulitan ketika penyimpanan. Beberapa bidang yang memanfaatkan HCl, baik pada skala industri maupun skala rumah tangga.
1. Asam klorida digunakan pada industri logam untuk menghilangkan karat atau kerak besi oksida dari besi atau baja.
2. Sebagai bahan baku pembuatan vinyl klorida, yaitu monomer untuk pembuatan plastik polyvinyl chloride atau PVC.
3. HCl merupakan bahan baku pembuatan besi (III) klorida (FeCl3) dan
polyalumunium chloride (PAC), yaitu bahan kimia yang digunakan sebagai bahan baku koagulan dan flokulan. Koagulan dan flokulan digunakan pada pengolahan air.
4. Asam klorida dimanfaatkan pula untuk mengatur pH (keasaman) air limbah cair industri, sebelum dibuang ke badan air penerima.
6. Di laboratorium, asam klorida biasa digunakan untuk titrasi penentuan kadar basa dalam sebuah larutan.
7. Asam klorida juga berguna sebagai bahan pembuatan cairan pembersih porselen.
8. HCl digunakan pada proses produksi gelatin dan bahan aditif pada makanan.
9. Pada skala industri, HCl juga digunakan dalam proses pengolahan kulit.
10. Campuran asam klorida dan asam nitrat (HNO3) atau biasa disebut
dengan aqua regia, adalah campuran untuk melarutkan emas.
Kegunaan-kegunaan lain dari asam klorida diantaranya adalah pada proses produksi baterai, kembang api dan lampu blitz kamera. 11 kegunaan asam klorida atau HCl di atas hanyalah sebagian diantaranya. Masih banyak bidang lain yang mempergunakannya (Hudiko, 2009).
2.3
. Landasan Teori
Limbah biji jagung dihasilkan dari proses pembibitan biji jagung unggulan. Limbah biji jagung ini memiliki kandungan bahan organik yang tinggi, selain itu mengandung senyawa sianida (pestisida) yang bersifat toksik. Kandungan bahan organik dalam limbah biji jagung ini sangat tinggi, pengolahan yang paling sesuai adalah secara biologi. Untuk membuat limbah biji jagung non benih sebagai bioethanol digunakan beberapa proses yaitu hidrolisa dan fermentasi.
Dalam pembuatan Bioethanol dilakukan beberapa proses yakni :
2.3.1. Proses Hidrolisis
amilase menjadi komponen disakarida yaitu maltosa. Dengan menggunakan enzim lain yaitu maltase, maltosa akan dihidrolisis menjadi glukosa (Sa’id, 1987).
(C6H10O5) + H2O HCl (C6H12O6)
Pati Bacillus subtilis Glukosa
Proses hidrolisis dipengaruhi dengan beberapa faktor, antara lain sebagai berikut : a. Kandungan pati pada bahan baku
Kandungan pati sedikit maka akan menghasilkan glukosa sedikit dan sebaliknya. Akan tetapi pengaruh dari kemampuan penguraian mikroba atau bakteri juga harus diperhatikan.
b. Suhu hidrolisis
Pada umumnya semakin tinggi suhu, semakin naik laju reaksi baik yang tidak dikatalis maupun yang dikatalis oleh enzim. Akan tetapi jika suhu yang terlalu tinggi dapat mempercepat pemecahan atau perusakan enzim. Hampir semua enzim mempunyai aktivasi optimal pada suhu 30 oC – 40 oC.
c. pH
pH berpengaruh terhadap jumlah produk hidrolisis. Enzim menunjukkan aktivitas maksimum pada suatu kisaran pH yang disebut pH optimum. Dimana pH optimum umumnya berkisar antara 4,5 – 8. pH optimum suatu enzim berbeda, bergantung pada asal enzim tersebut.
2.3.2. Proses Fermentasi
Bioethanol merupakan bentuk alami yang dihasilkan dari proses fermentasi yang banyak ditemukan dalam produk bir, anggur, spiritus, dan masih banyak lagi. Minuman beralkohol dapat digolongkan menjadi dua bagian, yaitu : 1. Produk hasil fermentasi yang dikonsumsi langsung.
Dalam pembentukan alkohol melalui fermentasi, peran mikroorganisme sangat besar dan biasanya mikroorganisme yang digunakan untuk fermentasi mempunyai beberapa syarat sebagai berikut :
1. Mempunyai kemampuan untuk memfermentasi glukosa secara cepat 2. Mempunyai genetik yang stabil (tidak mudah mengalami mutasi) 3. Toleran terhadap alkohol yang tinggi (antara 14 – 15%)
4. Mempunyai sifat regenerasi yang cepat.
Minuman beralkohol yang dihasilkan tanpa distilasi (hasil fermentasi) biasanya mempunyai kadar alkohol antara 12 – 15%. Untuk mempertinggi kadar alkohol sering dilakukan tahap lanjutan yaitu didistilasi dan kadar alkohol yang dihasilkan antara 95 – 96%. Prinsipnya reaksi proses pembentukan bioethanol dengan fermentasi sebagai berikut :
C6H12O6 Saccharomyces C. 2C2H5OH + 2CO2
Glukosa Bioethanol (Yuliana, 2005).
Faktor – faktor yang mempengaruhi dalam proses fermentasi antara lain sebagai berikut :
a. pH
pH yang baik untuk fermentasi, yaitu antara 4,5 – 5. pH ini adalah pH yang disenagi oleh ragi dan pada pH ini dapat menahan perkembangan banyak jenis bakteri. Untuk mengasamkan biasanya dipergunakan asam sulfat, yang lebih baik lagi adalah asam laktat, karena asam laktat baik untuk pertumbuhan ragi, tetapi keburukannya dapat tumbuh bakteri asam butirat yang dapat merugikan fementasi dan ragi.
b. Waktu
Apabila lebih dari 7 hari akan menyebabkan semakin tinggi kadar bioethanol yang dihasilkan sehingga terjadi kematian pada bakteri. (Yuliana, 2005) c. Suhu
Pada umumnya suhu yang baik untuk proses fementasi antara 25 – 30
o
C. Semakin rendah suhu fermentasi akan semakin tinggi alkohol yang dihasilkan. Hal ini dikarenakan pada suhu yang rendah fermentasi akan lebih lengkap dan kehilangan alkohol karena terbawa oleh gas karbondioksida akan lebih sedikit.
d. Bahan nutrient
Kecepatan fermentasi akan dipengaruhi oleh konsentrasi garam logam dalam perasan. Pada konsentrasi yang rendah akan menstimulur aktivitas dan pertumbuhan Saccaromyces cereviceae, sedangkan pada konsentrasi tinggi akan menghambat pertumbuhan Saccaromyces cereviceae. Unsur yang dibutuhkan untuk aktivitas Saccaromyces cereviceae antara lain Mg, K, Zn, CO, Fe, Ca, Cu, P, S, dan N. Sebagai sumber P dan N perlu ditambahkan ammonium phospat. Sebagai sumber N lainnya dapat pula ditambahkan ammonium klorida dan ammonium karbonat. Vitamin yang berfungsi sebagi faktor pertumbuhan Saccaromyces cereviceae.
2.4. Hipotesa
Kadar pati yang terkandung dalam limbah biji jagung dapat diproduksi menjadi bioethanol dengan proses hidrolisis dan fermentasi.
BAB III
PELAKSANAAN PENELITIAN
3.1. Bahan – bahan yang diperlukan
Pada penelitian ini bahan utama yang digunakan adalah Limbah Biji Jagung dari hasil pembibitan benih jagung yang kita dapatkan dari PT. Bisi Internasional. Bahan pendukung lainnya adalah Saccharomyces cereviceae dan Bacillus subtilis yang dibeli di beli di laboratorium Universitas Erlangga Surabaya. HCl yang kami beli di toko bahan kimia Brataco Tidar Surabaya dan kentang, glukosa, yeast, agar, aquadest sebagai bahan untuk membuat media agar.
3.2. Alat – alat yang digunakan
1. Alat Hidrolisis 2. Alat Fermentasi
3.3. Gambar dan Susunan Alat :
3.3.1. Gambar Alat Hidrolisis
1 2
Keterangan : 1. Pengaduk.
3.3.2. Gambar Alat Fermentasi
3.4. KONDISI
3.4.1. Hidrolisis
A. Kondisi yang ditetapkan
1. pH = 4,5 (dengan penambahan HCl atau NaOH).
2. Perbandingan jagung dengan air = 1:3 (333,3 gr jagung 1 liter H2O); 1:5 (200 gr jagung 1 liter H2O).
3. HCl = 20 ml.
4. Volume limbah biji jagung = 50 ml. 5. Suhu = 25 oC.
6. Bacillus subtilis = 5; 7,5; 10 (% v/v) dari filtrat.
1 2 4 3
Keterangan : 1. Botol
B. Kondisi yang dijalankan
1. Waktu Hidrolisa = 2; 4; 6 (hari).
3.4.2. Fermentasi
A. Kondisi yang ditetapkan
1. pH = 4,5 (dengan penambahan HCl atau NaOH).
2. Volume limbah biji jagung = 50 ml. 3. Suhu = 25 oC.
4. Bahan Nutrient = 70 – 400 gr per 100 lt.
5. Saccharomycess = 5; 7,5; 10 (% v/v) dari filtrat.
B. Kondisi yang dijalankan
1. Waktu fermentasi = 3 ; 6 ; 9 ; 12 ; 15 (hari).
3.5. Prosedur Penelitian
3.5.1. Pembuatan Media Agar (Media Pertumbuhan)
Setelah dingin, saring lalu ambil filtratnya. Filtratnya masukkan kedalam masing – masing tabung reaksi. Kemudian sterilkan dengan menggunakan autoclave, selama 3 jam dengan suhu 121 oC. Dinginkan sambil dimiringkan. Maka media tersebut siap untuk ditanami.
3.5.2. Pembuatan starter Bacillus dan Saccharomycess
Ambil 0,5 gr Bacillus Subtilis ditambah 1 gr glukosa lalu larutkan dengan aquadest sebanyak 100 ml. Kemudian sterilkan dalam autoclave pada suhu 121 oC selama 15 menit. Kemudian diinkubasi hingga terjadi gelembung – gelembung dipermukaan. Hal yang sama juga dilakukan pada Saccharomycess.
3.5.3. Pembuatan Bioethanol
Limbah biji jagung non benih direndam hingga warna merah yang ada pada limbah biji jagung tersebut hilang. Kemudian digiling hingga menjadi halus (tepung jagung). Limbah biji jagung yang telah menjadi tepung jagung dicampur H2O dengan perbandingan 1:3 (333,3 gr jagung
dan 1 liter H2O) dan 1:5 (200 gr jagung dan 1 liter H2O). Dilakukan
hidrolisa dengan penambahan HCl yang pHnya ditetapkan 4,5. Kemudian diinokulasi I yang bertujuan untuk menanamkan starter Bacillus subtilis
dengan konsentrasi 5; 7,5; 10 (% v/v), dengan waktu hidrolisa selama 3, 6, 9, 12, 15 hari.
Disaring dan diambil filtratnya lalu didistilasi dengan suhu 78 oC agar didapatkan kadar bioethanol yang murni.
3.6. Skema Penelitian
Bacillus Subtilis
0,5 gr
Glukosa 1 gr
Dilarutkan dalam H2O 100 ml
Sterilkan dalam inkubator pada suhu kamar
Inkubasikan Sampai terjadi gelembung
- gelembung dipermukaan
3.6.3. Pembuatan Starter Saccharomyces
Saccharomyces
0,5 gr
Glukosa 1 gr
Dilarutkan dalam H2O 100 ml
Sterilkan dalam inkubator pada suhu kamar
Inkubasikan Sampai terjadi gelembung
- gelembung dipermukaan
3.6.4. Pembuatan Bioethanol
Analisa Kadar Glukosa dan Pati sisa
Starter Saccharomyces Cereviceae 5%;7,5%;10 % v/v
Analisa bioethanol dan Glukosa sisa
Limbah Biji Jagung
Fermentasi(3,6,
Hidrolisis (125-200 rpm, 2,4,6 Hari) H2O
HCl
Nutrient
3.7. Metode Analisa
3.7.1. Analisa Kadar Ethanol
Menggunakan Spektrofotometer Pharo 100
Preparasi :
1. Pipet 0,2 ml sampel ke dalam cell bulat kosong.
2. Tambahkan 2 x 5.0 ml cell bulat, tutup dengan tutup ulir dan aduk.
3. Pipet 0.5 ml sampel terlarut ke dalam cell reaksi, tutup dengan penutup ulir dan larutkan granulat.
4. Biarkan selama 3 sampai 30 menit.
5. Tambahkan 5 ml air dengan pipet ke dalam cell reaksi, tutup dengan tutup ulir dan campur.
6. Waktu reaksi : 30 detik.
7. Tempatkan cell ke dalam ruang cell. Sejajarkan tanda pada cell dengan tanda pada fotometer.
3.7.2. Analisa Kadar Glukosa
Menggunakan Spektrofotometer Pharo 100
Preparasi :
Bahan – bahan kimia yang perlu disiapkan adalah :
a. Larutan I : larutan 12 g garam Rochells (Kna-tartarat) 24 g Na2CO3
anhidrat, 16 g NaHCO3 dan 144 g Na2SO4 anhidrat dalam air hingga
volumenya 800 ml.
b. Larutan II : larutan 4 g CuSO4.5H2O dan 36 g Na2SO4 dalam air,
hingga volumenya 200 ml.
c. Reagen Nelson : larutan 25 g ammonium molibdat (NH4)6
MO2O24.4H2O dalam air sebanyak 450 ml. Tambahkan H2SO4 pekat
sebanyak 21 ml. Selanjutnya larutan 3 g Na2H A SO4.7H2O (Sodium
sebelum dipakai larutan yang baik adalah berwarna kuning tanpa sebagian berwarna hijau.
3.7.3. Analisa Pati
Menggunakan Spektrofotometer Pharo 100
Preparasi :
Ekstraksi dengan ethanol panas 80% → timbang berat
Biarkan 1 – 2 jam suhu kamar
HCl 10 ml
Ditambahkan H2O → 100 ml, saring
Filtrat 50 ml pertama dibuang
Diambil 0,25 ml → diencerkan hingga 20 ml
Diambil 2 ml
Ditambah fenol 80 % 0,1 ml
Ditambah 5 ml H2SO4
Biarkan 10 menit
Digojog sekitar 20 menit
λ = 490 nm
3.7.4. Analisa Pestisida
- Mobile fasa
- Ret-time : 25 min
PREPARASI
~ ± 5 gr sampel → 100 ml H2O, saring
~ ambil 10 ml → dalam 100 ml H2O
BAB IV
HASIL DAN PEMBAHASAN
4.1. Hasil Penelitian
Dari penelitian yang dilakukan di Laboratorium Instrumentasi, didapatkan
data – data yang di tabelkan seperti di bawah ini.
5% 7,5 % 10% 5% 7,5 % 10%
1.21 1.21 1.21 17.36 17.36 17.36
2.11 5.31 3.09 16.98 15.56 16.05
5.34 8.35 5.97 15.31 12.91 14.53
6.33 9.52 7.46 13.76 10.01 12.31
0.81 0.81 0.81 11.19 11.19 11.19
3.32 6.32 5.17 10.77 9.15 10.12
5.09 10.65 7.45 10.01 8.76 9.32
7.43 15.22 11.12 9.31 7.13 8.11 Bahan Baku Waktu Hidrolisa (hari) Kadar Glukosa (%) Kadar Pati (%)
1 : 3
Tabel 4.1. Hasil analisis kadar glukosa dan pati sisa pada proses hidrolisa
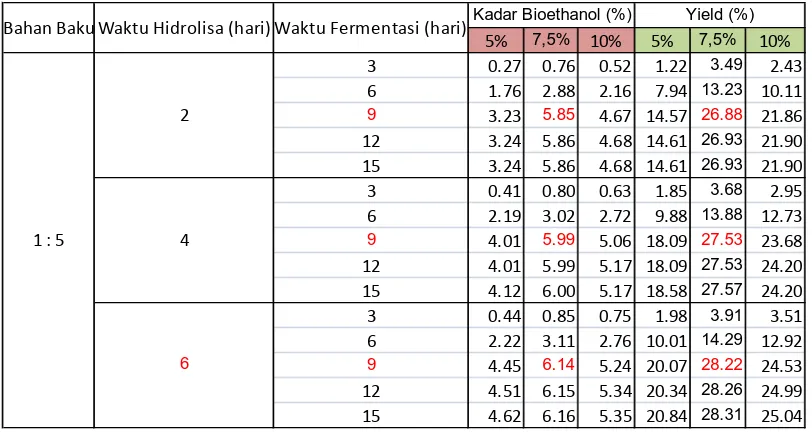
Tabel 4.2. Hasil analisis kadar bioethanol dan perhitungan yield pada proses fermentasi
5% 7,5% 10% 5% 7,5% 10%
3 0.27 0.76 0.52 1.22 3.49 2.43
6 1.76 2.88 2.16 7.94 13.23 10.11
9 3.23 5.85 4.67 14.57 26.88 21.86
12 3.24 5.86 4.68 14.61 26.93 21.90
15 3.24 5.86 4.68 14.61 26.93 21.90
3 0.41 0.80 0.63 1.85 3.68 2.95
6 2.19 3.02 2.72 9.88 13.88 12.73
9 4.01 5.99 5.06 18.09 27.53 23.68
12 4.01 5.99 5.17 18.09 27.53 24.20
15 4.12 6.00 5.17 18.58 27.57 24.20
3 0.44 0.85 0.75 1.98 3.91 3.51
6 2.22 3.11 2.76 10.01 14.29 12.92
9 4.45 6.14 5.24 20.07 28.22 24.53
12 4.51 6.15 5.34 20.34 28.26 24.99
15 4.62 6.16 5.35 20.84 28.31 25.04
Waktu Fermentasi (hari)Kadar Bioethanol (%) Yield (%)
1 : 5
2
4
6
4.2. Grafik dan Pembahasan
4.2.1. Hasil Analisis Kadar Glukosa dan Pati Pada Proses Hidrolisa
Grafik 4.1. Pengaruh waktu hidrolisa terhadap % glukosa Perbandingan 1:3
Grafik 4.2. Pengaruh waktu hidrolisa terhadap % pati sisa
Perbandingan 1:5
Grafik 4.3. Pengaruh waktu hidrolisa terhadap % glukosa
Grafik 4.4. Pengaruh waktu hidrolisa terhadap % pati sisa
Berdasarkan gambar 4.3.4, terlihat bahwa semakin lama waktu hidrolisa kadar pati sisa semakin kecil, karena semakin lama waktu hidrolisa maka semakin banyak pati yang terhidrolisa membentuk glukosa. Pada waktu hidrolisa yang sama, penambahan Bacillus sebesar 7,5% adalah pati yang tersisa berada pada titik terendah yaitu 7,13%.
4.2.2. Hasil Analisis Kadar Bioethanol pada Proses Fermentasi
Perbandingan 1:5
Grafik 4.5. Pengaruh waktu fermentasi terhadap % bioethanol, 2 hari hidrolisa
Saccarhomyces yang tinggi dengan jumlah glukosa yang tertentu mengakibatkan Saccarhomyces mengalami kematian karena kekurangan glukosa.
Grafik 4.6. Pengaruh waktu fermentasi terhadap % bioethanol, 4 hari hidrolisa
Grafik 4.7. Pengaruh waktu fermentasi terhadap % bioethanol, 6 hari hidrolisa
Berdasarkan gambar 6, terlihat bahwa semakin lama waktu fermentasi kadar bioethanol yang diperoleh semakin meningkat dan pada suatu saat kadar bioethanol akan konstan, hal ini disebabkan karena kehidupan mikroorganisme Saccarhomyces berbentuk logaritmik. Pada waktu fermentasi yang sama,
Penambahan Saccarhomyces sebesar 7,5%menghasilkan bioethanol yang terbesar
yaitu 6,14% dengan 28,22%. Karena pada Saccarhomyces yang rendah, mengakibatkan terurainya glukosa menjadi bioethanol kecil karena jumlah glukosa yang besar dengan Bacillus yang rendah. Pada konsentrasi Saccarhomyces yang tinggi dengan jumlah glukosa yang tertentu mengakibatkan Saccarhomyces mengalami kematian karena kekurangan glukosa.
BAB V
KESIMPULAN DAN SARAN
5.1. Kesimpulan
Berdasarkan hasil penelitian dapat disimpulkan beberapa hal yaitu :
1. Limbah jagung mengandung 63% pati dan 4,85% glukosa.
2. Proses hidrolisa pati menjadi glukosa terbaik pada perbandingan 1:5 (berat per
pelarut)dengan waktu hidrolisa 6 hari dan 7,5% bacillus diperoleh kadar glukosa 15,22%.
3. Pada proses fermentasi dengan perbandingan 1:5 (berat per pelarut) dengan
waktu fermentasi 9 hari dan 7,5% Saccarhomyces diperoleh kadar bioethanol terbaik yaitu 6,14%.
4. Yield yang didapat pada proses fermentasi pada perbandingan 1:5 (berat per
pelarut) dengan waktu fermentasi 9 hari dan 7,5% Saccarhomyces diperoleh kadar yield terbaik yaitu 28,22%.
5.2. Saran
Pada proses hidrolisa pati menjadi glukosa menggunakan bacillus tidak begitu memberikan hasil yang baik sehingga disarankan proses hidrolisa sebaiknya menggunakan asam klorida.
Anonimous, http://id.wikipedia.org/wiki/Amilum. Anonimous, http://en.wikipedia.org/wiki/Ethanol_fuel. Anonimous, http://en.wikipedia.org/wiki/Bacillus.
Budiyanto dan Krisno Agus H., 2002, Mikrobiologi Dasar, Universitas Muhammadiyah Malang.
Groggins, P. H, 1958, Unit Process in Organic Synthetic Fifth edition, Mc Graw Hill, Kogakasha.
Teo Hudiko, 2009, Pabrik Ethanol Fuel Grade Dari Rumput Gajah, UPN "Veteran" Jawa Timur, Surabaya.
Kirk, R. E., Othmer D. F, 1952, Encyclopedia of Chemical Thecnology, 2rd ed., Volume 10, Van Nostrand Peinhold Company, New York.
PT. Bisi Internasional Tbk., 2010
Rahman dan Ansori, 1989, Pengantar Teknologi Fermentasi, Departemen Pendidikan dan Kebudayaan Direktorat Jendral Pendidikan Tinggi Pusat Antar Universitas Pangan dan Gizi IPB Bogor.
Sa’id, E. dan Gumbira, 1987, Penerapan Teknologi Fermentasi, PT. Melton Putra ,Jakarta.
Sa’id, E. dan Gumbira, 1989, Fermentor, IPB Bogor.
Sari, N. K., 2009, Purifikasi Pemurnian Bioethanol Dari Rumput Gajah Dengan Destilasi Batch, Jurnal Teknik Kimia Indonesia Vol. 8, No. 3, Fakultas Teknik Kimia ITB Bandung.
Tjokroadikoesoemo, P. dan Soebijanto, 1986, HFS dan Industri Ubi kayu Lainnya, PT. Gramedia Pustaka Utama, Jakarta.
Winarno, F.G., 1994, Kimia Pangan dan Gizi, PT. Gramedia Pustaka Utama, Jakarta.
1. Analisa menggunakan Spektrofotometer
Pestisida
Introduction to HPLC P.224/Prosedur Analisis - Mobile Fasa :
= (50:1000)*200=10 , Mengandung 10 gr jagung
% yield = (Total bioethanol : Berat bahan)* 100% = (2.757 gr:10)* 100 = 27.57%
3. Perhitungan bacillus subtilis
Gambar Limbah Saat Dilakukan Perendaman dan Setelah di Grinding :
Gambar Pada Proses Hidrolisa: