Pembuatan Model Transmisi dan Dinamika Persebaran
Virus H5N1 Sebagai Sistem Manajemen Bencana Endemik
Flu Burung
di Kabupaten Semarang Provinsi Jawa Tengah
Dengan Pedekatan Statistik
Suprihadi1
Rudy Latuperissa2
e-mail :[email protected],[email protected]
Diterima : 20 April 2012 / Disetujui: 14 Juni 2012
ABSTRACT
Issues Avian Influenza outbreak in Indonesia that attacks on animals is now a very serious issue, and has spread to 23 provinces. In this study aims to develop models ofthe dynamics of transmission and spread of H5N1 virus in a system of disaster management outbreaks of H5N1 disease, so that they can become important tools in disaster management policy of the plague. The method used in this study is the SIR model (Suceptible-Infectious-recovered). The model is constructed in three stages of research. The first licensing arrangements related to the Department. Second,secondary data research and development the third mathematical model. The results of this study is to model the dynamics of transmission and spread of H5N1 virus in acommunity population. The results are expected to be utilized as a framework fordisaster management system of disease outbreaks. Outcomes research in the form of a mathematical model and strategic policies for development in the future.
Keywords: SIR, transmission model, the dynamics of the spread, the H5N1
ABSTRAK
Isu Wabah Flu Burung di Indonesia bahwa serangan pada hewan sekarang menjadi masalah yang sangat serius, dan telah menyebar ke 23 provinsi. Dalam studi ini bertujuan untuk
1 . Program Studi Fakultas Teknologi InformasiUniversitas Kristen Satya Wacana
Jl. Diponegoro 52 – 60, Salatiga – 50711, Indonesia
2 . Program Studi Fakultas Teknologi InformasiUniversitas Kristen Satya Wacana
mengembangkan model tersebut yang dinamika penularan dan penyebaran virus H5N1 pada sebuah sistem manajemen bencana wabah penyakit H5N1, sehingga mereka dapat menjadi alat penting dalam kebijakan pengelolaan bencana wabah. Metode yang digunakan dalam penelitian ini adalah model SIR (Suceptible-Infeksi-sembuh). Model ini dibangun dalam tiga tahap penelitian. Pengaturan lisensi pertama terkait dengan Departemen. Kedua, data sekunder penelitian dan pengembangan model matematis ketiga. Hasil penelitian ini adalah untuk memodelkan dinamika penularan dan penyebaran virus H5N1 pada populasi acommunity. Hasilnya diharapkan dapat dimanfaatkan sebagai sistem manajemen fordisaster rangka wabah penyakit. Hasil penelitian dalam bentuk model matematika dan kebijakan strategis untuk pengembangan di masa depan.
Kata kunci: SIR, transmisi model, dinamika penyebaran tersebut, H5N1
Pendahuluan
Wabah avian influenza atau flu burung (yang disebabkan oleh virus subtipe H5N1) pertama kali terdeteksi pada unggas di Korea Selatan pada bulan Desember 2003. Di Indonesia wabah flu burung yang menyerang pada hewan saat ini sangat serius, dan telah menyebar ke 23 propinsi, meliputi 151 kabupaten/kota. Sampai dengan Desember 2004, jumlah kumulatif kasus kematian ternak unggas akibat flu burung mencapai lebih dari 8 juta ekor. Penularan pada manusia telah dilaporkan sebanyak 241 kasus infeksi dan 141 diantaranya telah meninggal dunia sejak bulan Agustus 2006. Antara tahun 2006 sampai tahun 2008 Indonesia secara global merupakan negara yang paling parah terkena wabah virus H5N1 dengan jumlah kasus 137 dan jumlah penderita meninggal sebanyak 112 orang. Kerugian jangka pendek pandemi flu burung di Indonesia diperkirakan sebesar 14–48 triliun rupiah [1]. Penyebaran flu burung yang semakin meluas wilayahnya disebabkan oleh tidak terkontrolnya pergerakan unggas yang terinfeksi flu burung, produk hasil unggas dan limbahnya, tenaga kerja serta kendaraan pengangkut dari wilayah terinfeksi ke wilayah yang masih bebas, serta rendahnya kapasitas kelembagaan kesehatan hewan dan tenaga kesehatan hewan yang terlatih.
Secara kuantitas, individu yang telah terinfeksi dapat disimulasikan secara grafis menggunakan data sensus, data pola perubahan tata guna lahan dan data mobilitas penduduk. Model matematis dan analisis statistik dalam epidemiologi difokuskan untuk membuat prediksi faktor–faktor yang menjadi parameter terhadap transmisi penyakit dalam populasi (vektor maupun manusia)[9]. Model matematis persebaran penyakit yang memiliki validitas dan akurasi tinggi merupakan konsep dasar untuk memahami dampak penyakit dan menyusun strategi pengendaliannya. Dalam perumusan strategi pengendalian, model harus sudah memiliki parameter kunci seperti struktur sosiodemografi dalam populasi, konektivitas individu dalam populasi dan struktur geografi dimana populasi berada [3].
dapat dilakukan menggunakan aplikasi komputasi seperti Matlab dan R. SIR telah diterapkan untuk menganalisis kejadian demam berdarah dengue Kota Salatiga tahun 2000 – 2008 menggunakan Package Amei pada lingkungan pemrograman R [16].
Penelitian tentang H5N1 yang pernah dilakukan adalah pembangunan model kontrol endemik H5N1 dengan tujuan untuk menentukan target vaksinasi dan model surveillans yang dikembangkan [18].Penelitian sejenis lain adalah analisis statistika model transmisi virus H5N1 dan menghasilkan pola spasial endemik serta potensi distribusi penyakit di wilayah sekitarnya[4]. Penelitian yang berjudul “ Pembuatan Model Transmisi dan Dinamika Persebaran Virus H5N1 Sebagai Sistem Manajemen Bencana Endemik Flu Burung di Kabupaten Semarang” ini bertujuan untuk merancang, membangun dan menerapkan model spasial statistik pola transmisi dan persebaran virus H5N1 serta mengembangkan sebagai perangkat penting dalam kebijakan manajemen bencana wabah penyakit.
Pengembangan Metode Analisis menggunakan SuceptibleInfectious Recovered (SIR)
Terdapat berbagai tipe formulasi penyusun model (compartments), pemilihan penggunaan formulasi pembangun model berdasarkan pada karakteristik khusus penyakit yang akan dimodelkan dan tujuan pemodelan. Beberapa pola compartments yang sering digunakan adalah MSEIR, MSEIRS, SEIR, SEIRS, SIR, SIRS, SEI, SEIS, SI, and SIS [19]. Pemodelan persebaran penyakit dalam suatu populasi tertentu, bersifat epidemis dan disebabkan oleh virus dimodelkan menggunakan Suceptible Infectious Recovered (SIR)[21]. SIR adalah klasifikasi populasi berdasarkan pada derajad kerentanan terhadap penyakit dan mekanisme proses transmisi peyakit pada manusia. Ada tiga klasifikasi, kelompok populasi yang potensial/beresiko tertular (Susceptible), kelompok populasi yang telah terinfeksi/ penyebaran penyakit (Infectious) dan kelompok populasi yang telah mengalami penyembuhan (Removed/Recovered) sebagai akibat mekanisme sistem imun, atau proses karantina atau mengalami kematian [20]. Kelompok populasi pada vektor nyamuk terdiri dari dua klasifikasi, yaitu kelompok populasi yang potensial/beresiko menular (Susceptible) dan kelompok populasi terinfeksi/penyebaran penyakit (Infectious). Beberapa asumsi dasar model SIR adalah sebagai berikut :
1. Populasi bersifat tertutup, tidak ada kelahiran, kematian dan migrasi yang terepresentasi dalam model.
2. Populasi bersifat homogen dan acak, probabilitas kontak antar dua individual tidak hanya ditentukan oleh dua individu tersebut, dengan demikian memiliki karakteristik kontak yang sama dengan individu lainnya.
3. Populasi/penduduk suatu daerah diinisialisasi sebagai
N
−
m
, adanya individu yang telah terinfeksi pada suatu populasi/penduduk yang potensial/beresiko tertular.4. Proses penularan terjadi jika terjadi kontak antara kelompok individu yang potensial/ beresiko menular (Susceptible) dan kelompok populasi terinfeksi/penyebaran penyakit (Infectious).
N
β
yang mana
β
adalah rerata kontak atau rerata terinfeksi pada suatu populasi/pendudukN
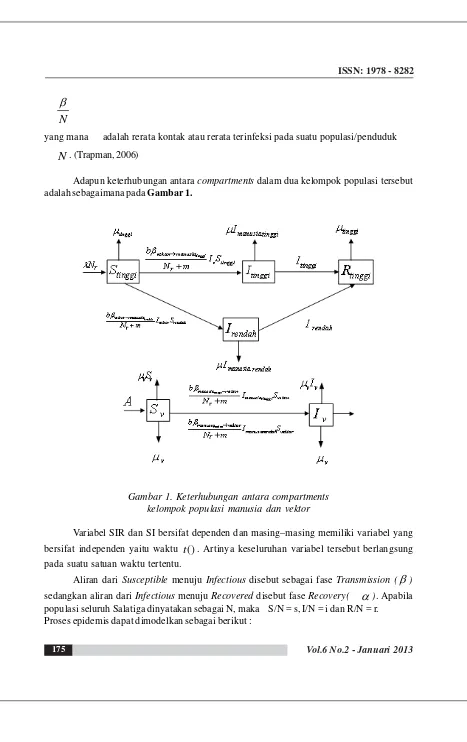
. (Trapman, 2006) [image:4.595.69.536.60.802.2]Adapun keterhubungan antara compartments dalam dua kelompok populasi tersebut adalah sebagaimana pada Gambar 1.
Gambar 1. Keterhubungan antara compartments kelompok populasi manusia dan vektor
Variabel SIR dan SI bersifat dependen dan masing–masing memiliki variabel yang
bersifat independen yaitu waktu
t
()
. Artinya keseluruhan variabel tersebut berlangsung pada suatu satuan waktu tertentu.Aliran dari Susceptible menuju Infectious disebut sebagai fase Transmission (
β
) sedangkan aliran dari Infectious menuju Recovered disebut fase Recovery(α
). Apabila populasi seluruh Salatiga dinyatakan sebagai N, maka S/N = s, I/N = i dan R/N = r.
i
dt
dr
i
si
dt
di
si
dt
ds
α
α
β
β
=
−
=
−
=
(persamaan 1)dimana,
β
adalah rerata transmisi penyakit melalui rerata kontak,α
adalah proses recovery, penyembuhan melalui imun, atau kematian yang tidak berpengaruh terhadap proses transmisi penyakit.
Sesuai dengan persamaan dasar pada persamaan 1 maka dinamika transmisi penyakit pada manusia dapat diuraikan sebagai berikut :
manusia hmanusia manusia manusia hrendah hmanusia manusia vektor T manusia vektor rendah manusia manusia manusia Vektor T htinggi vektor tinggi manusia V T manusia vektor V T manusia vektor mausia T manusia
R
I
I
r
dt
dr
I
r
s
I
m
N
b
dt
di
I
r
s
I
m
N
b
dt
di
s
I
m
N
b
I
m
N
b
N
dt
ds
rendah tinggi rendah tinggi rendah tinggiµ
µ
β
µ
β
β
β
µ
λ
−
+
=
+
−
+
=
+
−
+
=
+
+
+
+
−
=
→ → → →)
(
)
(
)
(
)
(
(persamaan 2)Dinamika transmisi penyakit pada vektor dapat diuraikan sebagai berikut :
vektor vektor manusia manusia T vektor manusia tinggi T vektor manusia vektor hmanusia manusia T vektor manusia tinggi T vektor manusia v manusia
I
s
I
m
N
b
I
m
N
b
dt
di
s
I
m
N
b
I
m
N
b
A
dt
ds
rendah rendah tinggi rendah rendah tinggiµ
β
β
β
β
µ
−
+
+
+
=
+
+
+
+
−
=
→ → → →)
)
(
(persamaan 3) Dimana, Ttinggi
S
adalah jumlah populasi manusia/penduduk yang beresiko tinggi tertular (Susceptible)tinggi
I
adalah jumlah populasi manusia/penduduk yang terinfeksi endemis tinggirendah
I
adalah jumlah populasi manusia/penduduk yang terinfeksi endemis rendahtinggi
R
adalah jumlah populasi manusia/penduduk yang mengalami penyembuhantinggi manusia vektor
b
β
→ adalah peluang terjadinya transmisi virus dari vektor ke manusia dalamendemis tinggi
rendah manusia vektor
b
β
→ adalah peluang terjadinya transmisi virus dari vektor ke manusia dalam endemis rendahm
N
T−
adalah individu yang telah terinfeksi pada suatu populasi/penduduk yang potensial/beresiko tertulartinggi manusia
I
µ
peluang terjadinya kematian sebagai akibat terinfeksi pada suatu populasi/ penduduktinggi
µ
peluang terjadinya kematian pada masa penyembuhanvektor manusiatinggi
b
β
→ adalah peluang terjadinya transmisi virus dari manusia ke vektor dalamendemis tinggi
vektor manusiarendah
b
β
→ adalah peluang terjadinya transmisi virus dari manusia ke vektor dalam endemis rendahvektor tinggi manusia
S
I
adalah peluang terjadinya infeksi pada manusia dalam endemis tinggiyang berasal dari vektor yang beresiko tinggi tertular.
vektor rendah manusia
S
I
adalah peluang terjadinya infeksi pada manusia dalam endemis rendah yang berasal dari vektor yang beresiko tinggi tertular.v
S
adalah jumlah populasi vektor yang beresiko menularkan penyakit (Susceptible)v
I
adalah jumlah populasi vektor yang beresiko terinfeksi penyakit (Infected)v
µ
peluang terjadinya kematian vektor.Metode Penelitian
G
ambar 2.Tahapan pengembangan sistem peringatan dini langkah 1 - 3Langkah ke 1
Langkah ke 1 adalah kegiatan pengurusan perijinan penelitian dilokasi penelitian yang meliputi :
1. Dinas Kesehatan Kabupaten Semarang. 2. Kesbangpolinmas Kabupaten semarang. 3. Dinas Peternakan Kabupaten semarang. 4. Bappeda Kabupaten Semarang.
Langkah ke 2
Langkah ke 2 adalah inventarisasi data primer dan sekunder. Metode yang digunakan adalah :
1. Inventarisasi data primer menggunakan wawancara dan kuosiner.
Wawancara dilakukan pada kelompok masyarakat yang telah dinyatakan sembuh oleh rumah sakit dari suspect H5N1. Kuesioner diberikan pada kelompok masyarakat yang selama ini bekerja pada sektor peternakan unggas.
2. Diskusi kelompok terfokus (Focus Group Discussion).
3. Mengkaji data sekunder (Secondary Data Review) yang meliputi :
a. Data Sosial dan Kependudukan
b. Data klimatologi
c. Data penyelidikan epidemiologi (PE)
Langkah ke 3
1. Penetapan parameter kunci KLB dengan metode FGD dan SDR.
Parameter kunci ditetapkan setelah dilakukan proses inventarisasi dan analisis data yang diperoleh dari langkah ke 2. Analisis data dilakukan untuk mengetahui sejauh mana keterhubungan antara parameter dengan kasus H5N1.
2. Penetapan metode analisis. Metode analisis yang digunakan dalam penelitian ini adalah sebagai beriku :
a. Asosiasi antar parameter ditentukan menggunakan persamaan Moran’s dan Geary dan tool OpenGeoda.
b. Pola transmisi penyakit ditentukan menggunakan Package Amei dalam lingkungan pemorgraman R.
Hasil Pengolahan Data
Berdasarkan hasil pengolahan data yang diperoleh dari wawancara, penyebaran kuisioner, dan ditambah dengan pelaksanaan Forum Group Discussion (FGD), didapatkan gambaran informasi sebagai berikut :
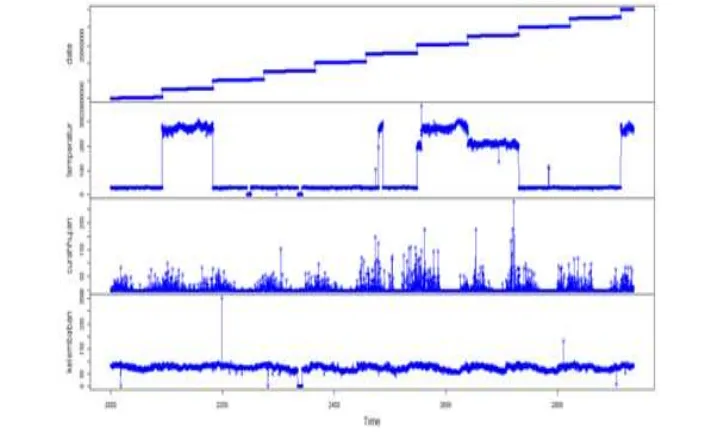
[image:8.595.118.477.401.620.2]Berdasarkan data klimatologi didapatkan data curah hujan, temperatur dan kelembaban yang terjadi sepanjang tahun 2001-2010, sebagaimana seperti grafik yang diperlihatkan pada Gambar 3.
Gambar 3. Data curah hujan, kelembaban, dan temperature sepanjang tahun 2001-2010
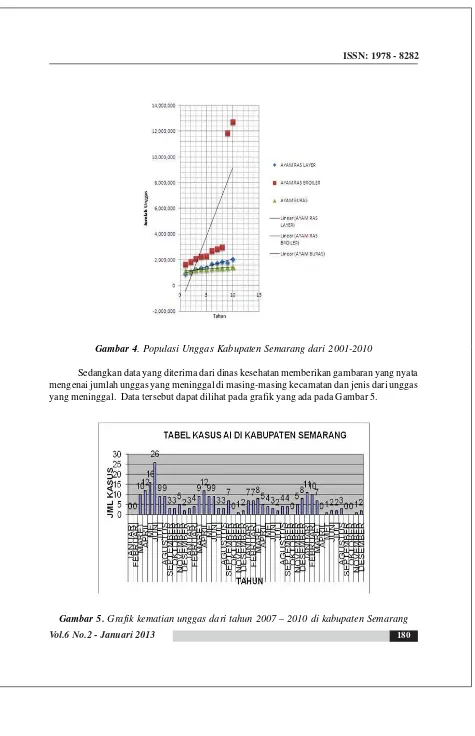
Gambar 4. Populasi Unggas Kabupaten Semarang dari 2001-2010
Sedangkan data yang diterima dari dinas kesehatan memberikan gambaran yang nyata mengenai jumlah unggas yang meninggal di masing-masing kecamatan dan jenis dari unggas yang meninggal. Data tersebut dapat dilihat pada grafik yang ada pada Gambar 5.
Analisis Dan Pembahasan
[image:10.595.187.404.372.572.2]Untuk membuat pemodelan SIR diperlukan data rerata transmisi virus(b), rerata penyembuhan (v), rerata kematian (µ) (dalam SIR dibuat asumsi nol) dan tingkat pencampuran populasi individu terinfeksi (k) [8]. Parameter biaya (cost) vaksinasi dihitung sebagai biaya vaksinasi tunggal dan perawatan individual. Dalam penelitian ini biaya vaksinasi diasumsikan nol (dengan pemikiran bahwa sebelum terjangkit, setiap individu belum mendapatkan vaksin dari Puskesmas setempat). Untuk melakukan simulasi jumlah populasi yang terjangkit, dan tingkat individu yang berada dalam Suspected, Infected dan Recovery dalam skala eksperimen maka digunakan fungsi Mcepi (Monte Carlo Epidemics). Parameter costs merupakan biaya untuk indikator vaksinasi, kematian dan terinfeksi. Pada penelitian ini diasumsikan tidak ada biaya yang dikeluarkan sehingga bernilai nol. Artinya jumlah yang divaksinasi, jumlah yang meninggal dan jumlah terinfeksi tidak ada biaya. Untuk melakukan simulasi strategi jumlah biaya vaksinasi terendah digunakan fungsi optvac yang bekerja secara stokastik epidemis, dapat dilihat pada gambar 6.
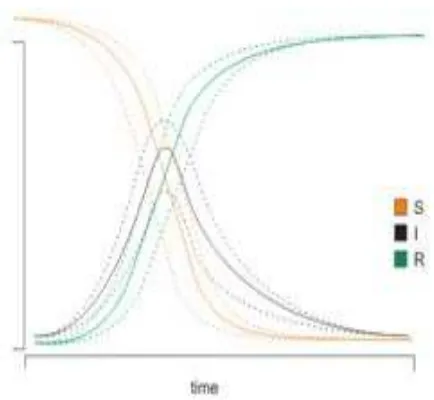
Gambar 6. Model SIR Pada Jumlah Penderita Infeksi Flu Burung Kabupaten Semarang Tahun 2000 – 2008
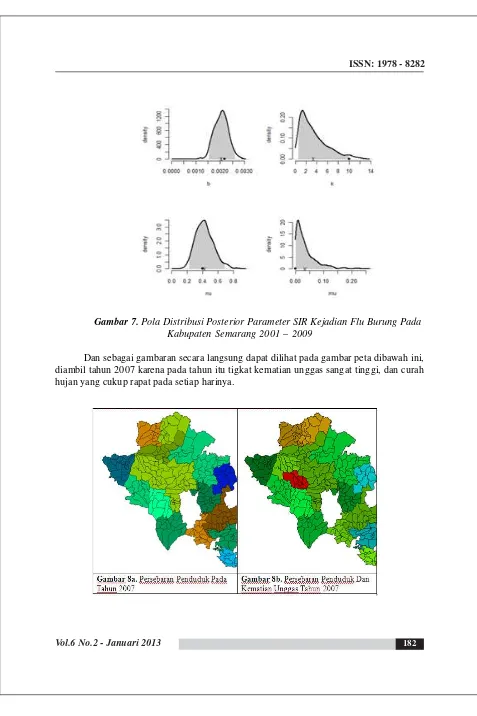
Gambar 7. Pola Distribusi Posterior Parameter SIR Kejadian Flu Burung Pada Kabupaten Semarang 2001 – 2009
Kesimpulan
Package Amei efektif diterapkan sebagai tool untuk pemodelan optimasi epidemiologi pada kejadian epidemis demam flu burung di kabupaten Semarang pada tahun 2000 sampai dengan 2008. Dengan perangkat ini dapat dilakukan analisis perbandingan pola penurunan jumlah individu yang berada dalam Suspected Infected dan Recovery secara lebih signifikan sebagai dampak proses vaksinasi. Pola distribusi posterior parameter
SIR
kejadian flu burung di kabupaten Semarang dapat dianalisis melalui parameter
rerata transmisi, parameter dispersi, rerata mortalitas dan rerata penyembuhan.
Nilai setiap parameter, nilai tengah posterior, dan wilayah distribusi posterior
sebesar 95%
DAFTAR PUSTAKA
[1] Asmara Widya, 2007, Peran Biologi Molekuler dalam Pengendalian Avian Influenza dan Flu Burung, Pidato Pengukuhan Guru Besar FKH – UGM,Yogyakarta.
[2] Atchade, Yves ; Gersende, Fort ; Moulines, Eric ; Priouret, Pierre, 199 . Adaptive Markov Chain Monte Carlo: Theory and Methods, University of Michigan, 1085 South University, Ann Arbor, 48109, MI, United States.
http://www.stat.lsa.umich.edu/~yvesa/afmp.pdf
[3] Barthelemy, Marc ; Barrat, Alain ; Pastor-Satorras, Romualdo ; Vespignani, Alessandro, 2005, Dynamical patterns of epidemic outbreaks in complex heterogeneous networks, Journal of Theoretical Biology 235 (2005) 275–288, School of Informatics and Biocomplexity Center, Indiana University, Bloomington, IN 47408, USA.
www.cc.gatech.edu/classes/AY2010/cs8803ns_fall/barthelemy.pdf,
[4] Eubank, Stephen ; Hasan, Guclu, S.; Kumar, Anil ; Marathe, Madhav V. ; Srinivasan, Aravind ; Toroczkai, Zolta ; Wang, Nan, 2008. Modelling disease outbreaks in realistic urban social networks, Basic and Applied Simulation Science Group, Los Alamos National Laboratory, MS M997, Los Alamos, New Mexico 87545, USA ndssl.vbi.vt.edu/Publications/modellingDisease.pdf.
[5] Harvey Neil, Aaron Reeves, Mark A. Schoenbaumc, Francisco J. Zagmutt-Vergara, Caroline Dube, Ashley E. Hill, Barbara A. Corso, W. Bruce McNab, Claudia I. Cartwright dan Mo D. Salman, 2007, The North American Animal Disease Spread Model: A simulation model to assist decision making in evaluating animal disease incursions, Preventive Veterinary Medicine 82 (2007) 176–197, USA
www.ncbi.nlm.nih.gov/pubmed/17614148.
[7] Karandikar Rajeeva, 2006. On the Markov Chain Monte Carlo (MCMC) method, Indian Statistical Institute, Sadhana Vol. 31, Part 2, April 2006, pp. 81–104. www.ias.ac.in/sadhana/Pdf2006Apr/81.pdf
[8] Keeling Matt dan Ken T.D Eames, 2005, Networks And Epidemic Models, Department of Biological Sciences & Mathematics Institute, University of Warwick, Gibbet Hill Road, Coventry CV4 7AL, UK. http://ukpmc.ac.uk/ articlerender.cgi?artid=1259156.
[9] Maiti A, S. Pathak dan Samanta G.P., 2004, Rich dynamics of an SIR epidemic model, Nonlinear Analysis: Modelling and Control, 2010, Vol. 15, No. 1, 71–81, Department of Mathematics, Presidency College, Kolkata-700073, India, http:// www.lana.lt/journal/36/Pathak.pdf.
[10] Merl Daniel, Leah R. Johnson, Robert B. Gramacy dan Marc S. Mangel, 2009. Amei: an R package for the Adaptive Management of Epidemiological Interventions, Department of Statistical Science, Duke University, Durham NC. cran.r-project.org/web/pa ck ag es /am ei /vignettes /am ei .pdp
[11] Pang Wan-Kai, Shui Hung Hou, Marvin D.Trout, Wing-Tong Yu, Ken W, 2007, A Markov Chain Monte Carlo Approach to Estimate the Risks of Extremely Large Insurance Claims, International Journal of Business and Economics, 2007, Vol. 6, No. 3, 225-236, Department of Applied Mathematics, The Hong Kong Polytechnic University, Hong Kong
http://www.ijbe.org/table%20of%20content/pdf/vol6-3/vol.6-3-04.pdf
[12] Skvortsov, Connell, Dawson dan Gailis, 2007, Epidemic Modelling: Validation of Agent-based Simulation by Using Simple Mathematical Models, Defence Science and Technology Organisation, PO Box 4331, Melbourne, VIC, 3001,
h t t p : / / m s s a n z . o r g . a u / M O D S I M 0 7 / p a p e r s / 1 3 _ s 2 0 / EpidemicModeling_s20_Skvortsov_.pdf.
[13] Soetaert Karline dan Thomas Petzoldt, 2010, Inverse Modelling, Sensitivity and Monte Carlo Analysis in R Using Package FME, Netherlands Institute of Ecology. Netherland cran.r-Project.org/web/packages/FME/vignettes/FMEother.pdf,
[14] Yulianto Sri, Kasmiyati, Kristoko D.H.,Maria Marina H., 2009, Pengurangan Potensi Bencana Epidemi, Wabah Dan KLB Beberapa Penyakit Tropis Melalui Penerapan Paradigma Pengurangan Resiko Yang Diintegrasikan Dengan Kurikulum Pembelajaran Pada Sistem Manajemen Bencana, Laporan Akhir Hibah Strategis Nasional Batch IV, Tahun ke 1,Universitas Kristen Satya Wacana Salatiga.
Central Java, Indonesia, International Conference on Soft Computing, Intelligent System and Information Technology, Petra Christian University Surabaya.
[16] Yulianto S. dan Subanar, 2010, Pemodelan SIR (Suspect Infected Recovery) Kejadian Demam Berdarah Dengue Kota Salatiga Tahun 2000 – 2008 Menggunakan Package Amei pada R, Belum dipublikasikan.
[17] Zaman Gul, Yong Han Kang dan Il Hyo Jung, 2007, Optimal vaccination and treatment in the SIR epidemic model, Department of Mathematics, Pusan National University, Busan 609-735, Korea.
www.ksiam.org/conference/annual072/upfile/Optimal%2 0SIR.pdf.
[18] Guan dkk, 2007, A model to control the epidemic of H5N1 influenza at the source, BMC Infectious Diseases 2007, 7:132, State Key Laboratory of Emerging Infectious Diseases, the University of Hong Kong, Pokfulam, Hong Kong SAR, China
[19] Hetchote Herbert, 2000, The Mathematics of Infectious Diseases, Department of Mathematics, University of Iowa, Iowa City. www.math.uiowa.edu/~hethcote/PDFs/ 2000SiamRev.pdf
[20] Regoes Roland, 2009. Stochastic simulation of epidemics, Institute of Integrative Biology