I. PENDAHULUAN A. Latar Belakang
Termodinamika berasal dari bahasa Yunani, thermos = panas dan dynamic = 'perubahan adalah fisika energi, panas, kerja,entropi dan kespontanan proses. Termodinamika berhubungan dekat dengan mekanika statistik di mana banyak hubungan termodinamika berasal.
Pengolahan tekanan tinggi atau lebih dikenal dengan istilah High Pressure Processing (HPP) adalah metode pengolahan makanan dimana makanan
mengalami tekanan tinggi (hingga 600 Mpa, atau 87.000 pound per inch persegi (psi) atau sekitar 6.000 atmosfer) dengan atau tanpa penambahan panas untuk inaktivasi mikroba atau untuk mengubah atribut pangan untuk mendapatkan kualitas yang diinginkan konsumen. Tekanan diberikan pada waktu tertentu biasanya sekitar 3-5 menit.
Hukum II Termodinamika, dengan pernyataan: “kalor mengalir secara alami
dari benda yang panas ke benda yang dingin, kalor tidak akan mengalir secara spontan dari benda dingin ke benda panas”.
Hukum II Termodinamika berpusat pada masalah entropi. Hukum kedua termodinamika bisa dinyatakan sebagai berikut: “Entropi dapat diciptakan tetapi tidak dapat dimusnahkan.” Berdasarkan postulat ini, entropi yang ada pada sebuah proses bisa tetap tidak berubah dan bisa pula naik, namun tidak mungkin berkurang. Entropi hanya bisa tetap tidak berubah pada sebuah proses reversible (s1 = s2).
1. Praktikan dapat memahami sistem terisolasi sesuai Hukum Termodinamika ke-2
2. Praktikan dapat memahami aplikasi sistem terisolasi pada kehidupan sehari hari
II. TINJAUAN PUSTAKA
Definisi gas yaitu suatu keadaan zat dalam ini molekul-molekulnya dapat bergerak sangat bebas, dan dapat mengisi seluruh ruangan yang ditempatinya. Gas adalah suatu fase benda. Seperti cairan, gas mempunyai kemampuan untuk mengalir dan dapat berubah bentuk. Namun berbeda dari cairan, gas yang tak tertahan tidak mengisi suatu volume yang telah ditentukan, sebaliknya mereka mengembang dan mengisi ruang apapun di mana mereka berada. Tenaga gerak/energi kinetis dalam suatu gas adalah bentuk zat terhebat kedua (setelah plasma). Karena penambahan energi kinetis ini, atom-atom gas dan molekul sering memantul antara satu sama lain, apalagi jika energi kinetis ini semakin bertambah (Samuel dkk, 1992).
Gas adalah zat yang selalu dapat bercampur sempurna satu sama lain membentuk satu fase yang homogen. Jika dicampurkan gas-gas O2, N2, dan CO2 di dalam ruang tertutup, maka akan diperoleh suatu campuran yang homogen, karena tidak terdapat perbedaan secara fisik gas satu dengan yang lain. Secara umum gas dapat dikelompokkan menjadi dua macam golongan, yaitu gas ideal atau gas sempurna dan gas real/nyata atau sejati.
Gas adalah uap secara alami berkaitan dengan pangan dan sistem pengolahan pangan. Diantaranya adalah penggunaan uap air (steam) sebagai media pemanasan, dimana diperlukan pengetahuan tentang sifat-sifat gas tersebut. Demikian juga dalam proses evaporasi atau penguapan air dari bahan pangan akan terjadi perubahan fase dari air menjadi uap, dimana sifat-sifat dari cair dan fase uap akan berbeda.
Sifat-sifat gas dapat dirangkumkan sebagai berikut: 1. Gas bersifat transparan
3. Gas dalam ruang akan memberikan tekanan ke dinding
4. Volume sejumlah gas sama dengan volume wadahnya. Bila gas tidak diwadahi, volume gas akan menjadi tak hingga besarnya, dan tekanannya akan menjadi tak hingga kecilnya
5. Gas berdifusi ke segala arah tidak peduli ada atau tidak tekanan luar 6. Bila dua atau lebih gas bercampur, gas-gas itu akan terdistribusi merata 7. Gas dapat ditekan dengan tekanan luar. Bila tekanan luar dikurangi, gas akan
mengembang
8. Bila dipanaskan gas akan mengembang, bila didinginkan akan mengkerut. Teori kinetik zat membicarakan sifat zat dipandang dari sudut momentum. Peninjauan teori ini bukan pada kelakuan sebuah partikel, tetapi diutamakan pada sifat zat secara keseluruhan sebagai hasil rata-rata kelakuan partikel-partikel zat tersebut.
Sifat gas umum sebagai berikut:
1. Gas mudah berubah bentuk dan volumenya
2. Gas dapat digolongkan sebagai fluida, hanya kerapatannya jauh lebih kecil. Kondisi gas ditentukan oleh tiga faktor yaitu : tekanan, suhu dan volume. Gas ideal adalah keadaan gas yang dianggap sempurna, memiliki sifat tertentu sehingga dapat diterapkan pada teori kinetik gas.
Anggapan gas ideal harus memenuhi syarat sebagai berikut:
1. Jumlah partikel gas banyak sekali tetapi tidak ada gaya tarik menarik antar partikel
2. Semua partikel bergerak dengan acak
3. Ukuran gas sangat kecil bila dibanding dengan ukuran wadah, jadi ukuran gas diabaikan
5. Partikel gas terdistribusi merata pada seluruh ruang dalam wadah 6. Partikel gas memenuhi Hukum Newton tentang gerak
Dalam fisika, dikenal 3 macam sistem terkait dengan gas sebagai berikut:
1. Sistem Terbuka; ada pertukaran massa dan energi sistem dengan lingkungannya. Contoh: lautan, tumbuh-tumbuhan.
2. Sistem Tertutup; ada pertukaran energi tetapi tidak terjadi pertukaran massa sistem dengan lingkungannya. Contoh: Green house ada pertukaran kalor tetapi tidak terjadi pertukaran kerja dengan lingkungan.
3. Sistem Terisolasi; tidak ada pertukaran massa dan energi sistem dengan lingkungan. Contoh: tabung gas yang terisolasi (Tim Asisten, 2016).
Hukum II Termodinamika berpusat pada masalah entropi. Hukum kedua termodinamika bisa dinyatakan sebagai berikut: “Entropi dapat diciptakan tetapi tidak dapat dimusnahkan.” Berdasarkan postulat ini, entropi yang ada pada sebuah proses bisa tetap tidak berubah dan bisa pula naik, namun tidak mungkin berkurang. Entropi hanya bisa tetap tidak berubah pada sebuah proses reversible (s1 = s2).
besar pula titik didih zat cair tersebut. Pada tekanan dan temperatur udara standar (76 cmHg, 25ºC) titik didih air sebesar 100ºC (Anonim, 2011).
Artinya pelarut murni akan mendidih bila tekanan uap jenuh pada permukaan cairan sama dengan tekanan udara luar. Pada sistem terbuka, tekanan udara luar adalah 760 mmHg (tekanan udara pada permukaan larutan) dan suhu pada tekanan udara luar 760 mmHg disebut titik didih normal. Titik didih suatu cairan adalah suhu pada saat tekanan uap jenuh cairan itu sama dengan tekanan luar (tekanan yang diberikan pada permukaan cairan). Dari definisi ini kita ketahui bahwa titik didih cairan bergantung pada tekanan udara pada permukaan cairan. Itulah sebabnya, titik didih air di gunung berbeda dengan di pantai. Pada saat tekanan uap sama dengan tekanan udara luar maka gelembung-gelembung uap dalam cairan bergerak ke permukaan dan masuk fase gas (Tahang, 2011).
Sumber : Internet
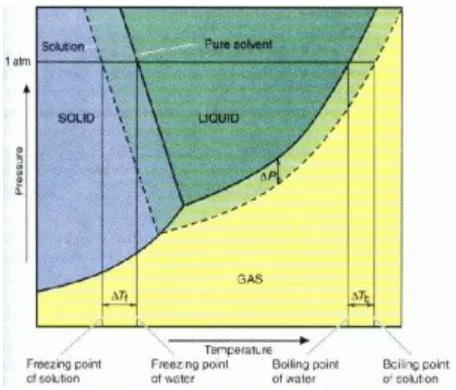
Tr = titik tripel, yaitu titik keseimbangan antara ketiga wujud padat-cair-gas. K = titik kritis, yaitu titik dimana gas di atas tekanan dan temperatur kritis tidak dapat dicairkan hanya dengan mengecilkan volumenya, gasnya berwujud stabil.
Garis AB adalah garis didih air, artinya setiap titik pada garis AB terdapat kesetimbangan antara cair dan gas. Garis AC adalah garis beku air artinya setiap titik pada garis AC terdapat kesetimbangan antara padat dan cair. Titik R disebut titik tripel air, artinya pada titik R itu tercapai kesetimbangan antara cair, padat dan gas. Titik tripel itu adalah 0,0099°C dan tekanan 0,0060 atm. Karena tekanan uap jenuh larutan lebih rendah daripada tekanan uap jenuh pelarut maka garis DE, yaitu garis didih larutan berada di bawah garis AB. Pada tekanan luar 1 atm, air mendidih pada suhu 100oC (titik B). Pada saat itu tekanan uap air juga 1 atm dan tekanan uap larutan masih di bawah 1 atm (titik L). jadi, agar larutan mendidih, perlu suhu diperbesar sehingga titik L pindah ke titik E’. Pada titik E, tekanan uap jenuh larutan sudah mencapai 1 atm (sama dengan tekanan udara luar). Jadi, pada titik E larutan mendidih dan suhu didihnya titik E’. Selisih titik didih larutan dengan titik didih pelarut disebut kenaikan titik didih (tb = boiling point).
tb = titik didih larutan – titik didih pelarut
titik beku pelarut dengan titik beku larutan disebut penurunan titik beku ( tf = freezing point) (Daryanto, 2003).
tf = titik beku pelarut – titik beku larutan Dari diagram P-T dapat disimpulkan bahwa :
1. Penambahan tekanan menaikkan titik didih dan titik lebur zat
2. Di atas titik tripel tidak mungkin merubah wujud zat dari padat langsung ke gas
3. Di atas titik kritis gas tidak dapat diembunkan tanpa menurunkan tekanannya.
III. METODOLOGI A. Alat dan Bahan 1. Panci presto
2. Air
3. Termometer raksa 4. Termokopel 5. Hybrid recorder 6. Stopwatch 7. Alat tulis
2. Panci presto diisi dengan air setengah penuh dan dipanaskan, suhu awal air dan setelah mendidih diukur, serta nyalakan stopwatch
3. Panci diisi kembali dengan air baru dan dipanaskan dengan kondisi ditutup dan suhu awal air dan suhu setelah mendidih diukur, serta durasinya dihitung dengan stopwatch
4. Hitung dengan rumus termodinamika dengan estimasi volume awal dan akhir tetap:
P1 = Tekanan Mendidih 1 P2 = Tekanan Mendidih 2 T1 = Suhu Mendidih1 T2 = Suhu Mendidih2
5. Massa 1 uap saat mendidih 1 dan massa uap 2 saat mendidih 2 (vacum) dihitung dengan rumus:
Tabel 1. High Pressure N
Tabel 2. Volume No Volume Spesifik
Uap V uap1 m uap1 V uap2
IV. HASIL DAN PEMBAHASAN
T1 (awal) = 29,5ºC (kondisi vakum) T2 (akhir) = 100,7ºC (kondisi vakum) P1 (awal) = 100 kPa
T1 (awal) = 30ºC (kondisi non vakum) T1 (akhir) = 100ºC (kondisi non vakum) t (vakum) = 191 detik 1) Mencari volume spesifik (P diketahui = 0,341 mPa)
0,3−0,341 2) Mencari volume uap
Volume uap air = volume panci – volume air = (4x10-3) – (0,5x10-3) = 3,5x10-3 m3
3) Mencari massa uap
Massa uap = volume uap volume spesifik
= 3,5x10−3 0,00107751 = 3,25 kg b. Kondisi non vakum
P1 1) Mencari volume spesifik (P diketahui = 0,341 mPa)
0,3−0,334 0,3−0,4 =
0,001073−x −0,001073−0,001084 −0,034
−0,1 =
0,001073 – x = -0,00000374 x = 0,00107674 m3/kg 2) Mencari volume uap
Volume uap air = volume panci – volume air = (4x10-3) – (0,5x10-3) = 3,5x10-3 m3
3) Mencari massa uap
Massa uap = volume uap
T1 (awal) = 32ºC (kondisi vakum) T2 (akhir) = 94ºC (kondisi vakum) P1 (awal) = 100 kPa
T1 (awal) = 31ºC (kondisi non vakum) T1 (akhir) = 98,3ºC (kondisi non vakum) t (vakum) = 421 detik 1) Mencari volume spesifik (P diketahui = 0,294 mPa)
0,2−0,294 2) Mencari volume uap
Volume uap air = volume panci – volume air = (8x10-3) – (0,7x10-3) = 7,3x10-3 m3
3) Mencari massa uap
Massa uap = volume uap volume spesifik
P1 P2
= T1 T2
P2 = 10030 x 100 = 333,34 kPa = 0,334 mPa 1) Mencari volume spesifik (P diketahui = 0,341 mPa)
0,3−0,317 0,3−0,4 =
0,001073−x −0,001073−0,001084 −0,017 2) Mencari volume uap
Volume uap air = volume panci – volume air = (8x10-3) – (0,7x10-3) = 7,3x10-3 m3
3) Mencari massa uap
Massa uap = volume spesifikvolume uap
= 7,3x10−3 0,00107487 = 6,79 kg Tabel 3. Pengamatan
N
o T didih (ºC) P2 didih (ºC) Keterangan Durasi (s)
1 100,7 341,35 Vakum 191
2 10 333,34 Non vakum 194
3 94 293,75 Vakum 421
4 98,3 317,09 Non vakum 542
Tabel 4. Hasil data perhitungan N
o
Volume spesifik
(m3/kg) Volume uap(m3) Massa uap(kg) Keterangan
1 0,00107751 3,5x10-3 3,25 Vakum
2 0,00107674 3,5x10-3 3,26 Non Vakum
3 0,00107228 3,5x10-3 6,81 Vakum
4 0,00107487 3,5x10-3 6,79 Non Vakum
Sumber : Internet
Gambar 2. Gelas ukur Fungsi bagian :
a. Gagang gelas, berfungsi sebagai pegangan gelas ukur b. Skala, berfungsi untuk ukuran volume
c. Tabung, berfungsi untuk menampung benda atau cairan yang ingin diukur volumenya
Sumber : Internet
Gambar 3. Kompor gas Fungsi bagian :
a. Lubang selang gas, berfungsi sebagai lubang selang gas b. Burner, berfungsi sebagai sumbu kompor
b
c
a
b a
c. Kerangka kompor gas, berfungsi sebagai kerangka/pelindung bagian dalam kompor
d. Tungku, berfungsi sebagai dudukan dari wajan/pamci
e. Pemantik gas, berfungsi untuk menyalakan api gas/membesar kecilkan api
Sumber : Laboratorium TP Gambar 4. Termometer raksa Fungsi bagian :
a. Skala, berfungsi untuk mengukur suhunya
b. Tabung kaca, berfungsi sebagai pelindung bagian dalam termometer c. Perak, berfungsi sebagai sensitivitas
Sumber : Laboratorium TP c
b a
b
h
c g
f e
Gambar 5. Termokopel dan Hybrid Recorder Fungsi bagian termokopel dan hybrid recorder :
a. Gagang hybrid recorder, berfungsi sebagai pegangan saat mengangkat hybrid recorder
b. Kerangka, berfungsi untuk melindungi bagian dalam hybrid recorder c. Display, berfungsi sebagai pembaca suhu
d. Printer, berfungsi sebagai mesin pencetak
e. Termokopel, berfungsi sebagai alat pengukur suhu
f. Cabang termokopel, berfungsi sebagai kabel/kawat logam penghubung ke dalam lubang hybrid recorder
g. Tombol, berfungsi sebagai tombol pengatur hybrid recorder h. Colokan kabel, berfungsi untuk menghubungkan ke arus listrik
Sumber : Internet
Gambar 6. Panci presto Fungsi bagian :
c a b
a. Ventilasi udara, berfungsi lubang ventilasi udara
b. Gagang tutup panci, berfungsi untuk membuka/menutup panci
c. Pengatur tekanan, berfungsi untuk mengatur tekanan yang ada di dalam panci
d. Tutup panci, berfungsi untuk meunutup panci bagian dalam agar terhindar dari kotoran yang masuk ke dalam panci
e. Gagang panci, berfungsi untuk pegangan panci
f. Wadah, berfungsi untuk menahan air/bahan atau sebagai tempatnya
Sumber : Internet Gambar 7. Stopwatch Fungsi bagian :
a. Tombol start/stop, berfungsi untuk memulai/mengakhiri waktu pengukuran
b. Tombol kalibrasi, berfungsi untuk mengkalibrasi sebelum pengukuran dan membuat posisi jarum menunjukkan angka nol
c. Skala pengukuran, berfungsi untuk mengetahui waktu yang digunakan dalam menit dan detik
d. Jarum penunjuk menit, berfungsi untuk menunjukkan hasil pembacaan dalam menit.
B. Pembahasan
Gas ideal adalah keadaan gas yang dianggap sempurna, memiliki sifat tertentu sehingga dapat diterapkan pada teori kinetik gas. Gas ideal adalah suatu gas yang diidekan oleh manusia, secara real gas ideal tidak ditemukan di permukaan bumi. Gas ideal adalah gas yang mematuhi persamaan gas umum dari PV = nRT dan hukum gas lainnya di semua suhu dan tekanan.
Faktor yang memepengaruhi gas ideal adalah tekanan, volume, suhu, jumlah partikel dan jenis gas. Sifat-sifat gas dapat dirangkumkan sebagai berikut:
1. Gas bersifat transparan
2. Gas terdistribusi merata dalam ruang apapun bentuk ruangnya 3. Gas dalam ruang akan memberikan tekanan ke dinding
4. Volume sejumlah gas sama dengan volume wadahnya. Bila gas tidak diwadahi, volume gas akan menjadi tak hingga besarnya, dan tekanannya akan menjadi tak hingga kecilnya
5. Gas berdifusi ke segala arah tidak peduli ada atau tidak tekanan luar 6. Bila dua atau lebih gas bercampur, gas-gas itu akan terdistribusi merata 7. Gas dapat ditekan dengan tekanan luar. Bila tekanan luar dikurangi, gas akan
mengembang
8. Bila dipanaskan gas akan mengembang, bila didinginkan akan mengkerut. Sedangkan sifat dari gas ideal, diantaranya :
1. Gas terdiri atas partikel-partikel dalam jumlah yang besar sekali, yang senantiasa bergerak dengan arah sembarang dan tersebar merata dalam ruang yang kecil
2. Jarak antara partikel gas jauh lebih besar daripada ukuran partikel, sehingga ukuran partikel gas dapat diabaikan
4. Hukum-hukum Newton tentang gerak berlaku.
Hukum II Termodinamika berpusat pada masalah entropi. Hukum II Termodinamika bisa dinyatakan sebagai berikut: “Entropi dapat diciptakan tetapi tidak dapat dimusnahkan.” Hubungan tekanan temperatur terhadap tingkat wujud suatu zat dapat dilihat dengan titik didih suatu zat cair yang dipengaruhi oleh tekanan udara, artinya makin besar tekanan udara makin besar pula titik didih zat cair tersebut. Pada tekanan dan temperatur udara standar (76 cmHg, 25ºC) titik didih air sebesar 100ºC (Anonim, 2011).
Termodinamika sudah sangat tidak asing didalam kehidupan sehari-hari, banyak sekali peristiwa termodinamika yang terjadi dalam kehidupan. Sebagai contohnya perubahan suhu yang terdapat pada badan kita, kemudian beberapa peralatan rumah tangga yang menggunakan konsep termodinamika dan beberapa peralatan lainnya.
Termodinamika telah merubah sistem industri di dunia, dari yang mulanya menggunakan kayu bakar untuk memasak sampai menggunakan listrik untuk memasak. Hal ini karena termodinamika merupakan hukum-hukum yang menyangkut banyak hal dalam kehidupan sehari-hari. Salah satu contoh yang paling sederhana adalah es di dalam gelas yang menyebabkan terjadi pengembunan di luar gelas, padahal terpisahkan oleh medium gelas (glass) yang memisahkan permukaan luar dan permukaan dalam.
dingin. Udara yang bersentuhan dengan gelas dingin ini akan turun suhunya. Uap air yang ada di udara pun ikut mendingin. Jika suhunya sudah cukup dingin, uap air ini akan mengembun membentuk tetes-tetes air di bagian luar gelas. Hal ini merupakan peristiwa termodinamika yang sesuai dengan hukum termodinamika yang ke dua yang berbunyi sebagai berikut “hukum kedua termodinamika terkait dengan entropi”.
Hukum ini menyatakan bahwa total entropi dari suatu sistem termodinamika terisolasi cenderung untuk meningkat seiring dengan meningkatnya waktu, mendekati nilai maksimumnya, dari hukum ini proses yang terjadi di dalam gelas merupakan proses penyerapan panas dengan kata lain udara akan berubah menjadi dingin, sementara udara mengandung kadar air yang tinggi pada kelembaban yang tinggi, sehingga ketika udara dingin akan membuatnya mengembun sehingga timbul air pada permukaan luar pada gelas.
Dari contoh es pada gelas di atas merupakan sistem pertukaran secara tertutup karena terjadi pertukaran panas tetapi tidak terjadi pertukaran benda dengan menggunakan media pembatas rigid (tidak boleh mempertukarkan kerja) dengan mempertukarkan panas melalui medium gelas.
termodinamika dengan sistem terbuka. Dimana ruang didalam silinder mesin merupakan sistem, kemudian campuran bahan bakar dan udara masuk ke dalam silinder, dan gas buang keluar sistem melalui knalpot.
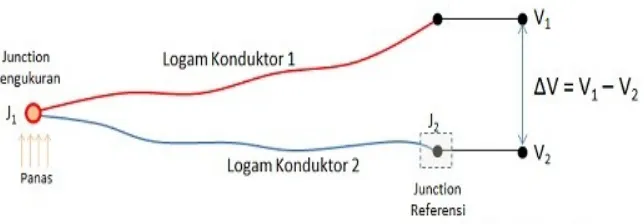
Termokopel (Thermocouple) adalah jenis sensor suhu yang digunakan untuk mendeteksi atau mengukur suhu melalui dua jenis logam konduktor berbeda yang digabung pada ujungnya sehingga menimbulkan efek “thermo-electric”.
Sistem kerja termokopel cukup mudah dan sederhana. Pada dasarnya termokopel hanya terdiri dari dua kawat logam konduktor yang berbeda jenis dan digabungkan ujungnya. Satu jenis logam konduktor yang terdapat pada termokopel akan berfungsi sebagai referensi dengan suhu konstan (tetap) sedangkan yang satunya lagi sebagai logam konduktor yang mendeteksi suhu panas.
Untuk lebih jelas mengenai sistem kerja termokopel, mari kita melihat gambar dibawah ini :
Sumber: Internet
Sumber : Laboratorium TP
Gambar 9. Termokopel dan Hybrid Recorder Fungsi bagian termokopel dan hybrid recorder :
a. Gagang hybrid recorder, berfungsi sebagai pegangan saat mengangkat hybrid recorder
b. Kerangka, berfungsi untuk melindungi bagian dalam hybrid recorder c. Display, berfungsi sebagai pembaca suhu
d. Printer, berfungsi sebagai mesin pencetak
e. Termokopel, berfungsi sebagai alat pengukur suhu
f. Cabang termokopel, berfungsi sebagai kabel/kawat logam penghubung ke dalam lubang hybrid recorder
g. Tombol, berfungsi sebagai tombol pengatur hybrid recorder h. Colokan kabel, berfungsi untuk menghubungkan ke arus listrik
Berikut ini adalah jenis-jenis atau tipe termokopel yang umum digunakan berdasarkan Standar Internasional.
1. Termokopel Tipe E
Bahan Logam Konduktor Positif : Nickel-Chromium Bahan Logam Konduktor Negatif : Constantan b
h
c g
f e
Rentang Suhu : -200˚C – 900˚C 2. Termokopel Tipe J
Bahan Logam Konduktor Positif : Iron (Besi) Bahan Logam Konduktor Negatif : Constantan Rentang Suhu : 0˚C – 750˚C
3. Termokopel Tipe K
Bahan Logam Konduktor Positif : Nickel-Chromium Bahan Logam Konduktor Negatif : Nickel-Aluminium Rentang Suhu : -200˚C – 1250˚C
4. Termokopel Tipe N
Bahan Logam Konduktor Positif : Nicrosil Bahan Logam Konduktor Negatif : Nisil Rentang Suhu : 0˚C – 1250˚C
5. Termokopel Tipe T
Bahan Logam Konduktor Positif : Copper (Tembaga) Bahan Logam Konduktor Negatif : Constantan Rentang Suhu : -200˚C – 350˚C
6. Termokopel Tipe U (kompensasi Tipe S dan Tipe R) Bahan Logam Konduktor Positif : Copper (Tembaga) Bahan Logam Konduktor Negatif : Copper-Nickel Rentang Suhu : 0˚C – 1450˚C
rentang suhu 0-100°C dengan keakuratan 0.1°C. Untuk aplikasi ini, Termistor dan RTD lebih cocok. Contoh Penggunaan Termokopel yang umum antara lain : 1. Industri besi dan baja
2. Pengaman pada alat-alat pemanas 3. Untuk termopile sensor radiasi
4. Pembangkit listrik tenaga panas radioisotop, salah satu aplikasi termopile. Termokopel menggunakan dua jenis logam yang berbeda untuk membangkitkan tegangan untuk kemudian tegangan tersebut dapat digunakan sebagai acuan dalam pengukuran suhu. Termokopel telah banyak dipakai dalam pengukuran suhu, khususnya dalam dunia industri. Beberapa jenis industri seperti industri besi dan baja, pengaman pada alat pemanas, thermopile sensor radiasi, pembangkit listrik tenaga panas radio isotop, dan lain-lain telah mendayagunakan termokopel. Kemampuan dari termokopel yang dapat mengukur suhu dari suhu yang sangat tinggi dan juga suhu rendah menjadi alasan mengapa termokopel banyak dipakai.
Berikut ini merupakan kelebihan dan kekurangan dari termokopel, yakni: Untuk kelebihannya, diantaranya :
1. Mudah dibaca, karena memiliki layar yang tidak mudah keruh dan skala yang jelas
2. Respon cepat untuk setiap adanya perubahan suhu 3. Akurasi yang tepat dalam pengukuran suhu
Untuk kekurangannya, diantaranya :
1. Kalibrasi yang sulit, saat termokopel dinyalakan, suhu yang tertera adalah suhu pada ruangan tersebut
2. Hanya dapat digunakan untuk mengukur perbedaan suhu
3. Termokopel membutuhkan perlengkapan tambahan yang harganya biasanya cukup mahal.
Prinsip dasar yang digunakan pada panci presto adalah kenaikan titik didih. Secara teori, air akan mendidih pada suhu 100°C pada tekanan 1 atmosfer. Karena panci presto terbuat dari bahan stainless yang tebal dan kuat serta mempunyai tutup yang rapat, maka uap air yang yang dihasilkan saat proses pendidihan tidak mungkin keluar dan hanya terkumpul dalam panci presto. Air yang terkumpul inilah yang membuat tekanan air dalam panci presto naik, yang menyebabkan temperatur didihnya juga naik menjadi >100 derajat Celsius. Kalau dengan sedikit teori anak sekolahan, itu seperti persamaan gas ideal, dimana PV = CT, dimana P = tekanan; V = volume; T = suhu ; C = konstanta kesebandingan gas, persamaan itu juga biasa disebut Hukum Gay-Lussac. Jadi dapat juga diartikan hubungan antara P dan T bahwa Penambahan tekanan menaikkan titik didih dan titik lebur zat.
Pada saat praktikum , kami mendapatkan hasil niai perhitungan yang berbeda setiap kelompoknya. Berikut ini merupakan data yang didapat pada saat praktikum :
Perhitungan : 1. Kelompok 1 dan 3
Volume panci = 4 L Volume air = 0,5 L
T1 (awal) = 29,5ºC (kondisi vakum) T2 (akhir) = 100,7ºC (kondisi vakum) P1 (awal) = 100 kPa
t (vakum) = 191 detik 1) Mencari volume spesifik (P diketahui = 0,341 mPa)
0,3−0,341 2) Mencari volume uap
Volume uap air = volume panci – volume air = (4x10-3) – (0,5x10-3) = 3,5x10-3 m3
3) Mencari massa uap
Massa uap = volume spesifikvolume uap
= 3,5x10−3 0,00107751 = 3,25 kg b. Kondisi non vakum
P1 P2 =
T1 T2
P2 = 10030 x 100 = 333,34 kPa = 0,334 mPa 1) Mencari volume spesifik (P diketahui = 0,341 mPa)
0,3−0,334 0,3−0,4 =
0,001073−x −0,001073−0,001084 −0,034 2) Mencari volume uap
Volume uap air = volume panci – volume air = (4x10-3) – (0,5x10-3) = 3,5x10-3 m3
3) Mencari massa uap
Massa uap = volume spesifikvolume uap
= 3,5x10
−3
= 3,25 kg 2. Kelompok 5 dan 7
Volume panci = 8 L Volume air = 0,7 L
T1 (awal) = 32ºC (kondisi vakum) T2 (akhir) = 94ºC (kondisi vakum) P1 (awal) = 100 kPa
T1 (awal) = 31ºC (kondisi non vakum) T1 (akhir) = 98,3ºC (kondisi non vakum) t (vakum) = 421 detik 1) Mencari volume spesifik (P diketahui = 0,294 mPa)
0,2−0,294 2) Mencari volume uap
Volume uap air = volume panci – volume air = (8x10-3) – (0,7x10-3) = 7,3x10-3 m3
3) Mencari massa uap
Massa uap = volume uap b. Kondisi non vakum
P1 1) Mencari volume spesifik (P diketahui = 0,341 mPa)
0,3−0,317 0,3−0,4 =
2) Mencari volume uap
Volume uap air = volume panci – volume air = (8x10-3) – (0,7x10-3) = 7,3x10-3 m3
3) Mencari massa uap
Massa uap = volume spesifikvolume uap
= 7,3x10
o T didih (ºC) P2 didih (ºC) Keterangan Durasi (s)
1 100,7 341,35 Vakum 191
2 10 333,34 Non vakum 194
3 94 293,75 Vakum 421
4 98,3 317,09 Non vakum 542
Tabel 6. Hasil data perhitungan N
1 0,00107751 3,5x10-3 3,25 Vakum
2 0,00107674 3,5x10-3 3,26 Non Vakum
3 0,00107228 3,5x10-3 6,81 Vakum
4 0,00107487 3,5x10-3 6,79 Non Vakum
Alat yang digunakan pada saat praktikum, sebagai berikut :
Sumber : Internet c
Gambar 10. Gelas ukur Fungsi bagian :
a. Gagang gelas, berfungsi sebagai pegangan gelas ukur b. Skala, berfungsi untuk ukuran volume
c. Tabung, berfungsi untuk menampung benda atau cairan yang ingin diukur volumenya
Sumber : Internet
Gambar 11. Kompor gas Fungsi bagian :
a. Lubang selang gas, berfungsi sebagai lubang selang gas b. Burner, berfungsi sebagai sumbu kompor
c. Kerangka kompor gas, berfungsi sebagai kerangka/pelindung bagian dalam kompor
d. Tungku, berfungsi sebagai dudukan dari wajan/pamci
e. Pemantik gas, berfungsi untuk menyalakan api gas/membesar kecilkan api
b a
e d
Sumber : Laboratorium TP Gambar 12. Termometer raksa Fungsi bagian :
a. Skala, berfungsi untuk mengukur suhunya
b. Tabung kaca, berfungsi sebagai pelindung bagian dalam termometer c. Perak, berfungsi sebagai sensitivitas
Sumber : Laboratorium TP
Gambar 13. Termokopel dan Hybrid Recorder Fungsi bagian termokopel dan hybrid recorder :
a. Gagang hybrid recorder, berfungsi sebagai pegangan saat mengangkat hybrid recorder
c b a
b
h
c g
f e
b. Kerangka, berfungsi untuk melindungi bagian dalam hybrid recorder c. Display, berfungsi sebagai pembaca suhu
d. Printer, berfungsi sebagai mesin pencetak
e. Termokopel, berfungsi sebagai alat pengukur suhu
f. Cabang termokopel, berfungsi sebagai kabel/kawat logam penghubung ke dalam lubang hybrid recorder
g. Tombol, berfungsi sebagai tombol pengatur hybrid recorder h. Colokan kabel, berfungsi untuk menghubungkan ke arus listrik
Sumber : Internet
Gambar 14. Panci presto Fungsi bagian :
a. Ventilasi udara, berfungsi lubang ventilasi udara
b. Gagang tutup panci, berfungsi untuk membuka/menutup panci
c. Pengatur tekanan, berfungsi untuk mengatur tekanan yang ada di dalam panci
d. Tutup panci, berfungsi untuk meunutup panci bagian dalam agar terhindar dari kotoran yang masuk ke dalam panci
c a b
e. Gagang panci, berfungsi untuk pegangan panci
f. Wadah, berfungsi untuk menahan air/bahan atau sebagai tempatnya
Sumber : Internet Gambar 15. Stopwatch Fungsi bagian :
a. Tombol start/stop, berfungsi untuk memulai/mengakhiri waktu pengukuran
b. Tombol kalibrasi, berfungsi untuk mengkalibrasi sebelum pengukuran dan membuat posisi jarum menunjukkan angka nol
c. Skala pengukuran, berfungsi untuk mengetahui waktu yang digunakan dalam menit dan detik
d. Jarum penunjuk menit, berfungsi untuk menunjukkan hasil pembacaan dalam menit.
V. KESIMPULAN DAN SARAN A. Kesimpulan
1. Hukum II Termodinamika bisa dinyatakan sebagai berikut: “Entropi dapat diciptakan tetapi tidak dapat dimusnahkan”
2. Aplikasi sistem terisolasi pada kehidupan sehari hari dapat digunakan dalam proses pengukuran suhu suatu zat ataupun media dengan menggunakan bantuan termometer sebagai alat pengukur suhunya 3. Kondisi gas ditentukan oleh tiga faktor yaitu : tekanan, suhu dan
volume. Gas ideal adalah keadaan gas yang dianggap sempurna, memiliki sifat tertentu sehingga dapat diterapkan pada teori kinetik gas.
B. Saran
DAFTAR PUSTAKA
Anonim. 2011. Hukum Termodinamika. kk.mercubuana.ac.id/files/13015-3-860358017731.doc
Daryanto. 2003. Dasar-dasar Teknik Mesin. Jakarta: PT. Bhineka Cipta Jakarta. Maron, Samuel H, and Lando, J.B. 1992 Fundamentals oh Physical Chemistry.
New York : Macmillan publishing co.inc.
Tahang. 2011. Penerapan Hukum-2 Termodinamika.
www.slideshare.net/tahangpette/penerapan-hukum-2-thermodinamika. Tim Asisten. 2016. Modul Praktikum Termodinamika. Purwokerto: Universitas