i
PREPARASI DAN KARAKTERISASI KOMPOSIT ZnO-ZEOLIT UNTUK FOTODEGRADASI ZAT WARNA CONGO RED
SKRIPSI
Diajukan kepada Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Negeri Yogyakarta untuk Memenuhi Sebagian
Persyaratan guna Memperoleh Gelar Sarjana Sains Bidang Kimia
Oleh :
Syaiful Amri
NIM : 12307144026
PROGRAM STUDI KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS NEGERI YOGAYAKARTA
ii
PERSETUJUAN
Skripsi yang berjudul “Preparasi dan Karakterisasi Komposit ZnO-Zeolit untuk
Fotodegradasi Zat Warna Congo Red” yang disusun oleh Syaiful Amri, NIM
12307144026 ini telah distujui oleh pembimbing untuk diajukan.
Yogyakarta, 20 November 2016
Menyetujui, PembimbingUtama
M. Pranjoto Utomo, M.Si NIP. 19710408 199802 1 002
Koordinator Tugas Akhir Skripsi Program Studi Kimia,
iii
PENGESAHAN
Skripsi yang berjudul “Preparasi dan Karakterisasi Komposit ZnO-Zeolit untuk
Fotodegradasi Zat Warna Congo Red” yang disusun oleh Syaiful Amri, NIM
12307144026 ini telah dipertahankan di depan Dewan Penguji pada tanggal 26
September 2016 dan dinyatakan lulus
DEWAN PENGUJI
Dr. Cahyorini Kusumawardani, M. Si NIP. 19770723 200312 2 001
Fakultas Matematika dan Ilmu Pengetahuan Alam Dekan
Dr. Hartono
iv
PERNYATAAN
Yang bertandatangan di bawah ini:
Nama : Syaiful Amri
NIM : 12307144026
Program Studi : Kimia
Fakultas : Matematika dan Ilmu Pengetahuan Alam
Judul Penelitian : Prepaasi dan Karakterisasi Komposit ZnO-Zeolit untuk
Fotodegradasi Congo Red.
Menyatakan bahwa penelitian ini adalah hasil pekerjaan saya sendiri, dan sepanjang pengetahuan saya tidak berisi materi yang sudah dipublikasikan atau ditulis oleh orang lain atau telah dipergunakan dan diterima sebagai persyaratan penyelesaian studi pada universitas atau institut lain, kecuali pada bagian-bagian tertentu yang telah dinyatakan dalam referensi.
Yogyakarta, November 2016 Yang menyatakan,
v Motto
“Tetap jalani kehidupan yang penuh MISTERI”
vi
HALAMAN PERSEMBAHAN
Puji Syukur Kehadirat Allah SWT atas rahmat dan hidayah-Nya yang telah
diberikan untuk meyelesaikan skripsi ini.
Skripsi ini saya persembahkan untuk:
1. Ibuku tercinta Sumarsih dan Bapakku Syafi’I yang selalu memberikan do’a, motivasi dan semangatnya.
2. Kakakku Ali Wahyudi, Hanik Mundirotun, dan adikku Nurul Khasanah serta seluruh kerabat keluarga yang turut mendoakan sehingga kuliahku bisa terselesaikan.
3. Sahabat-sahabat kos yang selalu memberikan semangat, Mas Ridho, Mas Yogo, Mas Aji, Mas Erwan, dan Mas Fredi dll.
4. Teman-teman KSI-Mist yang selalu memberikan semangat dan pembelajaran.
vii
KATA PENGANTAR
Puji syukur kehadirat Allah SWT yang selalu memberikan rahmat dan hidayahNya sehingga penulis dapat menyelesaikan skripsi dengan judul “Preparasi dan Karakterisasi Komposit ZnO-Zeolit untuk Fotodegradasi Zat
Warna Congo Red”.
Penelitian ini disusun untuk melengkapi syarat yang telah ditetapkan oleh Jurusan Pendidikan Kimia guna memperoleh gelar sarjana sains. Pada kesempatan ini perkenankanlah penulis mengucapkan terimakasih kepada:
1. Bapak Dr. Hartono, M.Si. selaku dekan FMIPA Universitas Negeri Yogyakarta.
2. Bapak Drs. Jaslin Ikhsan, M.App.Sc., Ph.D. selaku Ketua Jurusan Pendidikan Kimia FMIPA Universitas Negeri Yogyakarta.
3. Bapak Pranjoto Utomo, M.Si. selaku dosen pembimbing. 4. Ibu Dr.Cahyorini, M.Si. selaku dosen sekretaris penguji.
5. Bapak Prof. K.H. Sugijarto, Ph. D selaku dosen penguji utama. 6. Ibu Dr. Kun Sri Budiasih, M. Si selaku dosen penguji pendamping.
7. Seluruh Dosen, Staf, dan Laboran Jurusan Pendidikan Kimia FMIPA UNY yang telah banyak membantu selama perkuliahan dan penelitian. 8. Semua pihak yang telah membantu kelancaran terselesaikannya laporan ini
viii
Penulis menyadari bahwa masih banyak kekurangan dalam penyusunan skripsi ini, oleh karena itu penulis mengharapkan kritik dan saran dari berbagai pihak yang bersifat membangun. Semoga skripsi ini dapat bermanfaat bagi pembaca dan semua pihak.
Yogyakarta, 2016
ix
B. Identifikasi Masalah ... 4
C. Batasan Masalah... 4
7. Scanning Electron Microscopy-Electron Dispersive X-Ray Analyser (SEM-EDX) ... 24
x
B. Penelitian yang Relevan ... 27
C. Kerangka Berfikir... 29
BAB III METODE PENELITIAN ... 30
A. Subjek dan Objek Penelitian ... 30
B. Variabel Penelitian ... 30
C. Alat dan Bahan ... 30
D. Prosedur Kerja ... 31
E. Skema Rangkaian Alat ... 34
F. Diagram Alir Kerja... 35
BAB IV HASIL DAN PEMBAHASAN... 36
A. Pembuatan Komposit ZnO-Zeolit ... 36
B. Karakterisasi Komposit ZnO-Zeolit... 37
1. Spektroskopi Inframerah. ... 38
2. Difraksi Sinar X ... 40
3. Scanning Electron Microscopy-Electron Dispersive X-Ray Analyzer ... 41
4. Spektroskopi UV-Vis ... 43
C. Uji Aktivitas Fotokatalitik Komposit Zeolit-ZnO... 46
1. Menentukan Kurva Standar Congo Red.... 46
xi
DAFTAR GAMBAR
Halaman
Gambar 1. Struktur Kristal Zeolit ... 7
Gambar 2. Diagram Energi Celah Pita dari Metal, Isolator dan
Gambar 5. Skema Proses Fotokatalis pada Permukaan Semikonduktor ... 16
Gambar 6. Struktur Kimia Congo Red... 18
Gambar 7. Mekanisme Degradasi Congo Red Berdasarkan Analisis UV-Vis dan GC-MS ... 19
Gambar 8. Difraksi Sinar-X oleh Bidang Kristal ... 22
Gambar 9. Contoh Puncak-Puncak pada Difraktogram ... 23
Gambar 10. Diagram Alir Proses Penelitian ... 36
Gambar 11. Spektrum Inframerah Zeolit, Zeolit Aktivasi dan Zeolit-ZnO ... 38
Gambar 12. Pola Difraksi Zeolit dan Zeolit-ZnO ... 40
Gambar 13. Hasil SEM Komposit Zeolit-ZnO dengan Berbagai Perbesaran... 42
Gambar 14. Spektra EDX dari Komposit Zeolit-ZnO ... 43
Gambar 15. Spektrum Absorbansi dari Zeolit dan Komposit Zeolit-ZnO... 44
Gambar 16. Perhitungan Band Gap dari Zeolit dan Komposit Zeolit-ZnO... 45
Gambar 17. Kurva Standar Congo Red ... 46
Gambar 18. Grafik Persamaan Isoterm Langmuir ... 49
Gambar 19. Grafik Persamaan Isoterm Freundlich... 50
DAFTAR TABEL Halaman Tabel 1. Contoh Zeolit Alam yang Umum Ditemukan ... 8
Tabel 2. Rumus Oksida Beberapa Zeolit Sintetis ... 9
Tabel 3. Hasil Interpretasi FTIR Sampel Zeolit, Zeolit Teraktivasi dan Zeolit-ZnO... 38
Tabel 4. Perubahan Nilai Absorbansi dari Proses Adsorpsi... 47
xii
DAFTAR LAMPIRAN
Halaman
LAMPIRAN 1. Hasil dari Analisis XRD... 58
LAMPIRAN 2. Perhitungn Ukuran Kristal Zeolit dan ZnO-Zeolit ... 62
LAMPIRAN 3. Hasil dari Spekrta Absorbansi dan Reflektansi UV ... 65
LAMPIRAN 4. Hasil FTIR ... 71
LAMPIRAN 5. Hasil SEM-EDX... 73
LAMPIRAN 6. Pengenceran Larutan Standar Congo Red... 77
LAMPIRAN 7. Penentuan Lamda Maks Congo Red ... 78
xiii
PREPARASI DAN KARAKTERISASI KOMPOSIT ZnO-ZEOLIT UNTUK FOTODEGRADASI ZAT WARNA CONGO RED
Oleh: Syaiful Amri NIM. 12307144026
Pembimbing Utama: M. Pranjoto Utomo, M.Si. ABSTRAK
Penelitian ini bertujuan untuk mempreparasi dan mengkarakterisasi komposit ZnO-zeolit. Tujuan lainnya adalah mengetahui pola isoterm adsorpsi dan kinetika reaksi fotodegradasi congo red dengan komposit ZnO-zeolit.
Komposit ZnO-zeolit dapat disintesis dengan metode sol-gel menggunakan perkursor zeolit alam dan Zn(CH3COO)2. Hasil sintesis dikarakterisasi
menggunakan XRD, FTIR, UV-Vis Diffuse Reflectance dan SEM-EDX. Uji
aktivitas fotoakatalitik terdiri dari tiga bagian yaitu: uji adsorpsi pada keadaan gelap, uji aktivitas fotokatalitik dengan sinar UV dan uji aktivitas fotokatalitik dengan sinar tampak.
Analisis XRD zeolit-ZnO menunjukan ukuran kristal 26,07 nm. Spektra FTIR menunjukkan adanya serapan ZnO pada bilangan gelombang 468,24 cm-1. Analisis SEM material zeolit berukuran 4 -13 mikrometer. Sedangkan material Zink Oksida (ZnO) dengan ukuran 0,31-0,35 mikrometer. Analisi EDX komposit zeolit-ZnO menunjukkan persentase massa element Zn = 21.06%.. Analisis UV-Vis didapatkan energi celah pita dari komposit zeolit-ZnO adalah 2.15 eV. Uji adsorpsi pada keadaan gelap komposit ZnO-zeolit mengikuti pola isoterm Langmuir.
xiv
PREPARATION AND CHARACTERIZATION OF ZnO-ZEOLIT COMPOSITE FOR PHOTODEGRADATION OF CONGO RED
By: Syaiful Amri
Student’s Number. 12307144026 Supervisor: M. Pranjoto Utomo, M.Si.
ABSTRACT
This research was aimed to prepare and characterize ZnO-Zeolit composite, to determine the pattern of adsorption isotherms and kinetics of phtodegradation reaction congo red with ZnO-zeolite composite.
Composite ZnO-zeolite can be synthesized by sol-gel method using a precursor of natural zeolite and Zn(CH3COO)2. The synthesis result characterized
with XRD, FTIR, UV-Vis Diffuse Reflectance and SEM-EDX. Photocatalytic activity test consists of three parts: adsorption test in the dark, the photocatalytic activity test with UV light and photocatalytic activity test with visible light.
1 BAB I PENDAHULUAN A. Latar Belakang Masalah
Sektor industri tekstil di Indonesia mengalami perkembangan yang pesat dari tahun ke tahun. Perkembangan ini memberikan dampak positif dan negatif bagi masyarakat. Dampak positifnya yaitu perekonomian semakin meningkat. Dampak negatifnya industri tekstil yang tidak bertanggungjawab dengan melakukan pembuangan limbah hasil pewarnaan kelingkungan langsung tanpa dilakukan pengolahan terlebih dahulu dapat menimbulkan masalah lingkungan secara serius. Zat warna tekstil merupakan salah satu pencemar yang bersifat non-biodegradable, umumnya dibuat dari senyawa azo dan turunannya yang merupakan gugus benzena. Senyawa azo digunakan sebagai bahan celup, yang dinamakan azo dyes. Salah satu zat warna azo yang banyak digunakan adalah congo red. Senyawa azo bila terlalu lama
berada di lingkungan akan menjadi sumber penyakit karena sifatnya karsinogenik dan mutagenik, oleh karena itu perlu dicari metode yang efektif untuk menguraikan limbah tersebut (Maria, dkk., 2007).
2
terdapat kekurangan yang menyebabkan pengolahan limbah tersebut menjadi kurang optimal. Pengolahan limbah dengan metode koagulasi dan sedimentasi menimbulkan limbah baru yaitu koagulan yang tidak dapat digunakan lagi. Pada metode adsorpsi, zat warna yang diadsorpsi terakumulasi dalam adsorben tanpa menguraikan sifat toksik dan karsinogenik dari limbah zat warna tersebut sehingga menimbulkan masalah baru yang harus diselesaikan, sedangkan pada metode lumpur aktif, beberapa jenis limbah zat warna memiliki sifat yang resisten untuk didegradasi secara biologis (Nirmasari, Widodo dan Haris, 2009).
Salah satu metode alternatif pengolahan limbah zat warna yang telah dikembangkan pada saat ini yaitu metode fotodegradasi dengan menggunakan semikonduktor fotokatalis dan sinar ultraviolet (Widihati, Diantariani dan Nikmah, 2011). Proses fotokatalitik perlu dikembangkan lebih lanjut karena tidak seperti pengolahan limbah konvensional yang hanya memindahkan polutan dari suatu tempat ke tempat lainnya melainkan mampu mengubah polutan menjadi senyawa sederhana dan bersifat ramah lingkungan (Kabra, Chandhary dan Sawhney, 2004).
Beberapa faktor yang mempengaruhi aktivitas fotokatalisis yaitu energi celah pita atau band gap dan rekombinasi pasangan electron-hole dari
3
ukuran yang lebih baik dengan cara mendispersikan partikel semikonduktor pada material pendukung padat seperti kaca, silika, arang aktif, lempung dan zeolit (Tayade, Kulkarni dan Jasra, 2007).
Zeolit merupakan padatan pendukung yang baik untuk mendispersikan semikonduktor ZnO karena zeolit mempunyai luas permukaan dan volum pori yang besar serta keseragaman ukuran saluran. Zeolit menunjukkan keistimewaan lainnya yang menjadikan mereka cocok untuk digunakan sebagai padatan pendukung untuk fotokatalisis yaitu (Tayade, Kulkarni dan Jasra, 2007):
1. Stabil secara fotokimia serta lembam (inert) secara kimia dan suhu.
2. Dapat ditembus cahaya radiasi lebih dari 240 nm kemudian cahaya menetrasi ke dalam padatan zeolit untuk mencapai molekul substrat di dalam pori zeolit.
3. Zeolit mempunyai daya adsorpsi yang tinggi untuk senyawa organik dari larutan dengan mendekatkan pada sisi aktif fotokatalisis.
4. Kekuatan polaritas di dalam pori zeolit disebabkan oleh variasi muatan internal yang menyeimbangkan (kation) dan ukuran saluran.
5. Kemampuan kerangka (framework) zeolit untuk berpartisipasi aktif dalam
4 B. Identifikas i Masalah
Berdasarkan latar belakang yang telah dikemukakan, dapat diidentifikasi masalah-masalah dalam pembuatan komposit ZnO-Zeolit, antara lain sebagai berikut:
1. Bahan baku dan metode yang digunakan untuk preparasi komposit ZnO-zeolit.
2. Metode karakterisasi komposit ZnO-zeolit.
3. Uji aktivitas komposit ZnO-zeolit pada proses pendegradasian congo red.
C. Batasan Masalah
Berdasarkan identifikasi masalah yang disajikan di atas, maka batasan dalam penelitian ini adalah:
1. Bahan yang digunakan untuk preparasi komposit ZnO-zeolit adalah ZnO- zeolit alam (Chemic) dan Zn(CH3COO)2 serta metode yang digunakan
adalah sol-gel.
2. Proses karakterisasi yang digunakan adalah XRD, FTIR, SEM-EDX dan UV-Vis Diffuse Reflektansi.
3. Uji aktivitas komposit ZnO-Zeolit pada proses degradasi congo red
5 D. Rumusan Masalah
Berdasarkan pembatasan masalah di atas, dapat dirumuskan masalah yaitu:
1. Bagaimana preparasi komposit ZnO-zeolit?
2. Bagaimana karakter komposit ZnO-zeolit berdasarkan analisis FTIR, XRD, SEM dan UV-Vis Diffuse Reflektansi ?
3. Bagaimana pola isoterm adsorpsi komposit ZnO-zeolit terhadap congo
red?
E. Tujuan Penelitian
Berdasarkan latar belakang di atas tujuan penelitian ini adalah: 1. Mengetahui cara preparasi komposit ZnO-zeolit.
2. Mengetahui karakter komposit ZnO-zeolit berdasarkan analisis FTIR, XRD, SEM dan UV-Vis Diffuse Reflektansi.
3. Mengetahui pola isoterm adsorpsi komposit ZnO-zeolit terhadap congo
red.
F. Manfaat Penelitian
Manfaat dari penelitian ini adalah:
1. Memberikan informasi terkait preparasi komposit ZnO-Zeolit.
2. Memberikan informasi terkait karakter komposit ZnO-zeolit berdasarkan analisis FTIR, XRD, SEM dan UV-Vis Diffuse Reflektansi.
6 BAB II KAJIAN PUSTAKA A. Tinjauan Pustaka
1. Zeolit Alam
Zeolit merupakan endapan dari aktivitas vulkanik yang banyak menganndung unsur silika. Nama zeolit itu sendiri berasal dari bahasa Yunani yaitu Zeni dan Lithos yang berarti batu mendidih. Apabila zeolit dipanaskan maka akan membuih dan mengeluarkan air. Zeolit adalah material aluminosilikat alami yang telah banyak digunakan untuk pertukaran ion (ion exchange), adsorbsi, dan sifat katalis. Kemampuan
tersebut dimiliki oleh zeolit karena struktur kristalnya yang berongga-rongga. Material ini juga secara ekstensif diinvestigasi karena keanekaragaman strukturnya. Selain itu dengan keunikan dan beragamnya aplikasi dari zeolit telah mendorong pengembangan proses sintesis zeolit yaitu menciptakan material baru dengan dimensi pori, komposisi dan reaktivitas yang bervariasi (Rajic & Kaucic, 2002).
7
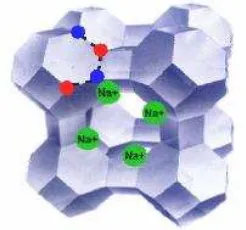
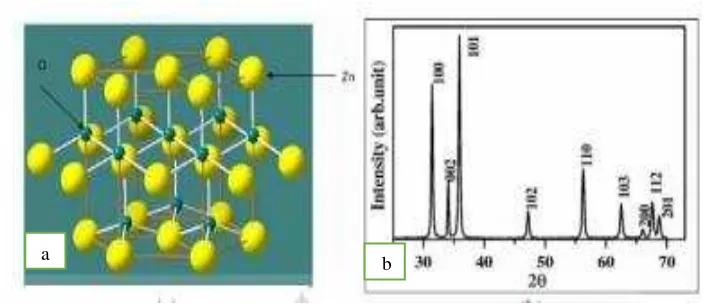
yang mengandung muatan positif dari ion-ion logam alkali dan alkali tanah dalam kerangka kristal tiga dimensi dengan setiap oksigen membatasi antara dua tetrahedron (Hay, 1996). Struktur kristal zeolit ditunjukkan pada Gambar 1.
Gambar 1. Struktur kristal zeolit
(Sumber : Eni Hartini, 2011).
Struktur zeolit dapat dibedakan dalam tiga komponen yaitu rangka aluminosilikat, ruang kosong saling berhubungan yang berisi kation logam dan molekul air dalam fasa occluded (Harben & Kuzvart, 1996). Jika
8
Berdasarkan asalnya zeolit dapat dibedakan menjadi dua macam, yaitu zeolit alam dan zeolit sintesis. Zeolit alam terbentuk dari reaksi air pori dengan berbagai material seperti gelas, poorly crystalline clay,
ataupun silika. Pembentukan zeolit ini tergantung pada komposisi dari batuan induk, temperatur, tekanan parsial air, pH dan aktivitas dari ion-ion tertentu (Romaida Hutabarat, 2012). Contoh macam-macam zeolit alam menurut Djarwanto & Pangestu (1993), dapat dilihat pada Tabel 1.
Tabel 1. Contoh Zeolit Alam yang Umum Ditemukan
9
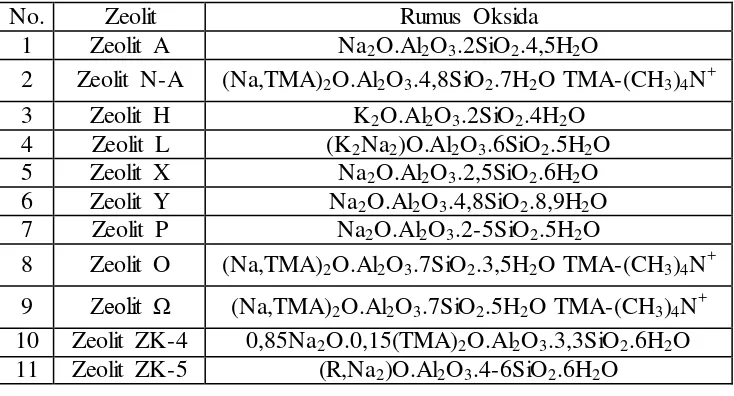
bentuk dan ukuran molekul. Secara konvensional, zeolit telah dimanfaatkan dalam berbagai bidang, seperti adsorben, agen penukar kation, maupun katalis (Tukur & Al-Khattar, 2011). Contoh macam-macam zeolit sintetis menurut Georgiev et al., (2009) dapat dilihat pada
Tabel 2.
Tabel 2. Rumus Oksida Beberapa Zeolit Sintetis
No. Zeolit Rumus Oksida
Pada penelitian ini, zeolit digunakan untuk mengurangi kelemahan yang dimiliki oleh proses fotokatalisis. Kelemahan tersebut adalah daya adsorspi yang lemah sehingga proses fotokatalisis ini perlu dikombinasikan dengan suatu material adsorben. Beberapa peneliti telah membuktikan bahwa penambahan adsorben, dalam hal ini karbon aktif pada fotokatalis TiO2, dapat meningkatkan laju degradasi berbagai
senyawa organik seperti dekomposisi propyzomide (Torimoto et al.,
10 2. Semikonduktor ZnO
Semikonduktor merupakan suatu zat yang mempunyai sifat di antara isolator dan konduktor. Perbedaan sifat isolator, konduktor dan semikonduktor menurut Yahdiana (2011), dapat dilihat dari ukuran
konduktivitas listrik (σ), struktur valensi, pita valensi dan pita konduksi,
yaitu:
a. Konduktor, merupakan suatu bahan yang dapat dengan mudah mengahantarkan arus listrik dengan nilai konduktivitas listrik (σ)
sebesar 104-106 ohm-1cm-1, mempunyai struktur dengan pita valensi berisi elektron dan pita konduksi kosong serta energi celah pita yang kecil serta struktur yang berhimpit
b. Isolator, merupakan bahan dengan daya hantar listrik yang sangat lemah atau bahkan tidak ada, dengan nilai konduktivitas listrik lebih kecil dari 10-15 ohm-1cm-1, mempunyai pita valensi yang terisi sebagian/penuh dan pita konduksi kosong, serta energi celah pita yang besar (lebih besar dari 4,0 eV).
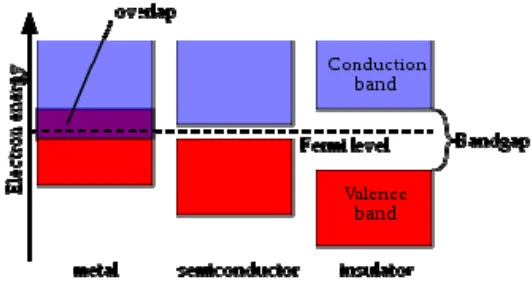
11
Gambar 2. Diagram Energi Celah Pita dari Metal (Konduktor), Isolator dan Semikonduktor
(Sumber : Eni Hartini, 2011)
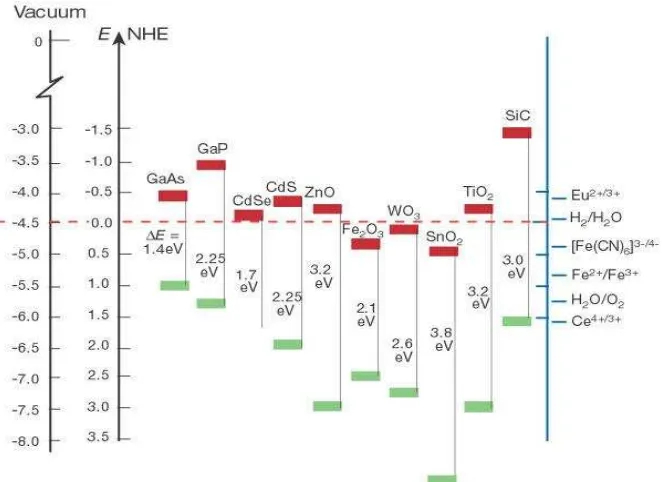
12
Gambar 3. Energi Celah Pita dan Harga Potensial Redoks dari Beberapa Semikonduktor
(Sumber : Eni Hartini, 2011).
Secara kristalografi, zink oksida memiliki tiga jenis struktur kristal, yaitu wurtzite, zincite atau zincblende dan rocksalt. Zink oksida yang
tersedia sebagai mineral di alam memiliki struktur zincite. Struktur kristal
ini berbentuk sphalerite dengan adanya atom Zn di setiap sudut dan bagian
tengah sisi (face centered cubic, FCC) dan atom O sebagai interstisi di
antara empat atom Zn yang berdekatan. Di lain hal, zink oksida yang biasa diproduksi secara komersial merupakan hasil sintesis dan berstruktur
wurtzite. Struktur ini memiliki bentuk heksagonal dan stabil pada suhu
ruang. Struktur kristal wurtzite dapat dilihat pada Gambar 4(a).
sedangkan pola difraksi sinar-X dari material ZnO nanorods dengan struktur wurtzite tersebut dapat dilihat pada Gambar 4(b). Berbeda
13 sangat luas. Zink oksida tidak hanya digunakan dalam bidang elektronik sebagai semikonduktor, tetapi juga dapat berperan sebagai material piezoelektrik, sensor, sel surya dan fotokatalis. Selain dari segi aplikasinya, ZnO mudah disintesis baik secara konvensional sekalipun. Serbuk ZnO dapat disintesis dengan metode reaksi pada kondisi solid (solid-state reaction) dan metode larutan-cair (liquid solution). Reaksi
pada kondisi padat dilakukan pada temperatur tinggi memiliki keuntungan antara lain ZnO yang dihasilkan memiliki kemurnian dan kristalinitas yang baik, akan tetapi ZnO yang disintesis dengan metode reaksi pada kondisi padat menghasilkan partikel dengan ukuran besar dan morfologi tidak teratur. Selain itu, proses ini memerlukan proses sintering dan pelelehan. Oleh karena itu, diperlukan suatu teknologi yang mampu mensistesis ZnO
14
pada suhu yang rendah. Metode yang tepat yang bisa digunakan untuk mengatasi kekurangan pada kondisi padat adalah metode kimia basah, antara lain metode sol-gel dan presipitasi. Metode presipitasi merupakan salah satu metode yang digunakan karena semua produk hasil reaksinya menghasilkan ukuran kristalit yang lebih kecil dibandingkan dengan hasil sol-gel. Metode presipitasi dilakukan dengan temperatur sistesis yang rendah, peralatan yang digunakan sederhana, proses yang sederhana, dan kemudahan dalam mengontrol setiap proses (Romaida Hutabarat, 2012).
Sayed-Dorraji, Danesvar & Abel (2009), menginvestigasi pembuatan nano partikel ZnO dengan metode presipitasi menggunakan ZnSO4.7H2O sebagai material awal dan NaOH sebagai precipitants tanpa
melalui pemurnian lanjutan. Behnajady, Modirshhla & Ghazalin (2011), juga melaporkan sintesis nanopartikel ZnO dengan menggunakan metode presipitasi dari ZnSO4.7H2O dengan menggunakan NaOH sebagai
pembasa dengan pengadukan ultrasonik dan teknik pengeringan pada suhu 1000C untuk menghasilkan bubuk nanopartikel ZnO.
3. Mekanisme Fotokatalisis
15
kemampuan untuk mengabsorpsi foton (Eni Hartini, 2011). Secara umum fotokatalisis dibagi menjadi dua macam (Vora et al., 2009), yaitu :
a. Fotokatalis Homogen
Fotokatalis homogen adalah proses fotokatalisis dengan katalis, medium, dan reaktan berada dalam fasa yang sama. Dalam kasus ini interaksi antara foton dengan spesi pengabsorpsi (senyawa koordinasi dari logam transisi zat warna organik), substrat (kontaminan) dan cahaya akan menyebabkan terjadinya modifikasi (perubahan) substrat. Proses fotokatalisis ini terjadi dengan bantuan zat pengoksidasi seperti ozon dan hidrogen peroksida.
b. Fotokatalis Heterogen
Pada proses fotokatalisis heterogen, katalis tidak berada pada satu fasa dengan medium reaktan. Konsep degradasi fotokatalisis heterogen ini cukup sederhana, yaitu irradiasi padatan semikonduktor yang stabil untuk menstimulasi reaksi antar fasa permukaan padat atau larutan. Sesuai dengan definisi ini maka zat padatnya tidak berubah dan dapat diambil lagi setelah beberapa kali siklus reaksi redoks.
Proses awal fotokatalis heterogen pada semikonduktor adalah terbentuknya pasangan elektron-hole dalam partikel semikonduktor. Suatu semikonduktor menyerap energi yang sebanding atau lebih besar dari energi celahnya, maka elektron (e) pada pita valensi (valence band, vb)
16
meninggalkan lubang positif (hole, h+). Reaksi awal pada proses
fotokatalisis :
Semikonduktor + hv h+ vb + e- cd
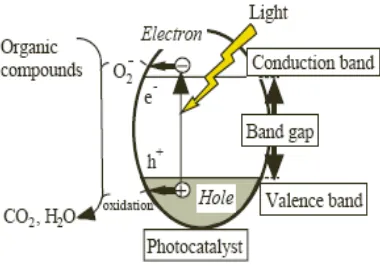
Skema proses fotokatalisis pada permukaan semikonduktor dijelaskan pada Gambar 5.
Gambar 5. Skema Proses Fotokatalis pada Permukaan Semikonduktor (Sumber : Eni Hartini, 2011).
Elektron pada pita konduksi akan mereduksi oksidan sedangkan
hole pada pita valensi akan mengalami reaksi oksidasi. Selain itu dapat
juga terjadi rekombinasi yaitu elektron dan lubang positif yang terbentuk tidak saling bereaksi dengan spesi lain tetapi bergabung kembali. Proses dapat terjadi di dalam semikonduktor dengan melepaskan panas.
Ketika semikonduktor disinari dengan cahaya yang memiliki energi E = hv setara atau melebihi dari energi celah pita, reaksi fotokatalitik heterogen akan terjadi. Semikonduktor membentuk sepasang lubang pita valensi ( VB) dan elektron pita konduksi (CB).
17
Secara umum lubang pita valensi mampu mengoksidasi substrat dan elektron pita konduksi mampu mereduksi substrat. Selanjutnya larutan yang mengandung spesi, misalnya OH- , H+ , O2- , H2O , H2O2 , O2
berinteraksi. Spesi-spesi tersebut juga mampu mengalami reaksi reduksi-oksidasi. Pembentukan anion radikal superoksida O2- dan OH radikal ditunjukkan pada reaksi sebagai berikut:
h+ (VB) + H
2O OHads + H+
h+ (VB) + OH-ads OH ads
e- (CB) + O2 O2
Keterangan “ads” merupakan spesi yang teradsorpsi pada
permukaan semikonduktor (Vora et al., 2009).
4. Zat Warna Congo red
Menurut Yahdiana (2011), zat warna azo umumnya mempunyai gugus auksokrom hidroksiamin dan gugus amino tersubtitusi. Zat warna azo adalah zat warna yang mempunyai gugus azo (-N=N-). Struktur umum dari zat warna azo yaitu R-N=N-R. Berdasarkan jumlah gugus azo yang terikat, maka struktur zat warna dapat dikelompokkan menjadi empat bagian, yaitu:
1. Moazo dengan satu gugus azo, (R-N=N-R)
2. Diazo dengan dua gugus azo, (R-N=N-R’-N=N-R”)
18
Senyawa congo red merupakan garam yang larut dalam air dan
disebut dengan nama asam benzidin diazo-bis-1-naftilamin-4-sulfonate.
Congo red berwarna merah dan sensitif terhadap asam. Congo red
digunakan sebagai indikator pada trayek pH : 3,0-6,2 dengan warna biru-ungu-merah. Senyawa ini akan menjadi biru dengan penambahan asam dan menjadi merah dengan penambahan basa.
Congo red merupakan zat warna langsung (direct dye) hasil
sintesis pertama yang sukses secara komersial karena kemampuannya dalam mewarnai katun (selulosa) dengan cara pencelupan yang sederhana.
Congo red disebut juga sebagai direct dye 28 yang merupakan turunan
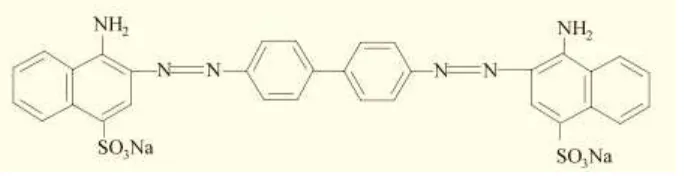
senyawa diazo yang disentesis pada tahun 1884 oleh Boettiger. Rumus bangun congo red tersaji pada Gambar 6.
Gambar 6. Struktur Kimia Congo red
(Sumber : Ni Luh Putu Widianti, James Sibarani & Manuntun Manurung, 2013)
Senyawa congo red memiliki berat molekul 696,68 g/mol dengan nama
IUPAC natrium difenildiazo-bis-α-naftilamin sulfonate. Rumus molekul
dari senyarwa congo red adalah C32H22N6Na2O6S2 dengan kelarutan dalam
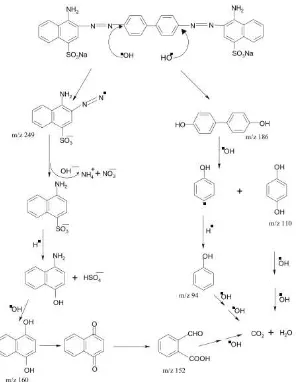
air mencapai 1g/30 mL. Mekanisme degradasi congo red berdasarkan
19
Gambar 7. Mekanisme Degradasi Congo red Berdasarkan Analsisis UV-
Vis dan GC-MS
(Sumber : Gomathi, Girish & Mohan, 2009).
Gomathi, Girish & Mohan (2009), melakukan penelitian terkait proses degradasi congo red dengan menggunakan hasil analsisis GC-MS.
Pada menit ke-50 spektra m/z menunjukkan intensitas 249, 253, 274 dan 186 yang menunjukkan terjadi pembelahan molekul congo. Intensitas 249 menunjukkan intermediat dari 4-amino, 3-azo napthalene sulphoric acid
dan intensitas 186 menunjukkan pembentukan intermediat 4,4, dihidroxy
20
dan 160 yang menunjukkan pembentukan intermediat quinol (1,4
dihydroxy benzene) dan 1,4 napthalene diol. Pengujian dilakukan pada 3,5
jam menunjukkan intensitas m/z pada 94 dan 152 yang menunjukkan pembentukan intermediat phenol dan 2-formylbenzoic acid. Pengujian
terakhir dilakukan pada 5 jam dan menunjukkan intensitas m/z yaitu 44 yang menunjukkan pembentukan CO2 dan menjadi proses akhir dari
degradasi congo red.
5. Spektroskopi Inframerah
Spektroskopi Inframerah merupakan suatu metode yang mengamati interaksi molekul dengan radiasi elektromagnetik. Penyerapan gelombang elektromagnetik dapat menyebabkan terjadinya eksitasi tingkat-tingkat energi dalam molekul berupa eksitasi elektronik, vibrasi atau rotasi. Pembagian daerah panjang gelombang sinar inframerah terbagi dalam daerah IR dekat (14290-4000 cm-1), IR jauh (700-200 cm-1) dan IR tengah (4000-666 cm-1). Spektroskopi Inframerah digunakan untuk mengidentifikasi senyawa, khususnya senyawa organik baik secara kualitatif maupun kuantitatif (Hardjono Sastrohamidjojo, 1992).
21
dengan gerakan ikatan. Hanya ikatan dengan momen dipol saja yang dapat menyerap radiasi inframerah (Hardjono Sastrohamidjojo, 2001).
Tidak ada dua molekul yang berbeda strukturnya akan mempunyai bentuk serapan inframerah yang tepat sama, karena tipe ikatan yang sama dalam dua senyawa berbeda terletak dalam lingkungan yang sedikit berbeda. Dua buah senyawa dapat diramalkan identik atau tidak dengan membandingkan spektrum inframerah dari kedua senyawa tersebut (Hardjono Sastrohamidjojo, 1992). Berdasarkan hasil spektra inframerah akan diperoleh informasi tentang pergeseran frekuensi getaran yang diakibatkan oleh kompleksasi ligan dan ada tidaknya pita-pita inframerah tertentu sehingga dapat digunakan untuk mengetahui informasi gugus khas suatu senyawa (Day & Selbin, 1985).
6. Difraksi Sinar-X (XRD)
Difraksi sinar-X (X-Ray Diffraction) merupakan salah satu metode
karakterisasi material kristalin untuk mengindentifikasi kristal dengan mengukur pola difraksi pada daerah sudut difraksi tertentu, yang dapat memberikan keterangan tentang struktur kristal secara spesifik (Klug & Alexander, 1962). Jumlah sampel minimal yang dibutuhkan untuk karakterisasi hanya beberapa milligram (Murthy & Reidinger, 1996).
22
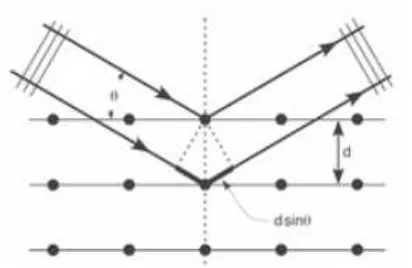
digunakan berupa radiasi sinar-X, elektron, dan neutron. Sinar-X yang terdifraksi oleh bidang permukaan sampel memiliki sudut refleksi yang sama dengan sudut sinar datang seperti yang ditunjukkan oleh Gambar 8. (West, 1989).
Gambar 8. Difraksi Sinar-X oleh Bidang Kristal
Gambar 8. menunjukkan sinar-X yang menumbuk suatu perangkat
bidang pada kisi dua dimensi. Berkas sudut difraksi (θ) tergantung pada
panjang gelombang (λ) berkas sinar-X dan jarak (d) antar bidang
(Smallman & Bishop, 2000). Sudut antara berkas sinar yang didifraksikan
dengan sinar ditransmisikan itu besarnya selalu 2θ. 2θ inilah yang terukur
oleh alat eksperimen difraksi sinar-X dan dikenal sebagai sudut difraksi. Pola difraksi sinar-X yang terjadi akan mengikuti hukum Bragg dengan persamaan: 2d sinθ = nλ.
23
Gambar 9. Contoh Puncak-puncak pada Difraktogram Hanya kristal yang berukuran besar dengan satu orientasi menghasilkan puncak difraksi yang mendekati sebuah garis vertikal. Lebar puncak difraksi tersebut memberikan informasi tentang ukuran kristal. Hubungan antara ukuran kristal dengan lebar puncak difraksi sinar-X dapat diproksimasi dengan persamaan Scherrer.
Dengan D merupakan ukuran kristal atau ukuran partikel (satuan:
nm), K merupakan konstanta material yang nilainya 0,9, λ merupakan
panjang gelombang sinar-X yang digunakan pada waktu pengukuran (nm),
β merupakan FWHM (Full Width at Half Maximum) puncak yang dipilih
(3 puncak utama) dan θ merupakan sudut difraksi berasal dari data grafik
2θ pada difraktogram. Analisis lebih lanjut dengan cara membandingkan
pola difraksi difraktogram dengan pola difraksi standar yang terdapat pada
24
7. Scanning Elektron Microscopy-Electron Dispersive X-Ray Analyser (SEM-EDX)
Analisis SEM digunakan untuk menentukan morfologi partikel (permukaan) dan ukuran partikel. Scanning Electron Microscopy (SEM)
adalah sebuah mikroskop elektron yang didesain untuk menyelidiki permukaan dari objek solid secara langsung. SEM memiliki perbesaran 10
– 3.000.000 kali, depth of field 4 – 0,4 mm dan resolusi sebesar 1 – 10 nm.
Kombinasi dari perbesaran yang tinggi, depth of field yang besar, resolusi
yang baik, kemampuan untuk mengetahui komposisi dan informasi kristalografi membuat SEM banyak digunakan untuk keperluan penelitian dan industri.
EDX menggunakan emisi spektrum sinar-X dari sampel yang ditembak dengan elektron yang terfokus untuk analisis kandungan kimianya. Analisis kuantitatif melibatkan identifikasi pada garis spektrum dari X-Ray dengan membandingkan setiap unsur pada sampel dengan unsur yang sama pada standar kalibrasi yang telah diketahui komposisinya (Goldstein, 2003). Kombinasi antara SEM dan EDX menghasilkan satu panel analitis sehingga mempermudah proses analisis.
25
ini dilakukan untuk melihat morfologi permukaan material dan mengetahui persentase komposisi suatu unsur atau senyawa dari material yang dianalisis, selain itu uji ini digunakan untuk mengetahui apakah partikel-partikel filler yang dikomposit telah tersebar merata di bagian permukaan serat.
8. Spektroskopi UV-Vis
Spektrofotometer UV-Vis merupakan alat yang digunakan untuk mengukur panjang gelombang dan intensitas penyerapan sinar-UV serta cahaya tampak. Eksitasi elektron dalam orbital molekul dari tingkat energi dasar ke tingkat energi yang lebih tinggi dapat terjadi akibat penyerapan sinar tampak atau ultraviolet oleh molekul tersebut. Hasil pengukuran UV-Vis berupa data hubungan antara panjang gelombang terhadap transmisi spektrum absorbansi dapat digunakan sebagai pengukuran awal untuk menentukan besarnya energi celah pita.
26
energi cahaya yang diberikan lebih besar maka elektron akan meloncat ke pita konduksi.
Material yang telah disintesis dapat diketahui besarnya energi celah pita dengan menggunakan metode spektrofotometri UV-Vis Diffuse
Reflectance. Energi celah pita diperoleh dengan mengubah besaran %R ke
dalam faktor Kubelka-Munk (F( R )), sesuai dengan rumus sebagai berikut:
Dimana, F( R ) adalah faktor Kubelka-Munk, K adalah koefisien
absorbansi, S merupakan koefisien scattering, dan R merupakan nilai
reflektansi. Energi celah pita diperoleh dari grafik hubungan antara hv (eV)
vs ( F ( R’∞)hv)1/2. Nilai hv (eV) ditentukan dengan persamaan berikut:
Dimana, Eg adalah energi celah pita (eV), h adalah tetapan Planck (6,624 x 10-34 Js), c adalah kecepatan cahaya di udara (2,998 x 108 m/s), dan λ adalah panjang gelombang (nm). Energi celah pita semikonduktor adalah besarnya hv pada saat (F (R’)hv)1/2 = 0, yang diperoleh dari
27 B. Penelitian yang Relevan
Penelitian tentang komposit ZnO-zeolit yang akan dilakukan didasarkan pada penelitian-penelitian sebelumnya.. Nevi Andari Dwi & Sri Wardhani (2014), telah melakukan penelitian tentang pengaruh konsentrasi dan pH metilen biru menggunakan fotokatalis TiO2-zeolit. Hasil penelitian
menunjukkan bahwa pada pH = 11 fotokatalis TiO2-zeolit bekerja secara
optimum. Sedangkan dari data konsentrasi menunjukkan bahwa semakin tinggi konsentrasi metilen biru yang digunakan kemampuan degradasi semakin menurun. Penelitian yang dilakukan menunjukkan penurunan konsentrasi metilen biru optimum pada konsentrasi 10 mg/mL. Data waktu kontak menunjukkan bahwa semakin lama waktu kontak semakin banyak zat warna metilen biru yang terdegradasi. Penelitian yang dilakukan menunjukkan bahwa waktu kontak optimum dicapai pada 50 menit.
28
besar. Pada waktu penyinaran 50 menit diperoleh persentase degradasi terbesar yaitu 88,49 % dengan penambahan hidorgen peroksida 0,4 mL.
29 C. Kerangka Berpikir
Limbah zat warna merupakan limbah yang dihasilkan dari proses pencelupan pada industri tekstil. Salah satu zat warna yang dapat berpotensi menjadi limbah zat warna adalah congo red. Limbah ini dapat menimbulkan
masalah yaitu kerusakan lingkungan. Oleh karena itu perlu mencari solusi yang tepat untuk menangani pencemaran lingkungan oleh limbah zat warna. Salah satu solusi yang pernah digunakan adalah menggunakan material penyerap atau pengadsorp dari zat warna tersebut adalah zeolit. Salah satu cara untuk mengurangi limbah zat warna tersebut adalah dengan menggunakan zat pengadsorpsi seperti zeolit. Namun zeolit saja masih belum efektif untuk mengurangi pencemaran zat warna tersebut. Oleh karena itu ditambahkan bahan yang mampu mendegradasi zat warna, seperti bahan semikonduktor. Salah satu contoh bahan semikonduktor adalah zink(II) oksida yaitu semikonduktor yang mempunyai energi celah pita sekitar 3,2 eV. Modifikasi zeolit dengan menyisipkan bahan semikonduktor ZnO diharapkan mampu mendegradasi zat warna congo red sehingga dapat mengurangi
30 BAB III
METODE PENELITIAN A. Subjek dan Objek Penelitian
1. Subjek Penelitian
Subjek dalam penelitian ini adalah komposit ZnO-Zeolit
2. Objek Penelitian
Objek dalam penelitian ini adalah karakter komposit ZnO-Zeolit dan aktivitas fotokatalitik komposit ZnO-Zeolit.
B. Variabel Penelitian 1. Variabel Bebas
Variabel bebas dalam penelitian ini adalah berat (gram) ZnO-zeolit, waktu penyinaran sinar tampak dan UV terhadap aktivitas fotodegradasi zat warna congo red
2. Variabel Terikat
Variabel terikat dalam penelitian ini adalah karakter yang meliputi gugus fungsional, ukuran dan morfologi partikel, komposisi unsur dalam senyawa, energi celah pita dan aktivitas fotokatalitik dari komposit ZnO-zeolit.
C. Alat dan Bahan Penelitian 1. Alat Penelitian
a. Alat-alat gelas dan ukur b. Heating dan magnetic stirrer
31
j. Fourirer Transform Infra Red (FTIR) Shimadzu IR Prestige-21 k. XRD Lab-X Type 6000 Shimadzu Japan
l. SEM-EDX JEOL JED-2300
m. UV-Vis 1700 Pharmaspec Spectrophotometer Specular Reflectance
32
alam dengan cara menghilangkan unsur-unsur pengotor dan menguapkan air yang terperangkap dalam pori kristal zeolit.
a. Aktivasi zeolit secara fisika
Aktivai zeolit secara fisika dengan cara mencampurkan sebanyak 1 : 3 zeolit alam dengan akuades kemudian diaduk selama 1 jam pada suhu 90oC. Selanjutnya campuran didekantasi untuk membuang pelarutnya kemudian dilakukan pengeringan pada suhu 120°C dalam oven, dan diakhiri dengan kalsinasi dalam tanur pada suhu 300°C selama 2 jam.
b. Aktivasi zeolit secara kimia dengan penyeragaman kation
Penyeragaman kation dilakukan dengan menambahkan larutan NaCl 1 M sebanyak 500 mL (perbandingan 2:1) ke dalam wadah yang berisi zeolit yang telah diaktivasi secara fisika dan mengaduknya selama 1 jam dengan magnetic stirrer pada suhu 80°C. Langkah selanjutnya endapan dipisahkan dan dikeringkan dalam oven 120°C. Langkah terakhir zeolit dikalsinasi pada suhu 300°C selama 2 jam.
2. Preparasi Larutan Congo red
a. Preparasi Larutan Congo red dan Penentuan Panjang Gelombang
Maksimum Congo red
Larutan stok congo red 1,0 x 10-3 M dibuat dengan cara
menimbang 0,179 gram congo red kemudian dilarutkan dengan
aquades di dalam labu ukur 250 mL. Larutan congo red 1,0 x 10-5 M
33
untuk diukur absorbanisnya menggunakan UV-Vis. Panjang gelombang maksimum didapatkan pada pengukuran 496 nm.
b. Membuat larutan standar congo red
Pembuatan larutan standar dilakukan melalui pengenceran larutan
congo red 10-3 M dengan variasi konsentrasi konsentrasi 1 x 10-5 M;
1,5 x 10-5 M; 2 x 10-5 M; 2,5 x 10-5 M; dan 3 x 10-5 M. Selanjutnya larutan standar diukur absorbansinya pada panjang gelombang maksimumnya.
3. Sintesis Komposit ZnO-Zeolit
Sintesis zeolit dilakukan dengan cara mencampurkan zeolit yang sudah diaktivasi, Zn(CH3COO)2 dan pelarut etanol, perbandingan
masing-masing komposisi 4:2:15. Kemudian campuran dipanaskan dan diaduk dengan heat dan magnetic stirrer pada suhu 50 °C selama 2 jam. Supaya
34 4. Uji Adsorpsi pada Keadaan Gelap
a. Sebanyak 10 ml larutan congo red dengan konsentrasi total yang
berbeda (1; 1,5; 2; 2,5; dan 3×10-5 mol/L) ditambahkan 0,2 gram ZnO-Zeolit.
b. Campuran diletakkan dalam tabung reaksi yang dibungkus dengan alumunium foil lalu diaduk dalam shaker selama 24 jam.
c. Campuran dipisahkan dengan sentrifuge. Filtrat diukur absorbansinya
35 E. Diagram Alir Penelitian
Diagram alir proses penelitian secara garis besar disajikan pada Gambar 11.
Gambar 10. Diagram Alir Proses Penelitian Preparasi dan Aktivasi Zeolit
Sintesis ZnO-Zeolit
Karakterisasi
- XRD
- FTIR
- UV-Vis Diffuse
Reflectance
- SEM-EDX
Pembuatan larutan standar congo red
UV-Vis
36 BAB IV
HASIL DAN PEMBAHASAN A. Pembuatan Komposit ZnO-Zeolit
Pembuatan komposit ZnO-Zeolit diawali dengan proses aktivasi dari material zeolit. Zeolit yang digunakan adalah jenis zeolit alam tipe klipnotiolit. Zeolit yang telah dihaluskan kemudian diaktivasi untuk mengurangi pengotor-pengotor yang menutupi pori dan rongga. Dengan demikian diharapkan luas permukaan zeolit tersebut akan semakin besar. Proses aktivasi ini dilakukan dengan cara fisika dan kimia. Tujuan dari proses fisika yaitu menghilangkan pengotor-pengotor yang bersifat fisik seperti pasir, tanah, dan lain sebagainya. Sedangkan proses kimia bertujuan untuk melarutkan pengotor yang bersifat asam maupun basa. Aktivasi secara kimia dilakukan dengan menggunakan larutan asam kuat encer dan basa kuat encer. Pengotor yang bersifat basa akan larut pada pencucian dengan larutan asam dan pengotor yang bersifat asam akan larut pada pencucian dengan larutan basa, dalam penelitian menggunakan larutan NaCl 1 M. Pada penelitian ini kation-kation yang terdapat pada zeolit digantikan dengan kation Na+, hal ini bertujuan untuk mempermudah pada saat proses pertukaran kation dengan Zn2+. Na-Zeolit dikalsinasi pada suhu
300 oC selama 2 jam. Pemanasan pada suhu tinggi akan menguraikan senyawa-senyawa organik yang terdapat dalam rongga, dan memperoleh rongga zeolit yang lebih terbuka.
37
berisi zeolit teraktivasi, kemudian dipanaskan dan diaduk pada 50°C selama 2 jam dengan sistem refluks, hal ini dilakukan supaya ion Zn2+ masuk ke dalam rongga-rongga atau pori-pori zeolit dan berikatan dengan zeolit. Supaya terbentuk komposit ZnO-zeolit, kemudian ditambahkan larutan NaOH 0,1 M kemudian diaduk selama 1jam. Penambahan NaOH dengan maksut supaya terjadi reaksi hidrolisis yang menghasilkan spesies Zn(OH)42- yang reaktif di
dalam zeolit, spesies ini akan menyebabkan terjadinya reaksi kondensasi, menghasilkan ikatan oksigen-logam, reaksinya adalah sebagai berikut,
Zn2+ + 4 OH-→ [Zn(OH)4]
2-zeolit + [Zn(OH)4]2-→ ZnO-zeolit + 2OH- + H2O
Setelah itu endapan ZnO-zeolit dipisahkan dari larutannya dan dilakukan pemanasan dalam oven pada suhu 120 °C dilanjutkan dengan
38
4000 – 400 cm-1 menggunakan spektrofotometer inframerah. Pelet KBr murni digunakan sebagai standar untuk setiap analisis. Hasil analisis spektroskopi inframerah dari zeolit, zeolit teraktivasi dan komposit ZnO-zeolit disajikan pada Gambar 11.
Gambar 11. Spektrum Inframerah Zeolit, Zeolit Aktivasi dan ZnO-zeolit Bilangan gelombang muncul sebagai puncak-puncak yang khas dengan nilai tertentu sehingga dapat dilakukan pembacaan atau interpretasi data. Hasil interpretasi FTIR dengan sampel zeolit, zeolit teraktivasi dan ZnO-zeolit disajikan pada Tabel 3.
Tabel 3. Hasil Interpretasi FTIR Sampel Zeolit, Zeolit Teraktivasi dan ZnO-zeolit
1050,46 1052,41 1079,16 Si-O-Si regangan
- - 468,24 Zn-O regangan
3469,97 3461,84 3470,22 O-H regangan
2338,93 2360,35 2328,39 Si-H regangan
1640,06 1636,27 1643,20 O-H tekuk
39
Tabel 3 menunjukkan hasil interpretasi dari sampel zeolit, zeolit aktivasi dan ZnO-zeolit. Ketiganya cenderung menghasilkan bilangan gelombang yang hampir sama dan tidak menunjukkan perbedaan hasil yang signifikan. Perbedaan hanya terlihat pada nilai persen tranmitansi dari masing-masing bialngan gelombang. Hal ini disebabkan oleh perlakuan sampel diantaranya dengan pemanasan, zeolit yang belum diaktivasi memberikan nilai tranmitansi lebih rendah dengan zeolit yang sudah diaktivasi. Hal ini menunjukkan bahwa radiasi sinar lebih banyak diteruskan oleh sampel zeolit yang sudah diaktivasi dibandingkan dengan zeolit biasa. Zeolit yang sudah diaktivasi memiliki struktur pori yang lebih banyak dibandingkan dengan zeolit biasa. Persen transmitansi terbesar ditunjukkan oleh sampel ZnO-zeolit.
Hasil karakterisasi dengan spektroskopi inftramerah terhadap sampel fotokatalis ZnO-zeolit, diketahui bahwa keberadaan ZnO dalam fotokatalis hasil sintesis dibuktikan dengan terbentuknya puncak karakteristik yang tajam pada bilangan gelombang 468,24 cm-1 (Purbo, 2012). Serapan kuat dan melebar yang terlihat pada bilangan gelombang 3470,22 cm-1 diidentifikasi sebagai vibrasi regangan O-H dari molekul
H2O yang terperangkap dalam kerangka zeolit karena memiliki sifat
higroskopis (Anwar, 2011). Sedangkan serapan yang muncul pada bilangan gelombang 1643,20 cm-1 menunjukkan vibrasi tekuk O-H dari molekul H2O. Serapan karakteristik zeolit muncul pada bilangan
gelombang 1079,16 cm-1 dan 790,34 cm-1 yang diidentifikasi merupakan
40 2. Difraksi sinar-X
Difraksi sinar-X (XRD) adalah salah satu karakterisasi yang digunakan untuk menganalisis struktur kristal. Analisis dilakukan dengan alat difraktometer sinar-X (XRD) Rigaku Miniflek 600 Benchtop dengan
range 2o sampai 90o, menggunakan radiasi CuKα sebesar 1,5406 Å,
tegangan 40 kW dan arus 15 mA. Gambar 12 memperlihatkan pola difraksi zeolit dan ZnO-zeolit.
Gambar 12. Pola Difraksi Zeolit dan ZnO-zeolit
Berdasarkan pola difraksi pada Gambar 12, puncak-puncak khas
zeolit yaitu pada sudut 2θ = 9,67° ; 11,05° ; 13,24° ; 15,12° ; 17,15° ;
19,42° ; 22,22° ; 25,4° ; 29,77° ; dan 35,42°. Hasil pencocokan nilai data
2θ zeolit dengan data JCPDS (Joint Comitte for Powder Diffraction
Standard) No. 39-1383 menggunakan software PCPDFWIN menunjukkan
41
zeolit yang digunakan pada penelitian ini adalah zeolit jenis Clinoptilolite
yang memiliki struktur moniklinik dengan beberapa titik kesamaan nilai 2θ
pada 9,87° ; 11,14° ; 13,05° ; 15,84° ; 17,3° ; 19,07° ; 22,34° ; 25,03° ; 29,77° dan 35,49°.
Komposit zeolit (clinoptilolite) dan ZnO menunjukkan puncak-puncak khas keduanya yaitu pada sudut 2θ = 9,75° ; 13,46° ; 21,69° ; 23,72° ; 25,62° ; 27,64° ; 31,82° ; 35,95° ; 56,71° ; 62,88° dan 68,30°. Pencocokan data komposit ZnO-zeolit dilakukan dengan data JCPDS dari zeolit (clinoptilolite) No. 39-1383 dan zink oxide (ZnO) No. 36-1451 menggunakan software PCDFWIN menunjukkan adanya beberapa titik
kesamaan nilai 2θ untuk zeolit yaitu pada 9,75° ; 13,46° ; 21,69° ; 23,72° ; 25,62° ; 27,64° dan ZnO pada 31,82° ; 35,95° ; 56,71° ; 62,88° dan 68,30°. Hal ini menunjukkan bahwa komposit ZnO-zeolit telah berhasil dipreparasi. Ukuran kristal dari zeolit aktivasi dengan komposit ZnO-zeolit dihitung dengan persamaan Scherrer sehingga didapatkan ukuran kristal
zeolit = 13,8 nm dan komposit ZnO-zeolit = 26,07 nm. Berdasarkan perhitungan tersebut ukuran kristal berukuran nanokristal karena berada pada rentang antara 10-200 nm.
3. Scanning Electron Microscopy-Electron Dispersive X-Ray Analyzer (SEM/EDX)
Analisis SEM digunakan untuk menentukan morfologi partikel (permukaan) dan ukuran partikel sedangkan hasil analisis EDX digunakan untuk menentukan komposisi senyawa dari suau sampel. Scanning
42
didesain untuk menyelidiki permukaan dari objek solid secara langsung. SEM memiliki perbesaran 10 – 3.000.000 kali, depth of field 4 -0, 4 mm
dan resolusi sebesar 1 – 10 nm. Hasil SEM dari komposit ZnO-zeolit dengan berbagai perbesaran disajikan pada Gambar 13.
Gambar 13. a. Hasil SEM Komposit ZnO-zeolit b. Perbesaran x2500 c. Perbesaran x10.000 d. Perbesaran x25.000
Analisis terhadap morfologi kompsosit ZnO-zeolit menunjukkan struktur yang menggumpal dengan permukaan gumpalan terdapat material berukuran kecil tersebar secara acak. Gumpalan tersebut diduga sebagai material zeolit dengan ukuran 4-13 mikrometer. Sedangkan material yang
a.
d. c.
43
tersebar secara acak di atas permukaan gumpalan diduga sebagail zink oksida (ZnO) dengan ukuran 0,31-0,35 mikrometer.
Analisi EDX komposit ZnO-zeolit menunjukkan persentase massa element O = 43,74%, Al = 5,12%, Si = 30,09%, dan Zn = 21,06%. Besar energy dispersi dari atom O = 0,525 keV, Al = 1,486 keV, Si = 1,739 keV, dan Zn = 1,012 keV. Data-data di atas membuktikan bahwa komposit ZnO-zeolit telah berhasil disintesis. Spektra EDX dari ZnO-zeolit disajikan pada Gambar 14.
Gambar 14. Spektra EDX dari Komposit ZnO-zeolit
4. Spektrofotometer UV-Vis
ZnO-44
zeolit yang telah dilarutkan dengan sedikit etanol pada kaca preparat. Kaca preparat yang telah berlapis sampel dipanaskan selama 30 menit dengan suhu 80°C untuk menguapkan etanol yang digunakan sebagai pelarut.
Sampel zeolit dan komposit ZnO-zeolit akan mengadsorpsi pada panjang gelombang tertentu. Pada penelitian ini pengukuran dilakukan pada panjnag gelombang 200-800 nm. Kisaran radiasi untuk UV adalah 180-380 nm sedangkan untuk visibel adalah 380-780 nm (Fessenden dan Fessenden, 1997). Dari data karakterisasi UV-Vis diperoleh data hasil absorbansi zeolit dan komposit ZnO-zeolit ditunjukkan oleh Gambar 15.
45
menunjukkan bahwa penambahan material ZnO dapat memperbaiki kualitas fotokatalis dari zeolit karena dapat memperbaiki kinerja dari daerah ultra violet ke daerah sinar tampak.
Energi celah pita merupakan besarnya energi yang digunakan untuk melepaskan elektron dari pita valensi ke pita konduksi. Energi celah pita mempengaruhi kemampuan fotokatalitik suatu katalis, sehingga sangat penting dilakukan pengukuran. Data reflektansi yang diperoleh dari pengukuran UV-Vis digunakan untuk menghitung energi celah pita (Eg) dengan menggunakan persamaan Kubelka-Munk. Perhitungan energi celah
pita pada sampel dengan menggunakan metode Kubelka-Munk diperoleh
dari hubungan antara eV dengan (F(R’∞ x hv)1/2 yang disajikan pada
Gambar 16.
Gambar 16. Perhitungan Band Gap dari a. Zeolit b. Komposit ZnO-zeolit
Dari perhitungan tersebut diperoleh besarnya energi celah pita pada material zeolit adalah 3.55 eV dan energi celah pita pada material
46
zeolit adalah 2.15 eV. Dapat disimpulkan bahwa penambahan material ZnO dapat menurukan besarnya energi celah pita.
C. Uji Aktivitas Fotokatalitik Kompsoit ZnO-zeolit
Pada penelitian ini dilakukan uji aktivitas material komposit ZnO-zeolit sebagai fotokatalis pada reaksi fotodegradasi pewarna congo red. Komposit
ZnO-zeolit yang telah berhasil dipreparasi dan dikarakterisasi menunjukkan nilai energi celah pita sebesar 2,15 eV. Hal ini menunjukkan bahwa komposit ZnO-zeolit dapat digunakan sebagai fotokatalis pada reaksi fotodegradasi.
1. Menentukan Kurva Standar Congo red
Pengukuran absorbansi larutan congo red dengan spektrofotometer
UV-Vis pada panjang gelombang maksimum yang telah diperoleh yaitu 496,8 nm dan digunakan sebagai kurva standar congo red yang ditunjukkan
pada Gambar 17.
47 2. Isoterm Adsorpsi Komposit ZnO-zeolit
Uji adsorpsi congo red dilakukan pada keadaan gelap, yaitu
keadaan dimana media yang digunakan tertutup sehingga tidak ada cahaya yang menginisiasi reaksi fotokatalitik, sehingga adsorpsi dapat berjalan secara natural. Proses adsorpsi menggunakan katalis ZnO-zeolit sebanyak 0,2 gram dan sebagai zat yang diadsorpsi adalah 10 mL larutan congo red
dengan variasi konsentrasi yaitu 1; 1,5; 2; 2,5; dan 3×10-5 mol/L. Adsorpsi
congo red oleh komposit ZnO-zeolit dilakukan selama 24 jam di dalam shaker dengan tujuan diperoleh keadaan setimbang dan tidak ada congo red
yang teradsorp oleh komposit dalam proses adosrpsi. Setelah itu, campuran larutan yang telah terdegradasi dipisahkan antara fasa cair dan endapannya dengan menggunakan sentrifuge dengan kecepatan 1000 rpm selama 15
menit sehingga endapan akan terendapkan semua dan mudah dipisahkan antara fasa cair dan endapannya. Filtrat dianalisis dengan Spectronic 20
dengan panjang gelombang maksimum 496 nm untuk mengatahui konsentrasi congo red setelah dilakukan adsorpsi dengan ZnO-zeolit.
Perubahan nilai absorbansi sebelum dan sesudah proses adsorpsi disajikan pada Tabel 4.
Tabel 4. Perubahan Nilai Absorbansi dari Proses Adsorpsi Konsentrasi Congo red Sebelum Sesudah
1,0 x 10-5 M 0,281 0,046
1,5 x 10-5 M 0,442 0,227
2,0 x 10-5 M 0,552 0,300
2,5 x 10-5 M 0,693 0,465
48
Pengujian pola isoterm adsorpsi yang sesuai untuk proses penyerapan larutan congo red oleh komposit ZnO-zeolit dilakukan dengan
perhitungan menggunakan persamaan Langmuir dan Freundlich. Uji persamaan Langmuir dilakukan dengan menggunakan persaamaan,
Sedangkan untuk uji persamaan Frendlich menurut I Nyoman Sukarta (2008), dilakukan dengan menggunakan persamaan,
49
Tabel 5. Perhitungan Harga x/m, Ce/(x/m), log Ce/(x/m) dan log Ce CC R awal
(M)
Ce (M) x/m (mol/gr)
Ce/(x/m) Log (x/m)
Log Ce
1,0x10-5 1,407x10-6 4,30x10-3 3,27x10-4 -2,36 -5,85 1,5x10-5 7,904x10-6 3,55x10-3 2,23x10-3 -2,45 -5,10 2,0x10-5 1,052x10-5 4,74x10-3 2,22x10-3 -2,32 -4,97
2,5x10-5 1,645x10-5 4,28x10-3 3,85x10-3 -2,36 -4,78 3,0x10-5 1,964x10-5 5,18x10-3 3,79x10-3 -2,28 -4,71
Persamaan Langmuir didapatkan dengan memplotkan harga Ce/(x/m) versus Ce dan Persamaan Freundlich didapatkan dengan memplotkan log (x/m) versus log Ce. Hasil pemetaan terlihat pada Gambar 18 dan Gambar 19.
50
Gambar 19. Grafik Persamaan Isoterm Freundlich
Pengujian persamaan adsorpsi Langmuir dan Freundlich dibuktikan dengan grafik linierisasi yang baik dan mempunyai harga koefisien determinasi R2 ≥ 0.9 (mendekati angka 1). Persamaan isoterm Langmuir bernilai y = 195,76x + 0,0003 sedangkan persamaan isoterm Freunlich bernilai y = 0,0433x – 2,139. Dari Gambar 19 dan Gambar 20 terlihat bahwa persamaan adsorpsi congo red oleh komposit ZnO-zeolit yang
memenuhi adalah persamaan adsorpsi Langmuir dengan R2 = 0,94 sedangkan pada persamaan isoterm Freundlich tidak memenuhi karena harga R2 = 0,1.
Isoterm Langmuir dibuat berdasarkan asumsi bahwa binding sites
terdistribusi secara homogen diseluruh permukaan adsorben, dimana adsorpsi terjadi pada satu lapisan (single layer) (Kunthi & Puspita, 2012).
51 BAB V
KESIMPULAN DAN SARAN
A. Kesimpulan
Berdasarkan penelitian yang telah dilakukan maka dapat disimpulkan :
1. Komposit ZnO-zeolit dapat disintesis dengan metode sol-gel menggunakan perkursor zeolit alam (clinoptilolite) dan
Zn(CH3COO)2.
2. Berdasarkan analisis XRD didapatkan bahwa ukuran kristal ZnO-zeolit adalah 26,07 nm. Spektra FTIR menunjukkan adanya serapan ZnO pada bilangan gelombang 468,24 cm-1. Analisis SEM material zeolit berukuran 4 -13 mikrometer. Sedangkan material Zink Oksida (ZnO) dengan ukuran 0,31-0,35 mikrometer. Analisis EDX komposit ZnO-zeolit menunjukkan persentase massa element Zn = 21.06%.. Analisis UV-Vis didapatkan energi celah pita komposit ZnO-zeolit adalah 2,15 eV.
52 B. Saran
Berdasarkan penelitian yang telah dilakukan, penulis memberikan saran sebagai berikut:
1. Perlu dilakukan variasi penambahan ZnO pada proses fotodegradasi
congo red dengan komposit ZnO-zeolit.
53
DAFTAR PUSTAKA
Anwar, D. I. (2011). Sintesis Komposit Fe-TiO2-SiO2 sebagai Fotokatalis pada
Degrasi Erionyl Yellow, Tesis. Fakultas Matematika dan Ilmu Pengetahuan
Alam Universitas Gajah Mada, Yogyakarta
Behnajady, M. A., Modirshahla, N., & Ghazalian, E. (2011). Synthesis of ZnO Nanoparticles at Different Conditions: A Comparasion of Photocatalytic Activity. Digest Journal of Nanomaterials And Biostructure Vol. 6, 1,
467-474.
Day, M.C., & Selbin, J. (1985). Kimia Anorganik Teori. Penerjemah: Wisnu
Susetyo.Yogyakarta: UGM Press.
Dewa Ayu Wismayanti., Ni Putu Diantariani & Sri Rahayu Santi . (2015). Pembuatan Komposit ZnO-Arang Aktif sebagai Fotokatalis untuk Mendegradasi Zat Warna Metilen Biru. Jurnal Kimia. ISSN 1907-9850
Djarwanto P.S. dan Pangestu Subagyo. (1993). Statistik Induktif. Yogyakarta:
BPFE.
Eni Hartini. (2011). Modifikasi Zeolit Alam dengan ZnO untuk degradasi fotokatalisis zat warna. Tesis. Depok: FMIPA. Universitas Indonesia.
Fessenden, R. J., & J. S. Fessenden. (1997). Kimia Organik Edisi Ketiga.
Penerjemah: A. H. Pudjaatmaka. Jakarta: Erlangga.
Garcia, Andreina & Juan Matos 2010. Photocatalytic Activity of TiO2 on
Activated Carbon Under Visible Light in The Photodegradation of Phenol.
The Open Materials Science Jurnal, 4.
Georgiev, D., Bogdanov, B., Angelova, K., Markovska, I., & Hristov, Y. (2009). Syntetic Zeolit-Structure Classification, Current Trends in Zeolit Synthetis.
International Science Conference. 7: 1.
Goldstein, Joseph. (2003). Scanning Electron Microscopy and X-Ray Microanalysis. The Journal of Scanning Microscopies. 27(4): 215-216.
Gomathy, L Devi., S. Girish Kumar & K. Mohan Reddy. (2009). Photo Fentin Like Process Fe3+/(NH4)2S208/UV for The Degradation of Di azo Dye Congo red Using Low Iron Concentration. Central Europen Journal of Chemistry: doi : 10.2478/s11532-009-0036-9.
Harben, P.W. & Kuzvart, M. (1996). Industrial Mineral: A Global Geology, Industrial Minerals Information Ltd. London : Metal Bulletin PLC. Hlm :
54
Hardjono Sastrohamidjojo. (1992). Spektroskopi Inframerah. Yogyakarta:
Liberty.
Hardjono Sastrohamidjojo. (2001). Spektroskopi. Yogyakarta: Liberty
Haslinda. (2009). Fabrication, Structural and Electrical Characteristic of Zinc Oxide (ZnO) Thin Films by Direct Current Sputtering. Thesis. Universiti
Sains Malaysia.
Hay, R.L. (1996). Zeolits and Zeolitic Reaction in Sedimentary Rocks. Journal Dept. Geology and Geophysics. University of California, Berkeley,
California.
Hongxia, Zhang, et al. (2007). Preparation of ZnO Nanorods Through Wet Chemical Method. Elsevier. Thesis. Herbin Engineering University.
I Nyoman Sukarta. (2008). Absorbsi Ion Cr3+ oleh Serbuk Gergaji Kayu Albizia. Sekolah Pasca Sarjana.IPB. Bogor.
Kabra, K., Chandhary, R dan Sawhney R.L. (2004). Treatment of Hazardous Organic and Inorganic Compounds Through Aqueous-Phase Photocatalysis:
A Riview. Ind. Eng. Chem. Res. No.24.Vol.43.7683-7696.
Khopkar, S. M. (2008). Konsep Dasar Kimia Analitik. Jakarta: UI Press.
Klug & Alexander. (1962). X-Ray Diffraction Procedures for Polycrystalline and Amorphous Materials. New York: John Wiley&Sons, Inc.
Kunthi & Puspita Kusmiyati A.L. (2012). Pemanfaatan Karbon Aktif Arang Batubara (KAAB) untuk Menurunkan Kadar Ion Logam Berat Cu2+dan Ag+ pada Limbah Cair Industri. Jurnal Reaktor. 14(1): 51-60.
M. Abdullah & Khairurijal. (2010). Karakterisasi Nanomaterial Teori, Penerapan, dan Pengolahan Data. Bandung: CV. Rezeki Putera Bandung
Maria Christina., Mu’nisatun., Rani Saptaaji & Djoko Marjanto. (2007). Studi
Pendahuluan Mengenai Degradasi Zat Warna Azo (Metil Orange) dalam Pelarut Air Meggunakan Mesin Berkas Elektron 350 Kev/10 Ma. Jurnal Forum Nuklir. No.1.Vol.1.31-44.
55
Methylene Blue dengan Menggunakan Fotokatalis ZnO-Zeolit. Kimia Student Journal. Vol. 2. No. 2, pp. 576-582. Universitas Brawijaya.
Murthy N., Sanjeva, & Reidinger, F. (1996). X-Ray Analysis, A Guide to Materials Characteritation and Chemical Analysis (2nded). New York:
VCH.
Nadhir Dicky Perdana., Sri Wardhani & Muhammad Misbah Khunur. (2014). Pengaruh Penambahan Hidrogen Peroksida (H2O2) terhadap Degradasi
Methylene Blue dengan Menggunakan Fotokatalis ZnO-Zeolit. Kimia Student Journal. Vol. 2. No. 2, pp. 576-582, Universitas Brawijaya
Nevi Andari Dwi dan Sri Wardhani. (2014). Fotokatalis TiO2-Zeolit untuk
Degradasi Metilen Biru. Jurnal. Jurusan Kimia FMIPA Universitas
Brawijaya.
Ni Luh Putu Widianti., James Sibarani & Manuntun Manurung. (2013). Studi Fotodegradasi Congo red Menggunakan UV/ZnO/Reagen Fenton. Jurnal Kimia. ISSN 1907-9850.
Nirmasari A.D., Widodo, D.S., & Haris, A. (2009). Pengaruh pH terhadap Elektrodekolorasasi Zat Warna Remazol Black B dengan Elektroda PbO2. Laporan Penelitian. Fakultas Matematika dan Ilmu Pengatuhuan Alam
Universitas Diponegoro: Semarang.
Ozgur, a b c., Alivov, Y. I., Liu, C., Take, A., Reshchikov, M.A., Dogan, S., Avrutin, V.,Cho, S.,J.et al. (2005). A Comprehensive Review of ZnO Materials and Device. Journal of Applied Physics 98:
041301.doi:10.1063/1.1992666.
Purbo, S. (2012). Sintesis dan Karakterisasi Nanopartikel-Nanofluida Undoped ZnO (Zink oksida) dengan Metode Kopresipitasi serta Aplikasinya pada Heat Pipe. Skripsi. FMIPA Universitas Indonesia, Depok.
Putri Dini., Eka Wahyu & Sri Wardhani. (2014). Degradasi metilen biru menggunakan fotokatalis ZnO-Zeolit. Universitas Brawijaya. FMIPA.
Chem. Prog. Vol. 7. No.1.
Rajic N., & V. Kaucic. (2002). I.T. Horvarth (Ed), Encyclopodia of Catalysis. John Wiley & Hoboken. Hlm : 189-236.
Romaida Hutabarat. (2012). Sintesis dan Karakterisk Fotokatalis Fe2+ -Zn Berabasis Zeolit Alam. Skripsi. Depok: Fakultas Teknik. Universitas