Atomic Absorption
Atomic Absorption
Spectroscopy (AAS)
Dr. WIDAYAT ST MT
JURUSAN TEKNIK KIMIA
FAKULTAS TEKNIK
UNIVERSITAS DIPONEGORO SEMARANG
2011
MATERI AAS
• OVERVIEW
• INSTRUMENTASI
• APLIKASI AAS
• APLIKASI AAS
Atomic Absorption Spectroscopy (AAS) adalah suatu teknik analisis untuk menetapkan konsentrasi suatu unsur (logam) dalam suatu sampel.
1800’s
: - Wallason mengobservasi pita hitam
Historis
1800 s
: Wallason mengobservasi pita hitam
dalam spektrum matahari.
- Fraunhofer merancang instrumen utk yg
k
00
i
merekam
±500 garis
absorpsi dalam spekturm sinar matahari
1860, 1861 :Kirchoff dan Bunsen membuat
,
spectrochemical analysis.
Kirchoff menerangkan pokok yang
mendasari hubungan antara emisi dan
mendasari hubungan antara emisi dan
absorpsi.
¾ 1950’s : AAS pertama kali dikembangkanoleh Sir
¾ 1950 s : AAS pertama kali dikembangkanoleh Sir
Alan Walsh
¾ 1960’s :
AAS
pertama kali
dikomersialkan oleh
Ferkin-Elmer; Beckman;
Jarrel-Ash
¾ 1970’s :
pengembangan & perbaikan graphite
furnace AAS
furnace AAS
¾ late 1970’s : Dikembangkan ICP Emission
Absorpsi Spektrometri Serapan Atom (AAS)
OVERVIEW
Teori
Spektrometri Serapan Atom (AAS = Absorption
spectrophotometry), merupakan salah satu cara
analisa yang dapat digunakan untuk menentukan
y
g
p
g
unsur-unsur dalam suatu bahan misalnya :
batu-batuan, tanah, tanaman, farmasi dan sebagainya
dengan hasil analisa yang peka dan sensitif.
Cara analisa ini berdasarkan pada proses
penyerapan energi radiasi dari sumber cahaya,
oleh atom-atom bebas dalam media pada tingkat
p
g
tenaga dasar (ground state).
Absorpsi Spektrometri Serapan Atom (AAS)
OVERVIEW
Teori
Pengurangan intensitas radiasi yang diberikan
sebanding dengan jumlah atom pada tingkat
tenaga dasar yang menyerap energi radiasi
g
y
g
y
p
g
tersebut. Dengan mengukur intensitas radiasi
yang diteruskan (transmitancy) atau mengukur
intensitas radiasi yang diserap (absorbancy),
k ko e t
i
d l
l
t
el
maka konsentrasi unsur dalam larutan sampel
dapat ditentukan.
Perkembangan terakhir cara analisa spektrometri
g
p
serapan atom ini, selama atomisasi dengan nyala
dapat pula dilakukan atomisasi tanpa nyala
(Flamless Atomizer), yaitu dengan menggunakan
energi listrik pada batang karbon (CRA = Carbon
energi listrik pada batang karbon (CRA = Carbon
Rod Atomizer), atau bahkan hanya dengan uapnya
saja misalnya pada analisis mercury (Hg).
OVERVIEW
Proses dalam AAS melibatkan 2 langkah, yaitu:
1 Atomisasi sampel
1. Atomisasi sampel
2. Absorpsi radiasi dari sumber sinar oleh atom
bebas.
bebas
• Sampel, biasanya berupa cairan atau padatan, terlebih
dahulu diubah menjadi atom, oleh perangkat atomisasi (berupa nyala atau tungku grafit).
• Selama proses absorpsi sinar UV-Vis, atom bebas akan
mengalami transisi elektronik dari ground state ke exited stated.
• Banyaknya atom yang mengalami transisi elektronik
bergantung pada temperatur, dirumuskan dengan Persamaan Boltzmann
OVERVIEW
Elements detectable by atomic
absorption are
highlighted in
pink
in this
periodic
OVERVIEW -
ABSORPSI vs EMISI
S ifi
Keuntungan
AAS
:
Specific Sensitivity
Low Cost Analysis Low Capital Cost (?)
Can Analyze Many Samples in Short Time for screening of a Single Analyte Metal.g g y
Kerugian
AAS
:
Single Element at a Time.
Requires more Set-up time between Elements. Not the preferred method for screening
Not the preferred method for screening samples for numerous elemental content
OVERVIEW -
ABSORPSI vs EMISI
Pengukuran spektroskopik secara umum dibedakan dalam 2 golongan : absorpsi dan emisi
i i l k ik j di bil l k b i d h
Transisi elektronik terjadi bila suatu elektron berpindah dari tingkat energi satu ke tingkat energi yang lain.
ABSORPSI
Jika elektron menyerap (mengabsorpsi) foton sehingga elektron berpindah dari orbital dengan tingkat energip g g g rendah ke tingkat energi tinggi.
OVERVIEW -
ABSORPSI vs EMISI
EMISI
Jika elektron berpindah dari tingkat energi tinggi kep g g gg tingkat energi rendah sehingga foton dipancarkan sebanding dengan perbedaan tingkat energi tsb.
OVERVIEW -
ABSORPSI vs EMISI
SPEKTRA EMISI ATOMIK
OVERVIEW
Peralatan AAS secara struktur dasar terbagi atas 4 bagian :
sumber cahaya (source) atomiser monokromator atau sumber cahaya (source), atomiser, monokromator atau filter, detektor dan penampilan data (readout).
Sumber cahaya adalah sebuah lampu katoda cekung
(Hollow Catode Lamp). Katoda lampu ini terbuat dari
( p) p
bahan yang aman dengan unsur yang akan ditetapkan dalam analisis, unutk menghasilkan emisi, katoda lampu ini diuapkan secara listrik.
At i d l h l t k b t l d
Atomiser adalah alat pengkabut sampel dan umumnya
alat ini digabungkan dengan arus gas ke flame (burner).
Monokhromator atau filter berfungsi untuk memilih
panjang gelombang yang akan diukur intensitasnya oleh panjang gelombang yang akan diukur intensitasnya oleh detektor. Panjang gelombang yang akan diukur ini
bersifat khas untuk sampel yang ditetapkan.
Detektor dan penampilan data : umumnya bekerja secara p p y j
INSTRUMENTASI
Detektor mengukur kekuatan sinar yang diteruskan dan Detektor mengukur kekuatan sinar yang diteruskan dan
penampilan data mungkin dalam bentuk absorbansi (cahaya yang diserap) atau transmittance (cahaya yang ditemukan). Mungkin juga langsung dalam bentuk konsentrasi (hanya pada alat-alat yang dilengkapi dengan sirkuit elektronis). Komponen-komponen ini dikontrol oleh piranti lunak komputer.
INSTRUMENTASI -
Source
Electrodeless Discharge Lamp (EDL)
• Untuk memperbaiki penentuan
absorpsi atom dengan menggunakan sumber yang lebih terang dan lebih stabil seperti EDL
Hollow Cathode Lamp (HCL)
stabil seperti EDL
• Dibutuhkan assesori power untuk
INSTRUMENTASI -
Source
Proses emisi pada Hollow Cathode Lamp Light Sources :
Light Sources : Light Sources : Light Sources :
•• Hollow cathode lamps Hollow cathode lamps -- HCLHCL
•• MultiMulti--element lampselement lamps Ult l
Ult l
•• Ultra lamps Ultra lamps
INSTRUMENTASI -
Source
Tungsten Anode Analyte Hollow Cathode
Quartz or Pyrex window Pyrex window Ne or Ar At 1 -5 torr Glass shield
INSTRUMENTASI –
Sample compartment
Atomization
Flame Electrothermal Graphite furnacep Hydride As, Sb, Sn, Se, Bi, and Pb
Cold vapor
Cold-vapor
Hg (ambient temperature vapor pressure)
• Elements to be analyzed needs to be in atomic state • Elements to be analyzed needs to be in atomic state
• Atomization is separation of particles into individual molecules and breaking molecules into atoms. This is done by exposing the analyte
h h fl h f
INSTRUMENTASI –
Sample compartment
Flame yang berbeda dapat diperoleh campuran gas tergantung pada temperatur dan kecepatan pembakaran yang diinginkan.
Beberapa unsur hanya dapat dirubah menjadi atom pada T tinggi. Bahkanp y p j p gg pada T tinggi jika terdapat ekses O2, beberapa logam membentuk oksida yang tidak terdissosiasi kembali menjati atom.
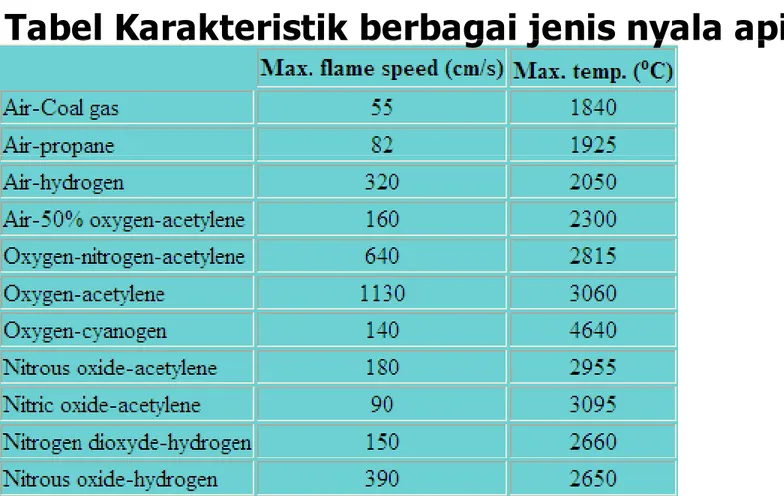
Untuk menghambat pembentukan oksida tersebut, kondisi flame mungking p , g dimodifikasi untuk mencapai pengurangan non-oxidizing flame.
Tabel Karakteristik berbagai jenis nyala api.
Tabel Karakteristik berbagai jenis nyala api.
INSTRUMENTASI –
Sample compartment
In AAS flame function as : (i) the sample holder
(ii) D l ti
(ii) Desolvation source (iii) A volatization source
FLAME ATOMIZATION
INSTRUMENTASI –
Sample compartment
N b li ti C i f th li id
FLAME ATOMIZATION
Nebulization : - Conversion of the liquid sample to a fine spray.
Desolvation : -Solid atoms are mixed with the gaseous fuel with the gaseous fuel. Volatilization : - Solid atoms
are converted to a vapor in the flame. There are three types of particles that exist in the flame:
t at e st t e a e 1) Atoms
2) Ions 3) M l l 3) Molecules
INSTRUMENTASI –
Sample compartment
The Flame process : “M
+”is a metal cation and “A
-” is the
FLAME ATOMIZATION
INSTRUMENTASI –
Sample compartment
FLAME ATOMIZATION
INSTRUMENTASI –
Sample compartment
Type Pneumatic Nebulizer :
FLAME ATOMIZATION a. Concentric b. Cross-flow c Fritted-disk c. Fritted-disk d. Barbington
Solvents yang umum
digunakan saat ini adalah
g
: 4-methyl-pentan-2-one
(MIBK), m-Xylene dan
cyclohexanone
cyclohexanone
FLAME ATOMIZATION
INSTRUMENTASI –
Sample compartment
Nebulizer
FLAME ATOMIZATION SAMPLE AEROSOLNebulizer
AEROSOLNebulizer : A device for converting
the solution into fine spray
or droplets
FLAME ATOMIZATION
INSTRUMENTASI –
Sample compartment
Primary zone = C2, CH and other radical emission
S d bl
Secondary zone = oxygen present so stable
moleculer oxides are
formed for metals
Interzonal zone = hot region, and widely used
ti f i
FLAME ATOMIZATION
INSTRUMENTASI –
Sample compartment
FLAME ATOMIZATION Fuel / Oxidant Temperature
acetylene / air 2100 °C – 2400 °C (most common) acetylene / air 2100 C 2400 C (most common)
acetylene / N2O2600 °C – 2800 °C acetylene / O2 3050 °C – 3150 °C • Pemilihan jenis nyala
bergantung pada temperatur penguapan atom yang
p g p y g
dianalisis.
• Parameter penting lain selain
temperatur adalah kecepatanp p
pembakaran (cm/s, or residence time)
ELECTROTHERMAL ATOMIZATION (ETA)
INSTRUMENTASI –
Sample compartment
Graphite Furnace
• Sampel cair dialirkan pada tabung silindris grafit yang ELECTROTHERMAL ATOMIZATION (ETA)
• Sampel cair dialirkan pada tabung silindris grafit yang
dilapisi bahan yang mencegah sampel terserap pada tabung.
Step Temperature Time
Drying 50° - 150°C ~ 60 s
Ashing 150° - 600°C ~ 60 s
Atomization 2000° - 3000°C ~ 5 s
Graphite Tube Furnace At i i l bih fi i
• Atomisasi lebih efisien
• Volume sampel lebih kecil
• Limits of detection lebih rendah • Limits of detection lebih rendah
INSTRUMENTASI –
Sample compartment
PERBANDINGAN FLAME DAN FURNACE AAS
Flame lebih sederhana
Furnace lebih sensitif
Furnace lebih sensitif
Furnace memiliki lebih banyak
interferensi
interferensi
Furnace lebih sedikit membutuhkan
l
sampel
PERBANDINGAN FLAME DAN FURNACE AAS
INSTRUMENTASI –
Sample compartment
Element
Element AAS FlameAAS Flame AAS ElectrothermalAAS Electrothermal
Al Al 3030 0.0050.005
Limit deteksi (ng/mL)
Accuracy Accuracy::
As As 100100 0.020.02 Ca Ca 11 0.020.02 Cd Cd 11 0.00010.0001–
Relative error of flame AA
is ~1–2%
–
Can be lowered with
Cr Cr 33 0.010.01 Cu Cu 22 0.0020.002 Fe Fe 55 0.0050.005
–
Can be lowered with
special precautions
–
Electrothermal
Hg Hg 500500 0.10.1 Mg Mg 0.10.1 0.000020.00002 Mn Mn 22 0.00020.0002 Mo Mo 3030 0 0050 005atomization has 5–10
times higher error than
than
flame AA
flame AA
Mo Mo 3030 0.0050.005 Na Na 22 0.00020.0002 Ni Ni 55 0.020.02 Pb Pb 1010 0.0020.002flame AA
flame AA
Sn Sn 2020 0.10.1 V V 2020 0.10.1 Zn Zn 22 0.000050.00005INSTRUMENTASI -
Wavelength
Dengan mengubah sudut grating akan menghasilkan
fokus pada panjang gelombang yang berbeda.
Fast Sequential Lamp Selection
High Speed High Speed High Speed High Speed High Speed Monochromator HC Lamps High Speed Monochromator HC Lamps High Speed Monochromator HC Lamps High Speed Monochromator HC Lamps Reference Beam D2 Lamp p Reference Beam D2 Lamp p Reference Beam D2 Lamp p Reference Beam D2 Lamp p Burner Motorised Mirror Burner Motorised Mirror Burner Motorised Mirror Burner Motorised Mirror Mirror Mirror Mirror MirrorINSTRUMENTASI -
Wavelength
Pemilihan panjang gelombang bergantung pada:
- Unsur yang dianalisis - Sensitivitas
INSTRUMENTASI -
Detector
INSTRUMENTASI -
Detector
Comparison of Techniques
ICP MS
ICP OES
FAAS
GFAAS
ICP-MS
ICP-OES
FAAS
GFAAS
Detection Limits Excellent good good Excellent Productivity Excellent very good good low LDR 108 105 103 102
Precision 1-3% 0.3-2% 0.1-1% 1-5% Spectral interference few common almost none very few
Chemical interference
moderate few many many
Ionization minimal minimal some minimal Mass Effects high on low mass none none none
Isotopes yes none none none
Dissolved solids 0 1-0 4% 2-25% 0 5-3% up to 20% Dissolved solids 0.1-0.4% 2-25% 0.5-3% up to 20% No. of elements 75 73 68 50 Sample usage low medium high very low
Semi-quantitative yes yes no no Isotope analysis yes no no no
Routine operation easy easy easy easy Method development skill req skill req easy skill req Running costs g highg high lowg medium Capital costs very high high low medium
INSTRUMENTASI
Preparasi Sampel
Timbang ± 2,5 g sampel, masukkan ke dalam gelas beker. Tambahkan 25 mL HNO3 pekat, tutup dengan
l l d d hk l k
gelas arloji, didihkan selama 30 – 45 menit untuk mengoksidasi senyawa organik. Dinginkan larutan secara perlahan, tambahkan 10 mL HClO4 70%. Didihkan kembali hingga larutan menjadi jernih
CARA BASAH
Didihkan kembali hingga larutan menjadi jernih.
Timbang ± 2,5 g sampel, masukkan ke dalam porselin. Panaskan dalam oven hingga suhu 550oC selama 4 jam
Panaskan dalam oven hingga suhu 550 C selama 4 jam. Dinginkan, tambahkan 10 mL HCl 3 N. Tutup dengan
gelas arloji, didihkan selama 10 menit. Dinginkan, saring dan masukkan ke dalam labu takar 100 mL,
CARA KERING
a g da a u a da a abu a a 00 ,
APLIKASI
Metode Seri Standar (Standar eksternal)
1. Ukur absorbansi dari seri larutan standar yang telah diketahui konsentrasinya.
2. Buat kurva hubungan antara absorbansi versus konsentrasi (Kurva Kalibrasi).
3. Dengan metode analisis regresi linier, turunkan persamaan regresi linier y = mx + c
persamaan regresi linier, y = mx + c
Hasil plotting ke persamaan regresi : Konsentrasi Cr = 3,45 ppm
APLIKASI
Metode Adisi Standar
Metode Adisi Standar
1. Siapkan dua buah larutan sampel yang identik. 2 Tambahkan sejumlah volume tertentu larutan 2. Tambahkan sejumlah volume tertentu larutan
standar pada salah satu larutan sampel. 3. Ukur absorbansi masing-masing larutan.
4. Hitung konsentrasi analit dengan persamaan berikut.
APLIKASI Kegunaan AAS :
1. Analisis Klinik 2. Analisis
Lingkungan
: Analisis logam dalam cairan biologis (darah, urine) : Monitoring lingkungan, memantau berbagai undur
di sungai, perairan laut, air minum, udara, minyak,
Lingkungan 3. Farmasi
di sungai, perairan laut, air minum, udara, minyak, dan minuman (anggur/wine, bir, jus buah)
: Dalam proses industri sering digunakan katalis (biasan a logam) ang seringkali 4 Industri
katalis (biasanya logam), yang seringkali terikut dalam produk akhir. Dengan AAS, unsur tsb dapat ditetapkan.
: Melakukan pengecekan apakah bahan 4. Industri
5. Pertambangan
: Melakukan pengecekan apakah bahan baku mengandung logam berat yang bersifat toksik.
: Menetapkan kandungan logam dalam : Menetapkan kandungan logam dalam batuan.
INTERFERENSI DALAM AAS
• Ada 2 jenis interferensi yang terjadi dalam AAS : A) Spectral Interferences
A) Spectral Interferences B) Chemical Interferences A.
A. Spectral Interferences Spectral Interferences
garis emisi dari spesies lain overlap/sangat dekat dengan
garis absorpsi analit, sehingga pemisahan dengan
monokromator sulit dilakukan
• Sources of Spectral Interference
monokromator sulit dilakukan.
1 Overlapping AA or AE lines 1. Overlapping AA or AE lines
• Jenis interferensi ini jarang terjadi.
• Selisih antar garis spektra harus < 0.01 nm utk bisa
g
p
menimbulkan interferensi ini.
INTERFERENSI DALAM AAS
2.
2. Background interference
• Disebabkan oleh scattering sumber sinar atau
adanya absorpsi molekular.
• Background interference menghasilkan
peningkatan sinyal output.
• Background correction digunakan untuk
li i
i i t f
i j
i i i
INTERFERENSI DALAM AAS
B.
B. Chemical interferencesChemical interferences
Hasil dari berbagai proses yang terjadi selama atomisasi yang mengubah karakteristik absorpsi analit
1. Pembentukan senyawa dengan volatilitas rendah yang mengubah karakteristik absorpsi analit.
• Anion yg terdapat dalam flame atau furnace dapat membentuk senyawa dengan volatilitas rendah dengan kation analit.
• metode yg biasa digunakan untuk mengatasi masalah ini adalah • metode yg biasa digunakan untuk mengatasi masalah ini adalah dengan menambahkan
release agents
atauprotective
agents
pada matriks sampel.Release Agent - bereaksi dengan zat yang menyebabkan interferensi dalam matriks sampel.
Protective Agent - bereaksi dengan analit tetapi menghasilkan Protective Agent bereaksi dengan analit tetapi menghasilkan
INTERFERENSI DALAM AAS
B.
B. Chemical interferencesChemical interferences 2. Kesetimbangan dissosiasi
• melibatkan pembentukan dan dissosiasi senyawa oksida logam dari sampel
dari sampel.
• Contoh: MO « M + O
M(OH)2 « M + 2OH
• Pergeseran kesetimbangan ke arah oksida logam akan
menghasilkan penurunan absorpsi radiasi oleh analit logam. • Proses ini sangat tergantung pada kondisi nyala (bahan bakar,
INTERFERENSI DALAM AAS
INTERFERENSI DALAM AAS
C.
C. Chemical interferencesChemical interferences
3. Ionisasi
b k l (k ) d l l
• Pembentukan ion logam (kation) dalam nyala.
• Ionisasi logam akan menyebabkan peningkatan temperatur.
• dapat diminimalkan dengan penambahan ionization suppressant pada matriks sampel yg akan menghasilkan konsentrasi elektron tinggi dalam nyala yg dapat menekan pembentukan ion logam tinggi dalam nyala yg dapat menekan pembentukan ion logam.
Mengendalikan interferences dalam GFAAS dengan :
1. Matrix modifiers
a NH4NO3 (helps minimize NaCl) Mg(NO3)2
a. NH4NO3 (helps minimize NaCl), Mg(NO3)2
b. Organic acids (e.g. ascorbic acid, oxalic acid): helps
make crystals smaller and more uniform; may help
reduce metal; other mysterious effects
reduce metal; other mysterious effects.
c. H3PO4, MgPO4
d. PdNO3
2. Matrix matching: make sure standards have same major
chemical composition as standards; compensate for
slight variability in major chemical composition.
3 M h d f
d d ddi i
if
d ' k
h
3. Method of standard additions: if you don't know what
the major element composition is and if it is highly
variable, then you should always use this method.
Reference
Reference
Beaty, R.D., Kerber, J.D., 2002, Concepts, Instrumentation and
techniques in Atomic Absorption Spectrophotometry,
PerkinElmer, Inc., Shelton, CT, USA.
Haswell S J 1991 Atomic Absorption Spectrometry; Theory
Haswell, S.J., 1991. Atomic Absorption Spectrometry; Theory,
Design and Applications. Elsevier, Amsterdam.
Moffet, J.H., February 2000. Why Calibration graphs curve in
atomic absorption spectrometry, Varian Australia Pty. Ltd.,
M l
Vi t i A t li
Mulgrave Victoria, Australia.
Reynolds, R.J. et al., 1970. Atomic Absorption Spectroscopy.
Barnes & Noble Inc., New York.
Skoog Holler and Nieman
Principles of Instrumental Analysis
Skoog, Holler and Nieman
Principles of Instrumental Analysis
Schrenk, W.G., 1975. Analytical Atomic Spectroscopy. Plenum
Press, New York.
Varma, A., 1985. Handbook of Atomic Absorption Analysis. Vol. I.
CRC P
B
R t
Gamma rays
Radio waves
Gamma rays
X rays
UV Infrared
Microwaves
Radio waves
1nm 100nm 1mm 1mVisible Region
600 650 750 560 500 430 500 560 600 650 750nm 430INSTRUMENTASI –
Sample compartment
FLAME
Flame AA hanya can only analyze solutions , where it
Flame AA hanya can only analyze solutions , where it
uses a slot type burner to increase the path length, and
therefore to increase the total absorbance.
Sample solutions are usually introduced into a nebuliser
by being sucked up a capillary tube. In the nebuliser the
sample is dispersed into tiny droplets, which can be
readily broken down in the flame.
The flame temperature is important because
it influences the distribution of atoms. It can
b
i
l
d b
id
d f
l
i
A Single-beam AA Spectrometer
A compesated single beam systems with source
A compesated single-beam systems with source
light directed through the sample path
A compesated double-beam systems with
Lamp for Services of Flame Atomic
Ab
ti
S
t
t
(FAAS)
Absorption Spectrometer (FAAS)
Single Lamp Multiple Lamp
El t L C t El t L C t
Element Lamp Current (mA)
Element Lamp Current (mA) Cu 3.0 Pb 5.0 Ca Fe 10.0 7.0 Mg Mn 3.0 5.0 Cd 3.0 Se Ti 10.0 18.0 Zn 5.0
Standard Analytical Data of The Elements
Standard Analytical Data of The Elements
Element Atomic Wt. Atomic Absorption Interference Lamp Current (mA) Flame Type (mA)
Cu 63.54 3.0 Air- C2H2 (oxidizing) Few interferences
Ca 40.08 10.0 N2O-C2H2 (oxidizing)
Strontium or Lanthanum 2,000-5,000 μg/ml
Fe 55.847 7.0 Air- C2H2 (oxidizing) H3PO4
Cd 112.40 3.0 Air- C2H2 (oxidizing) No major interferences
Pb 207.19 5.0 Air- C22H22 (oxidizing) 283.3 nm
Mg 24.312 3.0 Air- C2H2(oxidizing) Strontium or Lanthanum 2,000-5,000 μg/ml
Mn 54.938 5.0 Air- C2H2 (Stoichiometric)
N2O-C2H2 (Stoichiometric)
Se 78.96 10.0 N2O-C2H2 Hydride generation
Ti 47.90 18.0 N2O-C2H2 (reducing) KNO3 1,000-2,000μg/ml
Z 65 37 5 0 Ai C H ( idi i ) 213 9
Working Range and Sensitivity
Element Wavelength
(nm)
Slit width Working Range
(μg/ml) Sensitivity (μg/ml) Cu 324 7 0 5 0 0 5 0 025 Cu 324.7 327.4 217.9 222.6 0.5 0.5 0.2 1.0 0.0 – 5 0.0– 10 0.1 – 30 0.7 – 180 0.025 0.050 0.16 1.0 222.6 249.2 244.2 1.0 0.5 1.0 0.7 180 3.0 – 730 7.0 – 1700 1.0 4.0 9.0 Ca 422 7 0 5 1 – 4 0 0 02 Ca 422.7 239.9 0.5 0.5 1. 4.0 2.0 - 760 0.02 4.0 Fe 248.3 372 0 0.2 0 2 0.1 – 9.0 0 9 80 0 0.05 0 45 372.0 386.0 392.0 0.2 0.2 0.2 0.9 – 80.0 2.0 – 145.0 30 – 2700 0.45 0.80 15.0 Cd 228 8 0 5 0 0 1 8 0 009 Cd 228.8 326.1 0.5 0.5 0.0 – 1.8 3.0 – 800 0.009 4.0