i
LAPORAN AKHIR
PENELITIAN HIBAH BERSAING
PENGENDALIAN
Diaphorina citri
KUWAYAMA VEKTOR
PENYAKIT CVPD PADA TANAMAN JERUK DENGAN
CENDAWAN ENTOMOPATOGEN ISOLAT
LOKAL BENGKULU
Tahun ke 1 dari 3 tahun yang diusulkan
Oleh
Ir. Nadrawati, M.P. NIDN. 0012046011 (Ketua)
Sempurna Br Ginting, SP, M.Si. NIDN. 0023058204 (Anggota) Ir. Tri Sunardi, M.P. NIDN. 0028045603 (Anggota)
Dibiayai oleh :
Dana DIPA Universitas Bengkulu Tahun Anggaran 2014 Nomor: SP DIPA-23.04.2.415310/2014 Tanggal 5 Desember 2013
FAKULTAS PERTANIAN
UNIVERSITAS BENGKULU
iii RINGKASAN
Tanaman jeruk Rimau Gerga Lebong merupakan salah satu komoditas potensial desa Rimbo Pengadang, Kabupaten Lebong karena mampu meningkatkan penghasilan masyarakat. Produktivitas jeruk di Indonesia sampai saat ini masih rendah berkisar 8,6 – 15 ton/ha/tahun, sedangkan di daerah tropik lainnya mencapai 40 ton/ha (Ditlin, 1994). Produktivitas yang rendah tersebut disebabkan serangan Diaphorina citri Kuwayama (Homoptera: Psyllidae). D. citri merusak dengan mencucuk dan mengisap cairan sel pada tangkai daun, tunas-tunas muda atau jaringan tanaman lainnya yang masih muda sehingga daun jeruk mengkerut, menggulung dan pertumbuhannya menjadi terhambat. Pada serangannya berat, bagian tanaman yang terserang menjadi layu, kering dan kemudian mati. Upaya pengendalian D.citri yang dilakukan saat ini lebih dominan menggunakan pestisida kimia (informasi petani jeruk), kondisi ini menyebabkan matinya musuh alami dan mendorong terjadinya peledakkan populasi hama dan kerusakan lingkungan pada kurun waktu mendatang.
Cendawan entomopatogen adalah salah satu cara pengendalian yang berwawasan lingkungan yang saat ini sedang dikembangkan. Beberapa keunggulan lain dari cendawan tersebut adalah mudah dikembangkan dengan harga murah, efektif mengendalikan hama, dapat tersebar luas setelah bersporulasi pada inang sasaran dan dapat bertahan pada kondisi yang tidak menguntungkan. Cendawan entomopatogen dapat ditemukan di tanah maupun pada serangga sakit, dan di Bengkulu pencarian isolat dan pengujiannya pada serangga hama masih sangat terbatas dan khususnya pengujian pada D. citri belum pernah dilakukan, oleh karenanya perlu dilakukan koleksi cendawan entomopatogen dari tanah maupun serangga sakit khususnya disekitar pertanaman jeruk guna mendapatkan keragaman spesies dan isolat lokal yang efektif untuk mengendalikan serangga hama D. citri .
Langkah pencapaian tujuan tersebut mencakup eksplorasi, isolasi cendawan entomopatogen, melakukan identifikasi, skrining isolat yang ditemukan dan menguji patogenesitasnya dengan berbagai jumlah konidia pada D. citri di laboratorium.
Hasil pengujian diperoleh 8 jenis entomopatogen dari tanah dan serangga terinfeksi. Hasil pengujian seleksi cendawan entomopatogen terhadap seangga dewasa D. citri
diperoleh 4 isolat yang mematikan D. citri 50 persen atau lebih yaitu isolat Beauveria bassiana asal walang sangit Leptocorixa acuta Pondok Suguh, Metarrhizium anisopliae,
Verticillium lecanii asal tanah Rimbo Pegadang Lebong dan Metarrhizium spp. asal tanah Pasang Serai Bengkulu. Berdasarkan uji patogenesitas isolat terpilih didapatkan cendawan entomopatogen M. anisopliae dan B. bassiana dengan konsentrasi 1010 efektif mematikan nimfa D. citri 80-90% pada hari ke delapan setelah aplikasi, dengan LC 50 dan LC 80 M. anisopliae masing-masing 0,1 x 107 ; 0,1 x 1010 konidia/ml, dan B. bassiana 0,4 x 107 ; 0,8 x 1010 konidia/ml. Karakterisasi diameter koloni maupun daya kecambah untuk ketiga isolat yang diuji menunjukkan berbeda nyata, isolat dengan diamater koloni dan daya kecambah tertinggi terdapat pada M. anisopliae.
iv PRAKATA
Puji syukur kami panjatkan kehadirat Allah SWT karena atas izinnya-Nya laporan akhir kegiatan penelitian ini dapat diselesaikan. Kegiatan penelitian ini dilakukan di laboratorium Proteksi Tanaman Fakultas Pertanian Universitas Bengkulu. Tujuan kegiatan ini adalah untuk mendapatkan jenis entomopatogen yang efektif untuk mengendalikan
Diaphorina citri.
Dengan terselesaikannya laporan ini, kami selaku tim pelaksana penelitian menyampaikan banyak terima kasih kepada:
1. Direktorat Penelitian dan Pengabdian Kepada Masyarakat (DP2M) yang telah memberikan dana dalam penelitian Hibah Bersaing ini.
2. Lembaga Penelitian Universitas Bengkulu
3. Pihak – pihak yang telah banyak membantu dalam pelaksanaan kegiatan ini.
Kami sangat mengharap kegiatan penelitian ini dapat dilanjutkan sampain didapatkan entomopatogen yang efektif mengendalikan D. citri di lapangan.
Bengkulu, 10 Nopember 2014
v DAFTAR ISI HALAMAN JUDUL HALAMAN PENGESAHAN RINGKASAN PRAKATA DAFTAR ISI DAFTAR TABEL DAFTAR GAMBAR DAFTAR LAMPIRAN BAB 1. PENDAHULUAN BAB 2. TINJAUAN PUSTAKA
Cendawan entomopatogen Diaphorina citri
Gejala serangan D. citri
CVPD (Citrus Vein Floem Degeneration) Hasil Studi Pendahuluan
BAB 3. TUJUAN DAN MANFAAT BAB 4. METODE PENELITIAN
Eksplorasi/Koleksi Cendawan Entomopatogen Seleksi Isolat Entomopatogen
Uji Patogenesitas Entomopatogen pada D. citri
Uji Karakterisasi Cendwan Entomopatogen BAB 5. HASIL DAN PEMBAHASAN
BAB 6. RENCANA DAN TAHAP BERIKUTNYA BAB 7. KESIMPULAN DAN SARAN
DAFTAR PUSTAKA LAMPIRAN ... ... ... ... ... ... ... ... ... ... ... ... ... ... ... ... ... ... ... ... ... ... ... ... ... ... Halaman i ii iii iv v vi vii viii 1 3 3 4 5 6 7 8 9 9 9 10 11 12 19 20 21 23
vi DAFTAR TABEL
Tabel
1. Isolat cendawan entomopatogen asal Bengkulu 2. Rerata mortalitas nimfa D. citri setelah
diperlakukan dengan berbagai jenis dan konsentrasi cendawan entomopatogen 3. Karakterisasi fisiologi spesies cendawan
entomopatogen terpilih
4. Lethal concentration (LC) beberapa spesies cendawan entomopatogen terhadap nimfa D. citri
... ... ... ... Halaman 12 16 17 18
vii DAFTAR GAMBAR
Gambar
1. Gejala ulat hongkong terinfeksi cendawan entomopatogen
2. Koloni dan sel cendawan entomopatogen 3. Mortalitas D. citri setelah diperlakukan dengan
berbagai isolat cendawan entomopatogen 4. Gejala D. citri terinfeksi cendawan
entomopatogen
5. Sporulasi in vivo beberapa spesies cendawan entomopatogen pada tubuh nimfa setelah diinokulasi
6. Beberapa konidia cendawan entomopatogen yang sedang berkecambah ... ... ... ... ... ... Halaman 13 13 14 15 16 17
viii DAFTAR LAMPIRAN
Lampiran
Susunan Organisasi Tim Peneliti ...
Halaman 23
1 BAB 1. PENDAHULUAN
Latar Belakang
Tanaman jeruk Rimau Gerga Lebong merupakan salah satu komoditas potensial desa Rimbo Pengadang, Kecamatan Rimbo Pengadang, Kabupaten Lebong karena mampu meningkatkan penghasilan masyarakat. Jeruk Rimau Gerga berwarna kuning rasanya manis dan segar, buahnya cukup besar sehingga menjadikan jeruk ini sangat potensial untuk dikembangkan. Jeruk keprok ini dapat dijadikan salah satu produk unggulan hortikultura daerah maupun nasional. Pada tahun 2013 penambahan areal tanam seluas 500 ha (Supriyanto, 2013).
Produktivitas jeruk di Indonesia sampai saat ini masih rendah berkisar 8,6 – 15 ton/ha/tahun, sedangkan di daerah tropik lainnya mencapai 20 ton/ha, bahkan di daerah produsen utama jeruk dunia di daerah subtropik dapat mencapai 40 ton/ha (Ditlin, 1994). Produktivitas yang rendah itu antara lain disebabkan oleh adanya serangan Diaphorina citri
Kuwayama (Homoptera: Psyllidae). D. citri merupakan hama utama pada tanaman jeruk karena perannya sebagai vector penyakit CVPD (Citrus Vein Phloem Degeneration). CVPD disebabkan oleh bakteri Gram negatif Candidatus liberibacter asiaticus yang ditularkan serangga vektor Diaphorina citri dan melalui mata tempel pada pembibitan jeruk (Wirawan
et al., 2000). Di Indonesia serangan CVPD paling parah pernah terjadi di Sambas (Kalimantan Barat) dan Tejakula (Bali) pada tahun 1985 yang mengakibatkan terjadinya kematian ranting-ranting muda (Nurhadi et al.,1989). Serangan CVPD di Tulungagung sampai 62,34% dan di Bali Utara sampai 60% (Dwiastuti et al., 2003).
Upaya pengendalian D. citri yang dilakukan oleh petani sampai saat ini lebih dominan menggunakan pestisida kimia. Hal ini menyebabkan matinya musuh alami dan mendorong terjadinya kerusakan lingkungan serta peledakkan populasi hama pada kurun waktu mendatang. Berdasarkan undang-undang Republik Indonesia nomor 13 tahun 2010 pasal 32 menjelaskan bahwa pengendali OPT agar dilakukan dengan ramah lingkungan. Salah satu pengendalian hama yang ramah lingkungan dapat dilakukan dengan pengendalian hayati menggunakan cendawan entomopatogen.
Cendawan entomopatogen merupakan salah satu jenis agen hayati yang dapat digunakan untuk mengendalikan hama tanaman.Beberapa keuntungan yang dapat diperoleh dari pemanfaatan cendawan entomopatogen yakni mempunyai kapasitas reproduksi yang tinggi, siklus hidup yang pendek, dan dapat bertahan dalam kondisi yang tidak menguntungkan (Wahyono, 2006). Metarrhizium spp, Beauveria bassiana, Nomurae rileyi,
2
Hirsutella citiformis, Lecanicillium lecanii telah banyak diteliti dan dapat menimbulkan penyakit pada serangga hama. Metarrhizium spp yang diisolasi dari Spodoptera exempta
dapat mematikan S. litura 90% (Nadrawati, 2008); B. bassiana mampu membunuh kutu kebul Bemisia tabaci dengan mortalitas mencapai 50% pada kerapatan konidia 108/ml (Juniawan et al., 2013). Berikut L. lecanii dengan kerapatan konidia 107/ml matikan 100%
B. tabaci (Prayogo, 2012), dan H. citiformis dengan kerapatan konidia 108 konidia/ml dapat mematikan 50% imago D. citri pada waktu 11,72 hari (Dwiastuti dan Kurniawati, 2007). Berdasarkan hal tersebut perlu dilakukan eksplorasi cendawan entomopatogen guna mendapatkan keragaman spesies dan isolat lokal yang bisa diandalkan untuk mengendalikan
D. citri. Salah satu tolok ukurnya adalah mendapatkan cendawan yang mampu bersporulasi secara in vivo dan in vitro yang ditunjukkan dengan LC80 cendawan tersebut pada D. citri.
Hal ini dilakukan sehubungan dengan sifat spesifik cendawan entomopatogen terhadap inangnya dan potensinya untuk dapat diperbanyak secara massal dan dapat tersebar luas setelah bersporulasi pada inang sasaran.
3 BAB 2. TINJAUAN PUSTAKA
Cendawan Entomopatogen
Cendawan entomopatogen merupakan salah satu jenis agen hayati yang dapat digunakan untuk mengendalikan hama tanaman. Boucias dan Pendland (1998) mengemukakan, cendawan entomopatogen dicirikan oleh kemampuannya untuk menempel dan menembus kutikula inang dan dapat tumbuh ke bahagian internal inang (hemocoel) dan mengkonsumsinya sehingga nutrient di dalam hemolymph habis oleh pertumbuhan cendawan yang begitu cepat, ahirnya inang akan mati, di samping itu cendawan dapat menghancurkan jaringan lainnya atau dengan melepaskan zat beracun yang mengganggu perkembangan inang secara normal. Beberapa diantara zat beracun (toxin) yang dihasilkan cendawan yang dapat membunuh serangga adalah: beauvericin, bassianolide, cyclosporin A, tolypocladium, dan oosporein oleh B. bassiana; asam Oxalic oleh B. brongniartii; destruxins, cytochalasins, swainsonine oleh M. anisopliae, Keragaman intraspesies pada cendawan entomopatogen umum terlihat pada perbedaan virulensinya (Hajek & Leger, 1994), dan hal-hal yang mempengaruhi perbedaan intraspesies diantaranya adalah sumber isolat, inang dan faktor daerah geografis asal isolat (Beretta et al., 1998). Hal ini akan berakibat pada keragaman karakter di dalam spesies baik secara fisiologis maupun genetik. Secara umum dikemukakan bahwa strain dari spesies cendawan patogen yang diisolasi dari satu jenis inang lebih virulen untuk inang tersebut dari pada strain yang diisolasi dari inang yang lain.
Keefektifan cendawan emtomopatogen terhadap serangga hamajuga dipengaruhi oleh kerapatan konidia, umur dan stadia perkembangan inang serta waktu aplikasi (Prayogo, 2009). Salah satu faktor lain yang mempengaruhi keefektifan cendawan entomopatogen dalam mengendalikan hama adalah tingkat virulensi isolat. Virulensi antar isolat cendawan entomopatogen disebabkan karena adanya keragaman intraspesies. Hal ini disebabkan isolat yang diperoleh dari lokasi yang sama tetapi dari jenis serangga yang berbeda atau sebaliknya, yaitu isolat dari lokasi yang berbeda tetapi dari jenis serangga yang sama dimungkinkan memiliki karakter yang berbeda baik secara fisiologis maupun genetis.
Kesuksesan agens hayati seperti cendawan entomopatogen dalam mengendalikan hama harus mempunyai kemampuan untuk memproduksi inokulum dalam jumlah yang besar. Perbedaan media pertumbuhan yang digunakan untuk produksi massal tergantung pada kebutuhan nutrisi cendawan entomopatogen yang digunakan. Menurut Moore dan Prior (1993) karakteristik yang digunakan untuk produksi massal harus mempunyai sporulasi yang tinggi pada media buatan, virulensi yang tinggi dalam melawan organisme target, dan
4 kemampuan untuk bertahan pada lingkungan tempat hama tersebut berada. Indikator virulensi cendawan entomopatogen yang baik antara lain perkecambahan, pertumbuhan dan sporulasi yang tinggi.
Sumber nutrisi (media) berperan sebagai faktor yang menentukan bagi pertumbuhan dan virulensi cendawan entomopatogen. Nutrisi merupakan substansi yang digunakan sebagai biosintesis dan energi pembebasan yang menyajikan faktor utama dalam viabilitas, kelangsungan hidup, dan keberlanjutan organisme. Selain itu, pertumbuhan miselia dan spora pada media buatan tergantung pada isolat cendawan yang digunakan dan komponen yang digunakan dalam media. Pada umumnya, untuk menyelesaikan secara lengkap siklus hidup cendawan entomopatogen, maka kebanyakan patogen harus kontak dengan inangnya, masuk ke dalam tubuh inang, reproduksi di dalam jaringan inang dan mempunyai propagul untuk kontak dan menginfeksi inang baru.
Diaphorina citri
D. citri kutu loncat jeruk mempunyai tiga stadia hidup, yaitu serangga dewasa, telur, dan nimfa. Siklus hidupnya mulai dari telur sampai dewasa berlangsung antara 16- 18 hari pada kondisi panas, sedangkan pada kondisi dingin sampai 45 hari. Selama setahun serangga ini dapat mencapai 9 - 10 generasi.Stadium dewasa ditandai dengan terbentuknya sayap dan kutu ini dapat terbang atau meloncat.Warna kutu dewasanya coklat muda sampai coklat tua, matanya berwarna kelabu dan bercak-bercak coklat.Bagian abdomennya berwarna hijau terang kebiruan dan orange. Panjang tubuhnya sekitar 2,7– 3,3 mm. Ciri lainnya adalah pada saat makan, serangga ini posisinya menungging atau membentuk sudut 450 (Deptan. 2002).
Kopulasi segera berlangsung setelah serangga menjadi dewasa.Selanjutnya, serangga betina mencari ranting-ranting yang bertunas dan peletakan telurnya mulai berlangsung setelah 8 - 20 jam setelah kopulasi.Masa bertelur bervariasi yaitu antara 10 - 40 hari, sedangkan jumlah telurnya dapat mencapai 800 butir.Telur berbentuk lonjong dan agak menyerupai buah adpokat, warna kuning terang.Cara meletakkan telurnya tidak teratur, kadang-kadang berkelompok atau terpisah sendiri-sendiri. Bagian tanaman yang menjadi tempat meletakkan telur adalah tunas-tunas daun atau jaringan tanaman yang masih muda, seperti tangkai tunas dan permukaan daun bagian atas dan bawah yang belum membuka. Setelah 2- 3 hari telur menetas menjadi nimfa (Deptan. 2002).
Nimfa yang baru menetas hidup berkelompok pada jaringan tanaman muda dan mengisap cairan tanaman.Setelah nimfa berumur 2 - 3 hari, kemudian menyebar dan mencari makan pada daun-daun muda di sekitarnya.Periode nimfa berlangsung selama 12 - 17 hari
5 dan selama ini terjadi 5 kali pergantian kulit.Setelah pergantian kulit yang pertama nimfa bertambah aktif mencari makanan dan berpindah dari satu daun ke daun lainnya, dan nimfa tersebut merusak tanaman, bila dibandingkan dengan serangga dewasanya warna nimfa tersebut kuning sampai kuning kecoklatan. Kelima instar nimfa tersebut dapat dibedakan berdasarkan ukuran, bentuk awal perkembangan terbentuknya sayap dan penyusunan sklerit pada toraks bagian dorsal. D. citri tertarik pada tunas-tunas muda sebagai tempat peletakan telur, sehingga pertunasan tanaman merupakan faktor penting dalam perkembangbiakannya. Di Jawa Barat, tanaman jeruk bertunas 5 kali dalam setahun sehingga terdapat 5 periode kritis dimana D. citri mencapai jumlah yang sangat tinggi. Untuk mengetahui populasi D. citri
perlu diamati kuncup dan tunas (Deptan. 2002).
Telur pada pucuk Nimfa Nimfa instar 1 sampai 5
Buluh berlilin Kutu dewasa
Sumber:http://citrusbiosecurity.blogspot.com/2010/10/kutu-loncat-jeruk-asia-diaphorina-citri.html
Di Indonesia tersebar di Sumatera, Kalimantan, Jawa, Madura, Bali, dan Sulawesi. Hama ini juga diketahui telah menyebar di negara-negara Asia seperti Pakistan, India, Cina, Filipina, Jepang dan Amerika Selatan, Brazilia (Deptan. 2002)
Gejala Serangan Diaphorina citri
Kerusakan karena aktivitas D. citri adalah daun jeruk menjadi berkerut-kerut, menggulung atau kering, dan pertumbuhannya menjadi terhambat serta tidak sempurna.Selain daun yang masih muda, kutu ini dengan stiletnya menusuk dan menghisap cairan sel pada tangkai daun, tunas-tunas muda atau jaringan tanaman lainnya yang masih muda.Gejala lainnya adalah hasil sekresi alau kotorannya berupa benang yang berwarna putih dan bentuknya menyerupai spiral. Apabila serangannya berat, bagian tanaman yang terserang
6 menjadi layu, kering dan kemudian mati. Apabila hama ini menyerang satu tanaman dengan merata, maka pertumbuhan bunga menjadi terhambat dan produksi akan berkurang (Deptan. 2002).
CVPD (Citrus Vein Phloem Degeneration)
Bakteri patogen CVPD mempunyai bentuk pleomorpik (beberapa bentuk). Bentuk batang panjang berukuran 100-250 x 500-2.500 nm, berbentuk sperical (membulat) diameternya 700-800 nm. Bakteri ini tidak dapat dikulturkan. L. asiaticus hidup di dalam jaringan floem mengakibatkan sel-sel floem mengalami degenerasi sehingga menghambat tanaman menyerap nutrisi. Penyebaran ke bagian tanaman lain tergolong lambat, meskipun bakteri hidup dalam floem. Gejala baru terlihat 4-6 bulan setelah tanaman terinfeksi. Bahkan di lapangan gejala terlihat jelas setelah 1-3 tahun (Deptan, 2013).
Penyebaran CVPD antar daerah atau kebun (secara geografis) biasanya melalui mata-tempel atau bibit terinfeksi, sedangkan penyebaran di dalam kebun antar tanaman melalui serangga kutu loncat (Diaphorina citri) atau mata-tempel yang terinfeksi. Tipe hubungan patogen dalam tubuh serangga pembawa (vektor) bersifat persisten, sirkulatif dan non propagatif, artinya jika vektor CVPD telah mengandung L. asiaticus maka bila kondisinya ideal selama hidupnya akan terus mengandung bakteri, tetapi tidak diturunkan pada anaknya. Kutu loncat dapat menularkan CVPD pada tanaman sehat 168-360 jam setelah menghisap bakteri. Penularan melalui alat-alat pertanian terkontaminasi perlu diwaspadai seperti yang dilaporkan di Thailand. Sebaran geografis penyakit ini sangat luas terdapat pada hampir di semua sentra jeruk di Jawa, Bali, Sumatera, Sulawesi, dan NTB. Kalimantan yang selama ini bebas, mulai dicurigai tercemar juga. Penyakit ini ditemukan di daerah dengan ketinggian rendah (10 m dpl.) sampai ketinggian 1.000 m dpl. Sebagian besar varietas komersial peka terhadap penyakit ini kecuali varietas jeruk besar dan konde Purworejo bersifat toleran (Deptan, 2013).
Hasil Studi Pendahuluan
Hasil penelitian pendahuluan yang telah dilakukan di laboratorium Proteksi Tanaman Fakultas Pertanian Universitas Bengkulu memperlihatkan bahwa entomopatogen
Metarrhizium spp isolat lokal Bengkulu yang diperoleh dari serangga dapat mematikan 90%
S. litura (Nadrawati, 2008). Sementara hasil penelitian Sunardi dan Nadrawati (2008), penggunaan 200 g/l Metarrhizium pada media beras jagungdapat menekan populasi Plutella xylostella pada tanaman kubis, dan penelitian yang dilakukan oleh Ginting (2008),
7 penggunaan M. brunneum pada rayap Schedorhinotermes javanicus dengan kerapatan konidia 106 konidia/ml menyebabkan mortalitas 50%, sedangkan pada M. anisopliae hal tersebut terjadi pada kerapatan 5.106 konidia/ml dan B. bassiana pada kerapatan 107 konidia/ml.
Dari penelitian lain dilaporkan bahwa entomopatogen Nomurae rileyi dapat mematikan S. exigua pada tanaman bawang daun (Angraini, 2007), Dwiastuti dan Kurniawati (2007) melaporkan bahwa H. citiformis dengan konsentrasi 108 konidia/ml dapat mematikan 50% serangga uji D. citri dengan waktu 11,72 hari. Keterkaitan antar penelitian dapat dilihat pada diagram dibawah ini dan berdasarkan hasil penelitian di atas maka perlu dilakukan suatu penelitian yang komprehensif mengenai pengendalian D. citri pada tanaman jeruk dengan menggunakan cendawan entomopatogen khususnya isolat lokal Bengkulu yang berawasan lingkungan.
Informasi awal tentang penelitian cendawan entomopatogen yang sudah dilakukan:
Berdasarkan diagram diatas terlihat potensi penggunaan cendawan entomopatogen sebagai agen hayati pengendali hama, dan oleh karenanya perlu dilakukan sederan penelitian untuk memecahkan persoalan yang hama D. citri pada tanaman jeruk.
Riset Anggraini, 2007 (bimbingan Nadrawati). Patogenesitas Nomuraea rileyi pada S. exigua di laboratorium
Konsentrasi 10 10 per ml N. rileyi
mematikan 70 % S. exigua
Riset Nadrawati, 2008. Potensi
Metarrhizium pada S. litura
Metarrhizium spp yang diisolasi dari
S. exigua mematikan 90% S. litura
Riset Sunardi dan Nadrawati, 2008. Efektivitas Metarrhizium terhadap P. xylostella dan Crocidolomia
pavonana pada tanaman kubis
Metarrhizium dengan konsentrasi 200 g per liter efektif menurunkan
populasi P. xylostella
Riset Ginting, 2008. Patogenesitas beberapa isolat cendawan
entomopatogen pada rayap
Metarrhizium brunneum dan M. anisopliae lebih efektif dibandingkan
8 BAB 3. TUJUAN DAN MANFAAT
Tujuan
Adapun tujuan penelitian ini adalah:
1. Mendapatkan beberapa spesies dan isolat lokal cendawan entomopatogen di Bengkulu, dan memperbanyaknya pada medium beras jagung
2. Menguji spesies dan isolat tersebut pada D. citri di laboratorium 3. Menguji kemampuan daya kecambah cendawan entomopatogen
4. Mendapatkan spesies dan isolat lokal yang berdaya bunuh tinggi pada D. citri yang ditunjukkan dan mengetahui LC80.
Manfaat Penelitian
Manfaat penelitian antara lain menambah pengetahuan akan potensi entomopatogen isolat lokal Bengkulu yang berpeluang untuk dikembangkan sebagai kandidat agen pengendalian hayati yang bersifat ramah lingkungan, yang semuanya ini tidak terlepas dari pengelolaan ekosistem yang berwawasan lingkungan. Disamping itu diperoleh isolat lokal Bengkulu yang berpotensi untuk mengendalikan hama D. citri vektor CVPD, pengganti insektisida yang tidak berwawasan lingkungan.
9 BAB 4. METODE PENELITIAN
Penelitian dilaksanakan di Laboratorium Proteksi Tanaman Fakultas Pertanian Universitas Bengkulu. Khusus pengambilan sampel adalah sentra tanaman jeruk di Bengkulu. Pelaksanaan tahap-tahap penelitian adalah sebagai berikut:
Eksplorasi Jamur Entomopatogen.
Eksplorasi dilakukan dengan dua metode guna mendapatkan spesies cendawan entomopatogen. Pertama, menggunakan umpan serangga (insect bait method) seperti dilakukan Trizelia et al., (2011). Serangga umpan yang digunakan ialah larva Tenebrio monilitor Linn. (ulat Hongkong). Tanah yang digunakan untuk memerangkap cendawan entomopatogen diambil secara purposive sampling. Tanah diambil dari pertanaman jeruk petani. Tanah tersebut lalu digali sedalam 5-10 cm kemudian diambil sebanyak 1kg, lalu dimasukan kedalam kantung plastik diberi label berupa lokasi dan tanggal pengambilan sampel. Tanah kemudian diayak dengan ayakan dan dimasukan kedalam nampan plastik berukuran 35x28x7 cm2 dengan ketebalan tanah 5cm, setelah itu 50 ekor ulat hongkong masing-masing dimasukan kedalam nampan, tutup nampan dipasang kain puring putih yang telah dilembabkan. Tujuh hari kemudian ulat yang terinfeksi cendawan diisolasi di laboratorium pada laminar air flow yang telah disterilkan dengan alkohol 70%. Kedua mencari serangga terinfeksi cendawan di pertanaman jeruk petani dan sekitarnya. Serangga terinfeksi yang ditemukan dimasukan ke dalam cawan petri berdiameter 9 cm, yang telah dialasi dengan kertas saring, lalu ditutup rapat dan diproses lanjut di laboratorium.
Isolasi dan Identifikasi ulat hongkong yang terinfeksi cendawan permukaannya disterilkan dengan alkohol 70% selama tiga menit. Kemudian dibilas air steril sebanyak tiga kali dan dikeringanginkan diatas kertas saring steril. Lalu serangga tersebut diletakkan dalam cawan petri (diameter 9 cm) berisi tissue lembab steril dan diinkubasikan untuk merangsang tumbuhnya cendawan. Jamur yang keluar dari tubuh ulat bambu diambil dengan jarum inokulasi, dibiakan pada media PDA (Potato Dextrosa Agar) dan diinkubasikan selama enam hari pada suhu kamar. Cendawan tersebut diidentifikasi berdasarkan bentuk morfologinya, identifikasi menggunakan buku yang ditulis oleh Barnett (1962) dan jurnal terkait.
Seleksi Isolat Entomopatogen.
Cendawan entomopatogen yang telah ditemukan melalui eksplorasi, di isolasi dan identifikasi selanjutnya diseleksi. Seleksi dilakukan menggunakan serangga uji D.citri. Perbanyakan D. citri pada tanaman Muragaya (kemuning) dilakukan di rumah kasa.
10 Perbanyakan cendawan entomopatogen menggunakan media beras jagung. Setelah biakan isolat cendawan entomopatogen tersedia, lalu dilanjutkan dengan menyeleksi isolat cendawan tersebut. Seleksi isolat jamur entomopatogen ini dilakukan seperti metode Herlinda et al.,
(2008) dalam menyeleksi isolat-isolat B. bassiana pada walang sangit. Caranya ialah dengan menyemprotkan suspensi cendawan entomopatogen dengan kerapatan 108 konidia ml-1 pada serangga uji. D. citri diinfeskan 10 ekor ke tanaman kemuning dalam kurungan plastik berbentuk silinder (diameter 20 cm dan tinggi 30cm) yang bagian atasnya ditutupi kain kasa, setiap isolat cendawan entomopatogen disemprotkan ke serangga pada tanaman tersebut. Percobaan diulang tiga kali. Setiap 24 jam selama delapan hari dicatat jumlah serangga yang mati, sedangkan jumlah serangga yang tersisa juga dicatat. Cendawan entomopatogen yang paling efektif untuk D. citri dicirikan atas paling tingginya mortalitas D. citri tersebut.
Isolat yang bisa mematikan 50% serangga D. citri akan dilakukan uji patogenesitasnya pada D. citri tersebut, termasuk uji daya kecambah konidia, dan diameter koloni.
Uji patogenitas cendawan entomopatogen pada D. citri
Pengujian dilakukan terhadap nimfa instar 3-4 dengan menggunakan rancangan acak lengkap 2 faktor. Faktor pertama adalah jenis isolat/spesies, dan faktor kedua adalah jumlah konsentrasi konidia cendawan entomopatogen. Adapaun konsentrasi perlakukan adalah 1010 , 109 , dan 108 konidia/ml, dengan 3 ulangan. Pada setiap unit percobaan sebanyak 30 ekor nimfa yang sudah diinfeskan pada tanaman kemuning dalam polibag disemprot sesuai dengan konsentrasi perlakuan kemudian di kurung dengan kurungan plastik dan diatasnya bertutup kain kasa. Mortalitas dihitung setiap hari selama 8 hari setelah penyemprotan.
Data mortalitas diolah dengan sidik ragam dan kalau terdapat perbedaan yang nyata antar perlakuan maka dilanjutkan dengan uji DMRT 5%.
Persentase mortalitas larva dihitung dengan menggunakan rumus : M = A / B x 100 %
Keterangan :
M = Persentase mortalitas
A = Jumlah serangga yang mati terinfeksi cendawan B = Jumlah serangga yang diuji
Untuk menentukan patogenesitas cendawan entomopatogen dengan konsentrasi dan waktu lethal 50 dan 80% (LC50 dan LC80) dari masing-masing isolat maka data diolah dengan menggunakan analisis probit.
11 Uji Karakterisasi Fisiologi Cendawan Entomopatogen in Vitro
Uji karakterisasi cendawan entomopatogen dilakukan dengan mengamati daya kecambah konidia dan diameter koloni cendawan entomopatogen yang mematikan 50 % serangga D. citri.
Uji Daya kecambah konidia
Pengamatan daya kecambah dihitung dengan cara mengambil satu tetes suspensi dari setiap perlakuan konsentrasi dan diletakkan di atas objek gelas steril dan ditutup dengan cover glass, kemudian dimasukkan kedalam cawan petri yang telah berisi kertas saring lembab dan diinkubasi pada suhu 24 0C selama 12 - 24 jam. Masing-masing perlakuan diulang 4 kali. Pengamatan dilakukan dibawah mikroskop dengan perbesaran 400 kali, persentase konidia yang berkecambah dihitung dari 100 konidia. Konidia dinyatakan telah berkecambah apabila tabung kecambah (germ tubes) telah muncul lebih panjang dari diameter konidia.
Uji Diameter koloni
Media PDA yang telah ditumbuhi mycelium masing-masing isolat berumur 5 hari ditumbuhkan pada media PDA lainnya di dalam cawan petri dan diinkubasi dalam inkubator dengan suhu 24 0C. Diameter koloni dari masing-masing isolat diukur setiap 3 hari sampai hari ke 15.
12 BAB 5. HASIL DAN PEMBAHASAN
Isolat Jamur Entomopatogen.
Eksplorasi jamur entomopatogen yang telah dilakukan ditemukan 8 isolat cendawan entomopatogen di sentra produksi jeruk kecamatan Rimbo Pegadang, Kampung Melayu Padang Serai, Pondok Suguh (Tabel 1). Hasil penelitian menunjukkan metode eksplorasi dengan umpan serangga lebih efektif, karena sebagian besar B. bassiana dan M. anisopliae
yang diidentifikasi adalah dengan metode umpan serangga. Hal ini karena tanah merupakan habitat utama bagi cendawan entomopatogen dan sumber infeksi bagi serangga dilapangan sebagai faktor mortalitas hama secara alami (Deciyanto & Indrayani, 2008; Nuraida & Hasyim, 2009). Pada umpan serangga yang terserang B. bassiana tampak tubuh serangga mengeras, dan juga terdapat kelompok spora yang berwarna putih. Warna koloni semua isolat B. bassiana secara makroskopis adalah putih, sedangkan secara mikroskopis konidia berwarna hialin, berbentuk bundar dan terdiri dari satu sel basal yang sering mengembung, menghasilkan kuntum konidia berkelompok atau zigzag. Suharto et al., (1998) yang menyatakan spora B. bassiana berbentuk bulat, bersel satu, hialin dan terbentuk secara tunggal pada sterigma yang pendek. Sedangkan warna semua isolat M. anisopliae secara makroskopis di awal pertumbuhan berwarna putih, kemudian berubah warna menjadi hijau gelap. V. lecani dan Hirsutella ditandai dengan koloni berwarna putih, secara mikroskopis spora hialin, berbentuk silindris dan membentuk rantai. V. Lecanii pialit tunggal muncul pada konidiofora dengan posisi tegak dan sedikit berbeda dengan kedudukan hifa. Konidia di ujung aatau paralel berkelompok, silinder, ujung membulat atau berbentuk ellips (Gambar 1, 2). Hal ini diperjelas oleh Barnett (1962) yang menyatakan spora M. anisopliae bersel satu, hialin, dan berbentuk bulat silinder.
Tabel 1. Isolat cendawan entomopatogen asal Bengkulu
Isolat Inang Asal kecamatan Metode Eksplorasi
M. anisopliae 1 Tenebrio molitor Rimbo Pegadang Umpan serangga
B. bassiana 1 Tenebrio molitor Rimbo Pegadang Umpan serangga
Verticilium lecanii
Tenebrio molitor Rimbo Pegadang Umpan serangga
Metarrhizium spp Tenebrio molitor Padang Serai Umpan serangga
B. bassiana 2 Leptocorixa acuta Pondok Suguh Umpan serangga
B. bassiana 3 Tenebrio molitor Padang Serai Umpan serangga
M. anisopliae 2 Tenebrio molitor Pondok Suguh Umpan serangga
Hirsutella citriformis
13
B. bassiana V.lecanii M.anisopliae H. citriformis
Gambar 1. Gejala ulat hongkong terinfeksi cendawan entomopatogen
H. citriformis V. lecanii M. anisopliae B. bassiana
Konidia V. lecanii Konidia B. bassiana
Konidia M. anisopliae
Gambar 2. Koloni dan sel cendawan entomopatogen
Seleksi Cendawan entomopatogen Terhadap D. citri.
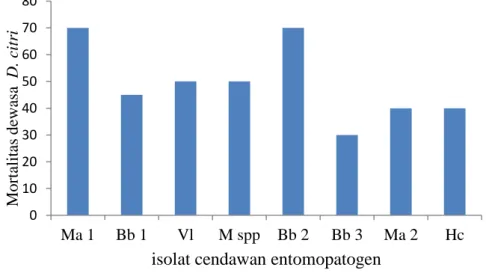
Hasil pelepasan dewasa D. citri dalam kurungan kasa yang diaplikasikan dengan beberapa jenis isolat cendawan menunjukkan bahwa kematian ditemukan pada semua perlakuan. Kematian D. citri pada semua perlakuan terjadi pada hari keempat setelah diaplikasikan dan mencapai puncak kematian pada hari ke delapan. Data mortalitas D. citri
pada masing-masing cendawan secara rinci dapat diikuti pada Gambar 3.
Pada inokulasi langsung terhadap serangga uji, konidia lebih cepat menempel dan berkecambah pada tubuh larva pada lipatan antar ruas tubuh serangga. Semakin banyak jumlah konidia yang menempel pada tubuh serangga, maka mortalitas akan semakin cepat apa lagi didukung dengan kondisi temperatur dan kelembaban yang sesuai dengan yang diinginkan cendawan entomopatogen. Banyaknya jumlah konidia jamur entomopatogen berhubungan dengan tingkat konsentrasi yang digunakan, karena semakin tinggi konsentrasi maka jumlah konidia semaki tinggi, dan mortalitas juga akan semakin tinggi (Hasyim dan
14 Azwana, 2007). Tabel 2, menunjukkan bahwa isolat M. anisopliae, B. bassiana, dan V. lecanii digolongkan ke dalam cendawan yang berpotensi untuk mengendalikan hama D. citri karena mampu mematikan serangga tersebut dirumah kasa sampai diatas 50%. Kematian tertinggi didapatkan dengan perlakuan M. anisopliae asal Rimbo Pegadang Lebong dan B. bassiana asal L. acuta. Hal ini dimungkinkan B. bassiana memproduksi toksin Beauvericin yang mengakibatkan gangguan pada fungsi hemolimfa, gangguan inti sel serangga inang dan hilang kesadaran serta kerusakan jaringan tubuh secara menyeluruh (Deciyanto & Indrayani, 2008). Dan M. anisopliae memproduksi cyclopeptida, destrtuxin A, B, C, D, E dan. Destruxin berpengaruh pada organela sel target (mitokondria, reticulum, endoplasma dan membran nukleus) menyebabkan paralisis sel dan kelainan fungsi lambung tengah, tubulus malphigi, hemocyt dan jaringan otot (Widiyanti dan Mulyadihardja, 2004).
Keterangan: Ma1 = isolat M. anisopliae asal tanah Rimbo Pegadang, Bb1 = B. bassiana asal tanah Rimbo Pegadang, Vl = V. lecanii asal tanah Rimbo Pegadang, M spp = asal walang sangit Pondok Suguh, Bb3 = B bassiana asal tanah Padang Serai, Ma2 = M anisopliae asal tanah Pondok Suguk dan Hc = H. citriformis asal ngengat Padang serai
Gambar 3. Mortalitas D. citri setelah diperlakukan dengan berbagai isolat cendawan entomopatogen
Isolat cendawan Verticillium lecanii yang diperoleh dari Rimbo Pegadang Lebong mampu menyebabkan mortalitas D. citri 50%. Menurut Prayogo dan Suhardono (2005), cendawan V. lecanii merupakan salah satu jenis cendawan yang dikatakan paling efektif untuk mengendalikan hama pengisap polong kedelai. Keefektifan terlihat dari mortalitas imago R. linearis hingga mencapai 81%. Keefektifan cendawan juga terlihat dari kerusakan polong yang setara dengan akibat aplikasi insektisida deltametrin. Dan beberapa serangga dewasa D. citri yang terinfeksi cendawan hasil pengujian dapat dilihat pada Gambar 4.
0 10 20 30 40 50 60 70 80 Ma 1 Bb 1 Vl M spp Bb 2 Bb 3 Ma 2 Hc Mor tal it as dewasa D . ci tri
15
B. bassiana adalah cendawan mikroskopik dengan tubuh berbentuk benang-benang halus (hifa). Kemudian hifa-hifa membentuk koloni yang disebut miselia. Cendawan ini tidak dapat memproduksi makanannya sendiri, oleh karena itu ia bersifat parasit terhadap serangga inangnya. Cendawan B. bassiana menyerang banyak jenis serangga, diantaranya kumbang, ngengat, ulat, kepik dan belalang. Cendawan ini umumnya ditemukan pada serangga yang hidup di dalam tanah, tetapi juga mampu menyerang serangga pada tanaman atau pohon.
D. citri yang terinfeksi jamur patogenik menyebabkan serangga kurang aktif, terjadi perubahan warna tubuh, integumen menjadi sedikit mengkerut. Herlinda et al. (2005) melaporkan bahwa gejala yang muncul pada D. citri terinfeksi cendawan patogenik adalah warna tubuh berubah dari hijau menjadi hijau kekuningan.
Metarrhizium Verticilium Beauveria
Gambar 4. Gejala D. citri terinfeksi cendawan entomopatogen
Uji Patogenesitas Cendawan Entomopatogen pada Nimfa D. citri
Berdasarkan seleksi cendawan entomopatogen pada D. citri diperoleh 3 jenis cendawan terpilih M. anisoplie, B. bassiana dan V. lecanii. Cendawan terpilih tersebut diuji patogenesitasnya pada nimfa D. citri instar 3-4 (Tabel 2).
Setiap spesies cendawan yang diuji pada penelitian ini, tingkat kerapatan konidia memperlihatkan reaksi yang nyata terhadap mortalitas nimfa D. citri. Secara umum terdapat korelasi antara tingkat kerapatan konidia dengan mortalitas, semakin tinggi tingkat kerapatan yang diperlakukan juga menunjukkan tingkat mortalitas nimfa D. citri yang tinggi, cendawan
M. anisopliae dan B. Bassiana dengan konsentrasi 108 -1010 konidia/ml mematikan >70% nimfa D. citri (Tabel 2). Dalam hal ini diperkirakan semakin tinggi kerapatan yang diaplikasikan pada nimfa, memunkinkan kontak konidia dengan tubuh nimfa dalam jumlah yang lebih banyak. Keadaan ini memberi peluang yang lebih baik bagi konidia untuk berkecambah dan menembus tubuh nimfa D. citri, kecuali perlakuan dengan V. lecanii. Disamping toksin yang dihasilkan oleh M. anisoplie seperti destruksin A, B, dan E yang
16 membunuh nimfa dengan meransang atau memacu terjadinya kemerosotan jaringan serangga sehingga kehilangan keutuhan struktur membrane dan pada akhirnya terjadi dehidrasi sel. Dan dimunkinkan juga terjadi peyumbatan spirakel yang dapat menyebabkan kematian sebelum serangan pada hemocoel. Sementara B. bassiana mengandung toksin beauverisin, beauverolit, isorolit dan asam oksalat. Menurut Soetopo dan Indrayani (2007), bahwa B. basiana menghasilkan toksin beauvericin yang dapat menyebabkan kerusakan jaringan yang terinfeksi secara menyeluruh sehinga dapat mengakibatkan kematian pada serangga.
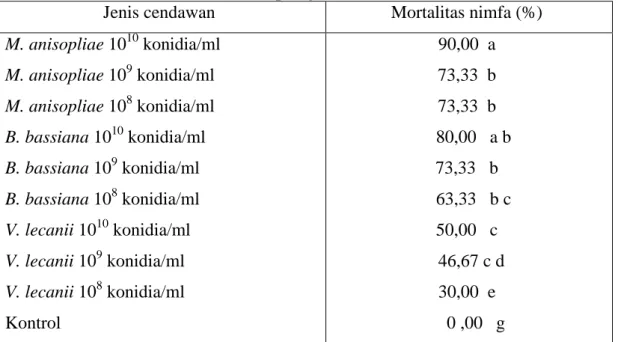
Tabel 2. Rerata mortalitas nimfa D. citri setelah diperlakukan dengan berbagai jenis dan konsentrasi cendawan entomopatogen
Jenis cendawan Mortalitas nimfa (%)
M. anisopliae 1010 konidia/ml M. anisopliae 109 konidia/ml M. anisopliae 108 konidia/ml B. bassiana 1010 konidia/ml B. bassiana 109 konidia/ml B. bassiana 108 konidia/ml V. lecanii 1010 konidia/ml V. lecanii 109 konidia/ml V. lecanii 108 konidia/ml Kontrol 90,00 a 73,33 b 73,33 b 80,00 a b 73,33 b 63,33 b c 50,00 c 46,67 c d 30,00 e 0 ,00 g
Keterangan. Angka-angka yang diikuti oleh huruf kecil yang sama adalah tidak berbeda nyata pada taraf 5 % menurut DMRT
Disamping mortalitas, kemampuan bersporulasi pada inang menjadi sangat penting bila untuk tujuan penularan pada serangga hidup yang lain, karena hifa maupun konidia yang muncul dari bangkai serangga mati akan menyebar dengan bantuan angin ataupun air. Gambar 5 menunjukkan gejala nimfa D. citri tersporulasi cendawan entomopatogen.
M. anisopliae M. anisopliae B. bassiana V. lecanii
Gambar 5 . Sporulasi in vivo beberapa spesies cendawan entomopatogen pada tubuh nimfa setelah diinokulasi
17 Karakterisasi Fisiologi Cendawan Terseleksi Pada Media PDA: Daya Kecambah dan Diameter Koloni
Kemampuan cendawan untuk tumbuh dan berkembang pada media buatan atau inang akan menjadi penting bila cendawan tersebut diperbanyak diperbanyak dalam skala luas untuk tujuan komersil. Namun pada umumnya cendawan entomopatogen dengan patogenesitas yang tinggi dapat direkomendasikan pada penelitian selanjutnya walaupun terdapat perbedaan dalam hal daya kecambah maupun diameter koloni.
Tabel 3. Karakterisasi fisiologi spesies cendawan entomopatogen terpilih: Diameter koloni dan daya kecambah
Isolat/spesies Sumber inokulum Diameter koloni (cm) Daya kecambah (%)
M. anisopliae B. bassiana V. lecanii Tanah Walang Sangit Tanah 5,1 a 4,5 b 9,0 c 24,00 a 42,25 b 82,50 c Keterangan: Angka-angka yang diikuti oleh huruf kecil yang sama pada kolom yang sama adalah berbeda tidak nyata menurut BNT %
Diameter koloni dari masing-masing spesies setelah 15 hari berkisar 4,5 cm – 9,0 cm, dan berdasarkan analisis statistik ketiga spesies tersebut berbeda nyata. Daya kecambah dari masing-masing spesies menunjukkan V. lecanii memiliki kemampuan yang tinggi untuk berkecambah dibandingkan dengan M. anisoplie maupun B. bassiana (Tabel 3). Kemampuan konidia untuk berkecambah merupakan faktor penting untuk berhasilnya melakukan penetrasi pada inang, namun pada penelitian ini ternyata V. lecanii yang mempunyai kemampuan berkecambah yang tinggi tidak efektif untuk mengendalikan D. citri, sementara untuk M. anisopliae maupun B. bassiana memperlihatkan laju pertumbuhan koloni yang tebal, dan ini mungkin yang menyebabkan spesies cendawan ini mampu mematikan D. citi.
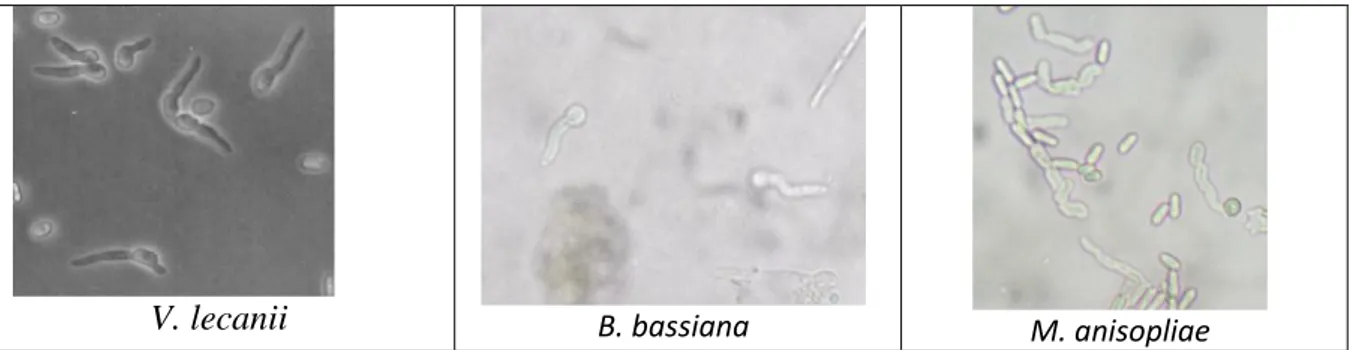
Perkecambahan masing entomopatogen yang diuji dapat dilihat pada Gambar 6.
V. lecanii B. bassiana M. anisopliae
18 Lethal Consentration (LC).
Hasil penelitian menunjukkan bahwa nilai LC50 dan LC80 M. anisopliae dan B. bassiana tergolong rendah dibandingkan dengan isolat V. lecanii yakni: 0,1 x 107 dan 0,1 x 1010 konidia/ml. Hal ini mengindikasikan bahwa M. anisopliae dan B. bassiana paling tinggi tingkat patogenesitasnya dibandingkan spesies V. lecanii terhadap nimfa D. citri (Tabel 4 ). Tabel 4. Lethal concentration (LC) beberapa spesies cendawan entomopatogen terhadap nimfa D. citri
Spesies cendawan LC
50% (konidia/ml) 80% konidia/ml)
M. anisopliae 0,1 x 107 0,1 x 1010
B. bassiana 0,4 x 107 0,8 x 1010
V. lecanii 4 x 107 Tidak terdeteksi
Masing-masing cendawan entomopatogen mempunyai patogenesitas yang berbeda-beda untuk mematikan nimfa D. citri. M. anisopliae mengeluarkan Destruxins sebagai metabolit sekunder sementara B. bassiana memiliki Beauverolit. V. lecanii pada penelitian ini sangat tidak efektif karena untuk mematikan 80 % serangga uji membutuhkan jumlah konidia melebihi konidia perlakuan. Dan hal ini menunjukkan bahwa cendawan entomopatogen memiliki kekhususan inang, (Prayogo 2012) mengemukakan bahwa V. lecanii mampu mematikan 81 % R. linearis sementara pada penelitian ini mematikan 80 % serangga uji pada konsentrasi yang melebihi konsentrasi perlakuan.
19 BAB 6. RENCANA DAN TAHAP BERIKUTNYA
Efektivitas entomopatogen pada serangga akan dipengaruhi oleh sumber makanan yang dalam hal ini berupa jenis medium maupun formulasi dan lama penyimpanan medium. Penyimpanan formulasi sampai waktu yang diperlukan merupakan salah satu faktor yang turut mendukung keberhasilan introduksi agens hayati di lapangan. Entomopatogen yang baik harus mampu bertahan dalam penyimpanan sampai dengan 18 bulan tanpa kehilangan potensinya. Di Indonesia, informasi pemanfaatan cendawan entomopatogen M. anisopliae
dan B. bassiana masih sedikit sehingga teknologi formulasi pada cendawan tersebut juga belum pernah dilaporkan. Oleh karena itu, kajian tentang formulasi kedua cendawan tersebut perlu dilakukan. Kegiatan selanjutnya yang akan dilakukan kajian mengenai :
1. Efikasi Jenis Medium dan Lama Penyimpanan Cendawan Entomopatogen terhadap
Diaphorina citri Kuwayama
2. Efikasi Cendawan Entomopatogen (Terpilih) pada Diaphorina citri Kuwayama di Lapang
20 BAB 7. KESIMPULAN DAN SARAN
Berdasarkan serangkaian penelitian yang sudah dilakukan maka dapat disimpulkan: 1. Koleksi entomopatogen dari tanah dan serangga terinfeksi didapatkan delapan isolat
entomopatogen dan isolat yang mampu mematikan 50 % serangga dewasa D. citri
adalah B. bassiana asal walang sangit L. acuta asal Pondok Suguh, Metarrhizium
asal tanah Rimbo Pegadang Lebong dan Padang Serai Bengkulu, dan V. lecanii asal tanah Rimbo Pegadang Lebong
2. M. anisopliae dan B. bassiana merupakan spesies cendawan entomopatogen yang paling efektif dengan tingkat patogenesitasnya paling tinggi dengan LC50, LC80 paling rendah terhadap D. citri. LC 50 M. anisopliae dan B. bassiana adalah 0,1 x 107 dan 0,4 x 107 . LC 80 masing-masing 0,1 x 1010 dan 0,8 x 1010 konia/ml.
SANWACANA
Terima kasih disampaikan kepada saudara Elya yang telah membantu dalam pencarian D. citri . Terima kasih juga disampaikan kepada Direktur DP2M Dikti, yang telah mendanai penelitian ini melalui Program Hibah Bersaing tahun 2014
21 DAFTAR PUSTAKA
Angraini, M. 2007. Patogenesitas Nomuraea rileyi pada Spodoptera exigua pada tanaman bawang daun. Skripsi Fakultas Pertanian Universitas Bengkulu. Unpublish
Barnett, H.L. 1962. Illustrated Genera of Imperfect Fungi. Second Edition. Burgess Publishing Company. Minneapolis, Minnesota.
Berretta MF, R.E. Lecuona, R.O. Zandomeni, O. Grau. 1998. Genotyping isolates of the entomopathogenic fungus Beauveria bassiana by RAPD with fluorescent labels. J. Invertebr. Pathol. 71: 145–150.
Boucias DG, J.C. Pendland. 1998. Principles of Insect Pathology. London: Kluwer Academic Publishers.
Deciyanto S & I.G.A.A. Indrayani. 2008. Jamur entomopatogen Beauveria bassiana: potensi dan prospeknya dalam pengendalian hama tungau. Perspektif 8 (2): 65-73.
Deptan. 2002. Pengenalan Penyakit CPVD Pada Tanaman Jeruk dan Upaya Pengendalianya. BPTP.Sulawesi Selatan.
Deptan. 2013. www.bkp-pangkalpinang.deptan.go.id . CVPD (Citrus Vein Phloem Degeneration). PDF.
[Ditlin] Direktur Bina Perlindungan Tanaman. 1994. Pengelolaan Organisme Pengganggu Tumbuhan secara Terpadu pada Tanaman Jeruk. Jakarta: Direktorat Jenderal Tanaman Pangan.
Dwiastuti, M.E., A. Triwiratno, dan Suhariyono. 2003. Pengenalan penyakit CVPD pada tanaman jeruk.Citrusindo Citrus Indonesia. Lolit Jeruk Vol 3.
Dwiastuti ME, dan M.Y. Kurniawati. 2007. Keefektifan entomopatogen Hirsutella citriformis (Deutromycetes: Moniliales) pada kutu psyllid Diaphorina citri Kuw. J. Hort. 17 (3): 244-252.
Ginting S. 2008. Patogenisitas beberapa isolat cendawan entomopatogen terhadap rayap tanah Coptotermes curvignathus Holmgren dan Schedorhinotermes javanicus
Kemmer (Isoptera:Rhinotermitidae) [Tesis]. Departemen Proteksi Tanaman, Sekolah Pascasarjana, Institut Pertanian Bogor.
Hajek A.E, and Leger R.J. 1994. Interactions between fungal pathogens and insect hosts. Annu. Rev. Entomol 39: 293-322.
Hasyim, A. dan Azwana. 2007. Patogenisitas Isolat Beauveria bassiana dalam mengendalikan hama penggerek bonggol pisang, Cosmopolites sordidus Germar. J. Horti. 13 (2): 120 – 130.
Herlinda S, S.I. Mulyati dan Suwandi. 2008. Selection of isolates of entomopathogenic fungi and the bioefficacy of their liquid production against Leptocorisa oratorius nymphs. J. Microbiol. Indones. 2 (3): 141-146.
22 Juniawan, M.F., F. Ulfi, Isnawati, dan Y. Prayogo. 2013. Pengaruh kombinasi jenis cendawan entomopatogen dan frekuensi aplikasi terhadap mortalitas kutu kebul (Bemisia tabaci). Lentera Bio 2 (1):37–41
Moore D, P.D. Bridge, P.M. Higgins, R.P. Bateman, C. Prior 1993. Ultra-violet radiation demage to Metarhizium flavoridae conidia and the protection given by vegetable and mineral oils and chemical sunscreens.Ann Appl Biol 122:605-616.
Nadrawati, 2008.Potensi M. anisopliae sebagai cendawan entomopatogen pada ulat grayak
S. litur.Jurnal Akta Agrosia 11(2): 151-156
Nuraida., A. Hasyim. 2009. Isolasi, identifikasi, dan karakterisasi jamur entomopatogen pada rhizosfir tanaman kubis. Jurnal Hortikultura 19 (4): 419-432
Nurhadi, L. Setyobudi, & Handoko. 1989. Biologi kutu psyllid Diaphorina citri Kuwayama (Homoptera: Psyllidae).Penelitian Hortikultura 3 (3). Solok: Balai Penelitian Hortikultura.
Prayogo, Y. 2012. Keefektifan cendawan entomopatogen Lecanicillium lecanii (Zare dan Gams) terhadap Bemicia tabaci Gen. sebagai vektor soybean mosaik virus (SMV) pada tanaman kedelai. Suara Perlindungan Tanaman. 2 (1):11-21
Soetopo D. dan I.G.A.A. Indrayani. 2007. Status teknologi dan prospek B. basisana untuk pengendalian seranga hama tanaman perkebunan yang ramah lingkungan. J. Perspektif. 6(1):29-46.
Sunardi, T. dan Nadrawati. 2008. Efektivitas Cendawan Metarrhizium anisopliae Sorokin terhadap Plutella xylostella Curt dan Crocidolomia binotalis Zeller. Jurnal Akta Agrosia 11 (2) : 157-161
Trizelia,. M.Y. Syahrawati, dan A. Mardiah. 2011. Patogenisitas beberapa isolat cendawan entomopatogen Metarhizium spp. terhadap telur Spodoptera litura Fabricius (Lepidoptera: Noctuidae). J. Entomol. Indon., 8 (1): 45-54
Suharto, Trisusilowati EB & Purnomo H. 1998. Kajian aspek fisiologik Beauveria bassiana
dan virulensinya terhadap Helicoverpa armigera. Jurnal Perlindungan Tanaman Indonesia 4(2): 112-119.
Supriyanto A, 2013. Jeruk Rimau Gerga. http://balitjestro.litbang.deptan.go.id/id/512.html Wahyono, ET. 2006. Pemanfaatan jamur entomopatogen dalam penanggulangan Helopeltis
antonii dan akibat serangannya pada tanaman Jambu Mente. Buletin Teknik Pertanian.11 (1): 17-22.
Widiyanti NLP, Mulyadihardja. 2004. Uji toksisitas jamur Metarhizium anisopliae terhadap larva nyamuk Aedes aegypti. Media Libang Kesehatan XIV (3)
Wirawan, I.G.P., L. Sulistyowati, and I.N. Wijaya. 2000. Penyakit CVPD Pada Tanaman Jeruk (Analisis Baru Berbasis Bioteknologi). Dirjen Perlindungan Hortikultura.
23 LAMPIRAN
Lampiran 1. Susunan Organisasi Tim Peneliti/Pelaksana dan Pembagian Tugas Tahun I.
N0 Nama / NIDN Instansi
Asal
Bidang Ilmu Alokasi Waktu (jam/ minggu) Tugas 1 Ir. Nadrawati, MP 0012046011 Hama Tanaman / Pengendalian hayati 15 Eksplorasi, identifikasi perbanyakan cendawan entomopatogen, skreening cendawan, uji patogenesitas cendawan, analisis data, pelaporan 2 Sempurna Br Ginting, SP, M.Si 0023058204 Hama Tanaman/Pen gendalian hayati 12 Eksplorasi, identifikasi perbanyakan cendawan entomopatogen, skreening cendawan, uji patogenesitas cendawan, analisis data, pelaporan 3 Ir. Tri Sunardi,
M.P
028045603 Hama Tanaman
12 Eksplorasi, perbanyakan
D. citri, uji patogenesitas cendawan, analisis data, pelaporan
4 Zul Efendi 1965061819 86031004
laboran 8 Persiapan alat, eksplorasi, pembuatan media,