UIN SYARIF HIDAYATULLAH JAKARTA
KARAKTERISASI SIFAT FISIK DAN
PERMEABILITAS KRIM GAMMA-ORYZANOL
DENGAN VARIASI NATRIUM LAURIL SULFAT
SKRIPSI
MUHAMMAD FAISAL
NIM: 1113102000064
FAKULTAS KEDOKTERAN DAN ILMU KESEHATAN
PROGRAM STUDI FARMASI
JAKARTA
AGUSTUS 2017
ii UIN Syarif Hidayatullah Jakarta
UIN SYARIF HIDAYATULLAH JAKARTA
KARAKTERISASI SIFAT FISIK DAN
PERMEABILITAS KRIM GAMMA-ORYZANOL
DENGAN VARIASI NATRIUM LAURIL SULFAT
SKRIPSI
Diajukan sebagai salah satu syarat untuk memperoleh gelar Sarjana Farmasi
MUHAMMAD FAISAL
NIM: 1113102000064
FAKULTAS KEDOKTERAN DAN ILMU KESEHATAN
PROGRAM STUDI FARMASI
JAKARTA
AGUSTUS 2017
iii UIN Syarif Hidayatullah Jakarta HALAMAN PERNYATAAN ORISINALITAS
Skripsi ini adalah karya saya sendiri,
dan semua sumber baik yang dikutip maupun dirujuk
telah saya nyatakan dengan benar.
Nama : Muhammad Faisal
NIM : 1113102000034
Tanda Tangan :
v UIN Syarif Hidayatullah Jakarta HALAMAN PENGESAHAN
vi UIN Syarif Hidayatullah Jakarta Judul : Karakterisasi Sifat Fisik dan Permeabilitas Krim
Gamma-Oryzanol dengan Variasi Natrium Lauril
Sulfat
Gamma-oryzanol merupakan senyawa antioksidan alami yang memiliki
aktivitas antioksidan mencapai empat kali lipat dari vitamin E dalam melindungi kulit dari radiasi ultraviolet dan meningkatkan kelembapan kulit sehingga dapat dimanfaatkan sebagai antikerut dan pelembab kulit. Penelitian ini bertujuan untuk mengamati pengaruh perbedaan konsentrasi natrium lauril sulfat terhadap sifat fisik dan pengujian mekanik serta profil penetrasi krim
gamma-oryzanol. Pengujian dilakukan dengan alat sel difusi franz
menggunakan membran spangler dan isopropanol-air sebagai medium kompartemen. Hasil pengujian yang didapat yaitu perbedaan konsentrasi natrium lauril sulfat tidak memberikan pengaruh bermakna terhadap profil
gamma-oryzanol. Jumlah kumulatif gamma-oryzanol terpenetrasi per luas
area selama 6 jam dari dua formula berturut-turut yaitu 50,60 μg/cm2 (F1) dan 48,41 μg/cm2 (F2). Fluks penetrasi gamma-oryzanol pada menit ke 10 untuk dua formula berturut-turut yaitu 109,70 μg/cm2 jam(F1) dan 103,18 μg/cm2 jam(F2).
Kata kunci : Gamma-Oryzanol, krim, karakterisasi sifat fisik, penetrasi, difusi franz
vii UIN Syarif Hidayatullah Jakarta ABSTRACT
Name : Muhammad Faisal Major : Pharmacy
Title : The Physical Properties Characterization and Permeability of the Gamma-Oryzanol Cream with Variations of Sodium Lauryl Sulphate
Gamma-oryzanol is a natural anti-oxidant compound that is four times more effective than vitamin E in protecting the skin from the UV radiation and improve the skin’s moisture which is essential to prevent the formation of wrinkles and maintain the skin’s moisture. The aims of this study is to observe the effect of different SLS concentration towards the physical and mechanical characteristics as well as the penetration profile of the gamma-oryzanol cream. This experiment has been performed by using a franz cell difusion device with a spangler membrane and isopropanol-water as the medium compartment. The obtained results of the different concentration of sodium lauril sulphate did not show any significant effect towards the profile of gamma-oryzanol. The cumulative amount of gamma-oryzanol penetrated per area at the 6th hour of the two formulations were 50,60 μg/cm2 (F1) and 48,41 μg/cm2 (F2), respectively. whereas, The gamma-oryzanol penetration flux at the 10th minute for the two formulas were 109,70 µg/cm2 h (F1) and 103,18 µg/cm2 h (F2), respectively.
Keywords : Gamma-Oryzanol, cream, the physical properties characterization, penetration, franz diffusion cell
viii UIN Syarif Hidayatullah Jakarta Alhamdulillahirabbal’alamiin, segala puji dan syukur penulis ucapkan
kehadirat Allah SWT yang telah melimpahkan rahmat dan ridho-Nya sehingga penulis dapat menyelesaikan penyusunan skripsi ini hingga selesai. Penulisan skripsi yang berjudul “Karakterisasi Sifat Fisik dan Permeabilitas Krim Gamma-Oryzanol dengan Variasi Natrium Lauril Sulfat” sebagai salah satu syarat untuk memperoleh gelar Sarjana Farmasi di Fakultas Kedokteran dan Ilmu Kesehatan Universitas Islam Negeri (UIN) Syarif Hidayatullah Jakarta.
Pada penulisan skripsi ini, penulis tidak terlepas dari bimbingan, semangat,motivasi, bantuan baik moral maupun material serta doa dari berbagai pihak. Oleh karena itu, dengan segenap kerendahan dan kesungguhan hati penulis ingin mengucapkan terima kasih yang sebesar-besarnya kepada:
1. Ibu Ofa Suzanti Betha, M.Si., Apt dan Ibu Yuni Anggraeni, M.Farm., Apt. Sebagai dosen pembimbing yang telah banyak memberikan bimbingan, waktu, tenaga, saran dan membantu penulis dalam penelitian hingga menyusun skripsi.
2. Prof. Dr. H. Arif Sumantri, SKM., M.Kes., selaku Dekan Fakultas Kedokteran dan Ilmu Kesehatan Universitas Islam Negeri Syarif Hidayatullah Jakarta.
3. Ibu Dr. Nurmeilis, M.Si., Apt. Selaku Ketua Program Studi Farmasi Fakultas Kedokteran dan Ilmu Kesehatan UIN Syarif Hidayatullah Jakarta.
4. Ibu Eka Putri, M.Si., Apt. sebagai pembimbing akademik yang telah membimbing dan memberikan dukungan dalam menghadapi permasalahan akademik.
5. Bapak dan Ibu staf pengajar, serta karyawan yang telah memberikan bimbingan dan bantuan selama menempuh pendidikan di Program Studi Farmasi Fakultas Kedokteran dan Ilmu Kesehatan UIN Syarif Hidayatullah Jakarta.
ix UIN Syarif Hidayatullah Jakarta Ibu Nadiah Idris yang selalu memberikan kasih sayang dan doa yang tiada
henti senantiasa mengiringi perjalanan hidup penulis, serta dukungan baik secara moril dan materil. Kepada Adikku tersayang Naura Shafarina yang telah memberikan doa dan semangat dalam menyelesaikan penulisan skripsi ini.
7. Teman seperjuangan penelitian, Thalita Amanda, Sinthiya Nur Septiani, Auliyani Rosdiana atas perhatian, kerja sama, kebersamaan dan waktu untuk mendengarkan segala keluh kesah selama penelitian.
8. Seluruh laboran, Kak Eris, Kak Rahmadi, Kak Yaenap, Kak Rani, Kak Tiwi, dan Kak Walid yang telah banyak membantu dalam penelitian ini. 9. Teman-teman seangkatan Farmasi 2013 yang telah memberikan semangat
dan doa selama ini
10. Semua pihak yang telah membantu penulis selama melakukan penelitian dan penulisan yang tidak dapat disebutkan satu per satu.
Penulis menyadari dalam penyusunan skripsi ini masih banyak kekurangan dan masih jauh dari kesempurnaan. Oleh karena itu, penulis mengharapkan kritik dan saran yang bersifat membangun demi perbaikan skripsi ini.Penulis berdoa semoga amal baik dari semua pihak yang telah membantu penulis mendapat balasan dari Allah SWT. Penulis berharap semoga skripsi ini dapat bermanfaat bagi pengembangan ilmu pengetahuan.
Ciputat, 09 Agustus 2017
x UIN Syarif Hidayatullah Jakarta Sebagai sivitas akademik Universitas Islam Negeri (UIN) Syarif Hidayatullah
Jakarta, saya yang bertanda tangan di bawah ini:
Nama : Muhammad Faisal
NIM : 11113102000064
Program Studi : Farmasi
Fakultas : Kedokteran dan Ilmu Kesehatan (FKIK) Jenis Karya : Skripsi
Demi perkembangan ilmu pengetahuan, saya menyetujui skripsi/karya ilmiah saya, dengan judul :
KARAKTERISASI SIFAT FISIK DAN PERMEABILITAS PENETRASI KRIM GAMMA-ORYZANOL DENGAN VARIASI
NATRIUM LAURIL SULFAT
Untuk dipublikasikan atau ditampilkan di internet atau media lain yaitu
Digital Library Perpustakaan Universitas Islam Negeri (UIN) Syarif
Hidayatullah Jakarta untuk kepentingan akademik sebatas sesuai dengan Undang-Undang Hak Cipta.
Dibuat di : Ciputat
Pada Tanggal : 09 Agustus 2017
Yang Menyatakan
xi UIN Syarif Hidayatullah Jakarta DAFTAR ISI
HALAMAN JUDUL ... ii
HALAMAN PERNYATAAN ORISINALITAS ... iii
HALAMAN PERSETUJUAN PEMBIMBING ...iv
HALAMAN PENGESAHAN ... v
ABSTRAK ...vi
ABSTRACT ... vii
KATA PENGANTAR ... viii
HALAMAN PERNYATAAN PERSETUJUAN PUBLIKASI ... x
DAFTAR TABEL ...xiv
DAFTAR GAMBAR ... xv
DAFTAR LAMPIRAN ...xvi
BAB 1 PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Rumusan Masalah ... 3
1.3 Tujuan Penelitian ... 4
1.4 Manfaat Penelitian ... 4
BAB 2 TINJAUAN PUSTAKA ... 5
2.1 Kulit ... 5
2.1.1 Definisi Kulit ... 5
2.1.2 Struktur Kulit ... 5
2.1.3 Penetrasi Obat Melalui Kulit ... 7
2.1.4 Faktor yang Mempengaruhi Absorbsi Perkutan ... 7
2.2 Krim ... 9
2.2.1 Sifat Fisik Krim ... 11
2.3 Preformulasi Bahan Sediaan Krim ... 12
2.3.1 Natrium Lauril Sulfat ... 12
2.3.2 Setil Alkohol ... 13
2.3.3 Propilen Glikol ... 14
2.3.4 Metil Paraben ... 14
2.3.5 Propil Paraben ... 15
xii UIN Syarif Hidayatullah Jakarta
2.4.2 Sifat Fisikokimia ... 18
2.4.3 Profil Keamanan... 18
2.5 Spektrofotomteri UV-Vis ... 19
2.5.1 Validasi Metode Analisa ... 21
2.6 Uji Difusi ... 22
BAB 3 METODOLOGI PENELITIAN ... 24
3.1 Tempat dan Waktu Penelitian ... 24
3.2 Alat dan Bahan ... 24
3.2.1 Alat ... 24
3.2.2 Bahan ... 24
3.3 Prosedur Kerja ... 24
3.3.1 Preparasi Sediaan Krim Gamma-oryzanol ... 24
3.3.2 Evaluasi Sediaan Krim Gamma-oryzanol ... 25
3.3.3 Validasi Metode Analisa Krim Gamma-oryzanol... 26
3.3.4 Uji Penetrasi Sediaan Krim Gamma-oryzanol ... 28
BAB 4 HASIL DAN PEMBAHASAN ... 32
4.1 Formulasi Sediaan Krim ... 32
4.2 Hasil Evaluasi Karakteristik Sediaan Krim Gamma-oryzanol ... 33
4.2.1 Pengamatan Organoleptis ... 33
4.2.2 Pengamatan Homogenitas ... 33
4.2.3 Pengukuran pH ... 34
4.2.4 Hasil Pengukuran Viskositas dan Sifat Alir Gamma-oryzanol ... 34
4.2.5 Hasil Uji Mekanik (Sentrifuge) ... 37
4.3 Validasi Metode Analisa Gamma-oryzanol ... 37
4.3.1 Penentuan Panjang Gelombang Maksimum ... 37
4.3.2 Hasil Kurva Kalibrasi dan Linieritas ... 38
4.3.3 Hasil Presisi Gamma-oryzanol dalam Etil Asetat ... 39
4.3.4 Pengukuran Kadar Gamma-oryzanol dalam sediaan ... 40
xiii UIN Syarif Hidayatullah Jakarta
4.5 Jumlah Kumulatif Zat Terpenetrasi ... 41
4.6 Fluks Penetrasi ... 44
BAB 5 KESIMPULAN DAN SARAN ... 46
5.1 Kesimpulan ... 46
5.2 Saran ... 46
xiv UIN Syarif Hidayatullah Jakarta
Tabel 3.1 Formula Sediaan Krim Gamma-oryzanol ... 25
Tabel 3.2 Komposisi Membran Difusi ... 28
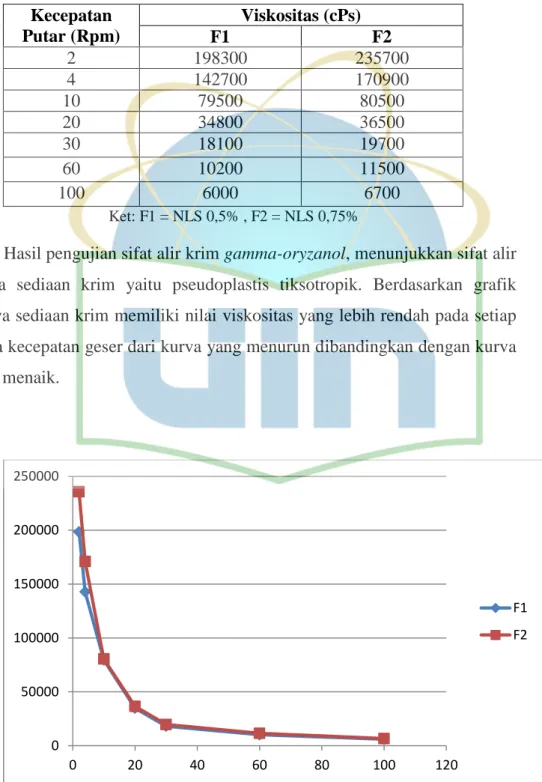
Tabel 4.1 Viskositas Krim Gamma-oryzanol ... 35
Tabel 4.2 Hasil Uji Presisi Gamma-oryzanol ... 39
Tabel 4.3 Jumlah Kumulatif Difusi Gamma-oryzanol Per Luas Area dari Sediaan Krim F1 dan F2 ... 42
Tabel 4.4 Persentase Kumulatif Difusi Gamma-oryzanol Per Luas Area ... 43
Tabel 4.5 Kecepatan Penetrasi (Fluks) Gamma-oryzanol Tiap Satuan Waktu ... 45
xv UIN Syarif Hidayatullah Jakarta DAFTAR GAMBAR
Gambar 2.1 Anatomi Kulit ... 7
Gambar 2.2 Struktur Natrium Lauril Sulfat ... 13
Gambar 2.3 Struktur Setil Alkohol ... 14
Gambar 2.4 Struktur Propilen Glikol ... 14
Gambar 2.5 Struktur Metil Paraben ... 15
Gambar 2.6 Struktur Propil Paraben ... 16
Gambar 2.7 Struktur Empat Komponen Mayor Gamma-oryzanol ... 19
Gambar 2.8 Franz Diffusion Cell ... 23
Gambar 4.1 Kurva krim Gamma-oryzanol ... 33
Gambar 4.2 Pengamatan homogenitas krim Gamma-oryzanol ... 34
Gambar 4.3 Grafik Viskositas krim Gamma-oryzanol ... 35
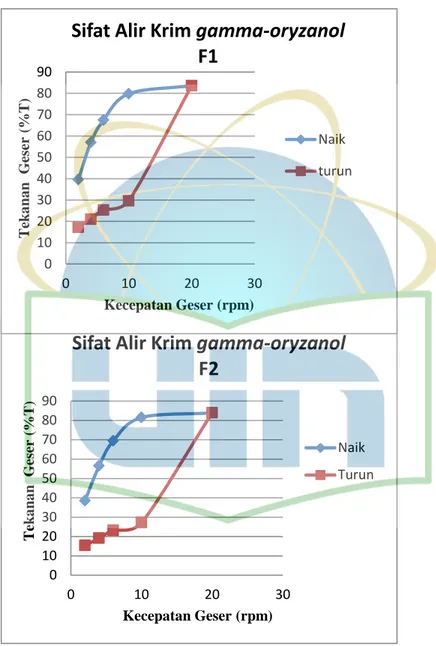
Gambar 4.4 Kurva sifat alir krim Gamma-oryzanol ... 36
Gambar 4.5 Hasil uji mekanik sediaan krim Gamma-oryzanol ... 37
Gambar 4.6 Kurva Kalibrasi Gamma-oryzanol dalam Etil Asetat ... 38
Gambar 4.7 Kurva Kalbirasi Gamma-oryzanol dalam Isopropanol:Air (1:1) ... 39
Gambar 4.8 Grafik Jumlah kumulatif Gamma-oryzanol yang berdifusi per luas area ... 42
xvi UIN Syarif Hidayatullah Jakarta
Lampiran 1 Skema Prosedur Penelitian ... 53
Lampiran 2 Panjang Gelombang Maksimum Gamma-oryzanol dalam Etil Asetat... 54
Lampiran 3 Kurva Kalibrasi Gamma-oryzanol dalam Etil Asetat ... 55
Lampiran 4 Hasil Penetapan Kadar Gamma-oryzanol dalam Sediaan ... 56
Lampiran 5 Data Hasil Pengukuran Sifat Alir Krim Gamma-oryzanol ... 57
Lampiran 6 Panjang Gelombang Gamma-oryzanol dalam Isopropanol:Aquadest (1:1) ... 58
Lampiran 7 Kurva Kalibrasi Gamma-oryzanol dalam Isopropanol:Air (1:1) ... 59
Lampiran 8 Data Absorbansi Penetrasi Gamma-oryzanol pada Krim ... 60
Lampiran 9 Data Hasil Uji Difusi F1 ... 61
Lampiran 10 Data Hasil Uji Difusi F2 ... 61
Lampiran 11 Data Fluks Penetrasi F1 ... 62
Lampiran 12 Data Fluks Penetrasi F2 ... 62
Lampiran 13 Hasil Uji Statistik Jumlah Kumulatif Gamma-oryzanol terpenetrasi per Luas Area ... 63
Lampiran 14 Hasil Uji Statistik Fluks Penetrasi Gamma-oryzanol ... 65
Lampiran 15 Contoh Perhitungan Penetrasi Kumulatif Gamma-oryzanol Per Luas Area ... 68
Lampiran 16 Contoh Perhitungan Fluks Penetrasi Gamma-oryzanol... 70
Lampiran 17 Uji Perolehan Kembali Gamma-oryzanol dalam Sediaan Krim ... 68
Lampiran 18 Uji Presisi Gamma-oryzanol dalam Sediaan Krim... 71
Lampiran 19 Perhitungan Membran Spangler ... 72
1
UIN Syarif Hidayatullah Jakarta BAB 1
PENDAHULUAN
1.1. Latar Belakang
Kulit merupakan jaringan perlindungan yang lentur dan elastis, menutupi permukaan tubuh dan merupakan 5% berat tubuh. Kulit sangat berperan pada pengaturan suhu tubuh, cairan tubuh dan mendeteksi adanya rangsangan dari luar (Aiache dkk., 1993).
Kulit terdiri dari beberapa lapisan, salah satunya lapisan dermis. Lapisan dermis merupakan lapisan kulit yang berperan untuk bertanggung jawab pada sifat elastisitas dan halusnya kulit. Apabila produksi kolagen menurun pada lapisan dermis kulit, maka kulit akan terlihat kering dan tidak elastis lagi dan terjadi penuaan dini (Mulyawan dan Suriana, 2013).
Di dalam tubuh manusia, sebenarnya telah terdapat pertahanan diri untuk melawan radiasi ultraviolet. Namun pada radiasi tingkat tinggi, pertahanan tersebut tidak dapat dilewati apabila salah satu substansi penting dalam tubuh mengalami kekurangan, yaitu antioksidan. Antioksidan berfungsi mengatasi atau menetralisir radikal bebas sehingga diharapkan dengan pemberian atau pemakaian produk yang mengandung antioksidan tersebut proses tua dihambat atau memperlama terjadinya kerusakan tubuh dari timbulnya penyakit degeneratif ( Kosasih, Tony & Hendro, 2006).
Minyak dedak padi (Rice Bran Oil/RBO) mengandung senyawa kimia yang memiliki aktivitas antioksidan tinggi seperti tokoferol/tokotrienol (hingga 300 mg/kg Vitamin E) dan gamma-oryzanol (hingga 3000 mg/kg)(Shin dkk., 1997; Xu dan Godber, 1999). Gamma-oryzanol yang merupakan senyawa antioksidan utama terdiri atas trans-ferulic acid ester (hingga 80%) dan fitosterol (sterol dan alcohol triterpen) seperti cycloartenol, beta sitosterol, 24-methylnecycloartenol, dan campesterol (Xu dan Godber, 2000).
Gamma-oryzanol merupakan senyawa antioksidan alami yang diperoleh dari
UIN Syarif Hidayatullah Jakarta
oil adalah minyak yang diekstraksi dari lapisan luar butiran padi dengan sejumlah
lembaga biji (Nasir dkk., 2009). Sejumlah penelitian telah melaporkan bahwa
gamma-oryzanol memiliki banyak manfaat di bidang kesehatan. Gamma-oryzanol
diketahui dapat melindungi kulit dari radiasi ultraviolet dan meningkatkan kelembapan kulit, sehingga dapat dimanfaatkan sebagai antikerut dan pelembab kulit di bidang kosmetik (Vorarat dkk., 2010).
Menurut Patel dan Naik (2004) Kemampuan gamma oryzanol sebagai antioksidan mencapai empat kali lipat dari vitamin E dalam menghentikan terjadinya oksidasi jaringan dalam tubuh. Selain itu, gamma-oryzanol juga memiliki peran protektif dalam proses peroksidasi lipid yang diinduksi pada peroksida dan karena itu digunakan sebagai agen tabis surya. Selanjutnya, Brigitte Kaiser (1995) dalam penelitianya telah mematenkan komposisi sunscreen kosmetik yang mengandung gamma-oryzanol dan asam ferulat, yaitu 0,05-5% asam ferulat dan 0,05-5% gamma-oryzanol (Brigitte, 1995).
Gamma-oryzanol memiliki sifat yang tidak larut dalam air, sehingga untuk
mengaplikasikannya dalam sebuah formula dibutuhkan bentuk sediaan yang dapat memfasilitasinnya. Terdapat beberapa bentuk sediaan topikal yaitu salep, krim,
lotion, gel dan emulgel (Khunt dkk., 2012), salah satu bentuk sediaan kosmetik
yang sering digunakan yaitu sediaan krim, krim merupakan bentuk sediaan setengah padat, berupa emulsi kental mengandung tidak kurang dari 60% air, dimaksudkan untuk pemakaian luar. Terdapat dua macam sistem dispersi sediaan krim fase air yang terdispersi dalam fase minyak (A/M) dan fase minyak yang terdispersi dalam fase air (M/A) (Lachman dkk., 1994) .
Krim yang dibuat pada penelitian ini adalah krim tipe (M/A), yang ditujukan untuk penggunaan kosmetika dan estetika (Juwita dkk., 2013). Sediaan krim dipilih karena memiliki beberapa keuntungan diantaranya; mudah diaplikasikan karena bentuknya yang semi padat, mampu melekat pada permukaan tempat pemakaian dalam waktu cukup lama, lebih nyaman digunakan pada wajah, tidak lengket dan mudah dibersihkan dengan air bila dibanding sediaan gel, salep, atau pasta (Sharon dkk., 2013).
Berdasarkan penelusuran literatur (Aulton, 2003), formulasi sediaan krim dengan penggunaan emulgator setil alkohol dan natrium lauril sulfat dapat
3
UIN Syarif Hidayatullah Jakarta berpengaruh terhadap kekentalan, menurunkan tegangan permukaan dan pH sediaan. Menurut Nurdianti (2016) dalam penelitiannya, disebutkan perlakuan variasi emulgator Setil alkohol : Natrium Lauril Sulfat (NLS) dapat memberikan perbedaan secara fisik yang meliputi pH, viskositas dan organoleptik karena sifatnya yang menurunkan tegangan permukaan, NLS dapat digunakan sebagai bahan pembasah atau wetting agent, bahan pengemulsi atau emulsifying agent dan bahan pelarut atau solubilizing agent (Ansel, 1989).
Salah satu cara untuk melihat efek yang optimal dari sediaan setengah padat adalah dengan melihat penetras obat melalui lapisan kulit teratas sehingga efek farmakologinya dapat dirasakan (Iswandana, 2011). Uji Pelepasan zat aktif dengan menggunakan metode in vitro adalah metode yang paling sederhana dan paling hemat dalam mengkarakterisasi absorpsi dan penetrasi sediaan ke dalam kulit (Witt, K & Buck, 2003). Hal tersebut diperlukan untuk pengembangan formula sediaan setengah padat agar diperoleh formula yang terbaik
Berdasarkan uraian di atas, penelitian ini bertujuan untuk mengamati evaluasi sifat fisik dan perbandingan uji penetrasi gamma-oryzanol dalam bentuk sediaan krim agar diketahui bentuk sediaan optimal yang diperlukan untuk menghasilkan produk kosmetik yang baik digunakan.
1.2 Rumusan Masalah
Berdasarkan latar belakang yang telah diuraikan maka dapat diidentifikasi masalah sebagai berikut:
a. Bagaimanakah hasil karakterisasi sifat fisik dan permeabilitas
gamma-oryzanol yang terkandung dalam sediaan krim?
b. Formulasi krim manakah yang memiliki permeabilitas senyawa
UIN Syarif Hidayatullah Jakarta 1.3 Tujuan Penelitian
a. Melihat hasil konsentrasi sifat fisik dan permeabilitas senyawa aktif
gamma-oryzanol pada sediaan krim dengan variasi konsentrasi natrium
lauril sulfat.
b. Menentukan sediaan formulasi natrium lauril sulfat yang memiliki penentrasi senyawa aktif gamma-oryzanol paling tinggi.
1.4 Manfaat Penelitian
Hasil penelitian ini diharapkan dapat memberikan informasi ilmiah mengenai sediaan krim dengan senyawa aktif gamma-oryzanol yang dapat digunakan dalam pengembangan formulasi sediaan untuk pemanfaatan di bidang industri kosmetik dan meningkatkan nilai manfaat senyawa aktif
5
UIN Syarif Hidayatullah Jakarta BAB 2
TINJAUAN PUSTAKA
2.1. Kulit
2.1.1 Definisi Kulit
Kulit adalah organ yang terletak paling luar dan membatasinya dari lingkungan hidup manusia. Luas kulit orang dewasa 2m2 dengan berat kira-kira 16% berat badan, kulit merupakan organ yang esensial dan vital serta merupakan cermin kesehatan dan kehidupan. Kulit juga sangat kompleks, elastis dan sensitif, bervariasi pada keadaan iklim, umur, jenis kelamin, ras dan juga bergantung pada lokasi tubuh (Tortora, Derrickson, 2009).
Dalam pemberian obat dengan rute transdermal, kulit merupakan tempat administrasi bukan sebagai organ sasaran (Honeywell-Nguyen & Bouwstra, 2005). Fungsi proteksi kulit adalah melindungi tubuh dari kehilangan cairan elektrolit, trauma mekanik dan radiasi ultraviolet sebagai barier dari invasi mikroorganisme patogen, merespon rangsangan sentuhan, rasa sakit dan panas karena terdapat banyak ujung saraf, tempat penyimpanan nutrisi dan air yang dapat digunakan apabila terjadi penurunan volume darah dan tempat terjadinya metabolisme vitamin D (Richardson, 2003; Perdanakusuma, 2007).
Pembagian kulit secara garis besar tersusun atas tiga lapisan utama yaitu lapisan epidermis atau kutikel, lapisan dermis, dan lapisan subkutis. Tidak ada garis tegas yang memisahkan dermis dan subkutis, subkutis ditandai dengan adanya jaringan ikat longgar dan adanya sel dan jaringan lemak (Tortora, Derrickson, 2009).
2.1.2 Struktur Kulit 1. Lapisan Epidermis
Epidermis merupakan lapisan terluar kulit yang terdiri dari epitel berlapis bertanduk, mengandung sel malonosit, Langerhans dan merkel. Tebal epidermis berbeda-beda pada berbagai tempat di tubuh, paling
UIN Syarif Hidayatullah Jakarta tebal terdapat pada telapak tangan dan kaki. Ketebalan epidermis hanya sekitar 5% dari seluruh ketebalan kulit.
Epidermis terdiri atas lima lapisan (dari lapisan yang paling atas sampai yang terdalam) yaitu stratum korneum, stratum lusidum, stratum granulosum, stratum spinosum dan stratum basale (stratum Germinatum) (Perdanakusuma, 2007).
2. Lapisan Dermis
Dermis tersusun oleh sel-sel dalam berbagai bentuk dan keadaan, dermis terutama terdiri dari serabut kolagen dan elastin. Serabut-serabut kolagen menebal dan sintesa kolagen akan berkurang seiring dengan bertambahnya usia sedangkan serabut elastin terus meningkat dan menebal, kandungan elastin kulit manusia meningkat kira-kira 5 kali dari fetus sampai dewasa. Pada usia lanjut kolagen akan saling bersilang dalam jumlah yang besar dan serabut elastin akan berkurang mengakibatkan kulit terjadi kehilangan kelenturannya dan tampak berkeriput (Perdanakusuma, 2007).
Di dalam dermis terdapat folikel rambut, papilla rambut, kelenjar keringat, saluran keringat, kelenjar sebasea, otot penegak rambut, ujung pembuluh darah dan ujung saraf dan sebagian serabut lemak yang terdapat pada lapisan lemak bawah kulit (Tranggono dan Latifah, 2007).
3. Hipodermis
Lapisan dermis atau jaringan subkutan berada dibawah lapisan dermis. Lapisan ini terdapat jaringan ikat yang menghubungkan kulit secara longgar dengan jaringan di bawahnya.memungkinkan kulit bergeser diatasnya. Hipodermis sering mengandung sel-sel lemak dengan jumlah yang bervariasi (Mescher, 2013). Selain itu, pada lapisan hipodermis juga terdapat pembuluh darah, saraf, dan limfe (Wasitaatmadja, 2010).
7
UIN Syarif Hidayatullah Jakarta Gambar 2.1 Anatomi Kulit
(Sumber: Mescher, 2013)
2.1.3 Penetrasi Obat Melalui Kulit
Penetrasi melintasi stratum korneum dapat terjadi karena adanya proses difusi melalui dua mekanisme, yaitu : transepidermal yang terdiri dari interselular dan transelular serta jalur transppendageal.
Pada rute transelular, molekul obat akan melewati kulit secara langsung melewati membran fosfolipid dan keratinosit. Jalur ini memungkinkan untuk obat yang bersifat polar dan hidrofilik. Sedangkan rute interselular adalah rute penetrasi utama untuk banyak molekul yang melewati stratum korneum. Pada jalur interselular, obat menembus lapisan kulit melalui ruang antar sel dari kulit, sehingga jalurnya menjadi berliku dan lebih panjang. Untuk jalur ini lebih cenderung untuk obat yang bersifat lipofilik karena akan larut dalam lemak yang terdapat di antara filamen (Lund, 1994).
Untuk jalur transappendageal molekul melewati kelenjar keringat dan melewati folikel rambut yang disebabkan adanya pori-pori diantaranya yang memungkinkan obat tersebut berpenetrasi. Jalur appendageal hanya mencakup 0,1% area untuk penyerapan pada kulit, sehingga jalur ini dianggap kurang potensial dibandingkan jalur transepidermal (Touitou & Barry, 2007).
2.1.4 Faktor yang Mempengaruhi Absorbsi Perkutan
Menurut Allen dan Ansel (2014), tidak semua senyawa obat dapat diberikan secara transdermal karena ada beberapa faktor yang dapat
UIN Syarif Hidayatullah Jakarta mempengaruhinya, secara umum faktor tersebut meliputi sifat fisikokimia obat seperti berat molekul, solubilitas, koefisien partisi dan konstanta disosiasi (pKa), faktor lainnya adalah sifat dari pembawa dan kondisi dari kulit. Di
bawah ini merupakan faktor-faktor yang ditemukan oleh para peneliti pada kulit yang normal, sedangkan pada kulit yang terluka sistem penghantaran obat transdermal tidak terjadi karena akan terakses langsung ke jaringan subkutan dan kapiler.
1. Konsentrasi obat merupakan faktor penting, umumnya jumlah obat yang terabsorbsi secara perkutan per unit luas permukaan setiap periode waktu bertambah sebanding dengan bertambahnya konsentrasi obat dalam suatu sistem penghantaran obat trasnsdermal.
2. Berat molekul obat, absorbsi berhubungan terbalik dengan berat molekul dan semakin kecil molekul semakin cepat penetrasinya kedalam kulit daripada yang berukuran besar. Semakin tinggi berat molekul semakin rendah tingkat penetrasi kedalam kulit.
3. Lipofilisitas, pengaruh koefisien partisi terhadap difusi molekul telah dipelajari dengan mengacu pada difusi pasif, peningkatan lipofilisitas obat menyebabkan berkurangnya permeasi.
4. Formulasi, faktor lain yang mempengaruhi penetrasi senyawa bioaktif melalui kulit adalah jenis formulasi yang dirancang untuk masuknya obat. Konsentrasi obat mempengaruhi penghantaran topikal dan formulasi memainkan peranan penting dalam pemasukan obat melalui kulit, dengan korelasi antara konsentrasi dan jumlah obat yang dihantarkan melalui kulit. Selanjutnya, peningkatan viskositas pada formulasi menurunkan penetrasi obat ke dalam kulit yang mungkin disebabkan oleh penurunan difusi.
5. Koefisien Partisi, koefisien partisi merupakan faktor yang penting untuk permeasi obat melalui stratum korneum untuk pemberian obat pertama sampai terakhir, obat harus memiliki karakteristik tertentu yang meliputi massa molekul rendah, kelarutan yang cukup dalam minyak, dan koefisien partisi yang cukup tinggi. Hal ini diamati bahwa
9
UIN Syarif Hidayatullah Jakarta semakin tinggi nilai koefisien partisi, obat lipofilik tidak mudah masuk ke stratum korneum (Prakash dan Thiagarajan, 2012).
6. Semakin besar area pengaplikasian, semakin banyak obat yang diabsorbsi.
7. Obat harus memiliki ketertarikan fisikokimia yang lebih besar kepada kulit dibandingkan dengan pembawa sehingga obat akan meninggalkan pembawa menuju kulit.
8. Obat dengan berat molekul 100 - 800 dan solubilitasnya cukup pada lipid dan air dapat mempenetrasi kulit. Berat molekul ideal pada sistem penghantaran obat transdermal dipercayai 400 atau dibawahnya. 9. Hidrasi pada kulit umumnya menyokong absorbsi perkutan. Sistem
penghantaran obat transdermal berperan sebagai barrier oklusif yang menghambat keringat untuk lewat sehingga meningkatkan hidrasi kulit.
10. Absorbsi perkutan tampak lebih baik apabila diaplikasikan pada area yang memiliki lapisan tanduk tipis dibandingkan dengan yang tebal. 11. Secara umum, semakin lama obat yang diaplikasikan berkontak
dengan kulit akan semakin banyak total obat yang diabsorbsi.
12. Enchancer atau peningkat penetrasi adalah bahan yang dapat meningkatkan permeabilitas kulit. Bahan peningkat penetrasi tidak memiliki efek terapi, tetapi dapat mentransport obat dari bentuk sediaan ke dalam kulit.
2.2. Krim
Krim adalah sediaan setengah padat berupa emulsi kental mengandung tidak kurang dari 60% air, dimaksudkan untuk pemakaian luar. Tipe krim ada 2 yaitu: krim tipe air dalam minyak (A/M) dan krim minyak dalam air (M/A). Untuk membuat krim digunakan zat pengemulsi, umumya berupa surfaktan-surfaktan anionik, kationik dan nonionik (Anief, 2008). Menurut (Ditjen POM, 1995) krim adalah bentuk sediaan setengah padat mengandung satu atau lebih bahan obat terlarut atau terdispersi dalam bahan dasar yang sesuai.
UIN Syarif Hidayatullah Jakarta Sifat umum sediaan semi padat terutama krim ini adalah mampu melekat pada permukaan tempat pemakaian dalam waktu yang cukup lama sebelum sediaan ini dicuci atau dihilangkan. Krim yang digunakan sebagai obat umumnya digunakan untuk mengatasi penyakit kulit seperti jamur, infeksi ataupun sebagai anti radang yang disebabkan oleh berbagai jenis penyakit (Anwar, 2012). Fungsi krim adalah sebagai bahan pembawa substansi obat untuk pengobatan kulit, sebagai pelumas bagi kulit, sebagai pelindung untuk kulit yaitu mencegah kontak langsung dengan zat-zat berbahaya (Anief,1999)
Menurut (Joenoes, 1998) Hal yang penting untuk diperhatikan dalam pembuatan krim adalah seleksi terhadap basis yang cocok, basis harus dapat campur secara fisika dan kimia dengan zat aktifnya, tidak merusak atau menghambat aksi terapi dari obat dan dapat melepas obat pada daerah yang diobati. Bila suatu obat digunakan secara topikal, maka obat akan keluar dari pembawanya dan berdifusi ke permukaan jaringan kulit. Jenis basis yang mempunyai viskositas tinggi akan menyebabkan koefisien difusi suatu obat dalam basis menjadi rendah, sehingga pelepasan obat dari basis akan kecil (Lachman dkk, 1994). Pelepasan bahan obat dari basis dipengaruhi oleh faktor fisika-kimia baik dari basis maupun dari bahan obatnya, kelarutan, viskositas, ukuran partikel, dan formulasi (Aulton, 2003). Selain itu, Formulasi pada sediaan krim akan mempengaruhi jumlah dan kecepatan zat aktif yang diabsorbsi. Zat aktif dalam sediaan krim masuk kedalam basis atau pembawa yang akan membawa obat untuk kontak dengan permukaan kulit. Bahan pembawa yang digunakan untuk sediaan topikal akan memiliki pengaruh yang sangat besar terhadap absorbsi obat dan memiliki efek yang menguntungkan jika dipilih secara tepat (Wyatt dkk., 2001).
Kualitas krim yang baik adalah yang mempunyai sifat stabil, lunak, mudah dipakai dan terdistribusi merata. Suatu krim dikatakan stabil apabila bebas dari inkompatibilitas, stabil pada suhu kamar dan kelembaban yang ada dalam kamar. Lunak berarti semua zat dalam keadaan halus dan semua produk menjadi lunak dan homogen karena krim akan digunakan pada kulit yang mudah teriritasi (Anief, 1999). Stabilitas krim rusak jika terganggu sistem campurannya terutama disebabkan karena perubahan suhu dan perubahan
11
UIN Syarif Hidayatullah Jakarta komposisi disebabkan penambahan salah satu fase secara berlebihan atau pencampuran dua tipe krim jika zat pengemulsinya tidak tercampurkan satu sama lain (Anonim, 1979). Sebagai penstabil krim, dapat ditambahkan zat antioksidan dan zat pengawet. Zat pengawet yang dapat digunakan ialah nipagin 0,12% - 0,18% dan nipasol 0,02% - 0,05% (Anief, 1999).
Penyimpanan krim biasanya dikemas baik dalam botol atau dalam tube, botol yang digunakan biasanya berwarna gelap atau buram. Wadah dari gelas buram dan berwarna berguna untuk krim yang mengandung obat yang peka terhadap cahaya. Tube dari krim kebanyakan dikemas dalam tube kaleng dan dapat dilipat yang dapat menampung (sekitar 8,5 gram krim). Tube krim untuk pemakaian topikal lebih sering dari ukuran 5 sampai 15 gram (Ansel, 1989).
2.2.1. Sifat Fisik Krim
Parameter-parameter yang digunakan dalam uji kestabilan fisik antara lain :
1. Uji Organoleptis Krim
Organoleptis yang meliputi parameter warna, bau, tekstur, dan homogenitasdapat digunakan sebagai indikator kualitatif ketidakstabilan fisik suatu sediaan yang bersifat subyektif (Sulaiman dan Kushwahyuning, 2008). Homogenitas berpengaruh terhadap efektivitas terapi karena berhubungan dengan kadar obat yang seragam pada setiap pemakaian. Jika sediaan homogen maka kadar zat aktif pada saat pemakaian atau pengambilan akan selalu sama. Kondisi ini dapat tercapai bila sediaan krim homogen (Alissya dkk., 2013).
2. Uji Viskositas
Viskositas dipengaruhi oleh temperatur sehingga viskositas suatu cairan akan menurun bila temperatur dinaikkan (Martin dkk., 1993). Berdasarkan (Hukum Stokes) kenaikan viskositas dapat meningkatkan kestabilaan sediaan.
UIN Syarif Hidayatullah Jakarta Uji pH berguna untuk mengetahui pH krim yang telah dihasilkan. Keasaman atau pH krim tidak boleh terlalu asam karena dapat mengiritasi kulit dan tidak boleh terlalu basa karena dapat membuat kulit menjadi bersisik. Oleh sebab itu, krim yang dihasilkan harus memiliki pH sesuai dengan pH normal kulit, yaitu 4,5- 7 (Wasitaatmadja, 1997). Penurunan pH yang terjadi pada produk kemungkinan karena pengaruh suhu dan adanya kandungan zat lain dalam sediaan yang dapat ikut bereaksi (Dureja, 2010, Vasiljevic, 2005).
4. Uji Daya Sebar
Salah satu syarat sediaan krim adalah mudah dioleskan dan mudah merata. Kemudahan dalam pengolesan tersebut dapat diketahui melalui uji daya sebar krim. Daya sebar berkaitan dengan sifat penyebaran krim ketika digunakan pada sediaan topikal dengan meningkatnya daya sebar maka luas permukaan kulit yang kontak dengan krim akan semakin luas dan zat aktif akan terdistribusi dengan baik. Krim yang baik memiliki daya sebar yang besar sehingga dapat diaplikasikan pada permukaan kulit yang luas tanpa penekanan yang berlebihan (Alissya dkk., 2013). Kemampuan daya sebar krim dilihat dari luas sebaran krim yang dihasilkan (Voigt, 1994).
5. Uji Daya Lekat
Krim harus dapat melekat pada kulit dalam waktu yang cukup untuk memungkinkan terjadinya kontak dengan kulit. Waktu kontak yang cukup akan memungkinkan krim bekerja efektif terhadap kulit sehingga kegunaan krim dapat dirasakan sesuai yang diinginkan (Betageri dan Prabhu, 2002).
2.3. Preformulasi Bahan Sediaan Krim 2.3.1 Natrium Lauril Sulfat
Natrium Lauril Sulfat (NLS) berbentuk serbuk putih, berbusa lembut, banyak dan tebal, merupakan surfaktan yang larut dalam air, berkinerja baik dan kuat membersihkan kotoran dan minyak, menghasilkan sediaan dengan warna yang baik tetapi memiliki kekurangan jika digunakan dalam konsentrasi
13
UIN Syarif Hidayatullah Jakarta tinggi dapat menyebabkan iritasi kulit. NLS merupakan tipe surfaktan anionik (Paye dkk., 2006).
NLS memiliki panjang rantai karbon 12, Surfaktan ini kurang ditoleransi oleh kulit ketika panjang rantai meningkat, yaitu antara C14 sampai C18, penetrasi melalui stratum korneum, potensi iritasi, dan kapasitas busa menjadi menurun. Lauril sulfat tersedia dalam bentuk berbagai garam, diantaranya: Natrium Lauril Sulfat (NLS), Amonium Lauril Sulfat (ALS), Magnesium Lauril Sulfat [Mg (LS)2] dan Trietanolamin Lauril Sulfat (TEALS). Toleransi lauril sulfat terhadap kulit berturut-turut sebagai berikut: Mg (LS)2> TEALS > NLS > ALS (Paye dkk., 2006).
Gambar 2.2 Struktur Natrium Lauril Sulfat [Sumber : Rowe, Sheskey & Quinn, 2009]
2.3.2 Setil Alkohol
Setil alkohol terutama terdiri dari campuran dari alkohol alifatik padat. Setil alkohol memiliki nama kimia hexadecane-1-ol dengan rumus kimia C16H34O dan memiliki berat molekul 242,44. Setil alkohol memiliki titik didih 316 - 344,344 untuk material murni, titik leleh 45 - 52,49° C untuk material murni. Setil alkohol merupakan suatu serpihan putih, bergranul bentuk dadu, lunak, berbau samar khas dan memiliki rasa hambar (Unvala, 2009).
Setil alkohol merupakan alkohol lemak yang berbentuk serpihan licin, granul, atau kubus yang mengandung susunan kelompok hidroksil. Setil alkohol banyak digunakan sebagai bahan pengemulsi dan pengeras dalam sediaan krim. Titik leleh dari setil alkohol sebesar 45° - 52º C. Bahan ini sangat mudah larut dalam etanol 95% dan eter serta tidak larut dalam air. Kelarutan akan meningkat bila suhunya dinaikkan. Konsentrasi umum digunakan sebagai pengeras adalah 2-10% dan sebagai bahan pengemulsi maupun emolien adalah 2-5%.
UIN Syarif Hidayatullah Jakarta Gambar 2.3 Struktur Setil Alkohol
[Sumber : Rowe, Sheskey & Quinn, 2009]
2.3.3 Propilen Glikol
Propilen glikol atau 1,2-dihidroksipropane; E1520; 2-hidroksi propanol; metil etilen glikol; metil glikol; propan-1,2-diol; propilenglikolum dengan rumus kimia C3H8O2 dan struktur dapat dilihat pada gambar 2.7,
memiliki fungsi sebagai pengawet antimikroba, disinfektan, humektan,
plasticizer, pelarut, dan kosolven yang bercampur dengan air. Pada
konsentrasi sekitar 15%, propilen glikol berfungsi sebagai humektan (Rowe, Sheskey & Quinn, 2009) yang digunakan untuk mencegah kekeringan pada produk setelah diaplikasikan ke kulit (Aulton, 2002). Selain itu, propilen glikol juga berperan sebagai peningkat penetrasi obat ke dalam kulit dan memiliki efek yang sinergis bersama dengan tween 80.
Gambar 2.4 Propilen glikol (Sumber: Rowe, Sheskey & Quinn, 2009)
Propilen glikol merupakan cairan jernih, tidak berwarna, kental (viskositas dinamik 58,1 cP pada suhu 20oC), dan tidak berbau. Propilen glikol dapat bercampur dengan aseton, kloroform, etanol 95%, gliserin dan air. Selain itu propilen glikol larut 1 bagian dalam 6 bagian eter, tidak bercampur dengan minyak mineral ringan atau fixed oil, tetapi larut dalam beberapa minyak esensial (Rowe, Sheskey & Quinn, 2009).
2.3.4 Metil Paraben
Metil paraben atau metil parahidroksi benzoat; metil hidroksi benzoat; metil-4-hidroksi benzoat; atau juga dikenal dengan nama nipagin M
15
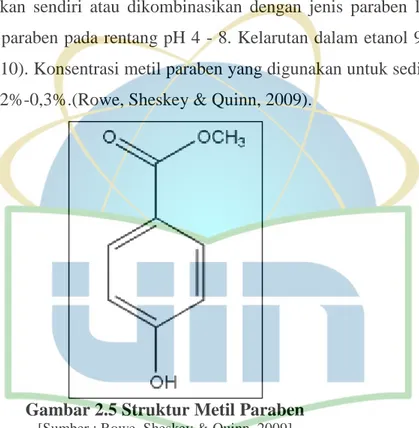
UIN Syarif Hidayatullah Jakarta merupakan pengawet antimikroba. Dalam sediaan farmasetika, produk makanan, dan kosmetik metil paraben digunakan sebagai bahan pengawet. Zat ini dapat digunakan sendiri atau dikombinasikan dengan jenis paraben lain. Efektifitas metil paraben pada rentang pH 4 - 8. Kelarutan dalam etanol 95% (1:3) dan eter (1:10). Konsentrasi metil paraben yang digunakan untuk sediaan topikal, yaitu 0,02%-0,3%.(Rowe, Sheskey & Quinn, 2009).
Gambar 2.5 Struktur Metil Paraben [Sumber : Rowe, Sheskey & Quinn, 2009]
Metil paraben memiliki kelarutan yang buruk dalam air yaitu 1 bagian larut dalam 400 bagian air pada suhu ruang dan agak sukar larut dalam air panas. Metil paraben mudah larut dalam etanol dan dalam propilen glikol namun praktis tidak larut dalam minyak mineral (Rowe, Sheskey & Quinn, 2009).
2.3.5 Propil Paraben
Propil paraben atau propil parahidroksi benzoat; propil hidroksi benzoat; propil-4-hidroksi benzoat; atau juga dikenal dengan nama nipasol M merupakan pengawet antimikroba. Propil paraben digunakan sebagai bahan pengawet. Aktivitas antimikroba ditunjukkan pada pH antara 4 - 8. Propil paraben digunakan sebagai bahan pengawet dalam kosmetik, makanan dan produk farmasetika. Penggunaan kombinasi paraben dapat meningkatkan aktivitas antimikroba, Konsentrasi propil paraben yang digunakan untuk sediaan topikal, yaitu 0,01%-0,6% (Rowe, Sheskey & Quinn, 2009).
UIN Syarif Hidayatullah Jakarta Gambar 2.6 Struktur Propil Paraben
[Sumber : Rowe, Sheskey & Quinn, 2009]
Propil paraben sangat larut dalam aseton dan eter, mudah larut dalam etanol dan metanol, sangat sedikit larut dalam air. Kelarutannya dalam air adalah 1 bagian larut dalam 2500 bagian air pada suhu ruang dan dalam 225 bagian air pada suhu 80oC. Propil paraben mudah larut dalam etanol 95% dan dalam propilen glikol (Rowe, Sheskey & Quinn, 2009).
2.3.6 Parafin Cair
Parafin cair (minyak mineral) dapat berfungsi sebagai emolien, pelarut dan digunakan sebagai fase minyak pada sediaan emulsi m/a. Parafin cair tergolong aman sehingga digunakan secara luas pada berbagai sediaan topikal. Minyak mineral ini bersifat transparan, tidak berasa, tidak berbau saat dingin dan berbau petroleum ketika dipanaskan. Parafin cair praktis tidak larut dalam etanol 95%, gilserin dan air. Tetapi, larut dalam aseton, benzen, kloroform, eter dan petroleum eter. Konsentrasi yang biasa digunakan untuk sediaan topikal adalah 1-32% (Rowe, Sheskey, dan Quinn, 2009).
2.3.7 Aquadest
Aquadest merupakan cairan jernih, tidak berbau, tidak berwarna dan tidak berasa. Dapat bercampur dengan pelarut polar lainnya. Memiliki titik beku : 0°C dan titik didih : 100°C digunakan sebagai pelarut dan fase air (Rowe, Sheskey & Quinn, 2009).
2.4 Gamma-Oryzanol
Gamma-oryzanol adalah antioksidan yang hanya terdapat pada bekatul,
17
UIN Syarif Hidayatullah Jakarta bebas dibanding vitamin E (Hadipernata, 2007). Gamma-Oryzanol merupakan campuran senyawa phytosteryl ferulate dan triterpen alkohol yang diekstraksi dari minyak kulit ari beras / Rice Brain Oil (RBO). Kandungan gamma oryzanol pada bekatul jumlahnya 10 sampai 20 kali lebih banyak dibandingkan total kandungan tokoferol dan tokotrienol (Bergman dan Xu 2003 dalam Chen dan Bergman 2005). Gamma-oryzanol dapat dipisahkan dan dikuantifikasi dengan high-perfomance liquid chromatography (Patel dan Naik, 2004). Menurut penelitian Chen dan Bergman (2005) kandungan
gamma-oryzanol pada masing-masing varietas akan berbeda. Selanjutnya,
Butsat dan Siriamornpun (2010) menyatakan bahwa kandungan gamma oryzanol pada padi dipengaruhi oleh varietas dan kondisi tempat tumbuh, karena komponen antioksidan akan memberikan respon yang berbeda terhadap perubahan lingkungan.
Pada mulanya gamma-oryzanol diduga merupakan komponen tunggal, namun pada akhirnya diketahui bahwa gamma-oryzanol mempunyai empat komponen utama, yaitu Cycloartenyl ferulate, 24-methylene cycloartenyl
ferulat, campesteryl ferulate dan sitosteryl ferulate. Keempat komponen ini
terdapat dalam jumlah 83,6% (Kim dkk, 2014).
2.4.1 Manfaat
Gamma-oryzanol dilaporkan memiliki beberapa manfaat dalam bidang
kesehatan yaitu : memperbaiki pola lipid plasma, menurunkan kolerterol total plasma dan meningkatan level kolesterol HDL serta menghambat agregrasi platelet. Gamma-oryzanol diketahui dapat melindungi kulit dari radiasi ultraviolet dan meningkatkan kelembapan kulit. Sehingga dapat dimanfaatkan sebagai antikerut dan pelembab kulit di bidang kosmetik (Vorarat dkk., 2010). Selain itu, gamma-oryzanol menunjukkan aktivitas sebagai antioksidan dalam sistem in vitro seperti seperti pyrogallol autoxidation, peroksidasi lipid yang diinduksi dalam homogenate retina babi oleh ion besi dan oksidasi kolesteol yang diinduksi oleh 2,2’-azobis(2-methylpropionamidine) (Juliano dkk., 2005).
Gamma-oryzanol mempunyai manfaat yang sangat tinggi bagi kesehatan,
anti-UIN Syarif Hidayatullah Jakarta imflamatori, serta dapat menghambat oksidasi kolesterol (Rong dkk., 1997; Akihisa dkk., 2000). Gamma-oryzanol juga terbukti dapat meningkatkan massa otot, memiliki aktivitas anti karsinogenik, mengobati hiperlipidemia, dan merupakan nutirisi penting untuk mencegah proses penuaan kulit (Patel dan Naik, 2004).
Kemampuan gamma-oryzanol dalam menurunkan kadar kolesterol darah terlihat dari menurunnya secara signifikan kadar total kolesterol, beta lipoprotein, dan LDL seseorang yang mengkonsumsi nasi yang telah diberi ekstrak beras pecah kulit yang mengandung inositol, gamma amino butyric acid (GABA), dan gamma-oryzanol (Patel dan Naik, 2004 ).
2.4.2 Sifat Fisikokimia
Gamma-oryzanol berwarna putih atau putih kekuningan, tidak berbau
dan berbentuk serbuk kristalin. Gamma-oryzanol bersifat hidrofob, mudah larut dalam kloroform, sukar larut dalam etanol dan tidak larut dalam air. Stabil pada suhu 30°C sampai 80 hari (Tsuno.co.jp).
2.4.3 Profil Keamanan
Menurut (Yahara dkk., 1973), dalam penelitianya menggunakan tikus menyatakan bahwa penghantaran gamma-oryzanol oral dan intraperitoneal 10.000 mg/kg tidak menyebabkan abnormalitas secara umum maupun setelah dibedah dan juga dihantarkan melalui subkutan sebesar 500 mg/kg. Data lain menyebutkan bahwa hanya terjadi iritasi kulit ringan pada test patch kulit menggunakan salep gamma-oryzanol 1% (Kobayasi, 1979). Hasato dkk., (1974) melaporkan bahwa tidak terjadi abnormalitas pada tikus setelah 6 bulan diberikan gamma-oryzanol peroral (30 - 1000 mg/kg).
19
UIN Syarif Hidayatullah Jakarta Gambar 2.7 Struktur Empat Komponen Mayor
Gamma-Oryzanol
(Sumber : Patel dan Naik, 2004 ; Islam dkk., 2009)
2.5 Spektrofotomteri UV-Vis
Spektrofotometri serap merupakan pengukuran interaksi antara radiasi elekfomagnetik panjang gelombang tertentu yang sempit dan mendekati monokromatik dengan molekul atau atom dari suatu zat kimia. Hal ini didasarkan pada kenyataan bahwa molekul selalu mengabsorbsi cahaya elektromagnetik jika frekuensi cahaya tersebut sama dengan frekuensi getaran dari molekul tersebut. Elektron yang terikat dan elektron yang tidak terikat akan tereksitasi pada suatu daerah frekuensi, yang sesuai dengan cahaya ultraviolet dan cahaya tampak (UV-Vis) ( Henry,Suryadi,Yanuar, 2002).
Menurut Gandjar dan Rohman (2007), metode spektrofotometri ultraviolet-visibel digunakan untuk menetapkan kadar senyawa obat dalam jumlah yang cukup banyak. Cara untuk menetapkan kadar sampel adalah dengan menggunakan perbandingan absorbansi sampel dengan absorbansi baku atau dengan menggunakan persamaan regresi linier yang menyatakan hubungan antara konsentrasi baku dengan absorbansinya. Persamaan kurva baku selanjutnya digunakan untuk menghitung kadar dalam sampel.
UIN Syarif Hidayatullah Jakarta Spektrum absorbsi daerah ini adalah sekitar 220 nm sampai 800 nm dan dinyatakan sebagai spektrum elektron. Suatu spektrum ultraviolet meliputi daerah bagian ultraviolet (190-380nm), spektrum Vis (Vis = Visibel) bagian sinar tampak (380-780 nm) ( Henry,Suryadi,Yanuar,2002).
Untuk mendapatkan hasil pengukuran yang optimum, setiap komponen dari instrumen yang dipakai harus berfungsi dengan baik. Komponen-komponen spektrofotometri UV-Vis meliputi sumber sinar, monokromator, dan sistem optik.
1. Sebagai sumber sinar; lampu deuterium atau lampu hidrogen untuk pengukuran UV dan lampu tungsten digunakan untuk daerah visibel. 2. Monokromator; digunakan untuk mendispersikan sinar ke dalam
komponen-komponen panjang gelombangnya yang selanjutnya akan dipilih oleh celah (slit). Monokromator berputar sedemikian rupa sehingga kisaran panjang gelombang dilewatkan pada sampel sebagai
scan instrumen melewati spektrum.
3. Optik-optik; dapat didesain untuk memecah sumber sinar sehingga sumber sinar melewati 2 kompartemen, dan sebagaimana dalam spektrofotometer berkas ganda (double beam), suatu larutan blanko dapat digunakan dalam satu kompartemen untuk mengoreksi pembacaan atau spektrum sampel. Blanko yang paling sering digunakan dalam spektrofotometri adalah semua pelarut yang digunakan untuk melarutkan sampel atau pereaksi (Rohman, 2007). Ada beberapa hal yang harus diperhatikan dalam analisis dengan spektrofotometri ultraviolet yaitu:
1. Penentuan panjang gelombang serapan maksimum
Panjang gelombang yang digunakan untuk analisis kuantitatif adalah panjang gelombang dimana terjadi absorbansi maksimum untuk memperoleh panjang gelombang serapan maksimum dapat diperoleh dengan membuat kurva hubungan antara absorbansi dengan panjang gelombang dari suatu larutan baku dengan konsentrasi tertentu.
21
UIN Syarif Hidayatullah Jakarta Dilakukan dengan membuat seri larutan baku dalam berbagai konsentrasi kemudian absorbansi tiap konsentrasi diukur lalu dibuat kurva yang merupakan hubungan antara absorbansi dengan konsentrasi. Kurva kalibrasi yang lurus menandakan bahwa hukum Lambert-Beer terpenuhi.
3. Pembacaan absorbansi sampel
Absorbansi yang terbaca pada spektrofotometer hendaknya antara 0,2 sampai 0,8 atau 15% sampai 70% jika dibaca sebagai transmitan. Hal ini disebabkan karena pada kisaran nilai absorbansi tersebut kesalahan fotometrik yang terjadi adalah paling minimal (Rohman, 2007).
2.5.1 Validasi Metode Analisa
Validasi metode adalah suatu proses yang menunjukkan bahwa prosedur analitik telah sesuai dengan penggunaan yang dikehendaki. Validasi metode analisis ditujukan untuk menjamin bahwa metode analisis memenuhi spesifikasi yang dapat diterima sesuai dengan tujuan yang diharapkan. Hal ini perlu dilakukan untuk menjamin bahwa setiap pengukuran serupa yang dilakukan di masa yang akan datang akan menghasilkan nilai terhitung (calculated value) yang cukup dekat atau sama dengan nilai sebenarnya dari jumlah analit yang terdapat dalam sampel. Adapun karakteristik dalam validasi yaitu akurasi/kecermatan, presisi/keseksamaan, spesifisitas, batas deteksi, batas kuantitasi, linieritas, rentang, kekasaran dan ketahanan
(robutness) (Gandjar dan Rohman, 2012).
a. Akurasi (Kecermatan)
Akurasi adalah kedekatan antara nilai hasil uji yang diperoleh melalui metode analitik dengan nilai sebenarnya. Pengujian senyawa obat akurasi diperoleh dengan membandingkan hasil pengukuran dengan bahan rujukan standar (stadar reference material, SRM). Akurasi dinyatakan dalam persen perolehan kembali (% recovery) (Gandjar dan Rohman, 2012).
UIN Syarif Hidayatullah Jakarta Presisi dari suatu metode analisis adalah derajat kesesuaian di antara masing-masing hasil uji, jika prosedur analisis diterapkan berulang kali pada sejumlah cuplikan yang diambil dari satu sampel homogen.Presisi dinyatakan sebagai deviasi standar atau deviasi standar relatif (koefisien variasi). Presisi dapat diartikan pula sebagai derajat keterulangan dari prosedur analisis pada kondisi kerja normal (Satiadarma dkk., 2004).
2.6 Uji Difusi
Studi penetrasi kulit in vitro dilakukan untuk mengukur kecepatan dan jumlah komponen yang melewati kulit dan jumlah komponen yang tertahan pada kulit. Salah satu cara metode in vitro untuk mengukur jumlah obat yang terpenetrasi melalu kulit yaitu dengan menggunakan sel difusi Franz yang terbagi atas dua kompartemen yaitu kompartemen donor dan kompartemen reseptor yang terpisahkan oleh suatu pelapis atau potongan kulit. Membran yang digunakan dalam uji penetrasi ini dapat digunakan membran berupa kulit manusia atau kulit hewan. Membran diletakkan di antara kedua kompartemen yang dilengkapi o-ring untuk menjaga letak membran, Selanjutnya kompartemen reseptor diisi dengan larutan penerima (Witt & Buck, 2003).
Kompartemen reseptor diisi dengan larutan penerima, biasanya digunakan dapar fosfat. Suhu sel dijaga dengan sirkulasi air menggunakan
water jacket disekeliling kompartemen reseptor. Sediaan yang akan diuji
diaplikasikan pada membran kulit. Pada interval waktu tertentu diambil beberapa mililiter cairan dari kompartemen reseptor dan jumlah obat yang terpenetrasi melalui kulit dapat dianalisis dengan metode yang sesuai. Setiap pengambilan sampel cairan dari kompartemen reseptor, harus selalu digantikan dengan cairan yang sama sejumlah volume terambil (Anggraeni, 2008).
23
UIN Syarif Hidayatullah Jakarta Gambar 2.8 Franz diffusion cell
24
UIN Syarif Hidayatullah Jakarta BAB 3
METODOLOGI PENELITIAN
3.1 Tempat dan Waktu Penelitian
Penelitian dilakukan di Laboratorium Penelitian II, Laboratorium Teknologi Sediaan Padat, Laboratorium Kimia Obat, Laboratorium Farmakognosi-Fitokimia Fakultas Kedokteran dan Ilmu Kesehatan Universitas Islam Negeri Syarif Hidayatllah Jakarta. Waktu penelitian dimulai pada bulan Desember 2016 hingga bulan Mei 2017.
3.2 Alat dan Bahan 3.2.1 Alat
Alat yang digunakan dalam penelitian ini adalah thermometer, kaca objek, timbangan analitik (AND GH-120), pengaduk magnetik, viskometer
HAAKE 6R(Thermo scientific), sonikator (Elmasonic), sentrifuge,
homogenizer (RW 20 Digital, IKA), pH meter (F-52, Horiba),
spektrofotometri UV-Vis (U- 2900, Hitachi), Franz Diffusion Cell dan alat-alat gelas yang sering dipakai di laboratorium.
3.2.2 Bahan
Bahan-bahan yang digunakan dalam penelitian ini adalah
gamma-oryzanol (Wako, Jepang), setil alkohol, propilen glikol, parafin cair, natrium
lauril sulfat, metil paraben, propil paraben, aquadest.
3.3 Prosedur Kerja
3.3.1 Preparasi Sediaan Krim Gamma-oryzanol
Pembuatan krim dilakukan dengan cara: masing-masing fase, yaitu fase minyak (gamma-oryzanol, setil alkohol, parafin cair,) dan fase air (propilen glikol, metil paraben, propil paraben, natrium lauril sulfat dan aquadest) dipanaskan di dalam beaker glass 200 ml yang berbeda pada suhu 70° - 80o C. Setelah semuanya melebur, dimasukkan fase minyak ke dalam fase air sedikit demi sedikit ke dalam beaker glass fase air, dihomogenkan dengan
25
UIN Syarif Hidayatullah Jakarta menggunakan homogenizer kecepatan 800 rpm selama 15 menit hingga terbentuk krim (Sharon dkk., 2013).
Tabel 3.1. Formula Sediaan Krim Gamma-oryzanol
Bahan Persentase Jumlah Bahan
(%b/b) F1 F2 Gamma-oryzanol 0,1 0,1 Setil Alkohol 13 13 Propil Paraben 0,03 0,03 Parafin Cair 12,5 12,5
Natrium Lauril Sulfat 0,5 0,75
Metil Paraben 0,2 0,2
Propilen Glikol 10 10
Aquadest Ad 100 Ad 100
[Sumber : Rahim F, 2004, dengan modifikasi] 3.3.2 Evaluasi Sediaan Krim Gamma-Oryzanol
a. Pengamatan Organoleptis
Pengamatan organolpetis dilakukan dengan mengamati sediaan krim secara visual dari segi warna dan tekstur (Elya dkk., 2013). b. Pengamatan Homogenitas
Pemeriksaan homogenitas dilakukan dengan menggunakan dua kaca objek. Cara pengujiannya sebagai berikut, sejumlah tertentu sediaan dioleskan pada sekeping kaca objek dan kemudian kaca objek yang lainnya ditempelkan pada kaca objek yang sudah diolesi sediaan. Suatu sediaan harus menunjukkan susunan yang homogen dan tidak terlihat adanya butiran kasar (Elya dkk., 2013). c. Pengukuran pH
Pengukuran pH dilakukan menggunakan pH meter. Sebelumnya pH meter dikalibrasi dengan larutan standar buffer pada pH 4 dan 7 dan pH 9. Kemudian elektroda dicelupkan ke dalam sediaan dan pH yang muncul dilayar yang stabil lalu dicatat. Pengukuran dilakukan terhadap masing-masing formula pada suhu ruang (25 ±
UIN Syarif Hidayatullah Jakarta 2oC) (DepKes RI, 1995). Masing-masing formula harus memenuhi rentang pH yang sesuai dengan pH kulit yaitu 4,5 - 7 ( Wasitaatmadja, 1997).
d. Pengukuran Viskositas dan Sifat Alir
Pengukuran viskositas dan sifat alir dilakukan dengan alat
Viscotester 6R HAAKE Pada temperature ruang (25 ± 2°C).
Sebanyak 100 g sediaan diukur sifat alirnya dengan menggunakan spindel nomor 6 yang sudah ditetapkan pada kecepatan 2, 4, 6, 10, 12, 20, 30, 50, 60, dan 100 rpm, kemudian kembali lagi dengan kecepatan 60, 50, 30, 20, 12, 10, 6, 4 dan 2 rpm. Setelah itu dibuat kurva sifat alir untuk mengetahui sifat alir sediaan antara % Torque (sb. x) dan rpm (sb. y) (Mortazafi dan Jafari, 2013 dalam Athiyah, 2015).
e. Uji Sentrifugasi (Mekanik)
Sebanyak 5 gram sampel dimasukkan ke dalam tabung sentrifugasi dan disentrifugasi dengan kecepatan 5000 rpm selama 30 menit yang setara dengan efek gravitasi kira-kira satu tahun. Kemudian diamati apakah terjadi pemisahan atau tidak (Smaoui dkk., 2012).
3.3.3 Validasi Metode Analisa Krim Gamma-oryzanol 1. Penentuan Panjang Gelombang Maksimum
Sebanyak 10 mg gamma oryzanol standar dilarutkan ke dalam 100 mL etil asetat sehingga diperoleh larutan induk dengan konsentrasi 100 ppm (Bucci dkk., 2003). Dari larutan induk, dipipet 1 mL larutan dan dimasukkan ke dalam labu ukur 10 mL, kemudian digenapkan dengan larutan etil asetat sehingga diperoleh larutan dengan konsentrasi 10 ppm. Larutan tersebut dimasukkan dalam kuvet dan diukur absorbansinya pada rentang panjang gelombang 200-500 nm (Rahayu dkk., 2009).
27
UIN Syarif Hidayatullah Jakarta 2. Pembuatan Kurva Kalibrasi dan Uji Linieritas
Larutan Standar dengan seri konsentrasi 8, 10, 12, 14, dan 16 ppm dibaca absorbansinya pada panjang gelombang maksimum. Dari data hasil absorbansi, selanjutnya dihitung persamaan kurvanya sehingga diperoleh persamaan garis linier y= bx + a. Linieritas dari kurva kalibrasi dapat dilihat dari nilai koefisien korelasi yang mendekati nilai 1 (Rahayu dkk., 2009).
3. Uji Presisi
Presisi dilakukan dengan mengukur deviasi dari nilai absorbansi yang diperoleh untuk masing-masing konsentrasi. Pengukuran dilakukan secara berulang sebanyak 5 kali kemudian dicari rata-rata absorbansi dari konsentrasi tersebut dan dicari dengan standar deviasinya (Rahayu dkk., 2009). Kemudian dihitung besarnya simpang deviasi dari masing-masing konsentrasi dengan rumus:
SD =
√
∑( )
Dimana x merupakan luas dari masing-masing konsentrasi, xi merupakan rata-rata konsentrasi, dan n merupakan jumlah injeksi. Setelah mendapat nilai SD kemudian dihitung nilai RSD dengan rumus:
% RSD =
x 100%
Syarat dari nilai RSD adalah < 2% (Rahayu dkk., 2009).
4. Uji Pengukuran Kadar
Ditimbang sediaan krim gamma-oryzanol 1 gr dan dilarutkan dalam pelarut etil asetat sebanyak 10 mL pada tube sentrifugasi. Kemudian sampel divortex selama 10 menit dan disonikasi dengan suhu 20oC selama 20 menit, lalu disentrifugasi pada 3500 rpm selama
UIN Syarif Hidayatullah Jakarta 15 menit. Supernatan dipipet sebanyak 1 mL dan dimasukkan ke dalam labu ukur 10 mL, diencerkan kembali dengan etil asetat sampai garis tanda. Kemudian dibaca absorbansinya menggunakan spektrofotometer UV-Vis pada panjang gelombang maksimum, kemudiaan ditetapkan kadarnya. Penetapan kadar dilakukan dengan pengulangan 3 kali. Dilakukan perlakuan yang sama terhadap basis (Rahayu dkk., 2009).
3.3.4 Uji Penetrasi Sediaan Krim Gamma-oryzanol a. Penyiapan Membran Difusi
Membran difusi yang digunakan adalah membran difusi dengan menggunakan kertas whatman® No1. yang diimpregnasikan terlebih dahulu dengan cairan spangler. Bahan untuk cairan spangler dilebur diawali dengan bahan bertitik lebur tertinggi dan diaduk sampai rata. Kertas whatman ditimbang, direndam selama 15 menit. Kertas diangkat dan diletakkan diantara 2 kertas saring agar cairan Spangler terhisap. Membran buatan yang telah siap ditimbang untuk mengetahui jumlah cairan yang diserap (Rahim, 2014).
Jumlah cairan yang terserap dihitung dengan rumus (Rahim, 2014): [ ]
Dengan W0 adalah berat membran sebelum direndam dan W1
adalah berat membran sesudah direndam. Membran memenuhi syarat uji keseragaman membran jika persentase cairan Spangler terserap antara 102,19-131,22% (Wirawan, 1993).
Tabel 3.2. Komposisi Membran Difusi
Komponen %(b/b) Minyak kelapa 15% Asam Oleat 15% Vaselin 15% Asam stearate 5% Kolesterol 5% Parafin cair 10% Asam Palmitat 10% Minyak zaitun 20%
29
UIN Syarif Hidayatullah Jakarta b. Pembuatan Kurva Kalibrasi Gamma-oryzanol dalam
Larutan Isopropanol:Air (1:1)
Dibuat larutan induk 100 ppm gamma-oryzanol dalam larutan Isopropanol:Air (1:1) sebanyak 100 mL dengan cara menimbang 10 mg gamma-oryzanol dilarutkan dalam Isopropanol:Air (1:1) sampai batas garis 100 mL. Larutan induk tersebut kemudian dibuat seri konsentrasi, sebelum diukur serapan pada masing-masing seri konsentrasi, terlebih dahulu ditentukan panjang gelombang maksimum pada satu konsentrasi. Kemudian dibuat seri konsentrasi 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 ppm diukur serapannya pada panjang gelombang yang telah didapatkan dan dibuat kurva kalibrasinya. Persamaan regresi linier yang didapatkan dari kurva kalibrasi kemudian digunakan untuk perhitungan kadar gamma-oryzanol terpenetrasi.
c. Uji Penetrasi Sediaan
Sebanyak 200 mg krim gamma-oryzanol ditmbang dan diratakan di atas membran. Suhu media adalah 37° ± 0,5°C dengan total volume cairan reseptor 21 mL serta diaduk dengan pengaduk magnetik dengan kecepatan 500 rpm. Proses dilakukan selama 360 Menit. Cuplikan diambil dari media kompartemen reseptor pada menit ke 10, 30, 60, 90, 120, 180, 240, 300 dan 360 sebanyak 1 ml dan segera digantikan dengan larutan Isopropanol:air (1:1) sejumlah volume yang sama (Anggraeni, 2008). Cuplikan yang diperoleh kemudian diukur serapannya menggunakan spektrofotometer UV-Vis pada panjang gelombang maksimal yang telah didapatkan sebelumnya. Proses yang sama dilakukan sebanyak 3 kali pengulangan.
d. Perhitungan Jumlah Kumulatif dan Kecepatan Penetrasi Zat Aktif
Jumlah kumulatif zat aktif yang terpenetrasi per luas area difusi (µg/cm2) dapat dihitung dengan rumus :
UIN Syarif Hidayatullah Jakarta ∑
Keterangan:
= Jumlah kumulatif yang terpenetrasi per luas area (µg/cm2) = Konsentrasi terpenetrasi pada menit ke-n
= Volume sel difusi (21ml) ∑
= Jumlah konsentrasi zat pada sampling menit sebelummnya
= Volume sampling = 1 ml = Luas area membrane = 3,14 cm2
Kemudian dilakukan perhitungan fluks (kecepatan penetrasi tiap satuan waktu) obat berdasarkan hukum Fick I :
Keterangan :
J = Fluks (µg cm-2jam-1) S = Luas area difusi (cm2)
M = Jumlah kumulatif zar yang melalui membran (µg) T = waktu (jam)
Setelah itu dibuat grafik jumlah kumulatif yang terpenetrasi (µg) perluas area difusi (cm-2) terhadap waktu (jam) (Ramadon, 2012).
32
UIN Syarif Hidayatullah Jakarta BAB 4
HASIL DAN PEMBAHASAN
4.1 Formulasi Sediaan Krim
Penelitian ini dilakukan untuk mengetahui dan membandingkan evaluasi sifat fisik dan daya penetrasi sediaan krim yang mengandung
gamma-oryzanol dengan memvariasikan konsentrasi natrium lauril sulfat, yaitu F1 dan
F2 secara berturut-turut adalah 0,5% dan 0,75%. Perbedaan konsentrasi natrium lauril sulfat sebagai emulgator dimaksudkan untuk melihat dan membandingkan perbedaan jumlah kumulatif dan kecepatan penetrasi zat aktif dalam masing-masing krim akhirnya akan didapatkan formula yang memiliki jumlah kumulatif dan kecepatan penetrasi zat aktif paling baik.
Fomula krim dibuat dan dikembangkan dari riset Nurdianti dkk., (2016) yang telah disesuaikan dengan ketersediaan bahan yang mudah diperoleh, kesesuaian zat aktif dengan bahan sediaan krim seperti, emulgator, humektan, stiffening agent, pengawet dan akuades. Emulgator berfungsi sebagai lapisan pelindung antarmuka, penurun tegangan permukaan dan membentuk lapisan film disekeliling lapisan terdispersi untuk mencegah terjadinya koalesen dan terpisahnya dua fase. Konsentrasi sediaan krim F1 dengan setil alkohol 13% dan natrium lauril sulfat 0,5%, krim F2 setil alkohol 13% dan natrium lauril sulfat 0,75%.
Basis yang digunakan pada penelitian kali ini adalah basis krim tipe minyak dalam air yaitu setil alkohol dan natrium lauril sulfat. Setil alkohol berfungsi sebagai agen pengemulsi yang dapat meningkatkan stabilitas dari sediaan krim. Kemudian natrium lauril sulfat yang mampu membantu terbentuknya basis krim karena dapat menurunkan tegangan permukaan. Nurdianti dkk, (2016) dalam penelitiannya telah menggunakan konsentrasi NLS untuk emulgator adalah 0,5%, pada sediaan krim yang akan dibuat dipilih beberapa konsentrasi yaitu 0,5 – 0,75% karena berdasarkan Handbook
of Pharmaceutical Excipients rentang konsentrasi yang digunakan untuk
sediaan topikal adalah 0,5 – 2,5%. Propilen glikol digunakan sebagai kosolven untuk melarutkan metil dan propil paraben, sebagai agen peningkat penetrasi
UIN Syarif Hidayatullah Jakarta dan sebagai humektan. Konsentrasi yang digunakan adalah 10% dan masih masuk ke dalam rentang penggunaan antara 5 - 80% untuk topikal (Rowe, Sheskey, 2009)
Metil dan propil paraben berfungsi sebagai pengawet dan antimikroba yang dapat menghambat pertumbuhan jamur dan bakteri serta membantu menstabilkan sediaan karena penggunaan yang berulang. Parafin cair berfungsi sebagai emolient dalam basis krim dan juga sebagai pelarut. Konsentrasi yang digunakan yaitu 12,5% karena berdasarkan Handbook of
Pharmaceutical Excipients rentang untuk sediaan topikal yang digunakan 1 -
32%. Zat Aktif yang digunakan dalam penelitian kali ini adalah senyawa
gamma-oryzanol yang bermanfaat sebagai antioksidan (Patel dan Naik, 2004).
4.2 Hasil Evaluasi Karakteristik Sediaan Krim Gamma-oryzanol Pada Evaluasi sifat fisik krim gamma-oryzanol dilakukan pengamatan organoleptis, homogenitas, pH, viskositas dan sifat alir, uji sentrifugasi (mekanik).
4.2.1 Pengamatan Organoleptis
Hasil pengamatan organoleptis krim gamma-oryzanol F1 dan F2 menunjukkan bahwa kedua formula mempunyai warna putih, lembut dan tidak terlalu lengket. Kedua krim yang dihasilkan tidak menimbulkan bau, memiliki tekstur yang lembut, mudah menyebar, membentuk konsistensi setengah padat.
Gambar 4.1 Krim gamma-oryzanol
4.2.2 Pengamatan Homogenitas
Pemeriksaan homogenitas pada kedua krim gamma-oryzanol bertujuan untuk mengamati adanya partikel-partikel kasar pada objek. Hasil pengamatan