Oleh:
ARSETYO RAHARDHIANTO NRP. 1507 100 016
DOSEN PEMBIMBING : Dra. Nurlita Abdulgani, M.Si
Ir. Ninis Trisyani, MP.
TUGAS AKHIR - SB 091358
Target peningkatan produksi ikan patin
oleh KKP pada tahun 2012
•Telur dan semen tidak tersedia
sepanjang tahun karena
termasuk ikan petelur
musiman
•Masa
pematangan gamet induk ikan tidak terjadi bersamaan
Ketersediaan benih tidak
stabil
Penyimpanan Diperlukan
Pengencer
FisiologisNaCl
•Sumber energi kurang mencukupi
•Hanya bisabertahan
± 60 menit pada penyimpanan Madu
Fruktosa, glukosa, air, maltose, trisakarida
dan beberapa polisakarida, mineral,
vitamin dan enzim NaCl Fisiologis
+ Madu diharapkan
dapat mendukung
daya hidup spermatozoa
dalam penyimpanan
Kualitas
sperma tetap baik:
• Motilitas Spermatozoa
•Viabilitas permatozoa
Kebutuhan pangan (ikan air
tawar) semakin meningkat
Apakah penambahan larutan pengencer terdiri dari madu dalam NaCl fisiologis dapat memengaruhi kualitas sperma yaitu meliputi motilitas spermatozoa dan viabilitas spermatozoa ikan patin (Pangasius pangasius) selama penyimpanan.
Berapakah dosis konsentrasi larutan madu dalam NaCl
fisiologis yang terbaik dalam proses penyimpanan
spermatozoa ikan patin (Pangasius pangasius).
Uji kualitas spermatozoa yang disimpan meliputi:
- Motilitas spermatozoa - Viabilitas spermatozoa
Pengamatan pendukung yang juga diamati dalam penelitian ini adalah konsentrasi sperma, motilitas spermatozoa segar dan viabilitas spermatozoa segar, derajat keasaman, volume dan warna sperma
Digunakan larutan pengencer yang terbuat dari madu dan
NaCl fisiologis sebagai tambahan dengan dosis
konsentrasi yaitu sebesar 0%, 0,2%, 0,4%, 0,6% dan
0,8%.
Mengetahui pengaruh larutan pengencer yakni campuran madu dan NaCl Fisiologis terhadap kualitas sperma yaitu meliputi motilitas spermatozoa dan viabilitas spermatozoa ikan patin (Pangasius pangasius).
Untuk menentukan dosis larutan pengencer yang
optimal pada media pengencer NaCl fisiologis terhadap
proses penyimpanan sperma ikan patin (Pangasius
pangasius).
Mendapatkan bahan pengencer yang mudah murah dan dapat dimanfaatkan untuk menyimpan sperma ikan patin.
Dapat meningkatkan stok sperma yang berkualitas bagi budidaya perikanan.
Membantu dalam pengemasan sperma untuk diedarkan
ke daerah yang membutuhkan sperma yang berkualitas.
Induk Ikan Patin jantan
Pengambilan Semen
Evaluasi/Pemeriksaan Kualitas Semen
Data makroskopis dan mikroskopis dicatat
Kontrol (Hanya Semen)
0 ml Madu + NaCl Fisiologis
0,2 ml Madu + NaCl Fisiologis
0,4 ml Madu + NaCl Fisiologis
0,6 ml Madu + NaCl Fisiologis
0,8 ml Madu + NaCl Fisiologis
Penyimpanan pada suhu 4oC
Dilakukan pengamatan setiap 6 jam sekali
Pemeriksaan Parameter Utama : Viabilitas dan Motilitas Spermatozoa Analisis Data
Kesimpulan
Februari – Maret 2012
Ikan diperoleh dari hasil kolam Unit Pengelola BudidayaAir Tawar (UPBAT) Dinas Kelautan dan Perikanan Propinsi Jawa Timur, Kec. Dlanggu, Mojokerto.
Laboratorium Zoology – Biologi FMIPA ITS.
Alat dan Bahan
Alat
• Mikroskop, gelas objek, gelas penutup, tabung Eppendorf, obyek glass, cover glass, thermometer, autoclave, Erlenmeyer, syringe tanpa jarum, handtally counter, timbangan analitik, gelas ukur, lap halus, kertas pH, pipet, haemocytometer, aluminium foil, tissue, toples plastik dan lemari pendingin
Bahan
• NaCl Fisiologis, madu, larutan eosin 2%, eosin, aquadest, Ikan Patin (Pangasius pangasius) jantan
TKG IV
Sterelisasi alat-alat dengan autoclave pada suhu 121
oC, 1,5 atm selama 15 menit
Tempat penyimpanan semen ikan patin berupa tabung eppendorf ukuran 1 ml.
Tahap Persiapan
Wadah tabung eppendorf
Tabung eppendorf
Pembuatan Larutan Pengencer
Linea lateralis
Lubang Genital
Semen yang keluar
ditempatkan pada wadah yang telah disediakan
Pengambilan ikan patin induk jantan
pada kolam
budidaya
Lemari pendingin
4
oC
D0 D1 D2 D3 D4 D5
Pengamatan sperma pada penelitian ini terdiri dari dua pengamatan yaitu - pengamatan makroskopis
- pengamatan makroskopis
Pengamatan selama 48 jam dengan interval waktu pengamatan 6 jam sekali.
Pengamatan utama : motilitas spermatozoa (%) viabilitas spermatozoa (%)
Pengamatan pendukung : konsentrasi spermatozoa (sel/ml) motilitas spermatozoa segar (%)
viabilitas spermatozoa segar (%)
derajat keasaman (pH), volume dan warna sperma
Perhitungan Volume Semen
Pengamatan Warna Semen
Pengukuran pH sperma dengan kertas pH-
Indikator khusus pH basa Perubahan warna kertas pH diamati dan
disesuaikan dengan warna standar
Penilaian Konsentrasi Spermatozoa
Eosin 2%
1
2
Σ ǫ = n.p
Keterangan:
V
Σ ǫ = Total spermatozoa (sel/ml N = sel yang terhitung pada kamar
hitung p = pengencer
V = Volume kamar hitung
(panjang : 1 mm, lebar : 1 mm, tebal : 0,1 mm. Jadi volume dari
Haemacytometer yaitu 1 x 1 x 0,1
= 0,1 mm3 = 10-4 ml)
Cover Glass
spermatozoa total – spermatozoa imotil Spermatozoa total
X100%
Cover Glass
Eosin
1
2
spermatozoa hidup
Spermatozoa total X100%
Eksperimental laboratoris
H0: Diduga bahwa konsentrasi larutan pengencer dari madu dalam NaCl fisiologis tidak memberikan pengaruh dalam proses penyimpanan sperma terhadap kualitas sperma (motilitas spermatozoa dan viabilitas spermatozoa) dan tidak dapat diketahui dosis larutan yang optimum.
H1: Diduga bahwa konsentrasi larutan pengencer
dari madu dalam NaCl fisiologis dapat
memberikan pengaruh dalam proses
penyimpanan sperma terhadap kualitas sperma
(motilitas spermatozoa dan viabilitas
spermatozoa) dan dapat diketahui dosis larutan
yang optimum.
Rancangan yang digunakan yaitu RAL (Rancangan Acak Lengkap)
Analisis Ragam (ANOVA)
Uji Jarak Berganda Duncan
HASIL DAN PEMBAHASAN
Pengamatan Hasil
Volume sperma 7,8 ml
Warna sperma Putih susu
pH sperma 7,6
Konsentrasi sperma 11,2x109sel/ml
Berat Ikan 2,6 kg
Umur Ikan 4 tahun
Motilitas 97 %
Viabilitas 98 %
Kualitas Sperma Segar Ikan Patin (Pangasius pangasius)
Sesuai dengan Chew et al (2010) :
•volume sperma 2 ml – 16 ml,
•konsentrasi spermatozoanya 9,4x109 sel sperma/ml,
•motilitasnya 70% - 99%.
Menurut Fujaya, 2002:
•pH sperma : pH 7,14-7,85 dan
•persentase hidup spermatozoa (Viabilitas) >70%.
Motilitas Spermatozoa Ikan Patin (Pangasius pangasius) yang Disimpan
Perlakuan Rata – Rata Motilitas (%)
d0 22.2775a
d4 27.8329b
d2 28.1550b
d1 29.6529b
d3 33.2554c
• Perlakuan d0 dan d3 berbeda nyata dengan perlakuan d1, d2 dan d4.
• Masing-masing perlakuan d0 dan d3 juga berbeda nyata.
• Perlakuan d1, d2 dan d4 tidak saling berbeda nyata.
Keterangan: Angka yang diikuti huruf superscript yang sama pada satu kolom menyatakan tidak ada pengaruh yang nyata akibat perlakuan pada p<0,05
•(D0) kontrol (sperma + 0 ml madu dalam 100 ml NaCl Fisiologis)
•(D1) 0,2 % larutan (sperma + 0,2 ml madu dalam 99,8 ml NaCl Fisiologis)
•(D2) 0,4 % larutan (sperma + 0,4 ml madu dalam 99,6 ml NaCl Fisiologis)
•(D3) 0,6 % larutan (sperma + 0,6 ml madu dalam 99,4 ml NaCl Fisiologis)
•(D4) 0,8 % larutan (sperma + 0,8 ml madu dalam 99,2 ml NaCl Fisiologis)
Mempertahankan motilitas selama kurang lebih 42 jam
Pada keadaan normal (tidak diberi
perlakuan/pengencer), sebagian besar spermatozoa ikan air tawar dapat bergerak tidak lebih dari dua sampai tiga menit setelah bersentuhan dengan air (Fujaya, 2002).
Spermatozoa memanfaatkan nutrisi yang diberikan
oleh pengencer yakni campuran madu dan NaCl
0.00 10.00 20.00 30.00 40.00 50.00 60.00 70.00 80.00 90.00
t1 t2 t3 t4 t5 t6 t7 t8
PersentaseMotilitasSpermatozoa (%)
Waktu Pengamatan
do d1 d2 d3 d4
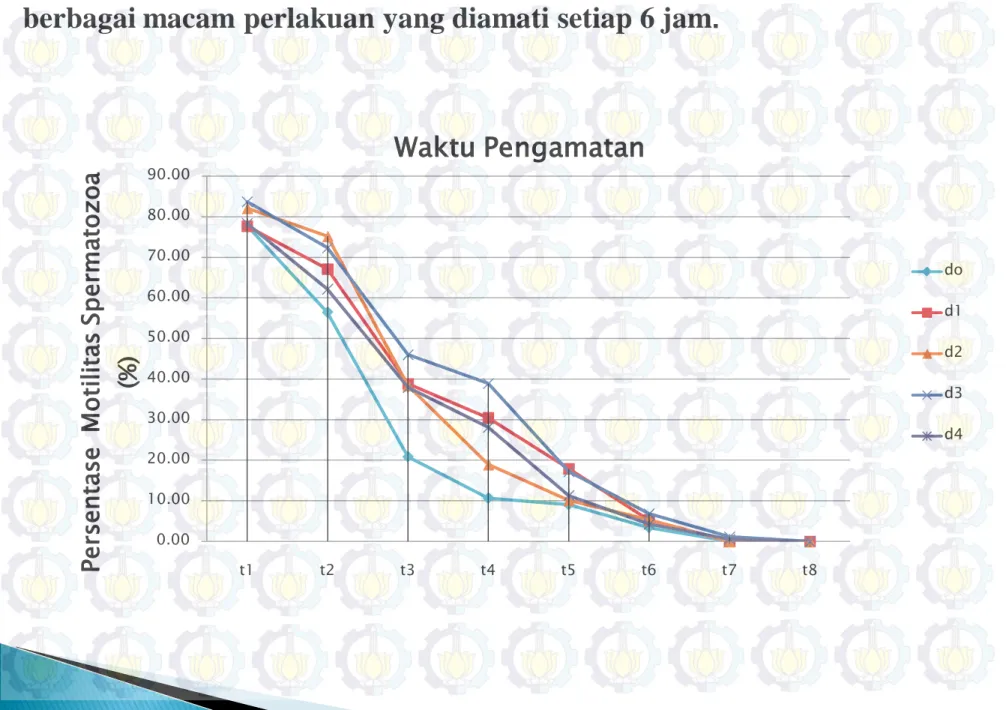
Grafik motilitas spermatozoa ikan patin (Pangasius pangasius) dengan berbagai macam perlakuan yang diamati setiap 6 jam.
Semakin lama proses penyimpanan sperma persentase motilitas spermatozoa juga semakin menurun.
Persentase rendah :perlakuan d0 di seluruh waktu pengamatan.
Persentase tinggi :perlakuan d3 dan d4 saat waktu pengamatan t1, t3, t4, t5, t6 dan t7.
Persentase tinggi pada waktu pengamatan t2 di perlakuan d2.
Diseluruh perlakuan pada waktu pengamatan t7 dan t8 rata – rata spermatozoa berhenti melakukan pergerakan.
Terjadi penurunan :
Persentase d3 > persentase d4
Berkurangnya ketersediaan nutrisi
Anaerob
kejutan dingin
Viabilitas Spermatozoa Ikan Patin (Pangasius pangasius) yang Disimpan
Pewarnaan sperma menggunakan eosin, pengamatan dengan
mikroskop compound dengan perbesaran 1000 X. Tanda panah A
adalah sperma mati dan tanda panah B adalah sperma hidup.
Perlakuan Rata – Rata Viabilitas (%)
d0 47.4946a
d1 56.3325b
d2 56.9363b
d4 58.7050bc
d3 59.8238c
Rata – Rata Persentase Viabilitas Spermatozoa Ikan Patin yang Disimpan
Keterangan: Angka yang diikuti huruf superscript yang sama pada satu kolom menyatakan tidak ada pengaruh yang nyata akibat perlakuan pada p<0,05
•(D0) kontrol (sperma + 0 ml madu dalam 100 ml NaCl Fisiologis)
•(D1) 0,2 % larutan (sperma + 0,2 ml madu dalam 99,8 ml NaCl Fisiologis)
•(D2) 0,4 % larutan (sperma + 0,4 ml madu dalam 99,6 ml NaCl Fisiologis)
•(D3) 0,6 % larutan (sperma + 0,6 ml madu dalam 99,4 ml NaCl Fisiologis)
•(D4) 0,8 % larutan (sperma + 0,8 ml madu dalam 99,2 ml NaCl Fisiologis)
•Persentase terendah yaitu pada perlakuan (d0) yang berbeda nyata dengan seluruh perlakuan.
•Perlakuan d4 tidak berpengaruh nyata pada perlakuan d3 serta d1 dan d2. Perlakuan d1, d2 dan d4 saling tidak berbeda nyata.
•Perlakuan d3 berpengaruh nyata terhadap seluruh perlakuan
0.00 10.00 20.00 30.00 40.00 50.00 60.00 70.00 80.00 90.00 100.00
t1 t2 t3 t4 t5 t6 t7 t8
PersentaseViabilitas Spermatozoa (%)
Waktu Pengamatan
do d1 d2 d3 d4
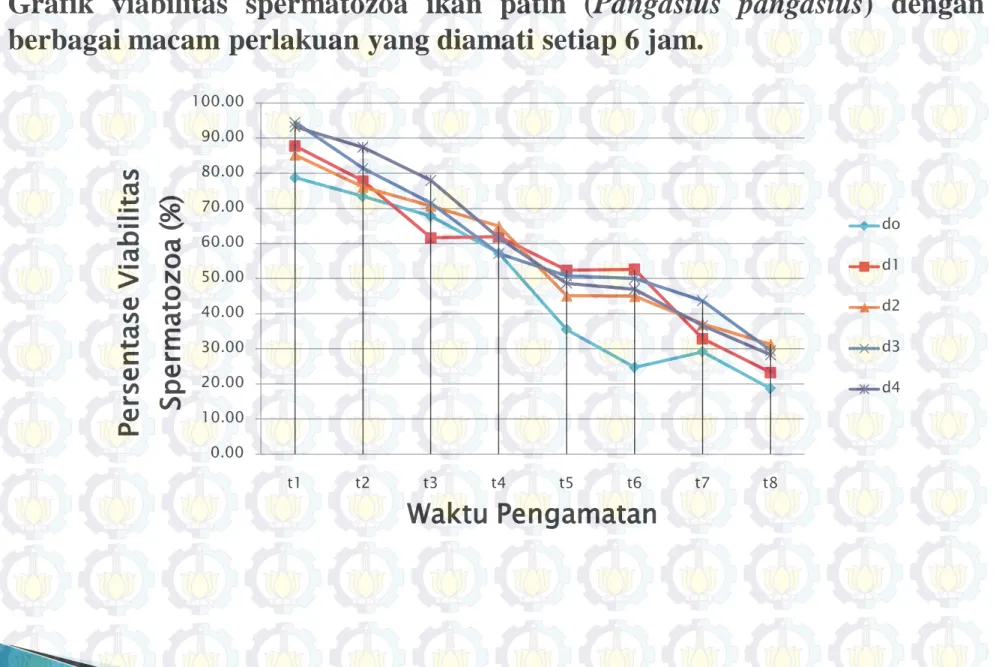
Grafik viabilitas spermatozoa ikan patin (Pangasius pangasius) dengan berbagai macam perlakuan yang diamati setiap 6 jam.
Semakin lama proses penyimpanan sperma persentase viabilitas spermatozoa juga semakin menurun.
Pada waktu pengamatan t1 hingga t3 perlakuan d4 memiliki persentase viabilitas spermatozoa tinggi dalam penyimpanan. Serta pada waktu pengamatan t4 perlakuan d2, waktu pengamatan t5 dan t6 perlakuan d1, waktu pengamatan t7 dan t8 perlakuan d3.
Persentase viabilitas spermatozoa rendah yakni pada perlakuan d0 di seluruh waktu pengamatan kecuali pada pengamatan t3, perlakuan d1 memiliki
persentase yang rendah.
Terjadi penurunan :
Berkurangnya ketersediaan nutrisi
Anaerob
kejutan dingin
Pada peneilitian ini pengamatan viabilitas menunjukkan seluruh konsentrasi pengencer yang digunakan untuk menyimpan sperma ikan Patin (Pangasius pangasius) berhasil mempertahankan hingga jam ke-48 pengamatan (bahkan bisa lebih) dengan rata-rata persentase 26,23%.
Tetapi dilain pihak rata-rata persentase motilitas pada penelitian ini hanya bisa bertahan rata-rata pada jam ke-36 pengamatan, hanya perlakuan d3 dan d4 saja yang dapat mempertahankan motilitas hingga jam ke-42 pengamatan.
Hal ini dapat dikatakan walaupun ketahanan hidup
spermatozoa bisa bertahan lama akan percuma jika tidak
memiliki daya pergerakan yang cukup untuk membuahi
pada Inseminasi Buatan (IB) pada hewan kelas ikan.
KESIMPULAN DAN SARAN
Kesimpulan
Adanya pengaruh larutan pengencer dari madu dalam NaCl fisiologis terhadap kualitas sperma ikan patin yang disimpan
Dosis larutan pengencer sperma yang optimum yaitu pada
perlakuan D3 (99,4 ml larutan NaCl fisiologis dan madu 0,6 ml)
Saran
Dilakukan penelitian lebih lanjut untuk mengetahui kemampuan spermatozoa dalam proses fertilisasi setelah proses penyimpanan.
Mencari bahan pengencer alami yang bernutrisi lain contohnya sari-sari buah.