Chemist's Smile
blog ini berisi kumpulan karya dari penulis. Cerita fiksi dan non fiksi bergabung menjadi satu. Dapat juga dijadikan referensi bagi pembaca sekalian.
Beranda
Selasa, 25 Juni 2013
contoh Laporan Praktik Kerja Lapangan (PKL)
Analisis Kadar Nitrat dan Nitrit dalam Sampel Air Menggunakan Spektrofotometer UV-Visibel
BAB I PENDAHULUAN
1.1 Latar Belakang Masalah
Air merupakan senyawa kimia yang sangat penting bagi kehidupan umat manusia dan
makhluk hidup lainnya dan fungsinya bagi kehidupan tersebut tidak akan dapat digantikan
oleh senyawa lainnya. Hampir semua kegiatan yang dilakukan oleh manusia membutuhkan
air, mulai dari membersihkan diri (mandi), membersihkan ruangan tempat tinggalnya,
menyiapkan makanan dan minuman sampai dengan aktivitas-aktivitas lainnya (Achmad,
2004).
Air yang masuk dalam tubuh manusia selain perlu cukup jumlahnya, jugaharus sesuai
dengan proses hayati. Oleh karena itu diperlukan persyaratan pokokyakni pesyaratan
biologis, fisik dan kimiawi. Dari persyaratan tersebut yang paling mudah diatasi adalah
pencemaran biologi karena umumnya mikroorganisme akan mati bila air dididihkan. Oleh
di negara berkembang adalah masalah kimiawi pada air bersih seperti deterjen, logam berat,
pestisida, dan nitrat tidak dapat diatasi dengan merebus air tersebut. Demikian pentingnya arti
air dalam kehidupan dan kesehatan manusia maka air yang digunakan untuk memenuhi
kebutuhan sehari-hari khususnya untuk penyediaan air minum harus memenuhi persyaratan
yang diatur dalam Permenkes RI No.416/Menkes/ Per/ IX/ 1990 tentang Syarat-syarat dan
Pengawasan Kualitas Air. Dengan kata lain bahwa air yang digunakan atau dikonsumsi harus
memenuhi persyaratan baik secara kualitas maupun kuantitas.
Air yang terdapat di alam mengandung bahan-bahan terlarut maupun bahan-bahan
tersuspensi. Begitu juga halnya dengan air yang berasal darisumber mata air mengandung
komponen-komponen terlarut seperti CO2, O2, N2dan bahan-bahan terlarut lainnya yang
terbawa dari atmosfer, serta bahan-bahanterlarut yang berasal dari lingkungan sekitarnya,
misalnya adanya NO2− dan NO3− yang berasal dari limbah pertanian maupun limbah dari
rumah tangga di sekitar sumber mata air tersebut.
Penurunan kualitas air tanah ditandai dengan terdeteksinya kehadiran beberapa
polutan diantaranya polutan nitrat dan nitrit, yang sangat berhubungan dengan kegiatan
manusia seperti pembuangan limbah domestik, pelindihan TPA, dan penggunaan pupuk yang
berlebihan.
Kandungan nitrat yang tinggi dalam air minum dapat menyebabkan gangguan sistem
peredaran darah pada bayi. Penyakit ini disebut gejala bayi biru (blue baby sydrome) dengan
gejala yang khas yaitu terlihat warna kebiruan pada daerah sekitar bibir dan bagian tubuh.
Saul (1990) melaporkan bahwa WHO mencatat 2000 kasus bayi biru diberbagai negara
karena bayi tersebut diberi air minum yang mengandung 20 mg nitrat/L air. Di lain pihak,
beberapa peneliti melaporkan bahwa nitrat yang direduksi oleh usus menjadi nitrit sehingga
Diperaian, nitrit (NO2-) biasanya ditemukan dalam jumlah yang sangat sedikit lebih
sedikit dari pada nitrat, karena tidak stabil dengan keberadaan oksigen. Nitrit (NO2-)
merupakan bentuk peralihan antara amonia dan nitrat (Effendi, 2003). Keberadaan nitrit
menggambarkan oksigen terlarut rendah. Sumber nitrit dapat berupa limbah industri dan
limbah domestik. Pada manusia, konsumsi nitrit berlebihan akan mengakibatkan
terganggunya proses pengikatan oksigen oleh hemoglobin darah, yang selanjutnya
membentuk methemoglobin yang tidak mampu mengikat oksigen.Di samping itu, NO2- juga
menimbulkan nitrosamin pada air buangan tertentu, nitrosamin tersebut dapat menyebabkan
kanker. Berdasarkan bahayanya Nitrat dan Nitrit bagi kesehatan manusia jika dikonsumsi
dalam kadar yangtinggi yang terdapat dalam air bersih, maka analisis nitrat dan nitrit dalam
sampel air ini perlu dilakukan agar kandungan nitrat dan nitrit dalam air dapat diketahui.
1.1 Rumusan Masalah
Berdasarkan latar belakang diatas, maka dapat dirumuskan masalah sebagai berikut:
1. Berapa kadar nitrat dan nitrit pada sampel air bersih yang diuji di Balai Laboratorium
Kesehatan Yogyakarta?
2. Apakah kadar Nitrat dan Nitrit yang diuji telah memenuhi persyaratan kualitas air bersih
sesuai Peraturan Menteri Kesehatan RI No.416/MENKES/PER/IX/1990 ?
1.2 Tujuan Penelitian
Berdasarkan rumusan masalah diatas, maka tujuan penelitian adalah sebagai berikut :
1. Untuk mengetahui kadar nitrat dan nitrit pada sampel air bersih yang diuji di Balai
Laboratorium Kesehatan Yogyakarta.
2. Untuk mengetahui apakah kadar Nitrat dan Nitrit yang diujikan tersebut telah memenuhi
persyaratan kualitas air bersih sesuai Peraturan Menteri Kesehatan RI
1.3 Manfaat
Manfaat yang diharapkan dari penulisan ini adalah :
1. Dapat mengetahui cara analisis kadar nitrat (NO3-) dan nitrit (NO2-) pada sampel air dengan
menggunakan metode spektrofotometer UV-Visible.
2. Memberikan informasi kepada masyarakat bahwa kadar nitrat (NO3-) dan nitrit (NO2-) untuk
Baku Mutu Persyaratan Kualitas Air Bersihyakni 10 mg/L untuk Nitrat (NO3-) dan 1 mg/L
untuk Nitrit (NO2-) sesuai dengan Peraturan Menteri Kesehatan RI
No.416/MENKES/PER/IX/1990.
BAB II
TINJAUAN PUSTAKA
2.1 Profil Balai Laboratorium Kesehatan Yogyakarta
Balai Laboratorium Kesehatan Yogyakarta adalah instansi pelayanan kesehatan milik
Pemerintah Daerah Provinsi DIY berdiri sejak tanggal 25 Januari 1950 merupakan
laboratorium type A. Sejak berlakunya otonomi daerah Balai Laboratorium Kesehatan
Yogyakarta yang sebelumnya merupakan UPT Departemen Kesehatan diserahkan kepada
Pemerintah Daerah Provinsi DIY merupakan Unit Pelaksana Teknis Dinas Kesehatan di
lingkungan Pemerintah Daerah Provinsi DIY.
2.1.1 Sejarah Berdirinya Balai Laboratorium Kesehatan Yogyakarta
Balai Laboratorium Kesehatan Yogyakarta merupakan Unit Pelayanan Teknis Daerah
(UPTD) Dinas Kesehatan Provinsi Daerah milik Pemerintah Daerah Provinsi DIY. Balai
laboratorium ini merupakan Laboratorium Assaineering DIY yang berada dibawah Fakultas
Teknik Universitas Gadjah Mada Yogyakarta. Kemudian pada tanggal 25 Januari 1950
laboratorium ini menerima gabungan dari bagian Kimia Laboratorium Pusat Klaten dan
disebut Laboratorium Umum atau Laboratorium Kesehatan Yogyakarta (SK Kem.Kes.
Nomor: 126/Secr.Dj./64 tanggal 25 Januari 1950), beralamat di Jl. Polowijan, Ngasem,
Yogyakarta. Bagian yang dimiliki adalah Kimia (termasuk Hortus Medicus di
Tawangmangu), bakteriologi, Serologi dan Kesehatan Teknik serta dipimpin oleh Prof. Dr.
Sardjito.
Pada tanggal 1 Januari 1952 nama Laboratorium diubah menjadi Laboratorium
Kesehatan Daerah Yogyakarta (Labkesda) dengan wilayah kerja meliputi Daerah Istimewa
Yogyakarta dan Jawa Tengah bagian Selatan. Pemimpin laboratorium pertama kali adalah M.
Soepadi Sastrodarsono dengan supervisor Prof. Dr. Sardjito. Pada bulan Agustus 1952,
bagian Kimia, Bakteriologi, dan Serologi pindah menempati lokasi di Jl. Malioboro 16
Yogyakarta. Sedangkan bagian Kesehatan Teknik bergabung dengan Laboratorium Ilmu
Kesehatan Teknik Bandung pada tanggal 1 Juli 1953.
Sejak 1 Maret 1960, Laboratorium Kesehatan Daerah menempati bekas Dalem
Ngadinegaran MD. VII/48 Yogyakarta atau sekarang Ngadinegaran MJ. III/62 Yogyakarta
bersama dengan Sekolah Jenjang Kesehatan Tingkat F (SPKF). Bulan Juni 1974
Laboratorium Kesehatan Yogayakarta ditetapkan sebagai nama dari Laboratorium Kesehatan
Daerah.
Berdasarkan SK MENKES RI Nomor : 142/Menkes/SK/IV/1978, pada tanggal 28
April 1978 Laboratorium Kesehatan Yogyakarta berubah menjadi Balai Laboratorium
Kesehatan Yogyakarta (BLK Yogyakarta). Sesuai Undang-Undang Nomor 22 Tahun 1999
tentang Pemerintah daerah, dan Peraturan Pemerintah Nomor 25 tahun 2000 tentang
Kesehatan Yogyakarta sebagai Unit Pelaksana Teknis (UPT), yang dikelola oleh Pusat
melalui kantor Wilayah Departemen Kesehatan Provinsi DIY, diserahkan kepada Pemerintah
Provinsi DIY. Saat ini, Balai Laboratorium Keshatan Yogyakarta adalah Balai Laboratorium
Kesehatan yang merupakan Unit Pelaksana Teknis Daerah (UPTD) di lingkungan Pemda
Provinsi DIY yang menyelenggarakan pelayanan pemeriksaan laboratorium kesehatan,
berada dibawah dan bertanggungjawab kepada Kepala Dinas Kesehatan Provinsi DIY.
2.1.2 Visi, Misi dan Tujuan Balai Laboratorium Kesehatan Yogyakarta
A. Visi
Balai Laboratorium Kesehatan Yogyakarta sebagai pusat pelayanan laboratorium dan
laboratorium rujukan berkualitas mendukung terbentuknya masyarakat sehat.
B. Misi
1. Memberikan pelayanan secara profesional, terjangkau semua lapisan masyarakat.
2. Menerapkan sistem mutu laboratorium.
3. Berperan dalam meningkatkan kesehatan masyarakat dan SDM di bidang kesehatan.
4. Mengembangkan dan menerapkan ilmu pengetahuan dan teknologi.
C. Tujuan
1. Meningkatkan kualitas pelayanan pemeriksaan laboratorium sehingga dapat memberikan
pelayanan yang tepat, cepat, akurat dapat menunjang ketepatan diagnosa dan dapat
memberikan kepuasan pelanggan.
2. Meningkatkan cakupan dan jangkauan pelayanan sehingga mudah diterima oleh masyarakat,
terjangkau dan dapat menjangkau semua lapisan masyarakat.
3. Meningkatkan kesehatan masyarakat.
4. Meningkatkan kualitas cakupan pembinaan sehingga dapat memberikan pembinaan secara
profesional serta meningkatkan SDM tenaga kesehatan yang berkualitas.
5. Meningkatkan penelitian yang didukung Sumber Daya Manusia (SDM) profesional dan
berpengalaman.
2.1.3 Fungsi dan Lingkup Tugas Balai Laboratorium Kesehatan Yogyakarta
Balai Laboratorium Kesehatan mampunyai tugas melaksanakan pelayanan meliputi
Istimewa Yogyakarta Nomor 160 Tahun 2002 tentang Uraian Tugas dan Tata Kerja Unit
Pelaksana Teknis Dinas Kesehatan Provinsi DIY, maka Balai Laboratorium Kesehatan
Yogyakarta mempunyai Fungsi dan Tugas sebagai berikut :
A. Fungsi
Balai Laboratorium Kesehatan mempunyai fungsi sebagai unsur pelaksana
operasional sebagian kewenangan dinas dalam bidang pelayanan laboratorium kesehatan
masyarakat melalui kegiatan pemeriksaan laboratorium dan kegiatan rujukan.
B. Tugas
1. Penyusunan program Balai.
2. Pelaksanaan kegiatan rujukan.
3. Pengelolaan sarana dan prasarana Balai.
4. Pelayanan pemeriksaan klinis, medis dan penunjang medis.
5. Pelayanan pengujian kesehatan masyarakat.
6. Pelayanan pengujian higiene sanitasi.
7. Penyelenggaraan pembinaaan laboratorium kesehatan.
8. Penyelenggaraan kerjasama pendidikan dan pelatihan teknis laboratorium.
9. Pelayanan konsultasi bidang kesehatan yang berkaitan dengan hasil pengujian laboratorium.
10. Pelaksanaan pemasaran produk Balai.
11. Penyediaan media dan reagensia untuk pengujian laboratorium.
12. Pelayanan sertifikasi tenaga analis kesehatan.
13. Pelaksanaan kegiatan ketatausahaan
2.2 Air
Air adalah senyawa kimia dengan rumus kimia H2O, artinya satu molekul air tersusun
atas dua atom hidrogen yang terikat secara kovalen pada satu atom oksigen. Air mempunyai
sifat tidak berwarna, tidak berasa dan tidak berbau pada kondisi standar, yaitu pada tekanan
karena mampu melarutkan banyak zat kimia lainnya, seperti garam, gula, asam, beberapa
jenis gas dan senyawa organik. Atom oksigen memiliki nilai keelektronegatifan yang sangat
besar, sedangkan atom hidrogen memiliki nilai keelektronegatifan paling kecil diantara
unsur-unsur bukan logam. Hal ini selain menyebabkan sifat kepolaran air yang besar juga
menyebabkan adanya ikatan hidrogen antar molekul air. Ikatan hidrogen terjadi karena atom
oksigen yang terikat dalam satu molekul air masih mampu mengadakan ikatan dengan atom
hidrogen yang terikat dalam satu molekul air yang lain. Ikatan hidrogen inilah yang
menyebabkan air memiliki sifat-sifat khas. Sifat-sifat khas air sangat menguntungkan bagi
kehidupan makhluk di bumi (Achmad, 2004).
2.2.1 Sumber dan Kegunaan Air
Kuantitas air berhubungan dengan adanya bahan-bahan lain terutama
senyawa-senyawa kimia baik dalam bentuk senyawa-senyawa organik maupun anorganik juga adanya
mikroorganisme yang memegang peranan penting dalam menentukan komposisi kimia air.
Seluruh peradapan manusia dan mahluk hidup lainnya dapat lenyap karena kurangnya
air yang disebabkan berbagai faktor terutama akibat dari perubahan iklim. Kualitas air yang
buruk yang disebabkan adanya berbagai jenis bakteri pathogen dan kandungan bahan-bahan
kimia berbahaya dapat membunuh berjuta manusia terutama di negara-negara sedang
berkembang.
Sebagian besar dari air ditemukan dalam bentuk lautan dan samudra. Bagian lainnya
terdapat dalam bentuk uap air di atmosfer. Air dalam bentuk padat juga ditemukan di bumi
yaitu yang membentuk salju di daerah kutub utara dan selatan.
Air permukaan terdapat dalam danau, sungai dan sumber-sumber air lainnya,
sedangkan air tanah (ground water), terdapat di dalam tanah. Air tanah dapat melarutkan
mineral-mineral bahan induk dari tanah yang dilewatinya. Sebagian besar mikroorganisme
Terdapat perbedaan yang cukup besar antara air tanah dengan air permukaan. Hai ini
disebabkan oleh kandungan berbagai zat, baik yang terlarut maupun yang tersuspensi dalam
perjalanan menuju ke laut. Air permukaan yang terkumpul dalam danau atau waduk
mengandung nutrisi penting untuk pertumbuhan ganggang. Air permukaan yang mengandung
bahan organik mudah terurai dalam konsentrasi tinggi secara normal akan mengandung
bakteri dalam jumlah tinggi pula yang mengandung bakteri dalam jumlah tinggi pula yang
mempunyai pengaruh cukup besar terhadap kualitas air permukaan.
Ada keterkaitan yang sangat kuat antara lapisan air dimana air berada dengan lapisan
tanah/lahan dimana keduanya dipengaruhi oleh kegiatan manusia. Misalnya, gangguan
terhadap hutan menjadi lahan pertanian dapat menyebabkan reduksi negative yang ada
diatasnya dan mengurangi proses transpirasi yaitu penguapan air oleh tanaman. Hal ini dapat
mempengaruhi iklim mikro di wilayah tersebut. Akibat dari hal tersebut adalah meningkatnya
limpasan air, erosi, dan akumulasi dari lumpur dalam badan air (sungai) serta dapat
meningkatkan unsur-unsur hara di permukaan air, sehingga siklus nutrient akan dipercepat.
Terjadinya percepatan siklus tersebut akan sangat memberikan pengaruh terhadap
karakteristik kimia dan biologi dari badan air.
Air yang digunakan oleh manusia adalah air permukaan tawar dan air tanah murni.
Pada daerah kering sebagian kebutuhan airnya berasal dari larutan, suatu sumber yang akan
menjadi penting setelah persediaan air tawar dunia relative berkurang dibandingkan
kebutuhan. Meningkatnya kebutuhan air ini bukan hanya disebabkan oleh jumlah penduduk
dunia yang makin bertambah juga sebagian akibat dari peningkatan taraf hidupnya yang
diikuti oleh peningkatan kebutuhan air untuk keperluan rumah tangga, industri, rekreasi
disamping pertanian (Achmad, 2004).
Air merupakan senyawa kimia yang terdiri dari atom H dan O. Sebuah molekul air
terdiri dari satu atom O yang berikatan kovalen dengan dua atom H. Molekul air yang satu
dengan molekul-molekul air lainnya yang bergabung dengan satu ikatan hydrogen antara
atom H dengan atom O dari molekul air yang lain. Adanya ikatan ikatan hydrogen inilah yang
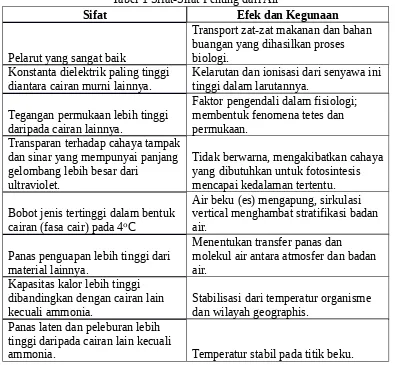
menyebabkan air mempunyai sifat-sifat yang khas seperti terlihat pada tabel 1.
Tabel 1 Sifat-Sifat Penting dari Air
Sifat Efek dan Kegunaan
Pelarut yang sangat baik
Transport zat-zat makanan dan bahan buangan yang dihasilkan proses biologi.
Konstanta dielektrik paling tinggi
diantara cairan murni lainnya. Kelarutan dan ionisasi dari senyawa initinggi dalam larutannya.
Tegangan permukaan lebih tinggi
Bobot jenis tertinggi dalam bentuk
cairan (fasa cair) pada 4 Cᵒ
Air beku (es) mengapung, sirkulasi vertical menghambat stratifikasi badan air.
Panas penguapan lebih tinggi dari material lainnya.
Menentukan transfer panas dan
molekul air antara atmosfer dan badan air.
Panas laten dan peleburan lebih tinggi daripada cairan lain kecuali
Air merupakan pelarut yang sangat baik bagi banyak bahan, sehingga air merupakan
media transport utama bagi zat-zat makanan dan produk buangan/ sampah yang dihasilkan
proses kehidupan. Oleh karena itu air yang ada di bumi tidak pernah terdapat dalam keadaan
murni, tetapi selalu ada senyawa atau mineral/ unsur lain yang terdapat di dalamnya.
Meskipun demikian tidak berarti bahwa semua perairan di bumi ini telah tercemar. Sebagai
contoh, air yang berasal dari sumber air di daerah pegunungan atau daerah hulu sungai dapat
dianggap sebagai air yang bersih (Achmad, 2004).
2.2.3 Pencemaran Air
Dewasa ini, air menjadi menjadi masalah yang perlu mendapat perhatian
yangseksama dan cermat. Untuk mendapatkan air yang baik ataupun yang sesuai dengan
standar tertentu, saat ini menjadi barang yang mahal karena air sudah banyaktercemar oleh
bermacam-macam limbah dari hasil kegiatan manusia, baik limbah darirumah tangga, limbah
dari kegiatan industri dan kegiatan-kegiatan lainnya (Ompusunggu, 2009).
Pencemaran air adalah penyimpangan sifat-sifat air dari keadaan normal, bukan dari
kemurniannya. Air yang tersebar di alam tidak pernah terdapat dalam bentuk murni, tetapi
bukan berarti semua air sudah terpolusi. Sebagai contoh meskipun di daerah pegunungan atau
hutan yang terpencil dengan udara yang bersih dan bebas dari polusi, air hujan selalu
mengandung bahan-bahan terlarut CO2, O2,dan N2 serta bahan-bahan tersuspensi dan
partikel-partikel lainnya yang trerbawa dari atmosfer.
Definisi pencemaran air menurut Surat Keputusan Menteri Negara Kependudukan
dan Lingkungan Hidup Nomor : KEP-02/MENKLH/I/1988 Tentang Penetapan Baku Mutu
Lingkungan adalah : masuk atau dimasukkannya mahluk hidup, zat, energi dan atau
komponen lain ke dalam air dan atau berubahnya tatanan air oleh kegiatan manusia atau oleh
proses alam, sehingga kualitas air turun sampai ke tingkat tertentu yang menyebabkan air
2004).
Dalam pasal 2, air pada sumber air menurut kegunaan/peruntukkannya digolongkan
menjadi:
1. Golongan A, yaitu air yang dapat digunakan sebagai air minum secara langsung tanpa
pengolahan terlebih dahulu.
2. Golongan B, yaitu air yang dapat dipergunakan sebagai air baku untuk diolah sebagai air
minum dan keperluan rumah tangga.
3. Golongan C, yaitu air yang dapat dipergunakan untuk keperluan perikanan dan peternakan.
4. Golongan D, yaitu air yang dapat dipergunakan untuk keperluan pertanian, dan dapat
dimanfaatkan untuk usaha perkotaan, industri, dan listrik negara.
Menurut definisi pencemaran air tersebut di atas bila suatu sumber air yang termasuk
dalam kategori golongan A, misalnya sebuah sumur penduduk kemudian mengalami
pencemaran dalam bentuk rembesan limbah cair dari suatu industri maka kategori sumur tadi
bukan golongan A lagi, tapi sudah turun menjadi golongan B karena air tadi digunakan
langsung sebagai air minum tanpa melalui pengolahan terlebih dahulu. Dengan demikian air
sumur tersebut menjadi kurang/ tidak berfungsi lagi sesuai dengan peruntukkannya (Achmad,
2004).
2.2.4 Air Bersih
Berdasarkan Peraturan Menteri Kesehatan No. 416 Tahun 1990 Tentang
”Syarat-syarat Dan Pengawasan Kualitas Air “, air bersih adalah air yang digunakan untuk keperluan
sehari-hari yang kualitasnya memenuhi syarat kesehatan dan dapat diminum apabila telah
dimasak.Air harus bebas dari kontaminasi kuman atau bibit penyakit. Air tidak boleh
mengandung bahan kimia yang berbahaya maupun beracun. Air tidak berasa dan tidak juga
berbau. Air harus memenuhi standar yang ditentukan oleh Badan Kesehatan Dunia (WHO)
2.3 Senyawa Nitrogen dalam Air
Senyawa-senyawa nitrogen terdapat dalam keadaan terlarut juga sebgai bahan
tersuspensi. Dalam air senyawa-senyawa ini memegang peranan sangat penting dalam
perairan reaksi-reaksi biologi perairan. Jenis-jenis nitrogen anorganik utama dalam air adalah
ion nitrat (NO3-), dan ammonium (NH4+). Dalam kondisi tertentu terdapat dalam bentuk nitrit
(NO2-). Sebagian besar dari nitrogen total dalam air terikat sebagai nitrogen organik, yaitu
dalam bahan-bahanyang berprotein, juga dapat berbentuk senyawa/ion-ion lainnya dari bahan
pencemar.
Nitrogen perairan merupakan penyebab utama pertumbuhan yang sangat cepat dari
ganggang yang menyebabkan eutrofikasi. Pada umumnya nitrogen anorganik dalam perairan
aerobic terdapat dalam keadaan bilangan oksidasi +5, yaitu sebagai NO3-, dan dengan
bilangan oksidasi +3, dalam keadaan anaerob, sebagai NH4+ yang stabil (Achmad, 2004).
2.4 Nitrat dan Nitrit
Nitrat (NO3-) dan Nitrit (NO2-) adalah ion-ion anorganik alami yang merupakan
bagian dari siklus Nitrogen.Aktivitas mikroba di tanah atau air menguraikan sampah yang
mengandung Nitrogen organik pertama–tama menjadi Amonia, kemudian dioksidasikan
menjadi Nitrit dan Nitrat. Oleh karena Nitrit dapat dengan mudah dioksidasikan menjadi
Nitrat, maka Nitrat adalah senyawa yang paling sering ditemukan di dalam air bawah tanah
maupun air yang terdapat di permukaan.
Nitrifikasi dapat didefenisikan sebagai konversi biologis dan nitrogen dari komponen
organik atau anorganik dari bentuk tereduksi ke bentuk teroksidasi. Pada penanganan polusi
air, nitrifikasi adalah proses biologis yang akan mengoksidasi ion ammonium menjadi bentuk
Nitrosospira, Nitrosococcus, Nitrosocystis. Sedangkan bakteri yang mengoksidasi nitrit
menjadi nitrat adalah Nitrobacter juga dari genus Nitrosogloea dan Nitrocystis.
Pada limbah yang belum diolah, nitrogen dijumpai dalam bentuk nitrogen organik dan
komponen amonium. Nitrogen organik akan diubah oleh aktivitas mikroba menjadi ion
amonium. Bila kondisi lingkungan mendukung maka mikroba nitrifikasi akan mampu
mengoksidasi amonia. Mikroba tersebut bersifat autotropik yaitu mendapatkan energinya
melalui proses oksidasi dari ion amonium. Reaksinya adalah sebagai berikut:
2NH4+ + 3O2 2NO2-+ 4H++ 2H2O + energi
bakteri
2NO2-+ O22NO3- + energi
bakteri
Nitrat (NO3-) adalah bentuk senyawa nitrogen yang merupakan sebuah senyawa yang
stabil. Nitrat merupakan salah satu unsur penting untuk sintesa protein tumbuh-tumbuhan dan
hewan, akan tetapi nitrat pada konsentrasi yang tinggi dapat menstimulasi pertumbuhan
ganggang yang tak terbatas (bila beberapa syarat lain seperti konsentrasi fosfat dipenuhi),
sehingga air kekurangan oksigen terlarut yang menyebabkan kematian ikan. NO3- dapat
berasal dari buangan industri bahan peledak, piroteknik, pupuk, cat dan sebagainya. Kadar
Nitrat secara alamiah biasanya agak rendah, namun kadar nitrat dapat menjadi tinggi sekali
pada air tanah di daerah-daerah yang diberi pupuk yang mengandung nitrat. Kadar nitrat tidak
boleh melebihi 10 mg NO3/L (di Indonesia dan A.S) (Alaert dan Sri Sumestri, 1984).
Analisa nitrat cukup sulit, karena rumit dan peka terhadap berbagai jenis gangguan.
Namun ada beberapa cara analisa yang tersedia antara lain:
1. Analisa spektrofotometris pada panjang gelombang 220 nm (sinar ultra ungu yang cocok
sebagai analisa penduga bagi air tanpa zat organis dengan kadar NO3-N antara 0,1 sampai 11
2. Analisa dengan elektroda khusus (dan pH meter) yang cocok sebagai analisa penduga baik
untuk air bersih maupun air buangan dengan skala kadar NO3-N antara 0,2 sampai 1400
mg/L.
3. Analisa dengan brusin untuk air dengan kadar 0,1 sampai 2 mg NO3-N/L.
4. Analisa dengan asam kromotropik untuk air dengan kadar 0,1 sampai 5 mg NO3-N/L.
5. Analisa dengan reduksi menurut Devarda untuk air dengan kadar NO3-N lebih dari 2 mg/L.
6. Analisa kolorimetris khusus bagi nitrit, setelah semua zat nitrat direduksi oleh butir kadmium
(Cd), metode ini cocok untuk air dengan kadar NO3-N antara 0,01 sampai 1 mg/L (Alaert dan
Sri Sumestri, 1984).
Dalam penelitian ini analisis nitrat dilakukan dengan metode brusin sulfat. Prinsip
dari pengujian nitrat nitrogen dengan metode brusin sulfat yaitu ion nitrat bereaksi
denganbrusin dalam suasana asam membentuk senyawaberwarna kuning. Jadi sampel yang
membentuk warna kuning pekat menunjukan konsentrasi nitrat nitrogen yang terkandung
pada sampel sangat besar, dan jika sampel yang diuji memiliki konsentrasi nitrat nitrogen
berada di luar kurva kalibrasi larutan standar maka sampel yang diuji harus diencerkan agar
bisa terbaca atau masuk dalam kurva kalibrasi.
Nitrat dalam jumlah besar dapat menyebabkan gangguan diare campur darah, disusul
oleh konvulsi, koma, dan bila tidak tertolong akan meninggal. Keracunan kronis dapat
menyebabkan depresi, sakit kepala. Methemoglobin adalah hemoglobin yang di dalamnya ion
Fe2+diubah menjadi ion Fe3+ dankemampuannya untuk mengangkut oksigen telah berkurang
dan menyebabkan darah menjadi coklat. Methemoglobin dapat terjadi apabila hemoglobin
terpapar oksidator termasuk nitrat. Sebenarnya darah manusia secara normal mengandung
methemoglobin pada konsentrasi tidak lebih dari 2% tetapi jika methemoglobin meningkat
menjadi 10%-20% akan mengakibatkan kemampuan darah untuk mengangkut oksigen
menjadi sangat terganggu. Darah mengandung methemoglobin yang tinggi disebut
methemoglobinemia dengan gejala tubuh berwarna biru (sianosis), sesak nafas, mual dan
70%.
Bayi pada umumnya lebih sensitif terhadap methemoglobin daripada orang dewasa.
Hal ini disebabkan beberapa faktor yakni:
1. Sebagian besar (60%) kandungan hemoglobin dalam darah bayi merupakan tipe yang sangat
peka terhadap nitrat.
2. Enzim methemoglobin reduktase yang terdapat dalam darah bayi untukmerubah
methemoglobin menjadi hemoglobin menjadi terbatas jumlahnya.
3. Percernaan bayi merupakan pH yang paling sensitif yang akan menjadi media yang baik
untuk pertumbuhan bakteri yang mengubah nitrat menjadi nitrit ( Harris dan Karmas, 1989).
Bakteri pereduksi nitrat dalam usus manusia atau hewan akan mengubah nitrat
menjadi nitrit. Nitrit tersebut akan mengoksidasi hemoglobin pada darah menjadi
methemoglobin yang tidak dapat mengikat oksigen. Walaupun nitrit penyebab masalah pada
tubuh manusia, namun karena sangat jarang dijumpai dalam makanan dan air maka standar
didasarkan pada nitrat yang dapat dijumpai pada makanan, air seperti halnya pada sayuran
daun dan bayam (Jenie dan Winiati, 1990).
Nitrit dan nitrat merupakan bentuk nitrogen yang teroksidasi, dengan tingkat oksidasi
masing-masing +3 dan +5. Nitrit biasanya tidak bertahan lama dan merupakan keadaan
sementara proses oksidasi antara amoniak dan nitrat, yang dapat terjadi pada instalasi
pengolahan air buangan, dalam air sungai dan sistem drainase, dan sebagainya. Nitrit sendiri
membahayakan kesehatan karena dapat bereaksi dengan hemoglobin dalam darah, hingga
darah tersebut tidak dapat mengangkut oksigen lagi. Di samping itu, NO2- juga menimbulkan
nitrosamin pada air buangan yang tertentu, nitrosamin tersebut dapat menyebabkan kanker
(Alaert dan Sri Sumestri, 1984).
Nitrit akan bereaksi dengan amino sekunder/tersier membentuk senyawa
N-nitrosamin yang bersifat mutagen dan karsinogen, selanjutnyaN-nitrosamine menunjukkan
kematian bila melebihi 15-20 mg/kg bobot badan yangmengkonsumsi. Nitrosamin adalah
Pada pH 2,0 – 2,5 berkaitan dengan hasil reaksi antara diazo asam Sulfanilatdan
N-1-naftil-etilendiamin dihidroklorida(NED dihidroklorida), maka akan terbentuk larutan berwarna
ungu kemerah-merahan. Warna tersebut mengikuti hukum Lambert-Beer dan menyerap sinar
pada panjang gelombang 543 nm. Metoda kolorimetris tersebut sangat peka, sehingga
biasanya perlu pengenceran sampel. Selain dari metoda ini, tidak ada cara analisa lain yang
dapat dianggap bersifat baku (Alaert dan Sri Sumestri, 1984).
Interferensi yang sering terjadi dalam analisis nitrit yaitu NCl3mengganggu warna
reaksi murni, tetapi jarang ditemui (hanya ada di dekat tempat proses klorinasi air minum)
dan dapat dihilangkan dengan penambahan Na2S2O3(natrium tiosulfat).
Kation-kation Fe3+, Pb2+, Hg2+, Ag2+, Sb3+, Au3+dan anion PtCl
62- dan VO32- juga
mengganggu analisa karena dapat mengendap selama analisa, kation-kation tersebut harus
dihilangkan. Gangguan Fe3+ dapa dihilangkan dengan mereduksi Fe3+dengan zat pereduksi
misalnya Na2S2O3sampai menjadi Fe2+, atau dengan mengendapkan Fe3+ sebagai Fe(OH)3
pada pH 7 sebelum analisa nitrit dimulai (Alaert dan Sri Sumestri, 1984).
2.5 Spektrofotometer UV-Vis
Spektrofotometri merupakan salah satu metode analisis instrumental yang didasarkan
pada interaksi radiasi elektromagnetik dengan atom maupun molekul suatu senyawa kimia.
Dengan mengetahui interaksi yang terjadi, dikembangkan teknik-teknik analisis kimia yang
beberapa peristiwa antara lain adalah: pemantulan, pembiasan/hamburan (scattering),
difraksi, penyerapan, (absorpsi), fluoresensi, fosforesensi dan emisi (Riyanto, 2009).
Spektrofotometer sesuai dengan namanya adalah alat yang terdiri dari spektrometer
dan fotometer. Spektrofotometer menghasilkan sinar dari spektrum dengan panjang
gelombang tertentu dan fotometer adalah alat pengukur intensitas cahaya yang ditransmisikan
atau yang diabsorpsi. Jadi spektrofotometer digunakan untuk mengukur energi secara relatif
jika energi tersebut ditransmisikan, direfleksikan atau diemisikan sebagai fungsi dari panjang
gelombang. Pada spektrofotometer, panjang gelombang yang benar-benar terseleksi dapat
diperoleh dengan bantuan alat pengurai cahaya seperti prisma. Suatu spektrofotometer
tersusun dari sumber spektrum tampak yang kontinu, monokromator, sel pengabsorpsi untuk
larutan sampel atau blanko dan suatu alat untuk mengukur perbedaan absorpsi antara sampel
dan blanko ataupun pembanding (Khopkar, 1990: 225).
Komponen-komponen pokok dari spektrofotometer meliputi:
1. Sumber radiasi
Sumber tenaga radiasi terdiri dari benda yang tereksitasi hingga ke tingkat tenaga yang tinggi
oleh sumber listrik bertenaga tinggi. Sumber radiasi ultraviolet yang banyak digunakan
adalah lampu hidrogen dan lampu deuterium. Sedangkan sumber radiasi visibleatau tampak
yang biasa digunakan adalah lampu filamen tungsten (Sastrohamidjojo, 2001).
2. Monokromator adalah suatu alat yang digunakan untuk memperoleh sumber sinar yang
monokromatis. Alatnya dapat berupa prisma atau grating. Untuk mengarahkan sinar
monokromatis yang diinginkan dari hasil penguraian ini dapat digunakan celah (Khopkar,
1990: 226). 3. Sel absorpsi
Pada pengukuran di daerah tampak kuvet kaca atau kuvet kaca corex dapat digunakan, tetapi
untuk pengukuran pada daerah UV harus menggunakan sel kuarsa karena gelas tidak tembus
cahaya pada daerah ini. Umumnya tebal kuvetnya adalah 10 mm. Sel yang bisa digunakan
Peranan detektor penerima adalah memberikan respon terhadap cahaya pada berbagai
panjang gelombang (Khopkar, 1990: 227).
Diagram sederhana dari spektrofotometer adalah sebagai berikut:
Sumber radiasi
sampel yang menyebabkan terjadinya transisi elektron suatu senyawa dari keadaan dasar
(ground state) yang energinya rendah ke keadaan tereksitasi (excited state) yang mempunyai
energi lebih tinggi. Frekuensi serapan tersebut dapat terukur dan menghasilkan spektra.
2.5.1 Persamaan Lambert-Beer
Jika suatu berkas melewati medium homogen, sebagian intensitas cahaya datang (Io)
diabsorpsi oleh medium sebesar Ia, sebagian intensitas dipantulkan sebesar Ir dan sisanya
ditransmisikan sebesar It.
Io = Ia + It + Ir...1)
Karena pada umumnya Ir sangat kecil maka Io = Ia + It.
Lambert (1760) dan Beer (1852) menunjukkan hubungan berikut:
T = = 10
-abc...2)dengan: T = transmitansi
a = tetapan absorbtivitas
b = jarak tempuh optik = tebal sampel
log
[
]
= log
[
]
= -abc
...3)atau A = abc...4)
dengan A = -log (T)
A disebut sebagai absorbansi larutan terhadap sinar ang dilewatkan.
Rumus (4) tersebut disebut sebagai rumus Lambert-Beer.
Dengan hukum Lambert-Beer ini, maka dengan mengukur absorbansi atau transmisi
dapat ditentukan kadar suatu zat bila tebal medium penyerap dan absorbsivitas diketahui.
Besarnya absorbsivitas ditentukan dengan cara mengukur absorbansi suatu zat yang sama
pada berbagai kadar yang telah diketahui. Kadar zat padat dinyatakan dalam berbagai cara
(misalnya, %, molar, gram/liter, miligram/100 ml, dll). Kemudian gambar dalam grafik, yang
menunjukkan hubungan antara absorbansi dan kadar, maka diperoleh kurva standar. Dari
kurva standar yang linear tersebut, dapat dihitung besarnya absorpsivitas yang merupakan
BAB III
METODE PENELITIAN
3.1 Alat
Alat-alat yang dipakai dalam percobaan ini antara lain:
1. Spektofotometer UV-Vis double beam, Shimadzu UV-1700
2. Pipet Ukur 2 mL
3. Labu Ukur 100 ml
4. Pipet Volume 10 mL, 50 mL
5. Erlenmeyer 50 mL, 100 mL
6. Kompor Listrik
7. Penangas air
8. Gelas Piala 100 mL
9. Kuvet
10. Bola Hisap
11. Corong Gelas
12. Pipet Mikro 100 µL
3.2 Bahan
Bahan-bahan yang digunakan dalam percobaan ini antara lain:
1. 5 sampel air bersih
2. Larutan induk NO3-N 1000 mg/L
3. Larutan campuran Brucin-asam sulfanilat
4. H2SO4 pekat
5. NaCl 30%
6. Akuadest
8. Larutan Asam Sulfanilat
9. Larutan N-1- Napthylethylene diamine dihidrochloride (NED dihidroklorida)
3.3 Cara Kerja
3.3.1 Pembuatan Larutan Standart
Pembuatan larutan standart nitrat NO3-N dengan tahapan sebagai berikut:
1. Sebanyak 0; 0,25; 0,50; 1,00 dan 2,00 mL larutan standar nitrat 100 mg/L dipipet dan
dimasukkan masing-masing ke dalam labu ukur 100 mL.
2. Air suling ditambahkan sampai tepat pada tanda tera sehingga diperoleh kadar nitrat-N 0,00;
0,25; 0,50; 1,00 dan 2,00 mg/L (SNI-06-2480-1991).
Pembuatan larutan standart nitrit NO2-N dengan tahapan sebagai berikut:
1. Sebanyak 0;0,01;0,02;0,05;0,10;0,15 dan 0,20 mL larutan standar nitrit 100 mg/Ldipipet dan
dimasukkan masing-masing ke dalam labu ukur 100 mL.
2. Air suling ditambahkan sampai tepat pada tanda tera sehingga diperoleh kadar nitrit-N
sebesar 0,00; 0,01; 0,02; 0,05; 0,10; 0,15 dan 0,20 mg/L (SNI-06-2484-1991).
3.3.2 Pembuatan Kurva Kalibrasi
Pembuatan kurva kalibrasi nitrat dengan tahapan sebagai berikut:
1. Alat spektrofotometer dioptimalkan sesuai petunjuk penggunaan alat untuk pengujian kadar
nitrat.
2. Sebanyak 10 mL masing-masing larutan standar dan blanko dimasukkan ke dalam labu
erlenmeyer 50 mL.
3. Sebanyak 2 mL larutan NaCl 30 % dan 10 mL larutan asam sulfat, ditambahkan ke dalam
masing-masing larutan tersebut, diaduk perlahan-lahan dan dibiarkan sampai dingin.
4. Sebanyak 0,5 mL larutan campuran brusin-asam sulfanilat ditambahkan aduk perlahan-lahan
dan dipanaskan diatas penangas air pada suhu tidak melebihi 95ºC selama 20 menit kemudian
dinginkan.
5. Masing-masing larutan dimasukkan ke dalam kuvet pada alat spektrofotometer, dibaca dan
dicatat serapannya pada panjang gelombang 410 nm.
6. Kurva kalibrasi dibuat dari hubungan antara serapan (A) Vs konsentrasi (C) dari larutan
Pembuatan kurva kalibrasi nitrit NO2-N dengan tahapan sebagai berikut:
1. Alat spektrofotometer dioptimalkan sesuai petunjuk penggunaan alat untuk pengujian kadar
nitrit.
2. Sebanyak 50 mL masing-masing larutan standar dan blanko dipipet kemudian dimasukkan ke
dalam labu erlenmeyer 100 mL.
3. Sebanyak 1 mL larutan asam sulfanilat ditambahkan dan dibiarkan larutan tersebut bereaksi
selama 2-8 menit.
4. Sebanyak 1 mL larutan NED dihidroklorida ditambahkan,diaduk dan dibiarkan paling sedikit
10 menit, tetapi tidak lebih dari 2 jam.
5. Masing-masing larutan dimasukkan ke dalam kuvet pada alat spektrofotometer, dibaca dan
dicatat serapannya pada panjang gelombang 543 nm.
6. Kurva kalibrasi dibuat dari hubungan antara serapan (A) dengan konsentrasi (C) dari larutan
standar nitrit dan tentukan persamaan garis lurusnya (SNI-06-2484-1991).
3.3.3 Penentuan Kadar NO3- dan NO2- pada Sampel Air bersih
Analisis kadar nitrat pada sampel air bersih dengan tahapan sebagai berikut:
1. Sebanyak 10 mL sampel air dengan salah satu sampel dibuat secara duplo dipipet dan
dimasukkan ke dalam labu erlenmeyer 50 mL.
2. Sebanyak 2 mL larutan NaCl 30 % dan 10 mL larutan asam sulfat ditambahkan, diaduk
perlahan-lahan dan dibiarkan sampai dingin.
3. Sebanyak 0,5 mL larutan campuran brusin-asam sulfanilat ditambahkan, diaduk
perlahan-lahan dan dipanaskan di atas penangas air pada suhu tidak melebihi 95ºC selama 20 menit
kemudian didinginkan.
4. Larutan sampel dimasukkan ke dalam kuvet pada alat spektrofotometer dan dibaca
absorbansinya pada panjang gelombang 410 nm.
5. Apabila perbedaan hasil pengukuran secara duplo lebih besar dari 2 %, periksa keadaan alat
dan diulangi tahapan 1 sampai dengan 4, apabila perbedaanya lebih kecil atau sama dengan 2
%, rata-ratakan hasilnya (SNI-06-2480-1991).
Rumus Perhitungan:
mg/L NO3-sebagai N = C × fp
C = konsentrasi yang didapat dari hasil pengukuran (mg/L)
Fp = faktor pengenceran
Analisis kadar nitrit pada sampel air bersih dengan tahapan sebagai berikut:
1. Sebanyak 50 mL sampel air dengan salah satu sampel dibuat secara duplo dipipet dan
dimasukkan ke dalam labu erlenmeyer 100 mL.
2. Sebanyak 1 mL larutan asam sulfanilat ditambahkan dan dibiarkan larutan tersebut bereaksi
selama 2-8 menit.
3. Sebanyak 1 mL larutan NED dihidroklorida ditambahkan,diaduk dan dibiarkan paling sedikit
10 menit, tetapi tidak lebih dari 2 jam.
4. Larutan sampel dimasukkan ke dalam kuvet pada alat spektrofotometer, dibaca dan dicatat
serapannya pada panjang gelombang 543 nm.
5. Apabila perbedaan hasil pengukuran secara duplo lebih besar dari 2 %, periksa keadaan alat
dan diulangi tahapan 1 sampai dengan 4, apabila perbedaanya lebih kecil atau sama dengan 2
%, rata-ratakan hasilnya (SNI-06-2484-1991).
Rumus Perhitungan:
mg/L NO2-sebagai N = C × fp
Dimana:
C = konsentrasi yang didapat dari hasil pengukuran (mg/L)
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil dan Pembahasan
Kegiatan PKL yang dilakukan di Balai Laboratorium Kesehatan Yogyakarta ini
meliputi analisis terhadap berbagai jenis sampel air dengan metode yang digunakan di
Laboratorium Kimia Air. Praktik kerja lapangan yang dilakukan di laboratorium kimia air
meliputi: analisis nitrat dan nitrit.
Pada laboratorium kimia air sampel didapat dari masyarakat yang akan menguji
berbagai parameter dari air minum, air bersih dan sampel air limbah yang kemudian diberi
nama sampel atau contoh uji tersebut dengan pemberian kode untuk memudahkan pengerjaan
di laboratorium.
Untuk mendapatkan data analisis yang akurat, diperlukan beberapa langkah penting
yang kadang-kadang kurang mendapatkan perhatian selama ini diantaranya: pengawetan
sampel dan metode analisis yang digunakan untuk memeriksa sampel. Banyaknya gangguan
yang timbul selama penyimpanan dan pengangkutan sampel dari lapangan ke laboratorium
dapat menyebabkan perubahan sampel dari keadaan aslinya. Oleh karena itu, perlu dilakukan
terhadap sampel yang akan dianalisis baik secara fisik maupun secara kimia agar keadaannya
tetap stabil. Cara pengawetan sampel tergantung dari jenis analisis yang akan dilakukan,
misalnya untuk analisis nitrat dan nitrit dalam air, pemeriksaan harus segera dilakukan setelah
pengambilan sampel. Kalau terpaksa diawetkan perlu penambahan asam sulfat pekat sampai
pH 2 kemudian didinginkan dalam lemari pendingin khusus pada suhu 4ºC atau dibekukan
pada suhu -20ºC dan sampel harus diperiksa maksimal 48 jam setelah dilakukan
penyamplingan. Hal ini disebabkan adanya oksigen terlarut dan bakteri-bakteri yang dapat
mengoksidasi ammonium (NH4+) menjadi nitrit (NO2-) atau nitrit (NO2-) menjadi nitrat
Untuk mengetahui kualitas dari air pada perairan, banyak sekali parameter yang
dianalisis. Parameter-parameter tersebut sudah ditetapkan oleh pemerintah melalui Peraturan
Menteri Kesehatan RI No. 416/MENKES/PER/IX/1990. Namun tidak semua parameter akan
ditentukan, hanya ada dua parameter yang dianalisis diantaranya adalah:
4.1.1 Analisis Nitrat
Tingginya kadar nitrat pada air bersih terutama yang berasal dari sungai atau sumur di
dekat pertanian. Hal ini sangat berbahaya bila kandungan nitrat ini dikonsumsi oleh anak bayi
dan dapat menimbulkan keracunan akut. Bayi yang baru berumur beberapa bulan belum
mempunyai keseimbangan yang baik antara usus dan bakteri usus. Sebagai akibatnya, nitrat
yang masuk dalam saluran pencernaan akan langsung diubah menjadi nitrit yang kemudian
berikatan dengan hemoglobin membentuk methemoglobin. Ketidakmampuan tubuh bayi
untuk mentoleransi adanya methemoglobin yang terbentuk dalam tubuh mereka akan
mengakibatkan timbulnya methemoglobinemia pada bayi.Methemoglobinemia juga disebut
"sindrom bayi biru". Penyakit ini disebut gejala bayi biru dengan gejala yang khas yaitu
terlihat warna kebiruan pada daerah sekitar bibir dan beberapa bagian tubuh. Pada bayi yang
telah berumur enam bulan atau lebih, bakteri pengubah nitrat di dalam tetap ada walau dalam
jumlah sedikit. Pada anak-anak dan orang dewasa, nitrat diabsorbsi dan di sekresikan
sehingga resiko untuk keracunan nitrat jauh lebih kecil.Oleh karena itu, parameter ini perlu
untuk dilakukan analisis.
Penentuan kadar nitrat dilakukan dengan metode spektrofotometer (SNI
06-2480-1991) pada kisaran kadar 0,1 mg/L – 2,0 mg/L dengan menggunakan metode brusin sulfat.
Prinsip dari percobaaan ini adalah Nitrat dalam air dalam suasana asam dengan Brusin
Sulfanilat dan Asam Sulfat membentuk senyawa yang berwarna kuning. Intensitas warna
yang terjadi diukur absorbansinya dengan spektrofotometer pada panjang gelombang 410
yang terkandung pada sampel sangat besar, dan jika sampel yang diuji memiliki konsentrasi
nitrat nitrogen berada di luar kurva kalibrasi larutan standar maka sampel yang diuji harus
diencerkan agar bisa terbaca atau masuk dalam kurva kalibrasi.
Konsentrasi nitrat dalam sampel air bersih diperoleh dengan cara absorbansi sampel
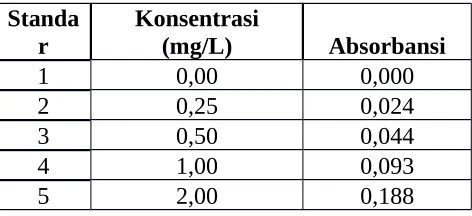
yang diukur dimasukkan ke dalam persamaan garis lurus larutan standar nitrat. Untuk itu
sebelum sampel air diuji, terlebih dahulu dibuat larutan standar dengan konsentrasi
masing-masing (0,00; 0,25; 0,50; 1,00; dan 2,00) mg/L dari larutan standar nitrat 100 mg/L. Larutan
standar ini berguna sebagai interval atau rentangan untuk menentukan apakah nilai absorban
sampel berada dalam rentangan larutan standar tersebut atau tidak. Untuk pembuatan kurva
kalibrasi masing-masing dari larutan standar yang telah dibuat kemudian diberi perlakuan
yang sama dengan blanko dan sampel air yang dianalisis. Setelah diukur dengan alat
spektrofotometer UV-Vis double beam atau berkas ganda maka dapat diketahui absorbansi
masing-masing larutan standar dan sampel air.
Tabel 2. Absorbansi larutan standar nitrat
Standa
Hubungan antara absorbansi larutan standar dengan konsentrasi yang dimiliki
masing-masing kemudian muncul sebagai kurva kalibrasi yang tampak pada gambar 1.
Gambar 1. Kurva larutan standar nitrat
Kurva kalibrasi pada gambar 1 memiliki persamaan garis regresi linear y = 0,0941x –
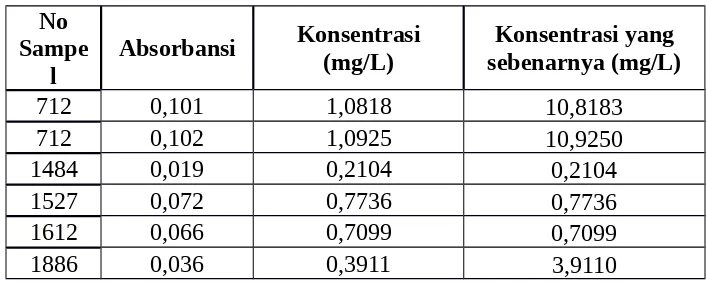
0,0008 dan memiliki nilai korelasi sebesar 0,9996. Kemudian kadar nitrat dapat dihitung
Tabel 3. Hasil analisis kadar nitrat
banyak. Selain itu tingginya kadar Nitrat disebabkan juga oleh limbah domestik dari lokasi
tersebut yang mengandung Amonia yang akan dioksidasi menjadi Nitrat, Sedangkan empat
sampel yang lain mengandung kadar nitrat di bawah ambang batas yang telah ditentukan
sehingga air tersebut masih layak digunakan untuk kebutuhan rumah tangga dan industri serta
masih dapat dikonsumsi.
4.1.2 Analisis nitrit
Kadar nitrit yang tinggi dapat membahayakan kesehatan karena dapat bereaksi dengan
hemoglobin dalam darah, hingga darah tersebut tidak dapat mengangkut oksigen lagi. Di
samping itu, NO2- juga menimbulkan nitrosamin pada air buangan yang tertentu, nitrosamin
tersebut dapat menyebabkan kanker.Maka parameter ini perlu untuk dilakukan analisis.
Penentuan kadar nitrit dilakukan dengan metode spektrofotometer (SNI
06-2484-1991) pada kisaran kadar 0,001 mg/L – 0,2 mg/L NO2-N dengan menggunakan metode asam
sulfanilat. Prinsip dari percobaaan ini adalah Nitrit dengan Asam Sulfanilat dan NED
merahkeunguan. Intensitas warna yang terjadi diukurabsorbansinyadengan spektrofotometer
pada panjang gelombang 543 nm.
Menurut Rilley dan Millero sebelum terbentuknya warna pink, terjadi pembentukkan
iondiazonium yang merupakan hasil reaksi dari nitrit dan sulfanilat yang terjadi menurut
reaksi berikut:
kondisi asam lemah pada pH 2,0 – 2,5 ion diazonium bereaksi dengan NED dihidroklorida
membentuk senyawa azo yang berwarna merah keunguan.
Konsentrasi nitrit dalam sampel air bersih diperoleh dengan cara absorbansi sampel
yang diukur dimasukkan ke dalam persamaan garis lurus larutan standar nitrit. Untuk itu
sebelum sampel air diuji, terlebih dahulu dibuat larutan standar dengan konsentrasi
masing-masing (0,00; 0,01; 0,02; 0,05; 0,10; 0,15 dan 0,20) mg/L dari larutan standar nitrat 100
mg/L. Larutan standar ini berguna sebagai interval atau rentangan untuk menentukan apakah
nilai absorbansi sampel berada dalam rentangan larutan standar tersebut atau tidak. Untuk
pembuatan kurva kalibrasi masing-masing dari larutan standar yang telah dibuat kemudian
diberi perlakuan yang sama dengan blanko dan sampel air yang dianalisis. Setelah diukur
dengan alat spektrofotometer UV-Vis double beam atau berkas ganda maka dapat diketahui
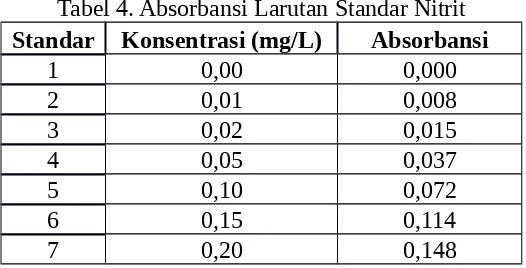
Tabel 4. Absorbansi Larutan Standar Nitrit
Hubungan antara absorbansi larutan standar dengan konsentrasi yang dimiliki
masing-masing kemudian muncul sebagai kurva kalibrasi yang tampak pada gambar 2.
Gambar 2. Kurva kalibrasi larutan standar nitrit
Kurva kalibrasi pada gambar 2 memiliki persamaan garis regresi linear y = 0,7435x –
0,0000 dan memiliki nilai korelasi sebesar 0,9994. Kemudian kadar nitrit dapat dihitung
dengan cara memasukkan absorbansi sampel yang terbaca dalam persamaan garis tersebut.
Tabel 4. Hasil analisis kadar nitrit
No Sampe
l
Absorbansi Konsentrasi(mg/L) sebenarnya (mg/L)Konsentrasi yang
712 0,002 0,0027 0,0027
Semua sampel yang telah dianalisis memiliki kadar nitrit dibawah ambang ambang
batas yang telah ditentukan di dalam PERMENKES RI No.416/MENKES/PER/IX/1990
kadar maksimal nitrit yang diperbolehkan di dalam air bersih adalah 1,0 mg/L.Menurut
Millero rendahnya konsentrasi nitrit disebabkan karena nitrit di perairan hanya sebagai
senyawa peralihan (intermediate product) dari reduksi senyawa nitrat atau oksidasi senyawa
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Berdasarkan percobaan yang telah dilakukan dalam analisis konsentrasi Nitrat (NO3-)
dan Nitrit (NO2-) dengan menggunakan sampel air bersih dapat disimpulkan sebagai berikut:
1. Dari perhitungan diperoleh kadar Nitrat (NO3-) adalah 10,8717 mg/L; 0,2104 mg/L; 0,7736
mg/L; 0,7099 mg/L dan 3,911 mg/L, sedangkan untuk kadar Nitrit (NO2-) adalah 0,0027
mg/L ; 0,0027 mg/L; 0,7130 mg/L; 0,0013 mg/L; dan 0,0013 mg/L.
2. Pada percobaan kadar nitrit semua sampel masih di bawah ambang batas yang telah
ditentukan sedangkan untuk kadar nitrat ada satu sampel yang melebihi baku mutu sehingga
PERMENKES RI No.416/MENKES/PER/IX/1990 yakni 10 mg/L untuk Nitrat (NO3-) dan
untuk Nitrit (NO2-) 1,0 mg/L.
5.2 Saran
Dalam analisisNitrat dan Nitrit ini penulis menyarankan agar menggunakan metode
atau instrumentasi yang lain yang dapat digunakan untuk mendukung validitas data tentang
kandungan zat pencemar dalam sampel air tersebut.
DAFTAR PUSTAKA
Achmad, R., 2004, Kimia Lingkungan, Penerbit Andi, Jakarta.
Alaerts, G. dan Santika, S.S., 1984, Metode Penelitian Air, Usaha Nasional, Surabaya.
Anonim, 2004, Metode Pengujian Kadar Nitrat dalam Air dengan Alat Spektrofotometer secara
Brusin Sulfat, SNI-06-2480-1991, BSN, Jakarta.
Anonim, 2004, Metode Pengujian Nitrit dalam Air dengan Alat Spektrofotometer secara Asam
Sulfanilat, SNI-06-2484-1991, BSN, Jakarta.
Anonim, 1990, Persyaratan Kualitas Air Bersih, Menteri Kesehatan RI, Jakarta.
Anonim, 2010, Persyaratan Kualitas Air Minum, Menteri Kesehatan RI, Jakarta.
Effendi, 2003, Telaah Kualitas Air Bagi Pengelolaan Sumber Daya Dan Lingkungan Perairan,
Kanisius, Yogjakarta.
Harris, R.S. dan Karmas, E., 1989, Evaluasi Gizi Pada Pengolahan Bahan Pangan, Penerbit ITB,
Bandung.
Jenie dan Winiati, 1990, Penanganan Limbah Industri Pangan, Institut Pertanian Bogor, Bogor.
Khopkar, S.M., 1990, Konsep Dasar Kimia Analitik, UI-press, Jakarta.
Millero, F.J., 2006, Chemical Oceanography, CRC press, Boca Raton.
Ompusunggu, H., 2009, Analisa Kandungan Nitrat Pada Air Sumur Gali Di Sekitar Tempat
Pembuangan Akhir (TPA) Sampah, skripsi, Program Sarjana, USU, Sumatera Utara.
Rilley, J.P., 1975, Analytical Chemistry of Sea Water,3, 2, 193-514.
Riyanto, 2009, Diktat Kuliah Kimia Analisis Instrumental 1, Prodi Kimia UII, Yogyakarta.
Sastrohamidjojo, H., 2001, Spektroskopi, Liberty, Yogyakarta.
LAMPIRAN
LAMPIRAN 1
PERHITUNGAN
Analisis Nitrat
Pengenceran Larutan Standart Nitrat
Diketahui : Konsentrasi larutan induk nitrat 1000 mg/L (M1)
Ditanya : Volume larutan induk (V1) jika konsentrasi larutan standar (M2)
100 mg/L ke dalam labu ukur 100 mL
Jawab :
Rumus Pengenceran : M1.V1 = M2.V2
M2= 100 mg/L
M1.V1 = M2.V2
1000 mg/L.V1 = 100 mg/L.100 mL
V1 = 10 mL
Ditanya : Volume larutan induk (V1) jika konsentrasi larutan standar (M2)
Diketahui :Konsentrasi larutan induk nitrit 1000 mg/L (M1)
Ditanya : Volume larutan induk (V1) jika konsentrasi larutan standar (M2)
100 mg/L ke dalam labu ukur 100 mL.
Jawab :
M2 = 100 mg/L
M1.V1 = M2.V2
1000 mg/L.V1 = 100 mg/L.100 mL
V1 = 10 mL
Diketahui :Konsentrasi larutan standar nitrit 100 mg/L (M1)
V1 = 0,20 mL
LAMPIRAN 3
PERHITUNGAN
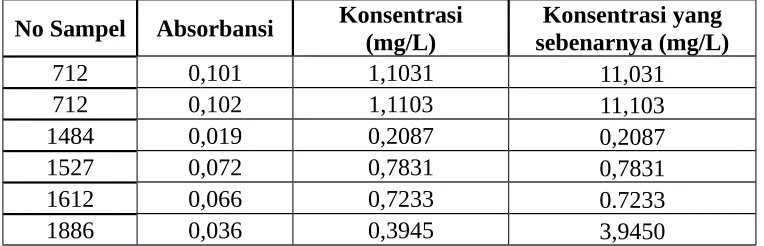
Analisis Kadar Nitrat
Tabel data :
No Sampel Absorbansi Konsentrasi
(mg/L)
Konsentrasi yang sebenarnya (mg/L)
712 0,101 1,1031 11,031
712 0,102 1,1103 11,103
1484 0,019 0,2087 0,2087
1527 0,072 0,7831 0,7831
1612 0,066 0,7233 0.7233
1886 0,036 0,3945 3,9450
Rumus Perhitungan:
mg/L NO3-sebagai N = C × fp
Dimana:
Fp = faktor pengenceran
1. No Sampel 712
Ada pengenceran 10× maka dikalikan dengan fp
C1= 1,1031 ; C2 = 1,1103
C = 1,1067
mg/L NO3-sebagai N = C × fp
mg/L NO3-sebagai N = 1,1067 × 10 = 11,067
2. No Sampel 1484
Tidak ada pengenceran maka tidak dikalikan dengan fp
mg/L NO3-sebagai N = C × fp
mg/L NO3-sebagai N = 0,2087 × fp = 0,2087
3. No Sampel 1527
Tidak ada pengenceran maka tidak dikalikan dengan fp
mg/L NO3-sebagai N = C × fp
mg/L NO3-sebagai N = 0,7831 × fp = 0,7831
4. No Sampel 1612
Tidak ada pengenceran maka tidak dikalikan dengan fp
mg/L NO3-sebagai N = C × fp
mg/L NO3-sebagai N = 0,7233 × fp = 0,7233
Ada pengenceran 10× maka dikalikan dengan fp
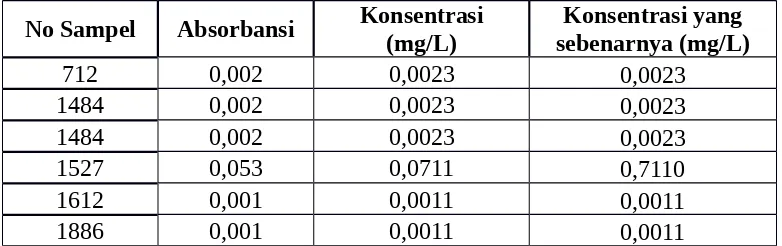
C = konsentrasi yang didapat dari hasil pengukuran (mg/L)
Fp = faktor pengenceran
1. No Sampel 712
Tidak ada pengenceran maka tidak dikalikan dengan fp
mg/L NO2-sebagai N = C × fp
mg/L NO2-sebagai N = 0,0023 × fp = 0,0023
2. No Sampel 1484
C1= 0,0023 ; C2 = 0,0023
C = 0,0023
mg/L NO2-sebagai N = C × fp
mg/L NO2-sebagai N = 0,0023 × fp = 0,0023
3. No Sampel 1527
Ada pengenceran 10× maka dikalikan dengan fp
mg/L NO2-sebagai N = C × fp
mg/L NO2-sebagai N = 0,0711 × 10 = 0,7110
4. No Sampel 1612
Tidak ada pengenceran maka tidak dikalikan dengan fp
mg/L NO2-sebagai N = C × fp
mg/L NO2-sebagai N = 0,0011 × fp = 0,0011
5. No Sampel 1886
Tidak ada pengenceran maka tidak dikalikan dengan fp
mg/L NO2-sebagai N = C × fp
mg/L NO2-sebagai N = 0,0011 × fp = 0,0011
LAMPIRAN 5
PERATURAN MENTERI KESEHATAN RI
NOMOR : 416/MENKES/PER/IX/1990
DAFTAR PERSYARATAN KUALITAS AIR BERSIH
2. Jumlah zat padat terlarut (TDS) mg/L 1500
3. Kekeruhan SkalaNTU 25
6. Kesadahan (CaCO3) mg/L 500
7. Klorida mg/L 600
8. Kromium, valensi 6 mg/L 0,05
9. Mangan mg/L 0,5
10. Nitrat, sebagai N mg/L 10
11. Nitrit, sebagai N mg/L 1,0
17. Timbal mg/L 0,05 b. Kimia Organik
1. Aldrin dan deildrin mg/L 0,0007
2. Benzene mg/L 0,01
3. Benzo (a) pyrene mg/L 0,00001
4. Chlordane (total isomer) mg/L 0,007
5. Chloroform mg/L 0,03
6. 2,4 - D mg/L 0,1
7. DDT mg/L 0,03
8. Deterjen mg/L 0,5
9. 1,2 - Dichloroethane mg/L 0,01
10. 1,1 - Dichloroethane mg/L 0,0003
11. Heptachlor dan heptachlor epoxide mg/L 0,03
12. Hexachlorobenzene mg/L 0,00001
1. Aktivitas Alpha (Gross Alpha Activity) Bq/L 0,1
2. Aktivitas Beta (Gross Beta Activity) Bq/L 1,0
mg : miligram
ml : mililiter
L : Liter
Bq : Bequerel
NTU : Nephelometrik Turbidity Units TCU : True Colour Units
Logam berat merupakan logam terlarut.
LAMPIRAN 6
Gambar-Gambar Percobaan Analisis Nitrat
Gambar 3. Spektrofotometer UV-VIS, Shimadzu UV 1700
Gambar 4. Sampel Air Bersih
Gambar 5. Sampel setelah penambahan NaCl 30%
Gambar 6. Sampel setelah penambahan Brusin-sulfanilat terbentuk larutan berwarna kuning
Diposkan oleh Ahmad Said di 10:56:00 AM
Kirimkan Ini lewat Email BlogThis! Berbagi ke Twitter Berbagi ke Facebook Bagikan ke Pinterest
Label: laporan - laporan
Tidak ada komentar:
Poskan Komentar
Posting Lebih BaruPosting LamaBeranda
What date is today?
Calendar
File's Blog
► 2016 (1)
► 2014 (15)
▼ 2013 (13)
o ► November (1)
o ► Juli (4)
o ▼ Juni (3)
contoh Laporan Praktik Kerja Lapangan (PKL)
Belajar Bahasa Arab Lagi
Inilah Rahasia Allah…
o ► Februari (5)
► 2012 (5)
Label
artikel (5)
fiksi (8)
laporan - laporan (1)
Renungan dan Motivasi Hidup (4)
soal - soal perkuliahan (12)
My profile
Enjoy with Music
divine-music.info
Total Tayangan Laman
Ahmad Said
Lihat profil lengkapku
Green Care
manusia yang peduli akan kehijauan dan berusaha menjaganya selalu
Google+
Followers
Tema Sederhana. Gambar tema oleh rocksunderwater. Diberdayakan oleh Blogger.
https://www.scribd.com/doc/180560728/LAPORAN-PELAKSANAAN-KULIAH-KERJA-LAPANGAN-pdf
PLTD