Pengaruh Variasi Jumlah Kitosan Terhadap
Karakterisasi Solid Polymer Electrolyte (SPE) Berbasis
Natrium Sulfit (Na2SO3) Pada Baterai Natrium-Ion
LAPORAN TUGAS AKHIR
Oleh:
Irvan Daniansyah
102216060
FAKULTAS TEKNOLOGI INDUSTRI
PROGRAM STUDI TEKNIK MESIN
UNIVERSITAS PERTAMINA
SEPTEMBER 2020
Universitas Pertamina - ii
Pe
ngar
uh
V
ariasi
Jumlah Kit
osan
Ter
had
ap
Ka
rakterisasi
Sol
id
P
ol
yme
r El
ec
trol
yt
e
(SP
E) B
er
basi
s Natrium
S
ulf
it
(N
a
2SO
3) Pad
a Bat
erai Na
trium
-Ion
Irvan D ani ans ya h 10 22 16 060Universitas Pertamina - ii
Pengaruh Variasi Jumlah Kitosan Terhadap
Karakterisasi Solid Polymer Electrolyte (SPE) Berbasis
Natrium Sulfit (Na2SO3) Pada Baterai Natrium-Ion
LAPORAN TUGAS AKHIR
Oleh:
Irvan Daniansyah
102216060
FAKULTAS TEKNOLOGI INDUSTRI
PROGRAM STUDI TEKNIK MESIN
UNIVERSITAS PERTAMINA
SEPTEMBER 2020
Universitas Pertamina - i
LEMBAR PENGESAHAN
Judul Tugas Akhir
:
Pengaruh Variasi Jumlah Kitosan Terhadap
Karakterisasi Solid Polymer Electrolyte (SPE)
Berbasis Natrium Sulfit (Na
2SO
3) Pada Baterai
Natrium-Ion
Nama Mahasiswa
: Irvan Daniansyah
Nomor Induk Mahasiswa
: 102216060
Program Studi
: Teknik Mesin
Fakultas
: Teknologi Industri
Tanggal Lulus Sidang Tugas Akhir : 11 September 2020
Jakarta, 16 September 2020
MENGESAHKAN
Pembimbing I
Pembimbing II
Dr. Eng. Sri Hastuty
Sylvia Ayu Pradanawati, Ph. D
NIP. 116104
NIP. 119031
MENGETAHUI,
Ketua Program Studi
Dr. Eng. Purwo Kadarno, S.T., M. Eng.
NIP. 116113
Universitas Pertamina - ii
LEMBAR PERNYATAAN
Dengan ini saya menyatakan bahwa Tugas Akhir berjudul Pengaruh Variasi Jumlah
Kitosan Terhadap Karakterisasi Solid Polymer Electrolyte (SPE) Berbasis
Natrium Sulfit (Na
2SO
3) Pada Baterai Natrium-Ion ini adalah benar-benar
merupakan hasil karya saya sendiri dan tidak mengandung materi yang ditulis oleh
orang lain kecuali telah dikutip sebagai referensi yang sumbernya telah dituliskan
secara jelas sesuai dengan kaidah penulisan karya ilmiah.
Apabila di kemudian hari ditemukan adanya kecurangan dalam karya ini, saya bersedia
menerima sanksi dari Universitas Pertamina sesuai dengan peraturan yang berlaku.
Demi pengembangan ilmu pengetahuan, saya menyetujui untuk memberikan kepada
Universitas Pertamina hak bebas royalti noneksklusif (non-exclusive royalty-free right)
atas Tugas Akhir ini beserta perangkat yang ada. Dengan hak bebas royalti
noneksklusif
ini
Universitas
Pertamina
berhak
menyimpan,
mengalih
media/formatkan, mengelola dalam bentuk pangkalan data (database), merawat, dan
mempublikasikan Tugas Akhir saya selama tetap mencantumkan nama saya sebagai
penulis/pencipta dan sebagai pemilik Hak Cipta.
Demikian pernyataan ini saya buat dengan sebenarnya
Garut, 15 September 2020
Yang membuat pernyataan,
Irvan Daniansyah
Universitas Pertamina - iii
ABSTRAK
Irvan Daniansyah. 102216060. Pengaruh Variasi Jumlah Kitosan Terhadap
Karakterisasi Solid Polymer Electrolyte (SPE) Berbasis Natrium Sulfit (Na
2SO
3) Pada
Baterai Natrium-Ion.
Penelitian ini tentang sintesis Solid Polymer Electrolyte (SPE) dengan tujuan untuk
mengetahui pengaruh variasi jumlah kitosan terhadap karakterisasi Solid Polymer
Electrolyte (SPE) serta mengetahui komposisi kitosan paling optimum yang dapat
diaplikasikan untuk Solid Polymer Electrolyte (SPE) berbasis natrium sulfit (Na
2SO
3)
pada baterai natrium-ion. Metode yang dipergunakan untuk membuat sampel adalah
casting yang kemudian di karakterisasi menggunakan X-Ray Diffraction (XRD),
Differential Scanning Calorimetry (DSC), dan Fourier Transform Infra-Red (FTIR).
Selanjutnya dilakukan analisis kualitatif dan kuantitatif menggunakan Electrochemical
Impedance Spectroscopy (EIS) dan juga pengujian tarik menggunakan Ultimate Machine
Testing (UTM). Hasilnya menunjukkan bahwa variasi jumlah kitosan mempengaruhi
karakterisasi Solid Polymer Electrolyte (SPE). Komposisi kitosan paling optimum yang
dapat diaplikasikan pada Solid Polymer Electrolyte (SPE) berbasis natrium sulfit
(Na
2SO
3) adalah 1 gram. Pada komposisi ini, SPE memiliki karakterisasi paling baik
karena memiliki konduktivitas ionik yang sudah memenuhi standar yakni sebesar
4.243 x 10-7 S cm-1.Pengujian DSC menunjukkan bahwa SPE tersebut memiliki titik leleh
118.5
0C. Sementara itu hasil pengujian tarik didapatkan nilai kuat tarik, elastisitas, dan
juga modulus young secara berturut-turut adalah 0.788 MPa, 13.3%, dan 0.059 MPa.
Kata kunci: solid polymer electrolyte (SPE), kitosan, Na
2SO
3,baterai natrium-ion,
Universitas Pertamina - iv
ABSTRACT
Irvan Daniansyah. 102216060. Pengaruh Variasi Jumlah Kitosan Terhadap
Karakterisasi Solid Polymer Electrolyte (SPE) Berbasis Natrium Sulfit (Na
2SO
3) Pada
Baterai Natrium-Ion.
This research is about the synthesis of Solid Polymer Electrolyte (SPE) with the
purpose to determine the effect of variations in the amount of chitosan on the
performance of Solid Polymer Electrolyte (SPE) and to determine the optimum
composition of chitosan that can be applied to Solid Polymer Electrolyte (SPE) based
on sodium sulfite (Na2SO3) in batteries. sodium-ion. The method used to make the
sample is casting which is then characterized using X-Ray Diffraction (XRD),
Differential Scanning Calorimetry (DSC), and Fourier Transform Infra-Red (FTIR).
Furthermore, qualitative and quantitative analyzes were carried out using
Electrochemical Impedance Spectroscopy (EIS), as well as tensile testing use Ultimate
Machine Testing (UTM). The results show that variations in the amount of chitosan
affect the performance of Solid Polymer Electrolyte (SPE). The optimum composition
of chitosan that can be applied to Solid Polymer Electrolyte (SPE) based on sodium
sulfite (Na2SO3) is 1 grams. In this composition, SPE has the best characterization
because it has the standar ionic conductivity, which is 4.243 x 10
-6 S cm-1. DSC test shows
that the SPE has a melting point of 118.5
0C. Meanwhile, the tensile test results showed
that the tensile strength, elasticity, and modulus young values were 0.788 MPa, 13.3%,
and 0.059 MPa, respectively.
Keyword:
solid polymer electrolyte (SPE), chitosan, Na
2SO
3,sodium-ion battery,
Universitas Pertamina - v
KATA PENGANTAR
Alhamdulillahirobbil’alamin. Puji syukur penulis panjatkan kepada Allah SWT
yang telah melimpahkan rahmat dan karunia-Nya sehingga naskah skripsi berjudul
“PENGARUH VARIAS JUMLAH KITOSAN TERHADAP KARAKTERISASI SOLID
POLYMER ELECTROLYTE (SPE) BEBASIS NATRIUM SULFIT (Na
2SO
3) PADA
BATERAI NATRIUM-ION” dapat diselesaikan dengan baik. Tulisan ini tidak akan
terwujud dengan baik tanpa bantuan dan dukungan dari semua pihak. Untuk itu
penulis mengucapkan berterima kasih yang sebesar-besarnya kepada:
1. Kedua orang tua yang tidak pernah henti memberikan semangat, dukungan
serta doa dalam penyusunan skripsi ini.
2. Dr. Eng. Sri Hastuty dan Sylvia Ayu Pradanawati, Ph.D., selaku dosen
pembimbing I dan II yang telah memberikan pengarahan dan bimbingan selama
proses penyusunan naskah skripsi ini.
3. Seluruh laboran yang telah membantu pengambilan data saat penulis
melaksanakan penelitian.
4. Seluruh dosen Teknik Mesin khususnya Muhammad Akbar Barrinaya MT.,
selaku dosen wali penulis yang telah memberikan semangat dan masukan
selama proses belajar di Universitas Pertamina.
5. Seluruh teman-teman di Universitas Pertamina, khususnya di Teknik Mesin
Angkatan 2016.
Penulis menyadari bahwa penulisan naskah tugas akhir ini tidak lepas dari
kekurangan. Oleh karena itu, penulis terbuka terhadap kritik dan saran yang
membangun. Semoga tugas akhir ini memberikan manfaat bagi penulis dan pembaca.
Jakarta, 21 Agustus 2020
Universitas Pertamina - vi
DAFTAR ISI
LEMBAR PENGESAHAN ... ii LEMBAR PERNYATAAN ... ii ABSTRAK ... iii ABSTRACT ...iv KATA PENGANTAR ... vDAFTAR ISI ...vi
DAFTAR TABEL ... viii
DAFTAR GAMBAR ... ix DAFTAR SINGKATAN ... xi BAB I PENDAHULUAN ... 2 1.1 Latar Belakang ... 2 1.2 Rumusan Masalah ... 4 1.3 Batasan Masalah ... 4 1.4 Tujuan Penelitian ... 5 1.5 Manfaat Penelitian ... 5 1.6 Lokasi Penelitian ... 5
1.7 Waktu Pelaksanaan Penelitian ... 5
BAB IITINJAUAN PUSTAKA ... 8
2.1 Baterai Natrium-ion ... 8
2.2 Solid Polymer Electrolyte (SPE) ... 10
2.3 Kitosan ... 12
2.4 Natrium Sulfit (Na2SO3) ... 13
2.5 Sifat Fisis Material ... 14
2.6 Sifat Mekanis Material ... 15
2.7 X-Ray Diffraction (XRD) ... 17
2.8 Differential Scanning Calorimetry (DSC) ... 19
2.9 Fourier Transform Infra-Red (FTIR) ... 20
2.10 Electrochemical Impedance Spectroscopy (EIS) ... 23
BAB III METODE PENELITIAN ... 26
Universitas Pertamina - vii
3.2 Bentuk Penelitian ... 27
3.3 Metode Pengumpulan Data ... 27
3.4 Alat dan Bahan ... 27
3.5 Metode Analisis Data ... 27
3.5.1 pembuatan film ... 27
3.5.2 karakterisasi dan analisis sampel film ... 28
BAB IV HASIL DAN PEMBAHASAN ... 31
4.1 Hasil Sintesis Solid Polymer Electrolyte (SPE) ... 31
4.2 Hasil Karakterisasi Kristal Menggunakan XRD ... 32
4.3 Hasil Analisis Thermal Menggunakan DSC ... 34
4.4 Hasil Karakterisasi Gugus Fungsi Menggunakan FTIR ... 36
4.5 Hasil Analisis Konduktivitas Menggunakan EIS ... 40
4.6 Hasil Uji Tarik ... 44
4.7 Penentuan Karakterisasi SPE Terbaik ... 47
BAB V KESIMPULAN DAN SARAN... 50
5.1 Kesimpulan ... 50
5.2 Saran ... 50
DAFTAR PUSTAKA ... 52
Universitas Pertamina - viii
DAFTAR TABEL
Tabel 2. 1 Perbandingan Karakteristik Lithium dan Natrium ... 8
Tabel 2. 2 Perbandingan Karakteristik Baterai Natrium-ion Dengan Baterai Lithium Ion... 9
Tabel 2. 3 Perbedaan Tegangan Standar Baterai Natrium-ion dan Lithium Ion ... 10
Tabel 2. 4 Perbandingan Harga dan Radius Anion Garam Untuk Penggunaan SPE ... 13
Tabel 2. 5 Daerah Frekuensi Untuk Gugus Fungsi Organik ... 22
Tabel 2. 6 Serapan FTIR Karakterisasi untuk Kitin dan Kitosan ... 23
Tabel 3. 1 Variasi Kitosan pada Sampel Pengujian ... 28
Tabel 4. 1 Hasil Pembacaan Kurva DSC ... 36
Tabel 4. 2 Panjang Gelombang Daerah Absorpsi FTIR Pada Berbagai Variasi SPE ... 38
Tabel 4. 3 Perbandingan Parameter Sirkuit Model Masing-masing SPE………. 41
Tabel 4. 4 Nilai Resistensi Bulk dan Konduktivitas Ionik untuk Masing-masing SPE ... 42
Tabel 4. 5 Hubungan Ketebalan (mm) dengan Nilai Konduktivitas Ionik (S cm-1) ... 43
Tabel 4. 6 Hasil Uji Tarik dari Beberapa Variasi SPE ... 45 Tabel 4. 7 Rangkuman Parameter Hasil Karakterisasi dan Analisis pada Masing-masing SPE 48
Universitas Pertamina - ix
DAFTAR GAMBAR
Gambar 2. 1 Prinsip Kerja Baterai Natrium-ion (Pan, Hu, & Chen, 2013) ... 9
Gambar 2. 2 Salah Satu Contoh Solid Polymer Electrolyte yang terbuat dari PEO/NaClO4 (Ni’mah, Cheng, Cheng, Rick, & Bing-Joe, 2014) ... 11
Gambar 2. 3 Perbedaan Struktur Kitin dan Kitosan (Yahya & Arof, 2002) ... 13
Gambar 2. 4 Struktur crystalline pada SiO2 (Callister, 2007) ... 14
Gambar 2. 5 Struktur noncrystalline (amorphous) pada SiO2 (Callister, 2007) ... 14
Gambar 2. 6 Hubungan Stress dan Strain dalam Membentuk Modulus Young (Callister, 2007) ... 16
Gambar 2. 7 Hubungan Stress dan Strain Pada Material Brittle & Ductile (Callister, 2007) ... 16
Gambar 2. 8 Diagram Skematis Difraksi Sinar X Berdasarkan Persamaan Braag... 17
Gambar 2. 9 Fenomena Destruktif Pada XRD (Callister, 2007) ... 18
Gambar 2. 10 Fenomena Konstruktif Pada XRD (Callister, 2007) ... 18
Gambar 2. 11 Skema perubahan fasa yang diakibatkan oleh perubahan termal pada pengujian DSC (Skoog, Holler, & Crouch, 2007). ... 19
Gambar 2. 12 Hasil Pengujian DSC pada Beberapa Komposisi SPE Berbahan dasar PEO (Ni’mah, Cheng, Cheng, Rick, & Bing-Joe, 2014) ... 20
Gambar 2. 13 Skema Alat Spektroskopi IR (1) Sumber inframerah, (2) Pembagi berkas (beam spliter), (3) Kaca pemantul, (4) Sensor inframerah, (5) Sampel, (6) Display (Anam, Sirojudin, & Firdausi, 2007) ... 21
Gambar 2. 14 Pola Hasil Pengujian FTIR pada Kitosan Murni dan juga Kitosan-litium (Asnin, et al., 2016) ... 21
Gambar 2. 15 Contoh Kurva Impedansi dari SPE dengan Komposisi Kitosan-ZrO2-LiClO4- Gliserol (Yulianti, Luthfiah, & Sudaryanto, 2017) ... 24
Gambar 4. 1 Hasil Sintesis SPE dengan CH3COOH 5%, Sorbitol 40%, Na2SO3 40%, dan Kitosan dengan Variasi (a) 0.25 gram, (b) 0.5 gram, (c) 0.75 gram (d) 1 gram, dan (e) 1.25 gram. ... 31
Gambar 4. 2 Sampel SPE yang Telah di Tumbuk Halus untuk Pengujian XRD ... 32
Gambar 4. 3 Hasil Karakterisasi SPE Menggunakan XRD ... 32
Gambar 4. 4 Hasil Pengujian DSC pada SPE dengan Variasi Jumlah Kitosan ... 35
Gambar 4. 5 Hasil Karakterisasi Gugus Fungsi Pada SPE Menggunakan FTIR... 37
Gambar 4. 6 Skematik Ikatan Silang Antara Kitosan dengan Natrium Sulfit ... 39
Gambar 4. 7 Plot impedansi Z real vs Z imaginer Berbagai Variasi SPE Pada Suhu Ruang ... 40
Gambar 4. 8 Sirkuit Model Pengujian EIS Pada SPE Dengan Kandungan Kitosan: (a) 0.25 gram, (b) 0.5 gram, (c) 0.75 gram, (d) 1 gram, dan (e) 1.25 Gram di Room Temperature………41
Universitas Pertamina - x Gambar 4. 10 Hasil Sintesis Untuk Uji Tarik Dengan Standar ASTM D-638 ... 44 Gambar 4. 11 Hubungan Beban Maksimum (N) Vs Elongasi (%) pada SPE dengan Kandungan Kitosan 1 gram ... 45 Gambar 4. 12 Hubungan Penambahan Konsentrasi Kitosan Pada SPE Terhadap Sifat Mekanis Kuat Tarik dan Elongasi ... 46
Universitas Pertamina - xi
DAFTAR SINGKATAN
Lambang/Singkatan Arti Keterangan
SPE Solid Polimer Electrolyte
Na2SO3 Natrium Sulfit
CH3COOH Asam Asetat
XRD X-Ray Diffraction
FTIR Fourier Transform Infra-Red
DSC Differential Scanning Calorimetry
Universitas Pertamina - 2
BAB I
PENDAHULUAN
1.1
Latar Belakang
Seiring dengan kebutuhan energi yang terus meningkat, dibutuhkan suatu teknologi penyimpanan energi yang handal dan efisien. Terlebih lagi saat ini trend penggunaan pembangkit listrik energi terbarukan dan kehadiran mobil listrik setiap tahunnya cenderung terus meningkat (Yuspandi, 2020). Sejauh ini baterai lithium ion masih mendominasi penggunaan penyimpanan energi di seluruh dunia. Hal ini dikarenakan baterai lithium ion dapat digunakan secara berulang-ulang (rechargeable), memiliki densitas energi yang tinggi, serta muatan yang ada dalam baterai akan lamban hilangnya saat perangkat tidak digunakan (Taib & Idris, 2014).
Cadangan lithium saat ini semakin berkurang dan diprediksi akan habis dalam kurun waktu 50 tahun dari sekarang (Yuspandi, 2020). Padahal lithium ini merupakan bahan utama pembuatan baterai lithium ion. Selain persediaannya yang semakin menipis, persebaran lithium yang ada di dunia juga bisa dikatakan tidak merata. Hampir 70% dari total cadangan lithium yang ada di dunia berada di Amerika Selatan, tepatnya di negara Chile, Argentina dan Bolivia (Pan, Hu, & Chen, 2013). Berdasarkan hal tersebut, sudah semestinya dicari material alternatif yang melimpah, murah, dan menunjukkan kinerja yang baik untuk dapat menggantikan litium sebagai unit penyimpanan energi di masa depan.
Salah satu material yang diproyeksikan dapat menggantikan lithium di masa yang akan datang adalah natrium. Selain karena ada kesamaan antar sifat fisik dan kimianya dengan lithium (Pan, Hu, & Chen, 2013), natrium juga harganya jauh relatif lebih murah dan ketersediaan nya di alam cukup melimpah (Hwang, Myung, & Sun, 2017). Oleh karena itu baterai natrium-ion sangat potensial untuk diterapkan sebagai media penyimpanan energi yang handal, efisien, dan juga ekonomis di masa yang akan datang.
Baterai natrium-ion sebenarnya bukanlah hal yang baru di bidang penyimpanan energi. Baterai jenis ini sudah dikembangkan sejak tahun 1970 yang lalu. Namun dikarenakan baterai natrium menghasilkan tegangan yang lebih rendah daripada baterai lithium ion, maka baterai lithium ion dikomersialisasikan terlebih dahulu (Widowati, 2020). Pada tahun 2015, baterai natrium ion mulai menjadi perhatian berbagai pihak dikarenakan sejumlah ilmuwan dari berbagai universitas di Prancis telah berhasil membuat prototipe baterai jenis ini (CNRS, 2020). Kemudian pada tahun 2017, sebuah perusahaan start-up yang bertempat di Amiens yaitu Tiamat melanjutkan hasil penelitian para ilmuwan Prancis tersebut. Jika dibandingkan dengan baterai lithium yang memiliki
Universitas Pertamina - 3 jangka waktu pemakaian 3-4 tahun, Tiamat mengklaim bahwa baterai natrium ion memiliki jangka waktu pemakaian yang lebih panjang yaitu 10 tahun (CNRS, 2020).
Melihat potensinya yang begitu menjanjikan, maka baterai natrium-ion lambat laun akan menggantikan peran baterai lithium-ion sebagai media penyimpanan energi di masa yang akan datang. Terlebih lagi ketersediaan natrium yang ada di bumi sangat melimpah, yaitu 2.6%. Hal ini jauh lebih besar jika dibandingkan dengan ketersediaan lithium di bumi yang hanya mencapai 0.06% (CNRS, 2020). Salah satu sumber terbesar penghasil natrium adalah air laut. Sekitar 86% kandungan air laut merupakan natrium klorida (NaCl) (James Murray, 2004 dalam Paweka, 2017). Indonesia yang merupakan negara dengan luas lautan mencapai 3.351 juta km2 (Badan Pusat Statistik, 2018) sudah dipastikan mempunyai
cadangan natrium yang sangat besar. Oleh karena itu, untuk mengoptimalkan hal tersebut Indonesia harus selangkah lebih maju daripada negara lainnya dalam riset mengenai baterai natrium-ion.
Secara umum ada tiga komponen utama yang menjadi penyusun dari sebuah baterai yaitu anode, katode, dan juga elektrolit. Dalam pengembangan baterai natrium ion, salah satu tantangan yang dihadapi sampai sekarang adalah belum ditemukannya material elektrolit yang memiliki nilai konduktivitas ionik Na yang tinggi, konduktivitas listrik yang memadai, dan juga stabil secara kimia, mekanik, dan elektrokimia (Yuspandi, 2020).
Elektrolit cair yang saat ini umum digunakan pada baterai ternyata memiliki beberapa kekurangan seperti rentan terhadap kebocoran sehingga mudah meledak, bersifat racun, harganya mahal, dan juga stabilitas kimianya yang buruk (Prihandoko, 2008). Terlebih lagi natrium cair memiliki sifat reaktif dan akan sangat mudah meledak jika terkena air (Widowati, 2020) sehingga ditinjau dari faktor keamanannya kurang memungkinkan jika baterai natrium ion menggunakan elektrolit cair sebagai media transfer ion natrium nya. Salah satu solusi dari permasalahan tersebut yaitu mengganti elektrolit cair dengan elektrolit padat seperti Solid Polymer Electrolyte (SPE) yang jauh lebih aman. Hanya saja SPE juga memiliki kekurangan berupa rendahnya konduktivitas ion pada suhu ruang sehingga menjadi kurang efisien jika langsung diaplikasikan pada baterai natrium ion (Linden & Reddy, 2002). Diperlukan beberapa treatment khusus supaya nilai konduktivitas ion yang dibutuhkan memenuhi nilai standar minimum.
Berbagai penelitian telah dilakukan untuk mencari bahan SPE yang paling optimal sehingga memungkinkan (feasible) untuk diaplikasikan pada baterai, khususnya pada baterai natrium ion. Hanya saja sampai dengan saat ini masih belum ditemukan suatu bahan pembuat SPE yang dapat memenuhi nilai konduktivitas ion minimum yang dibutuhkan. Salah satu bahan yang bisa digunakan untuk pembuatan SPE ini adalah polimer yang berasal dari alam dan juga limbah. Hal ini dikarenakan bahan tersebut
Universitas Pertamina - 4
biodegradable, tidak beracun, dan juga murah (Vishakha S., Kishor D., & Sudha S., 2012).
Dikarenakan limbah sangat erat kaitannya dengan isu lingkungan, maka pada penelitian ini akan dibuat SPE yang terbuat dari limbah berpolimer. Selain untuk mengatasi permasalahan lingkungan yang ada, penelitian ini juga bertujuan agar limbah memiliki nilai tambah berupa pemanfaatannya menjadi energi (waste to energy).
Salah satu limbah yang sangat potensial untuk digunakan sebagai bahan pembuat SPE adalah limbah kitin. Selain produksi limbahnya yang mencapai 17000 ton setiap tahunnya di Indonesia (KKP, 2015), kitin juga merupakan bahan dasar dari kitosan yang mana merupakan polimer dan sangat memungkinkan untuk diaplikasikan sebagai bahan pembuat SPE. Dengan penambahan Asam Asetat (CH3COOH), sorbitol, dan garam berupa
Natrium Sulfit (Na2
SO
3) diharapkan SPE yang akan dibuat memiliki nilai konduktivitasyang memadai, fleksibilitas yang baik, dan feasible untuk diaplikasikan.
Dikarenakan belum diketahuinya komposisi jumlah kitosan paling optimum untuk dapat menghasilkan SPE yang paling baik, maka penelitian ini dilakukan untuk mengetahui jumlah kitosan optimum supaya dihasilkan SPE yang memiliki nilai konduktivitas tinggi, fleksibilitas yang baik, dan juga tidak mudah terbakar.
1.2 Rumusan Masalah
Berdasarkan latar belakang, maka rumusan masalah untuk penelitian ini adalah sebagai berikut:
1. Bagaimana pengaruh variasi jumlah kitosan terhadap karakterisasi Solid Polymer
Electrolyte (SPE) berbasis Natrium Sulfit (
Na
2SO
3) pada baterai natrium-ion?2. Berapa komposisi kitosan optimum yang bisa diaplikasikan pada Solid Polymer
Electrolyte (SPE) berbasis Natrium Sulfit (
Na
2SO
3) pada baterai natrium-ion?1.3 Batasan Masalah
Polimer kitosan yang digunakan pada penelitian ini memiliki mesh 100 dengan kemurnian 98%. Pelarut yang digunakan untuk melarutkan serbuk kitosan adalah larutan asam asetat 5%. Untuk meningkatkan konduktivitas ion digunakan garam berupa natrium sulfit 40% (b/b) dengan campuran sorbitol 40% (b/b) (Hartono, 2018). Variasi yang dilakukan dalam penelitian ini adalah jumlah kitosan: 0.25 gram, 0.5 gram, 0.75 gram, 1 gram, dan 1.25 gram. Setelah itu, campuran tersebut dicetak pada teflon casting berdiamer 20mm dengan kedalaman 2mm (Ni’mah, et. al., 2014) dan juga teflon dengan desain mengikuti ASTM D 1882 – 99 tipe L untuk uji tarik (ASTM D 1882 - 99, 2013). Campuran tersebut selanjutnya akan dikeringkan pada suhu ruang sampai terbentuk sebuah film untuk selanjutnya dilakukan karakterisasi dan pengujian.
Universitas Pertamina - 5
1.4 Tujuan Penelitian
Tujuan dari penelitian ini adalah untuk:
1. Mengetahui pengaruh variasi jumlah kitosan terhadap karakterisasi Solid Polymer
Electrolyte (SPE) berbasis Natrium Sulfit (
Na
2SO
3).2. Mengetahui komposisi kitosan paling optimum yang bisa diaplikasikan pada Solid
Polymer Electrolyte (SPE) berbasis Natrium Sulfit (
Na
2SO
3).1.5 Manfaat Penelitian
1. Universitas Pertamina
a. Menambah literatur mengenai pengaruh variasi jumlah kitosan pada Solid Polymer
Electrolyte sebagai bahan kajian bagi mahasiswa-mahasiswa Universitas
Pertamina.
b. Menghasilkan publikasi penelitian di tingkat universitas.
2. Peneliti
a. Sebagai salah satu syarat kelulusan dari Program Studi Teknik Mesin Universitas Pertamina.
b. Mendapatkan pengetahuan dan penerapan ilmu material sciences, energy storage, dan juga elektrolit padat berbasis polimer untuk diaplikasikan pada Solid Polymer
Electrolyte (SPE).
c. Menghasilkan publikasi dari penelitian yang sudah dilakukan di tingkat lokal maupun internasional untuk bidang ilmu yang berhubungan.
1.6 Lokasi Penelitian
Penelitian ini dilaksanakan di Laboratorium Kimia Terintegrasi Universitas Pertamina, Laboratorium Operasi Teknik Kimia (OTK) Universitas Pertamina, Laboratorium Material
& Science Universitas Pertamina, Laboratorium Teknik Geologi Universitas Pertamina, dan
Laboratorium Biofisik, Departemen Fisika – FMIPA IPB.
1.7 Waktu Pelaksanaan Penelitian
Penelitian ini dilaksanakan dari bulan Januari hingga bulan Agustus 2020. Berikut ini merupakan rincian kegiatan yang telah dilakukan dalam hitungan minggu.
Universitas Pertamina - 6 Tabel 1. 1 Waktu Pelaksanaan Penelitian
Kegiatan Januari Februari Maret April - Juni Juli Agustus
I II III IV I II III IV I II III IV I II III IV I II III Persiapan alat dan bahan Perizinan Laboratorium Pembuatan Sampel Film (Sintesis) 1 Pengujian XRD 1 Amplas Stainless
Steel Teflon Rod
Pembuatan Sampel Film (Sintesis) 2 Tinjauan Pustaka Seminar Kemajuan Perizinan Laboratorium Pembuatan Sampel Film (Sintesis) 3 Pengujian EIS Pengujian FTIR Pengujian XRD 2 Pelaksanaan Uji Tarik Pengujian DSC Pengujian SEM Analisis Data & Penyusunan
Universitas Pertamina - 8
BAB II
TINJAUAN PUSTAKA
2.1 Baterai Natrium-ion
Baterai Natrium-ion merupakan baterai yang diproyeksikan akan menggantikan baterai lithium ion di masa yang akan datang. Hal ini dikarenakan persediaan lithium semakin menipis dan diprediksi akan habis dalam kurun waktu 50 tahun dari sekarang (Yuspandi, 2020). Selain itu, persebaran lithium yang ada di dunia juga tidak merata karena hampir 70% dari total cadangan lithium yang ada di dunia berada di Amerika Selatan (Pan, Hu, & Chen, 2013). Selain karena ada kesamaan sifat fisik dan kimia antara natrium dengan lithium (Pan, Hu, & Chen, 2013), natrium juga harganya jauh relatif lebih murah dan ketersediaan nya di alam cukup melimpah (Hwang, Myung, & Sun, 2017) yaitu 2.6%. Hal ini jauh lebih besar jika dibandingkan dengan ketersediaan lithium di bumi yang hanya mencapai 0.06% saja (CNRS, 2020). Oleh karena itu baterai natrium-ion sangat potensial untuk diterapkan sebagai media penyimpanan energi yang handal, efisien, dan juga ekonomis di masa yang akan datang.
Tabel 2. 1 Perbandingan Karakteristik Lithium dan Natrium
Parameter Lithium Natrium
Jari-jari kation (pikometer) 68 97
Berat atom (gram/mol) 6.9 23
Densitas (g/cm3) 0.354 0.97
Titik leleh (oC) 180.5 97.7
Ketersediaan di bumi (%) 0.06 2.6
Distribusi 70% di Amerika Selatan Tersebar merata di dunia
Harga ($/ton karbonat) 5000 150
Sumber: (Pan, Hu, & Chen, 2013) dan (Eshetu, et al., 2020)
Seperti baterai pada umumnya, baterai natrium-ion juga tersusun atas tiga komponen utama yaitu, anode, katode, dan juga elektrolit. Anode merupakan elektrode negatif sementara katode adalah elektrode positif. Kedua elektrode ini harus dipisahkan oleh separator supaya tidak terjadi short-circuit. Sedangkan elektrolit memiliki fungsi sebagai media untuk terjadinya proses perpindahan ion natrium. Secara umum, baterai Natrium-ion ini memiliki prinsip kerja yang sama dengan baterai Lithium-Natrium-ion. Perbedaan mendasarnya hanya terletak pada ion yang dibawa dalam perpindahan nya. Jika pada baterai lithium-ion terjadi perpindahan ion lithium, maka pada baterai natrium-ion
Universitas Pertamina - 9 natrium akan terjadi perpindahan ion natrium saat proses charging ataupun discharging terjadi. Skema nya bisa dilihat pada gambar di bawah ini.
Gambar 2. 1 Prinsip Kerja Baterai Natrium-ion (Pan, Hu, & Chen, 2013)
Pada baterai natrium-ion sekunder, akan terjadi proses charging (pengisian) dan juga
discharging (penggunaan). Saat proses charging, elektron dan juga ion natrium akan
berpindah dari katode menuju anode. Sementara saat proses discharging maka elektron dan juga ion natrium akan mengalami perpindahan dari anode menuju ke katode. Ion natrium akan berpindah melalui elektrolit sementara elektron akan berpindah melalui sirkuit luar. Proses ini terus berulang sampai terbentuk siklus tertentu. Jika dibandingkan dengan baterai Lithium-ion, baterai natrium-ion juga mempunyai jangka waktu pemakaian yang lebih panjang. Tiamat yang merupakan perusahaan start-up mengklaim bahwa baterai Natrium-ion memiliki jangka waktu pemakaian selama 10 tahun, lebih lama jika dibandingkan dengan baterai lithium-ion yang hanya 3-4 tahun (CNRS, 2020). Ke depannya, baterai natrium-ion ini akan diproyeksikan untuk memenuhi kebutuhan baterai yang terus meningkat, baik untuk mobil listrik ataupun kebutuhan elektronik yang lainnya. Berikut ini adalah perbandingan karakteristik antara baterai natrium-ion dengan lithium-ion jika dilihat dari beberapa parameter.
Tabel 2. 2 Perbandingan Karakteristik Baterai Natrium-ion Dengan Baterai Lithium Ion
Parameter Baterai Natrium-ion Baterai Lithium-ion
Energy Density (Wh/kg) 1165 3829 Harga Anode Current Collector
($ per metrik ton) 1885 (Al) 5719 (Cu)
Universitas Pertamina - 10
Parameter Baterai Natrium-ion Baterai Lithium-ion
Kapasitas Elektrode Metal Secara
Teoretis (mAh/cm3) 1131 2062
Efisiensi Tinggi (>90%) Tinggi (>90%)
Keamanan Tinggi Rendah
Sumber: (Eshetu, et al., 2020), (Yang, et al., 2019), dan (Rudola, 2019)
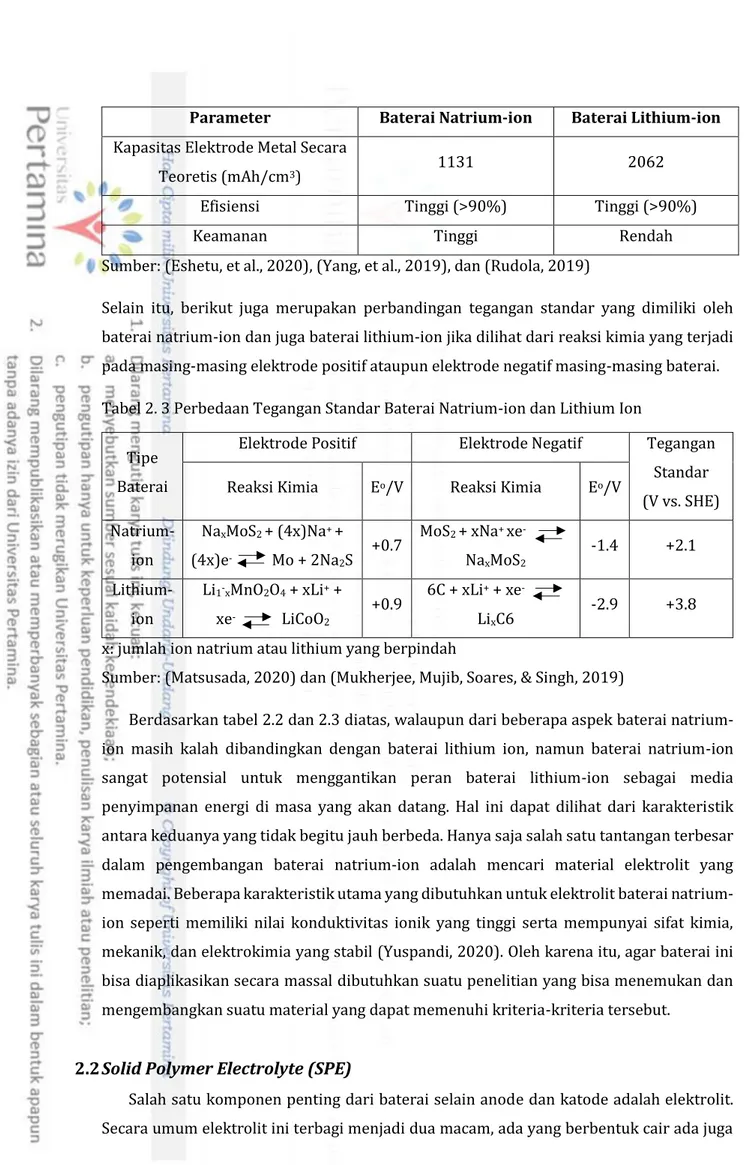
Selain itu, berikut juga merupakan perbandingan tegangan standar yang dimiliki oleh baterai natrium-ion dan juga baterai lithium-ion jika dilihat dari reaksi kimia yang terjadi pada masing-masing elektrode positif ataupun elektrode negatif masing-masing baterai. Tabel 2. 3 Perbedaan Tegangan Standar Baterai Natrium-ion dan Lithium Ion
Tipe Baterai
Elektrode Positif Elektrode Negatif Tegangan Standar (V vs. SHE) Reaksi Kimia Eo/V Reaksi Kimia Eo/V
Natrium-ion NaxMoS2 + (4x)Na+ + (4x)e- Mo + 2Na2S +0.7 MoS2 + xNa+ xe- NaxMoS2 -1.4 +2.1 Lithium-ion Li1-xMnO2O4 + xLi+ + xe- LiCoO2 +0.9 6C + xLi+ + xe- LixC6 -2.9 +3.8 x: jumlah ion natrium atau lithium yang berpindah
Sumber: (Matsusada, 2020) dan (Mukherjee, Mujib, Soares, & Singh, 2019)
Berdasarkan tabel 2.2 dan 2.3 diatas, walaupun dari beberapa aspek baterai natrium-ion masih kalah dibandingkan dengan baterai lithium natrium-ion, namun baterai natrium-natrium-ion sangat potensial untuk menggantikan peran baterai lithium-ion sebagai media penyimpanan energi di masa yang akan datang. Hal ini dapat dilihat dari karakteristik antara keduanya yang tidak begitu jauh berbeda. Hanya saja salah satu tantangan terbesar dalam pengembangan baterai natrium-ion adalah mencari material elektrolit yang memadai. Beberapa karakteristik utama yang dibutuhkan untuk elektrolit baterai natrium-ion seperti memiliki nilai konduktivitas natrium-ionik yang tinggi serta mempunyai sifat kimia, mekanik, dan elektrokimia yang stabil (Yuspandi, 2020). Oleh karena itu, agar baterai ini bisa diaplikasikan secara massal dibutuhkan suatu penelitian yang bisa menemukan dan mengembangkan suatu material yang dapat memenuhi kriteria-kriteria tersebut.
2.2 Solid Polymer Electrolyte (SPE)
Salah satu komponen penting dari baterai selain anode dan katode adalah elektrolit. Secara umum elektrolit ini terbagi menjadi dua macam, ada yang berbentuk cair ada juga
Universitas Pertamina - 11 yang berbentuk padat atau solid. Hanya saja elektrolit cair yang saat ini banyak digunakan pada berbagai jenis baterai memiliki beberapa keterbatasan seperti rentan terhadap kebocoran sehingga mudah meledak, bersifat racun, harganya mahal, dan juga stabilitas kimianya yang buruk (Prihandoko, 2008).
Solid Polymer Electrolyte atau SPE adalah jenis elektrolit padat yang diharapkan bisa
mengatasi berbagi kekurangan yang dimiliki oleh elektrolit cair. Hal ini dikarenakan SPE memiliki beberapa kelebihan seperti memiliki densitas energi yang tinggi, anti terhadap kebocoran, memiliki konduktivitas ionik yang tinggi dan sifat elektrokimia yang stabil, serta mudah di desain dalam berbagai macam bentuk (Kim & Kim, 1999). Selain bertindak sebagai elektrolit, SPE juga dapat bertindak sebagai separator sehingga tidak memerlukan separator tambahan lagi dalam pengaplikasiannya pada baterai (Yulianti, Luthfiah, & Sudaryanto, 2017). Hal ini dikarenakan polimer merupakan isolator elektrik yang baik sehingga bisa mencegah kontak yang terjadi antar elektrode (Sequeira & Santos, 2010). Terlepas dari kelebihan yang dimilikinya, SPE juga memiliki beberapa kekurangan seperti rendahnya konduktivitas ion pada suhu ruang sehingga menjadi kurang efisien jika langsung diaplikasikan pada sebuah baterai, khususnya baterai natrium ion (Linden & Reddy, 2002). Oleh karena itu, diperlukan beberapa treatment khusus supaya nilai konduktivitas ion yang dihasilkan dapat memenuhi nilai standar minimum yang dibutuhkan.
Gambar 2. 2 Salah Satu Contoh Solid Polymer Electrolyte yang terbuat dari PEO/NaClO4
(Ni’mah, Cheng, Cheng, Rick, & Bing-Joe, 2014)
Saat ini berbagai penelitian telah banyak dilakukan untuk mencari komposisi SPE yang paling optimal sehingga feasible untuk diaplikasikan pada baterai, khususnya pada baterai natrium ion. Hanya saja sampai dengan saat ini masih belum ditemukan suatu bahan pembuat SPE yang dapat memenuhi kriteria dan memiliki nilai konduktivitas ion minimum yang dibutuhkan. Salah satu bahan yang bisa digunakan untuk pembuatan SPE ini adalah
Universitas Pertamina - 12 polimer yang berasal dari alam dan juga limbah. Hal ini dikarenakan bahan tersebut
biodegradable, tidak beracun, dan juga harga nya murah (Vishakha S., Kishor D., & Sudha
S., 2012). Limbah kitin merupakan sebuah limbah yang sangat potensial untuk digunakan sebagai bahan pembuat SPE. Selain produksi limbahnya yang mencapai 17000 ton di Indonesia (KKP, 2015), kitin juga merupakan bahan dasar dari kitosan yang mana merupakan polimer dan sangat memungkinkan untuk diaplikasikan sebagai bahan pembuat SPE.
Unsur kitin bisa ditemukan pada ekoskeleteon dari crustaceas yang terdapat pada lobster, udang, kepiting, ataupun kerang (Brück, Slater, & Carney, 2011). Untuk menghasilkan unsur kitin, dibutuhkan setidaknya tiga tahapan yaitu demineralisasi, deproteinisasi, dan penghilangan pigmen serta lipid. Hal ini dikarenakan selain mengandung 15%-40% kitin, kutikula pada ekoskeleteon juga mengandung 20%-40% protein, 20%-50% kalsium, dan sisanya pigmen serta lemak (Brück, Slater, & Carney, 2011). Selanjutnya unsur kitin tersebut bisa diubah menjadi kitosan melalui proses deaselitasi (Yulianti, Saputra, Sudaryanto, Jodi, & Salam, 2013). Untuk menghasilkan kitosan dengan konduktivitas ion yang tinggi, maka kitosan perlu dilarutkan dalam asam asetat (Subban, Arof, & Radhakrisna, 1999). Campuran ini akan membentuk acetylated kitosan yang mudah dicetak sehingga menghasilkan sebuah film.
Treatment lainnya yang bisa dilakukan untuk meningkatkan nilai konduktivitas ion
pada polimer adalah dengan penambahan plasticizer. Beberapa penelitian yang telah dilakukan sebelumnya menyebutkan bahwa SPE yang tanpa ditambahkan plasticizer hanya memiliki nilai konduktivitas ionik kurang dari 10-4 S/cm (Aziz, Abdullah, Rasheed, &
Ahmed, 2017). Beberapa bahan plasticizer yang bisa digunakan untuk biopolimer adalah bahan organik yang memiliki molekul kecil seperti sorbitol dan gliserol (Setiawan, Faizal, & Amrullah, 2015) (Sanjaya & Puspita, 2012). Dari kedua bahan tersebut, mengacu pada penelitian yang telah dilakukan oleh Hartono, Indra (2017) maka sorbitol dipilih sebagai
plasticizer dalam penelitian ini karena memberikan efek plasticizing yang lebih besar.
Dengan dilakukannya penambahan plasticizer, maka konduktivitas ion dari SPE diharapkan akan meningkat sampai dengan dua orde (Harun, Ali, Ali, & Yahya, 2011).
2.3 Kitosan
Kitosan adalah salah satu polimer rantai panjang yang merupakan turunan paling sederhana dari kitin. Untuk dapat diperoleh kitosan, dibutuhkan proses deasitilasi sempurna atau sebagian untuk menghilangkan gugus asetil (NHCOCH3) yang terdapat pada
kitin menjadi gugus amina (NH2) dengan bantuan hidrogen (H) (Smith, 2005). Berikut ini
Universitas Pertamina - 13 Gambar 2. 3 Perbedaan Struktur Kitin dan Kitosan (Yahya & Arof, 2002)
Bentuk dari kitosan adalah spesifik dan mengandung gugus amino dalam rantai panjangnya. Hanya saja karena penggunaan dari kitosan ini sangat luas, maka mutu kitosan yang terdapat di pasaran berbeda-beda tergantung penggunaannya. Beberapa parameter yang mempengaruhi mutu dari kitosan ini adalah kadar air, kadar abut, dan juga derajat deastilasi (Bastaman, 1989).
2.4 Natrium Sulfit (Na
2SO
3)
Natrium Sulfit (Na2
SO
3) merupakan salah satu garam natrium yang bisa digunakanuntuk meningkatkan konduktivitas ionik suatu material. Beberapa contoh garam natrium yang telah dilakukan penelitian sebelumnya yaitu NaPF6, NaClO4, NaTf, NaTFSI, NaFSI,
Na2SO4, NaCF3SO3, dan NaPO3 (Mohapatra, 2008 dalam Priyambono 2017).
Konduktivitas ion juga bisa ditingkatkan dengan cara melarutkan kitosan dengan garam natrium. Hal ini dikarenakan kitosan dapat melarutkan garam dan merupakan host polimer untuk menjadi sebuah elektrolit. Garam tersebut nantinya akan terdisosiasi sehingga akan meningkatkan konduktivitas.
Na
2SO
3 merupakan garam yang harganyajauh lebih murah jika dibandingkan dengan garam-garam yang digunakan pada penelitian sebelumnya. Berikut ini adalah perbandingan beberapa garam yang sudah digunakan dengan natrium sulfit jika ditinjau dari sisi harga dan juga radius anion nya.
Tabel 2. 4 Perbandingan Harga dan Radius Anion Garam Untuk Penggunaan SPE
Jenis Garam Harga (SGD/100 gram) Radius Anion (Angstrom)
NaFSI 3995 5.234
NaPF6 814 4.02
NaClO4 98.1 4.154
Na2SO4 57.5 3.9611
Universitas Pertamina - 14 Berdasarkan tabel perbandingan tersebut maka natrium sulfit memiliki keunggulan dari sisi harganya yang jauh lebih murah jika dibandingkan dengan garam-garam lainnya. Selain itu jari-jari anion (SO32-) yang dimiliki oleh natrium sulfit juga tidak begitu jauh
berbeda dengan jari-jari anion yang dimiliki garam-garam lainnya. Hal ini menjadikan natrium sulfit dapat diaplikasikan pada SPE mengingat ion natrium (Na+) masih bisa
bergerak bebas karena ukuran jari-jarinya yang relatif jauh lebih kecil yakni 0.97 angstrom. Dengan pertimbangan hal tersebut, maka pembuatan SPE dengan harga yang jauh lebih murah pun bisa untuk diaplikasikan.
2.5 Sifat Fisis Material
Sifat fisis material merupakan sifat alami yang dimiliki suatu material. Secara umum, suatu material tersusun atas beberapa atom yang membentuk menjadi sebuah struktur. Jika dilihat dari strukturnya, maka material dibagi menjadi dua yaitu material crystalline dan noncrystalline (amorphous). Material crystalline merupakan sebuah material yang memiliki struktur atom rapi dan periodik. Beberapa material yang memiliki struktur
crystalline adalah metal dan juga keramik (Callister, 2007). Berikut ini adalah contoh
struktur crystalline yang terdapat pada SiO2.
Gambar 2. 4 Struktur crystalline pada SiO2 (Callister, 2007)
Sementara itu material noncrystalline atau yang biasa disebut material amorphous merupakan sebuah material yang memiliki struktur atom acak dan tidak beraturan. Struktur ini biasanya terjadi pada beberapa material polimer dan juga material yang memiliki struktur yang kompleks (Callister, 2007). Berikut ini adalah contoh struktur
amorphous yang terdapat pada SiO2.
Universitas Pertamina - 15 Salah satu sifat yang diharapkan dari pembuatan SPE adalah material yang memiliki struktur amorphous. Hal ini dikarenakan semakin amorphous suatu material maka nilai konduktivitas ionik yang dimiliki akan semakin meningkat (Hartono, 2018). Hal inilah yang dibutuhkan untuk diaplikasikan pada baterai Natrium-ion sebagai elektrolit. Oleh karena itu, pada penelitian ini akan dicari suatu komposisi penyusun SPE yang material nya memiliki struktur amorphous paling tinggi.
2.6 Sifat Mekanis Material
Sifat mekanis yang menjadi perhatian utama pada penelitian ini adalah tingkat fleksibilitas film yang dapat diketahui dengan cara dilakukan uji tarik. Beberapa parameter yang akan didapatkan dari hasil uji tari adalah kuat tarik (stress), elongasi (strain), dan modulus young. Kuat tarik atau yang didefinisikan juga sebagai stress merupakan perbandingan antara beban maksimum dengan luas permukaan film (Callister, 2007). Persamaannya bisa ditulis seperti dibawah ini:
𝜎 =𝐹 𝐴
(2.1)
Dimana:
𝜎 : kuat tarik atau stress (MPa) F : beban maksimum (N)
A : luas permukaan sampel (mm2).
Sementara elongasi adalah besarnya perpanjangan yang terjadi sebelum film yang diberikan beban mengalami fracture atau patah (Callister, 2007). Besarnya elongasi dapat diketahui mengikuti persamaan dibawah in:
𝜀 =𝐿𝑜− 𝐿𝑖 𝐿𝑖
𝑥100 (2.2)
Dimana:
𝜀 : elongasi (%)
Lo : panjang awal sampel (mm),
Li : panjang sampel tepat sebelum (mm).
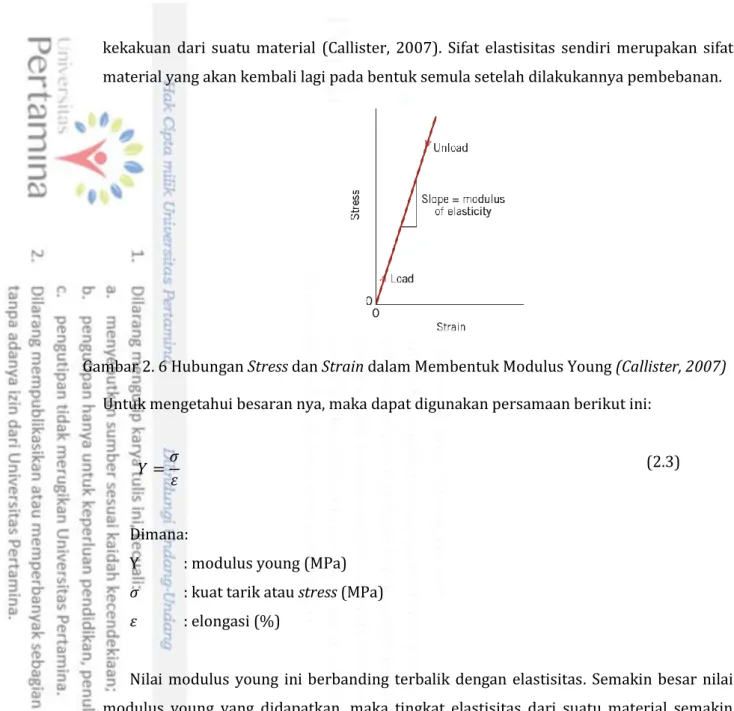
Perbandingan antara kuat tarik dan elongasi dinamakan modulus young. Secara sederhana, besaran dari modulus young ini akan menggambarkan elastisitas atau
Universitas Pertamina - 16 kekakuan dari suatu material (Callister, 2007). Sifat elastisitas sendiri merupakan sifat material yang akan kembali lagi pada bentuk semula setelah dilakukannya pembebanan.
Gambar 2. 6 Hubungan Stress dan Strain dalam Membentuk Modulus Young (Callister, 2007) Untuk mengetahui besaran nya, maka dapat digunakan persamaan berikut ini:
𝑌 =𝜎 𝜀
(2.3)
Dimana:
Y : modulus young (MPa) 𝜎 : kuat tarik atau stress (MPa) 𝜀 : elongasi (%)
Nilai modulus young ini berbanding terbalik dengan elastisitas. Semakin besar nilai modulus young yang didapatkan, maka tingkat elastisitas dari suatu material semakin rendah, artinya material akan cenderung lebih kaku (britle). Suatu material dikatakan elastis (ductile) apabila memiliki nilai modulus young yang kecil. Perbedaan antara keduanya bisa dilihat pada gambar di bawah ini.
Universitas Pertamina - 17 Dari gambar diatas dapat diketahui perbedaan kurva yang akan didapatkan dari hasil pengujian tarik untuk material elastis dan juga material kaku. Untuk material elastis elongasi atau strain yang akan didapatkan cenderung lebih besar sementara untuk material kaku sebaliknya.
2.7 X-Ray Diffraction (XRD)
X-Ray Diffraction (XRD) atau difraksi sinar X merupakan sebuah metode yang dilakukan
untuk mengetahui pola struktur, fasa, dan detail dari suatu material. Panjang gelombang yang dapat diukur oleh XRD ini adalah panjang gelombang sinar X yang memiliki panjang gelombang 10-6 sampai 10-9 m (Callister, 2007). Penggunaan XRD ini akan mengikuti
Persamaan Bragg yang dituliskan seperti di bawah ini:
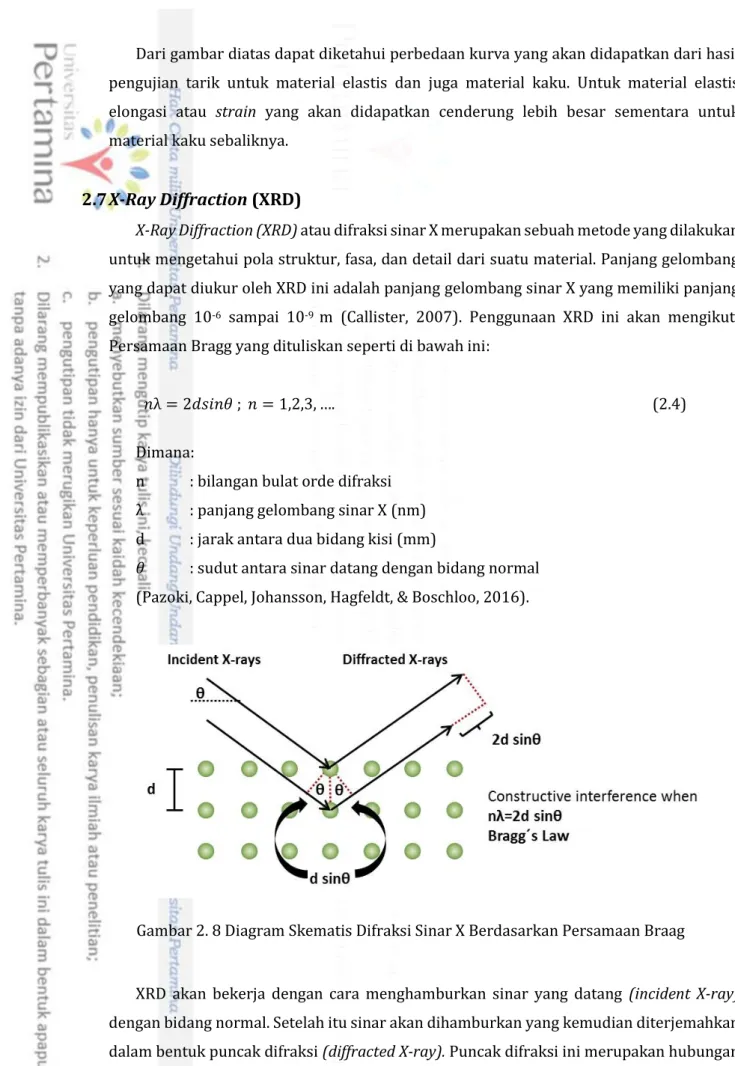
𝑛λ = 2𝑑𝑠𝑖𝑛𝜃 ; 𝑛 = 1,2,3, …. (2.4)
Dimana:
n : bilangan bulat orde difraksi λ : panjang gelombang sinar X (nm) d : jarak antara dua bidang kisi (mm)
𝜃 : sudut antara sinar datang dengan bidang normal (Pazoki, Cappel, Johansson, Hagfeldt, & Boschloo, 2016).
Gambar 2. 8 Diagram Skematis Difraksi Sinar X Berdasarkan Persamaan Braag
XRD akan bekerja dengan cara menghamburkan sinar yang datang (incident X-ray) dengan bidang normal. Setelah itu sinar akan dihamburkan yang kemudian diterjemahkan dalam bentuk puncak difraksi (diffracted X-ray). Puncak difraksi ini merupakan hubungan antara dua atau lebih gelombang yang telah dihamburkan oleh bidang normal. Setidaknya
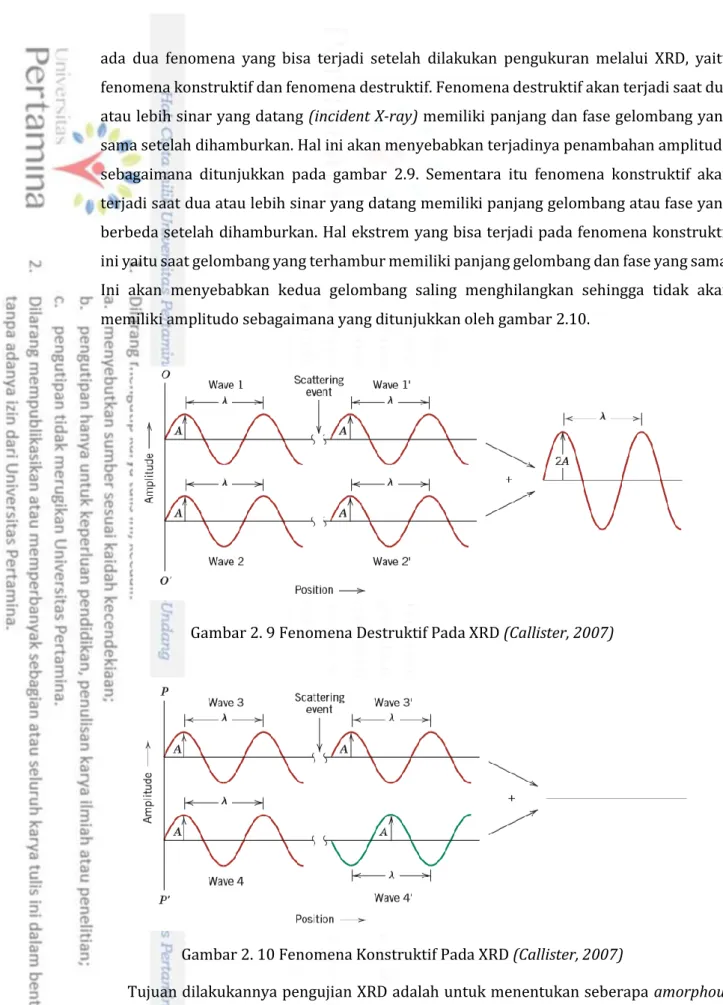
Universitas Pertamina - 18 ada dua fenomena yang bisa terjadi setelah dilakukan pengukuran melalui XRD, yaitu fenomena konstruktif dan fenomena destruktif. Fenomena destruktif akan terjadi saat dua atau lebih sinar yang datang (incident X-ray) memiliki panjang dan fase gelombang yang sama setelah dihamburkan. Hal ini akan menyebabkan terjadinya penambahan amplitudo sebagaimana ditunjukkan pada gambar 2.9. Sementara itu fenomena konstruktif akan terjadi saat dua atau lebih sinar yang datang memiliki panjang gelombang atau fase yang berbeda setelah dihamburkan. Hal ekstrem yang bisa terjadi pada fenomena konstruktif ini yaitu saat gelombang yang terhambur memiliki panjang gelombang dan fase yang sama. Ini akan menyebabkan kedua gelombang saling menghilangkan sehingga tidak akan memiliki amplitudo sebagaimana yang ditunjukkan oleh gambar 2.10.
Gambar 2. 9 Fenomena Destruktif Pada XRD (Callister, 2007)
Gambar 2. 10 Fenomena Konstruktif Pada XRD (Callister, 2007)
Tujuan dilakukannya pengujian XRD adalah untuk menentukan seberapa amorphous atau anisotropy berbagai variasi komposisi SPE yang telah di sintesis menjadi film. Sifat
amorphous pada suatu material dapat diketahui apabila hasil XRD menunjukkan sudut
Universitas Pertamina - 19 itu, puncak yang tidak tajam dan melebar juga menunjukkan bahwa struktur crystallite memiliki ukuran yang kecil (Saujanya & Radhakrishnan, 2001). Hal ini jugalah yang menandakan adanya bagian rantai penyusun crystallite yang menjadi amorphous.
Semakin amorphous struktur polimer maka nilai konduktivitas yang dihasilkan juga akan semakin meningkat (Yulianti, Luthfiah, & Sudaryanto, 2017). Pada penelitian sebelumnya yang dilakukan Mauricio-Sanchez dkk (2017), didapatkan pola difraksi kitosan murni pada puncak difraksi 2𝜃 9.940 and 20.010. Pola difraksi semacam ini
menunjukkan bahwa material yang terbentuk memiliki struktur semikristalin. Sementara setelah dilakukan penambahan asam asetat didapatkan struktur yang lebih amorphous.
2.8 Differential Scanning Calorimetry (DSC)
Differential Scanning Calorimetry (DSC) adalah sebuah instrumen termodinamika yang
digunakan untuk menganalisis suhu. Prinsip kerja dari instrumen yang satu in yaitu membandingkan suhu dari sampel yang akan di uji dengan material acuan yang inert secara terprogram selama berlangsungnya perubahan suhu (Setiabudi, Hardian, & Mudzakir, 2012). Jika pada saat proses pemanasan tidak terjadi peristiwa termal seperti pelelehan, perubahan struktur kristal, ataupun dekomposisi, maka suhu sampel dan referen akan sama sehingga akan dihasilkan grafik yang cenderung datar. Sementara jika salah satu proses termal terjadi selama pengujian maka akan terjadi perubahan grafik yang signifikan. Jika grafik menunjukkan perubahan puncak area ke bawah, maka terjadi peristiwa endoterm. Namun jika sebaliknya maka peristiwa termal yang terjadi pada sampel bersifat eksoterm.
Gambar 2. 11 Skema perubahan fasa yang diakibatkan oleh perubahan termal pada pengujian DSC (Skoog, Holler, & Crouch, 2007).
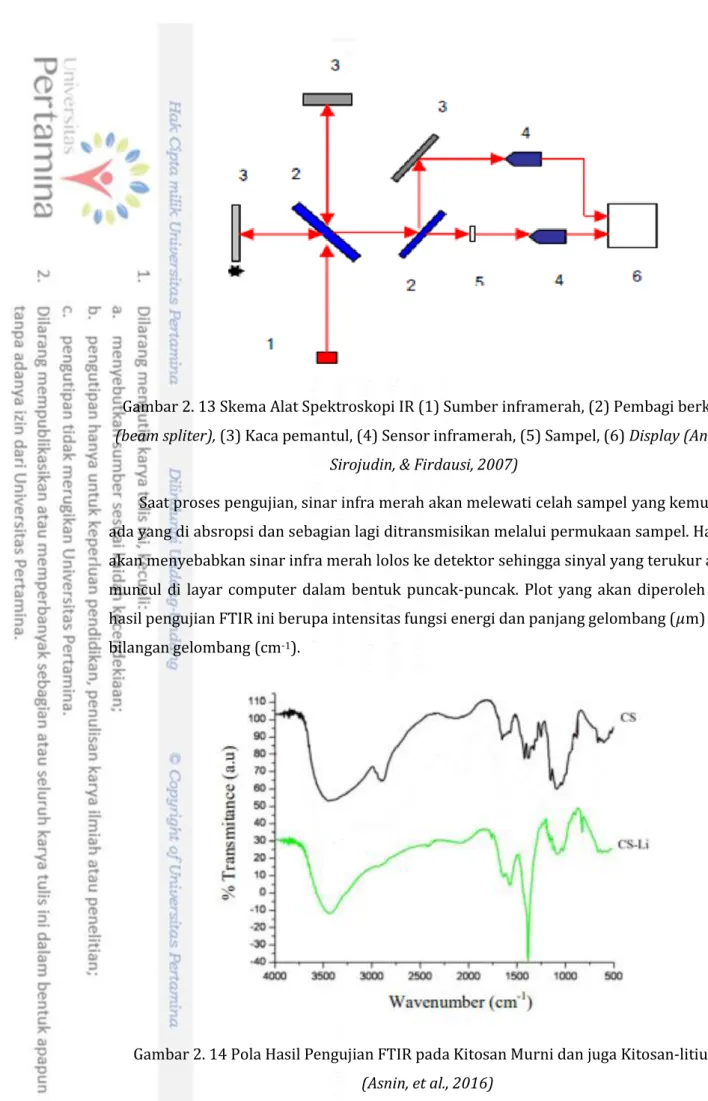
Universitas Pertamina - 20 Pada penelitian ini, data yang akan dibutuhkan dari pengujian DSC adalah kurva yang menunjukkan hubungan antara heat flow (W/g) dengan temperature (OC). Dari kurva tersebut akan diketahui nilai titik leleh atau melting temperature (Tm) dari SPE yang telah disintesis. Caranya yaitu dengan melihat penyimpangan grafik yang dihasilkan berupa puncak yang tajam sebagai sebab dari berlangsungnya peristiwa termal pada sampel (Setiabudi, Hardian, & Mudzakir, 2012). Berikut ini adalah salah satu contoh data pengujian yang telah dilakukan pada SPE yang terbuat dari PEO.
Gambar 2. 12 Hasil Pengujian DSC pada Beberapa Komposisi SPE Berbahan dasar PEO
(Ni’mah, Cheng, Cheng, Rick, & Bing-Joe, 2014)
Dari gambar 2.12 di atas diketahui bahwa seiring dengan penambahan konsentrasi Na yang semakin tinggi, maka titik leleh atau melting temperature (Tm) nya juga semakin berkurang. Sehingga dapat disimpulkan bahwa penambahan konsentrasi garam yang semakin tinggi menyebabkan titik leleh dari suatu SPE berkurang.
2.9 Fourier Transform Infra-Red (FTIR)
Fourier Transform Infra-Red (FTIR) adalah metode untuk mengidentifikasi gugus
fungsi pada suatu sampel yang dianalisis secara kualitatif. Analisis dilakukan dengan melihat bentuk spektrum dan puncak spesifik yang menunjukkan jenis gugus fungsional yang dimiliki oleh senyawa yang dianalisis. Untuk bisa melihat hasil yang didapatkan, maka sampel harus menggunakan bantuan senyawa ATr atau KBr. Mekanisme penggunaan FTIR dapat dilihat pada Gambar 2.13 di bawah.
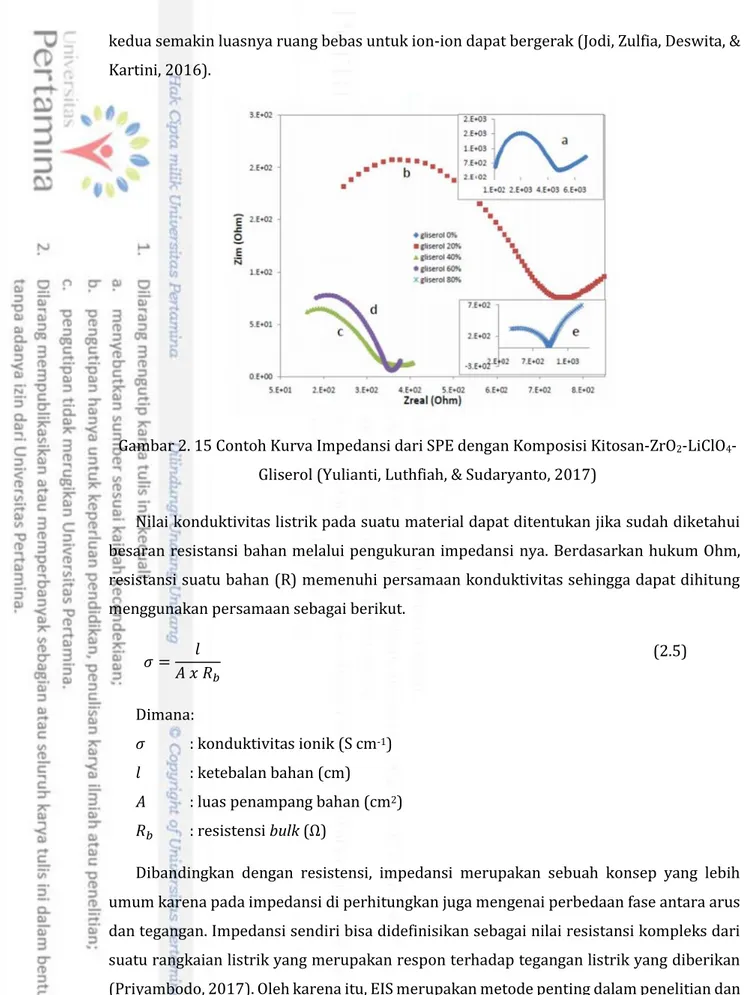
Universitas Pertamina - 21 Gambar 2. 13 Skema Alat Spektroskopi IR (1) Sumber inframerah, (2) Pembagi berkas
(beam spliter), (3) Kaca pemantul, (4) Sensor inframerah, (5) Sampel, (6) Display (Anam, Sirojudin, & Firdausi, 2007)
Saat proses pengujian, sinar infra merah akan melewati celah sampel yang kemudian ada yang di absropsi dan sebagian lagi ditransmisikan melalui permukaan sampel. Hal ini akan menyebabkan sinar infra merah lolos ke detektor sehingga sinyal yang terukur akan muncul di layar computer dalam bentuk puncak-puncak. Plot yang akan diperoleh dari hasil pengujian FTIR ini berupa intensitas fungsi energi dan panjang gelombang (𝜇m) atau bilangan gelombang (cm-1).
Gambar 2. 14 Pola Hasil Pengujian FTIR pada Kitosan Murni dan juga Kitosan-litium
Universitas Pertamina - 22 Gambar 2.14 diatas merupakan salah satu contoh hasil spektroskopi infra merah dari kitosan dan campuran kitosan-litium yang dilakukan oleh Asnin, dkk (2016). Untuk bisa mengetahui gugus fungsi apa saja yang terkandung di dalamnya maka harus dilakukan perbandingan antara pita absorpsi yang terbentuk pada spektrum infra merah dengan tabel korelasi spektrum senyawa pembanding nya (Anam, Sirojudin, & Firdausi, 2007).
Tabel 2. 5 Daerah Frekuensi Untuk Gugus Fungsi Organik
Sumber: (Wardhani, 2017)
Sementara itu untuk kitin dan kitosan, telah dilakukan karakterisasi FTIR oleh Gyliene, Razmute, Tarozaite, & Nivinskiene (2003). Hasil yang didapatkan dari hasil penelitian tersebut. Ditunjukkan pada tabel dibawah ini.
Universitas Pertamina - 23 Tabel 2. 6 Serapan FTIR Karakterisasi untuk Kitin dan Kitosan
Sumber: (Gyliene, Razmute, Tarozaite, & Nivinskiene, 2003)
2.10 Electrochemical Impedance Spectroscopy (EIS)
Electrochemical Impedance Spectroscopy (EIS) merupakan sebuah metode yang
digunakan untuk mengetahui nilai konduktivitas ionik pada suatu material. Pergerakan elektron dan ionik dalam suatu material bisa diamati secara elektrokimia dengan menggunakan metode yang satu ini. Data yang dihasilkan dari percobaan EIS merupakan grafik yang terdiri dari frekuensi tinggi dan frekuensi rendah. Frekuensi tinggi ditunjukkan dengan kurva setengah lingkaran (semicircle) yang akan mewakili kapasitor. Kurva ini pararel dengan tahanan atau hambatan. Sementara itu frekuensi rendah ditunjukkan dengan kurva loncatan (spike) yang mewakili kapasitansi.
Kapasitor yang terbentuk menggambarkan rantai polimer yang tidak bergerak
(immobile anions) dan resistor yang terjadi karena pergerakan ion. Sementara kapasitansi
akan terbentuk saat terjadi hubungan antara elektrolit dan elektrode pada saat proses pengukuran. Kedua hal ini terjadi secara bersamaan atau pararel (Jodi, Syahrial, Sudaryanto, & Kartini, 2017). Kenaikan konduktivitas yang terjadi pada sampel yang di uji dapat diakibatkan oleh dua hal, pertama meningkatnya konsentrasi pembawa ion dan
Universitas Pertamina - 24 kedua semakin luasnya ruang bebas untuk ion-ion dapat bergerak (Jodi, Zulfia, Deswita, & Kartini, 2016).
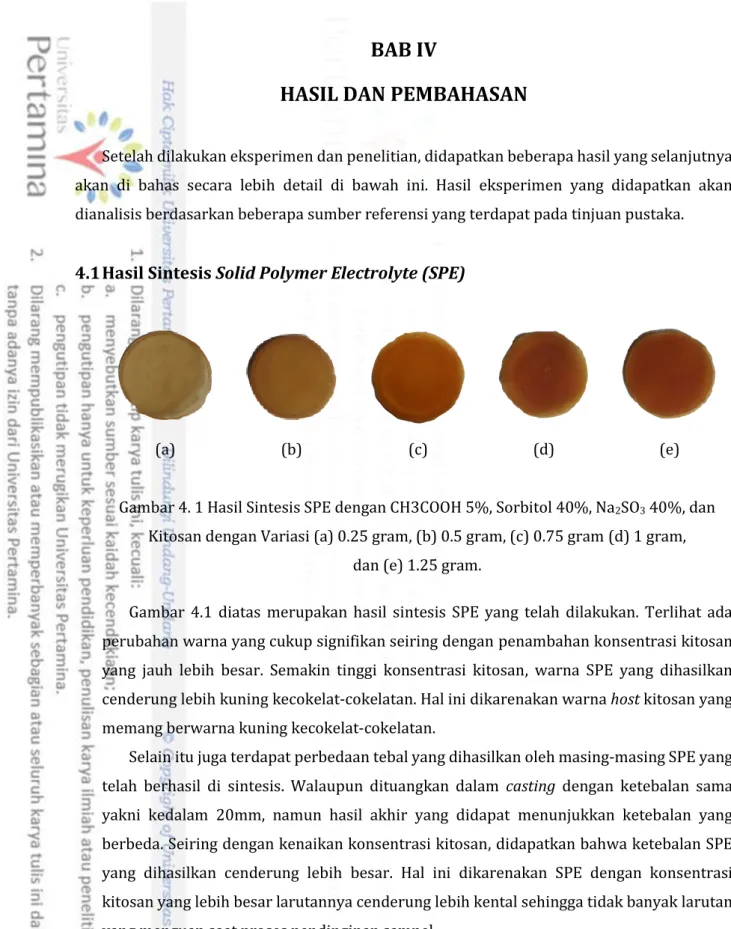
Gambar 2. 15 Contoh Kurva Impedansi dari SPE dengan Komposisi Kitosan-ZrO2-LiClO4-
Gliserol (Yulianti, Luthfiah, & Sudaryanto, 2017)
Nilai konduktivitas listrik pada suatu material dapat ditentukan jika sudah diketahui besaran resistansi bahan melalui pengukuran impedansi nya. Berdasarkan hukum Ohm, resistansi suatu bahan (R) memenuhi persamaan konduktivitas sehingga dapat dihitung menggunakan persamaan sebagai berikut.
𝜎 = 𝑙 𝐴 𝑥 𝑅𝑏 (2.5) Dimana: 𝜎 : konduktivitas ionik (S cm-1) 𝑙 : ketebalan bahan (cm)
𝐴 : luas penampang bahan (cm2)
𝑅𝑏 : resistensi bulk (Ω)
Dibandingkan dengan resistensi, impedansi merupakan sebuah konsep yang lebih umum karena pada impedansi di perhitungkan juga mengenai perbedaan fase antara arus dan tegangan. Impedansi sendiri bisa didefinisikan sebagai nilai resistansi kompleks dari suatu rangkaian listrik yang merupakan respon terhadap tegangan listrik yang diberikan (Priyambodo, 2017). Oleh karena itu, EIS merupakan metode penting dalam penelitian dan pengembangan ilmu material untuk mengetahui pengaruh beberapa treatment yang diberikan terhadap sifat konduktansi suatu material.
Universitas Pertamina - 26
BAB III
METODE PENELITIAN
3.1 Diagram Alir Analisis Data
Persiapan Alat dan Bahan Pembuatan SPE SPE Sesuai Karakterisasi SPE Analisis Ya Tidak
Mulai
Selesai
Universitas Pertamina - 27
3.2 Bentuk Penelitian
Bentuk penelitian ini merupakan penelitian laboratorium.
3.3
Metode Pengumpulan Data
Pengumpulan data untuk referensi dilakukan dengan cara studi literatur dari berbagai sumber. Sementara pengumpulan data untuk analisis dilakukan dengan cara pengujian dan karakterisasi sampel di laboratorium menggunakan beberapa instrumen.
3.4 Alat dan Bahan
Bahan: Kitosan, Sorbitol, Natrium Sulfit (
Na
2SO
3), Asam Asetat (CH3COOH), dan Aquades.Alat: Teflon cell CV, Teflon casting berdiameter 20mm dengan kedalaman 2mm, Teflon
casting sesuai standar ASTM D-1882 tipe L, Labu ukur 1000mL, Pipet Ukur, Batang strirer magnetic 3cm, Gelas beaker, Hot Plate, Gelas ukur vial 25 mL, Neraca analitik, Spatula,
Batang pengaduk, Mortar, Oven, Amplas, X-Ray Diffraction (XRD), Electrochemical
Impedance Spectroscopy (EIS), LCR meter, Fourier Transform Infra-Red (FTIR), Energy Dispersive Spectroscopy (EDS), Ultimate Machine Testing (UTM), dan Differential Scanning Calorimetry (DSC).
3.5 Metode Analisis Data
3.5.1 pembuatan film
Prosedur pembuatan film elektrolit dimulai dari proses pembuatan larutan asam asetat, pengadukan, casting, dan pengeringan. Tahapan lebih spesifik nya dijelaskan sebagai berikut.
a. 10 ml asam asetat 5% dilarutkan dengan kitosan.
b. Setelah kedua bahan tercampur, selanjutnya ditambahkan natrium sulfit dan juga sorbitol.
c. Semua bahan yang telah tercampur selanjutnya diaduk menggunakan magnetic
stirer pada suhu ruang (Setyaningum, Sumarni, & Widiarti, 2015) selama 180 menit
atau sampai terbentuk larutan homogen.
d. Tuangkan larutan yang sudah homogen ke dalam teflon casting. e. Diamkan pada suhu ruang hingga kering dan terbentuk film.
f. Lakukan pembuatan film dengan variasi sampel seperti yang ditunjukkan pada tabel di bawah ini.
Universitas Pertamina - 28 Tabel 3. 1 Variasi Kitosan pada Sampel Pengujian
Sampel Asam Asetat Natrium Sulfit Sorbitol Kitosan
SPE 0.25 5% (v/v) 40% (b/b) 40% (b/b) 0.25 gram SPE 0.5 0.5 gram SPE 0.75 0.75 gram SPE 1 1 gram SPE 1.25 1.25 gram
g. Langkah (a) sampai (e) terus berulang secara periodik sampai tercetak sampel film yang dibutuhkan untuk berbagai pengujian.
3.5.2 karakterisasi dan analisis sampel film
3.5.2.1 analisis kristal
Karakterisasi XRD dilakukan untuk mengetahui dan mengamati struktur film pada SPE yang telah berhasil dibuat. Film akan di pindai dengan berkas radiasi Cu Kα dengan λ= 0.15406 nm, 0.02 deg/step pada sudut 2θ di 5o-60o (Yulianti, Luthfiah, & Sudaryanto,
2017). Jenis XRD yang akan digunakan pada penelitian ini adalah BTX III.
3.5.2.2 analisis thermal performance
Thermal Performance akan diukur menggunakan instrumen Differential Scanning Calorimetry (DSC). Melalui instrumen ini akan diketahui suhu maksimum sebuah SPE yang
telah berhasil dibuat dapat bekerja. Pada penelitian pembuatan SPE sebelumnya yang berbahan dasar PEO, SPE akan dipanaskan dari suhu 25C – 300C dengan rata-rata pemanasan 10 C/menit (Ni’mah, Cheng, Cheng, Rick, & Bing-Joe, 2014).
3.5.2.3 analisis gugus fungsi
Gugus fungsi pada suatu material dapat dianalisis menggunakan Fourier Transformed
Infra-Red (FTIR). Pada penelitian ini dilakukan pengujian FTIR pada bilangan gelombang
4000 – 500 cm-1 (Asnin, et al., 2016). Setelah dilakukan pengujian FTIR, akan didapatkan
data kualitatif berupa perubahan gugus fungsional akibat pengaruh variasi kitosan pada SPE yang telah berhasil dibuat.
3.5.2.4 analisis konduktivitas
Konduktivitas ion merupakan salah satu parameter yang penting untuk mengetahui performa dari suatu elektrolit. Alat yang digunakan untuk mengetahui nilai konduktivitas
Universitas Pertamina - 29 ion pada penelitian ini adalah Electrochemical Impedance Spectroscopy (EIS) dengan rentang frekuensi dari 42 Hz – 1 MHz (Yulianti, Sudaryanto, & Ginting 2015) pada suhu ruang. Nantinya sampel akan di jepit pada dua elektrode yang terhubung dengan LCR meter sehingga diketahui nilai konduktivitas ionik nya. Selain itu, untuk membandingkan konduktivitas yang didapatkan dilakukan juga pengujian menggunakan Potensiostat. Berdasarkan penelitian yang dilakukan oleh (Aziz, Abdullah, Rasheed, & Ahmed, 2017), rentang suhu ideal untuk menganalisis SPE dimulai dari 303 K sampai dengan 413 K. Hanya saja karena ada sedikit kendala pada penelitian ini maka dilakukan pengujian potensiostat pada suhu ruang saja.
3.5.2.5 analisis uji tarik
Ultimate Testing Machine (UTM) merupakan instrumen yang digunakan untuk
mengetahui sifat elastisitas suatu material dengan cara dilakukan uji tarik. Pelaksanaan uji tarik pada penelitian ini bertujuan untuk mengetahui tingkat fleksibilitas SPE yang telah berhasil di cetak. Prosedur pengujian yang dilakukan pada uji tarik ini mengacu pada ASTM D-1822 tipe L (Yulianti, Luthfiah, & Sudaryanto, 2017).
Universitas Pertamina - 31
BAB IV
HASIL DAN PEMBAHASAN
Setelah dilakukan eksperimen dan penelitian, didapatkan beberapa hasil yang selanjutnya akan di bahas secara lebih detail di bawah ini. Hasil eksperimen yang didapatkan akan dianalisis berdasarkan beberapa sumber referensi yang terdapat pada tinjuan pustaka.
4.1 Hasil Sintesis Solid Polymer Electrolyte (SPE)
(a) (b) (c) (d) (e)
Gambar 4. 1 Hasil Sintesis SPE dengan CH3COOH 5%, Sorbitol 40%, Na2SO3 40%, dan
Kitosan dengan Variasi (a) 0.25 gram, (b) 0.5 gram, (c) 0.75 gram (d) 1 gram, dan (e) 1.25 gram.
Gambar 4.1 diatas merupakan hasil sintesis SPE yang telah dilakukan. Terlihat ada perubahan warna yang cukup signifikan seiring dengan penambahan konsentrasi kitosan yang jauh lebih besar. Semakin tinggi konsentrasi kitosan, warna SPE yang dihasilkan cenderung lebih kuning kecokelat-cokelatan. Hal ini dikarenakan warna host kitosan yang memang berwarna kuning kecokelat-cokelatan.
Selain itu juga terdapat perbedaan tebal yang dihasilkan oleh masing-masing SPE yang telah berhasil di sintesis. Walaupun dituangkan dalam casting dengan ketebalan sama yakni kedalam 20mm, namun hasil akhir yang didapat menunjukkan ketebalan yang berbeda. Seiring dengan kenaikan konsentrasi kitosan, didapatkan bahwa ketebalan SPE yang dihasilkan cenderung lebih besar. Hal ini dikarenakan SPE dengan konsentrasi kitosan yang lebih besar larutannya cenderung lebih kental sehingga tidak banyak larutan yang menguap saat proses pendinginan sampel.
Universitas Pertamina - 32
4.2 Hasil Karakterisasi Kristal Menggunakan XRD
Gambar 4. 2 Sampel SPE yang Telah di Tumbuk Halus untuk Pengujian XRD
Sampel SPE yang telah di gerus seperti gambar di atas kemudian di haluskan kembali menggunakan meshing 100 agar memenuhi standar XRD dengan merk BTX yang digunakan pada penelitian ini. Setelah itu baru dilakukan pengujian XRD dan dihasilkan data seperti gambar 4.3 di bawah. Karakterisasi pola difraksi ini sangat diperlukan untuk mengetahui perubahan struktur SPE akibat adanya variasi penambahan jumlah kitosan.
Gambar 4. 3 Hasil Karakterisasi SPE Menggunakan XRD
Dari grafik yang dihasilkan tampak bahwa Na2SO3 memiliki struktur yang kristalin. Hal
ini terlihat dari banyaknya puncak yang muncul dengan sudut sempit dan intensitas puncak yang cukup tinggi (Callister, 2007). Hasil ini juga dikonfirmasi oleh data dari
software Match! 3 yang menunjukkan bahwa natrium sulfit memiliki bentuk kristal trigonal (hexagonal axis) dengan besar unit sel a=5.4410 Å dan c=6.1330 Å. Dari hasil search and
Universitas Pertamina - 33
match dengan bantuan software didapatkan bahwa terdapat beberapa puncak yang
memang berasal dari natrium sulfit. Puncak-puncak tersebut berada pada 2𝜃 14.630,
18.850, 24.100, 34.920, 38.300, 41.020, 44.780, 48.800, 51.480, dan 53.550. Sementara itu hasil
XRD yang lainnya tidak bisa dilakukan search and match menggunakan software Match! 3 dikarenakan strukturnya yang semikristalin ataupun amorphous. Oleh karena itu dilakukan analisis secara manual dikarenakan software Match! 3 hanya dapat membaca data sampel dengan struktur yang kristal saja.
Dari hasil analisis tampak bahwa pada kitosan murni setidaknya terdapat dua puncak yang sangat jelas terlihat pada 2𝜃 2.500, 23.100, dan juga satu puncak kecil pada 2𝜃 34.450.
Hasil XRD pada kitosan murni ini hampir sama dengan yang sudah dilakukan oleh Mauricio-Sanchez dkk (2017). Dari data tersebut dapat diketahui bahwa struktur polimer kitosan murni merupakan semikristalin. Penambahan sorbitol dan asam asetat pada kitosan murni menyebabkan puncak pada 2𝜃 23.100 sedikit bergeser dan menjadi tidak
begitu tajam serta terjadi pelebaran sudut yang menandakan terjadi perubahan struktur menuju amorphous. Sementara itu penambahan asam asetat, natrium sulfit, dan sorbitol pada kitosan murni sebagai bahan pembuat SPE membuat pola difraksi yang dihasilkan mengalami perubahan. Hal ini menandakan bawa terjadi interaksi antara kitosan murni dengan asam asetat, natrium sulfit, dan juga sorbitol saat proses sintesis SPE dilakukan.
SPE dengan jumlah kitosan 0.25 gram membuat puncak 2𝜃 2.50 intensitasnya menurun.
Selain itu, intensitas puncak pada 2𝜃 23.10 juga berkurang yang diikuti dengan melebarnya
sudut yang terjadi. Puncak pada 2𝜃 34.450 sudah tidak terlihat lagi namun muncul puncak
baru dengan intensitas yang tidak terlalu tinggi dan sudut yang kecil pada 2𝜃 37.40. Puncak
ini berasal dari natrium sulfit yang bergeser dari 2𝜃 38.300. Karakteristik hasil XRD yang
ditunjukkan oleh SPE 0.25 ini menunjukkan struktur yang amorphous (Callister, 2007). Tidak banyak perubahan hasil XRD yang ditunjukkan oleh SPE 0.5, hanya saja muncul puncak baru pada 2𝜃 26.450 dan 39.450 dengan intensitas yang tidak terlalu tinggi.
Puncak-puncak ini sebelumnya terdapat pada natrium sulfit pada 2𝜃 24.100 dan 38.300 namun
sudah mengalami sedikit pergeseran sehingga dapat dikatakan bahwa natrium sulfit sudah bercampur dengan bahan pembuat lainnya pada SPE 0.5 ini.
Sementara itu pada SPE 0.75 sampai dengan SPE 1.25 terjadi perubahan struktur dari yang awalnya amorphous menjadi semikristalin. Hal ini tampak dari munculnya puncak baru yang yang tidak dimiliki oleh SPE 0.25 dan juga SPE 0.5. Selain itu, puncak-puncak pada sudut 2𝜃 23.10, 37.40, dan 39.450 yang terdapat pada SPE sebelumnya juga
intensitasnya meningkat walaupun peningkatannya bervariasi untuk masing-masing SPE. Adapun puncak-puncak baru yang teramati pada SPE 0.75 sampai dengan SPE 1.25 bisa dilihat pada sudut pada 2𝜃 32.550 dan 33.70. Seluruh puncak-puncak baru yang muncul ini