i
FORMULASI EKSTRAK UBI JALAR UNGU
(Ipomooea batatas L. Poir) DENGAN VARIASI POLIMER
SEBAGAI PENGISI TUNGGAL DALAM SEDIAAN TABLET
Tugas Akhir II
KADEK SASTRA NEGARA
1108505035
JURUSAN FARMASI
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS UDAYANA
i
FORMULASI EKSTRAK UBI JALAR UNGU
(Ipomooea batatas L. Poir) DENGAN VARIASI POLIMER
SEBAGAI PENGISI TUNGGAL DALAM SEDIAAN TABLET
Tugas Akhir II
KADEK SASTRA NEGARA
1108505035
JURUSAN FARMASI
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS UDAYANA
ii
Lembar Pengesahan
FORMULASI EKSTRAK UBI JALAR UNGU (Ipomooea
batatas L. Poir) DENGAN VARIASI POLIMER
SEBAGAI PENGISI TUNGGAL DALAM SEDIAAN
TABLET
Tugas Akhir II
Tugas Akhir ini diajukan sebagai syarat untuk memperoleh gelar sarjana
farmasi (S.Farm) di Jurusan Farmasi Fakultas Matematika dan Ilmu
Pengetahuan Alam Universitas Udayana
Oleh
KADEK SASTRA NEGARA
1108505035
Menyetujui:
Pembimbing I Pembimbing II
I G. N. Jemmy Anton P. S.Farm., M.Si., Apt. Cokorda Istri Sri Arisanti S.Farm., M.Si., Apt
NIP. 198501052008121002 NIP. 198011222006042023
Mengesahkan:
Ketua Jurusan Farmasi
Fakultas Matematika dan Ilmu Pengetahuan Alam
Dr. rer. nat. I Made Agus Gelgel Wirasuta, M.Si., Apt.
iii
KATA PENGANTAR
Puji syukur penulis panjatkan kehadapan Tuhan Yang Maha Esa, karena atas berkat dan rahmat-Nya lah penulis dapat menyelesaikan Tugas Akhir II yang dan Ilmu Pengetahuan Alam Universitas Udayana.
2. Dr. rer. nat. I Made Agus Gelgel Wirasuta, M.Si., Apt., selaku Ketua Jurusan Farmasi Fakultas MIPA Universitas Udayana. Terima kasih atas bimbingan dan bantuannya.
3. I G N Jemmy Anton Prasetia S.Farm., M.Si., Apt. selaku dosen pembimbing I yang telah bersedia meluangkan waktunya dan dengan penuh kesabaran membimbing, mengarahkan, serta memberikan motivasi dan perhatian kepada penulis dalam penyusunan skripsi ini.
4. Cokorda Istri Sri Arisanti S.Farm., M.Si., Apt selaku dosen pembimbing II yang telah bersedia meluangkan waktunya membimbing, mengarahkan, serta memberikan motivasi dan perhatian kepada penulis dalam penyusunan skripsi ini.
5. Ni Kadek Warditiani S.Farm., M.Sc., Apt. selaku dosen Pembimbing Akademik. Terimakasih atas bimbingan, dukungan, saran serta motivasi yang telah diberikan kepada penulis.
iv
7. Gede Pasek Budiyadnya selaku laboran yang telah penulis anggap sebagai pembimbing III secara tidak resmi, untuk informasi, arahan, serta motivasi kepada penulis dalam penyusunan skripsi ini.
8. Orang-orang sangat tersayang seperti xylem yang selalu memberikan sinar disaat penulis tersesat di kegelapan dalam proses penyusunan Tugas Akhir I ini .
9. Orang-orang tersayang seperti koala yang selalu memberikan motivasi, dukungan, dan semangat dalam penyusunan Tugas Akhir I ini.
10.Kepada sahabat grup Mosquito yaitu Jeffry, Buntil, Dwi, Andre, Dewa, Prima, Krisna, Ian, Perbawa, Sami, Indra, dll. yang senantiasa menemani disaat susah maupun senang.
11.Kepada teman-teman Teknolabilitas 2011, Sayu, Dwi, Yunita, Merlina, Narita, Sera, Intan, Ode, Dewa, Gung Dedy, Sayu atas dukungan serta motivasi yang diberikan kepada penulis
12.Sahabat penulis yaitu seluruh rekan Lumiere Onze Vauquelin yang senantiasa menyadarkan penulis ketika penulis merasa malas.
13.Kepada semua pihak yang namanya tidak bisa penulis sebutkan satu per satu, penulis mengucapkan terima kasih yang sebesar-besarnya
Penulis menyadari bahwa penyusunan ini masih jauh dari sempurna. Untuk itu, penulis mengharapkan kritik dan saran yang membangun demi perbaikan penyusunan ini selanjutnya. Harapan penulis, semoga Tugas Akhir II ini dapat bermanfaat kedepannya.
Bukit Jimbaran, 15 Januari 2016
v
DAFTAR SINGKATAN DAN ISTILAH ... viii
DAFTAR TABEL ... ix
2.4 Uji Kompresibilitas Serbuk... 10
2.5 Evaluasi ... 12
2.5.1 Uji Organoleptis ... 11
2.5.2 Uji Keseragaman Ukuran Tablet ... 12
2.5.3 Uji Keseragaman Bobot Tablet ... 13
vi
3.5 Variabel Penelitian ... 22
3.5.1 Variabel Bebas ... 22
3.5.2 Variabel Terikat ... 22
3.5.3 Variabel Terkendali ... 22
3.5.4 Batasan Operasional ... 22
3.6 Prosedur Penelitian ... 23
3.6.1 Determinasi Serbuk dan Tanaman ... 23
3.6.2 Persiapan Sampel ... 24
3.6.3 Ekstraksi Ubi Jalar Ungu ... 24
3.6.4 Pembuatan Amilum Singkong ... 24
3.6.5 Pembuatan amilum singkong partially pregelatinized ... 25
3.6.6 Pembuatan Formula Tablet ... 25
3.6.7 Metode Uji Komresibilitas Campuran Serbuk ... 26
3.6.8 Metode Pembuatan Tablet Ekstrak Ubi Jalar Ungu ... 26
3.6.9 Uji Sifat Fisik Tablet ... 27
vii
3.6.11 Penentuan Total Antosianin Menggunakan Metode
pH Differential ... 29
3.6.12 Verifikasi Formula Optimal ... 30
BAB IV HASIL DAN PEMBAHASAN 4.1 Formulasi Tablet Ubi Jalar Ungu ... 32
4.2 Uji Kompresibilitas Serbuk ... 32
4.3 Uji Sifat Fisik Tablet ... 33
4.3.1 Uji Organoleptik ... 34
4.3.2 Uji Keseragaman Ukuran ... 35
4.3.3 Uji Keseragaman Bobot ... 36
4.3.4 Uji Keseragaman Kandungan ... 37
4.3.5 Uji Kekerasan Tablet ... 37
4.3.6 Uji Kerapuhan Tablet ... 39
4.3.7 Uji Waktu Hancur Tablet ... 39
4.3.8 Uji Disolusi ... 41
4.4 Penentuan Formula Terpilih ... 46
BAB IV KESIMPULLAN DAN SARAN 5.1 Kesimpulan ... 47
5.1 Saran……. ... 47
viii
DAFTAR SINGKATAN DAN ISTILAH
Eksipien : Bahan tambahan.
pH differential : Salah satu metode penentuan kandungan total antosianin pada suatu sampel, memanfaatkan sifat antosianin yang mengalami perubahan struktur dan serapan pada pH 1 dan 4,5.
ix
DAFTAR TABEL
Halaman
Tabel 2.1 Hubungan Kompresibilitas Dengan Sifat Alir ... 12
Tabel 2.2 Persyaratan Uji Keseragaman Bobot Tablet ... 13
Tabel 3.1 Formula Tablet Ekstrak Ubi Jalar Ungu ... 24
Tabel 3.2 Hubungan Kompresibilitas dengan Sifat Alir ... 26
Tabel 4.1 Rata-rata kompresibilitas serbuk formula tablet ekstrak ubi jalar Ungu ... 33
Tabel 4.2 Hasil uji organoleptik tablet ekstrak ubi jalar ungu ... 34
Tabel 4.3 Hasil uji keseragaman ukuran tablet ekstrak ubi jalar ungu ... 35
Tabel 4.4 Hasil uji keseragaman bobot tablet ekstrak ubi jalar ungu ... 36
Tabel 4.5 Keseragaman Kandungan Tablet ... 37
Tabel 4.6 Rata-rata kekerasan tablet ekstrak ubi jalar ungu ... 38
Tabel 4.7 Rata-rata kerapuhan tablet ekstrak ubi jalar ungu ... 39
Tabel 4.8 Rata-rata waktu hancur tablet ekstrak ubi jalar ungu ... 40
Tabel 4.9 Rata-rata persentase antosianin pada tablet yang terdisolusi ... 42
x
DAFTAR GAMBAR
Halaman Tabel 2.1 Ubi Jalar Ungu ... 7 Tabel 2.2 Alat Uji Disolusi Tipe 2 ... 16 Tabel 3.1 Profil disolusi tablet ekstrak ubi jalar ungu pada formula I, II,
xi
ABSTRAK
Salah satu permasalahan dalam pengembangan obat herbal menjadi sediaan tablet adalah kesulitan dalam menghasilkan sediaan yang memenuhi persyaratan sifat fisik dan pelepasan zat aktif obat. Penggunaan ekstrak sebagai bahan aktif obat memiliki kesulitan tersendiri, yang mana terdapat sifat fisikokimia dari ekstrak maupun dari kandungan yang terdapat pada ekstrak yang membuatnya sulit untuk diformulasikan. Penelitian ini bertujuan untuk mengetahui polimer yang sesuai sebagai pengisi tunggal dalam sediaan tablet herbal sehingga menghasilkan tablet yang memenuhi persyaratan fisik dan disolusi sediaan tablet. Digunakan 3 variasi polimer sebagai bahan pengisi yaitu avicel® PH 102, natrium alginat dan amilum singkong Amilum singkong partialy pregelatinized dengan ekstrak ubi jalar ungu sebagai permodelan bahan aktif.
Ekstrak ubi jalar ungu dikeringkan terlebih dahulu menggunakan aerosil dengan perbandingan 1 : 1 sebelum siap untuk dicetak. Pembuatan tablet dilakukan menggunakan metode kempa langsung dengan perbandingan ekstrak : eksipien yaitu 1 : 4. Tablet yang dihasilkan selanjutnya dievaluasi meliputi uji organoleptis, keseragaman bobot, kekerasan, kerapuhan, waktu hancur, dan uji disolusi.
Hasil menunjukkan bahwa dari seluruh pengujian sifat fisik tablet yang dilakukan, hanya tablet dengan bahan pengisi avicel® PH 102 yang memenuhi seluruh persyaratan uji sifat fisik. Dilihat dari laju disolusinya, tablet dengan bahan pengisi avicel® PH 102 memiliki kecepatan disolusi yang cukup baik yaitu >80% dalam 30 menit, meskipun lebih rendah dibanding pengisi amilum singkong partialy pregelatinized. Sehingga dapat disimpulkan perbedaan variasi polimer sebagai pengisi dapat menghasilkan tablet dengan sifat fisik dan profil disolusi yang berbeda. Formula yang menggunakan bahan avicel® PH 102 sebagai pengisi tunggal dipilih sebagai formula terpilih.
xii
ABSTRACT
The problems in the development of herbal medicine into a tablet dosage form is the difficulty in producing pharmaceutical preparations that meet the requirements of the physical properties and the release of the active drug substance. The use of plant extract as the active ingredient for pharmaceutical preparation has its own difficulties, which are the properties of the extract that usually thick and soft, and the presence of certain compounds in the extract that needs to be preserved, makes it difficult to formulate into solid dosage form. The aim of this study is to determine the appropriate polymer that can be used as a single filler to produce a tablet that meets the requirements for physical properties and dissolution profile. Three variation of polymer were used in study, that is avicel® PH 102, sodium alginate and partially pregelatinized cassava starch. Purple sweet potato extract were used as the main active ingredient.
Purple sweet potato extract is dried prior to use, using aerosil as the absorbent at the ratio of 1:1. The tablets were manufactured by using direct compression method with a ratio of extracts: excipients is 1: 4. The prepared tablets were evaluated for organoleptic test, uniformity of weight, hardness, friability, disintegration time and dissolution test.
Results showed that only the tablet with a filler material avicel® PH 102 meets all the requirements of physical properties. Judging from the rate of dissolution the tablet excipients avicel® PH 102 have a good disolution rate or more than 80% release in 30 minutes despite the value is lower than the disolution rate of partially pregelatinized cassava starch. Therefore we can conclude that the variation of polymer used as a single filler can produce a tablet with different physical properties and dissolution profiles. The formula that uses avicel® PH 102 as a single filler is choosen as the best formula.
1
BAB I
PENDAHULUAN
1.1 Latar Belakang
Obat herbal didefinisikan sebagai obat-obat yang dibuat dari bahan alami seperti tumbuhan yang sudah dibudidayakan maupun tumbuhan liar. Selain itu, obat herbal juga bisa terdiri dari obat yang berasal dari sumber hewani, mineral atau gabungan antara ketiganya (Mangan, 2003). Akhir-akhir ini penggunaan obat herbal mulai diminati oleh masyarakat baik di negara maju dan negara berkembang. Hal ini dikarenakan obat herbal dipercaya memiliki beberapa keuntungan dibanding obat modern diantaranya yaitu efek samping yang minimal jika digunakan secara tepat, harganya yang relatif lebih murah dibanding obat modern, serta tidak memerlukan teknologi yang rumit dalam pengolahannya (Payyappallimana, 2010). Dalam upaya untuk memanfaatkan potensi obat herbal yang begitu besar serta untuk meningkatkan penerimaan masyarakat terhadap obat herbal, maka perlu dilakukan pengembangan obat herbal menjadi bentuk sediaan farmasi.
Rute oral adalah rute yang paling sering dan nyaman digunakan untuk pemberian obat atau sediaan farmasi, oleh sebab biaya terapi yang relatif rendah dan kemudahan penggunaannya yang mengarah pada tingginya kepatuhan pasien untuk menggunakan obat dalam rute oral (Dash and Verma, 2013). Salah satu bentuk sediaan yang dapat digunakan secara oral adalah bentuk sediaan tablet. Tablet adalah sediaan padat kompak, dibuat secara kempa cetak, dalam bentuk
2
tabung pipih atau sirkuler, kedua permukaannya rata atau cembung, mengandung satu jenis obat atau lebih dengan atau tanpa zat tambahan (Depkes RI, 1979). Keunggulan sediaan ini antara lain proses produksinya yang mudah serta ekonomis, stabilitas yang relatif lebih baik, distribusi dan penyimpanannya yang mudah, nyaman dalam penggunaanya dan dosis lebih akurat dibandingkan sediaan cair oral (Harbir, 2012).
Salah satu permasalahan dalam pengembangan obat herbal menjadi sediaan tablet adalah kesulitan dalam menghasilkan sediaan yang memenuhi persyaratan sifat fisik, stabilitas fisika dan kimia, serta pelepasan bahan aktif yang mengarah pada bioavailabilitas bahan aktif obat. Sebagian besar komponen utama obat herbal yang digunakan adalah dalam bentuk ekstrak kental, yang mana pada ekstrak tersebut terdapat kandungan air atau pelarut yang membuatnya sedikit basah sehingga sulit untuk diformulasikan terutama menjadi bentuk sediaan padatan seperti tablet. Permasalahan lainnya dari penggunaan ekstrak sebagai komponen utama yaitu ekstrak pada umumnya memiliki daya alir dan kompresibilitas yang buruk meskipun sudah dalam bentuk kering, sehingga susah untuk dikempa secara langsung (Gallo et al., 2013). Oleh karena itu, peneliti merasa perlu untuk melakukan penelitian tentang formulasi sediaan tablet menggunakan ekstrak tumbuhan yang berkhasiat obat sebagai bahan aktif.
3
dapat diekstraksi dengan mudah yaitu menggunakan metode maserasi dengan pelarut etanol asam, dan telah ditemukan metode untuk menganalisis antosianin secara kuantitatif dengan mudah yaitu menggunakan metode pH differential (Jiao
et al., 2012; Huang et al., 2010; Giusti dan Worlstad, 2001). Permasalahan dalam penggunaan ekstrak ubi jalar ungu sebagai bahan aktif adalah daya alir ekstrak yang kurang baik dan senyawa aktif ekstrak yaitu antosianin dapat berubah menjadi senyawa bermuatan, yang mana senyawa antosianin dalam ekstrak ubi jalar ungu pada suasana asam dapat berubah bentuk menjadi senyawa kation (bermuatan positif), yang memungkinkan terjadinya interaksi zat aktif dan eksipien jika diformulasikan dengan eksipien ionik baik anion maupun kation (Giusti dan Worlstad, 2001; Crowley and Martini, 2001). Berdasarkan informasi tersebut, formulasi ekstrak ubi jalar ungu merupakan langkah yang kompleks, dan eksipien yang tepat perlu ditambahkan pada ekstrak.
Dalam pembuatan tablet, metode yang umum digunakan adalah metode kempa langsung. Beberapa penelitian tentang formulasi tablet herbal dengan metode kempa langsung yang pernah dilakukan, menggunakan permodelan tablet dengan perbandingan zat aktif : eksipien yaitu 1:4, menghasilkan tablet dengan profil disolusi yang baik dan sifat fisik tablet yang memenuhi persyaratan (Majekodunmi et al., 2008; Rojas et al., 2013). Pada penelitian ini akan digunakan rasio ekstrak : eksipien 1:4 dalam pembuatan tablet secara kempa langsung.
4
dibagi menjadi dua jenis yaitu polimer dan dan non polimer (Shah et al., 2014). Eksipien polimer sering digunakan untuk memformulasi matriks tablet. Pemilihan polimer tergantung pada sifat fisikokimia bahan obat yang akan dimasukkan ke dalam sistem matriks dan jenis pelepasan obat yang dibutuhkan. Eksipien polimer dibagi menjadi dua yaitu non ionik (pH independent) dan ionik (pH dependent). Eksipien polimer ionik dapat menimbulkan terjadinya interaksi ionik dengan zat aktif yang memiliki muatan. Senyawa yang bermuatan dapat saling tarik-menarik dengan senyawa yang memiliki muatan berlawanan, dan tolak-menolak dengan senyawa yang bermuatan sama, hal tersebut dapat mempengaruhi kelarutan dan pelepasan senyawa aktif dari matriks tablet (Yoshida et al., 2013; Crowley and
Martini, 2001). Oleh karena itu kemampuan eksipien untuk terionisasi juga perlu diperhatikan dalam memformulasi suatu bahan aktif yang memiliki muatan.
5
1.2 Rumusan Masalah
Berdasarkan latar belakang masalah di atas, dapat dirumuskan masalah yaitu apakah terdapat perbedaan pada sifat fisik serta profil disolusi tablet ekstrak ubi jalar ungu setelah dilakukan variasi terhadap polimer yang digunakan sebagai pengisi dalam proses pembuatan tablet dengan metode kempa langsung ?
1.3 Tujuan Penelitian
Tujuan dari penelitian ini adalah untuk memperoleh polimer yang sesuai sebagai bahan pengisi dalam memformulasi suatu sediaan farmasi tablet dengan bahan aktif ekstrak ubi jalar ungu sehingga menghasilkan tablet yang memenuhi persyaratan fisik dan disolusi sediaan tablet.
1.4 Manfaat Penelitian
6
BAB II
TINJAUAN PUSTAKA
2.1 Ekstrak Ubi Jalar Ungu
2.1.1. Ubi Jalar Ungu
Klasifikasi tanaman ubi jalar ungu,
Kingdom : Plantae
Divisi : Spermatophyta Subdivisi : Angiospermae Kelas : Dicotyledonae Ordo : Convolvulales Famili : Convulvulaceae Genus : Ipomoea
Spesies : Ipomoea batatas L. Poir
(Rukmana, 1997). Tanaman Ipomoea batatas L. Poir termasuk tanaman semusim (annual) yang memiliki ciri-ciri susunan tubuh utama terdiri atas batang, daun, bunga, buah, biji,
dan umbi. Batang tanaman berbentuk bulat, tidak berkayu, dan berbuku-buku.
Tipe pertumbuhan tegak dan merambat/menjalar, dengan warna umbi bervariasi
yaitu putih, krem, orange, dan ungu (Suprapti, 2003). Ubi jalar ungu merupakan
salah satu jenis ubi jalar yang banyak ditemui di Indonesia. Ubi jalar ungu jenis
Ipomoea batatas L. Poir memiliki warna ungu yang cukup pekat pada daging
ubinya. Adanya antosianin yang menyebar dari bagian kulit sampai dengan
7
dagingnya, membuat ubi jalar ungu memiliki warna ungu yang khas. Kandungan antosianin pada ubi jalar ungu cukup tinggi yaitu mencapai 519 mg/100 g berat basah (Apriliyanti, 2010). Ubi jalar ungu memiliki beberapa aktivitas farmakologi seperti antioksidan, antiulcer, antimutagenik, hepatoprotektif, serta antidiabetik (Montila et al., 2011).
Gambar 2.1. Ubi jalar ungu (Jusuf dkk., 2008).
2.1.2. Ekstrak
Ekstrak adalah sediaan kering, kental atau cair yang diperoleh dengan mengekstraksi senyawa aktif dari simplisia nabati atau simplisia hewani menggunakan pelarut yang sesuai, kemudian semua atau hampir semua pelarut diuapkan dan massa atau serbuk yang tersisa diperlakukan sedemikian hingga memenuhi baku yang telah ditetapkan (Depkes RI, 1995).
2.1.3. Ekstrak Ubi Jalar Ungu
8
dapat digunakan adalah metode maserasi (Huang et al., 2010). Ekstraksi ubi jalar ungu menggunakan etanol 75% sebagai pelarut dapat menghasilkan rendemen sebesar 3,9 % (Hambali dkk., 2014).
2.2 Tablet
Tablet adalah sediaan padat kompak, dibuat secara kempa cetak, dalam bentuk tabung pipih atau sirkuler, kedua permukaannya rata atau cembung, mengandung satu jenis obat atau lebih dengan atau tanpa zat tambahan. Zat tambahan yang digunakan dapat berfungsi sebagai zat pengisi, zat pengembang, zat pengikat, zat pelicin, zat pembasah, atau zat lain yang cocok (Depkes RI, 1979). Tablet menjadi sediaan yang paling banyak diproduksi karena memiliki beberapa keuntungan seperti ketepatan dosis, biaya produksi dan pengemasan lebih murah dan relatif lebih stabil dibanding bentuk sediaan lain (Harbir, 2012).
2.2.1 Metode Pembuatan Tablet
Tablet dapat diproduksi dengan cara cetak atau kempa. Tablet cetak diproduksi menggunakan mesin tablet atau secara manual dengan memberikan tekanan pada bahan tablet dengan menggunakan cetakan sehingga menghasilkan bentuk tablet yang diinginkan. Tablet yang tercetak kemudian dikeluarkan dan dibiarkan hingga kering. Tablet cetak biasanya digunakan pada produksi skala kecil dan laboratorium (Harbir, 2012).
9
granulasi karena bahan-bahan yang digunakan telah memiliki laju alir dan kompresibilitas yang baik (Dokala, 2013).
Keunggulan yang dimiliki metode kempa langsung sehingga banyak digunakan dalam formulasi sediaan tablet antara lain efektif, stabilitas, disolusi yang lebih cepat, dan beberapa keuntungan lainnya. Metode tersebut melalui tahapan yang lebih singkat sehingga lebih efektif dari segi biaya dan waktu produksinya. Peningkatan stabilitas pada zat aktif sediaan yang sensitif terhadap panas dan lembab. Peningkatan tersebut terjadi karena metode ini tidak melalui tahap pembasahan dan pengeringan. Disolusi yang lebih cepat terjadi karena pada proses disolusi tablet kempa langsung, tablet langsung terdisintegrasi menjadi pertikel tanpa melalui fase granul terlebih dahulu. Keunggulan lainnya yang dimiliki tablet kempa langsung seperti kontaminasi yang rendah karena bahan-bahan diproses dalam jangka waktu yang cepat dan pertumbuhan mikroba yang lebih rendah karena dalam metode tersebut tidak menggunakan air (Dokala, 2013). Polimer yang sering digunakan sebagai eksipien tunggal dalam pembuatan sediaan tablet secara kempa langsung diantaranya mikrokristalin selulosa (avicel®), natrium alginat dan amilum terpregelatinasi karena umumnya bahan-bahan tersebut memiliki sifat alir yang baik sehingga cocok untuk dikempa langsung (Majekodunmi et al., 2008; Ahmad et al., 2014; Rojas et al., 2013).
2.3 Polimer
10
identik (Denis, 2010). Polimer banyak digunakan dalam bidang farmasi, salah satnya adalah sebagai eksipien tablet. Bahan-bahan yang tergolong polimer adalah selulosa dan pati, yang merupakan eksipien alami. Selulosa dan pati serta turunan-turunanya dapat digunakan sebagai pengisi sediaan jika jumlah obat dalam tablet sedikit. Selain itu eksipien polimer juga dapat berperan sebagai disintegrant untuk pembuatan tablet konvensional yang memerlukan disintegrasi yang cepat pada medium air (Denis, 2010). Eksipien polimer dibagi menjadi dua yaitu non ionik (pH independent) dan ionik (pH dependent). Contoh polimer ionik adalah mikrokristalin selulosa/avicel®, karboksimetil selulosa, alginat, kitosan dan lain-lain. Contoh polimer nonionik antara lain polivinil pirolidon (PVP), hidroksi propil metil selulosa (HPMC), kopovidon, hidroksi propil selulosa (HPC) dan lain-lain (Troy and Paul, 2006; Shah et al., 2014).
2.4 Uji Kompresibilitas Serbuk
Uji kompresibilitas diperlukan untuk dapat menentukan bagaimana sifat aliran dari campuran serbuk. Sifat alir ini sangat berperan penting untuk dapat menghasilkan tablet yang kompak dan stabil. Dalam uji kompresibilitas perlu ditentukan terlbih dahulu nilai bobot jenis nyata dan bobot jenis mampat dari serbuk (Lachman et al., 2008).
a. Bobot jenis nyata
11
Bobot jenis mampat adalah perbandingan berat serbuk dengan volume serbuk setelah dilakukan pengentukkan hingga volumenya konstan (Voigt, 1995). Selanjutnya dihitung bobot jenis mampatnya dengan persamaan sebagai berikut:
volumesetelah pemampatan( )
Kompaktibilitas adalah kemampuan suatu bahan untuk berkurang volumenya pada saat mendapatkan tekanan. Sehingga hal ini menentukan kemampuan serbuk untuk menjadi bentuk yang lebih stabil jika mendapat tekanan, yaitu mudah menyusun diri pada saat memasuki ruang cetak kemudian mengalami perubahan bentuk menjadi bentuk yang mampat dan akhirnya menjadi massa yang kompak dan stabil (Lachman et al., 2008). Persen kompaktibilitas dihitung berdasarkan data yang diperoleh dari pengukuran bobot jenis nyata dan bobot jenis mampat. Berikut ini adalah persamaan untuk menghitung % kompaktibilitas:
12
Tabel 2.1 Hubungan Kompresibilitas Dengan Sifat Alir Kompresibilitas (%) Sifat aliran
Uji organoleptis merupakan uji dengan menggunakan indera manusia sebagai alat utama untuk pengukuran daya penerimaan terhadap produk. Penampilan umum tablet meliputi ukuran tablet, bentuk, warna, ada tidaknya bau, rasa, dan bentuk permukaan dan cacat fisik. Penampilan umum tablet penting bagi penerimaan konsumen (Lachman et al., 2008).
2.5.2. Uji Keseragaman Ukuran Tablet
Metilselulosa Uji dilakukan untuk mengetahui konsistensi ukuran tablet yang dihasilkan. Diukur diameter dan tebal dari 20 tablet menggunakan jangka sorong. Diameter tablet tidak lebih dari 3 kali dan tidak kurang dari 1 1/3 tebal tablet (Anief, 2010).
2.5.3. Uji Keseragaman Bobot Tablet
13
bobot rata-rata. Persyaratan uji keseragaman bobot tablet ditunjukkan pada tabel 2.2 berikut.
Tabel 2.2. Persyaratan uji keseragaman bobot tablet (Anief, 2010).
Keterangan : Tidak boleh lebih dari dua tablet yang bobotnya menyimpang dari bobot rata-ratanya lebih besar dari harga yang ditetapkan kolom A dan tidak satu tablet pun yang bobotnya menyimpang dari bobot rata-ratanya lebih besar dari harga yang ditetapkan kolom B.
2.5.4. Uji Kekerasan Tablet
Kekerasan adalah parameter yang menggambarkan ketahanan tablet terhadap tekanan mekanik seperti goncangan, kikisan, dan keretakan tablet selama pembungkusan, pengangkutan, dan pemakaian. Tablet tidak boleh terlalu rapuh dan terlalu keras. Jika tablet terlalu rapuh kemungkinan tablet dapat rusak sebelum diterima pasien, sedangkan jika tablet terlalu keras dapat mempengaruhi disolusi tablet didalam tubuh. Tablet diambil sebanyak 10 tablet, lalu dimasukkan satu per satu ke dalam alat hardness tester dan alat dinyalakan. Data hasil pengujian kekerasan tablet dicatat. Kekerasan tablet biasanya 4-8 kg (Lachman et al., 2008).
2.5.5. Uji Kerapuhan Tablet
Uji kerapuhan tablet dilakukan karena pada saat pengemasan dan pengepakan serta pengangkutan kemungkinan tablet mengalami benturan. Benturan pada proses tersebut dapat menghilangkan partikel-partikel obat yang berada di permukaan tablet. Tablet yang mudah menjadi bubuk, menyerpih dan pecah akan menyebabkan berkurangnya akseptibilitas sediaan oleh pasien dan menimbulkan
Bobot rata-rata Penyimpangan bobot rata-rata dalam %
A B
25 mg atau kurang 15% 30%
25 mg sampai dengan 150 mg 10% 20%
150 mg sampai dengan 300 mg 7,5% 15%
14
variasi pada berat dan keseragaman isi tablet. Uji kerapuhan di laboratorium menggunakan alat uji kerapuhan. Alat tersebut memiliki sejenis kotak plastik yang berputar pada kecepatan 25 rpm, menjatuhkan tablet sejauh enam inci pada setiap putaran. Tablet diambil sebanyak 30 tablet lalu dibersihkan, kemudian ditimbang (W1 gram), lalu dimasukkan ke dalam alat uji kerapuhan untuk diuji. Alat diset dengan kecepatan putaran 25 rpm selama 4 menit. Tablet dikeluarkan, lalu bersihkan dan ditimbang kembali (W2 gram). Dihitung persentase kerapuhan tablet. Kehilangan berat kurang dari 1 % masih dapat diterima (Ansel, 2005). Persentase kerapuhan tablet dapat dihitung menggunakan persamaan berikut.
% Kerapuhan tablet = �1−�2
�1 x 100 %...persamaan (2.4)
2.5.6. Uji Waktu Hancur Tablet
Waktu hancur adalah hal yang penting untuk sediaan yang diberikan secara oral. Tablet harus segera terlarut untuk dapat diabsorbsi. Sediaan hancur sempurna bila sisa sediaan yang tertinggal pada kasa alat uji merupakan massa lunak yang tidak mempunyai inti yang jelas. Memasukkan 1 tablet pada masing-masing 6 tabung dari keranjang. Memasukkan satu cakram pada setiap tabung dan menjalankan alat. Digunakan air bersuhu 37 ± 2˚C sebagai media dengan volume
15
2.5.7. Uji Disolusi Tablet
Disolusi adalah proses pemindahan molekul obat dari bentuk padat ke dalam larutan pada suatu medium. Disolusi merupakan salah satu faktor penentu proses absorbsi obat dalam tubuh manusia, terutama apabila zat aktif tersebut kelarutan yang kecil dalam medium gastrik intestinal. Disolusi juga sangat mempengaruhi efektivitas bahan obat dalam sediaan tablet (Fudholi, 2013). Uji disolusi dilakukan untuk mengetahui proses melarutnya suatu zat kimia atau senyawa obat dari sediaan padat ke dalam suatu medium tertentu. Uji disolusi berguna untuk menentukan jumlah obat yang melarut dalam medium asam atau basa (Ansel, 2005). Karakteristik fisik sediaan, proses pembasahan sediaan, kemampuan penetrasi media disolusi ke dalam sediaan, proses disintegrasi dan deagragasi sediaan merupakan sebagian dari faktor yang mempengaruhi karakteristik disolusi obat dari sediaan (Fudholi, 2013). Pada Farmakope Indonesia dijelaskan uji disolusi dapat dilakukan dengan 2 tipe alat, alat Tipe 1 (metode keranjang) dan alat tipe 2 (metode dayung).
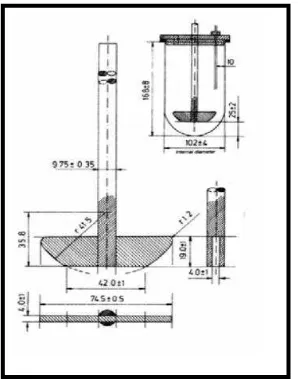
16
mm, dengan volume sampai 1000 ml. Batang logam berada pada posisi tertentu sehingga sumbunya tidak lebih dari 2 mm dan berputar dengan halus tanpa goyangan yang berarti. Jarak antara daun dan bagian dalam dasar wadah dipertahankan selama pengujian berlangsung. Daun dan batang logam yang merupakan satu kesatuan dapat disalut dengan suatu penyalut inert yang sesuai. Sediaan dibiarkan tenggelam ke dasar wadah sebelum dayung mulai berputar (Depkes RI, 1979).
Gambar 2.2 Alat uji disolusi tipe 2 (Depkes RI, 1979).
Untuk tablet konvensional, diharapkan obat terlepas sebanyak ≥85% dari
jumlah yang tertera pada kemasan dalam waktu 30 menit (Rathod, 2014).
2.6 Eksipien
2.6.1 Avicel®
Avicel® merupakan nama dagang dari mikrokristalin selulosa. Avicel® dibuat dari hidrolisis terkontrol α-selulosa dengan larutan asam mineral encer. Sebagai
17
granulasi maupun cetak langsung, bahan penghancur tablet, adsorben dan bahan anti lekat. Avicel® diketahui mempunyai sifat alir dan kompresibilitas yang sangat baik. Avicel® sering dilakukan co-processing dengan karagenan, sodium karboksimetilselulosa dan guar gum (Rowe et al., 2003).
Mikrokristalin selulosa dapat diperoleh secara komersial dari berbagai kualitas dan merek dagang. Salah satu produk selulosa mikrokristal di perdagangan dikenal dengan merek dagang Avicel®. Ada beberapa macam jenis avicel®, salah satunya avicel® PH 102. Avicel® PH 102 merupakan selulosa yang terdepolimerasi parsial berwarna putih, tidak berasa, tidak berbau, serbuk kristal yang terdiri atas partikel porous, tidak larut dalam asam encer dan sebagian pelarut organik (Maryatun, 2010).
Avicel® PH 102 merupakan produk aglomerasi dengan distribusi ukuran partikel yang besar dan menunjukkan sifat alir serta kompaktibilitas yang baik. Ikatan yang terjadi antar partikelnya adalah ikatan hidrogen, ikatan ini sangat berperan terhadap kekerasan dan kohesifitasnya. Pada tekanan kompresi partikelnya mengalami deformasi plastis, sehingga dapat menaikkan kompaktibilitas (Sheth and Shangraw, 1980).
2.6.2 Natrium Alginat
18
juga dpat digunakan sebagai pengisi (Rowe et al., 2009). Natrium alginat layak digunakan sebagai eksipien untuk pembuatan tablet dengan metode kempa langsung karena memiliki daya alir dan kompaktibilitas yang cukup baik (Rojas et al., 2013).
2.6.3 Amilum Pregelatinasi
Amilum pregelatin adalah amilum yang telah mengalami proses modifikasi fisik dengan adanya penambahan air dan atau pemanasan sehingga memecah semua atau sebagian ikatan dari butir–butir amilum. Amilum yang dihasilkan memiliki sifat alir yang lebih baik serta dapat digunakan sebagai bahan pembawa cetak langsung (Rowe et al., 2009). Amilum pregelatin dibuat dengan cara memanaskan suspensi amilum dalam airdisekitar suhu gelatinisasinya, kemudian dilakukan pengeringan. Pemanasan suspensi amilum dalam air disekitar suhu gelatinisasi akan memutus struktur dari granul amilum dan dengan masuknya air ke dalam granul secara perlahan, terjadi pengembangan struktur granul karena air masuk dengan jumlah besar sehingga menyebabkan pecahnya granul amilum dan menyebabkan amilum dapat larut dalam air (Yusuf dkk., 2008).
2.6.4 Magnesium Stearat
19
2.6.5 Talk
Talk adalah magnesium silikat hidrat alam, kadang-kadang mengandung sedikit aluminium silikat. Pemerian berupa serbuk hablur sangat halus, putih atau putih kelabu. Berkilat, mudah melekat pada kulit dan bebas dari butiran (DepKes RI, 1995).
2.6.6 Aerosil