ANALISIS KADAR ASAM ASKORBAT DALAM EKSTRAK DAUN KELOR (Moringa oleifera Lam) DARI DAERAH PESISIR DAN PEGUNUNGAN SERTA
POTENSINYA SEBAGAI ANTIOKSIDAN Resky Dwi Cahyati, Hasnah Natsir, Abd. Wahid Wahab
Jurusan Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Hasanuddin Jl. Perintis Kemerdekaan Km. 10 Makassar 90245 email: reskydc@ymail.com
ABSTRACT
This research is aiming to determine the level of ascorbic acid in young and old moringa leaves (Moringa oleifera Lam) from seaboard and highlands and also to determine the antioxidant activity. Moringa leaves were extracted using water and sodium oxalate (Na-2C2O4) by maceration method, centrifuged at 2000 rpm for 10 minutes and analyzed using 1,1-diphenyl-2-picrylhydrazil (DPPH) method which observed parameter are the free radical reduction at 30thminute with diverse concentration (1 ppm, 2 ppm, 3 ppm, 4 ppm and 5 ppm) and IC50value (Inhibitory Concentration) analyzed using regression equation. Result shows the level of ascorbic acid in young leaves from seaboard is 361,71 mg/L, old leaves from seaboard is 363,49 mg/L, young leaves from mountains is 308,66 mg/L, and old leaves from mountain is 312,05 mg/L. Examination result of antioxidant activity using UV-Vis spectrophotometer at wavelenght 515 nm obtained the IC50in young leaves from seaboard is 9,901 μg/mL, old leaves from seaboard is 26,109 μg/mL, young leaves from mountains is 6,583μg/mL, and old leaves from mountains is 7,891μg/mL, so that were categorized as very strong antioxidant. Antioxidant activity of moringa old leaves extract is stronger than moringa young leaves, however its weaker than vitamin C and BHT with IC50value 2,87 μg/mL and 7,00μg/mL.
Key words: Ascorbic acid (vitamin C), antioxidant activity, moringa leaf (Moringa oleifera Lam), DPPH, mountains, seaboard, UV-Vis Spectrophotometer.
ABSTRAK
Penelitian ini bertujuan untuk menentukan kadar asam askorbat (vitamin C) dalam daun muda dan daun tua kelor (Moringa oleifera Lam) dari daerah pesisir dan pegunungan serta menentukan aktivitas antioksidannya. Daun kelor diekstraksi menggunakan air dan natrium oksalat (Na2C2O4) dengan metode maserasi, disentrifuge pada 2000 rpm selama 10 menit dan dianalisis vitamin C dengan Spektrofotometer UV-Vis. Pengujian aktivitas antioksidan dengan metode 1,1-diphenyl-2-picrylhydrazil (DPPH) dengan parameter yang diamati adalah persen peredaman radikal bebas pada menit ke-30 dengan konsentrasi berbeda (1 ppm, 2 ppm, 3 ppm, 4 ppm dan 5 ppm) dan nilai IC50 (Inhibitory Concentration) dianalisis menggunakan persamaan regresi. Hasil penelitian menunjukkan kadar asam askorbat (vitamin C) daun kelor muda pesisir adalah 361,71 mg/L, daun kelor tua pesisir adalah 363,49 mg/L, daun kelor muda pegunungan adalah 308,66 mg/L, dan daun kelor tua pegunungan adalah 312,05 mg/L. Hasil pemeriksaan aktivitas antioksidan dengan menggunakan spektrofotometer UV-Vis pada panjang gelombang 515 nm diperoleh IC50 dari daun kelor muda pesisir adalah 9,901 μg/mL, daun kelor tua pesisir adalah 26,109 μg/mL, daun kelor muda pegunungan adalah 6,583
μg/mL, dan daun kelor tua pegunungan adalah 7,891 μg/mL, sehingga digolongkan sebagai antioksidan sangat kuat. Aktivitas antioksidan ekstrak daun kelor tua lebih kuat dibandingkan daun kelor muda, namun lebih lemah dibandingkan vitamin C dan BHT dengan nilai IC502,87
μg/mL dan 7,00 μg/mL.
Kata kunci : Asam askorbat (vitamin C), aktivitas antioksidan, daun kelor (Moringa oleifera Lam), DPPH, pegunungan, pesisir, spektroforometer UV-Vis.
PENDAHULUAN
Di Indonesia terdapat beberapa masalah gizi utama, salah satunya adalah anemia gizi besi atau yang dikenal masyarakat sebagai penyakit kurang darah. Penyebab langsung anemia gizi adalah selain jumlah Fe dalam tubuh manusia tidak cukup, juga diakibatkan oleh absorbsi atau penyerapan zat besi yang rendah (Citrakusumasari, 2012). Oleh karena itu, dibutuhkan suatu zat yang dapat membantu penyerapan zat besi dalam tubuh.
Vitamin C adalah vitamin yang larut dalam air yang berfungsi dalam metabolisme zat besi di usus dan pemindahannya ke dalam darah. Vitamin C dapat terlibat dalam mobilisasi simpanan besi terutama hemosiderin dalam limpa (Linder, 1992). Menurut penelitian Zarianis (2006), defisiensi zat besi penyebabnya bukan karena asupan besi yang kurang dari makanan, ternyata dengan pemberian vitamin C dapat meningkatkan kadar hemoglobin serta dapat menurunkan prevalensi anemia. Vitamin C merupakan vitamin yang tidak dapat tersimpan lama dalam tubuh, sehingga perlu dikonsumsi setiap hari. Salah satu tanaman yang kaya akan vitamin C adalah tanaman kelor, khususnya pada bagian daun.
Kelor (Moringa oleifera Lam) adalah tanaman yang memiliki banyak nama di berbagai negara. Diduga berasal dari kawasan pegunungan Himalaya dan India, untuk daratan Asia termasuk Indonesia, tanaman kelor yang tumbuh masuk dalam spesies Moringa oleifera dari genus Moringacae. Dalam dunia ilmu pengetahuan mengakui bahwa tanaman kelor merupakan tanaman yang kaya akan nutrisi khususnya vitamin. Karena kandungan nutrisi yang terkandung dalam tanaman kelor, maka tanaman tersebut dapat dijadikan sebagai alternatif sumber antioksidan alami (Krisnadi, 2015).
Antioksidan merupakan senyawa kimia yang dapat menyumbangkan satu atau lebih elektron (electron donor) kepada radikal bebas, sehingga radikal bebas dapat
diredam. Senyawa ini memiliki berat molekul yang kecil, tetapi mampu menginaktivasi berkembangnya reaksi oksidasi dengan cara mencegah terbentuknya radikal (Winarsi, 2007)
Hasil penelitian spesies Moringa
oleifera sebelumnya menunjukkan bahwa,
hasil uji aktivitas antioksidan ekstrak daun kelor menggunakan metode DPPH memiliki nilai IC50 pada kisaran 5,72 -42,56 μg/mL, sehingga dapat
dikategorikan sebagai antioksidan kuat yang mampu menangkal radikal bebas dalam jumlah besar (Unuigbe, dkk. 2014). Sedangkan menurut Aslam, dkk. (2005), menyatakan bahwa perbedaan regional atau lokasi tumbuh daun kelor dapat berpengaruh terhadap kuantitas kandungan nutrisinya. Fatchurrozak, dkk. (2013) menyebutkan bahwa semakin tinggi ketinggian tempatnya, maka semakin tinggi pula stress lingkungan. Ketika tanaman mengalami stress, maka produksi metabolit sekunder termasuk produksi vitamin mengalami peningkatan.
METODOLOGI Waktu dan Tempat
Analisis dilakukan pada bulan Februari-Juni 2016 bertempat di Laboratorium Biokimia, Laboratorium Kimia Terpadu, Jurusan Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, dan Laboratorium Bioteknologi, Fakultas Peternakan, Universitas Hasanuddin, Makassar.
Alat dan Bahan
alat-alat gelas yang biasa digunakan di laboratorium, pipet mikro, vortex, spektrofotometer UV-2600 Shimadzu,
sentrifuge dingin Universal 320 R, neraca
analitik, blender, daun kelor, Na2C2O4, C6H8O7.H2O, Na2HPO4.2H2O p.a, asam askorbat, DPPH, BHT metanol p.a, kertas saring, aluminium foil, dan akuades.
Prosedur Kerja Analisis Kadar Asam Askorbat
Pembuatan Larutan Buffer Fosfat Sitrat pH 5
Larutan buffer fosfat sitrat pH 5 dibuat dengan cara mencampurkan sebanyak 121,25 mL asam sitrat (C6H8O7.H2O 0,1 M) dan 128,75 mL Na2HPO4.2H2O 0,2 M ke dalam labu ukur 250 mL kemudian dihomogenkan.
Pembuatan Larutan Natrium Oksalat 0,01 N
Padatan Na2C2O4 ditimbang sebanyak 0,1675 gram kemudian dilarutkan dengan larutan buffer fosfat sitrat pH 5. Larutan dimasukkan ke dalam labu ukur 250 mL dan dihimpitkan hingga tanda batas lalu dihomogenkan.
Pembuatan Larutan Induk Asam Askorbat 1000 ppm
Asam askorbat sebanyak 0,05 gram dimasukkan ke dalam gelas kimia 50 mL kemudian dilarutkan dengan Na2C2O4 0,01 N. Larutan kemudian dimasukkan ke dalam labu ukur 50 mL dan dihimpitkan dengan Na2C2O4 0,01 N hingga tanda batas dan dihomogenkan. Pembuatan Larutan Asam Askorbat 500 ppm
Larutan induk asam askorbat 1000 ppm dipipet sebanyak 12,5 mL lalu dimasukkan ke dalam labu ukur 25 mL. Selanjutnya larutan dihimpitkan dengan Na2C2O4 0,01 N hingga tanda batas dan dihomogenkan.
Pembuatan Larutan Standar Asam Askorbat 20 ppm; 40 ppm; 60 ppm; 80 ppm; dan 100 ppm
Larutan asam askorbat 500 ppm dipipet secara berturut-turut masing-masing sebanyak 0,4 mL; 0,8 mL; 1,2 mL, 1,6 mL, dan 2,0 mL lalu dimasukkan ke dalam labu ukur 10 mL. Kemudian dihimpitkan dengan Na2C2O4 0,01 N hingga tanda batas dan dihomogenkan. Setelah itu, diukur absorbansinya dengan
spektrofotometer UV-Vis pada panjang gelombang maksimum. Kemudian dibuat kurva kalibrasi antara konsentrasi (x) dan absorbansi (y) sehingga diperoleh persamaan garis lurus.
Penentuan Kandungan Vitamin C dengan Spektrofotometer UV-Vis
Sampel daun kelor dari daerah pesisir dan pegunungan dibersihkan dan dihaluskan kemudian diambil yang mewaliki keseluruhan sampel lalu ditimbang sebanyak 1 gram. Selanjutnya masing-masing sampel diekstraksi dengan 4 mL larutan Na2C2O4 0,01 N kemudian
disentrifuge pada 2000 rpm selama 10
menit. Setelah disentrifuge, larutan didekantasi lalu dipisahkan. Proses
sentrifuge diulangi hingga residu sampel
menjadi tidak berwarna. Filtrat sampel yang telah dipisahkan kemudian diukur absorbansinya dengan spektrofotometer UV-Vis pada panjang gelombang maksimum.
Prosedur Uji Aktivitas Antioksidan dengan Metode DPPH (Molyneux, 2004) Pembuatan Larutan DPPH
Sebanyak 1,97 mg DPPH dilarutkan dengan metanol p.a dalam labu ukur sampai 100 mL sehingga diperoleh larutan dengan konsentrasi 0,05 mM. Penentuan Panjang Gelombang Maksimum (λmaks) DPPH
Sebanyak 4 mL larutan DPPH 0,05 mM dan ditambahkan dengan 1 mL methanol p.a. Setelah dibiarkan selama 30 menit ditempat gelap, serapan larutan diukur dengan spektrofotometer UV pada panjang gelombang 400-600 nm.
Pembuatan Larutan Pembanding (Vitamin C dan BHT)
Vitamin C dan BHT masing-masing ditimbang sebanyak 10 mg dalam gelas kimia yang berbeda dan dilarutkan dalam 10 mL metanol p.a sehingga diperoleh masing-masing konsentrasi 1000 ppm sebagai larutan induk. Kemudian
larutan induk dipipet sebanyak 1 mL lalu diencerkan dengan metanol p.a dalam labu ukur 10 mL. Dari 100 ppm dibuat seri konsentrasi 1, 2, 3, 4, dan 5 ppm dengan memipet berturut-turut 50, 100, 150, 200,
dan 250 μL. Larutan DPPH ditambahkan
sebanyak 4 mL dan dicukupkan volumenya hingga 5 mL dengan metanol p.a.
Pengujian Aktivitas Antioksidan
Larutan induk dari ekstrak asam askorbat daun kelor yang telah diketahui konsentrasinya dibuat dalam seri konsentrasi 1, 2, 3, 4, dan 5 ppm dengan memipet larutan induk berturut-turut
dengan volume tertentu, kemudian ditambahkan larutan DPPH sebanyak 4 mL, dan dicukupkan volumenya hingga 5 mL dengan metanol p.a, dan sebagai pembanding digunakan vitamin C dan BHT dengan seri konsentrasi 1, 2, 3, 4, dan 5 ppm. Campuran tersebut dikocok menggunakan vortex dan dibiarkan selama 30 menit pada suhu kamar (37 oC) dan pada ruangan yang terlindungi dari cahaya matahari. Absorbansi (A) diukur pada panjang gelombang 515 nm menggunakan spektrofotometer UV. Persentase pengikat radikal bebas dihitung menggunakan rumus:
% inhibisi =absorbansi blanko-absorbansi sampel
absorbansi blanko X 100 %
HASIL DAN PEMBAHASAN
Hasil Analaisis Kadar Asam Askorbat Tabel 1. Kadar Asam Askorbat dalam
Daun Kelor
Jenis Daun Kadar Asam Askorbat (mg/100 g)
DKMP 361,71
DKTP 363,49
DKMG 308,66
DKTG 312,05
DKMP = Daun Kelor Muda Pesisir; DKTP = Daun Kelor Tua Pesisir;
DKMG = Daun Kelor Muda Pegunungan; DKTG = Daun Kelor Tua Pegunungan
Tabel 1 menunjukkan kadar asam askorbat daun kelor daerah pesisir lebih tinggi daripada di daerah pegunungan. Hasil tersebut sedikit berbeda dengan pendapat Karamoy (2009) yang menyatakan bahwa pengaruh ketinggian tempat berkaitan dengan proses metabolisme tanaman, seperti proses biokimia dan sintesis senyawa metabolit sekunder. Hal tersebut akan mempengaruhi pertumbuhan, karakter morfologi, maupun kandungan senyawa aktif pada suatu tanaman. Semakin tinggi ketinggian
tempatnya, maka semakin tinggi pula stress lingkungan, misalnya suhu semakin rendah, kelembaban semakin tinggi, intensitas cahaya matahari semakin kecil, lama penyinaran semakin singkat. Stres suhu, cahaya, kelembaban, dan lain-lain dapat mempengaruhi produksi metabolit sekunder tanaman. Ketika tanaman mengalami stress, maka produksi metabolit sekunder termasuk produksi vitamin C mengalami peningkatan (Fatchurrozak, dkk., 2013).
Semakin rendah ketinggian tempat, intensitas sinar matahari dan temperatur semakin tinggi, maka vitamin C semakin mudah teroksidasi menjadi asam dehidroaskorbat yang masih mempunyai keaktifan sebagai vitamin C. Dimana asam dehidroaskorbat ini merupakan senyawa yang sangat tidak stabil dan dapat mengalami perubahan lebih lanjut manjadi asam diketogulonat yang tidak lagi memiliki aktivitas sebagai vitamin C (Widodo, 2006), sehingga kadar vitamin C di daerah pesisir (Kab. Barru) seharusnya lebih rendah dibanding daerah pegunungan (Kab. Soppeng), Namun, pada dasarnya setiap tanaman memiliki suhu optimum untuk berlangsungnya metabolisme. Begitu juga tanaman kelor (Moringa oleifera
Lam.) memiliki suhu optimum untuk metabolismenya, termasuk metabolisme vitamin C (Fatchurrozak, dkk., 2013). Dari data penelitian dapat disebutkan bahwa suhu optimum tanaman kelor untuk berlangsungnya metabolisme vitamin C adalah suhu pada daerah pesisir Kabupaten Barru.
Kandungan asam askorbat pada daun tua lebih tinggi dibandingkan dengan daun muda. Hal ini dikarenakan daun muda aktif secara fisiologi daripada daun tua. Daun muda memerlukan lebih banyak vitamin C dan tidak dapat mengumpulkan cukup vitamin C untuk memenuhi proses fisiologinya. Sebaliknya, daun tua memiliki kemampuan yang tinggi untuk mensintesis vitamin C tetapi pemanfaatannya lebih rendah. Perbedaan tersebut disebabkan oleh translokasi asam askorbat dari sumber produksi untuk daun
muda yang membutuhkan lebih banyak vitamin. Nutrisi selalu disimpan dalam daun tua dan kemudian ditransfer ke daun muda untuk pertumbuhan dan perkembangannya. Daun muda tidak memiliki bentuk organ untuk penyimpanan nutrisi. Akibatnya, translokasi nutrisi lebih banyak pada daun muda dari pada daun tua. Pada daun tua, vitamin C ada dalam bentuk aktif tetapi diubah menjadi tidak aktif asam dihidroaskorbat pada daun muda (Ayua, dkk., 2006). Lee dan Kader (2000) menemukan bahwa asam askorbat oksidase ditemukan pada bagian tanaman yang perkembangannya cepat. Asam askorbat oksidase (AAO) mengoksidasi vitamin C menjadi asam dehidroaskorbat. Ini juga merupakan alasan mengapa vitamin C lebih banyak dalam daun tua
dari pada daun muda.
Hasil Uji Aktivitas Antioksidan dengan Metode DPPH 0.000 5.000 10.000 15.000 20.000 25.000 1 DKMP 2.762 DKTP 1.923 A k ti vi tas A n ti ok si d an (% ) 0.000 5.000 10.000 15.000 20.000 25.000 30.000 35.000 40.000 1 DKMG 4.678 DKTG 2.000 A k ti vi tas A n ti ok si d an (% )
Lam.) memiliki suhu optimum untuk metabolismenya, termasuk metabolisme vitamin C (Fatchurrozak, dkk., 2013). Dari data penelitian dapat disebutkan bahwa suhu optimum tanaman kelor untuk berlangsungnya metabolisme vitamin C adalah suhu pada daerah pesisir Kabupaten Barru.
Kandungan asam askorbat pada daun tua lebih tinggi dibandingkan dengan daun muda. Hal ini dikarenakan daun muda aktif secara fisiologi daripada daun tua. Daun muda memerlukan lebih banyak vitamin C dan tidak dapat mengumpulkan cukup vitamin C untuk memenuhi proses fisiologinya. Sebaliknya, daun tua memiliki kemampuan yang tinggi untuk mensintesis vitamin C tetapi pemanfaatannya lebih rendah. Perbedaan tersebut disebabkan oleh translokasi asam askorbat dari sumber produksi untuk daun
muda yang membutuhkan lebih banyak vitamin. Nutrisi selalu disimpan dalam daun tua dan kemudian ditransfer ke daun muda untuk pertumbuhan dan perkembangannya. Daun muda tidak memiliki bentuk organ untuk penyimpanan nutrisi. Akibatnya, translokasi nutrisi lebih banyak pada daun muda dari pada daun tua. Pada daun tua, vitamin C ada dalam bentuk aktif tetapi diubah menjadi tidak aktif asam dihidroaskorbat pada daun muda (Ayua, dkk., 2006). Lee dan Kader (2000) menemukan bahwa asam askorbat oksidase ditemukan pada bagian tanaman yang perkembangannya cepat. Asam askorbat oksidase (AAO) mengoksidasi vitamin C menjadi asam dehidroaskorbat. Ini juga merupakan alasan mengapa vitamin C lebih banyak dalam daun tua
dari pada daun muda.
Hasil Uji Aktivitas Antioksidan dengan Metode DPPH 2 3 4 2.762 9.116 13.536 17.680 24.862 1.923 4.670 6.593 8.242 9.615 2 3 4 4.678 12.281 20.468 30.994 35.965 2.000 9.375 16.571 23.143 29.714
Lam.) memiliki suhu optimum untuk metabolismenya, termasuk metabolisme vitamin C (Fatchurrozak, dkk., 2013). Dari data penelitian dapat disebutkan bahwa suhu optimum tanaman kelor untuk berlangsungnya metabolisme vitamin C adalah suhu pada daerah pesisir Kabupaten Barru.
Kandungan asam askorbat pada daun tua lebih tinggi dibandingkan dengan daun muda. Hal ini dikarenakan daun muda aktif secara fisiologi daripada daun tua. Daun muda memerlukan lebih banyak vitamin C dan tidak dapat mengumpulkan cukup vitamin C untuk memenuhi proses fisiologinya. Sebaliknya, daun tua memiliki kemampuan yang tinggi untuk mensintesis vitamin C tetapi pemanfaatannya lebih rendah. Perbedaan tersebut disebabkan oleh translokasi asam askorbat dari sumber produksi untuk daun
muda yang membutuhkan lebih banyak vitamin. Nutrisi selalu disimpan dalam daun tua dan kemudian ditransfer ke daun muda untuk pertumbuhan dan perkembangannya. Daun muda tidak memiliki bentuk organ untuk penyimpanan nutrisi. Akibatnya, translokasi nutrisi lebih banyak pada daun muda dari pada daun tua. Pada daun tua, vitamin C ada dalam bentuk aktif tetapi diubah menjadi tidak aktif asam dihidroaskorbat pada daun muda (Ayua, dkk., 2006). Lee dan Kader (2000) menemukan bahwa asam askorbat oksidase ditemukan pada bagian tanaman yang perkembangannya cepat. Asam askorbat oksidase (AAO) mengoksidasi vitamin C menjadi asam dehidroaskorbat. Ini juga merupakan alasan mengapa vitamin C lebih banyak dalam daun tua
dari pada daun muda.
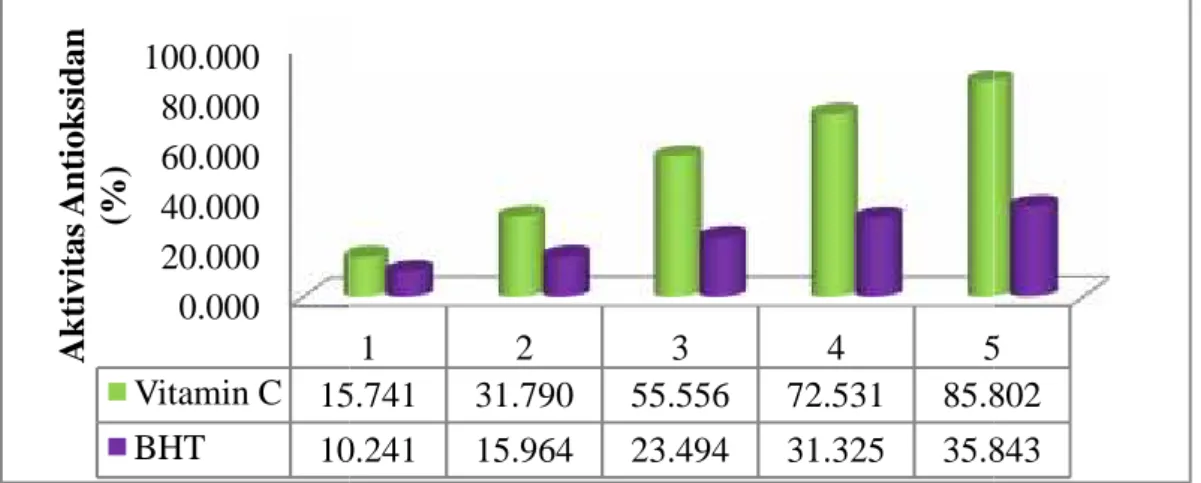
Hasil Uji Aktivitas Antioksidan dengan Metode DPPH 5 24.862 9.615 5 35.965 29.714
Adanya aktivitas antioksidan dari sampel mengakibatkan perubahan warna pada larutan DPPH dalam metanol yang semula berwarna violet pekat menjadi kuning pucat (Permana, dkk., 2003). Semakin tinggi konsentrasi sampel yang mengandung senyawa antioksidan maka warna kuning yang terbentuk akan semakin terang. Perubahan warna DPPH ini terkait dengan energi yang dimiliki radikal bebas. Saat berada dalam keadaan radikal, DPPH cenderung tidak stabil. Hal tersebut ditunjukkan dengan adanya pemudaran warna ungu dari larutan DPPH, karena
dipheniylpicrylhydrazyl (DPPH)
mempunyai satu atom N yang elektronnya
tidak berpasangan dan apabila bereaksi dengan senyawa yang dapat meredam radikal bebas maka akan terjadi pengikatan satu elektron dengan atom yang dapat mendonorkan elektronnya (atom H) membentuk dipheniylpicrylhydrazyne yang stabil (DPPH-H) (Molyneux, 2004).
Uji aktivitas antioksidan menggunakan larutan pembanding (kontrol positif) vitamin C dan BHT (butil hidroxi
toluene) karena kedua senyawa ini
mempunyai kemampuan meredam atau manangkal radikal bebas yang sangat baik dan banyak digunakan oleh peneliti-peneliti sebagai kontrol positif pada uji aktivitas antioksidan.
Parameter yang dugunakan untuk menunjukkan aktivitas antioksidan adalah
Inhibition Concentration (IC50) yaitu konsentrasi suatu zat antioksidan yang dapat menyebabkan 50 % DPPH kehilangan karakter radikal. Jika aktivitas antioksidannya semakin tinggi maka nilai
IC50 akan semakin kecil (Molyneux, 2004). Persen inhibisi ini didapatkan dari perbedaan serapan antara absorbansi DPPH dengan aborbansi sampel yang diukur menggunakan spektrofotometer UV-Vis (Andayani, dkk., 2008).
Tabel 2. Nilai IC50dan Tingkat Kekuatan Antioksidan Sampel Daun Kelor dan Pembanding (Kontrol Positif)
Sampel/
pembanding Nilai IC50 Intensitas
Sampel
DKMP 9,901 μg/mL Sangat Kuat
DKTP 26,109 μg/mL Sangat Kuat
DKMG 6,583 μg/mL Sangat Kuat
DKTG 7,891 μg/mL Sangat Kuat
Pembanding (Kontrol Positif)
Vitamin C 2,87 μg/mL Sangat Kuat
BHT 7,00 μg/mL Sangat Kuat 0.000 20.000 40.000 60.000 80.000 100.000 1 Vitamin C 15.741 BHT 10.241 A k ti vi tas A n ti ok si d an (% )
Adanya aktivitas antioksidan dari sampel mengakibatkan perubahan warna pada larutan DPPH dalam metanol yang semula berwarna violet pekat menjadi kuning pucat (Permana, dkk., 2003). Semakin tinggi konsentrasi sampel yang mengandung senyawa antioksidan maka warna kuning yang terbentuk akan semakin terang. Perubahan warna DPPH ini terkait dengan energi yang dimiliki radikal bebas. Saat berada dalam keadaan radikal, DPPH cenderung tidak stabil. Hal tersebut ditunjukkan dengan adanya pemudaran warna ungu dari larutan DPPH, karena
dipheniylpicrylhydrazyl (DPPH)
mempunyai satu atom N yang elektronnya
tidak berpasangan dan apabila bereaksi dengan senyawa yang dapat meredam radikal bebas maka akan terjadi pengikatan satu elektron dengan atom yang dapat mendonorkan elektronnya (atom H) membentuk dipheniylpicrylhydrazyne yang stabil (DPPH-H) (Molyneux, 2004).
Uji aktivitas antioksidan menggunakan larutan pembanding (kontrol positif) vitamin C dan BHT (butil hidroxi
toluene) karena kedua senyawa ini
mempunyai kemampuan meredam atau manangkal radikal bebas yang sangat baik dan banyak digunakan oleh peneliti-peneliti sebagai kontrol positif pada uji aktivitas antioksidan.
Parameter yang dugunakan untuk menunjukkan aktivitas antioksidan adalah
Inhibition Concentration (IC50) yaitu konsentrasi suatu zat antioksidan yang dapat menyebabkan 50 % DPPH kehilangan karakter radikal. Jika aktivitas antioksidannya semakin tinggi maka nilai
IC50 akan semakin kecil (Molyneux, 2004). Persen inhibisi ini didapatkan dari perbedaan serapan antara absorbansi DPPH dengan aborbansi sampel yang diukur menggunakan spektrofotometer UV-Vis (Andayani, dkk., 2008).
Tabel 2. Nilai IC50dan Tingkat Kekuatan Antioksidan Sampel Daun Kelor dan Pembanding (Kontrol Positif)
Sampel/
pembanding Nilai IC50 Intensitas
Sampel
DKMP 9,901 μg/mL Sangat Kuat
DKTP 26,109 μg/mL Sangat Kuat
DKMG 6,583 μg/mL Sangat Kuat
DKTG 7,891 μg/mL Sangat Kuat
Pembanding (Kontrol Positif)
Vitamin C 2,87 μg/mL Sangat Kuat
BHT 7,00 μg/mL Sangat Kuat
1 2 3 4 5
15.741 31.790 55.556 72.531 85.802 10.241 15.964 23.494 31.325 35.843 Adanya aktivitas antioksidan dari sampel
mengakibatkan perubahan warna pada larutan DPPH dalam metanol yang semula berwarna violet pekat menjadi kuning pucat (Permana, dkk., 2003). Semakin tinggi konsentrasi sampel yang mengandung senyawa antioksidan maka warna kuning yang terbentuk akan semakin terang. Perubahan warna DPPH ini terkait dengan energi yang dimiliki radikal bebas. Saat berada dalam keadaan radikal, DPPH cenderung tidak stabil. Hal tersebut ditunjukkan dengan adanya pemudaran warna ungu dari larutan DPPH, karena
dipheniylpicrylhydrazyl (DPPH)
mempunyai satu atom N yang elektronnya
tidak berpasangan dan apabila bereaksi dengan senyawa yang dapat meredam radikal bebas maka akan terjadi pengikatan satu elektron dengan atom yang dapat mendonorkan elektronnya (atom H) membentuk dipheniylpicrylhydrazyne yang stabil (DPPH-H) (Molyneux, 2004).
Uji aktivitas antioksidan menggunakan larutan pembanding (kontrol positif) vitamin C dan BHT (butil hidroxi
toluene) karena kedua senyawa ini
mempunyai kemampuan meredam atau manangkal radikal bebas yang sangat baik dan banyak digunakan oleh peneliti-peneliti sebagai kontrol positif pada uji aktivitas antioksidan.
Parameter yang dugunakan untuk menunjukkan aktivitas antioksidan adalah
Inhibition Concentration (IC50) yaitu konsentrasi suatu zat antioksidan yang dapat menyebabkan 50 % DPPH kehilangan karakter radikal. Jika aktivitas antioksidannya semakin tinggi maka nilai
IC50 akan semakin kecil (Molyneux, 2004). Persen inhibisi ini didapatkan dari perbedaan serapan antara absorbansi DPPH dengan aborbansi sampel yang diukur menggunakan spektrofotometer UV-Vis (Andayani, dkk., 2008).
Tabel 2. Nilai IC50dan Tingkat Kekuatan Antioksidan Sampel Daun Kelor dan Pembanding (Kontrol Positif)
Sampel/
pembanding Nilai IC50 Intensitas
Sampel
DKMP 9,901 μg/mL Sangat Kuat
DKTP 26,109 μg/mL Sangat Kuat
DKMG 6,583 μg/mL Sangat Kuat
DKTG 7,891 μg/mL Sangat Kuat
Pembanding (Kontrol Positif)
Vitamin C 2,87 μg/mL Sangat Kuat
BHT 7,00 μg/mL Sangat Kuat
5 85.802 35.843
Tabel 2 menunjukkan bahwa ekstrak daun kelor muda mempunyai daya peredam radikal bebas yang lebih besar dibanding ekstrak daun kelor tua. Hal ini terjadi karena kandungan metabolit sekunder pada daun dapat berbeda-beda karena perbedaan umur dan bagian tanaman (Achakzai, dkk., 2009). Daun muda umumnya memiliki kandungan metabolit sekunder dan enzim yang tinggi karena diperlukan dalam proses pertumbuhan, perkembangan, dan pembelahan sel-sel daun tersebut. Pada perkembangannya konsentrasi metabolit sekunder tanaman akan berangsur menurun seiring penurunan aktivitas perkembangan daun tersebut (Prayitno dan Nuryandani, 2011).
Ekstrak daun kelor daerah pesisir memiliki nilai IC50 lebih tinggi dibandingkan daun kelor daerah pegunungan, artinya daun kelor daerah pegunungan memiliki aktivitas antioksidan lebih tinggi dibandingkan daerah pesisir. Hal ini karena semakin bertambah ketinggian tempat maka kandungan antioksidannya semakin tinggi. Hasil tersebut sesuai dengan pendapat yang menyatakan bahwa pengaruh ketinggian tempat, berkaitan dengan proses metabolisme tanaman (Karamoy, 2009), seperti proses biokimia dan sintesis senyawa metabolit sekunder. Hal tersebut akan mempengaruhi pertumbuhan, karakter morfologi, maupun kandungan senyawa aktif pada suatu tanaman.
KESIMPULAN
1. Kadar asam askorbat (vitamin C) dalam 100 gram daun kelor muda pesisir adalah 361,71 mg, daun kelor tua pesisir adalah 363,49 mg, daun kelor muda pegunungan adalah 308,66 mg, dan daun kelor tua pegunungan adalah 312,05 mg.
2. Ekstrak daun kelor (Moringa oleifera Lam.) daerah pesisir dan pegunungan menunjukkan adanya aktivitas antiosidan yang tinggi dengan nilai IC50 dari ekstrak daun kelor muda pesisir adalah 9,901 μg/mL, daun
kelor tua pesisir adalah 26,109 μg/mL,
daun kelor muda pegunungan adalah
6,583 μg/mL, dan daun kelor tua pegunungan adalah 7,891 μg/mL,
sehingga digolongkan sebagai antioksidan sangat kuat. Sebagai kontrol positif vitamin C dengan nilai IC502,87 μg/mL, dan BHT adalah 7,00
μg/mL.
DAFTAR PUSTAKA
Andayani, R., Maimunah, dan Lisawati, Y., 2008, Penentuan Aktivitas Antioksidan, Kadar Fenolat Total dan Likopen pada Buah Tomat (Solanum lycopersicum L), Jurnal
Sains dan Teknologi Farmasi, 13(1).
Aslam, M., Anwar, F., Nadeem, R., Rashid, U., Kazi, T. G., dan Nadeem, M., 2005, Mineral compositiom of
Moringa oleifera Leaves and pods
from different region of Punjab, Pakistan, Asian Journal of Plant
Sciences, 4(4): 417-421.
Ayua, E., Mugalavai, V., Simon, J., Weller, S., Obura, P., dan Nyabinda, N., 2016, Ascorbic Acid Content In Lea Ves of Nightshade (Solanums
Sp.) and Spider Plant (Cleome
gynandra) Varieties Grown Under
Different Fertilizer Regimes In Western Kenya, African Journal of
Biotechnology, 15(7): 199-206.
Citrakusumasari, 2012, Anemia Gizi,
Masalah dan Pencegahannya,
Kalika, Yogyakarta.
Fatchurrozak, Suranto, dan Sugiyarto, 2011, Pengaruh Ketinggian Tempat Terhadap Kandungan Vitamin C Dan Zat Antioksidan Pada Buah Carica Pubescens Di Dataran Tinggi Dieng, Jurnal Pasca UNS, 1(1): 24-31. Karamoy, L, 2009, Hubungan Antara Iklim
dengan pertumbuhan Kedelai (Glicine max L. Merrill), Soil Environment, 7(1): 65-68.
Krisnadi, A. D., 2015, Kelor Super Nutrisi, Pusat Informasi dan Pengembangan Tanaman Kelor Indonesia, e-Book
(online), (http://www.kelorina.com, diakses tanggal 11 September 2015). Lee, S. K., dan Kader, A. A., 2000,
Preharvest and postharvest factors influencing vitamin C content of horticultural crops, Postharvest Biology and Technology, 20: 207–
220.
Linder, M. C., 1992, Biokimia Nutrisi dan
Metabolisme, Diterjemahkan oleh
Aminuddin Parakkasi, 1992, UI-PRESS, Jakarta.
Molyneux, P., 2004, The use of the stable free radikal diphenyl picrylhydrazyl (DPPH) for estimating antioxidant activit, Journal Science of Technology 26(2): 211-219.
Selimovic, A., Saikic, M., dan Selimovic, A., 2011, Direct Spectrophotometric Determination of L-Ascorbic Acid in Pharmaceutical Preparation Using Sodium Oxalate As Stabilizer,
IJBAS, 11(2): 125-131.
Unuigbe, C. A., Okeri, H. A., Erharuyi, O., Oghenero, E. E., dan Obamedo, D. A., 2014, Phytochemical And Antioxidant Evaluation Of Moringa
Oleifera (Moringaceae) Leaf And
Seed, Journal Of Pharmacy And
Bioresources, 11(2): 51-57.
Permana, D., Lajis, N., Abas, F., A. othman, G., Ahmad, R., Kitajama, M., Takayama, H., Aimi, N., dan Cl, 2003, Antioxidative Constituents Of Hedotis Diffusa Wild, Natural Product Sciences, 9(1): 7-9.
Prayitno, E., dan Nuryandani, E., 2011, Optimalisasi Ekstraksi DNA Jarak Pagar (Jatropha curcas) Melalui Pemilihan Daun yang Sesuai,
Nusantara Bioscience, 3: 1-6.
Widodo, W., 2006, Dasar Ilmu Nutrisi, (online), (http:// wahyu widodo.staff. umm.ac.id/files/2010/01/DASAR_IL MU_NUTRISI.pdf, diakses tanggal 22 Oktober 2015).
Winarsi, H., 2007, Antioksidan Alami dan Radikal Bebas, Kanisius, Yogyakarta.
Zarianis, 2006, Efek Suplementasi
Besi-Vitamin C dan Besi-Vitamin C Terhadap Kadar Hemoglobin Anak Sekolah Dasar yang Anemia Di Kecamatan Sayung Kabupaten Demak, Tesis,