SENATEK 2015| Malang, 17 Januari 2015 851
Studi Inhibitor Korosi Berbahan Dasar Imidazoline Dengan
Menggunakan Metode Model Adsorpsi
Andi Rustandi1, Johny Wahyuadi Soedarsono2, Mayang Centya Febriary3, M.
Akbar Barrinaya4
1, 2, 3, 4 Teknik Metalurgi dan Material, Fakultas Teknik,
Universitas Indonesia, Depok 16424, Indonesia.
e-mail: [email protected] ,[email protected], [email protected] Telp. 085718340407, 081314527646
ABSTRAK
Mekanisme inhibisi korosi dari inhibitor berbahan dasar imidazoline pada baja API 5L Grade B di lingkungan NaCl 3,5% diinvestigasi dengan menggunakan metode model adsorpsi yang didapat dari hasil pengujian Tafel Polarisasi, Linier Polarisasi dan Electrochemical Impedance Spectroscopy (EIS) dengan menggunakan variasi konsentrasi 0 ppm, 50 ppm, 100 ppm, 150 ppm, 200 ppm dan 250 ppm. Senyawa imidazoline yang teradsorpsi pada permukaan logam diinvestigasi dengan menggunakan pengujian Fourier Transform InfraRed (FTIR). Hasilnya didapatkan bahwa proses adsorpsi inhibitor imidazoline terjadi secara spontan
mengikuti mode adsorpsi Langmuir isoterm. Berdasarkan nilai Goads antara -16,2 kJ/mol
sampai -17,5 kJ/mol menunjukkan bahwa inhibitor imidazoline menginhibisi korosi dengan cara adsorpsi fisika (interaksi elektrostatis antara muatan negatif molekul inhibitor dengan muatan positif permukaan logam) membentuk lapisan tunggal di permukaan logam sehingga dapat menghambat proses korosi. Besarnya efisiensi inhibisi inhibitor berbahan dasar imidazoline bergantung pada konsentrasi inhibitor. Efisiensi inhibisi tertinggi diperoleh pada konsentrasi imidazoline 250 ppm sebesar 72,69% berdasarkan hasil pengujian Linier polarisasi.
Kata kunci : inhibitor korosi; model adsorpsi; senyawa imidazoline Pendahuluan
Pipa sebagai salah satu peralatan produksi yang berfungsi untuk mengalirkan fluida merupakan komponen yang sangat rentan terhadap korosi internal pada sektor industri produksi minyak dan gas. Kandungan fluida yang mengalir di dalam pipa terdapat campuran
minyak, air laut, dan gas alam seperti CO2 dan H2S yang bersifat korosif. Sehingga diperlukan
suatu metode pengendalian laju korosi internal pipa, inhibitor korosi merupakan salah satu metode perlindungan korosi internal pada pipa. Inhibitor organik lebih banyak digunakan dibandingkan inhibitor anorganik karena inhibitor organik bersifat non-toksik, murah, sudah tersedia di alam, mudah diperbaharui dan tidak merusak lingkungan.
Inhibitor organik nitrogen-based seperti imidazoline banyak digunakan sebagai inhibitor
korosi di industri minyak. Pada penelitian ini akan membahas mekanisme inhibisi korosi dan perilaku adsorpsi dari inhibitor berbahan dasar imidazoline pada baja karbon API 5L Grade B di lingkungan NaCl 3,5%. Tujuan dari penelitian ini adalah untuk mengetahui efisiensi inhibisi dari imidazoline dalam lingkungan netral, mencari konsentrasi optimum dari imidazoline dalam proses inhibisi korosi, mengetahui mekanisme inhibisi korosi dari imidazoline pada permukaan logam dan mengetahui jenis adsorpsi isoterm dari imidazoline.
Komposisi sampel uji baja API 5L Grade B diuji dengan Optical Emission Spectroscopy
(OES). Mekanisme inhibisi dari senyawa yang terkandung dalam imidazoline diinvestigasi dengan menggunakan model adsorpsi isoterm dari hasil pengujian linier polarisasi, tafel
polarisasi dan EIS (Electrochemical Impedance Spectroscopy). Efisiensi inhibisi juga dapat
ditentukan dari ketiga pengujian tersebut. Gugus fungsi yang imidazoline serta gugus fungsi
yang teradsorpsi pada permukaan logam diinvestigasi dengan menggunakan FTIR (Fourier
SENATEK 2015| Malang, 17 Januari 2015 852
digunakan antara lain 0 ppm, 50 ppm, 100 ppm, 150 ppm dan 250 ppm yang ditambahkan ke dalam larutan NaCl 3,5%.
Tinjauan Teoritis
Inhibitor korosi merupakan senyawa kimia yang ditambahkan dalam konsentrasi rendah ke lingkungan untuk menurunkan laju dari korosi logam. Inhibitor yang paling umum digunakan pada industri minyak dan gas adalah inhibitor organik umumnya mengandung gugus polar, yang memiliki atom N, S dan O, serta senyawa heterosiklik dengan gugus polar atau ikatan ganda terkonjugasi. Salah satu jenis inhibitor organik yang banyak digunakan adalah imidazoline. Imidazoline merupakan senyawa organik yang memiliki dua atom nitrogen yang terikat dalam suatu cincin lima. Gugus utama berfungsi untuk membentuk ikatan molekul yang kuat ke
permukaan logam dan menghasilkan lapisan, rantai pendant berfungsi untuk meningkatkan
adsorpsi molekul ke permukaan logam sementara rantai hidrokarbon berfungsi untuk menyelimuti permukaan logam sehingga bersifat hidrofobik.
Adsorpsi merupakan proses yang terjadi ketika gas atau liquid terlarut terakumulasi pada
permukaan padatan atau liquid (adsorbent), membentuk lapisan molekul atau atomik
(adsorbate). Adsorpsi terbagi menjadi dua jenis, yaitu adsorpsi fisika dan adsorpsi kimia.
Adsorpsi fisika terjadi akibat adanya gaya elektrostatik antara muatan ion atau dipol pada
molekul inhibitor dan muatan listrik logam pada interface logam/elektrolit. Proses adsorpsi fisika
berlangsung cepat namun memiliki ikatan yang lemah pada permukaan logam serta peningkatan temperatur menyebabkan kinerja inhibitor menurun. Adsorpsi kimia terjadi karena adanya pemakaian bersama muatan atau transfer muatan dari molekul inhibitor ke permukaan logam untuk membentukan ikatan koordinat. Adsorpsi kimia memiliki ikatan adsorpsi yang kuat. Peningkatan temperatur menyebabkan kinerja inhibitor semakin baik.
Pada temperatur tertentu, hubungan antara jumlah dari spesies atau molekul yang teradsorpsi pada permukaan logam disebut sebagai adsorpsi isoterm. Kekuatan dari adsorpsi diketahui dari jenis adsorpsi isoterm yang menunjukkan hubungan kesetimbangan antara konsentrasi inhibitor di permukaan dan dalam larutan ruah. Terdapat beberapa jenis mode adsorpsi isoterm yang mengindikasi mekanisme adsorpsi inhibitor seperti yang terlihat pada Tabel 1.
Tabel 1. Adsorpsi Isoterm
Adsorpsi isoterm sangat tergantung dari besarnya surface coverage () dari inhibitor. Surface
coverage merupakan fraksi dari jumlah daerah (site) yang ditempati molekul teradsorpsi
terhadap jumlah daerah yang tersedia. Perhitungan dari surface coverage dapat dilakukan
dengan beberapa metode pengujian, antara lain:
a. Tafel polarisasi
(i)
b. Linier polarisasi
SENATEK 2015| Malang, 17 Januari 2015 853
c. EIS (Electrochemical Impedance Spectroscopy)
(iii)
Untuk menentukan jenis adsorpsi isoterm, dilakukan plot grafik dari surface coverage dan
konsentrasi inhibitor yang digunakan sesuai dengan verification plot. Jenis adsorpsi isoterm
yang paling sesuai dapat dilihat dari nilai koefisien korelasi/regresi linier ( R2) yang paling besar.
Dari nilai surface coverage yang didapat dari persamaan (i) sampai (iii), selanjutnya dapat
diolah untuk mendapatkan nilai efisiensi inhibisi dari inhibitor dengan menggunakan persamaan (iv).
(iv) Mode adsorpsi Langmuir isoterm mengasumsikan bahwa proses adsorpsi dari molekul
organik pada permukaan logam merupakan lapisan tunggal (monolayer) dan molekul yang
teradsorpsi hanya menempati satu daerah (site) serta tidak adanya interaksi antara molekul
teradsorpsi lainnya. Hubungan antara surface coverage (θ) dengan konsentrasi dari molekul
inhibitor (C) dinyatakan dengan persamaan (v) atau (vi).
(v)
(vi)
dimana K adalah konstanta kesetimbangan adsorpsi, C adalah konsentrasi adsorbat dan θ
adalah surface coverage
Dari persamaan linier tersebut, dapat dibuat grafik dengan C/θ sebagai sumbu-x dan C sebagai sumbu-y. Nilai K dapat ditentukan dari kebalikan titik potong sumbu-y. Nilai K pada proses adsorpsi mengindikasikan daya ikat dari inhibitor ke permukaan logam dan berhubungan
dengan energi bebas dari adsorpsi (Goads) seperti pada persamaan berikut:
(vii)
Nilai 55,5 merupakan konsentrasi molar dari air dalam larutan dengan satuan (mol L-1).
Nilai Goads yang negatif bersama dengan nilai K yang besar mengindikasi proses adsorpsi yang
spontan dan kestabilan kimia yang baik dari senyawa inhibitor yang didapatkan dari ikatan kimia antara logam dan molekul inhibitor.
Proses adsorpsi akan menurunkan energi permukaan dari suatu material. Penurunan energi bebas permukaan yang dihasilkan merupakan energi bebas adsorpsi. Dari persamaan (vi) dapat
dihitung besarnya nilai Goads yang selanjutnya dapat menentukan tipe adsorpsi dari inhibitor.
Nilai Goads inhibitor yang kurang dari – 40 kJ mol-1 menunjukkan inhibitor termasuk dalam
jenis adsorpsi kimia, sementara jika nilai Gads inhibitor lebih dari – 20 kJ mol-1 maka inhibitor
termasuk dalam jenis adsorpsi fisika.
Metode Penelitian
Pada penelitian ini, peralatan yang digunakan antara lain gerinda, timbangan digital,
beaker glass, cawan petri, magnetic stirer, kabel, solder, pipet volumetrik, elektroda standar Ag/AgCl, instrumen potensiostat Autolab PGSTAT302N untuk pengujian elektrokimia, instrumen Perkin Elmer 1430 untuk FTIR dan instrumen Foundry-Master untuk OES. Sementara itu, bahan yang digunakan antara lain garam NaCl padat, epoxy resin, hardener, air distilasi, sampel baja karbon API 5L grade B (dimensi 1cm x 1cm x 3mm) dan inhibitor imidazoline merk CORTON SRN 4694. Baja API 5L Grade B dihubungkan dengan kawat Cu lalu di-mounting dengan epoxy resin. Sampel baja diamplas dengan kertas amplas grit 1200. Uji
komposisi kimia dari baja API 5L Grade B dilakukan menggunakan Optical Emission
SENATEK 2015| Malang, 17 Januari 2015 854
dengan konsentrasi imidazoline 0,02 ml (20ppm); 0,05 ml (50ppm); 0,1 ml (100ppm); 0,15 ml (150ppm); 0,2 ml (200ppm) dan 0,25 ml (250ppm) .
Pengujian elektrokimia dilakukan menggunakan instrumen potensiostat Autolab PGSTAT302N yang dilengkapi dengan software Nova 1.8, Tafel Polarisasi untuk mendapatkan
nilai icorr (ASTM G3), Linier Polarisasi untuk mendapatkan nilai Rp (ASTM G3) dan EIS untuk
mendapatkan nilai Rct (ASTM G106). Elektroda yang digunakan yaitu grafit sebagai counter
electrode, elektroda standar Ag/AgCl sebagai reference electrode dan sampel API 5L Grade B
sebagai working electrode dengan lama waktu pengondisian 30menit. Pengujian Tafel Polarisasi
dilakukan dengan scanning rate 5 mVs-1, dalam rentang potensial -300 mV hingga +300 mV dari
nilai Open Circuit Potential (OCP). Pengujian Linier Polarisasi dilakukan dalam prosedur liniear
sweep voltammetry potentiostatic dengan scanning rate 0,125 mVs-1 dalam rentang potensial -10
mV hingga +10 mV dari nilai Open Circuit Potential (OCP). Pengujian EIS dilakukan
menggunakan sinyal AC dengan amplitudo gelombang sinusoidal 10 mV dan rentang frekuensi 10 kHz - 10 mHz.). Nilai-nilai icorr dari hasil pengujian Tafel Polarisasi, nilai Rp dari hasil
pengujian Linier Polarisasi dan nilai Rct dari hasil pengujian EIS kemudian diolah berdasarkan
persamaan (i) sampai (iii) untuk mengetahui tipe adsorpsi isoterm dari imidazoline.
Untuk uji kandungan senyawa aktif dari imidazoline dilakukan dengan pengujian FTIR menggunakan spektometer dengan daerah spektrum pada interval panjang gelombang 4000
hingga 450 cm-1.
Hasil dan Pembahasan Material Uji
Komposisi kimia dari sampel baja API 5L Grade B dapat dilihat pada Tabel 2. Baja karbon
API 5L Grade B merupakan jenis baja karbon rendah yang digunakan sebagai material pipeline.
Spesifikasi dari baja ini terdapat pada Standar API 5L Specification for Line Pipe.
Tabel 2. Komposisi kimia baja API 5L Grade B
C (%) Si (%) S (%) P (%) Mn (%) Cr (%) Mo (%)
0,148 0,198 0,004 0,012 0,425 0,010 0,008
Ni (%) Ti (%) Cu (%) Nb (%) V (%) Al (%) Fe (%)
<0,005** <0,002** 0,007 <0,002** <0,002** 0,002 Balance
** (<) rnenunjukkan nilai berada di bawah batas kuantifikasi alat uji.
Imidazoline
Hasil pengujian FTIR untuk mengetahui gugus fungsi yang terkandung dalam inhibitor berbahan dasar imidazoline dapat dilihat pada Gambar 1A.
Gambar 1. Grafik hasil pengujian FTIR. (A) Hasil pengujian FTIR inhibitor imidazoline (B) Hasil pengujian lapisan inhibitor pada sampel.
Grafik di atas menunjukkan beberapa peak inhibitor dengan panjang gelombang antara lain
3307 cm-1 untuk ikatan N-H (NH2) stretch dari 1o, 2oamines, 1636 cm-1 untuk ikatan C=N stretch
dari imidazoline ring, 1333 cm-1 untuk ikatan C-N-C stretch dari imidazoline ring dan 1182 cm-1
untuk ikatan C-N stretch dari aliphatic amines.
Pengujian FTIR juga digunakan untuk mengidentifikasi keberadaan gugus dari imidazoline yang teradsorpsi pada permukaan logam seperti yang terlihat pada Gambar 1B. Dari grafik tersebut terlihat ada kemiripan peak antara grafik FTIR imidazoline (warna biru) dan grafik FTIR sampel yang telah direndam larutan uji (warna merah). Terdapat satu peak dengan gugus
SENATEK 2015| Malang, 17 Januari 2015 855
fungsi berbeda yaitu pada panjang gelombang 901 cm-1 untuk ikatan C-H bend dari gugus fungsi
alkil. Kemiripan grafik membuktikan bahwa inhibitor imidazoline teradsorpsi pada permukaan logam untuk membentuk lapisan inhibisi.
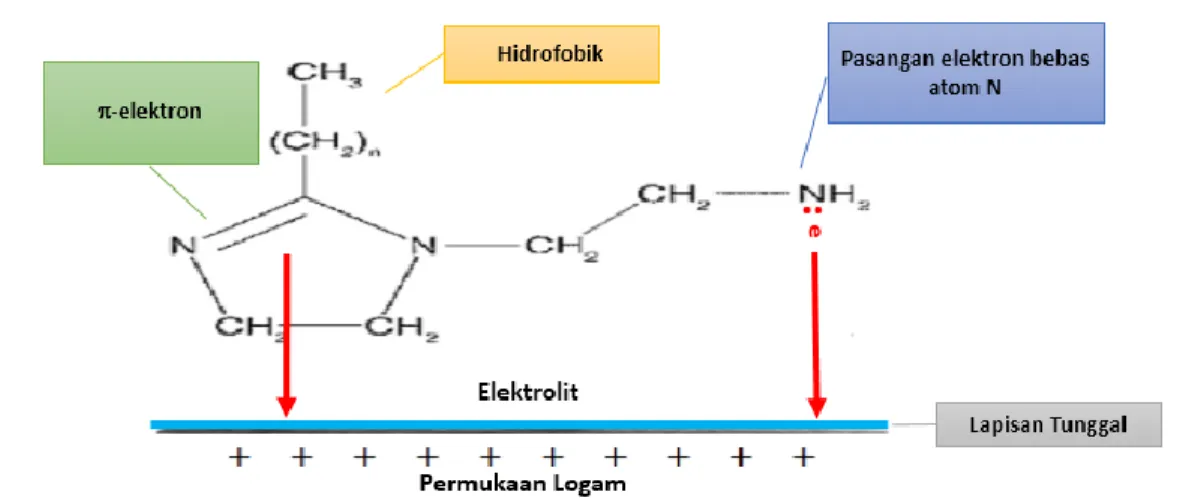
Gambar 2. Gugus dan karakteristik yang terkandung dalam senyawa imidazoline
Ikatan C-H sebagai gugus alkil (rantai cabang) menunjukkan adanya gugus hidrokarbon pada permukaan logam yang menyebabkan inhibitor memiliki kemampuan menolak molekul air (hidrofobik). Adanya ikatan C=N dan C-N-C menunjukkan terdapat gugus utama imidazoline
yaitu cincin imidazoline pada permukaan logam serta ikatan -NH2 menunjukkan terdapat gugus
pendant yang menyebabkan senyawa bersifat hidrofilik (polar). Cincin imidazoline dan ikatan
-NH2 menyebabkan senyawa imidazoline dapat teradsorpsi pada permukaan logam dan
membentuk lapisan inhibisi. Adsorpsi Isoterm
Mode adsorpsi isoterm diketahui dari hasil pengujian tafel polarisasi, linier polarisasi dan
EIS dan diolah untuk mendapatkan nilai surface coverage.
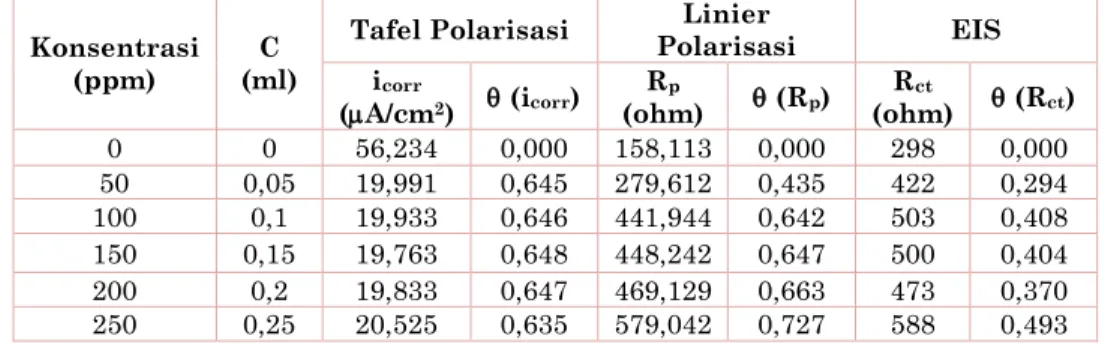
Tabel 3. Surface coverage () terhadap variasi konsentrasi dari pengujian tafel polarisasi, linier polarisasi dan EIS
Konsentrasi (ppm) (ml) C
Tafel Polarisasi Polarisasi Linier EIS icorr (A/cm2) (icorr) Rp (ohm) (Rp) Rct (ohm) (Rct) 0 0 56,234 0,000 158,113 0,000 298 0,000 50 0,05 19,991 0,645 279,612 0,435 422 0,294 100 0,1 19,933 0,646 441,944 0,642 503 0,408 150 0,15 19,763 0,648 448,242 0,647 500 0,404 200 0,2 19,833 0,647 469,129 0,663 473 0,370 250 0,25 20,525 0,635 579,042 0,727 588 0,493
Hubungan antara konsentrasi dan surface coverage yang didapat dari ketiga pengujian
tersebut dimasukkan ke dalam grafik sesuai verification plot dan didapatkan hasil nilai koefisien
korelasi berikut:
Tabel 3. Nilai koefisien korelasi dari lima jenis adsorpsi isoterm
R2 Temkin Frumkin Bockris - Swinkels Langmuir Parson Virial
(icorr) 0,0488 0,4029 0,4029 0,99 0,2955
(Rp) 0,0043 0,8829 0,9011 0,989 0,1704
(Rct) 0,009 0,6652 0,7684 0,94 0,1734
Nilai koefisien relasi paling besar (mendekati 1) didapatkan pada mode adsorpsi Langmuir
isoterm yang mengindikasikan bahwa inhibitor teradsorpsi pada satu site permukaan baja
dengan membentuk lapisan tunggal (monolayer), dan tidak ada interaksi antara molekul
teradsorpsi lainnya. Terbentuknya lapisan tunggal yang menginhibisi logam akan mengontrol proses transfer muatan dan meningkatkan energi aktivasi sistem sehingga proses korosi akan terhambat.
SENATEK 2015| Malang, 17 Januari 2015 856 Gambar 4. Grafik adsorpsi Langmuir isoterm untuk senyawa imidazoline pada baja API 5L Grade B dari
hasil pengujian (a) tafel polarisasi, (b) linier polarisasi dan (c) EIS
Tipe Adsorpsi
Tipe adsorpsi dapat diketahui dari nilai Goads yang dihitung sesuai dengan persamaan
(vii). Temperatur yang digunakan pada penelitian adalah temperatur ruang 25oC (298K).
Hasil perhitungan Goads untuk ketiga pengujian, yaitu tafel polarisasi (icorr), linier polarisasi
(Rp), dan EIS (Rct) dapat dilihat pada Tabel 5.
Tabel 4. Perhitungan nilai Goads dari hasil pengujian tafel polarisasi, linier polarisasi dan EIS Persamaan Kads Goads (kJ/mol)
(icorr) y = 0,0783x + 0,0795 12,57862 -16,202
(Rp) y = 0,0604x + 0,0485 20,61856 -17,426
(Rct) y = 0,1078x + 0,0714 14,0056 -16,468
Nilai Goads yang negatif menunjukkan bahwa proses adsorpsi molekul inhibitor berbahan
dasar imidazoine pada permukaan logam terjadi secara spontan. Nilai Goads dari inhibitor
berbahan dasar imidazoline sekitar -16,2 kJ/mol sampai -17,4 kJ/mol yang menunjukkan bahwa
inhibitor memiliki tipe adsorpsi fisika. Inhibitor teradsorpsi karena ada interaksi elektrostatis
antara muatan ion atau dipol pada molekul inhibitor dan muatan listrik logam pada interface
logam/elektrolit.
Mekanisme Inhibisi Inhibitor
Mekanisme inhibisi dari inhibitor imidazoline pada permukaan logam dapat dilihat secara skematis pada Gambar 5.
SENATEK 2015| Malang, 17 Januari 2015 857 Gambar 5. Skema mekanisme adsorpsi inhibitor imidazoline
Senyawa imidazoline dapat teradsorpsi secara fisika ke permukaan logam disebabkan
adanya ikatan N=C-N pada cincin imidazoline menyebabkan terdapat -elektron, serta atom N
pada gugus –NH2 menyebabkan adanya pasangan elektron bebas. Adanya -elektron dan
elektron bebas atom N menyebabkan senyawa imidazoline memiliki muatan negatif. Sementara
itu, permukaan logam umumnya memiliki muatan positif yang terdapat pada interface
logam/elektrolit.
Adanya perbedaan muatan antara molekul inhibitor dan permukaan logam menyebabkan terjadinya interaksi elektrostatis antara molekul dari senyawa imidazoline dengan permukaan logam sehingga terbentuk ikatan. Ikatan tersebut akan membentuk lapisan tunggal pada satu
daerah aktif dari permukaan logam pada interface logam/elektrolit, sesuai dengan mode adsorpsi
Langmuir isoterm. Adanya gugus fungsi C-H pada permukaan logam mengindikasikan bahwa permukaan logam diselimuti oleh gugus hidrokarbon yang bersifat hidrofobik yang akan mencegah molekul air dari lingkungan untuk berinteraksi dengan permukaan logam sehingga logam akan terinhibisi dari korosi.
Kinerja Inhibitor
Kinerja inhibitor dapat dilihat dari nilai efisiensi inhibisinya yang didapat dari pengujian tafel polarisasi, linier polarisasi dan EIS berikut.
Tabel 5. Efisiensi % () inhibitor terhadap variasi konsentrasi dari pengujian tafel polarisasi, linier polarisasi dan EIS
Konsentrasi (ppm)
Tafel Polarisasi Linier Polarisasi EIS
icorr (A/cm2) % (icorr) Rp (ohm) % (Rp) Rct (ohm) % (Rct)
0 56,234 0,00 158,113 0,00 298 0,00 50 19,991 64,45 279,612 43,45 422 29,38 100 19,933 64,55 441,944 64,22 503 40,76 150 19,763 64,86 448,242 64,73 500 40,40 200 19,833 64,73 469,129 66,30 473 37,00 250 20,525 63,50 579,042 72,69 588 49,32
SENATEK 2015| Malang, 17 Januari 2015 858 Gambar 6. Hubungan efisiensi inhibitor dengan variasi konsentrasi senyawa imidazoline
Berdasarkan Tabel 6 dan Gambar 6, diketahui bahwa efisiensi inhibitor cenderung meningkat seiring dengan penambahan konsentrasi inhibitor terjadinya penurunan efisiensi inhibitor seiring penambahan konsentrasi inhibitor dari hasil pengujian EIS dapat disebabkan oleh faktor ketidakhomogenan permukaan yang terjadi dan terukur pada pengujian EIS.
Inhibitor berbahan dasar imidazoline menginhibisi logam karena adanya molekul dari senyawa imidazoline yang teradsorpsi secara horizontal pada permukaan logam sehingga
meningkatkan nilai surface coverage pada konsentrasi rendah. Molekul teradsorpsi pada satu
daerah di permukaan logam dan membentuk lapisan tunggal pada konsentrasi optimal. Penurunan efisiensi inhibitor setelah melewati konsentrasi optimal dari inhibitor dapat disebabkan karena lapisan adsorpsi rusak dan terjadinya interaksi antara molekul teradsorpsi,
sehingga nilai surface coverage akan menurun.
Kesimpulan
Berdasarkan hasil pengujian dan analisa yang telah dilakukan pada penelitian mengenai inhibitor berbahan dasar imidazoline yang diaplikasikan pada baja API 5L Grade B di lingkungan NaCl 3,5%, maka dapat ditarik beberapa kesimpulan, yaitu:
1. Inhibitor berbahan dasar imidazoline dapat menginhibisi korosi dari baja API 5L Grade B di
lingkungan NaCl 3,5% dengan membentuk lapisan inhibisi.
2. Mekanisme inhibisi dari inhibitor imidazoline pada beberapa variasi konsentrasi mengikuti
mode adsorpsi Langmuir isoterm.
3. Besarnya nilai Goads antara -16,2 kJ/mol sampai -17,5 kJ/mol mengindikasikan bahwa
proses adsorpsi molekul inhibitor terjadi secara fisika (physisorption).
4. Inhibitor teradsorpsi secara fisika ke interface logam/elektrolit dan membentuk lapisan
tunggal pada permukaan logam sehingga dapat menginhibisi korosi.
5. Efisiensi inhibitor imidazoline cenderung meningkat seiring penambahan konsentrasi
inhibitor. Nilai efisiensi inhibitor optimal dari hasil pengujian tafel polarisasi sebesar 64,86% pada konsentrasi 150 ppm, hasil linier polarisasi sebesar 72,69% pada konsentrasi 250 ppm dan hasil EIS sebesar 40,76% pada konsentrasi 100 ppm.
Daftar Pustaka
1. U. Osukogwu and E. Oghenekaro. “Effectiveness in Oilfield Production Operations”.
International Journal of Scientific & Technology Research, Vol.1 (2012).
2. P.A., Schweitzer. 2007. Corrosion of Linings and Coatings Cathodic and Inhibitor Protection
and Corrosion Monitoring. Taylor & Francis Group.
3. Roberge, Pierre. 1999. Handbook of Corrosion Engineering. McGraw-Hill.
4. G. Trabanelli. “Inhibitors – an old remedy for a new challenge”. Corrosion vol. 47, 410 (1991)
5. Fontana, Mars. 1986. Corrosion Engineering. McGraw-Hill International Edition.
6. C.G. Hao dan Z.J.Mao. “Corrosion Inhibition of Imidazoline Derivates with Benzene Rings on
Mild Steel in CO2-Saturated Brine Solution”. Chem. Res. Chinese Universities, 28:4.(2012):
691-695.
7. G. Gusmano, et.al. “Study of the Inhibition Mechanism of Imidazolines by Electrochemical
Impedance Spectroscopy”. Corrosion Science Section, (2006): 576-583.
8. Bockris, J. O. M. and Swinkels, D. A. J. “Adsorption of n-Decylamine on Solid Metal
Electrodes”. J. Electrochem. Soc.,8:111 (1964): 736-743.
9. Znini, M., et al. “Essential Oil of Salvia Aucheri Mesatlantica as a Green Inhibitor for the
SENATEK 2015| Malang, 17 Januari 2015 859
10. O.O. Xometl, et. al., “Surface analysis of inhibitor films formed by imidazolines and amides
on mild steel in an acidic environment”. Applied Surface Science. 252 (2006): 2139-2152.
11. H.Jafari., et.al., “Electrochemical and Theoretical Studies of Adsorption and Corrosion
Inhibition of N,N′-Bis(2-hydroxyethoxyacetophenone)-2,2-dimethyl- 1,2-propanediimine on
Low Carbon Steel (API 5L Grade B) in Acidic Solution”. Ind. Eng. Chem. Res. 52 (2013):
6617-6632.
12. W. Deana, et. al. “The Synthesis of Imidazoline Derivative Compounds as Corrosion Inhibitor
towards Carbon Steel in 1% NaCl Solution”. ITB J. Sci. Vol. 40A (2008) 33-48.
13. A.A. Ismail, et.al. “Some Imidazoline Derivatives as Corrosion Inhibitors”. J Surfact Deterg.
13 (2010): 247–254.
14. Indrafusa, Vicky. ”Studi Pengaruh Senyawa Fenolik Minyak Zaitun sebagai Inhibitor
Ramah Lingkungan pada Baja API 5L Grade B di Lingkungan NaCl 3,5 %”. Teknik