2.1 Tumbuhan Senduduk (Melastoma malabathricum Linn)
Senduduk merupakan salah satu dari 22 spesies yang ditemukan di kawasan Asia Tenggara. Senduduk dianggap sebagai tumbuhan asli Asia tropis, subtropis dan Kepulauan Pasifik. Tumbuhan senduduk ini umumnya ditemukan di semak-semak, persawahan dan lereng gunung. Tumbuhan ini diyakini sebagai obat herbal oleh rakyat Cina, India dan Indonesia. Temuan ilmiah mengungkapkan pemanfaatan senduduk sebagai obat seperti obat luka, diare, wasir, disentri, sakit perut. Adapun bagian yang digunakan adalah daun, tunas, kulit, biji dan akar dari tumbuhan senduduk. Penemuan lain juga mengungkap senduduk dapat digunakan secara farmakologi, seperti antiseptik, antiinflamasi, antitoksik dan antioksidan (Joffry et al, 2012). Tumbuhan senduduk merupakan suku melastomataceae yang umumnya
berupa semak, perdu atau pohon. Daun berhadapan atau berkarang, tunggal, biasanya dengan 3-9 tulang yang melengkung, jarang bertulang menyirip tanpa daun penumpu. M. malabathricum L merupakan tanaman perdu, tinggi
0,5 - 4m, cabang yang muda bersisik. Daun bertangkai, berhadapan, memanjang atau bulat telur memanjang dengan ujung runcing, bertulang daun 3-20 kali 1-8 cm. Kedua belah sisinya berbulu. Bunga mengelompok pada ujung cabang, berwarna ungu muda, berbunga sepanjang tahun. Buah buni, kulit buah warna coklat muda, bulat seperti vas bunga. Daging buah warna ungu, rasanya manis, pada kulit buah terdapat banyak biji, buah yang matang kulitnya pecah. Senduduk berkembang biak dengan biji (Tjitrosoepomo, 2007).
Ciri-ciri dari tumbuhan senduduk yang paling umum dan membedakannya dengan tanaman perdu lainnya adalah bentuk daun yang bulat telur dengan ujung lancip, permukaan yang kasar. Buah berbentuk unik, kecil, bergerombol berwarna ungu seperti anggur. Adapun bentuk dari tumbuhan senduduk yaitu sebagai berikut:
Gambar 2.1 Bentuk tumbuhan senduduk
Nama lain dari senduduk (M. malabathricum L.) adalah Melastoma affine G.Don., Melastoma polyanthum BI. Di Indonesia senduduk dikenal dengan
nama haredong (Sunda), senggani (Jawa), kemanden (Madura) dan senduduk (Sumatera) (Steenis, 2005).
Adapun sistematika tumbuhan senduduk adalah sebagai berikut: Kingdom : Plantae (Tumbuh-tumbuhan)
Divisio : Spermatophyta Kelas : Dicotyledoneae
Ordo : Melastomales
Family : Melastomataceae
Genus : Melastoma
Spesies : Melastoma malabathricum Linn
2.2Manfaat dan Kandungan Senyawa Kimia Daun Senduduk
Beberapa masyarakat memanfaatkan daun senduduk secara tradisional antara lain dengan cara daun dikunyah, ditumbuk, dan dioleskan pada luka
cacar, untuk mengobati disentri dan diare. Daun muda dimakan untuk mengobati diare dan disentri. Pucuk daun dikonsumsi untuk mengobati infeksi, tekanan darah tinggi dan diabetes. Daun juga bisa dijus dan dapat digunakan sebagai obat kumur untuk meredakan sakit gigi. Selain manfaat diatas, daun terkadang digunakan untuk mengobati bisul, tukak lambung, bekas luka, jerawat dan bintik hitam di kulit (Joffry et al, 2012).
2.3 Senyawa Metabolit Sekunder
Menurut Azis Saifudin (2002) Senyawa alami secara umum adalah molekul kimia berupa mineral, metabolit primer dan metabolit sekunder. Secara famili besar metabolit primer dan sekunder adalah senyawa organik.
Bahan alam dibedakan menjadi dua berdasarkan fungsi terhadap makluk hidup yaitu metabolit primer dan metabolit sekunder. Metabolit sekunder adalah senyawa yang disintesis oleh makluk tumbuhan, mikroba atau hewan melewati proses biosintesis yang digunakan untuk menunjang kehidupan namun tidak vital sebagaimana gula, asam amino dan asam lemak. Metabolit
sekunder ini memiliki aktivitas farmakologi dan biologi. Di bidang farmasi secara khusus metabolit sekunder digunakan dan dipelajari sebagai kandidat obat atau senyawa penuntun untuk melakukan optimasi agar diperoleh
senyawa yang lebih paten dengan toksisitas minimal. Metabolit sekunder memiliki ciri-ciri sebagai berikut:
a. Tidak terlibat langsung dalam metabolisme/kehidupan dasar: pertumbuhan, perkembangan dan reproduksi.
b. Tidak esensial, ketiadaan jangka pendek tidak berakibat kematian, ketiadaan jangka panjang mengakibatkan kelemahan dalam pertahanan diri, survival, estetika, menarik serangga.
c. Golongan metabolit sekunder distribusi hanya pada spesies pada filogenetik/ familia tertentu.
d. Seringkali berperan di dalam pertahanan terhadap musuh.
f. Pengolongan utama: terpenoid, fenil propanoid, poliketida, flavonoid dan alkaloid adalah metabolit sekunder.
g. Pemanfaatan oleh manusia untuk obat, parfum, aroma, bumbu dan relaksasi.
Menurut Simanjuntak (2009) ekstrak daun senduduk memiliki beberapa kandungan senyawa kimia flavonoid, tanin, saponin, glikosida dan steroid/triterpenoid.
2.3.1 Flavonoid
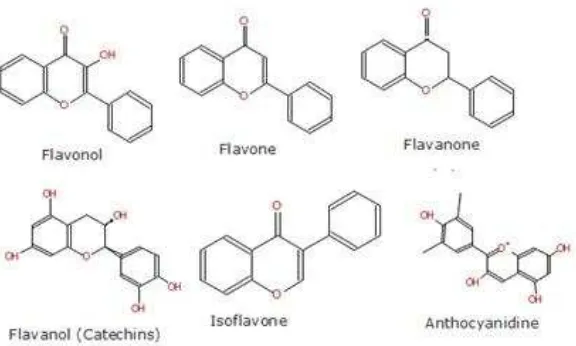
Flavonoid adalah sekelompok besar senyawa polifenol tanaman yang tersebar luas dalam berbagai bahan makanan. Flavonoid merupakan kandungan khas tumbuhan hijau. Flavonoid terdapat pada semua tumbuhan hijau termasuk daun, akar, kulit kayu, bunga, buah dan biji. Flavonoid mengandung 15 atom karbon dalam inti dasarnya, yang tersusun dari dua cincin aromatis yang dihubungkan oleh satuan tiga karbon yang dapat membentuk cincin keton. Flavonoid merupakan golongan terbesar dari senyawa fenolik disamping fenol sederhana, fenil
propanoid dan kuinon fenolik. Senyawa golongan flavonoid termasuk senyawa polar dan dapat diekstraksi dengan pelarut yang bersifat polar. Beberapa pelarut yang bersifat polar diantaranya etanol, air, dan etil
asetat (Liana, 2010).
Gambar 2.2 Struktur Flavonoid
Fungsi flavonoid bagi tumbuhan untuk menarik serangga, yang membantu proses penyerbukan dan untuk menarik perhatian binatang yang membantu penyebaran biji. Bagi kehidupan manusia dalam dosis kecil flavon bekerja sebagai stimulat pada jantung, herperidin mempengaruhi pembuluh darah kapiler. Flavon terhidrolisa bekerja sebagai diuretik dan antioksidan pada lemak (Sirait, 2007).
2.3.2 Tanin
Tanin secara umum didefinisaikan sebagai senyawa polifenol yang memiliki berat molekul cukup tinggi ( lebih dari 1000) dan dapat membentuk kompleks dengan protein (Hagerman et al., 2002). Tanin dapat diekstraksi dari seluruh bagian tumbuhan, meliputi daun, cabang, batang, akar dan buah. Namun, umumnya ekstraksi tanin dilakukan dari daun dan batang tumbuhan. Jaringan yang diekstrak dapat berupa jaringan segar maupun yang sudah kering (Scalbert et al, 2005).
Dalam industri tanin adalah senyawa yang berasal dari tumbuhan yang mampu mengubah kulit hewan yang mentah menjadi kulit siap pakai karena kemampuannya menyambung silang protein. Berdasarkan
strukturnya tanin dibedakan menjadi dua kelas yaitu tanin terkondensasi (condensed tannins) dan tanin terhidrolisiskan (hydrolysable tannins)
a. Tanin terkondensasi
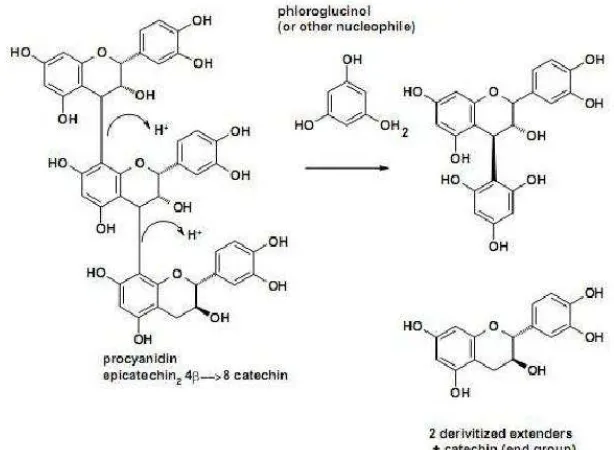
Tanin terkondensasi secara biosintesis terbentuk dengan cara kondensasi tunggal (galokatekin) yang membentuk senyawa dimer dan oligomer yang lebih tinggi. Ikatan karbon-karbon menghubungkan satu flavon dengan satuan berikutnya dengan ikatan 4-8 dan 6-8. Kebanyakan flavolan memiliki 2-20 sauan flavon. Tanin terkondensasi disebut juga dengan proantosianidin karena jika direaksikan dengan asam panas, beberapa ikatan karbon penghubung satuan akan terputus dan dibebaskanlah monomer antosianin (Harborne, 1995).
Sumber : Manitto, 1995
Gambar 2.3 Tanin Terkonjugasi
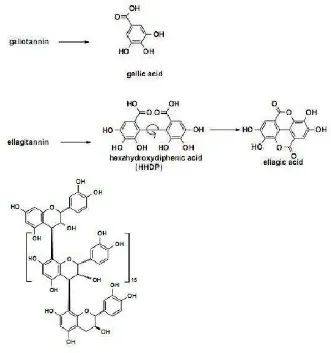
b. Tanin terhidrolisis
terhidrolisis yang bisa disebut ellagitanin. Ellagitanin sederhana disebut juga ester asam hexahydroxydiphenic (HHDP). Senyawa ini dapat terpecah menjadi asam galik jika dilarutkan dalam air.
Sumber: Manitto, 1995
Gambar 2.4 Tanin Terhidrolisis
2.3.3 Alkaloid
Alkaloida adalah senyawa kimia yang secara khas diperoleh dari tumbuhan dan hewan, bersifat basa, mengandung satu atau lebih atom nitrogen (biasanya dalam cincin heterosiklik), dibiosintesis dari asam amino, banyak diantaranya memiliki aktivitas biologis pada manusia dan hewan.
Alkaloid sebagai golongan dibedakan dari sebagian besar komponen tumbuhan lain berdasarkan sifat basanya (kation). Oleh karena itu senyawa ini biasanya terdapat dalam tumbuhan sebagai garam berbagai asam organik dan sering ditangani di laboratorium sebagai garam dengan asam hidroklorida dan asam sulfat. Garam ini, dan sering alkaloid bebas, berupa senyawa padat berbentuk kristal tanwarna. Beberapa alkaloid berupa cairan, dan alkaloid yang berwarna pun langka (berberina dan serpentina berwarna kuning) (Robinson, 1995).
Menurut Harbone (1995) Secara kimia, alkaloid merupakan suatu
golongan heterogen. Alkaloid banyak yang mempunyai kegiatan fisiologi yang menonjol, jadi digunakan secara luas dalam bidang pengobatan.
Menurut Hegnauer, alkaloid dikelompokkan sebagai:
a. Alkaloid sesungguhnya
Alkaloid sesungguhnya adalah racun, senyawa tersebut menunjukkan aktivitas phisiologi yang luas, hampir tanapa terkecuali bersifat basa; lazim mengandung nitrogen dalam cincin heterosiklis; diturunkan dari asam amino; biasanya terdapat dalam tanaman sebagai garam asam organik. Beberapa perkecualian terhadap aturan tersebut adalah kolkhisin dan asam aristolokhat yabg bersifat bukan basa dan tidak memiliki cincin heterosiklis dan alkaloid kuartener, yang bersifat agak asam daripada basa.
b. Protoalkaloid
Protoalkaloid diperolehberdasarkan biosintesis dari asam amino yang bersifat basa. Contoh, adalah meskalin, ephedin, dan N,N-dimetiltriptamin.
c. Pseudoalkaloid
Pseudoalkaloid tidak diturunkan dari precursor asam amino. Senyawa biasanya bersifat basa. Ada dua seri alkaloid yang penting dalam klas ini, yaitu alkaloid steroidal (contoh konessin) dan purin (contoh kaffein) (Sastrohamidjojo, 1996).
2.3.4 Saponin
Saponin adalah glikosida triterpenoid dan sterol. Saponin berasal
dari bahasa latin “sapo” yang berarti sabun, diberi nama demikian karena
sifatnya yang menyerupai sabun. Saponin adalah senyawa aktif permukaan yang kuat yang menimbulkan busa jika dikocok dalam air dan pada konsentrasi yang rendah sering menyebabkan hemolisis sel darah merah. Dalam larutan yang sangat encer saponin sangat beracun
untuk ikan, dan tumbuhan yang mengandung saponin telah digunakan sebagai racun ikan selama beratus-ratus tahun. Beberapa saponin juga bekerja sebagai antimikroba (Robinson, 1995).
2.3.5 Terpenoid
2.4 Antioksidan
Antioksidan merupakan senyawa pemberi elektron (electron donor) atau reduktan. Senyawa ini memiliki berat molekul kecil, tetapi mampu mengaktivasi berkembangnya reaksi oksidasi, dengan cara mencegah terbentuknya radikal. Radikal bebas adalah atom atau senyawa yang kehilangan pasangan elektronnya. Radikal bebas dapat dihasilkan dari proses metabolisme tubuh sendiri dan bisa melalui faktor eksternal seperti lingkungan sekitar kita. Penyakit yang disebabkan oleh radikal bebas bersifat kronis. Contoh penyakit yang sering dihubungkan dengan radikal bebas adalah kanker, serangan jantung dan penurunan fungsi ginjal. Untuk mencegah atau mengurangi penyakit karena radikal bebas diperlukan antioksidan (Iswari, 2011).
Antioksidan dapat diperoleh:
1. Dari luar tubuh (eksogen) dengan cara melalui makanan dan minuman yang mengandung vitamin C, E, atau betakaroten.
2. Dari dalam tubuh (endogen), yakni dengan enzim superoksida
dismutase (SOD), gluthatione, peroksidasi, dan katalase yang diproduksi oleh tubuh sebagai antioksidan. (Kosasih et al, 2006).
Sebenarnya tubuh sendiri mempunyai sistem antioksidan termasuk
superoksid dismutase, katalase, dan glutation, akan tetapi jika terjadi paparan oksidan yang berlebihan, antioksidan tubuh ini tidak akan mampu untuk mengatasinya. Sehingga tubuh memerlukan pasokan antioksidan dari luar (Nordmann,1993).
2.4.1 Antioksidan Alami
Senyawa antioksidan alami tumbuhan umumnya adalah senyawa fenolik atau polifenolik yang dapat berupa golongan flavonoid, turunan asam sinamat, kumarin, tokoferol dan asam-asam organik polifungsional. Golongan flavonoid yang memiliki aktivitas antioksidan meliputi flavon, flavonol, isoflavon, kateksin, flavonol dan kalkon. Sementara turunan asam sinamat meliputi asam kafeat, asam ferulat, asam klorogenat dan lain - lain.
2.4.2 Antioksidan Sintetik
Antioksidan sintetik adalah antioksidan yang diperoleh dari hasil sintesis reaksi kimia. Senyawa fenol sintetis seperti Butil Hidroksianisol (BHA) dan Butil Hidroksitoluen (BHT) bukan antioksidan yang baik, sebab pada pemaparan yang lama dapat menyebabkan efek negatif terhadap kesehatan serta meningkatkan terjadinya karsinogenesis. Antioksidan alami
adalah antioksidan hasil ekstraksi bahan alam. Antioksidan alami seperti α -tokoferol dan asam askorbat, memiliki efek samping merugikan yang lebih kecil, tetapi aktivitasnya lebih tinggi daripada antioksidan sintetik .
Beberapa contoh antioksidan sintetik yang diijinkan penggunaanya untuk makanan dan penggunaannya telah sering digunakan, yaitu butil hidroksi anisol (BHA), butil hidroksi toluen (BHT), propil galat (PG),
tert-butil hidoksi quinon (TBHQ) dan tokoferol. Antioksidan-antioksidan tersebut merupakan antioksidan alami yang telah diproduksi secara sintetis untuk tujuan komersial. Senyawa antioksidan yang diisolasi dari sumber alami dan ditambahkan ke makanan sebagai bahan tambahan pangan (Pratt et al, 1992).
2.4.3 Metode Pengukuran Aktivitas Antioksidan
Pengukuran aktivitas antioksidan dapat dilakukan dengan tiga metode yaitu:
1. Metode DPPH (2,2-diphenyl-1-pikril-hydrazyl)
memberikan efek warna ungu pada panjang gelombang 517nm dalam pelarut etanol (Hirota et al, 2000).
DPPH sering digunakan sebagai salah satu metode untuk mengukur aktivitas antioksidan. Prinsipnya adalah penangkapan hidrogen oleh DPPH dari zat antioksidan. DPPH yang berperan sebagai radikal bebas akan bereaksi dengan senyawa antioksidan, sehingga DPPH akan berubah menjadi diphenilpycrilhydrazine akan ditandai dengan perubahan warna ungu menjadi warna kuning pucat (Molyneux, 2004).
Gam bar 2.5 Reaksi DPPH
Hasil dari metoda DPPH umumnya dibuat dalam bentuk IC50 (Inhibitor Concentrasi 50) yang didefinisikan sebagai konsentrasi
larutan substrat atau sampel yang akan menyebabkan tereduksi aktivitas DPPH sebesar 50%. Semakin besar aktivitas antioksidan maka nilai IC50 akan semakin kecil. Suatu senyawa antioksidan dinyatakan baik jika nilai IC50 semakin kecil (Molyneux, 2004). 2. Metode FRAP (Ferric Reducing Antioxidant Power)
3. Metode Cuprac (Cupric Ion Reducing Antioxidant Capacity)
Pada metode CUPRAC, kompleks bisneokuproin-tembaga(II) akan mengoksidasi senyawaan antioksidan dalam ekstrak tanaman dan mengalami reduksi membentuk kompleks bis-neokuproin-tembaga(I). Secara visual hal ini dapat dilihat dari perubahan warna kompleks larutan dari biru toska menjadi kuning. Pereaksi CUPRAC merupakan pereaksi yang selektif karena memiliki nilai potensial reduksi yang rendah, yaitu sebesar 0,17 V (Widyastuti, 2010).
2.4.4 Spektrofotometer
Spektrofotometer adalah alat yang terdiri dari spektrometer dan fotometer. Spektrum elektromagnetik dibagi dalam beberapa daerah cahaya. Suatu daerah akan diabsorbsi oleh atom atau molekul dan panjang gelombang cahaya yang diabsorbsi dapat menunjukan struktur senyawa yang diteliti. Spektrum elektromagnetik meliputi suatu daerah panjang gelombang yang luas dari sinar gamma
gelombang pendek berenergi tinggi sampai pada panjang gelombang mikro.
Spektrum UV-Vis mempunyai bentuk yang lebar dan hanya
sedikit informasi tentang struktur yang bisa didapatkan dari spektrum ini. Tetapi spektrum ini sangat berguna untuk pengukuran secara kuantitatif. Konsentrasi dari analit di dalam larutan bisa ditentukan dengan mengukur absorban pada panjang gelombang tertentu dengan menggunakan hukum Lambert-Beer (Khopkar, 2007).
a. Sebagai sumber sinar; lampu deuterium atau lampu hidrogen untuk pengukuran UV dan lampu tungsten digunakan untuk daerah visibel.
b. Monokromator; digunakan untuk mendispersikan sinar ke dalam komponen-komponen panjang gelombangnya yang selanjutnya akan dipilih oleh celah (slit). Monokromator berputar sedemikian rupa sehingga kisaran panjang gelombang dilewatkan pada sampel sebagai scan instrumen melewati spektrum.
c. Optik-optik; dapat didesain untuk memecah sumber sinar sehingga sumber sinar melewati 2 kompartemen, dan sebagai mana dalam spektrofotometer berkas ganda (double beam), suatu larutan blanko dapat digunakan dalam satu kompartemen untuk mengkoreksi pembacaan atau spektrum sampel. Yang paling sering digunakan sebagai blanko dalam spektrofotometri adalah semua pelarut yang digunakan untuk melarutkan sampel atau pereaksi (Rohman, 2007).
2.5 Antibakteri
Antibakteri adalah senyawa yang digunakan untuk mengendalikan pertumbuhan bakteri yang bersifat merugikan. Pengendalian pertumbuhan
mikroorganisme bertujuan untuk mencegah penyebaran penyakit dan infeksi, membasmi mikroorganisme pada inang yang terinfeksi, dan mencegah pembusukan serta perusakan bahan oleh mikroorganisme (Sulistyo, 1971). Antimikrobia meliputi golongan antibakteri, antimikotik, dan antiviral.
dan dapat menghambat pertumbuhan mikroba lain. Senyawa antibakteri dapat bekerja secara bakteriostatik, bakteriosidal, dan bakteriolitik (Pelczar et al, 1988).
Menurut Madigan dkk. (2000), berdasarkan sifat toksisitas selektifnya, senyawa antimikrobia mempunyai 3 macam efek terhadap pertumbuhan mikrobia yaitu:
1. Bakteriostatik memberikan efek dengan cara menghambat pertumbuhan tetapi tidak membunuh. Senyawa bakterostatik seringkali menghambat sintesis protein atau mengikat ribosom. Hal ini ditunjukkan dengan penambahan antimikrobia pada kultur mikrobia yang berada pada fase logaritmik. Setelah penambahan zat antimikrobia pada fase logaritmik didapatkan jumlah sel total maupun jumlah sel hidup adalah tetap.
2. Bakteriosidal memberikan efek dengan cara membunuh sel tetapi tidak terjadi lisissel atau pecah sel. Hal ini ditunjukkan dengan penambahan antimikrobia pada kultur mikrobia yang berada pada fase logaritmik. Setelah penambahan zat antimikrobia pada fase logaritmik didapatkan
jumlah sel total tetap sedangkan jumlah sel hidup menurun.
3. Bakteriolitik menyebabkan sel menjadi lisis atau pecah sel sehingga jumlah sel berkurang atau terjadi kekeruhan setelah penambahan
antimikrobia. Hal ini ditunjukkan dengan penambahan antimikrobia pada kultur mikrobia yang berada pada fase logaritmik. Setelah penambahan zat antimikrobia pada fase logaritmik, jumlah sel total maupun jumlah sel hidup menurun.
2.5.1 Bakteri
Berdasarkan perbedaan di dalam menyerap zat warna gram, maka bakteri dibagi atas dua golongan yaitu gram positif dan gram negatif.
a. Bakteri Staphylococcus aureus
S. aureus adalah bakteri Gram positif yang menghasilkan pigmen
kuning, bersifat aerob fakultatif, tidak menghasilkan spora dan tidak motil, umumnya tumbuh berpasangan maupun berkelompok, dengan diameter sekitar 0,8-1,0 μm. Klasifikasi S. aureus adalah:
Kerajaan : Bacteria Filum : Firmicutes Kelas : Bacilli Bangsa : Bacillales
Suku : Staphylococcaceae Marga : Staphylococcus Jenis : Staphylococus aureus
S. aureus merupakan bakteri osmotoleran, yaitu bakteri yang dapat
hidup di lingkungan dengan rentang konsentrasi zat terlarut (contohnya
garam) yang tinggi, dan dapat hidup pada konsentrasi NaCl sekitar 3 Molar. S. aureus tumbuh dengan optimum pada suhu 37oC dengan waktu pembelahan 0,47 jam. Bakteri ini biasanya terdapat pada saluran pernafasan atas dan kulit, keberadaan S. aureus pada saluran pernafasan
atas dan kulit pada individu jarang menyebabkan penyakit, individu sehat biasanya hanya berperan sebagai karier.
b. Bakteri Escherichia coli
E. coli pertama kali ditemukan oleh seorang bacteriologist yang
berasal dari Jerman bernama Theodor Von Escherich pada tahun 1885. Secara alamiah E. coli adalah penghuni umum dalam pencernaan manusia dan hewan. Adapun taksonomi dari E. coli sebagai berikut:
Kingdom : Prokaryota
Filum : Proterobacteria
Kelas : Bacteria
Ordo : Enterobacteriales
Family : Enterobacteriaceae
Genus : Escherichia
Species : Escherichia coli
E.coli merupakan bakteri yang secara normal terdapat dalam
usus dan berperan dalam proses pembusukan sisa makanan. Keberadaan bakteri ini merupakan parameter ada tidaknya materi fecal di dalam suatu habitat khususnya air. E.coli adalah salah satu jenis bakteri yang ada dalam tinja manusia dan dapat mengakibatkan gangguan pencernaan
seperti diare.
Kemampuan suatu senyawa dalam menghambat pertumbuhan bakteri dipengaruhi oleh beberapa faktor, diantaranya:
a. Konsentrasi kandungan senyawa antibakteri b. Jumlah, umur, jenis dan keadaan mikroba c. Suhu yang sesuai untuk pertumbuhan optimal d. Waktu pertumbuhan mikroba
e. Sifat-sifat kimia dan fisika seperti kadar air dan pH
2.5.2 Metoda Pengujian Aktivitas Antibakteri 1. Metode difusi agar
mengukur diameter zona bening (clear zone) yang merupakan petunjuk adanya respon penghambatan pertumbuhan bakteri oleh suatu senyawa antibakteri dalam ekstrak. Syarat jumlah bakteri untuk uji kepekaan/sensitivitas yaitu 105-108 CFU/mL (Hermawan dkk., 2007).
2. Metode dilusi
Metoda ini menggunakan antimikroba dengan kadar yang menurun secara bertahap, baik dengan metoda cair atau padat. Kemudian media diinokulasi bakteri uji dan dieramkan. Tahapan akhir dilarutkan antimikroba dengan kadar yang menghambat atau mematikan. Uji kepekaan cara dilusi agar memakan waktu dan penggunaannya dibatasi pada keadaan tertentu saja.
3 Cara turbidimetri
Pada metoda ini digunakan media cair. Pertama dilakukan menuang media ke dalam tabung reaksi, lalu ditambahkan suspensi bakteri, kemudian dilakukam pemipetan larutan uji, dan diinkubasi.
Selanjutnya dilakukan pengukuran kekeruhan yang disebabkan oleh pertumbuhan bakteri diukur dengan menggunakan alat instrumen yang sesuai, seperti nephelometer setelah itu dilakukan potensi antimikroba.
2.6 Teknik Pemisahan
Ekstraksi adalah kegiatan penarikan kandungan kimia yang dapat larut sehingga terpisah dari bahan yang tidak dapat larut dengan pelarut cair. Cara ekstraksi yang tepat tergantung pada bahan tumbuhan yang diekstraksi dan jenis senyawa yang diisolasi. Sebelum ekstraksi dilakukan biasanya bahan-bahan dikeringkan lebih dahulu kemudian dihaluskan pada derajat kehalusan tertentu (Harborne, 1995).
Beberapa metode ekstraksi dengan menggunakan pelarut yaitu: 1. Cara Dingin
Maserasi
Maserasi adalah proses penyarian simplisia menggunakan pelarut dengan
Keuntungan ekstraksi dengan cara maserasi adalah pengerjaan dan peralatan yang digunakan sederhana, sedangkan kerugiannya yakni cara pengerjaannya lama, membutuhkan pelarut yang banyak dan penyarian kurang sempurna.
Perkolasi
Perkolasi adalah ekstraksi dengan pelarut yang selalu baru sampai terjadi penyarian sempurna yang umumnya dilakukan pada temperatur kamar. Proses perkolasi terdiri dari tahap pengembangan bahan, tahap perendaman antara, tahap perkolasi sebenarnya(penampungan ekstrak) secara terus menerus sampai diperoleh ekstrak (perkolat). Untuk menentukan akhir dari pada perkolasi dapat dilakukan pemeriksaan zat secara kualitatif pada perkolat akhir.
2. Cara Panas Refluks
Refluks adalah ekstraksi pelarut pada temperatur titik didihnya, selama waktu tertentu dan jumlah pelarut terbatas yang relatif konstan dengan adanya pendingin balik.
Digesti
Digesti adalah maserasi dengan pengadukan kontiniu pada temperatur
lebih tinggi dari temperatur ruangan (umumnya 25-30oC) Sokletasi
Sokletasi adalah ekstraksi mengunakan pelarut yang selalu baru, dengan menggunakan alat sokhlet sehingga terjadi ekstraksi kontiniu dengan jumlah pelarut relatif konstan dengan adanya pendingin balik.
Infundasi