EFEKTIVITAS ARANG AKTIF DALAM MENGADSORPSI LOGAM Cd dan Pb DALAM AIR LIMBAH INDUSTRI
1A.Arief Azis,2Mary Selintung2Achmad Zubair
1Mahasiswa Program Studi Teknik Lingkungan Jurusan teknik Sipil, Universitas Hasanuddin 2Dosen Pengajar Prodi Teknik Lingkungan Jurusan Teknik Sipil, Universitas Hasanuddin
Email :ariefazis92@gmail.com
Abstrak:
Perkembangan teknologi mendorong pertumbuhan industry yang menghasilkan limbah yang mengandung logam berat, diantaranya adalah Logam Pb2+ dan Cd2+. Penelitianini bertujuan untuk mengetahui efektifitas arang aktif dalam mengadsorbsi logam Pb2+ dan
Cd2+ dalam limbah industry dengan variasi pengaktivasi yang berbeda. Penelitian ini
menggunakan limbah artifisial dengan konsentrasi 10 ppm dengan metode kolom adsorbsi. Limbah dialirkan kedalam tiga kolom dengan pengaktivasi yang berbeda (Pemanasan, H3PO4
10 %, NaOH 10 %) dengan lama waktu kontak 480 menit dan dianalsis dengan Spekrofotometer Serapan Atom (AAS). Hasil penelitian ini menunjukkan bahwa pengaktivasi yang paling baik digunakan untuk mengadsorbsi logam Pb2+dan Cd2+adalah H3PO4 dengan
persentase penyerapan untuk logam Pb2+ sebesar 51,41 % dan untuk logam Cd2+ sebesar
59,90 %. Kapasitas adsorbsi (qe) terbesar logam Pb2+ dan Cd2+ juga terjadi pada variasi
pengaktivasi dengan menggunakan H3PO4 sebesar 0,24679 mg/g dan 0,28752 mg/g.
Sedangkan kapasitas adsorbsi terkecil logam Pb2+dan Cd2+terjadi pada pengaktivasi dengan
pemanasan sebesar 0,18711 mg/g dan 0,13328 mg/g. Kata Kunci: Logam Berat, Adsorbsi, Arang Aktif
BAB I. PENDAHULUAN
Perkembangan teknologi yang pesat mendorong pertumbuhan industri yang memiliki peran besar terhadap pencemaran lingkungan. Industri-industri yang berdiri banyak menghasilkan limbah cair yang memiliki tingkat konsentrasi pencemaran diatas nilai ambang batas minimum yang telah ditetapkan. Bahan pencemar yang biasanya dihasilkan oleh industry berupa logam berat, diantaranya Pb(Timbal) dan Cd(Kadmium).
Pencemaran logam berat terhadap lingkungan merupakan suatu proses yang erat hubungannya dengan penggunaan
logam tersebut oleh manusia. Dalam suatu proses produksi industri yang memerlukan suhu tinggi, seperti pemurnian minyak, pertambangan batubara, pembangkit tenaga listrik dengan energi minyak, dan pengecoran logam, banyak mengeluarkan limbah pencemar, terutama pada logam-logam yang relatif mudah menguap dan larut dalam air (bentuk ion), seperti arsen (As), kadmium (Cd), timbal (Pb) dan merkuri (Hg). Selain itu pencemaran juga dapat disebabkan oleh pabrik produksi semen, limbah pabrik peleburan besi baja, dan pengabuan sampah (Purwanti Yoga Ningrum, 2006).
Umumnya logam berat dalam industri dipakai sebagai bahan baku, aditif dan katalisator. Beberapa hasil penelitian mengungkapkan bahwa terdapat beberapa macam penyakit pada manusia akibat memakan makanan yang mengandung logam berat seperti kanker, gangguan saluran cerna, ginjal, dll. Pencemaran merkuri di Minamata Jepang (1953- 1960 ) dan Niaga Jepang (1968) berasal dari limbah industri plastik yang memakai katalisator merkuri clorida menyebabkan tingginya kadar merkuri pada ikan yang berasal dari hasil laut sekitarnya dan
menyebabkan masyarakat yang
mengkomsumsikannya keracunan merkuri. Akibatnya timbul berbagai penyakit seperti depresi, gangguan jiwa dan cacat. Tercatat pada periode 1953-1960 di Minamata 111 orang meninggal dan di Nigata (1968) 5 orang meninggal 25 cacat (Palar, 1994).
Kasus pencemaran Cd di Jepang bila mengacu kepada perundangan-undangan di Indonesia memang masuk dalam kategori pencemaran berat. Disebutkan bahwa kandungan kadmium di dalam padi pada area tercemar berkisar antara 1,00 ppm sampai 6,88 ppm serta 4,04 ppm di sungai Jinzu itu tidak sesuai dengan peraturan mentri lingkungan hidup tahun 2010 bahwa standar baku mutu air limbah kawasan industri yang hanya diperbolehkan 0,1 mg/l. Kadar kadmium di sungai Jinzu juga sebaiknya tidak dikonsumsi sebagai air minum bila mengacu kepada standar kualitas air minum yang ditetapkan oleh kementerian kesehatan di negeri ini yang hanya mengizinkan 0,003 mg/l (Festri, 2014).
Adsorpsi
Proses adsorbsi dapat digambarkan
sebagai proses dimana molekul
meninggalkan larutan dan menempel pada permukaan zat. Proses adsorbsi biasanya dilakukan dengan mengontakkan larutan atau gas dengan padatan, sehigga sebaian komponen larutan atau gas dijerap pada permukaan pori padatan, akibatnya akan mengubah koposisi larutan tersebut (Reri Afrianita, 2012).
Faktor Yang Mempengaruhi Adsorpsi
Beberpa faktor yang mempengaruhi adsorpsi pada permukaan zat padat antara lain:
a. Jenis adsorben
Syarat-syarat yang harus dipenuhi dalam pemilihan adsorben adalah memiliki permukaan kontak yang luas, mempunyai pori-pori aktif dan murni serta tidak bereaksi dengan adsorbat.
b. Jenis adsorbat
Syarat-syarat yang diperlukan agar adsorbat terjerap dengan baik adalah:
1. Ukuran adsorbat
Molekul terjerap haruslah mempunyai ukuran partikel yang lebih kecil dari ukuran diameter pori adsorben. Pada penelitian yang dilakukan Riki Irwandi ( 2015) terhadap daya serap karbon aktif pada logam Pb dengan variasi massa adsorben 1, 2, dan 3 gram dengan waktu kontak 30, 60, 90 dan 120 menit di dapatkan massa karbon aktif yang paling baik pada penelitian ini adalah 3 gram, hal ini menunjukkan bahwa semakin besar massa adsorben
maka semakin besar daya serap karbon aktif terhadap logam yang dihasilkan.
Menurut wijayanti (2009)
menyatakan bahwa pada saat adanya peningkatan massa karbon aktif maka
ada peningkatan presentase
penyerapan terhadap logam yang diserap, pemilihan massa karbon aktif terbaik dapat dilihat dari kemampuan karbon aktif untuk menurukan konsentrasi logam dalam sampel. 2. Jenis kepolaran adsorbat
Umumnya adsorbat bersifat ionic dengan polaritas tinggi, jika diameternya sebanding maka molekul-molekul polar terjerap lebih kuat daripada molekul nonpolar.
3. Jenis ikatan
Senyawa tidak jenuh lebih baik dijerap bila dibandingkan dengan senyawa jenuh.
c. Temperatur
Pada adsorpsi fisis kenaikan
temperatur menyebabkan adsorpsi
menurun. Hal ini disebabkan mobilitas dari atom-atom suatu zat yang diadsorsi bertambah dengan naiknya temperatur. Oleh karena itu, zat yang dijerap cenderung meninggalkan zat penjerap. Sedangkan pada adsorpsi kimia, adsorpsi bertambah dengan naiknya temperatur.
Kenaikan temperature juga dapat
menyebabkan pori-pori adsorben lebih terbuka karena unsur-unsur pengotor pada permukaan akan teroksidasi.
d. pH
Adsorpsi antara fasa padat-cair sangat dipengaruhi oleh pH larutan. Adsorpsi yang dilakukan pada pH tinggi cenderung memberikan hasil yang kurang sempurna, karena pada kondisi basa terbentuk senyawa oksida dari unsur pengotor lebih besar sehingga akan menutupi permukaan adsorben. Hal ini sesuai dengan penelitian yang dilakukan Indri Ayu Lestari (2014) dan Erika Mulyana Gultom (2014) dimana dalam penelitian yang dilakukan ternyata semakin tinggi pH maka daya serap akan
menurun sehingga didapatkan pH
optimum untuk proses adsorpsi adalah pH 3 – 4.
e. Waktu Kontak
Kemampuan daya jerap meningkat dengan lamanya waktu kontak antara
adsorben dengan adsorbat hingga
mencapai kesetimbangan (Sunarno, 2000).
BAB III. METODE PENELITIAN
A. Jenis Penelitian
Jenis penelitian ini adalah analisis eksperimental, yaitu melakukan pengujian eksperimen di laboratorium terhadap objek yang diteliti, yang bertujuan menganalisis tingkat adsorpsi logam Timbal (Pb) dan Kadmium (Cd) dengan memanfaatkan karbon aktif dengan variasi pengaktivasi yang berebeda sebagai adsorben.
B. Alat dan Bahan yang Digunakan
Alat-alat yang digunakan pada penelitian ini adalah : Oven, Tanur, Botol Sampel, Pipet Volume, Timbangan digital (ohaus), Spektrofotometer Serapan Atom (SSA), Pipa PVC, Kain Penyaring, Beaker gelas, Ayakan , Botol semprot, Cawan
porselin. Bahan yang digunakan pada penelitian ini adalah: Arang kayu, Larutan Pb 10 mg/L, Lautan Cd 10 mg/L, NaOH 10 %, H3PO4 10%, Aquadest.
C. Prosedur Penelitian
a. Preparasi Aktivasi Arang
Aktifasi arang berarti menghilangkan zat-zat yang menutupi pori-pori pada permukaan arang dan memperluas pori-pori arang. Dimana dalam penelitian ini digunakan 3 cara pengaktivasi yaitu
dengan mengaktivasi dengan asam
(H3PO4), Basa (NaOH) dan Pemanasan.
1. Pengaktivasi dengan asam (H3PO4)
Arang diaktifasi di dalam larutan aktifator H3PO4 10 % dengan waktu 24
jam. Sampel kemudian disaring, dan dicuci dengan aquadest hingga pH 7. Sampel dikeringkan dalam oven dari suhu kamar sampai suhu 110oC selama 2 jam.
2. Pengaktivasi dengan Basa (NaOH) Arang diaktifasi di dalam larutan aktifator NaOH 10 % dengan waktu 24 jam. Sampel kemudian disaring, dan dicuci dengan aquadest hingga pH 7. Sampel dikeringkan dalam oven dari suhu kamar sampai suhu 110oC selama
2 jam.
3. Pengaktivasi dengan Pemanasan Pada Suhu Tinggi
Arang dimasukkan ke dalam oven kemudian ditutup rapat. Tanur diatur pada suhu awal 0-400oC selama ± 4 jam.
Setelah mencapai suhu optimum 400oC
selama ± 60 menit maka proses aktifasi arang telah selesai. Arang aktif yang dihasilkan dibiarkan sampai dingin, setelah itu arang aktif dapat dikeluarkan
b. Pengukuran adsorben berdasarkan lama waktu kontak
Sebanyak 29.000 ml larutan timbal dan kadmium di masukkan kedalam wadah atau kolom yang berisi arang aktif yang telah diaktifasi dengan pemanasan pada suhu 4000C sebanyak 200 gram. Larutan
yang mengalir melewati arang aktif tersebut dilewatkan berdasarkan lama waktu tinggal sesuai dengan pengaturan debit bukaan keran dengan variasi pengambilan filtrat 15 menit, 30 menit, 60 menit, 120 menit, 180 menit, 240 menit, 300 menit, 360 menit, 420 menit, dan 480 menit. Hasil filtrat tersebut kemudian
ditampung dan diukur dengan
menggunakan spektrofotometer serapan atom (SSA). Selanjutnya percobaan kemudian diulangi dengan menggunakan variasi pengaktifasi arang H3PO410 % dan
NaOH 10 % dengan lama waktu kontak 15 menit, 30 menit, 60 menit, 120 menit, 180 menit, 240 menit, 300 menit, 360 menit, 420 menit, dan 480 menit
D. Pengolahan Data
Kurva breakthrough diperoleh dengan cara memplotkan data Ct/C0 Vs Waktu, dimana C0 merupakan konsentrasi larutan logam awal, dan Ct merupakan konsentrasi larutan logam yang keluar dari kolom. Berdasarkan kurva tersebut kemudian ditentukan waktu breaktrhough (tb), 0,9 (90% breakthrough). Selanjutnya, menentukan parameter breakthrough berupa massa total logam yang terserap (qtotal), massa ion logam yang melewati kolom (mtotal), persentase penghilangan ion logam (%R), kapasitas adsorpsi (qeq), dengan menggunakan persamaan berikut:
(1) (2)
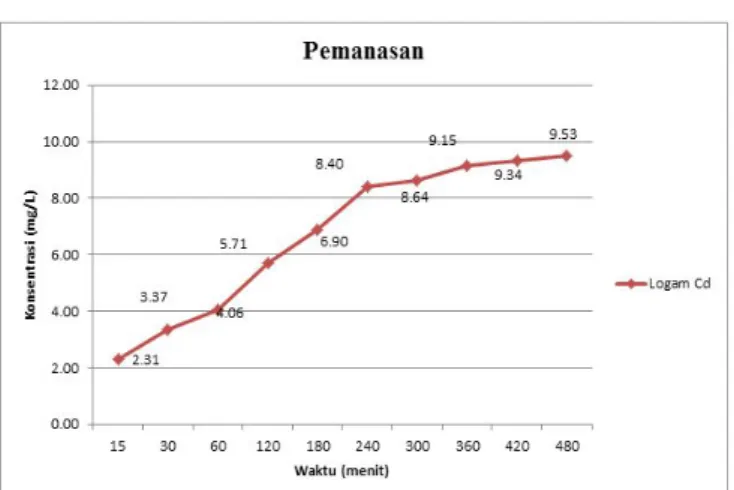
Gambar Grafik Penyerapan Ion Logam
Kadmium (Cd) Dengan Pengaktivasi Pemanasan
Gambar Grafik Penyerapan Ion Logam
Kadmium (Cd) Dengan Pengaktivasi H3PO4
(3) (4) (5) Dimana, Q adalah debit (mL/mnt), C0
adalah konsentrasi influent (mg/L), X massa adsorbent yang digunakan pada kolom (g), ttotal waktu jenuh total (menit).
BAB IV. HASIL DAN PEMBAHASAN A. Data Hasil Uji Laboratorium
1. Konsentrasi Akhir Logam Pb
v
Dari Grafik tersebut dapat di lihat bahwa sama halnya dengan logam Timbal
Gambar Grafik Penyerapan Ion Logam Timbal (Pb) Dengan
Pengaktivasi Pemanasan
Gambar Grafik Penyerapan Ion Logam Timbal (Pb) Dengan
Pengaktivasi H3PO4
Gambar Grafik Penyerapan Ion Logam Timbal (Pb) Dengan Pengaktivasi NaOH 2. Konsentrasi Akhir Logam Cd
pengaktivasi yang paling baik digunakan untuk menyerap ion logam Kadmium (Cd) adalah H3PO4, karena waktu yang
dibutuhkan adsorben untuk mencapai titik jenuhnya lebih lama dibandingkan dengan menggunkan pengativasi pemanasan dan
NaOH. Hal ini disebabkan karena
penggunaan pengativasi asam lebih
banyak membuka pori-pori karbon
sehingga kapasitas penyerapan adsorben lebih besar dibandingkan dengan variasi pengaktivasi lainnya.
B. Analisa Data Penelitian
Tabel Hasil Perbandingan Ct/Co Logam Cd dan Pb
Berdasarkan data hasil pengujian ion logam timbal (Pb) dan Kadmium (Cd) seperti yang terlampir pada Lampiran 1. Data tersebut dapat digunakan untuk menggambarkan kurva breaktrough. Kurva breakthrough dapat menjelaskan parameter lamanya waktu kontak (sumbu x) dalam satuan menit terhadap perbandingan konsentrasi akhir (Ct) dan konsentrasi awal (Co) (sumbu y).
Apabila nilai perbandingan
konsentrasi awal dan konsentrasi akhir (Ct/Co) mendekati nilai 1, maka dapat dikatakan bahwa pada waktu tersebut kondisi adsorben telah mencapai titik jenuh. Waktu jenuh adalah waktu yang dibutuhkan effluent untuk mencapai Ct/Co 90% dari konsentrasi awal. Untuk mencapai nilai 100% dibutuhkan waktu yang lama sehingga 90% dipilih sebagai nilai yang efektif dalam penelitian.
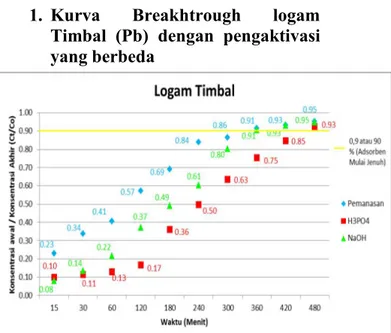
1. Kurva Breakhtrough logam Timbal (Pb) dengan pengaktivasi yang berbeda
GambarHubungan antara waktu dan ct/c0
berdasarkan pengaruh
pengaktivasi yang berbeda pada logam Timbal (Pb)
Berdasarkan Gambar tersebut
terlihat adanya perbedaan daya serap arang aktif dengan pengaktivasi yang berbeda dapat diketahui bahwa pada logam Timbl (Pb) dengan variasi pengakativasi yang berbeda memiliki titik jenuh yang berbeda-beda. Pada Gambar 12 dapat dilihat bahwa
proses pengaktivasi dengan cara
pemanasan lebih cepat mencapai titik jenuhnya yaitu pada menit ke 300 dengan Ct/Co 0,905, dan pada proses pengaktivasi dengan cara perendaman dengan larutan asam fosfat (H3PO4) mencapai titik
jenuhnya pada menit ke 480 dengan Ct/Co 0,925, sedangkan pada proses pengaktivasi dengan natrium hidroksida (NaOH) mencapai titik jenuhnya pada menit ke 420 dengan Ct/co 0,943. Dari Gambar 12 dapat disimpulkan bahwa pengaktivasi yang baik digunakan pada arang aktif untuk mengadsorbsi logam Timbal (Pb) adalah pengaktivasi dengan menggunakan larutan asam dalam hal ini adalah asam posfat (H3PO4) karena asam posfat lebih banyak
membuka pori arang sehingga arang aktif yang dihasilkannya memiliki daya serap yang tinggi.
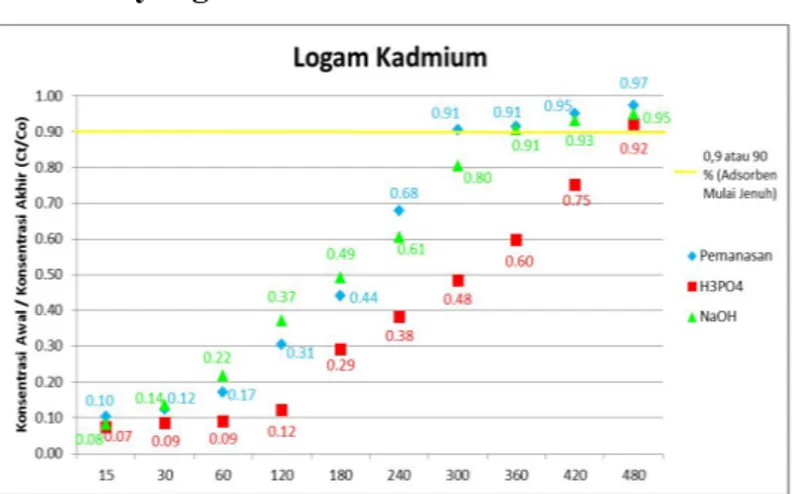
2. Kurva Breakhtrough logam Kadmium (Cd) dengan pengaktivasi yang Berbeda
GambarHubungan antara waktu dan ct/c0
berdasarkan pengaruh
pengaktivasi yang berbeda pada logam Kadmium (Cd)
Sedangkan pada logam Kadmium
(Cd) pada Gambar diatas, dengan
perbedaan cara pengaktivasi juga memiliki titik jenuh yang berbeda-beda. Dimana pada proses pengaktivasi dengan cara pemanasan dan pengaktivasi dengan natrium hidroksida (NaOH) lebih cepat mencapai titik jenuhnya dibandingakan dengan pengaktivasi dengan larutan asam dalam hal ini asam posfat (H3PO4).
Dengan nilai Ct/co untuk pengaktivasi dengan pemanasan adalah 0,905 yang terjadi pada menit ke 360 dan untuk nilai Ct/co pada proses pengaktivasi dengan natrium hidroksida (NaOH) adalah 0,906 pada menit ke 360, sedangkan nilai Ct/co untuk pengaktivasi dengan asam posfat (H3PO4) adalah 0,921 yang terjadi pada
menit ke 480. Sama halnya dengan logam Timbal (Pb) pada logam kadmium (Cd) pengaktivasi yang paling baik digunakan adalah pengaktivasi dengan larutan asam dalam hal ini asam posfat (H3PO4) karena
memiliki titik jenuh yang lebih lama sehingga cocok digunakan dalam sebuah industry.
Kemampuan pengaktif dalam proses aktivasi arang dapat dipengaruhi oleh faktor stabilitas termal dari pengaktif tersebut (Koleangan,2008). Stabilitas
termal dari pengaktif tercermin dari entalpi dekomposisi (ΔH0) masing-masing
pengaktif, dimana stabiltas termal akan semakin baik dengan semakin tingginya entalpi dekomposisi (shriver, 1990). Dari penelusuran pustaka diketahui ΔH0 NaOH
= 426,8 kj/moldan ΔH0 H
3PO4 = 964,4
kj/mol. Dari data ini tampak bahwa H3PO4
memiliki stabilitas termal lebih baik dari pada NaOH sehingga daya jerap arang yang dihasilkan dengan pengaktivasi dengan menggunakan H3PO4 lebih besar
dibandingkan dengan menggunakan NaOH dan Pemnasan.
C. Efektivitas Adsorpsi
Parameter Btreakthrough adsorbsi ion Logam Cd & Pb
Berdasarkan Tabel diatas, diketahui bahwa pengaktivator yang paling baik digunakan adalah H3PO4 karena mempunyai massa
total logam yang terserap (qtotal) sebanyak
57,504 mg untuk logam Kadmium dan 49,358 mg untuk logam Timbal, massa ion logam kadmium dan timbal yang melewati kolom (m total)masing-masing sebesar 96 mg,sehingga kapasitas adsorpsi (qe) untuk logam kadmium sebesar 0,2875 mg/g dan utuk logam timbal sebesar 0,2467 mg/g dan didapatkan efisiensi penyerapan (%R) dengan menggunakan H3PO4 lebih besar
dibandingkan dengan pemanasan dan NaOH yaitu untuk logam Kadium sebesar 59,90 % dan untuk logam Timbal sebesar 51,41%.
Gambar Persentase penyerapan logam Kadmium dan Timbal dengan variasi pengaktivasi
Dari Gambar diatas terlihat adanya perbedaan persentase penyerapan arang aktif yang diaktivasi dengan activator yang berbeda, dimana persentase penyerapan terbesar untuk logam Kadmium dan Timbal adalah dengan menggunakan pengaktivasi asam posfat (H3PO4). Hal ini
karena asam posfat lebih baik dalam membuka pori-pori arang yang tertutupi pengotor yang terjebak dalam pori-pori
sehingga daya adsorbsi semakin
meningkat, hal ini juga disebabkan karena stabilitas termal asam posfat lebih tinggi dibandingakn dengan pengaktif lainnya.
BAB V. PENUTUP A. Kesimpulan
Adapun kesimpulan yang diperoleh pada penelitian pemanfaatan arang aktif sebagai adsorben dalam menurunkan logam Cd dan Pb pada air limbah yaitu sebagai berikut :
1. Berdasarkan penelitian dapat
disimpulkan bahwa pengaktivasi yang
paling baik digunakan untuk
mengadsorbsi logam Cd dan Pb adalah pengaktivasi dengan menggunakan larutan asam dalam hal ini H3PO4.
2. Persentase penyerapan karbon aktif terhadap logam Cd dan Pb dengan pengaktivasi menggunakan H3PO4
sebesar 59,90 % untuk logam Cd dan 51,41 % untuk logam Pb.
3. Kapasitas adsorbsi (qe) terbesar logam Cd dan Pb terjadi pada variasi pengaktivasi dengan H3PO4 sebesar
0,28752 mg/g dan 0,24679 mg/g. sedangkan kapasitas adsorbsi terkecil
logam Cd dan Pb terjadi pada
pengaktivasi dengan pemanasan sebesar 0,13328 mg/g dan 0,18711 mg/g.
B. Saran
1. Untuk pengembangan penelitian ini, sebaiknya perlu dilakukan beragam variasi penelitian seperti pengaruh debit aliran dan tinggi kolom.
2. Sebaiknya untuk penelitian selanjutnya menggunakan pompa pada alat kolom untuk mempermudah aliran debit yang masuk dan keluar.
DAFTAR PUSTAKA
Apriliani, Ade. 2010. “Pemanfaatn Arang Ampas Tebu Sebagai Adsorben Ion Logam Cd, Cr, Cu Dan Pb Dalam
Air Limbah”. Jakarta: Universitas
Islam Negeri Syarif Hidayatullah Ayu Lestari, Indri. 2014. “Adsorbsi Logam
Kadmium (Cd) Oleh Arang Aktif Tempurung Aren (Arenga Pinnata)
Dengan Aktivator Hcl”. Jurnal
Kimia Mulawarman Vol: 12 No: 1 Bella Santa Rossi dan Yuli Ristianingsih.
2014. “Penurunan Konsentrasi
Logam Pb2+dan Cd2+pada Limbah
Cair Industri sasirangan dengan
metode fitoremediasi”. Jurnal
Teknologi Agro-Industri Vol : 1 No: 1
Effendi, Rohmad. 2015. “Adsorbsi Logam
Ni(II) dan Pb (II) Dengan
Menggunakan Arang Sekam Padi
Yang Teraktivasi H3PO4”.
Yogyakarta: Universitas Islam Negri Sunan Kalijaga
Endang Kwartiningsih dan Nanda Setiarini. 2005. “Adsorbsi Logam Cu Dari
Menggunakan Karbon Aktif Dalam
Kolom Fixed Bed”. Ekuilibrum Vol:
4 dan No: 2
Festri Istarani dan Ellina S. Pandebesie. 2014. “Studi Dampak Arsen (As)
dan Kadmium (Cd) terhadap
penurunan kualitas lingkungan”. Jurnal Teknik POMITS Vol: 3 No: 1 Harti, Retno. 2014. “Karakterisasi dan
Modifikasi Karbon Aktif Tempurung Kelapa Sawit Dengan Asam Nitrat Untuk Menjerap Logam Besi dan
Tembaga Dalam Minyak Nilam”.
Yogyakarta : Universitas Islam Indonesia
Hatta, M. Dahlan Dan Hariman P SIregar. 2013. “Penggunaan Karbon Aktif Dari BIji Kelor Dapat Memurnikan
Minyak Jelantah”. Jurnal Teknik
Kimia Vol : 19 , No : 3
Hidayati, Ika. 2006. “Kadar Logam Cd (Kadmium) dalam daging Kerang Thothok (Gelonia Erosa), air, dan
Sedimen Mangrove di Segara
Anakan Cilacap”. Surakarta:
Universitas Sebelas Maret
Imawati, Anita. 2015. “Kapasitas Adsorbsi Maksimum Ion Pb(II) Oleh Arang Aktif Ampas Kopi Teraktivasi HCl
Dan H3PO4”. Jurnal Universitas
Tanjungpura Vol: 4, No: 2, Hal 50-61
Koleangan, H. S. J dan A.D. Wuntu. 2008.
“Kajian Stabilitas Termal Dan
Karakter Kovalen Zat Pengaktif Pada Arang Aktif Limbah Gergajian
Kayu Meranti (Shorea spp) “. Jurnal
Chem.Prog Vol : 1, No: 1
Marianus Bangun, Julius.
2005. ”Kandungan Logam Berat Timbal (Pb) Dan Kadmium (Cd) Dalam Air, Sedimen dan Organ Tubuh Ikan Sokang (Triachanthus nieuhofi) Di Perairan Ancol Teluk Jakarta”. Bogor : Institut Pertanian Bogor
Mulyana Gultom, Erika. 2014. “ Aplikasi Karbon Aktif Dari Cangkang Kelapa Sawit Dengan Aktivator H3PO4 Untuk Penyerapan Logam Berat Cd
dan Pb”. Jurnal Teknik Kimia USU
Vol: 3, No: 1
Mody Lempang, Wasrin Syafii, dan Gustan Pari. 2012. “Sifat dan Mutu Arang Aktif Tempurung Kemiri
(Properties and Quality of
Candlenut Shell Activated Chacoal)”. Jurnal Penelitian Hasil Hutan Vol: 30, No: 2
Naibaho, Marlundu . 2011. “Kajian
Experimental Evaporator Untuk
Mesin Pendingin Siklus Adsorpsi
Yang Digerakkan Energi Surya”.
Medan : universitas sumatera utara
Ni Ketut Sari. 2010. “Analisa
Instrumentasi”. Surabaya: Yayasan
Humaniora
Nunik Prabirini dan DG Okayadnya. 2013.
“ Penyisihan Logam Besi (Fe) Pada
Air Sumur Dengan Karbon Aktif
Dari Tempurung Kemiri”. Jurnal
Ilmiah Teknik Lingkungan Vol: 5, No : 2
Nur, A. Dan Y.C Danarto. 2007. “Adsorpsi Kadmium Dengan Biomassa Bekas
Fermentasi Pabrik Alkohol”.
Surakarta: Universitas Sebelas Maret Noorazis, Ishanifana. 2012. “Uji Cemaran
Logam Timah Dalam Minuman Bersoda Kemasan Kaleng Dengan Metode Spektrofotometri Serapan
Atom”. Purwekerto: Universitas
Muhammadiyah Purwokerto
Palar Heryando Drs. 1994. Pencernaan &
Toksikologi Logam berat. Rineka
Cipta, Jakarta
Rachma sari,yulike. 2012. “Identifikasi Cemaran Logam Timbal Dalam Air Minum Isi Ulang Yang Beredar Di
Purwokerto Dengan Metode
Spektrofotometri Serapan Atom
“.Purwokerto : Universitas
Muhammadiyah Purwokerto
Reri Afrianita dan Yommi Dewilda. 2012.
“Studi Penentuan Kondisi Optimum
Fly Ash Sebagai Adsorben Dalam Menyisihkan Logam Berat Timbal (Pb)”. Jurnal Teknik Lingkungan UNAND Vol: 9, No : 1, Hal : 37 – 43
Wijayanti, Ria. 2009. “Arang Aktif dari Ampas Tebu Sebagai Adsorben Pada
Pemurnian Minyak Goreng Bekas”.
Bogor: Institut Pertanian Bogor Riki Irwandi dan Silvia Reni Yenti. 2015.
“Penetuan Massa dan waktu Kontak
Optimum Adsorbsi Karbon Aktif dari Ampas Tebu Sebagai Adsorben
Logam Berat Pb”. JOM FTEKNIK
Vol: 2, No: 2
Shiriver,E,F. P.W. Atkins, C.H. Langford. 1990. “Ionganic Chemistry”. Oxford : Oxford University Press. Sukreni, T, 2002,” Penggunaan Zeolit
untuk Pengolahan Limbah Cair yang Mengandung Logam Berat Pb dan Ni: Kinetika Pertukaran Ion Pb dan/atau Ni pada Zeolit”, Jogjakarta: Universitas Gajah Mada
Sulistyawati S. 2008. “Modifikasi Tongkol Jagung sebagai Adsorben Logam
Berat Pb (II)”. Bogor : Institute
Pertanian Bogor
Tamar Jaya, Ferawati. 2014. “Adsorpsi Emisi Gas CO, NO, Dan NOx menggunakan Karbon Aktif dari
Limbah Kulit Buah Kakao
(Theobrama Cacao L) Pada
Kendaraan Bermotor Roda Empat”.
Makassar: Universitas Hasanuddin Tri Kurnia Dewi dan Arif Nurrahman.
2009. “Pembuatan Karbon Aktif Dari Kulit Ubi Kayu (Mannihot
esculenta)”. Jurnal Teknik Kimia
Vol: 16, No 1
Umi Baroroh Lili Utami, Taufiqur
Rohman dan Mahmud. 2009.
“Adsorpsi Pb(II) Oleh Kitosan
Terlapiskan Pada Arang Aktif
Cangkang Kelapa Sawit”. Jurnal
sains MIPA Vol : 15, No : 2, Hal 89 -99
Yoga Ningrum, Purwanti . 2006.
“Kandungan Logam Berat timbal
(Pb) Serta Struktur Mikroanatomi Branchia Hepar, dan musculus ikan
belanak (Mugil Chepalus) Di
Perairan Cilacap”. Surakarta: