BAB 2
TINJAUAN PUSTAKA
2.1 Tumbuhan Pirdot (Saurauia vulcani Korth)
Tumbuhan pirdot seperti terlihat pada Gambar 2.1 dan hasil identifikasi yang dilakukan di laboratorium Herbarium Medanense, Universitas Sumatera Utara, adalah sebagai berikut :
Dunia : Plantae
Divisio (Divisi) : Magnoliophyta (Spermatophyta)
Class (Kelas) : Magnoliospida (Dicotyledonae)
Ordo (Bangsa) : Ericales
Familia (Suku) : Actinidiaceae
Genus (Marga) : Saurauia
Spesies (Individu) : Saurauia vulcani Korth
Nama Daerah : Pirdot (Sumatera Utara)
Saurauia yang dikenal dengan nama cepcepan di daerah Kabupaten Karo merupakan tanaman kecil, perdu, tangkai daun menggugurkan daunnya setiap tahun, daun memiliki dua sisi yang berbeda bagian atas berwarna hijau bagian bawah berwarna coklat pucat, pangkal daun bertoreh dan berlekuk seperti jantung membulat telur sampai lonjong, ujung daun meruncing, tepi daun bergerigi, permukaan daun muda banyak memiliki bulu sesudah dewasa tidak berbulu, helai daun tebal dan kaku, bunga berbentuk cawan terletak pada ketiak daun, letak daun pada batang melingkar 3/4 , daun-daun pelindung membulat telur sampai lonjong meruncing, memiliki 5 tangkai kepala putik (Miquel, 1859).
Genus saurauia hidup pada daerah lembab atau daerah basah seperti dekat air terjun, aliran sungai, jurang, gunung yang lembab, daerah hutan hujan, hutan lumut, dan daerah yang berawan (mendung). Kebanyakan spesies hidup pada tanah yang berpasir, banyak humus, tanah liat, jarang terdapat pada batu (Soejarto, 1980). Daun pirdot digunakan sebagai obat luka dan diabetes dalam pengobatan tradisional (Adiastuti, 2007).
2.2 Seyawa Metabolit Sekunder
Senyawa metabolit sekunder merupakan biomolekul yang dapat digunakan sebagai lead compounds dalam penemuan dan pengembangan obat-obat baru (Atun,2003). Senyawa-senyawa kimia yang merupakan hasil metabolisme
sekunder pada tumbuhan sangat beragam dan dapat diklasifikasikan dalam beberapa golongan senyawa bahan alam yaitu alkaloid, flavonoid, terpenoid,
prekursor bagi sintesis obat baru atau prototipe obat beraktivitas tertentu (Rasyid,2012). Identifikasi ini merupakan uji fitokimia. Metode yang dilakukan merupakan metode uji berdasarkan yang telah dimodifikasi. Uji yang dilakukan antara lain uji flavonoid, senyawa fenolik, alkaloid, saponin, tanin dan terpenoid (Harbone, 1987).
2.2.1 Flavonoid
Flavanoid merupakan senyawa polar yang umunya mudah larut dalam pelarut polar yang umumnya mudah larut dalam pelarut polar seperti etanol, metanol, dan aseton (Markham, 1998).
Flavonoid merupakan golongan terbesar dari senyawa fenol, senyawa fenol mempunyai sifat efektif menghambat pertumbuhan virus, bakteri, dan jamur. Khunaifi (2010) menambahkan bahwa senyawa-senyawa flavonoid umumnya bersifat antioksidan banyak telah digunakan sebagai komponen bahan baku obat-obatan. Senyawa flavonoid dan turunannya memiliki dua fungsi fisiologi tertentu, yaitu sebagai bahan kimia untuk mengatasi serangan penyakit (sebagai antibakteri) dan anti virus bagi tanaman. Para peneliti lain juga menyatakan pendapat sehubungan dengan mekanisme kerja dari flavonoid dalam menghambat pertumbuhan bakteri,antara lain bahwa flavanoid terjadinya kerusakan permeabilitas dinding sel bakteri (Sabir, 2008). Flavonoida pada tumbuhan berfungsi dalam pengaturan fotosintesis, kerja antimikroba dan antivirus dan kerja
terhadap serangga (Robinson, 1995). Adapun fungsi flavonoida dalam kehidupan manusia yaitu sebagai stimulant pada jantung, hesperidin mempengaruhi pembuluh darah kapiler. Flavon terhidrolisasi bekerja sebagi diuretik dan antioksidan pada lemak (Sirait, 2007).
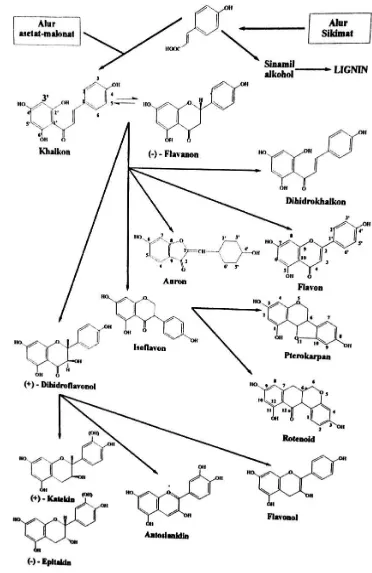
Kerangka dasar karbon pada flavonoid merupakan kombinasi antara jalur sikhimat dan jalur asetat-malonat yang merupakan dua jalur utama biosintesis cincin aromatik. Cincin A dari struktur flavonoid berasal dari jalur poliketida (jalurasetat-malonat), yaitu kondensasi tiga unit asetat atau malonat, sedangkan cincin B dan tiga atom karbon dari rantai propan berasal dari jalur fenil propanoid (jalur sikhimat) (Achmad, 1985).
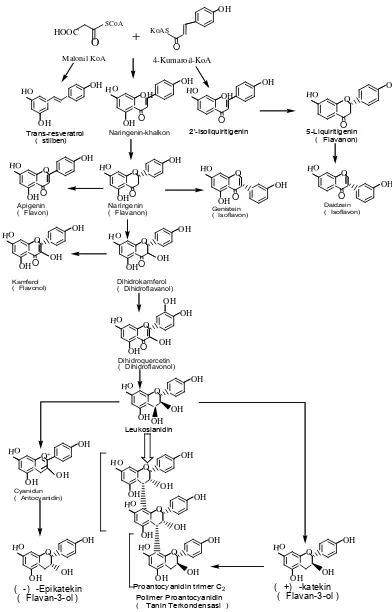
Markham (1988) menyatakan bahwa flavonoid pertama yang dihasilkan pada alur biosintesis flavonoid ialah khalkon, dan semua bentuk lain diturunkan darinya melalui berbagai alur (Gambar 2.2). Semua golongan flavonoid saling berkaitan, Karena berasal dari alur biosintesis yang sama. Cincin A terbentuk karena kondensasi ekor-kepala dari tiga unit asam asetat-malonat atau berasal dari jalur poliketida. Cincin B serta satu atau tiga atom karbon dari rantai propan yang merupakan kerangka dasar C6 – C3 berasal dari jalur asam sikimat (Manitto, 1981).
Berikut merupakan alur biosintesis flavonoid:
2.2.2 Alkaloid
Alkaloid merupakan senyawa kimia bersifat basa yang mengandung satu atau lebih atom nitrogen, umumnya tidak berwarna, dan berwarna jika mempunyai struktur kompleks dan bercincin aromatik. Alkaloid pada umumnya juga mempunyai kereaktifan fisiologi yang menonjol, sehingga oleh manusia alkaloida sering dimanfaatkan sebagai pengobatan. Secara kimia, alkaloid merupakan suatu golongan heterogen. Secara fisik, alkaloida dipisahkan dari kandungan tumbuhan lainnya sebagai garamnya dan sering diisolasi sebagai kristal hidroklorida atau pikrat (Harbone, 1987).
Alkaloid merupakan golongan zat tumbuhan sekunder yang terbesar. Alkaloid memiliki kemampuan sebagai antibakteri. Mekanisme yang diduga adalah dengan cara mengganggu komponen penyusun peptidoglikan pada sel bakteri,sehingga lapisan dinding sel terbentuk secara utuh dan menyebabkan kematian sel tersebut (Robinson, 1995).
Menurut Hegnauer, alkaloid dikelompokkan sebagai berikut : a. Alkaloid sesungguhnya
Alkaloid sesungguhnya adalah racun, senyawa tesebut menunjukkan aktivitas phisiologi yang luas, hampir tanpa terkecuali bersifat basa ; lazim menggunakan nitrogen dalam cincin heterosiklis, diturunkan dari asam amino, biasanya terdapat dalam tanaman sebagai garam basa organik. Beberapa perkecualian terhadap
aturan tersebut adalah kolkhisin dan asam aristolokhat yang bersifat bukan basa dan tidak memiliki cincin heterosiklis dan alkaloid kuartener yang bersifat agak asam.
b. Protoalkaloid
c. Pseudoalkaloida
Pseudoalkaloida tidak diturunkan dari prekursor asam amino. Senyawaini biasanya bersifat basa. Ada dua seri alkaloid yang penting dalam kelas ini, yaitu alkaloid stereoidal (contoh, konnesin) dan purin (contoh, kafein ) (Sastrohamidjojo, 1996).
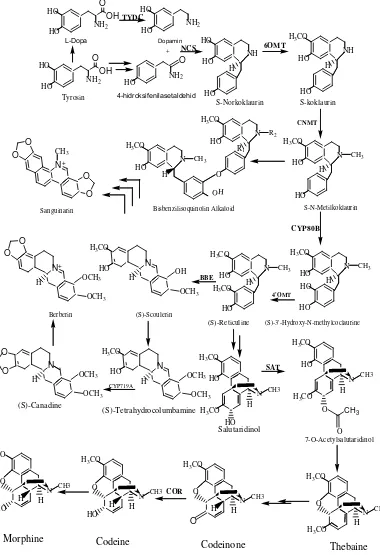
Biosintesis Benzylisoquinoline alkaloid dimulai dengan tahap
dekarboksilasi, orto-hidroksilasi dan deaminasi yang mengkonversi tirosin baik
dopamin dan 4-hidroksifenil acetaldehid (4-HPAA) (Gambar 2.3). Molekul klon
untuk senyawa aromatik asam dekarboksilase l-amino (TYDC) yang
mengkonversi tirosin dan dopa menjadi tirosin dan dopamin, masing-masing,
telah diisolasi. Kondensasi Norcoclaurine sintase (NCS) dengan dopamin dan
4-HPAA menghasilkan (S)-norcoclaurine, yang merupakan prekursor pusat untuk
semua benzylisoquinoline alkaloid pada tanaman. (S)-Norcoclaurine dikonversi
ke (S)-reticuline oleh 6-O-metiltransferase (6OMT), N-metiltransferase (CNMT),
hidroksilase P450 (CYP80B) dan 4-O-metiltransferase (4 OMT). Molekul klon
telah diisolasi untuk semua enzim yang terlibat dalam konversi (S)-norcoclaurine
ke (S)-reticuline, yang merupakan cabang-titik menengah dalam biosintesis
berbagai jenis benzylisoquinoline alkaloid. Intermediet dari jalur (S)-reticuline
juga berfungsi sebagai prekursor untuk lebih dari 270 dimer alkaloid
bisbenzylisoquinoline seperti (+)-Tubokurarin. Molekul klon untuk oksidasi P450
(CYP80A) dengan (R) N-metilcoclaurine ke (R) atau (S) N-metilcoclaurine untuk
menghasilkan bisbenzylisoquinoline alkaloid, yang masing-masing telah diisolasi
dari barberry (Berberis stolonifera). Banyak pekerjaan telah difokuskan pada jalur
cabang yang mengarah ke benzophenanthridine alkaloid, seperti sanguinarine,
alkaloid protoberberine, seperti berberin, dan morphinan alkaloid , seperti morfin .
Sebagian besar enzim yang terlibat dalam jalur ini , dimana ada lima enzim sesuai
dengan molekul klon , telah diisolasi ( Gambar 2.3 ) . Langkah pertama yang
dilakukan dalam biosintesis benzophenanthridine dan protoberberine alkaloid
melibatkan konversi (S)-reticuline ke (S)-scoulerine oleh jembatan enzim
berberin (BBE) . (S)-Scoulerine dapat dikonversi ke (S)-stylopine oleh dua
oksidase P450 . Setelah N-metilasi (S)-stylopine oleh metiltransferase tertentu,
dihydrosanguinarine, yang teroksidasi untuk menghasilkan sanguinarine. Eksudat
dari banyak sepsis Papaveraceae, seperti Sanguinaria Canadensis dan Eschsholzia
californica, berwarna merah karena akumulasi sanguinarine dan alkaloid
benzophenanthridine lainnya. Dalam beberapa tanaman, terutama berberidaceae
dan Ranunculaceae, (S)-scoulerine termetilasi oleh SAM
scoulerine-9-O-metiltransferase (SOMT) untuk menghasilkan (S)-tetrahydrocolumbamine
(Gambar2.3). Molekuler Klon untuk SOMT dan P450 (S)-synthase canadine
(CYP719A), yang mengubah (S)-tetrahydrocolumbamine ke (S)-canadine, telah
diisolasi. (S)-Canadine teroksidasi untuk menghasilkan berberin. Pada beberapa
spesies papaver, (S)-reticuline yang epimeris ke (R)-reticuline sebagai langkah
pertama dalam biosintesis alkaloid morphina. Selanjutnya, (R)-reticuline diubah
dalam dua langkah ke (7S)-salutaridinol oleh enzim P450 dan sebuah oksidoreduk
tase NADPH. Morphina alkaloid tebain dihasilkan dari (7S)-salutaridinol melalui
asetil koenzim A: salutaridinol-7-O-asetiltransferase (SAT). Tebain diubah
menjadi codeinone, dengan mereduksi codeine oleh enzim NADPH
codeinnonereduktase (COR). Molekuler SAT dan COR telah diisolasi dari opium
poppy. Tahap ahir, kodein demetilasi untuk menghasilkan morfin (Crozier et al,
Berikut merupakan alur biosintesis dari alkaloid :
2.2.3 Terpenoid
Terpenoid adalah senyawa alam yang terbentuk dengan proses biosintesis, terdistribusi luas dalam dunia tumbuhan dan hewan. Terpenoid ditemui tidak saja pada tumbuhan tingkat tinggi namun juga pada terumbu karang dan mikroba. Struktur terpenoid dibangun oleh molekul isoprena, CH2=C(CH3)-CH=CH2,
kerangka terpenoid terbentuk dari dua atau lebih banyak satuan unit isoprena (C5).
Terpenoid yang disebut juga isoprenoid, diklasifikasikan atas jumlah unit isoprena yang membangunnya, dengan demikian ada yang terdiri atas dua (C10), tiga (C15),
empat (C20), enam (C30), atau delapan (C40) isoprena. Terpenoid dapat juga
dikelompokkan menjadi monoterpen, seskuiterpen, diterpen, triterpen dan tetraterpen. Senyawa terpenoid berkisar dari senyawa volatil, yaitu komponen minyak atsiri, yang merupakan mono dan seskuiterpen (C10 dan C15), senyawa
yang kurang volatil, yakni diterpen (C20), sampai senyawa nonvolatil seperti
triterpenoid dan sterol (C30) seperti karatenoid (Sirait, 2007).
Beberapa hasil penelitian menunjukkan bahwa senyawa terpenoid dapat menghambat pertumbuhan dengan mengganggu proses terbentuknya membran dan atau dinding sel,membran atau dinding sel tidak terbentuk atau terbentuk tidak sempurna (Ajizah, 2004).
Berbagai macam aktivitas fisiologi yang menarik ditunjukkan oleh beberapa
Secara umum biosintesa terpenoida terjadinya dengan 3 tahap reaksi dasar yaitu:
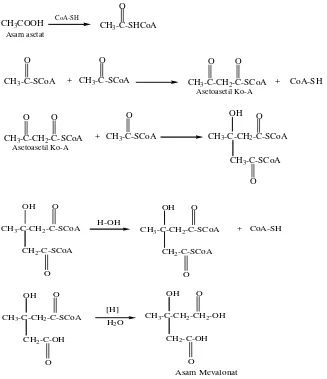
1. Pembentukan isoprena aktif berasal dari asam asetat melalui asam mevalonat. Asam asetat setelah diaktifkan oleh koenzim A (Ko-A) melakukan kondensasi jenis Claisen menghasilkan Asetoasetil Ko-A. Senyawa ini dengan Asetil Ko-A melakukan kondensasi jenis Aldol menghasilkan rantai karbon bercabang sebagaimana ditemukan pada asam mevalonat yang terlihat pada gambar 2.4 (Pinder,1960).
Gambar 2.4 Pembentukan Asam Mevalonat (Pinder, 1960)
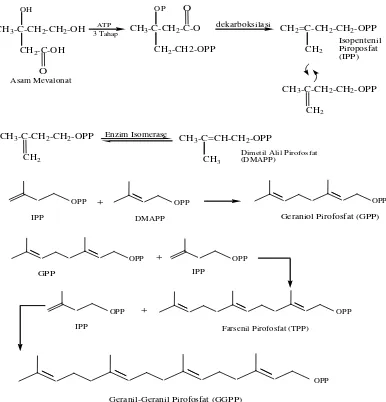
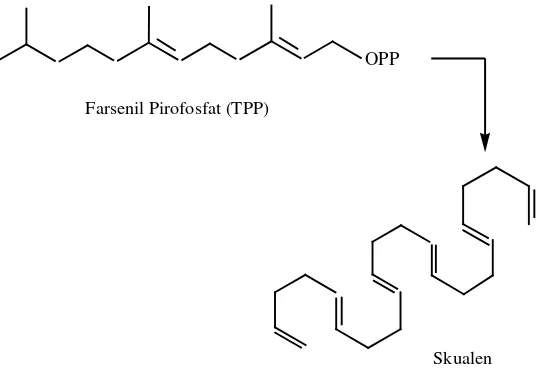
2. Penggabungan kepala dan ekor dua unit isoprena akan membentuk mono-, seskui-, di-, sester-, dan poli- terpenoida.
Penggabungan ini terjadi karena serangan elektron dari ikatan rangkap IPP terhadap atom karbon dari DMAPP yang kekurangan elektron diikuti oleh penyingkiran ion pirofosfat mengasilkan Geranil Pirofosfat (GPP) yaitu senyawa antarsemua senyawa monoterpenoida. Penggabungan selanjutnya antara satu unit IPP dan GPP dengan mekanisme yang sama menghasilkan Farnesil Pirofosfat (FPP) yang merupakan senyawa antara bagi semua senyawa seskuiterpenoida. Senyawa diterpenoida diturunkan dari Geranil – Geranil Pirofosfat (GGPP) yang berasal dari kondensasi antara satu unit IPP dan GPP dengan mekanisme yang sama terlihat pada gambar 2.5 (Pinder, 1960).
+
IPP Farsenil Pirofosfat (TPP)
Geranil-Geranil Pirofosfat (GGPP)
OPP OPP
3. Penggabungan ekor dan ekor dari unit C15 atau unit C20 menghasilkan
triterpenoida dan steroida.
Triterpenoida (C30) dan tetraterpenoida (C40) berasal dari dimerisasi C15 atau C20
dan bukan dari polimerisasi terus-menerus dari unit C5. Yang banyak diketahui
ialah dimerisasi FPP menjadi skualena yang merupakan triterpenoida dasar dan sumber dari triterpenoida lainnya dan steroida yang terlihat pada gambar 2.6. Siklisasi dari skualena menghasilkan tetrasiklis triterpenoida lanosterol ( Pinder, 1960).
Farsenil Pirofosfat (TPP)
OPP
Skualen
Gambar 2.6 Pembentukan Skualen (Triterpenoida Dasar) (Pinder, 1960)
2.2.4 Saponin
Saponin merupakan glukosida yang larut dalam air dan etanol,tetapi tidak larut dalam eter. Saponin bekerja sebagai antibakteri dengan mengganggu stabilitas membran sel bakteri sehingga menyebabkan sel bakterilisis,jadi mekanisme kerja saponin termasuk dalam kelompok antibakteri yang mengganggu pemeabilitas membran sel bakteri, yang mengakibatkan kerusakan membran sel dan
menyebabkan keluarnya berbagai kompone penting dari dalam sel bakteri yaitu protein, asam nukleat dan nukleotida (Ganiswarna,1995).
2.2.5 Tanin
Tanin merupakan salah satu metabolit sekunder yang dapat digunakan tumbuhan untuk melindungi dari serangan bakteri dari cendawan (Salisbury, 1995).
Apabila tanin direaksikan dengan air membentuk larutan koloid yang memberikan reaksi asam dan reaksi yang tajam (Harborne, 1996). Tanin memiliki peranan fisiologis yang kompleks mulai dari pengendap protein hingga pengkhelat logam. Tanin juga dapat berfungsi sebagai antioksidan biologis (Hagerman, 2002).
Secara kimia terdapat dua jenis tanin yang tersebar tidak merata dalam dunia tumbuhan yaitu tanin terkondensasi (Proantosianidin) dan tanin terhidrolisis (Hydrolyzable tannin) (Harbone, 1987). Kedua golongan tanin menunjukkan reaksi yang berbeda dalam larutan garam Fe (III). Tanin terkondensasi menghasilkan warna hijau kehitaman sedangkan tanin terhidrolisis memberikan biru kehitamanan.
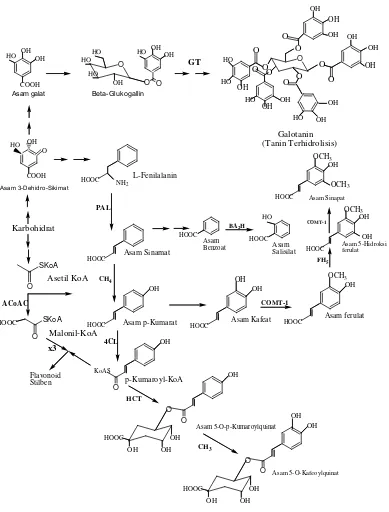
1. Tanin terhidrolisis
Tanin terhidrolisis biasanya berupa senyawa amorf, higrokopis, berwarna coklat kuning yang larut dalam air (terutama air panas) membentuk larutan koloid bukan larutan sebenarnya. Makin murni tanin, makin kurang kelarutannya dalam air dan makin mudah diperoleh dalam bentuk kristal. Tanin ini larut dalam pelarut organik yang polar, tetapi tidak larut dalam pelarut organik nonpolar seperti benzene atau kloroform (Robinson, 1995).Tanin ini biasanya berikatan dengan karbohidrat dengan membentuk jembatan oksigen, maka dari itu tanin ini dapat dihidrolisis dengan menggunakan asam sulfat atau asam klorida (Hagerman, 2002). Salah satu contoh jenis tanin ini adalah galotanin yang merupakan senyawa
HO
Gambar 2.7 Biosintesis Galotanin (Crozieret al, 2006)
2. Tanin terkondensasi
HOOC
( Flavon) Naringenin( Flavanon) Genistein( Isoflavon)
Daidzein
( Flavonol) Dihidrokamferol( Dihidroflavanol)
O
Proantocyanidin trimer C2
( -) -Epikatekin ( Flavan-3-ol )
( +) -katekin ( Flavan-3-ol )
Polimer Proantocyanidin ( Tanin Terkondensasi )
2.3 Ekstraksi
Ekstrak adalah sediaan pekat yang diperoleh dengan mengekstraksi zat aktif dari simplisia nabati dan simplisia hewani menggunakan pelarut yang sesuai, kemudian semua atau hampir semua pelarut diuapkan dan massa atau serbuk yangtersisa diperlakukan sedemikian hingga memenuhi baku yang ditetapkan. Ekstraksi adalah suatu proses pemisahan kandungan senyawa kimia dari jaringan tumbuhan atau hewan dengan menggunakan penyari tertentu (Depkes RI, 2000).
Berdasarkan prinsipnya, proses ekstraksi dapat berlangsung bila terdapat kesamaan dalam sifat kepolaran antara senyawa yang diekstraksi dengan senyawa pelarut. Suatu zat memiliki kemampuan terlarut yang berbeda dalam pelarut yang berbeda. Hal ini menunjukkan adanya interaksi antara zat terlarut dengan pelarut. Senyawa polar akan larut dalam pelarut polar, begitu juga sebaliknya. Sifat penting yang harus diperhatikan dalam pemilihan pelarut adalah kepolaran senyawa yang dilihat dari gugus polarnya (seperti OH, COOH, dan lain sebagainya). Hal ini yang perlu diperhatikan dalam pemilihan pelarut adalah selektivitas, kemampuan untuk mengekstrak, toksisitas, kemudahan untuk diuapkan, dan harga (Harbone, 1987).
Metode ekstraksi dengan menggunakan pelarut dapat dilakukan dengan beberapa cara :
1. Maserasi
2. Perkolasi
Perkolasi berasal dari kata “colore”artinya menyerkai dan “per”artinya menembus. Dengan demikian,perkolasi adalah suatu cara penarikan simplisia dengan menggunakan alat yang disebut perkolator dimana simplisia terendam dalam cairan penyari, zat-zat akan terlarut dan larutan tersebut akan menetes secara beraturan (Syamsuni,2006). Prosesnya terdiri dari tahapan pengembangan bahan, tahap perendaman antara, tahap perkolasi sebenarnya (penetesan/penampungan perkolat) sampai diperoleh ekstrak (Depkes,2000). Keuntungan dari metode perkolasi ini adalah proses penarikan zat berkhasiat dari tumbuhan lebih sempurna,sedangkan kerugiannya adalah membutuhkan waktu yang lama dan peralatan yang digunakan mahal (Agoes,2007).
3. Refluks
Refluks adalah ekstraksi dengan pelarut pada temperatur titik didihnya, selama waktu tertentu dan pelarut akan terdestilasi menuju pendingin dan akan kembali ke labu (Depkes,2000).
4. Sokletasi
Sokletasi adalah ekstraksi kontinu menggunakan alat soklet,dimana pelarut akan terdestilasi dari labu menuju pendingin,kemudian jatuh membasahi dan merendam sampel yang mengisi bagian tengah alat soklet setelah pelarut mencapau tinggi
tertentu maka akan tirin ke labu destilasi, demikian berulang-ulang (Depkes,2000).
5.Infudasi
Infus adalah ekstraksi dengan pelarut air pada temperatur penangas air atau bejana infus tercelup dalam penangas air mendidih pada temperatur 96 o C selama 15-20 menit (Depkes,2000).
6.Dekoktasi
2.4 Radikal bebas
Radikal bebas adalah atom atau senyawa yang kehilangan pasangan elektronnya (Kumalaningsih, 2006). Radikal bebas adalah atom atau molekul yang tidak stabil dan sangat reaktif karena mengandung satu atau lebih elektron tidak berpasangan pada orbital terluarnya. Untuk mencapai kestabilan atom atau molekul, radikal bebas akan bereaksi dengan molekul di sekitarnya untuk memperoleh pasangan elektron (Maulida, 2010). Radikal bebas dapat dihasilkan dari metabolisme tubuh sendiri, dan bisa pula lewat eksternal seperti lingkungan sekitar kita (Iswari, 2011).
Rangkaian reaksi yang membentuk radikal bebes dapat dibagi menjadi tiga langkah yang berbeda yaitu inisiasi, propagasi, terminasi. Inisiasi adalah proses awal dimana jenis radikal tertentu akan bereaksi dengan asam lemak dalam tubuh membentuk radikal alkil (R•).
Tahap selanjutnya propagasi dimana radikal alkil dapat bereaksi dengan oksigen menghasilkan radikal peroksil (ROO•) kemudian radikal peroksil selanjutnya bereaksi dengan asam lemak tubuh membentuk peroksida lipid (ROOH)dan radikal alkil (R•). Pada tahap terminasi radikal peroksil dapat bereaksi dengan sesama peroksil menghasilkan senyawa yang tidak bersifat radikal, radikal alkil juga dapat bereaksi dengan sesamanya membentuk senyawa yang tidak radikal,
peroksil dapat bereaksi dengan alkoksil membentuk senyawa yang tidak radikal.
Berikut gambaran rangkaian pembentukan radikal bebas dalam tubuh:
1. Inisiasi
X•+ RH R• + X H
2. Propagasi
R• + O2 ROO•
3. Terminasi
ROȮ• + ROO• ROOR non radikal
ROO•+ R• ROOR non radikal
R• + R• R 2 non radikal
Keterangan:
R• : Radikal Alkil
ROOH : Lipid Peroksida
ROO• : Radikal Peroksida
X• : Jenis Radikal Bebas
RH : Asam Lemak Dalam Tubuh
(Cui K et al, 2004,di dalam Roking,2007).
2.5 Antioksidan
Antioksidan adalah senyawa yang mempunyai struktur molekul yang dapat memberikan elektronnya kepada molekul radikal bebas dan dapat memutus reaksi berantai dari radikal bebas (Kumalaningsih, 2006).
Ciri utama senyawa antioksidan adalah kemampuannya dalam meredam radikal bebas. Radikal bebas merupakan senyawa yang mengandung elektron tidak berpasangan yang bertindak sebagai akseptor elektron. Radikal bebas ini berbahaya karena sangat reaktif mencari pasangan elektronnya. Radikal bebas ini memerlukan elektron yang berasal dari pasangan elektron molekul sekitarnya.
menyebabkan atom atau molekul sangat terpengaruh oleh medan magnet. Energi untuk memutuskan ikatan kovalen berasal dari panas, radiasi elektromagnetik atau reaksi redoks berlebihan. Hilang atau bertambahnya satu elektron pada molekul lain menyebabkan terjadinya radikal bebas baru dan mengakibatkan perubahan dramatis secara fisik dan kimiawi dalam tubuh manusia. Mula-mula diransang (initiation) terjadinya radikal bebas, kemudian radikal bebas cenderung bertambah banyak membentuk (propagasi) rantai reaksi dengan molekul lain. Senyawa reaksi berantai ini mempunyai massa paruh yang lebih panjang dan potensial menyebabkan kerusakan sel. Fase inisiasi dan propagasi dapat dinetralisir oleh antioksidan yang berasal dari endogen dan eksogen (Kosasih, 2004).
Menurut Kosasih (2004), antioksidan tubuh dikelompokkan menjadi tiga yaitu : 1. Antioksidan primer yang berfungsi untuk mencegah pembentuk senyawa
radikal baru karena dapat merubah radikal bebas yang ada menjadi molekul yang berkurang dampak negatifnya, sebelum radikal bebas ini sempat bereaksi.
Contoh : enzim superoksida dismutase (SOD) yang berfungsi sebagai pelindung hancurnya sel-sel dalam tubuh karena radikal bebas.
2. Antioksidan sekunder adalah senyawa yang berfungsi menangkap senyawa serta mencegah terjadinya reaksi berantai.
Contoh: Vitamin E, C dan beta karoten yang diperoleh dari berbagai buah.
3. Antioksidan tersier adalah senyawa yang memperbaiki kerusakan sel-sel dan jaringan yang disebabkan radikal bebas.
Berdasarkan sumbernya antioksidan terbagi atas,yaitu : a. Antioksidan alami
Merupakan antioksidan yang merupakan hasil dari ekstraksi bahan alami. Antioksidan alami dalam makanan dapat berasal dari senyawa antioksidan yang sudah ada dari 1 atau 2 komponen makanan, senyawa antioksidan yang terbentuk dari reaksi-reaksi selama proses pengolahan, senyawa antioksidan yang diisolasi dari sumber alami dan ditambahkan ke makanan sebagai bahan tambahan pangan.
b. Antioksidan sintetik
Adalah antioksidan yang diperoleh dari hasil reaksi kimia. Contoh antioksidan sintetik yang diijinkan untuk makanan dan sering digunakan, yaitu butil hidroksi anisol (BHA), butil hidroksi toluen (BHT), propil galat, tert-butil hidroksi quinon (TBHQ), dan tokoferol. Antioksidan-antioksidan tersebut merupakan antioksidan alami yang telah diproduksi secara sintesis untuk tujuan komersial.
Pengukuran aktivitas antioksidan dapat dilakukan dengan beberapa metode yaitu:
1. Metode DPPH (2,2-diphenyl-1-pikril-hydrazyl)
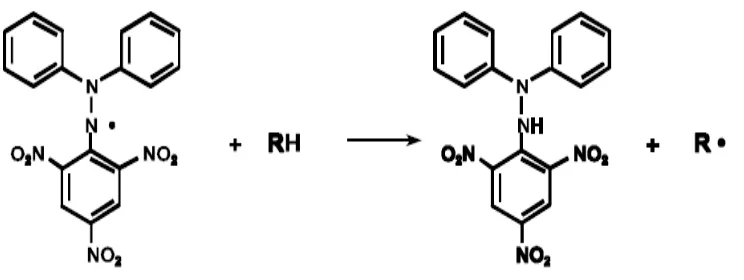
DPPH merupakan suatu radikal bebas yang stabil karena mekanisme delokalisasi elektron bebas oleh molekulnya, sehingga molekul ini tidak mengalami reaksi dimerisasi yang sering terjadi pada sebagian besar radikal bebas lainnya. Delokalisasi juga memberikan efek warna ungu pada panjang gelombang 517 nm dalam pelarut etanol (Hirota et al, 2000). DPPH sering digunakan sebagai salah
Pengukuran aktivitas antioksidan dilakukan dengan inkubasi DPPH dengan ekstrak selama 30 menit sehingga menghasilkan larutan ungu yang lebih memudar kemudian dilakukan pengukuran panjang gelombang pada 517 nm (Mosquera, 2007).
Gambar 2.9 Mekanisme Penghambatan Radikal DPPH
Hasil dari metode DPPH umumnya dibuat dalam bentuk IC50 (Inhibitor
Concentration 50), yang didefinisikan sebagai konsentrasi larutan substrat atau sampel yang akan menyebabkan tereduksi aktivitas DPPH sebesar 50%. Semakin besar aktivitas antioksidan makan nilai IC50 akan semakin kecil. Suatu senyawa
antioksidan dinyatakan baik jika nilai IC50-nya semakin kecil (Molyneux, 2004).
3. Metode FRAP (Ferric Reducing Antioxidant Power)
Pengujian aktivitas antioksidan dengan metode FRAP (Ferric Reducing Antioxidant Power) didasarkan atas kemampuan senyawa antioksidan dalam mereduksi senyawa besi(III)-tripridil-triazin menjadi besi(II)-tripiridil triazin pada pH 3,6. Pengukuran FRAP memberikan urutan respon yang samadengan metode
CUPRAC. Namun hasilnyamenunjukkan aktivitas yang lebih kecildibandingkan dengan data pengujianCUPRAC ataupun DPPH. Hal ini didugakarena larutan FRAP bersifat kurang stabilsehingga harus dibuat secara in time dan harussegera dipergunakan (Widyastuti, 2010). Reaksinya sebagai berikut :
Menurut Ou et al. (2002), pengukuranantioksidan dengan metode FRAP dapatberjalan akurat apabila dilakukan padasenyawaan antioksidan yang bisa mereduksiFe(III)TPTZ pada kodisi reaksi secaratermodinamika dan memiliki laju reaksi yangcukup cepat. Selain itu, antioksidan yangteroksidasi dan semua produk reaksisekundernya harus tidak memiliki serapanmaksimum pada absorbansi 598 nm atauserapan Fe(II)TPTZ (Widyastuti, 2010).
4. Metode CUPRAC (Cupric Ion Reducing Antioxidant Capacity)
Prinsip dari uji CUPRAC (Cupric Ion Reducing Antioxidant Capasity) adalah pembentukan kelat oleh bis (neukropin) besi (II) menggunakan pereaksi redoks kromogenik pada pH 7. Absorbansi dari pembentukan kelat Cu(I) merupakan hasil reaksi redoks dengan mereduksi polifenol yang diukur pada panjang gelombang 450 nm. Untuk spektrum Cu(I) Ne diperoleh dengan mereaksikan asam askorbat berbagai konsentrasi reagen, pH dan waktu oksidasi pada suhu kamar dan peningkatan suhu pada percobaan dapat berasal dari sumber lain.
Reaksinya sebagai berikut :
nCu(Nc)22+ + AR(OH)n nCu(Nc)2+ + AR(=O)n + nH+
Kelebihan dari metode CUPRAC adalah pereaksi yang digunakan cukup cepat bekerja, selektif, lebih stabil, mudah didapatkan dan mudah untuk diaplikasikan (Erawati, 2002).
Beberapa nilai IC50 untuk senyawa antioksidan (mg/mL): :
Asam askorbat :1,96+/-0,013 Alpa-tokoferol :7,3+/-0,308 Sayur-sayuran :4,7
2.6 Spektrofotometri UV-Vis
Spektrofotometer adalah alat yang terdiri dari spektometer dan fotometer. Spektrometer menghasilkan sinar dari spektrum dengan panjang gelombang tertentu dan fotometer adalah alat pengukur intensitas cahaya yang ditransmisikan atau yang diabsorpsi. Jadi spektrofotometer digunakan untuk mengukur energi secara relatif jika energi tersebut ditransmisikan, direfleksikan atau diemisikan sebagai fungsi dari panjang gelombang. Kelebihan spektrometer dibandingkan fotometer adalah panjang gelombang dari sinar putih dapat lebih terseleksi yang diperoleh dengan alat pengurai seperti prisma, grating ataupun celah optis (Khopkar, 2007).
Spektrofotometer UV-Vis adalah pengukuran panjang gelombang dan intensitas sinar ultraviolet dan cahaya tampak yang diabsorpsi oleh sampel. Sinar ultraviolet dan cahaya tampak memiliki energi yang cukup untuk mempromosikan elektron pada kulit terluar ke tingkat energi yang lebih tinggi. Spektroskopi UV-Vis biasanya digunakan untuk molekul atau ion anorganik atau kompleks di dalam larutan. Spektrum UV-Vis mempunyai bentuk yang lebar dan hanya sedikit informasi tentang struktur yang bisa didapatkan dari spektrum ini. Tetapi spektrum ini sangat berguna untuk pengukuran secara kuantitatif. Konsentrasi dari analit di dalam larutan bisa ditentukan dengan mengukur absorban pada panjang gelombang tertentu dengan menggunakan hukum Lambert-Berr. Sinar ultraviolet berada pada panjang gelombang 200-400 nm sedangkan sinar tampak berada pada
panjang gelombang 400-800 nm (Rohman, 2007).
2.7Bakteri
Bakteri adalah mikroorganisme bersel tunggal yang tidak terlihat oleh mata,tetapi dapat dilihat dengan bantuan mikroskop. Ukuran bakteri berkisar antara panjang 0,5 sampai 10µ dan lebar 0,5 sampai 2,5µ (µ = 1 mikron = 0,001mm) tergantung dari jenisnya. Bakteri terdapat secara luas dilingkungan alam yang berhubungan dangan hewan,udara,air dan tanah. Bakteri berkembang biak secara aseksual yaitu dengan proses pembelahan diri menjadi dua (Buckle, 2007).
Mikroorganisme memang peranan penting dalam menganalisis sistem enzim dan dalam mengalisis komposisi suatu makanan. Bakteri merupakan organisme yang sangat kecil (berukuran mikroskopis). Bakteri rata-rata berukuran lebar 0,5 – 1 mikron dan panjang hingga 10 mikron (1 mikron - 103mm). Untuk melihat
bakteri dengan jelas, tubuhnya perlu diisi dengan zat warna, pewarna ini disebut pengecatan bakteri.
Cat yang umum dipakai adalah cat Gram. Diantara bermacam-macam bakteri yang dicat,ada yang dapat menahan zat warna ungu dalam tubuhnya meskipun telah didekolorisasi dengan alkohol dan aseton. Dengan demikian tubuh bakteri itu tetap berwarna ungu meskipun disertai dengan pengecatan oleh zat warna kontras,warna ungu itu tetap dipertahankan. Bakteri yang memberikan reaksi semacam ini dinamakn bakteri Gram positif. Sebaliknya,bakteri yang tidak dapat menahan zat warna setelah didekolorisasi dengan alkohol akan kembali menjadi tidak berwarna dan bila diberikan pengecatan dengan zat warna kontras,akan berwarna sesuai dengan zat warna kontras. Bakteri yang memperlihatkan reaksi semacam ini dinamakan bakteri Gram negatif (Irianto,
2006).
Kelompok mikroorganisme yang paling penting dan beraneka ragam, yang
Berdasarkan perbedaan respons terhadap prosedur pewarnaan gram dan strktur dinding bakteri, bakteri diklasifikasikan menjadi bakteri gram negatif dan bakteri gram positif.
2.7.1 Bakteri gram positif
Bakteri gram positif lebih sensitif terhadap penisilin, tetapi lebih tahan terhadap perlakuan fisik dibandingkan bakteri gram negatif. Bakteri gram positif sering berubah sifat pewarnaannya sehingga menunjukkan reaksi gram variabel. Sebagai contoh, kultur gram positif yang sudah tua dapat kehilangan kemampuannya untuk menyerap pewarna violet kristal sehingga dapat berwarna merah seperti bakteri gram negatif. Perubahan tersebut dapat juga disebabkan oleh perubahan kondisi lingkungan atau modifikasi teknik pewarnaan (Fardiaz, 1992). Ciri-cirinya:
• Dinding sel mengandung peptidoglikan yang tebal serta diikuti pula dengan adanya ikatan benang-benang teichoic dan teichoronic acid
• Pada umunya berbentuk bulat (coccus)
• Pada perwarnaan gram, bakteri jenis ini berikatan dengan zat warna utama
yaitu gentian violet dan tidak luntur bila dicelupkan kedalam larutan alkohol
• Dibawah mikroskop tampak berwarna ungu (Nasution, 2014).
Contoh dari bakteri gram positif : a. Staphylococcus ureus
Staphylococcus aureus merupakan bakteri Gram positif berbentuk bulat berdiameter 0,7-1,2 µm,tersusun dalam kelompok-kelompok yang tidak teratur seperti buah anggur,fakultatif anaerob,tidak membentuk spora,dan tidak bergerak . Bakteri ini tumbuh pada suhu optimum 37 ̊C,tetapi membentuk pigmen paling baik pada suhu kamar (20-25 ̊C) (Jawetz et al,1994).
fagositosis), menghasilkan pigmen kuning dan mungkin memproduksi eksotoksin Staphylococcus aureus berdiam di mukosa hidung manusia atau di kulit; kuman ini menyebar melalui tangan, bersin dan lesi kulit (Hawley, 2003). Gambar bakteri Staphylococcus aureus dapat dilihat pada gambar 2.10 dibawah ini:
Gambar 2.10 Bakteri Staphylococcus aureus
Penyakit yang disebabkan oleh bakteri Staphylococcus aureus terdiri atas empat jenis :Keracunan makanan Staphylococcus aureus dari enterotoksin stabil terhadap panas yang terjadi akibat makanan yang kurang mendapat pendinginan dan tercemar oleh Staphylococcus aureus (misal, ham, daging yang diasinkan atau dikalengkan, kue custard, atau salad kentang). Ingesti toksin menyebabkan nyeri abdomen, muntah dan diare dengan onset cepat (1-6 jam) dan Infeksi kulit atau subkutis yang disebabkan oleh Staphylococcus aureus sering muncul sebagai nyeri dan panas, kemerahan dan pembengkakan subkutis. Infeksi dapat menyebabkan penyakit kulit eksfoliativa (scalded skin syndrome) bila strainnya menghasilkan eksofoliatin. (Hawley, 2003).
b. Staphylococcus epidermidis
Staphylococcus epidermidis adalah salah satu spesies bakteri dari genus staphylococcus yang diketahui dapat menyebabkan infeksi oportunistik (menyerang individu dengan system kekebalan tubuh yang lemah) ( Jodi, 2008).Beberapa karakteristik bakteri ini adalah fakultatif, koagulase negatif, katalase positif, gram-positif,berbentuk kokus,dan berdiameter 0,5-1,5 µm ( Lisa,
1998). Bakteri ini secara alami hidup pada kulit dan membran mukosa manusia.Infeksi S.epidermidis dapat terjadi karena bakteri ini membentuk biofilm
2.7.2 Bakteri gram negatif
Bakteri gram negatif lebih sensitif terhadap antibiotik lainnya seperti streptomisin dan bersifat lebih konstan terhadap reaksi pewarnaan (Fardiaz, 1992). Dinding sel bakteri gram negatif tersusun atas satu lapisan peptidoglikan dan membran luar. Dinding selnya tidak mengandung teichoic acid. Membran luar terususun atas lipopolisakarida, lipoprotein dan pospolipid (Tortora, 2001). Ciri-cirinya:
• Mengandung sedikit sekali peptidoglikan dan tidak terdapat ikatan
benang-benang teichoic acid dan teichoronic acid
• Pada umunya berbentuk batang (basil) kecuali basillus antharias dan
basillus sereus
• Pada pewarnaan gram, bakteri jenis ini tidak mampu berikatan dengan zat
warna utama yaitu gentian violet dan luntur bila dicelupkan kedalam larutan alkohol
• Dibawah mikroskop tampak berwarna merah (Nasution, 2014).
Contoh bakteri gram negatif :
a. Escherichia coli
Escherichia berbatang pendek.Habitat utamanya adalah usus manusia dan hewan. Escherichia coli dipakai sebagai organism indikator, karena jika terdapat dalam jumlah yang banyak menunjukkan bahwa pangan atau air telah mengalami pencemaran (Gaman, 1992).
b. Salmonella thypi
S. Typhi memiliki keunikan hanya menyerang manusia, dan tidak ada inang lain. Infeksi salmonella dapat berakibat fatal kepada bayi, balita, ibu hamil dan kandungannya serta orang lanjut usia. Hal ini disebabkan karena kekebalan tubuh mereka yang menurun (Taylor, 1970).
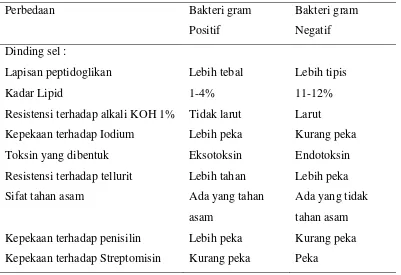
Beberapa perbedaan sifat yang dapat dijumpai antara bakteri gram positif dan bakteri gram negatif adalah sebagai berikut :
Tabel 2.1 Perbedaan bakteri gram positif dan gram negatif :
Perbedaan Bakteri gram
Positif
Bakteri gram Negatif
Dinding sel :
Lapisan peptidoglikan Lebih tebal Lebih tipis
Kadar Lipid 1-4% 11-12%
Resistensi terhadap alkali KOH 1% Tidak larut Larut
Kepekaan terhadap Iodium Lebih peka Kurang peka Toksin yang dibentuk Eksotoksin Endotoksin Resistensi terhadap tellurit Lebih tahan Lebih peka Sifat tahan asam Ada yang tahan
asam
Ada yang tidak tahan asam Kepekaan terhadap penisilin Lebih peka Kurang peka Kepekaan terhadap Streptomisin Kurang peka Peka
(Syahrurachaman, dkk., 1993).
2.7.3 Pengukuran Aktivitas Antimikroba
Metode-metode utama yang dapat digunakan adalah : a.Metode Dilusi
Sejumlah antimikroba dimasukkan kedalam medium bakteriologi padat atau cair. Biasanya digunakan pengenceran dua kali lipat zat antimikroba. Medium akhirnya diinokulasikan dengan bakteri yang diuji dan diinokulasi. Tujuan akhirnya adalah mengetahui seberapa banyak jumlah antimikroba yang diperlukan untuk menghambat pertumbuhan atau membunuh bakteri yang diuji. Uji kerentanan dilusi agar membutuhkan waktu yang lama.
b. Metode Difusi
Metode yang paling sering digunakan adalah metode difusi agar dengan menggunakan cakram kertas, cakram kaca, pencetak lubang. Prinsip metode ini adalah mengukur zona hambatan pertumbuhan bakteri yang terjadi akibat difusi zat yang bersifat antibakteri di dalam media padat melalui pencadang. Daerah hambatan pertumbuhan bakteri adalah daerah jernih disekitar cakram. Luas daerah hambatan berbanding lurus dengan aktivitas antibakteri, semakin kuat daya aktivitas antibakterinya maka semakin luas daerah hambatnya. Metode ini dipengaruhi oleh banyak faktor fisik dan kimia, misalnya : pH, suhu, zat inhibitor, sifat dari media dan kemampuan difusi, ukuran molekul dan stabilitas dari bahan obat (Jawetz et al, 1996).
2.7.4 Mekanisme Kerja Antibakteri a. Inhibitor Sintesis Dinding Sel
b. Inhibitor Fungsi Membran sel
Biasanya merupakan senyawa yang bekerja langsung pada membran sel mikroorganisme, mempengaruhi permeabilitas dan menyebabkan kebocoran senyawa-senyawa intraseluler. Dalam hal ini termasuk senyawa yang bersifat detergen seperti polimiksin dan amfoterisin B yang berikatan dengan sterl-sterol dinding sel (Chamber, 2007). Kerusakan membran sel akan mengakibatkan keluarnya berbagai komponen penting dalam sel bakteri yaitu protein, asam nukleat dan lain-lain (Setiabudi, 1995).
c. Inhibitor Sintesis Protein Sel
Unit ribosom pada bakteri adalah 30S dan 50S. Sintesis protein dihambat dengan mempengaruhi fungsi subunit ribosom 30S dan 50S sehingga menyebabkan penghambatan sintesis protein yang reversibel dan mengakibatkan kematian sel. Obat bakteriostatik ini meliputi kloramfenikol, golongan tetrasiklin, eritromisin, dan klindamisin (Setiabudi, 1995).
d. Inhibitor Sintesis Asam nukleat
Antibakteri yang tergolong dalam kelompok ini adalah golongan kuinolon dan rifampin. Dalam hal ini, derivat rifampin akan berikatan dengan enzim polimerisasi-RNA (pada sub unit) sehingga menghambat sintesis RNA oleh enzim
tersebut. Sementara asam nalidiksat bekerja dnegan mengganggu sintesin DNA (Bilbiana, 1992).
e. Inhibitor Metabolisme Sel Bakteri