RINGKASAN/RANGKUMAN LAPORAN PRAKTIKUM KIMIA ORGANIK RINGKASAN/RANGKUMAN LAPORAN PRAKTIKUM KIMIA ORGANIK
Judul Percobaan : Pengenalan Pelarut Organik Judul Percobaan : Pengenalan Pelarut Organik Tujuan
Tujuan : : a. a. Dapat Dapat menyebutkan menyebutkan berbagai berbagai pelarut pelarut organikorganik
b. Dapat menjelaskan sifat kelarutan pelarut-pelarut organik didalam air b. Dapat menjelaskan sifat kelarutan pelarut-pelarut organik didalam air
c. Dapat menjelaskan sifat kelarutan pelarut-pelarut organik satu terhadap c. Dapat menjelaskan sifat kelarutan pelarut-pelarut organik satu terhadap
yang lainnya yang lainnya Skema kerja :
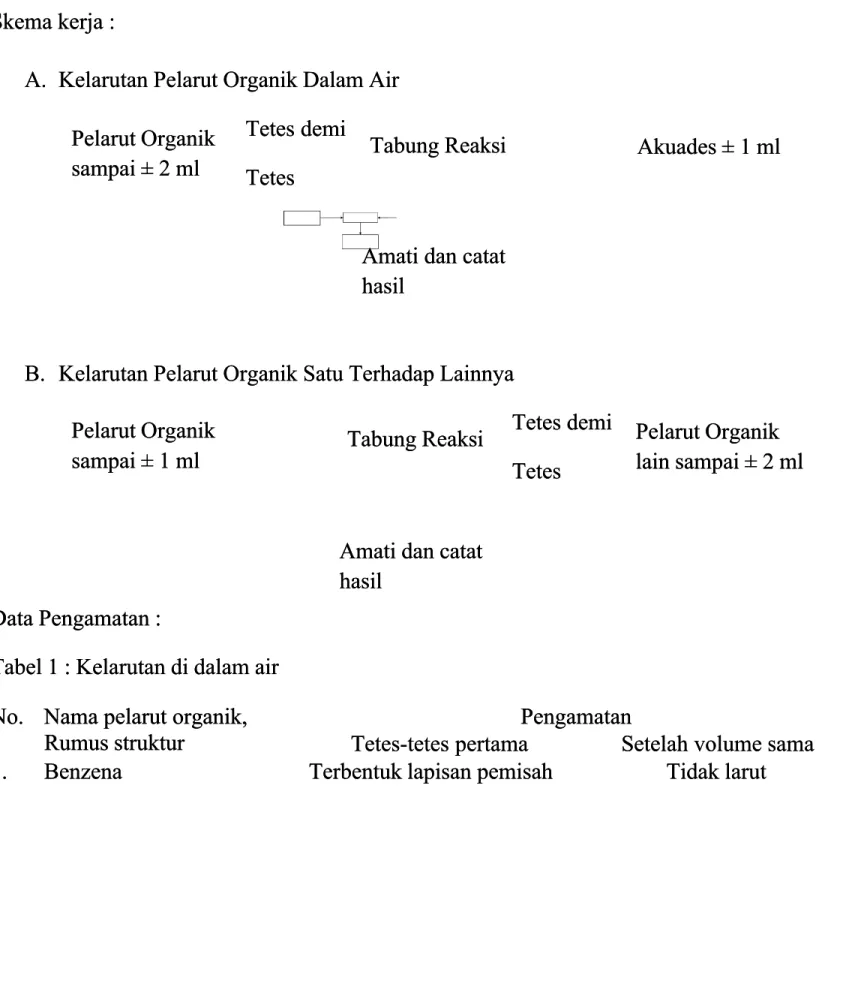
Skema kerja : A.
A. Kelarutan Pelarut Organik Dalam AirKelarutan Pelarut Organik Dalam Air Tetes demi
Tetes demi Tetes
Tetes
B.
B. Kelarutan Pelarut Organik Satu Terhadap LainnyaKelarutan Pelarut Organik Satu Terhadap Lainnya
Tetes demi Tetes demi Tetes Tetes Data Pengamatan : Data Pengamatan :
Tabel 1 : Kelarutan di dalam air Tabel 1 : Kelarutan di dalam air No.
No. Nama pelarut organik,Nama pelarut organik, Rumus struktur
Rumus struktur
Pengamatan Pengamatan Tetes-tetes
Tetes-tetes pertama pertama Setelah Setelah volume volume samasama 1.
1. Benzena Benzena Terbentuk Terbentuk lapisan lapisan pemisah pemisah Tidak Tidak larutlarut Pelarut Organik
Pelarut Organik sampai ± 2 ml sampai ± 2 ml
Tabung Reaksi
Tabung Reaksi Akuades ± 1 mlAkuades ± 1 ml
Amati dan catat Amati dan catat hasil
hasil
Tabung Reaksi
Tabung Reaksi Pelarut OrganikPelarut Organik lain sampai ± 2 ml lain sampai ± 2 ml Pelarut Organik Pelarut Organik sampai ± 1 ml sampai ± 1 ml
Amati dan catat Amati dan catat hasil
2. Toluena Terbentuk lapisan pemisah Tidak larut
3. n-heksana Terbentuk lapisan pemisah Tidak larut
4. Metanol Larut dalam air Larut
5. Etanol Larut dalam air Larut
6. Isopropanol Terbentuk lapisan pemisah Tidak larut
7. Butil etanol Terbentuk lapisan pemisah Tidak larut
8. Kloroform Pelarut memisah kebawah Tidak larut
9. TCE Pelarut memisah kebawah Tidak larut
10. Aseton Larut dalam air Larut
Tabel 2 : Kelarutan pelarut organik satu terhadap lainnya Benzen Toluen
n-heksana
Siklo heksan
Metanol etanol Isopropil etanol Butil etanol Kloro-form TCE Aseton Benzena - * + ** + * + ** + * + ** + * ** -* + ** + * + ** + * + ** + * + ** + * + ** + * + ** + Toluena * + ** + - * + ** + * + ** + * + ** + * ** -* + ** + * + ** + * + ** + * + ** + * ** -n-heksana * + ** + * + ** + - * + ** + * ** * ** -* + ** + * + ** + * + ** + * + ** + * + ** + sikloheksan * + ** + * + ** + * + ** + - * ** * ** * ** -* + ** + * ** -* + ** + * ** -metanol * ** -* + ** + * ** * ** -- * + ** + * + ** + * + ** + * + ** + * + ** + * + ** + etanol * + ** + * ** * ** * ** -* + ** + - * + ** + * + ** + * + ** + * + ** + * + ** + Isopropil etanol * + ** + * + ** + * + ** + * ** -* + ** + * + ** + - * + ** + * + ** + * + ** + * + ** + Butil etanol * + ** + * + ** + * + ** + * + ** + * + ** + * + ** + * + ** + - * + ** + * + ** + * + ** + kloroform * + ** + * + ** + * + ** + * ** -* + ** + * + ** + * + ** + * + ** + - * + ** + * + ** + TCE * + ** + * + ** + * + ** + * + ** + * + ** + * + ** + * + ** + * + ** + * + ** + - * + ** + Aseton * + ** + * ** -* + ** + * ** -* + ** + * + ** + * + ** + * + ** + * + ** + * + ** +
-Ket : * Pengamatan pada tetes pertama
** Pengamatan setelah volume total ± 2 ml
“+” larut
“-“ tidak larut
Pembahasan :
Pelarut organik adalah suatu pelarut dengan struktur molekul berpusat pada suatu atom karbon atau lebih yang membentuk kerangka molekul. Semakin besar atau panjang gugus fungsinya dapat menyebabkan kelarutan pelarut organik menjadi terbatas. Pada percobaan ini dapat diketahui bahwa pelarut yang digunakan ada yang bersifat polar dan non-polar. Pada percobaan pertama dari data pengamatan pelarut organik yang termasuk polar dalam air
adalah metanol, etanol, dan aseton. Karena ketiga pelarut dapat membentuk ikatan hidrogen dengan air. Sedangkan pelarut yang lain adalah pelarut yang bersifat non-polar.
Pada percobaan kedua, pelarut organik yang bersifat polar akan mudah larut dengan pelarut yang sama-sama bersifat polar. Seperti metanol, etanol, dan aseton. Ketiganya bila
Tidak akan terlarut disebabkan karena perbedaan sifat kepolaran. Begitu pula dengan pelarut yang bersifat non-polar akan mudah larut dengan pelarut non-polar. Dalam percobaan ini pelarut non-polar adalah benzena, toluena, n-heksana, sikloheksana, isopropil etanol, butil
etanol, kloroform, dan TCE. Akan tetapi menurut literatur bahwa senyawa golongan alkohol, alkanon (aseton) memiliki sifat dapat larut dalam air (polar) berbeda dengan yang kami
dapatkan. Pelarut isopropil etanol dan butil etanol tidak dapat larut dalam air, tetapi dapat larut dengan pelarut lain. Dan pelarut metanol,etanol,aseton juga dapat larut dalam pelarut lain. Hal ini mungkin disebabkan karena adanya faktor kesalahan dalam pengamatan. Kesimpulan :
1. Senyawa yang bersifat polar akan mudah larut dalam pelarut polar dan sebaliknya (like dissolves like).
2. Dari data pengamatan yang termasuk pelarut bersifat polar adalah Metanol, Etanol, dan Aseton. Sedangkan pelarut yang lain bersifat non-polar.
RINGKASAN/RANGKUMAN LAPORAN PRAKTIKUM KIMIA ORGANIK
Judul Percobaan : Kelarutan Senyawa Organik
Tujuan : a. Dapat menyebutkan sifat kelarutan beberapa senyawa organik didalam air
b. Dapat menyebutkan sifat kelarutan beberapa senyawa organik didalam pelarut-pelarut organik
c. Dapat mendeskripsikan sebab terjadinya kelarutan/ketidak-larutan bahan organik dalam pelarut-pelarut
Skema kerja :
Data pengamatan :
Metanol Benzena TCE Aseton Akuades
Lilin ++ ++ ++ ++ ++ Sabun +- +- -- +- +-Karet -- -- -- -- --Steroform -- ++ ++ +- --Vit B12 +- -- -- +- ++ Putih telur +- +- +- +- +-Minyak -- ++ ++ -- --Grease -- ++ ++ -- --Ket : (++) larut (+-) larut sebagian (- -) tidak larut Sedikit bahan organik Tabung Reaksi 1 ml Pelarut Organik
Amati dan catat hasil
Struktur Molekul Senyawa Organik : 1. Metanol : 2. Benzena : 3. TCE : 4. Aseton ; 5. Akuades : Pembahasan :
Kelarutan suatu senyawa organik selain dipengaruhi oleh kepolaran air juga sangat tergantung pada kemampuan senyawa organik untuk membentuk ikatan hidrogen dengan atom-atom elektronegatif sehingga dapat larut dalam senyawa polar. Pada percobaan ini, dilakukan pengujian kelarutan beberapa bahan organik dalam berbagai jenis pelarut. Senyawa - senyawa tersebut yaitu lilin, sabun, karet, steroform, vit. B12, putih telur, minyak, dan
grease. Dan pelarutnya adalah metanol, benzena, TCE, aseton, dan akuades.
Berdasarkan hasil yang diperoleh pada praktikum ini, hanya lilin yang menunjukan kelarutan pada segala jenis pelarut. Lilin merupakan asam lemak dengan monohidraksi alkohol yang mempunyai rantai karbon dengan panjang 14 sampai 34 atom karbon. Pelarut yang dapat melarutkan lilin disebut juga sebagai pelarut lemak. Sabun memiliki rantai
hidrogen CH3(CH2)16 yang bersifat hidrofobik (tidak suka air) dan merupakan garam logam
alkali dari asam-asam lemak yang dapat bersifat hidrofilik (suka air). Oleh karena itu dari hasil pengamatan kelarutan sabun hanya larut sebagian pada semua pelarut. Menurut literatur karet adalah senyawa non-polar lebih mudah larut dalam pelarut non-polar, tetapi sukar larut dalam pelarut polar. Tetapi dari hasil pengamatan karet t idak menunjukan kelarutan pada
semua pelarut. Steroform memiliki sifat tidak larut dalam air oleh karena itu steroform hanya larut pada pelarut non-polar. Vitamin b12 tidak larut pada semua pelarut, tetapi setelah
dipanaskan vitamin b12 yang berisi pelarut metanol dan aseton hanya larut seba gian sementara dengan pelarut air larut sempurna. Jadi vitamin b12 dapat bersifat semi-polar. Kelarutan protein dalam berbagai pelarut berlainan. Protein tidak larut dalam air tetapi kaya akan radikal-radikal yang bermuatan dan mudah larut dalam garam-garam net ral. Minyak dan grease bersifat non-polar akan larut dengan sempurna pada pelarut non-polar.
Kesimpulan :
1. Bahan yang bersifat polar : lilin
2. Bahan yang bersifat non-polar : steroform, karet, minyak, dan grease 3. Bahan yang bersifat semi-polar : sabun, vitamin b12, protein.
4. Senyawa organik dapat larut dalam pelarut polar dan non polar. Kelarutan
senyawa organik tergantung pada kemampuan senyawa organik untuk membentuk ikatan hidrogen dengan atom-atom elektronegatif sehingga dapat larut dalam senyawa polar.
5. Berdasarkan hukum kelarutan like disolved like, bahwa senyawa polar larut dalam pelarut polar
dan senyawa non-polar larut dalam pelarut non-polar.
Nama : Apriliyani Indiastari Kelas /Prodi : 1D/D3 Tekkim NIM : 1631410088